竹叶花椒(Zanthoxylum armatum DC.)为芸香科花椒属(Zanthoxylum L.)植物的成熟果实,主产于四川盆地及其周边山地和重庆江津一带[1]。新鲜竹叶花椒含水率通常在50%以上,采摘后如果不及时进行处理,极易褐变长霉,影响其经济价值和品质。对竹叶花椒进行干燥处理,能够有效地降低竹叶花椒中的含水量,延长其货架期。
花椒干燥的研究逐年增多,研究者优化了花椒的不同干燥工艺,结果显示,温度是影响花椒干燥品质的主要因素,最佳干燥温度集中在45~65 ℃,研究人员还利用经典的干燥数学模型对花椒的干燥过程进行了进一步描述[2-9]。但目前干燥工艺优化主要以感官评价为指标,不同干燥条件下花椒中活性成分及其风味成分的变化情况还有待研究,且经典数学模型中各项参数意义不明确,极大限制了其使用价值和实际意义。
本试验在前人研究基础上,利用热风干燥对竹叶花椒进行处理,并结合Weibull函数对其干燥特性进行深入解析。目前花椒产地主要采用分阶段热风干燥的方式对竹叶花椒进行干燥,本文考察了不同干燥温度下竹叶花椒中黄酮、多酚、酰胺和挥发性成分的变化情况,旨在为竹叶花椒的干燥技术的深入研究提供一定的参考和依据。
1 材料与方法
1.1 实验材料
芦丁标准品(AF9022006)、没食子酸标准品(wkq20010905),成都克洛玛生物科技有限公司;β-羟基山椒素标准品(AF9100404),成都艾法生物科技有限公司;Folin-Ciocalteu试剂、甲醇(均为分析级)、正己烷(色谱级),成都市科隆化学品有限公司。
新鲜竹叶花椒,四川省巴中市巴山麻王有限公司提供,实验当天运送至成都,挑选其中大小均匀、无机械损伤、无病虫害的样品,经成都中医药大学鉴定为竹叶花椒。
1.2 仪器与设备
7890Aglient GC型气相色谱仪、5975 MSD型质谱仪、质谱检索数据库NIST 14、HP-5MS 5%苯基甲基硅氧烷气相色谱柱、安捷伦Agilent 8435紫外-分光光度计,美国Aglient公司;DHG电热鼓风干燥机、电子天平,德国Sartorius公司;CM-5型分光测色仪,柯尼卡美能达公司。
1.3 实验方法
1.3.1 热风干燥
恒温热风干燥:实验设置3个温度处理,为45、55、65 ℃,每个温度重复处理3批样品,每批样品花椒质量约200 g,将样品均匀平铺于样品筛中,每隔40 min取出样品进行质量测定,至2次称量之差<0.05 g时,认为其达到平衡含水率[10]。
产地加工(分阶段热风干燥):竹叶花椒由四川省巴中市巴山麻王有限公司提供,采用分阶段热风干燥的方式对竹叶花椒进行干燥,见表1。初始时,干燥温度接近夏季室温35~37 ℃,带走竹叶花椒表面大部分水分后,开始升温至40 ℃以上,干燥至大部分竹叶花椒完全开口后,干燥结束。目前产地加工干燥温度设置常根据人为经验,随意性较大,且干燥时间较长,不同生产企业干燥后竹叶花椒品质差异较大。
表1 分阶段热风干燥表
Table 1 Staged hot air drying table

阶段干燥时间/h温度/℃10~33523~83738~1143411~1447614~1848
1.3.2 干燥参数计算[11-12]
(1)干基含水率(moisture, M)、水分比(moisture ration, MR)和干燥速率(drying rate, DR)的计算分别如公式(1)~公式(3)所示:
(1)
![]()
(2)
(3)
式中:Mt、Mt+Δt分别表示竹叶花椒干燥t和t+Δt时刻时的干基含水率;M0表示初始含水率;Wt表示其t时刻的质量;Wd为其干基的质量。
(2)水分扩散速率(Deff)根据Fick方程来进行描述,当所有样品都有相同的初始速率时,其有效的水分扩散系数计算如公式(4)所示:
(4)
式中:Deff为有效水分扩散系数,m2/s;t为干燥时间,min;L为竹叶花椒厚度的半径,2 mm。
(3)活化能通过阿伦尼乌斯公式(5)计算物料的活化能。
(5)
式中:R为气体摩尔常数[8.314 J/(mol·k)];Ea为活化能(kJ/mol);D0为阿伦尼乌斯扩散因素(m2/s);T为绝对温度(K)。
(4)Weibull分布函数过程拟合如公式(6)所示:
(6)
式中:α为尺度参数,min;β为形状参数,t为干燥时间,min。
通过决定系数(coefficients of determination,R2)、均方根误差(root mean square error,RMSE)、卡方值(chi-square value,χ2)对拟合的结果进行评估,如公式(7)~公式(9)所示:
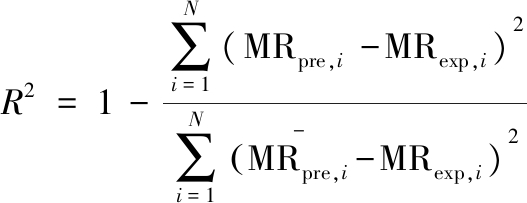
(7)
(8)
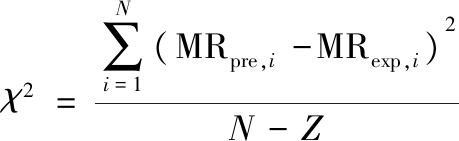
(9)
式中:MRexp,i为任意时刻试验值;MRpre,i为任意时刻预测值;N为观测值的个数;Z为模型待定系数的个数。
1.3.3 颜色测定
利用CM-5型分光测色仪进行测量,测量中使用CIELab表示色度空间[13]。由于竹叶花椒不同个体表面色泽差异大,为使测量结果准确,取竹叶花椒粉末(过4号筛)进行测定,记录其L*、a*、b*值即可。以鲜花椒为对照。
1.3.4 总酚、总黄酮、总酰胺含量的测定
(1)提取液制备:取竹叶花椒粉末(过3号筛)0.3 g,加甲醇50 mL,称定重量,超声提取30 min,称定并补齐减失重量,过滤,取上清液,用于测定黄酮、总酚、酰胺类成分的含量。
(2)总酚含量测定:采用Folin-Ciocalteu法,测定参考姚佳[14]的方法,略有改动;以没食子酸为标准品绘制标准曲线,得Y1=70.636X1+0.035 2,R2=0.999 2(Y1:吸光度,X1:没食子酸质量浓度mg/mL);总酚含量以没食子酸计。
(3)总黄酮含量测定:根据郭换等[13]的方法;以芦丁为标准品绘制标准曲线,得Y2=11.917X2-0.015,R2=0.999 9(Y2:吸光度,X2:芦丁质量浓度mg/mL);总黄酮含量以芦丁计。
(4)总酰胺含量测定:测定方法参考四川药品监督管理局标准(SCYBZ 2019—001);以羟基-β-山椒素为标准品绘制标准曲线,得Y3=107.74X3-0.008 2,R2=0.999 8(Y3:吸光度,X3:羟基-β-山椒素质量浓度mg/mL);总酰胺以羟基-β-山椒素计。
1.3.5 挥发油含量及其成分检测
(1)挥发油含量的测定[15]:取花椒粉末样品,粉碎过2号筛,混匀,每组取15 g(精确至0.01 g),平行3次,加水200 mL,振摇混合均匀,浸泡2 h,按《中国药典》2020版四部(2204)挥发油测定甲法蒸馏得到挥发油,收集并计算供试品中挥发油的含量。
(2)供试品溶液制备:取挥发油0.5 mL,加正己烷定容至10 mL,混匀后过0.22 μm微孔滤膜,即得。
(3)GC-MS测定条件:参考卢俊宇等[16]的条件对挥发油中挥发性成分进行测定。
1.3.6 数据分析
结果以均值±标准差![]() 表示;利用SPSS 22.0进行方差分析;利用Origin 9.1作图。
表示;利用SPSS 22.0进行方差分析;利用Origin 9.1作图。
2 结果与分析
2.1 不同温下干燥特性的比较
2.1.1 干燥速率、水分比
不同温度下竹叶花椒干燥速率变化,如图1所示。如图1-a所示,随着温度的升高,竹叶花椒的干燥速率也相应升高,其中65 ℃的干燥速率变化幅度最大。竹叶花椒干燥过程当中主要分为加速期和降速期2个阶段,且以降速期为主;这是由于干燥前期物料中自由水的含量很高,与热空气接触时,形成了较大的水分梯度,增强了水分迁移能力,干燥速率快速升到最大,而干燥后期物料中自由水减少,水分梯度减小,此外,一部分水为结合水,流动性较差,难以除去,故干燥速率逐渐减慢,转为降速阶段[17-18]。
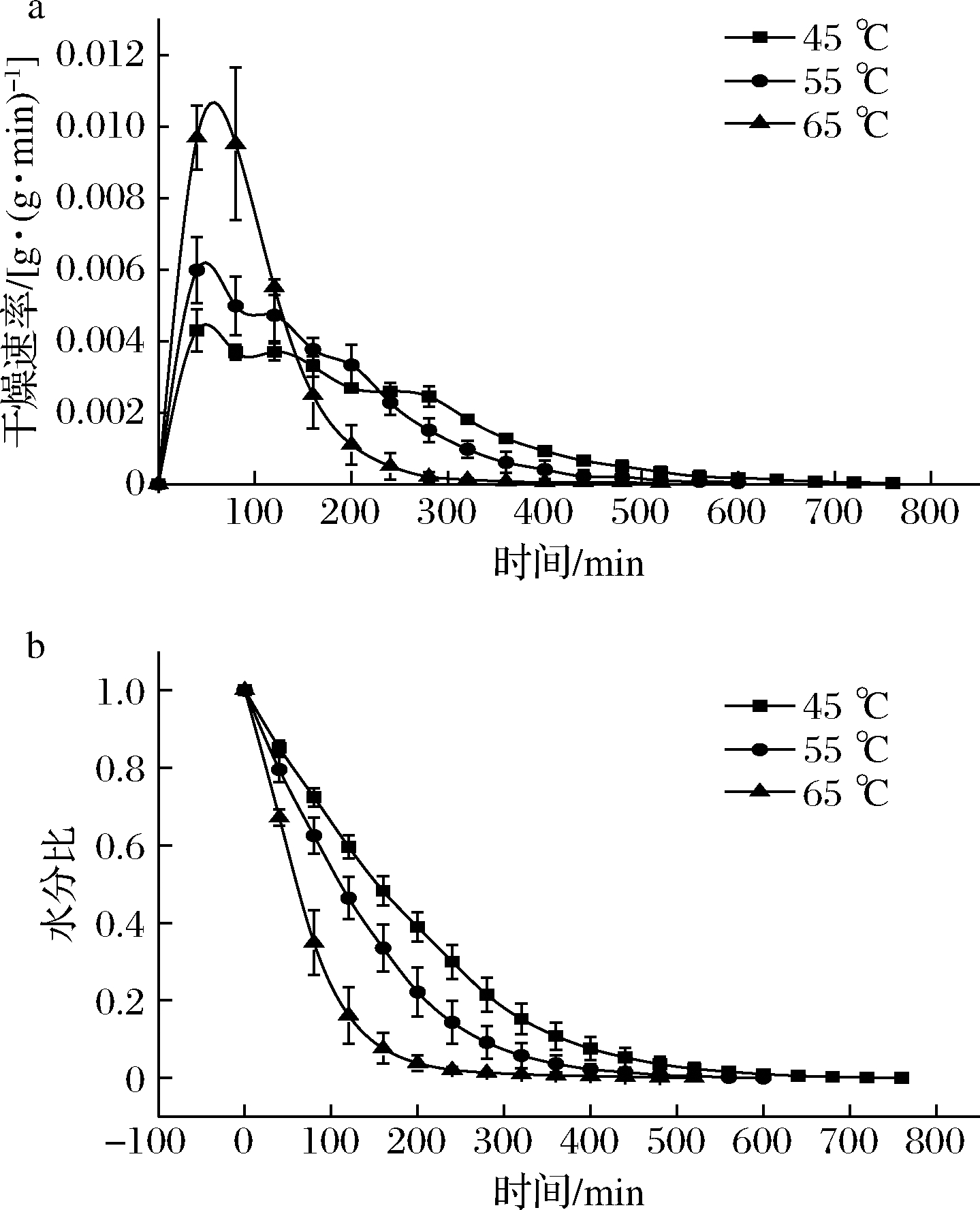
a-干燥速率变化曲线;b-水分比变化曲线
图1 不同干燥温度下竹叶花椒的干燥速率 及水分比变化曲线(n=3)
Fig.1 Variation curve of the drying rate and moisture ratio of Zanthoxylum armatum DC.under different drying temperatures (n=3)
图1-b反应了竹叶花椒在不同温度下水分比的变化规律,从图1-b中可以看出45、55、65 ℃干燥至平衡水分所用的时间分别为760、600、520 min,温度越高达到平衡水分所用的时间越短。
2.1.2 水分有效扩散系数
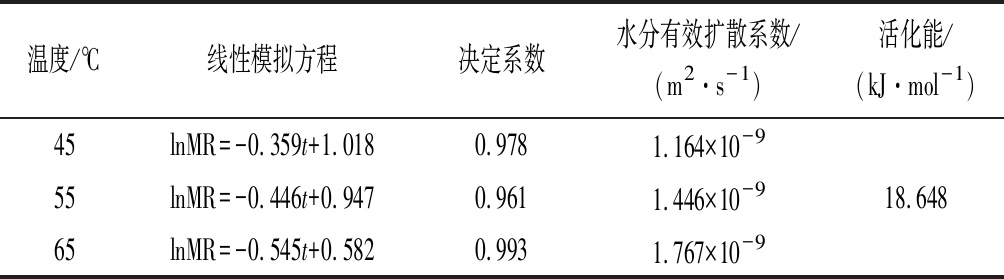
利用公式(4)、公式(5)对竹叶花椒水分扩散系数及其活化能进行计算,结果见表2。
由表2可知,竹叶花椒的水分有效扩散系数随着温度的升高而增大,进一步说明了升高温度可以增强干燥过程中的传热传质,提高干燥效率。通过与文献比较,竹叶花椒的热风干燥活化能(18.648 kJ/mol)低于真空干燥时的活化能(24.36 kJ/mol),说明竹叶花椒易于干燥[3]。
表2 不同温度下竹叶花椒水分扩散系数
Table 2 Water diffusion coefficient of Zanthoxylum armatum DC.at different temperatures
温度/℃线性模拟方程决定系数水分有效扩散系数/(m2·s-1)活化能/(kJ·mol-1)45lnMR=-0.359t+1.0180.9781.164×10-955lnMR=-0.446t+0.9470.9611.446×10-918.64865lnMR=-0.545t+0.5820.9931.767×10-9
2.1.3 基于Weibull函数的竹叶花椒热风干燥特性曲线拟合
不同温度下竹叶花椒Weibull函数模拟结果见表3。
表3 竹叶花椒热风干燥Weibull模型拟合结果
Table 3 Weibull model fitting results of hot air drying of Zanthoxylum armatum DC.
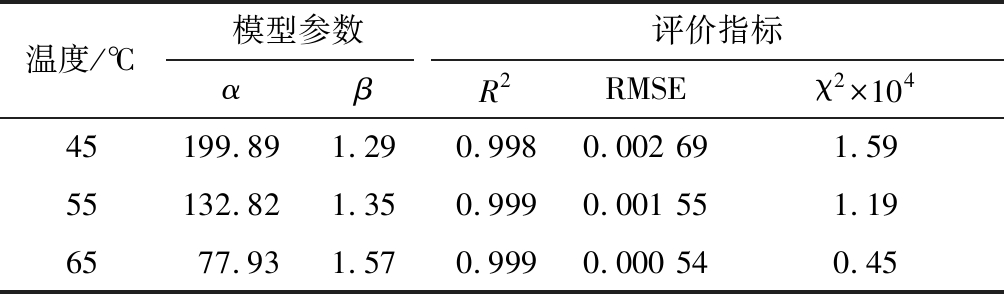
温度/℃模型参数评价指标αβR2RMSEχ2×10445199.891.290.9980.002 691.5955132.821.350.9990.001 551.196577.931.570.9990.000 540.45
表3表明,尺度参数α随着温度升高逐渐降低,说明提高温度可以有效缩短干燥时间。不同的干燥温度下竹叶花椒的形状参数β>1,说明竹叶花椒在干燥过程存在短暂的加速阶段,与图1描述一致。表3中,各条件下 Weibull拟合R2>0.998,RMSE在0.000 54~0.002 69,χ2在0.45×10-4~1.59×10-4,由此可见Weibull函数可以很好地模拟竹叶花椒的热风干燥过程。
2.1.4 Weibull模型的建立
以尺度参数α和形状参数β为因变量,以热风干燥温度(T)为自变量,利用公式(10)、公式(11)对Weibull 模型参数进行1次多项式拟合,得Weibull函数的分布方程为(12):
α=a0+a1lnT
(10)
β=b0+b1lnT
(11)
(12)
2.1.5 Weibull模型验证
利用45 ℃对Weibull模型进行验证,拟合R2为0.998,RMSE为0.002,χ2为1.28×10-5,说明实验值和预测值的一致性较好(图2),因此 Weibull函数可以较好地反应竹叶花椒热风干燥过程水分变化情况。
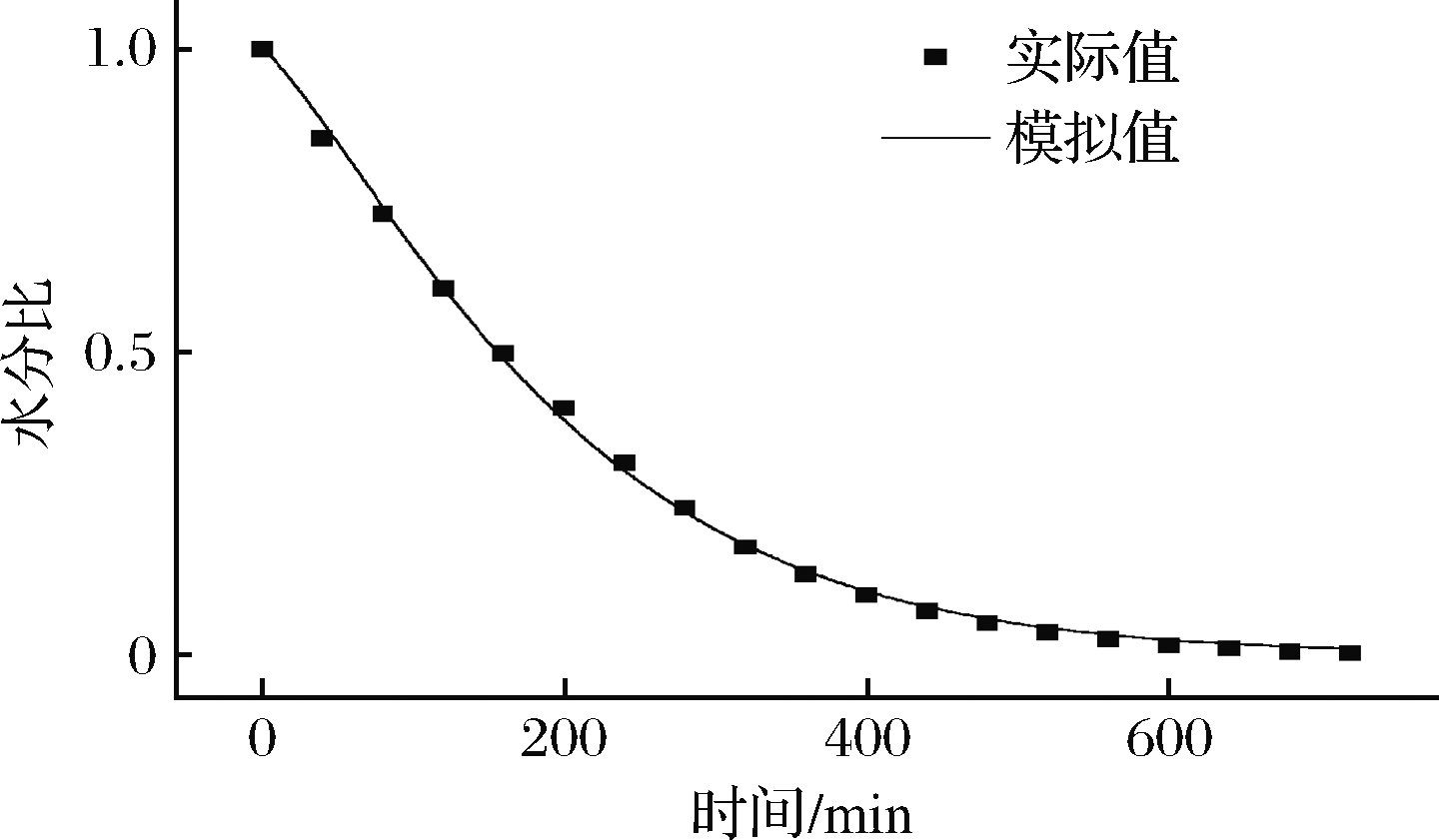
图2 Weibull模型验证
Fig.2 Weibull model verificatio
2.2 色度测量
颜色是评价竹叶花椒品质的重要指标之一,其中颜色鲜艳且翠绿的干花椒质量较好。试验过程中发现随着温度的升高,竹叶花椒褐变程度逐渐加重,整体呈棕褐色,影响了竹叶花椒的色泽品质。本文利用CIELab系统,对干燥后竹叶花椒的色泽进行测定,结果见表4。L*值代表亮度;a*代表红绿色度(-a颜色偏绿,+a颜色偏红);b*代表黄蓝色度(+b颜色偏黄,-b时颜色偏蓝)[19]。
由表4可知,干燥后竹叶花椒亮度值L*明显增大,说明干燥后竹叶花椒色泽更加明亮,随着温度的升高竹叶花椒亮度逐渐减小,在45 ℃下进行干燥竹叶花椒明亮度最高;红绿值(a*)是评价竹叶花椒干燥后是否仍为绿色的重要指标,干燥后所有组别a*值均增大,45 ℃组竹叶花椒a*值仍为负数(-0.18±0.01),说明干燥结束后,只有45 ℃组竹叶花椒仍呈绿色;对比b*值,产地加工组花椒颜色偏蓝,45 ℃组颜色偏黄。综合分析在45 ℃下对竹叶花椒进行干燥,可以使竹叶花椒保持较好的色泽。
表4 不同温度下竹叶花椒色度L*值、a*值、b*值的比较
Table 4 Comparison of L* value、b* value and a* value of Zanthoxylum armatum DC.at different temperatures
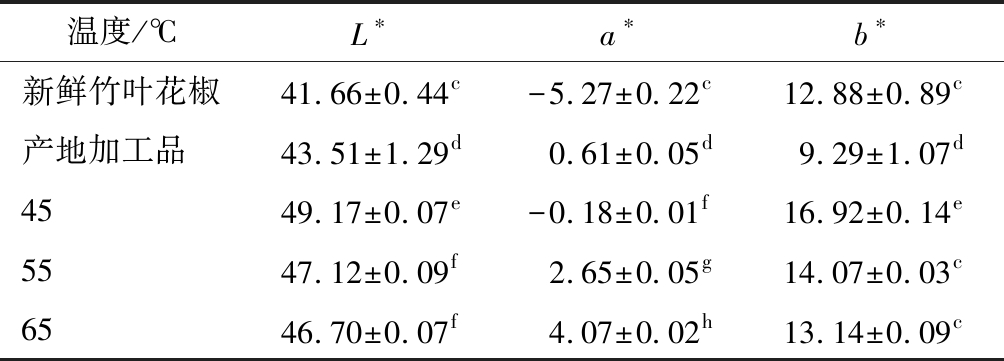
温度/℃L∗a∗b∗新鲜竹叶花椒41.66±0.44c-5.27±0.22c12.88±0.89c产地加工品43.51±1.29d0.61±0.05d9.29±1.07d4549.17±0.07e-0.18±0.01f16.92±0.14e5547.12±0.09f2.65±0.05g14.07±0.03c6546.70±0.07f4.07±0.02h13.14±0.09c
注:同一列中字母不同表示具有显著性差异(P<0.05)(下同)
2.3 总黄酮、总酚、总酰胺、挥发油含量比较
竹叶花椒不同温度下总黄酮、总酚、总酰胺、挥发油含量的比较见表5。
表5 不同温度竹叶花椒黄酮、多酚、酰胺、 挥发油含量(n=3)
Table 5 Zanthoxylum armatum DC.flavone, polyphenol, amide, volatile oil content at different temperatures(n=3)

温度/℃黄酮含量/(mg·g-1)多酚含量/(mg·g-1)酰胺含量/(mg·g-1)挥发油含量/[mL·(100g)-1]产地加工品65.24±0.24c74.686±2.00c99.00±1.59c8.50±0.50c4565.62±2.53c94.34±3.74d126.51±1.45d14.02±0.06d5550.00±1.32d71.58±2.81c118.12±1.91e11.63±0.51e6542.67±2.56e59.43±1.67e112.27±1.15f10.46±0.16e
由表5可知不同干燥温度下所得竹叶花椒干制品中黄酮、总酚、总酰胺、挥发油的含量差异显著(P<0.05)。45 ℃下黄酮、总酚、总酰胺、挥发油的含量最高。与45 ℃相比,55、65 ℃的黄酮含量各降低23.80%、34.97%;多酚含量各降低24.12%、37.00%;总酰胺含量各降低6.63%、11.26%;挥发油含量各降低17.05%、25.39%。综上可知,温度对竹叶花椒中黄酮、多酚、酰胺、挥发油的含量有显著影响,这可能由于是高温促使竹叶花椒发生了酶促褐变,引起了黄酮和多酚类物质分解或聚合,导致竹叶花椒中黄酮和多酚类物质减少[20]。相比于45 ℃组,产地加工品多酚、酰胺、挥发油的含量均显著降低,这可能是由于产地加工方法干燥时间较长,从而导致竹叶花椒中多酚、酰胺、挥发油发生降解。
2.4 不同温度花椒挥发性风味成分的比较
按2.5中GC-MS方法对不同条件下的竹叶花椒干制品中的挥发性成分进行检测,通过查阅文献及检索比对NIST 14.0标准质谱图谱库,对匹配度>80%的化合物进行分析,共鉴定出34个成分,相对含量见表6。
表6 竹叶花椒不同温度挥发性成分GC-MS分析
Table 6 GC-MS analysis of volatile components of Zanthoxylum armatum DC.at different temperatures

编号保留时间化合物名称CAS号相对含量/%产地加工品45 ℃55 ℃65 ℃16.3882-甲基-5-(1-甲基乙基)-双环[3.1.0]-2-己烯2867-05-20.140.12NN26.536α-蒎烯80-56-80.590.370.28N37.714桧烯3387-41-513.9913.5211.848.447.777β-蒎烯127-91-30.50.520.440.3158.196β-月桂烯123-35-33.043.222.92.5568.54α-水芹烯99-83-20.330.11NN78.9032-蒈烯554-61-00.210.460.310.3989.341D-柠檬烯5989-27-522.8418.8118.0217.4399.547反式-β-罗勒烯3779-61-1N0.07NN109.853β-罗勒烯13877-91-30.610.560.560.581110.16γ-松油烯99-85-40.330.720.520.691210.448(2R,5R)-2-甲基-5-丙烷-2-基双环[3.1.0]己烷-2-醇17699-16-00.490.230.310.271311.029萜品油烯586-62-90.260.340.30.361411.705方樟醇78-70-648.6953.2457.0460.211511.974侧伯酮546-80-50.260.230.230.241612.13顺式-4-(异丙基)-1-甲基环己-2-烯-1-醇29803-82-5N0.09N1.441712.987香茅醛106-23-0N0.1NN1813.732(-)-萜烯-4-醇20126-76-50.531.441.06N1914.132α-松油醇98-55-50.420.490.490.552014.251桃金娘烯醛564-94-30.210.160.170.192114.507正癸醛112-31-2N0.07NN2215.952乙酸芳樟酯115-95-70.680.951.11.082317.379十一醛112-44-7N0.07NN2418.2171,5,5-三甲基-6-亚甲基环己烯514-95-4N0.12N0.162519.439乙酸香叶酯105-87-3N0.05NN2619.681β-榄香烯515-13-90.24NNN2719.887十四烷629-59-4N0.07NN2820.456石竹烯87-44-51.001.021.161.362921.375律草烯6753-98-60.580.380.450.533022.095大牛儿烯-D23986-74-51.71.711.962.283122.402双环吉马烯24703-35-30.56N0.510.63222.4891,5,5-三甲基-6-亚甲基-1-环己烯514-95-4N0.44NN3323.621榄香醇639-99-6NN0.170.193424.159反式-橙花叔醇40716-66-31.8NNN总化合物24(100)30(99.68)21(99.82)21(99.81)单萜烯11(42.84)13(39.26)9(35.17)8(30.17)倍半萜烯5(4.08)3(3.11)4(4.08)4(4.77)醇5(51.93)5(55.49)5(59.07)5(62.66)羰基化合物3(1.15)5(1.58)3(1.50)2(1.51)其他化合物(酯类、烷烃)1(0.68)3(1.07)1(1.1)1(1.08)
注:N表示未检测出,括号前的数字是化合物总数,括号内的数字表示化合物总含量
由表6可知,从45、55、65 ℃分阶段热风干燥加工品中分别鉴定出30、21、21、24种挥发性成分,其中共有成分17种,相对含量达96.56%~97.8%,其中芳樟醇(48.69%~60.21%)、D-柠檬烯(17.43%~22.84%)、桧烯(8.4%~13.99%)、β-月桂烯(2.55%~3.22%)、大牛儿烯-D(1.7%~2.28%)为其中的主要成分,这与文献报道一致[16,21]。
单萜烯、醇类化合物是竹叶花椒挥发油的主要成分,随着温度的升高竹叶花椒挥发油中的单萜烯类成分的相对含量逐渐降低,由39.26%下降至30.17%,其中代表性化合物桧烯下降趋势较大,由13.52%降至8.4%;醇类化合物相对含量逐渐增加,由55.49%上升至62.66%,其中芳樟醇由55.49%增加至62.66%。这可能是由于温度的升高使部分低沸点单萜烯类成分挥发引起挥发性成分种类减少,从而导致萜烯类成分相对含量减少,而醇类成分的相对含量增加。
3 结论与讨论
本研究对竹叶花椒热风干燥特性进行了深入解析,结果表明,竹叶花椒的热风干燥过程为典型的降速干燥过程,随着温度的升高,竹叶花椒的干燥时间明显缩短。Weibull函数可以很好地描述竹叶花椒在不同干燥温度下水分的变化情况。竹叶花椒干燥尺度参数ɑ随着温度升高而降低,表明温度对干燥速率影响极大,形状参数β>1,说明竹叶花椒干燥前期有明显的延滞阶段。竹叶花椒的水分扩散系数(Deff)随着温度的升高逐渐增大,且竹叶花椒的热风干燥活化能(18.65 kJ/mol)较低,表明其易于干燥。
本研究发现温度对竹叶花椒色泽品质及黄酮、多酚、酰胺、挥发油的含量有显著的影响,随着温度的升高竹叶花椒各类成分均呈下降的趋势。对竹叶花椒挥发性成分进行解析发现,不同温度下竹叶花椒挥发油中主要成分相似,但相对含量差异较大;随着温度升高起萜烯类成分如:桧烯、D-柠檬烯等成分的相对含量减少,醇类成分如:芳樟醇的相对含量增加。综合分析,在45 ℃下对竹叶花椒进行干燥时黄酮(65.62±2.53) mg/g、酰胺(126.51±1.45) mg/g、挥发油(14.02±0.06) mL/100g、总酚(94.34±3.74) mg/g的含量均达到最高水平,且此温度下竹叶花椒中挥发性成分最多,表明在45 ℃下干燥有利于竹叶花椒中活性成分和风味成分的保留。
目前产地主要采用分阶段热风干燥的方式对竹叶花椒进行干燥,相比于产地加工品,本研究发现在45 ℃下对竹叶花椒进行恒温热风干燥,可以缩短近40%的干燥时间,黄酮、多酚、酰胺、挥发油类成分的含量均高于产地加工的产品,且其色泽更优,因此在产地加工时干燥温度宜控制在45 ℃左右。本实验发现在45 ℃下干燥竹叶花椒褪绿同样比较严重,后期将对竹叶花椒的干燥前处理技术进行研究,以期优化竹叶花椒的干燥工艺。
[1] 胡芳名, 谭晓峰, 刘惠民.中国主要经济树种栽培与利用[M].北京:中国林业出版社, 2005.
HU F M, TAN X F, LIU H M.Cultivation and Utilization of Main Economic Tree Species in China [M].Beijing:China Forestry Publishing House, 2005:683-688.
[2] 杨兵, 梅晓飞, 彭林, 等.热风干制对青花椒品质的影响及工艺优化[J].食品与发酵工业, 2018, 44(11):251-258.
YANG B, MEI X F, PENG L, et al.Effects of hot air drying on the quality of Zanthoxylum schinifolium and its optimization[J].Food and Fermentation Industries, 2018, 44(11):251-258.
[3] 罗传伟. 花椒真空干燥动力学模型及干燥工艺研究[D].重庆:西南大学, 2017.
LUO C W.The Study on vacuum drying model and method of the Zanthoxylum bungeanum [D].Chongqing:Southwest University, 2017.
[4] 赵超. 花椒间歇式微波干燥理论及工艺优化的试验研究[D].重庆:西南大学, 2006.
ZHAO C.Experimental research on intermittent microwave drying theory and technology optimization of chinese prickly ash[D].Chongqing:Southwest University, 2006.
[5] 祝瑞雪, 高鸿, 赵志峰, 等.响应面法优化青花椒微波干燥工艺[J].中国调味品, 2012, 37(1):51-55.
ZHU R X, GAO H, ZHAO Z F, et al.Optimization of microwave drying technology of Zanthoxylum schinifolium Sieb.et Zucc by response surface methodology[J].Chinese Condiment, 2012, 37(1):51-55.
[6] 王云龙. 花椒高压电场干燥工艺与特性研究[D].呼和浩特:内蒙古大学, 2019.
WANG Y L.Study on high voltage electric field drying technology and characteristics of Zanthoxylum bungeanum[D].Hohhot:Inner Mongolia University, 2019.
[7] 杨兵, 梅小飞, 阚建全.热泵干制对青花椒色差和品质的影响及工艺优化[J].食品与发酵工业, 2019, 45(12):140-145;151.
YANG B, MEI X F, KAN J Q.Effects of heat pump drying Zanthoxylum L.and on chromatism and quality of process optimization [J].Food and Fermentation Industries, 2019, 45(12):140-145;151.
[8] 李兴东, 常迎香, 刘海忠, 等.花椒热风干燥特性的实验分析与数学模型[J].食品工业科技, 2011, 32(4):145-147.
LI X D, CHANG Y X, LIU H Z, et al.Study on hot-air drying behavior and mathematical models of Zanthoxylum[J].Science and Technology of Food Industry, 2011, 32(4):145-147.
[9] 田冰, 王玲, 彭林, 等.多指标综合评分法优化青花椒热泵-微波联合干燥工艺[J].食品研究与开发, 2019, 40(19):149-155.
TIAN B, WANG L, PENG L, et al.Optimization of heat pump-microwave combined drying process for Zanthoxylum schinifolium by multi-index comprehensive scoring method[J].Food Research and Development, 2019, 40(19):149-155.
[10] 黎斌, 彭桂兰, 罗传伟, 等.基于Weibull分布函数的花椒真空干燥动力学特性[J].食品与发酵工业,2017,43(11):58-64.
LI B, PENG G L, LUO C W, et al.Vacuum drying kinetics characteristics of Chinese prickly ash based on Weibull distribution [J].Food and Fermentation Industries, 2017, 43(11):58-64.
[11] MARTIN-G J,  NGELES V M, MERID J, et al.The influence of berry perforation on grape drying kinetics and total phenolic compounds [J].Journal of the Science of Food and Agriculture, 2019, 99:4 260-4 266.
NGELES V M, MERID J, et al.The influence of berry perforation on grape drying kinetics and total phenolic compounds [J].Journal of the Science of Food and Agriculture, 2019, 99:4 260-4 266.
[12] BOZKIR H, RAYMAN E A, SERDAR E, et al.Influence of ultrasound and osmotic dehydration pretreatments on drying and quality properties of persimmon fruit[J].Ultrason Sonochem, 2019, 54:135-141.
[13] 郭换, 刘飞, 梅国荣, 等.色度分析花椒黄酮类成分含量与颜色值的相关性[J].中国实验方剂学杂志, 2017, 23(6):91-97.
GUO H, LIU F, MEI G R, et al.Correlation between flavonoids and color values of Zanthoxyli pericarpium based on chromatometry[J].Chinese Journal of Experimental Traditional Medical Formulas, 2017, 23(6):91-97.
[14] 姚佳. 青花椒贮藏技术研究及褐变机理初探[D].成都:四川农业大学, 2011.
YAO J.Study on the storage technology and exploring on the enzymatic browning mechanism of Zanthoxylum Schinifolium Sieb.et Zucc[D].Chengdu:Sichuan Agricultural University, 2011.
[15] 中华人民共和国卫生部药典委员会. 中华人民共和国药典(四部)[M].北京:中国医药科技出版社, 2020.
The Pharmacopoeia Committee of the Ministry of Health of the People′s Republic of China.The Pharmacopoeia of the People′s Republic of China (Part IV)[M].Beijing:China Medical Science and Technology Press, 2020.
[16] 卢俊宇, 梅国荣, 刘飞, 等.GC-MS-AMDIS结合保留指数分析比较青椒与竹叶花椒挥发油的组成成分[J].中药与临床, 2015, 6(5):18-21;35.
LU J Y, MEI G R, LIU F, et al.The armatum analysis and comparison of components of volatile oil in Zanthoxylum schinijblium sieb.et Zucc.and Z.anthoxylum DC.by combination of GC-MS-AMDIS and retention index[J].Pharmacy and Clinics of Chinese Materia Medica, 2015, 6(5):18-21;35.
[17] RANI P, TRIPATHY P P, Effect of ultrasound and chemical pretreatment on drying characteristics and quality attributes of hot air dried pineapple slices[J].Journal of Food Science and Technology, 2019, 56:4 911-4 924.
[18] 吴钊龙, 林芳, 陈振林, 等.蚕蛹热泵干燥特性及其动力学模型研究[J].食品研究与开发, 2020, 41(18):1-6.
WU Z L, LIN F, CHEN Z L, et al.Heat pump drying characteristics and kinetic modeling of silkworm pupa[J].Food Research and Development,2020, 41(18):1-6.
[19] SENADEERA W, ADILETTA G, ÖNAL B, et al.Influence of different hot air drying temperatures on drying kinetics, shrinkage, and colour of persimmon slices[J] Foods, 2020, 9(1):101-112.
[20] 戴亚峰, 王东慧, 卿鹏程, 等.霍山石斛花的热风干燥特性、品质及其护色应用研究[J].食品与发酵工业, 2021, 47(1):193-197.
DAI Y F, WANG D H, QING P C, et al.Study on the characteristics, quality and color protection application of Dendrobium huoshanense flower during hot-air drying processes[J].Food and Fermentation Industries, 2021, 47(1):193-197.
[21] LIU Y P,LI Q R,YANG W X, et al.Characterization of the potent odorants in Zanthoxylum armatum DC Prodr.pericarp oil by application of gas chromatography-mass spectrometry-olfactometry and odor activity value[J].Food Chemistry, 2020, 319:12 656.