从植物中提取的精油越来越多地被用作天然抗菌剂和抗氧化剂[1]。柑橘精油(citrus essential oil,CEO)是一种天然、无毒、无害的天然抗菌剂和植物添加剂,被普遍认为是一种安全的物质[2]。从植物组织中提取的柑橘精油具有抗氧化、抗微生物、抗炎、清除自由基、抗肿瘤以及细胞保护等多重功效[3-4],被广泛应用于食品、饮料、药品以及化妆品等领域[5]。
精油作为一种典型的疏水性物质,水溶性差,同时,精油具有高挥发性,对光、热、氧气等环境因素敏感,稳定性差[6]。鉴于此,开发具有高溶解度、强抗氧化和稳定性的精油包埋技术是必要的。
微乳液(microemulsions,ME)是由水相、油相、表面活性剂和助表面活性剂按一定比例自发形成的热力学稳定、透明或半透明、各向同性的液体分散体系,粒径为1~100 nm[7]。微乳液是油不溶性或水不溶性化合物运输和增溶的极好载体,是增强被包埋物水溶性和稳定性的有效措施[8]。ME主要分为3类:水包油型(O/W)、双连续的和油包水型(W/O)。每种ME类型的形成与油、两亲性物质和水的质量分数以及界面膜的性质有关[9]。微乳液具有以下优点:首先,ME可以有效减少精油中生物活性化合物的挥发,提高其在水中的溶解度和抗氧化活性;其次,ME可以很好地保护包埋物免受外部环境因素(如氧气、温度、光等)的影响,提高包埋物的生物利用率等[10]。ME作为一种疏水化合物的传递载体,在食品、化工、医药等领域得到了广泛的应用[11]。
本研究采用滴加水法制备柑橘精油微乳体系来克服精油低水溶性、高挥发性等弊端,通过绘制伪三元图优化微乳体系形成的工艺条件,以制备稳定的、可稀释性柑橘精油微乳液(microemulsions containing citrus essential oils,ME/CEO)。采用粒径分析、流变、温度稳定性和体外抗氧化活性等方法对制备的柑橘精油微乳液的理化性质进行研究,以期为提高CEO稳定性、生物利用率及商业化应用提供技术借鉴。
1 材料与方法
1.1 材料与试剂
柑橘精油,江西省吉水县康民本草药用油提炼厂。
吐温 80、吐温 60、吐温 40、苏丹红III,均为化学纯,天津市光复精细化工研究所;无水乙醇、亚甲基蓝,均为分析纯,天津渤化化学试剂有限公司;1,2-丙二醇、丙三醇、正丁醇,均为分析纯,天津市化学试剂供销公司;抗坏血酸,分析纯,天津市元立化工有限公司;DPPH(1,1-二苯基-2-三硝基苯肼)、ABTS(2,2-联氮-二(3-乙基-苯并噻唑-6-磺酸)二铵盐),均为分析纯,成都艾科达化学试剂有限公司。
1.2 仪器设备
H1850台式高速冷冻离心机,长沙高新技术产业开发区湘仪离心机仪器有限公司;UV—6100紫外可见分光光度计,上海美谱达仪器有限公司;ME104/02电子天平,上海梅特勒-托利多仪器有限公司;BT90纳米粒度分析仪,辽宁丹东百特仪器有限公司;MCR 301流变仪,奥地利安东帕公司;FE 28 pH 计,梅特勒-托利多仪器(上海)有限公司。
1.3 试验方法
1.3.1 伪三元图的构建
采用滴加水法制备柑橘精油微乳液,即通过在室温下用水滴定油和表面活性剂的混合物的方法绘制拟三元相图。各组分的最佳浓度是绘制拟三相图的必要条件,并可用于确定微乳液的形成区域,以筛选出微乳体系的最佳配方。先配制表面活性剂与助表面活性剂的混合液,即混表面活性剂,两者的质量比为Km。以9∶1、8∶2、7∶3、6∶4、5∶5、4∶6、3∶7、2∶8、1∶9 的不同比例制备了油和混合表面活性剂的混合物,精密称取混合于50 mL小烧杯中,在磁力搅拌器搅拌下缓慢滴加去离子水,溶液由澄清变浑浊,再变澄清,最终记录临界点样品各成分的百分含量,试验重复进行,以确保重现性,分别以油相、水相和混表面活性剂为三相图顶点,利用Origin 8.5软件进行伪三元图的绘制,确定微乳液区域,利用Auto CAD 2007软件计算微乳区域的面积。
1.3.2 柑橘精油微乳液的条件优化
1.3.2.1 表面活性剂对ME/CEO形成的影响
表面活性剂分别选定为吐温 40、吐温 60、吐温 80、吐温 80+ 吐温 40(1∶1,质量比)、吐温 80+ 吐温 60(1∶1,质量比),表面活性剂的HLB值如表1。将表面活性剂与无水乙醇按3∶1比例混合均匀作为混表面活性剂,按1.3.1制备微乳液,绘制拟三相图。
表1 制备微乳液所选表面活性剂的特性
Table 1 Characteristics of surfactants selected in preparation of ME
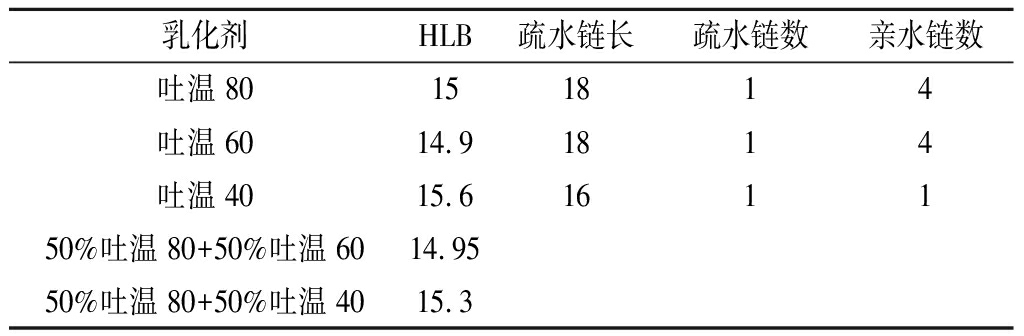
乳化剂HLB疏水链长疏水链数亲水链数吐温80151814吐温6014.91814吐温4015.6161150%吐温80+50%吐温6014.9550%吐温80+50%吐温4015.3
1.3.2.2 助表面活性剂对ME/CEO形成的影响
选取无水乙醇、1,2-丙二醇、甘油、正丁醇为助表面活性剂,混表面活性剂的比例为3∶1,按1.3.1制备微乳液,绘制拟三相图。
1.3.2.3 Km值对ME/CEO形成的影响
Km 为表面活性剂(吐温 80与吐温 40质量比1∶1)与助表面活性剂无水乙醇的质量比,Km 分别选定为 2、3、4、5,按1.3.1制备微乳液,绘制拟三相图。
1.4 柑橘精油微乳液性质的研究
1.4.1 粒径分布、大小测定
采用纳米粒度分析仪测定微乳液的液滴粒径分布、多分散指数(polydispersiry,PDI)和平均粒径。测试温度为 25 ℃,散射角为90 ℃。
1.4.2 微乳液外观和类型鉴定
微乳液制备完成后,按照国家标准,产品在保存期间应保持透明或半透明,不发生分层或破乳等现象,视为合格。微乳类型用染色法鉴定[12]。
1.4.3 微乳液黏度、pH值、密度测定
微乳液的黏度用流变仪测定,取样品0.5 mL,选用PP 50转子,剪切速率范围10-2~103 s-1,扫描温度25 ℃。
用pH计测定pH值。微乳液密度的测定参考陈硕等[13]的方法。
1.4.4 离心稳定性
取适量制备好的柑橘精油微乳,于4 000、6 000、8 000、10 000 r/min下离心30 min,观察是否分层,若无分层,以去离子水为空白对照,测定离心前后550 nm下的吸光度,透光率按公式(1)计算:
(1)
式中:T,透光率;A0,离心前微乳吸光度;A1,离心后微乳吸光度。
1.4.5 热稳定性
将适量的微乳液分别在40、50、60、70、80和90 ℃的恒温水浴中加热30 min。通过视觉观察(相分离)和透光率来评价微乳液的稳定性。以去离子水作为空白对照,使用紫外分光光度计在550 nm波长处测量加热前后微乳液的吸光度,透光率按公式(2)计算:
透光率![]()
(2)
式中:A2,加热前微乳液吸光度;A3,加热后微乳液吸光度。
1.4.6 低温稳定性
将微乳液置于4 ℃低温环境中储存,采用公式(2)测定第1、5、15、30、60、90天微乳液的透光率。
1.4.7 CEO及其ME/CEO抗氧化活性的分析和比较
1.4.7.1 DPPH自由基清除能力的测定
测定DPPH自由基的清除率参考ABD-ELGAWAD等[14]的方法,并稍加修改。DPPH粉末用无水乙醇溶解并稀释成2 mmol/L的储备液。取2 mL不同质量浓度(2、4、6、8 mg/mL)的CEO和ME/CEO溶液加入2 mL 经稀释后的DPPH溶液,混合溶液在室温下经涡旋均匀后,避光反应30 min,在 517 nm波长处测定吸光值Ai;以无水乙醇作为空白调零,以2 mL对应浓度的样品溶液加2 mL无水乙醇作为对照(Aj);2 mL无水乙醇加2 mL DPPH溶液的吸光值为Ak。以维生素C作为阳性对照,实验重复3次,DPPH自由基的清除率按公式(3)计算:
DPPH清除率![]()
(3)
1.4.7.2 ABTS自由基清除能力的测定
参考GUO等[15]方法,并稍加修改。取0.2 mL的待测样品(CEO、ME/CEO)加入2 mL ABTS阳离子自由基溶液中,将该混合物在室温条件下涡旋混匀10 min,在734 nm波长处测定其吸光度A1。测定2 mL ABTS阳离子自由基溶液与样品等体积的乙醇混合后的吸光度A0。以维生素C作为阳性对照,实验重复3次,ABTS阳离子自由基的清除率按公式(4)计算:
ABTS清除率![]()
(4)
1.5 数据分析
实验数据采用 Origin 8.5 软件绘图,采用 SPSS 23对数据进行差异性分析,实验重复3次,取平均值。
2 结果与讨论
2.1 表面活性剂对ME/CEO形成的影响
表面活性剂是形成微乳液最基本的物质,选择合适的表面活性剂对稳定微乳液的形成极为重要,表面活性剂可以有效地降低界面张力,促进微乳液的形成[16]。常用的表面活性剂有吐温系列、司盘系列以及烷基葡萄糖苷等[17]。
从图1可知,吐温 80∶吐温 40(1∶1,质量比,HLB=15.3)是最好的表面活性剂,因为与其他表面活性剂相比,它在伪三元相图中可以产生最大的微乳液区域。单一的表面活性剂有时很难达到理想的乳化效果,需要将表面活性剂进行复配,提高其乳化能力[18]。研究表明,表面活性剂的复配可以增强微乳液的乳化能力,并产生协同效应[19]。
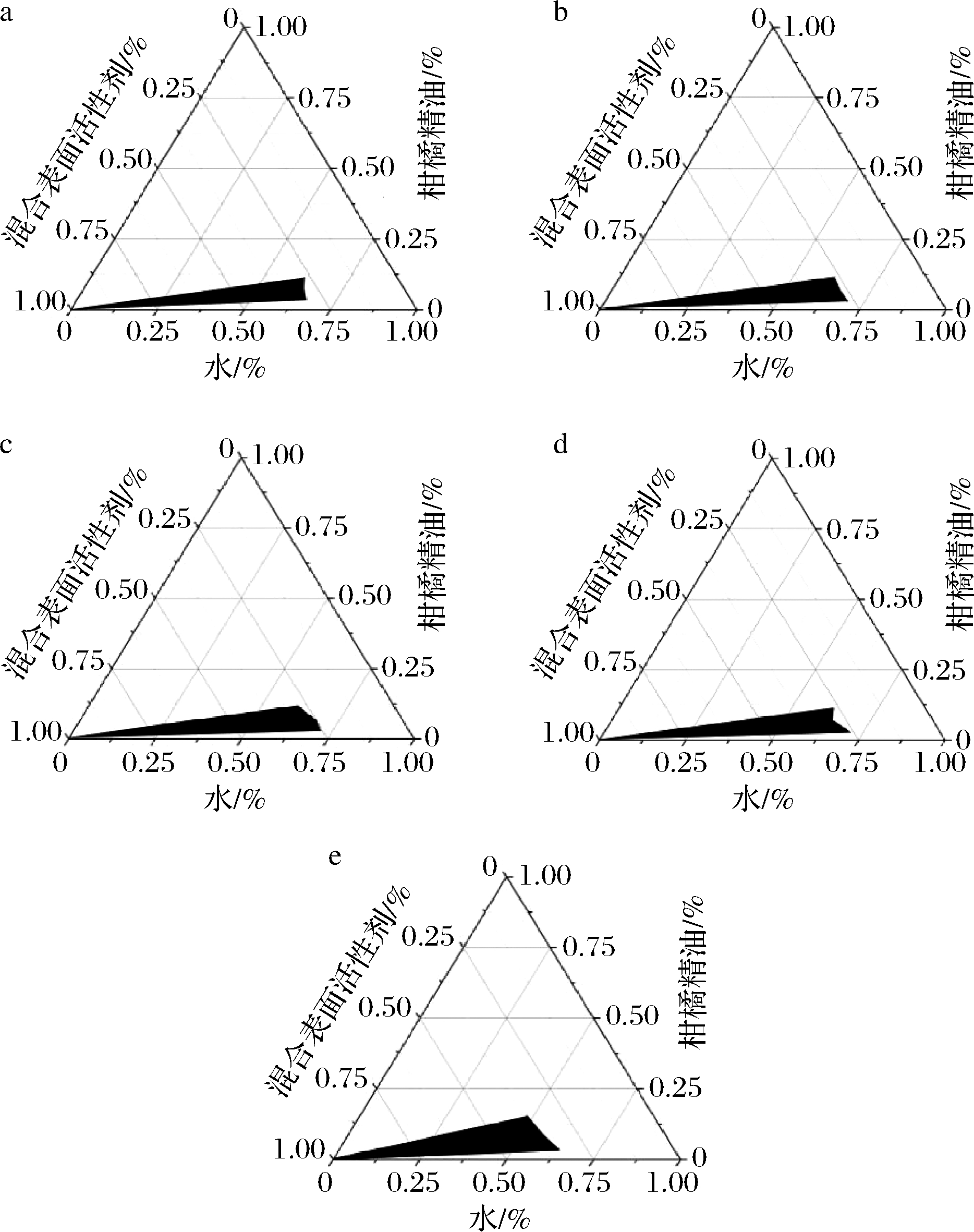
表面活性剂为:a-吐温 80;b-吐温 60;c-吐温 40;d-吐温 80+吐温 60(1∶1,质量比);e-吐温 80+ 吐温 40(1∶1,质量比)
图1 不同表面活性剂参与下柑橘微乳液在25 ℃的伪三元相图
Fig.1 Pseudo-ternary phase diagrams of ME/CEO using different surfactants at 25 ℃
注:阴影部分代表微乳液的面积
此外,从实验中发现,表面活性剂的HLB不能用于确保微乳液的形成,这或许与吐温的化学结构和饱和度有关[20]。因此,选择吐温 80∶吐温 40(1∶1,质量比)作为最佳表面活性剂。
2.2 助表面活性剂对ME/CEO形成的影响
助表面活性剂对微乳液的稳定性起着基础性的作用,它主要镶嵌在表面活性剂的分子之间,在油水界面形成混合吸附膜,降低界面膜的曲率和刚性,增强界面流动性和柔性,调节表面活性剂HLB值,提高乳化效果,促进微乳液的形成[21]。此外,助表面活性剂的作用效果与醇链的大小和所带基团有关[22]。
由图2可知,正丁醇形成的微乳液区域最大,甘油最小,乳化效果为正丁醇>无水乙醇>1,2-丙二醇>甘油。结果表明,正丁醇作为助表面活性剂可以降低体系的黏度和表面张力,提高体系的流动性,调节界面水相和油相的分布。因此,选择正丁醇作为助表面活性剂进行进一步研究。
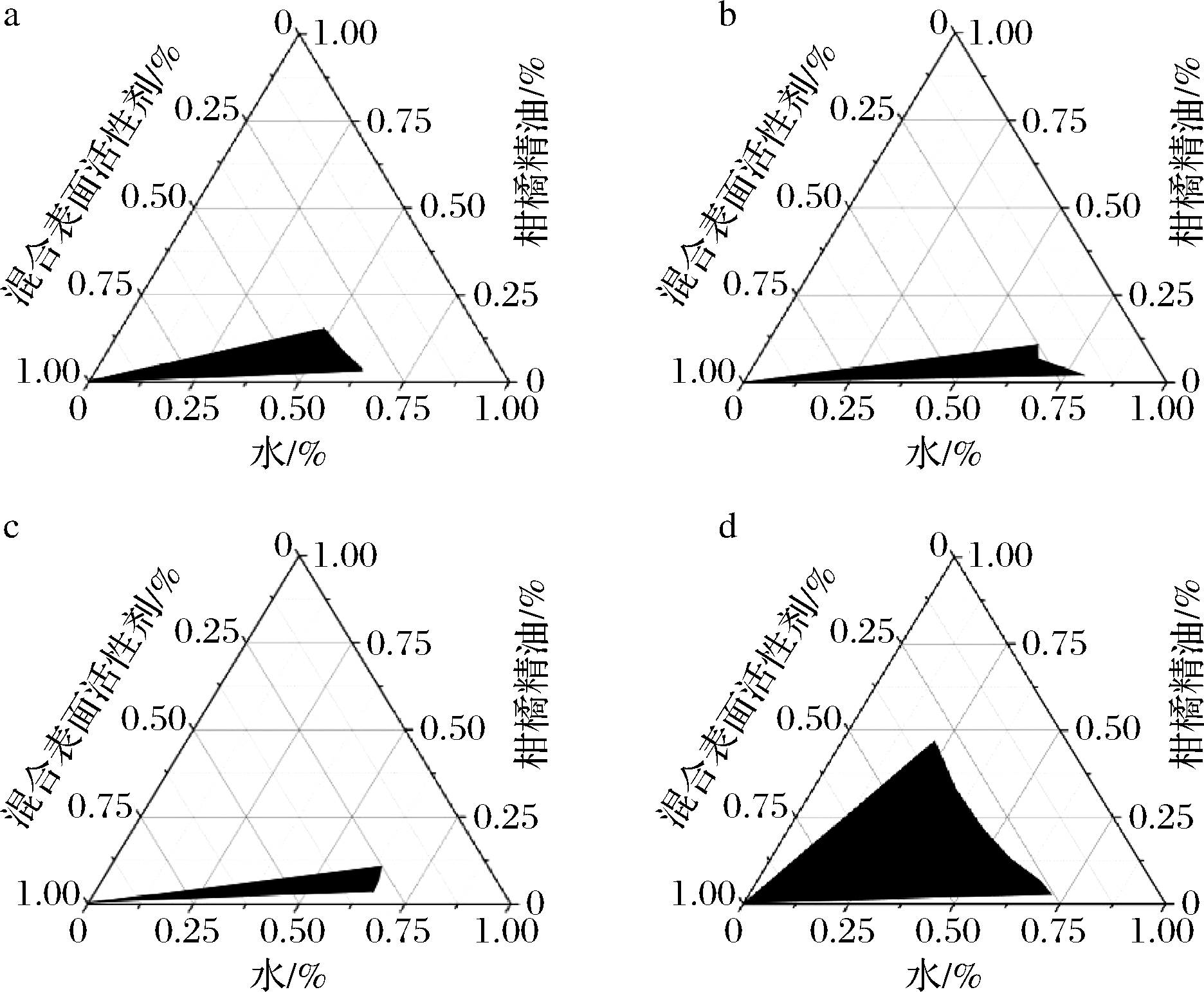
助表面活性剂为:a-无水乙醇;b-1,2-丙二醇;c-丙三醇;d-正丁醇
图2 不同助表面活性剂参与下柑橘微乳液在25 ℃时的伪三元相图
Fig.2 Pseudo-ternary phase diagrams of ME/CEO using different co-surfactants at 25 ℃
2.3 Km对ME/CEO形成的影响
由图3可知,随着Km值的增加,所形成微乳液的面积先增加后减少。与其他Km值相比,Km=4形成的微乳液区域最大,这可能与助表面活性剂镶嵌在表面活性剂分子结构的位置有关。可能是由于正丁醇存在于表面活性剂和界面之间,并参与液滴界面膜的形成。同时,它也分布在水相和油相中,改善了两相的性能,导致界面张力降低和微乳液的形成[23]。因此,选择Km=4进行下一步研究。
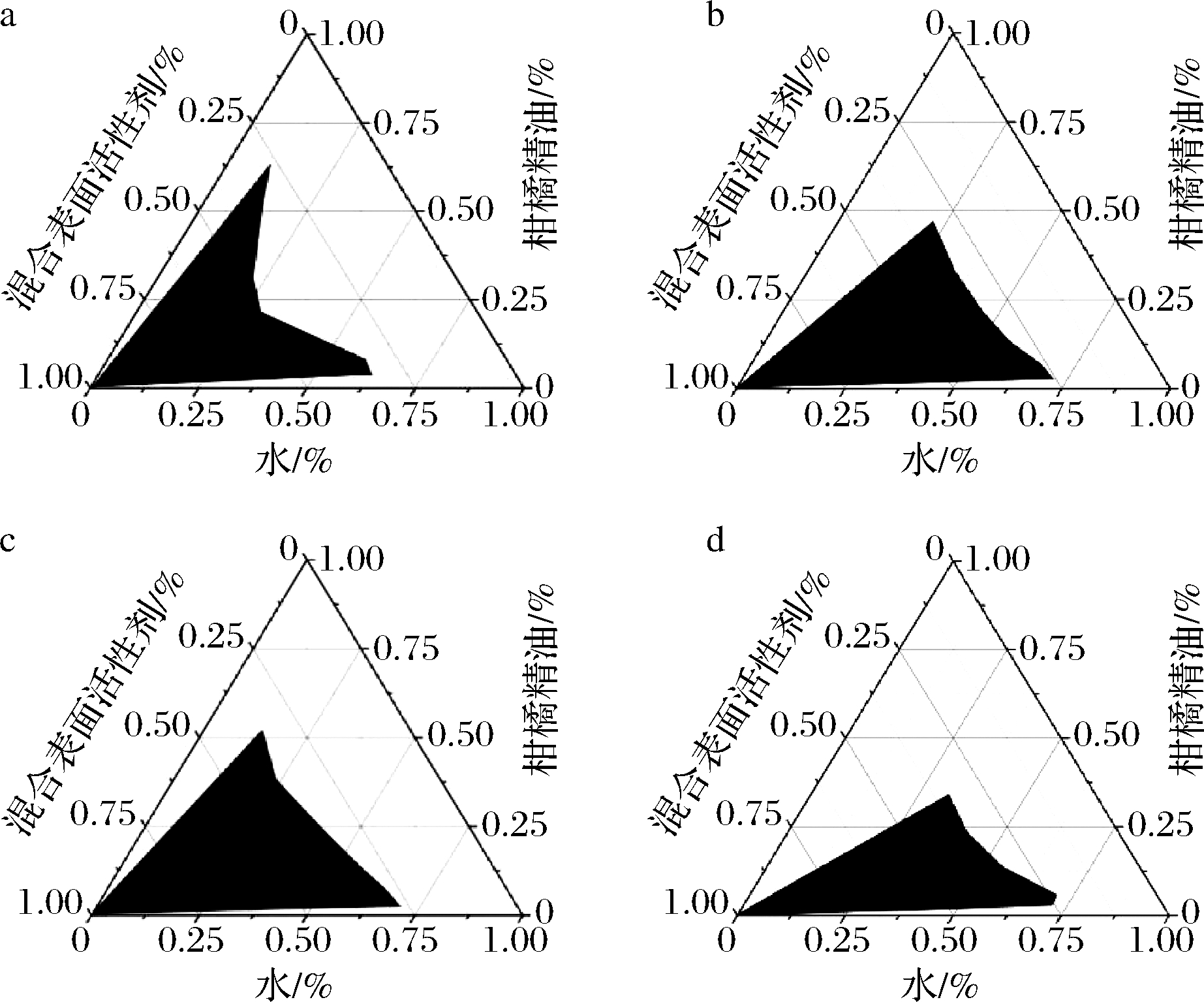
a-Km=2;b-Km=3;c-Km=4;d-Km=5
图3 不同Km值对ME/CEO形成的影响
Fig.3 Pseudo-ternary phase diagrams of ME/CEO with different Km
2.4 微乳液配方的确定
根据上述实验结果,确定了ME/CEO的最佳配方为:m(吐温 80)∶m(吐温 40)=1∶1为表面活性剂,正丁醇为助表面活性剂,Km=4。如图4所示,在混合表面活性剂与油相的所有比例(4∶6~9∶1)中都能得到均一、透明的ME/CEO,与微乳液的外观特征相符。降低油相中乳化剂的浓度会使微乳液体系产生浑浊,当比例低于4∶6时,由于相分离迅速,系统变得不稳定。因此,从载油量和乳化效果考虑,选择微乳液配方7∶3作为样品进行下一步研究。

图4 不同比例的相形成的微乳液
Fig.4 Microemulsions formed by different proportions of phases
2.5 柑橘精油微乳液性质的研究
2.5.1 粒径分布、大小测定
粒径和PDI决定了微乳液的性质,如光学外观、长期稳定性等[24]。PDI值通常为0~1,PDI值越小,表明微乳液粒径分布越集中,体系均一性越好[25]。结果表明,ME的粒径分布均匀,呈单峰分布,平均粒径为(28.83±0.95)nm,PDI为(0.06±0.05),微乳液液滴尺寸在纳米范围内,如图5所示。
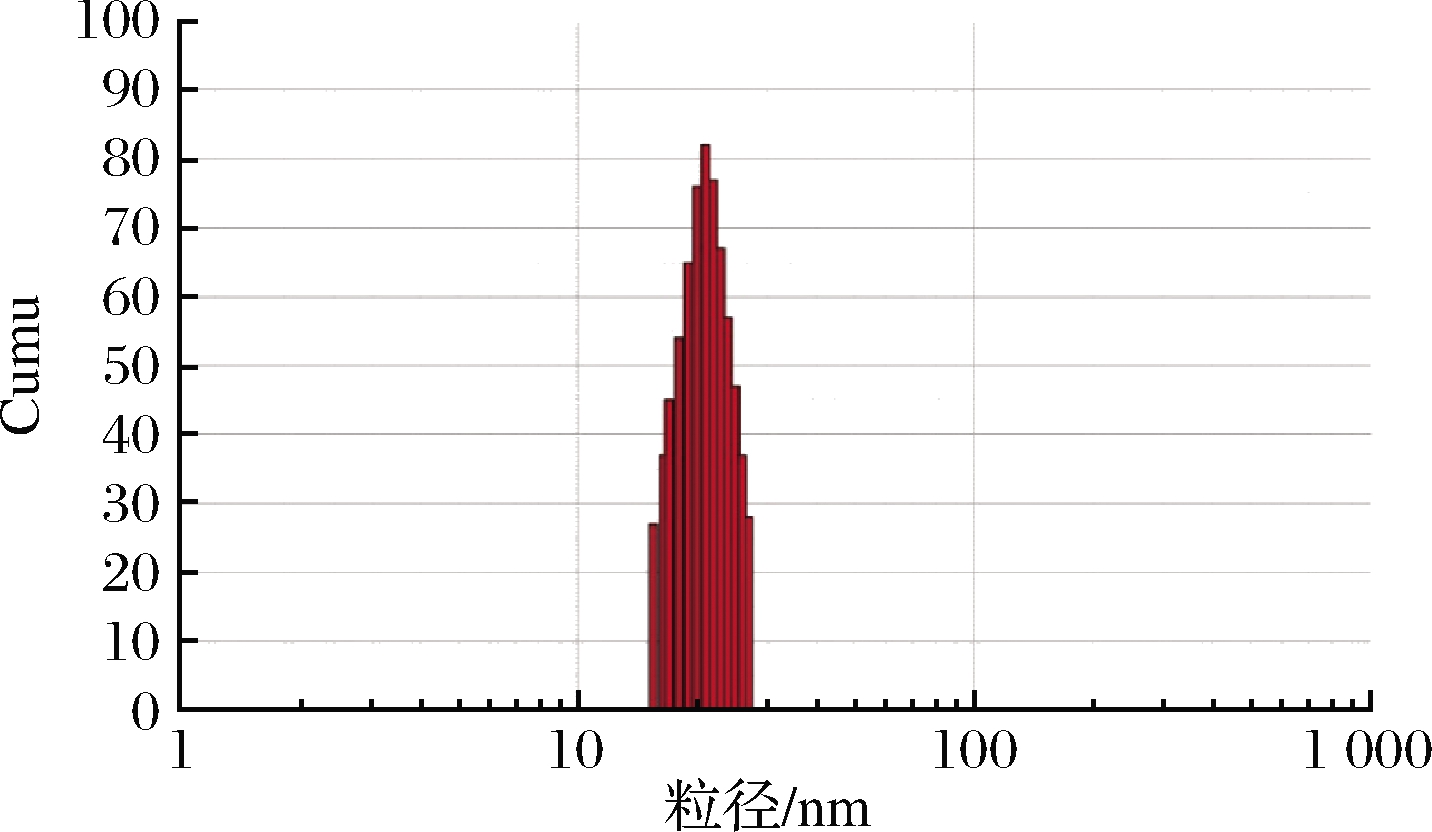
图5 微乳液的粒径分布
Fig.5 Droplet size distribution of microemulsions
2.5.2 微乳液外观和类型鉴定
染色法判定微乳液的类型是基于“相似相溶”原理,水溶性染料亚甲基蓝在水相中扩散速度快,而油溶性的苏丹III在油相中扩散速度较快。由图6可知,亚甲基蓝的扩散速度快于苏丹III,表明制备的ME/CEO是O/W型。

图6 染色法测定微乳液的类型
Fig.6 ME type identification using dyeing method
2.5.3 微乳液黏度、pH值和密度
流变学实验表明,当剪切速率为0.01~0 s-1时,ME/CEO的黏度随剪切速率的增大而降低。当剪切速率>0 s-1时,ME/CEO的黏度基本保持不变,表现出低黏度牛顿行为,平均黏度为(17.6±1.33)mPa·s,这可以归因于它们的高含水量,如图7所示。

图7 不同剪切速率微乳液黏度的测定
Fig.7 Variable shear rates of ME/CEO for viscosity measurement
表面活性剂是两性化合物,在pH接近中性时不带电。结果表明,配方7∶3的ME/CEO的pH值为6.54,接近中性。因此,可以得出表面活性剂不影响水的pH值。此外,微乳液的密度为(0.958±0.03)g/mL,小于水的密度。
2.5.4 离心稳定性
如果微乳体系不稳定,在储存过程中会产生浑浊、液体分层、絮凝等现象。因此,通过离心加速这一变化,来考察微乳液的稳定性。结果表明,在不同离心条件下,微乳液微乳外观清澈透明,未发生相分离、凝固、乳化等现象,且透光率均大于100%,如图8所示。表明微乳液体系具有良好的离心稳定性。
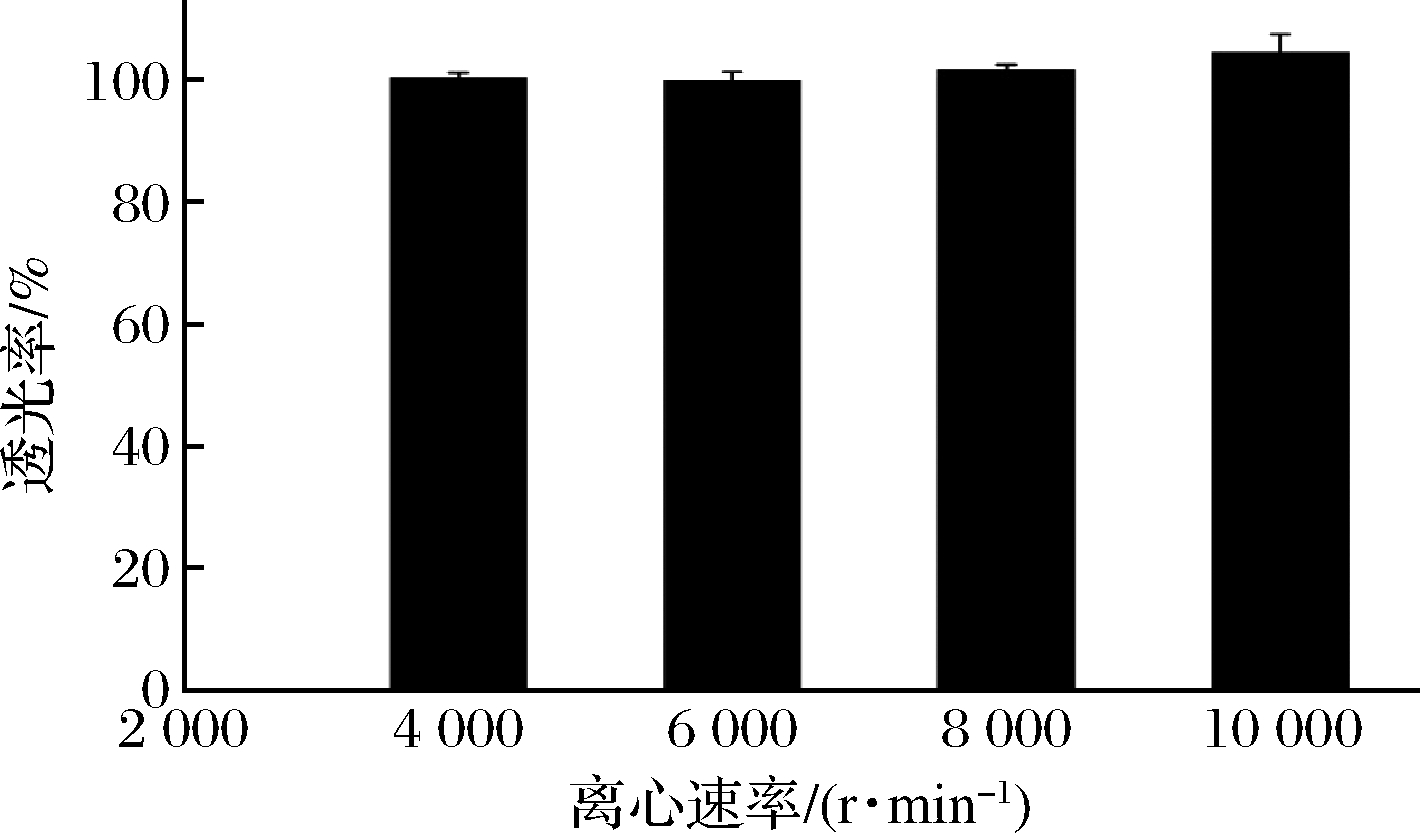
图8 不同离心速率下微乳液的透光率
Fig.8 Luminousness of microemulsions at different centrifugation rates
2.5.5 温度稳定性
由图9和肉眼观察结果可知,不同加热温度下,微乳液的外观呈清澈透明状态,透光率均大于92%。表明本研究所制得的ME/CEO具有良好的热稳定性。

图9 不同温度下微乳液的透光率
Fig.9 Luminousness of microemulsions with different heating temperatures
将ME/CEO分别在4 ℃下保存1、5、10、15、30、60、90 d。ME/CEO的外观清澈透明,未出现凝固、乳化、相分离等现象,透光率均大于95%,如图10所示,且ME/CEO在4 ℃下至少能稳定90 d。本研究所制备的ME/CEO在低温条件下具有良好的稳定性。

图10 不同贮藏时间微乳液的透光率
Fig.10 Luminousness of microemulsions at different storage time at 4 ℃
2.6 CEO及其ME/CEO抗氧化活性的分析和比较
2.6.1 DPPH自由基清除率
DPPH乙醇溶液呈深紫色,在波长517 nm处有最大吸收峰。在DPPH分子结构中带有未配对电子的氮原子可以捕获自由基。当存在自由基清除剂时,它将与DPPH分子上的单个电子配对,形成DPPH-H,使溶液颜色变浅或消失[26]。采用DPPH法分析比较了纯挥发油和ME的体外抗氧化作用。CEO及其ME/CEO的DPPH自由基清除能力如图11所示,结果表明,CEO和ME/CEO对DPPH自由基清除能力随浓度的增加而增大,ME/CEO对DPPH自由基的清除能力优于CEO,但要弱于阳性对照维生素C对DPPH自由基的清除能力(P<0.05)。

图11 精油和微乳液的DPPH自由基清除率
Fig.11 DPPH radicals scavenging ability of pure essential oil and ME
2.6.2 ABTS阳离子自由基清除率
ABTS被活性氧氧化生成稳定的蓝绿色ABTS阳离子自由基。在此物质中加入抗氧化剂,与ABTS阳离子自由基反应,使反应体系变色,在734 nm波长处检测吸光度变化[27]。它与抗氧化剂的生物活性有很强的相关性,在测定血清、果蔬等生物样品的抗氧化能力方面得到了广泛的应用。CEO和ME/CEO对ABTS阳离子自由基清除能力如图12所示,CEO和ME/CEO具有较强的ABTS阳离子自由基清除能力;同时,ME/CEO的抗氧化能力优于CEO,且与浓度呈正相关,但要弱于阳性对照维生素C(P<0.05)。
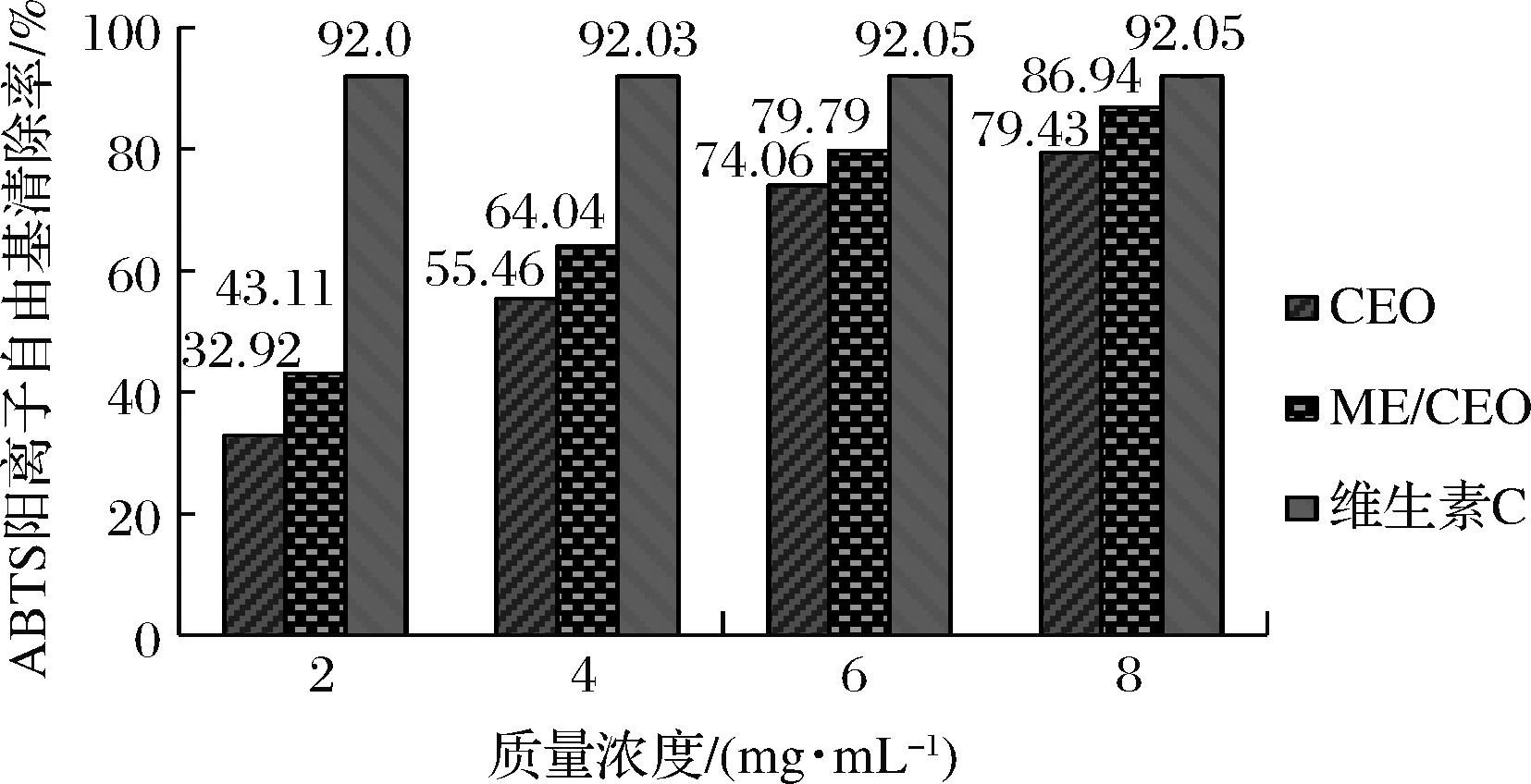
图12 精油和微乳液的ABTS阳离子自由基清除率
Fig.12 ABTS cation ion radicals scavenging ability of pure essential oil and ME
含柑橘精油的微乳液配方能有效提高柑橘精油在水相环境中的抗氧化活性,但精油和微乳液的自由基清除能力要弱于维生素C。微乳液具有较强的自由基清除能力可能是由于体系中油相油滴粒径的减小从而具有更大的反应表面积、超低界面张力及纳米级分散相等[28]。同时,微乳液体系的抗氧化性能也强烈依赖于水相的含量,即使精油浓度降低,微乳体系的抗氧化活性也会随着水相的增加而显著提高[29]。
3 结论
本研究通过微乳化技术构建了柑橘精油微乳体系,解决了柑橘精油在水相环境中应用受到制约以及稳定性差等问题。对制备的微乳体系进行稳定性(低温、室温、高温以及离心)分析,微乳液体系没有产生絮凝、分层、乳化和沉淀等不稳定现象,表明微乳液具有良好的储存稳定性。微乳液能够有效地提高精油在水相环境中的抗氧化活性,具有开发天然抗菌剂和抗氧化剂的潜力。
[1] VANHAUTE S,RAES K,VAN DER MEEREN P,et al.The effect of cinnamon,oregano and thyme essential oils in marinade on the microbial shelf life of fish and meat products[J].Food Control,2016,68(10):30-39.
[2] CUI H Y,LI W,LI C Z,et al.Liposome containing cinnamon oil with antibacterial activity against methicillin-resistant Staphylococcus aureus biofilm[J].Biofouling,2016,32(2):215-225.
[3] JEMAA M B,FALLEH H,SERAIRI R,et al.Nanoencapsulated Thymus capitatus essential oil as natural preservative[J].Innovative Food Science & Emerging Technologies,2018,45(2):92-97.
[4] SMERIGLIO A,ALLOISIO S,RAIMONDO F M,et al.Essential oil of Citrus lumia Risso:Phytochemical profile,antioxidant properties and activity on the central nervous system[J].Food Chemistry Toxicol,2018,119(9):407-416.
[5] MITROPOULOU G,FITSIOU E,SPYRIDOPOULOU K,et al.Citrus medica essential oil exhibits significant antimicrobial and antiproliferative activity[J].LWT-Food Science and Technology,2017,84(10):344-352.
[6] FEYZIOGLU G C,TORNUK F.Development of chitosan nanoparticles loaded with summer savory(Satureja hortensis L.)essential oil for antimicrobial and antioxidant delivery applications[J].LWT-Food Science and Technology,2016,70(7):104-110.
[7] GHARBAVI M,DANAFAR H,SHARAFI A.Microemulsion and bovine serum albumin nanoparticles as a novel hybrid nanocarrier system for efficient multifunctional drug delivery[J].Journal of Biomedical Materials Research Part A,2020,108(8):1 688-1 702.
[8] WAN J,ZHONG S B,SCHWARZ P,et al.Physical properties,antifungal and mycotoxin inhibitory activities of five essential oil nanoemulsions:Impact of oil compositions and processing parameters[J].Food Chemistry,2019,291(9):199-206.
[9] HELLWEG T.Phase structures of microemulsions[J].Current Opinion in Colloid & Interface Science,2002,7(1):50-56.
[10] ZHANG L H,CRITZER F,DAVIDSON P M,et al.Formulating essential oil microemulsions as washing solutions for organic fresh produce production[J].Food Chemistry,2014,165(12):113-118.
[11] DUANGJIT S,CHAIRAT W,OPANASOPIT P,et al.Application of design expert for the investigation of capsaicin-loaded microemulsions for transdermal delivery[J].Pharmaceutical Development & Technology,2016,21(6):698-705.
[12] 程作慧, 段慧娟,崔子祥,等.香茅精油微乳液的制备及其抑菌活性[J].分子科学学报,2019,35(4):304-311.
CHENG Z H,DUAN H J,CUI Z X,et al.Preparation and antibacterial activity of Citronella oil micro-emulsion[J].Journal of Molecular Science,2019,35(4):304-311.
[13] 陈硕, 徐马俊坤,张赟彬,等.薄荷精油微乳体系的构建及其抑菌性[J].现代食品科技,2014,30(11):139-144;104.
CHEN S,XU M J K,ZHANG Y B,et al.Construction of a microemulsion system and the antibacterial performance of peppermint essential oil[J].Modern Food Science and Technology,2014,30(11):139-144;104.
[14] ABD-ELGAWAD A,EL GENDY A E,EL-AMIER Y,et al.Essential oil of Bassia muricata:Chemical characterization,antioxidant activity,and allelopathic effect on the weed Chenopodium murale[J].Saudi Journal of Biological Sciences,2020,27(7):1 900-1 906.
[15] GUO J J,GAO Z P,XIA J L,et al.Comparative analysis of chemical composition,antimicrobial and antioxidant activity of citrus essential oils from the main cultivated varieties in China[J].LWT-Food Science and Technology,2018,97(8):825-839.
[16] PAL N,SAXENA N,& MANDAL A.Synthesis,characterization,and physicochemical properties of a series of quaternary gemini surfactants with different spacer lengths[J].Colloid and Polymer Science,2017,295(12):2 261-2 277.
[17] 李帅涛.美藤果油微乳液体系构建及性质研究[D].上海:上海应用技术大学,2018.
LI S T.Construction and properties of Sacha inchi oil microemulsion system[D].Shanghai:Shanghai University of Applied Technology,2018.
[18] LIANG W P,TADROS T.Novel method to prepare O/W microemulsions within a wide temperature range[J].Acta Physico-Chimica Sinica,2000,16(6):538-542.
[19] LI P,GHOSH A,WAGNER R F,et al.Effect of combined use of nonionic surfactant on formation of oil-in-water microemulsions[J].International Journal of Pharmaceutics,2005,288(1):27-34.
[20] ![]() S,PO
S,PO A M.The influence of the structure of selected Brij and Tween homologues on the thermodynamic stability of their binary mixed micelles[J].The Journal of Chemical Thermodynamics,2017,110(7):41-50.
A M.The influence of the structure of selected Brij and Tween homologues on the thermodynamic stability of their binary mixed micelles[J].The Journal of Chemical Thermodynamics,2017,110(7):41-50.
[21] SHAABAN H A,EDRIS A E.Factors affecting the phase behavior and antimicrobial activity of carvacrol microemulsions[J].Journal of Oleo Science,2015,64(4):393-404.
[22] 陶紫, 赵振刚.香茅草精油微乳液的构建及其抗氧化活性分析[J].现代食品科技,2018,34(10):156-164.
TAO Z,ZHAO Z G.Preparation of microemulsion of Cymbopogon citratus(DC)stapf essential oil and analysis of antioxidant activity[J].Modern Food Technology,2018,34(10):156-164.
[23] ZHU X C,HE M,ZHANG W,et al.Formulation design of microemulsion collector based on gemini surfactant in coal flotation[J].Journal of Cleaner Production,2020,257(6):120 496.
[24] FERNANDEZ P,ANDRÉ V,RIEGER J,et al.Nano-emulsion formation by emulsion phase inversion[J].Colloids and Surfaces A:Physicochemical and Engineering Aspects,2004,251(1):53-58.
[25] URMALIYA H,GUPTA M K.Formulation development and evaluation of microemulsion gel of Ketoconazole as an antifungal agent[J].Pharmacia:An International Journal of Pharmaceutical Sciences,2016,2(3):120-130.
[26] WANG M,SHAO Y,LI J,et al.Antioxidative phenolic glycosides from sage(Salvia officinalis)[J].Journal of Natural Products,1999,62(3):454-456.
[27] 邢玉娟.来凤凤菊精油的化学成分、生物活性及微乳化研究[D].武汉:武汉轻工大学,2018.
XING Y J.Study on chemical composition,biological activity and microemulsion of the Dendranthelna indicum essential oil[D].Wuhan:Wuhan Polytechnic University,2018.
[28] SIENIAWSKA ![]()
 ,WOTA M,et al.Microemulsions of essentials oils-Increase of solubility and antioxidant activity or cytotoxicity[J].Food and Chemical Toxicology,2019,129(7):115-124.
,WOTA M,et al.Microemulsions of essentials oils-Increase of solubility and antioxidant activity or cytotoxicity[J].Food and Chemical Toxicology,2019,129(7):115-124.
[29] DENG L L,TAXIPALATI M,SUN P,et al.Phase behavior,microstructural transition,antimicrobial and antioxidant activities of a water-dilutable thymol microemulsion[J].Colloids Surface B Biointerfaces,2015,136(12):859-866.