果汁自然发酵生产果酒是一个复杂的过程,涉及果汁中多种微生物(细菌和酵母)间的相互作用,其中起着核心作用的是酿酒酵母菌株[1]。使用酿酒酵母对果汁进行纯种发酵,可以更好地控制发酵过程,避免感官偏差,确保产品品质的均一性[2-3]。不同酿酒酵母代谢特征和生理特性的差异使最终产品表现出不同的风味特征,进一步影响果酒的感官特性。近年来,酿酒行业更加关注能够生产具有果酒特征香气的酵母菌株,野生酿酒酵母的选择和利用受到大量关注。理想的酵母菌株需要满足某些指标,最重要的是能在高糖浓度下生长,乙醇、二氧化硫的耐受性,硫化氢、挥发酸的低产量等[4-5]。
桃属于蔷薇科,李属,其发源于我国的西北高原,后广泛分布于亚、非、欧、美、澳5个大洲。从营养角度来看,桃子是碳水化合物、有机酸、膳食纤维、维生素B、维生素C、叶酸、矿物质和饮食抗氧化剂(酚类化合物和类胡萝卜素)的良好来源[6-7]。桃品种按照果肉的颜色可以分为白肉桃、红肉桃、黄肉桃和绿肉桃。其中黄肉桃由于糖含量低,有机酸含量高,更适合进一步的工业加工[8]。黄桃果酒是黄桃较理想的食用途径和深加工模式,它可以最大限度的保留黄桃中原有的营养成分,减少收获后多余水果的损失,还可以满足果酒市场多样化的需求。
目前,有大量的文献数据涉及葡萄酒的研究,但少见黄桃果酒酵母筛选及发酵特性的研究[8]。筛选适用于黄桃果汁发酵的酿酒酵母,是提高黄桃果酒香气质量的根本所在。为此,本研究以分离自黄桃果汁自然发酵液和实验室贮存的共403株潜在的酿酒酵母菌株为研究对象,根据其在高糖条件下起始发酵的能力、乙酸和硫化氢生产能力、胁迫条件下的生长能力进行了筛选研究。在此基础上,选择了10株优选酿酒酵母菌株进一步发酵黄桃汁进行香气分析和感官评估,最终获得了4株具有不同理化特性和挥发特性的酿酒酵母菌株,对黄桃果酒质量的提高具有重要的参考价值和实际应用意义。
1 材料与方法
1.1 材料与试剂
1.1.1 培养基
碳酸钙琼脂培养基:0.3%酵母粉、18%葡萄糖、0.3%碳酸钙、1.5%琼脂(均为质量分数);商业Biggy agar培养基,青岛海博生物技术有限公司;黄桃浓缩汁:可溶性固形物44.5%、总酸(18.05±0.11)g/L,福建绿泉公司。
1.1.2 试剂
葡萄糖、蛋白胨、酵母浸粉、琼脂,均为分析纯,国药集团化学试剂有限公司;白砂糖,市售。
1.2 仪器与设备
BSP-250生化培养箱,上海博讯公司;恒温摇床,太仓市强乐实验设备有限公司;立式压力蒸汽灭菌锅,上海实验仪器有限公司;超净工作台,苏净集团苏州安康空气技术有限公司;Waters 1525高效液相色谱仪,美国Waters公司;气相色谱串联质谱联用仪,赛默飞世尔科技有限公司。
1.3 实验方法
1.3.1 酵母菌株的分离
购买来自湖北、山东武台、山东蒙阴、安徽砀山4个不同产地的新鲜黄桃,分别取3~5个黄桃榨汁,调整糖度至20 °Brix,倒入无菌三角瓶中,28 ℃培养箱中自然发酵,发酵后期取样,用0.85%生理盐水连续稀释后取不同浓度的稀释液涂布于YPD平板中,28 ℃ 培养2 d。每组3个平行。从合适稀释度的平板中挑取酿酒酵母形态的菌落,并在YPD琼脂平板上纯化2次,纯化的分离物划线到YPD琼脂斜面上于4 ℃保存,分别编码为HB-1~HB-25,WT-1~WT-25,MY-1~MY-25,DS-1~DS-24。
304株分离自其他水果,保存在实验室的潜在酿酒酵母菌株,编码为A-1~A-304。
酿酒酵母D254作为对照菌株。
1.3.2 酵母菌株性能筛选
1.3.2.1 起始发酵能力[9]
将保存的菌株在10 mL YPD液体试管中28 ℃活化18~24 h后,接种于含糖量200 g/L的含杜氏小管的黄桃汁中,20 ℃静置培养。通过杜氏小管内截留的气泡,观察发酵。48 h内气泡充满杜氏小管的菌株评为起酵能力好,其余菌株评为起酵能力较差。
1.3.2.2 乙酸生产能力
在果酒的发酵过程中,由于溶质浓度高,酵母承受较大的高渗胁迫,这种压力与最终产品中乙酸的产量有关[9]。根据VALLES等[10]描述的方法,将菌株活化后,分别取5 μL点样在碳酸钙琼脂培养基上来测试该特征。酵母产生乙酸的能力是通过菌落周围透明圈的大小进行评价,28 ℃培养3 d后,晕圈<3 mm 的菌株为低产乙酸菌株,晕圈>3 mm的菌株为中产或高产乙酸菌株。
1.3.2.3 硫化氢生产能力
酵母产生的硫化氢与发酵产品中的异味有关,对果酒产生负面影响,发酵过程中硫化氢的形成具有菌株依赖性。将菌株活化后,分别取5 μL点样在Biggy agar培养基上来测试该特征[11-12]。酵母产生硫化氢的能力是通过菌落的颜色进行评价,28 ℃培养2 d后,颜色为白色及浅褐色的菌株评为不产及低产硫化氢菌株,颜色为深棕色及黑色的菌株评为中产及高产硫化氢菌株。
1.3.2.4 乙醇和二氧化硫耐受性
分别在体积分数为8%、12%的乙醇和150、200 mg/L二氧化硫的黄桃培养基中测试菌株耐受性,接种5%,28 ℃活化18 h的菌液,28 ℃,180 r/min培养10~32 h,每隔2 h取样,测定生长曲线。以稳定其平均存活率、滞后时间和比生长速率评价菌株耐受性。
1.3.3 菌株18S rDNA鉴定和系统发育分析
将斜面保藏的菌株活化后,取适量的培养液,采用酵母DNA提取试剂盒提取菌体DNA,用酵母ITS通用引物(引物序列见表1)扩增基因组DNA,测序PCR产物。采用BLAST方式将测定的18S rDNA序列与GenBank中酵母菌的序列进行比对。系统发育和分子进化分析通过分子进化遗传分析软件进行。使用领接(Neihbour-joining,NJ)法计算距离和聚类分析。使用步长检验评估NJ树的拓扑结构。
表1 酵母ITS通用引物序列
Table 1 Sequence of ITS primers

引物名称序列ITS1F-1FCTTGGTCATTTAGAGGAAGTAAITS4B-1RCAGGAGACTTGTACACGGTCCAG
1.3.4 黄桃果酒的发酵
调整浓缩黄桃汁成分至含糖量180 g/L,可滴定酸5.68 g/L,105 ℃灭菌10 min。将菌株活化后以106 个/mL接种于黄桃果汁中,25 ℃发酵。每24 h测定质量损失以监测发酵,当每100 mL发酵液24 h内失重<0.1 g视为发酵结束,发酵结束后离心分离黄桃酒。设置3个生物学平行。
1.3.5 感官分析
感官品评小组由11名老师和同学组成,所有感官品评成员均经过专业培训。在(22±1)℃的室温下,将黄桃酒样品通过品评杯呈递给小组成员。小组成员讨论选择了10个评价指标,包括果香(香气)、甜香(香气)、花香(香气)、愉悦程度(香气)、酸(口感)、甜(口感)、异味(口感)、平衡(口感)、丰满度(口感)、嗜好程度,以描述和区分样品,并使用0~10分对每个属性的强度进行评分。
1.3.6 黄桃果酒的化学分析
残糖、可滴定酸、挥发酸总二氧化硫根据GB/T 15038—2006[13]中描述的方法测定,酒精度根据GB 5009.225—2016[14]中描述的方法测定。
葡萄糖、果糖、蔗糖、甘油和山梨醇的含量通过Waters 1525 HPLC折射率检测器,使用Sugarpak 1 (6.5 mm×300 mm)阳离子交换柱进行分析,流动相为超纯水,流速0.3 mL/min,柱温85 ℃,进样体积 10 μL。有机酸含量通过Waters 1525 HPLC紫外检测器,使用色谱柱Waters X select HSS T3(4.6 mm×250 mm)在206 nm下进行分析,流动相是0.02 mol/L(pH 2.5)磷酸二氢钾缓冲液,流速0.5 mL/min,柱温40 ℃。根据峰的保留时间和它们的峰面积与相应的标准品比较,使用校准曲线进行定量测定。
通过固相微萃取-气相色谱-质谱联用(headspace-solid phase micro extraction-GC-MS,HS-SPME-GC-MS)测定黄桃果酒中挥发性化合物,GC-MS条件参照李凯等[15]的方法。未知化合物的定性通过与NIST 05质谱库中标准谱图比对确定,化合物的定量通过在体积分数10%的乙醇溶液中配制待测化合物标准溶液并绘制标准曲线,依据标准曲线确定果酒中挥发性化合物的浓度。气味活性值(odor activity value,OAV)计算为在果酒中测得的某种物质浓度与其在葡萄酒中气味阈值之间的比率[2]。
1.4 数据处理与统计分析
所有实验数据均以3个独立实验的平均值和标准差表示。使用Origin 2020b和IBM SPSS Statistics 25.0软件进行绘图和显著性分析,SIMCA-P 14.1软件用于偏最小二乘回归分析。
2 结果与分析
2.1 酵母菌株的初筛
在该试验中,从黄桃果汁自然发酵液中分离了99个菌株,以及实验室保藏的304株潜在的酿酒酵母菌株,共有403个菌株用于进一步表征。第一个筛选标准是起始发酵的能力,20 ℃静置48 h后有158个菌株没有产生气泡或产生的气泡没有充满杜氏小管,这意味着它们可能发酵缓慢甚至不发酵糖,起酵能力的筛选排除了这158个菌株。对于乙酸的生产,酿酒酵母菌株在碳酸钙琼脂培养基上显示出很大差异,在该实验中有213个菌株产生的透明圈在3 mm以下,为低产乙酸菌株。通过在Biggy agar培养基上菌株的色素沉着评估酵母产生硫化氢的能力,其中202个菌株形成了白色或浅棕色菌落,归类为低产硫化氢菌株。在403个菌株中有39个菌株起酵速度慢、硫化氢、乙酸产量高。通过以上3个筛选标准排除了317个不适合黄桃果酒发酵的菌株,其他86个菌株表现出较好的发酵性能,对这些菌株进行下一步的技术表征。菌株的分类如图1所示。
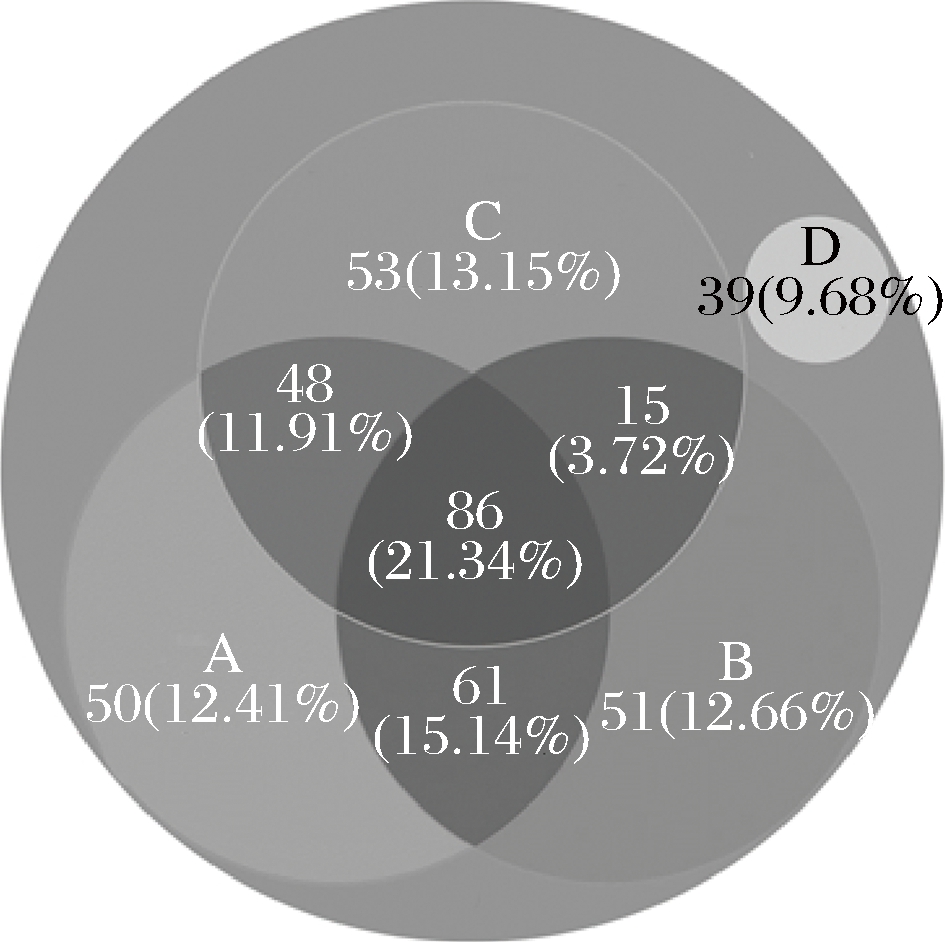
A-起酵速度快;B-低产乙酸;C-低产硫化氢;D-其他
图1 菌株的初步筛选结果韦恩图
Fig.1 Venn diagram of preliminary screening results of strains
优良的酿酒酵母菌株需要能够耐受一定浓度的二氧化硫和乙醇,试验考察了150、200 mg/L二氧化硫对菌株生长的影响,几乎所有菌株都能耐受150~200 mg/L二氧化硫的压力,与空白对照相比,多数菌株没有延迟或在0~4 h的延迟期后达到稳定期,稳定期存活率略有下降。相比之下,乙醇的添加对酵母生长产生较大的影响,不同的乙醇添加量对酵母的抑制程度显示出较大的差异,大部分菌株能够耐受体积分数为8%的乙醇,有43株菌在32 h内表现出明显增长并达到稳定期,然而在体积分数为12%的乙醇条件下,只有10株菌在32 h内表现出明显的增长。乙醇和二氧化硫对菌株生长的影响如表2所示。
表2 乙醇和二氧化硫对菌株生长的影响
Table 2 Effects of ethanol and sulfur dioxide on the growth of strains
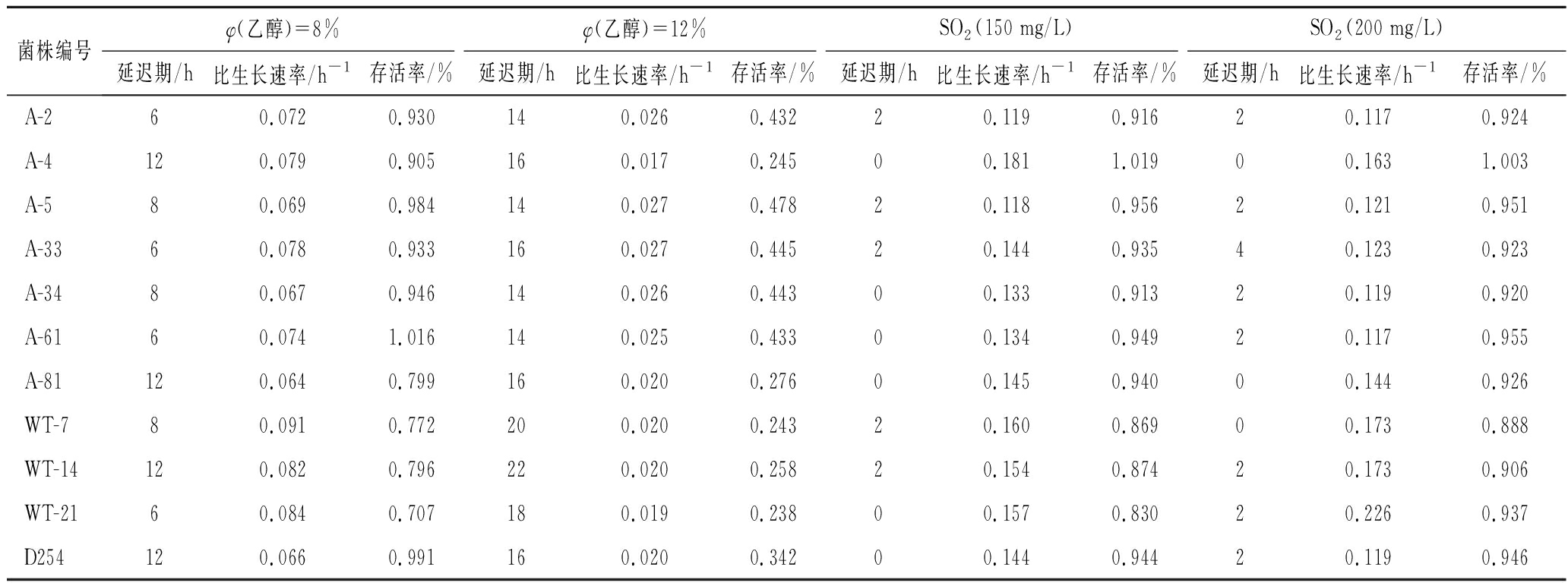
菌株编号φ(乙醇)=8%φ(乙醇)=12%SO2(150 mg/L)SO2(200 mg/L)延迟期/h比生长速率/h-1存活率/%延迟期/h比生长速率/h-1存活率/%延迟期/h比生长速率/h-1存活率/%延迟期/h比生长速率/h-1存活率/%A-260.0720.930140.0260.43220.1190.91620.1170.924A-4120.0790.905160.0170.24500.1811.01900.1631.003A-580.0690.984140.0270.47820.1180.95620.1210.951A-3360.0780.933160.0270.44520.1440.93540.1230.923A-3480.0670.946140.0260.44300.1330.91320.1190.920A-6160.0741.016140.0250.43300.1340.94920.1170.955A-81120.0640.799160.0200.27600.1450.94000.1440.926WT-780.0910.772200.0200.24320.1600.86900.1730.888WT-14120.0820.796220.0200.25820.1540.87420.1730.906WT-2160.0840.707180.0190.23800.1570.83020.2260.937D254120.0660.991160.0200.34200.1440.94420.1190.946
2.2 菌株鉴定
初步筛选获得了10个优选菌株,测定以上10个菌株的18S rDNA序列,并通过NJ法生成了系统发育树。所有筛选菌株与酿酒酵母模式菌株CBS405T,S288CT在100%的步长检验置信度水平上形成了一个簇,表明所有筛选菌株均为酿酒酵母,结果如图2所示。

图2 基于18S rDNA测序构建的酵母菌株系统发育树
Fig.2 Phylogenetic tree of Saccharomyces cerevisiae based on 18S rDNA sequencing
2.3 黄桃果酒的发酵
基于在上述实验中评估的野生酵母的发酵性能,选择了10株发酵性能优良的酿酒酵母进行黄桃果酒的发酵实验,同时以商业酿酒酵母D254作为对照组。发酵完成后,对黄桃果酒的基础理化指标、非挥发性化合物、感官得分和挥发性化合物进行了比较和分析。
2.3.1 基础理化指标分析
黄桃果酒的基础理化指标如表3所示,酿酒酵母WT-7,WT-14,WT-21与商业酿酒酵母D254有相当的发酵速度,均在14 d内完成发酵,而其余菌株在第16天完成发酵,WT系列菌株筛选自黄桃鲜果自然发酵,表明原生环境中的酿酒酵母菌株可能更适合黄桃的发酵。其中有7个菌株的乙醇产量与对照菌株D254没有显著差异,均可以达到体积分数10.50%以上,仅有A-33菌株发酵乙醇含量最低,体积分数为9.56%,发酵相对缓慢。黄桃果酒中的总糖也表现出明显差异,菌株A-5,A-34,WT-7,WT-14,WT-21发酵后总糖相对较少,低于7.24 g/L,相对应的菌株A-33发酵的果酒中总糖含量最高,高达16.15 g/L。该实验中所有发酵后黄桃果酒可滴定酸均高于6.50 g/L,总体酸度较高。所有菌株发酵后的挥发酸度值均低于敏感阈值(0.8 g/L)[11]。
表3 黄桃果酒理化指标
Table 3 Physiochemical indexes of yellow peach wine

编号发酵时间/d酒精度(φ)/%总糖/(g·L-1)pH总酸/(g·L-1)挥发酸/(g·L-1)总SO2/(mg·L-1)A-21610.62±0.09a9.21±1.44b,c3.17±0.05a6.84±0.05a,b0.73±0.02a68.80±2.26abA-41610.50±0.04a9.45±0.68b,c3.22±0.04a7.09±0.10a,b0.72±0.04a72.00±2.26abA-51610.72±0.09a5.79±0.13c3.22±0.02a7.04±0.13a,b0.67±0.05a,b75.20±2.26aA-33169.56±0.16c16.15±0.51a3.18±0.01a7.02±0.05a,b0.71±0.04a65.60±2.26a,bA-341610.60±0.04a6.30±0.34c3.21±0.00a6.82±0.29a,b0.64±0.03a,b72.00±2.26a,bA-611610.13±0.01b12.13±1.91a,b3.22±0.02a7.00±0.08a,b0.42±0.04c46.40±6.79cA-81169.95±0.03b11.82±0.61b3.24±0.01a6.91±0.05a,b0.46±0.00c60.80±0.00bWT-71410.61±0.1a7.24±1.48c3.19±0.01a7.02±0.26a,b0.45±0.01c75.20±2.26aWT-141410.71±0.11a6.53±0.81c3.19±0.03a7.18±0.13a0.45±0.04c75.20±2.26aWT-211410.71±0.00a6.12±1.10c3.19±0.00a7.11±0.03a0.46±0.01c72.89±2.51aD2541410.57±0.14a9.14±0.65b,c3.16±0.04a6.50±0.21b0.55±0.04b,c73.60±0.00a
注:不同字母的值有显著差异(Tukey检验,P<0.05)(下同)
2.3.2 非挥发性组分分析
黄桃果酒中非挥发性组分主要由糖和有机酸组成。研究进一步考察了黄桃果酒样品中的糖和有机酸组成,结果分别如表4和表5所示。对于所有菌株发酵的黄桃果酒,葡萄糖转化率接近100%,蔗糖转化率>95.60%,而果糖转化率在81.40%~96.0%,存在显著差异。其中菌株A-5、A-34、WT-7、WT-14和WT-21发酵后果糖含量低于4.00 g/L,用于黄桃果汁发酵存在显著的优势。黄桃果酒中甘油的质量浓度在3.64~5.22 g/L,菌株A-61发酵黄桃酒甘油含量最高,菌株WT-7和商品菌D254发酵黄桃酒甘油含量最低,甘油的存在会增加果酒的复杂性,赋予果酒甜味,使果酒更加柔和[16]。
表4 黄桃果酒中糖及糖醇含量 单位:g/L
Table 4 Sugar and sugar alcohols of yellow peach wine
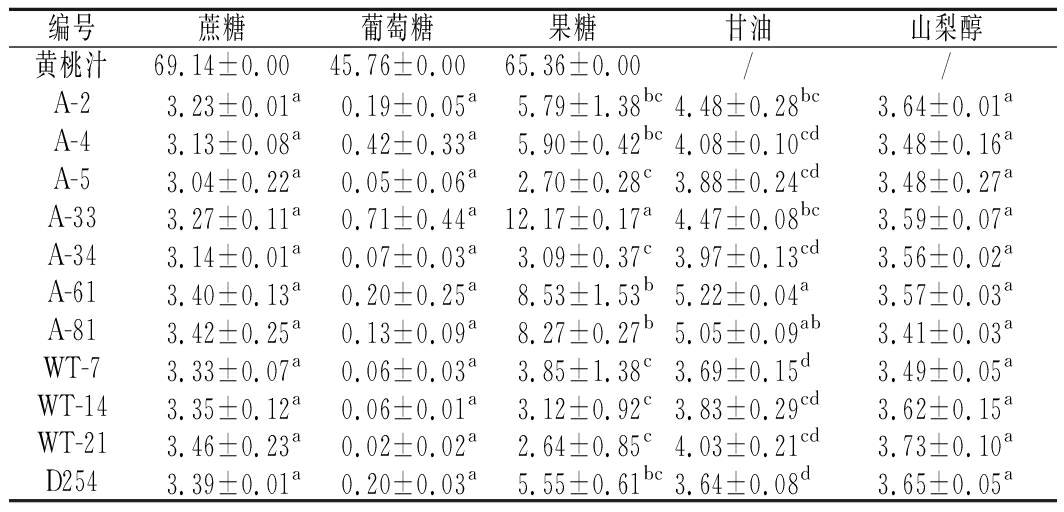
编号蔗糖葡萄糖果糖甘油山梨醇黄桃汁69.14±0.0045.76±0.0065.36±0.00//A-23.23±0.01a0.19±0.05a5.79±1.38bc4.48±0.28bc3.64±0.01aA-43.13±0.08a0.42±0.33a5.90±0.42bc4.08±0.10cd3.48±0.16aA-53.04±0.22a0.05±0.06a2.70±0.28c3.88±0.24cd3.48±0.27aA-333.27±0.11a0.71±0.44a12.17±0.17a4.47±0.08bc3.59±0.07aA-343.14±0.01a0.07±0.03a3.09±0.37c3.97±0.13cd3.56±0.02aA-613.40±0.13a0.20±0.25a8.53±1.53b5.22±0.04a3.57±0.03aA-813.42±0.25a0.13±0.09a8.27±0.27b5.05±0.09ab3.41±0.03aWT-73.33±0.07a0.06±0.03a3.85±1.38c3.69±0.15d3.49±0.05aWT-143.35±0.12a0.06±0.01a3.12±0.92c3.83±0.29cd3.62±0.15aWT-213.46±0.23a0.02±0.02a2.64±0.85c4.03±0.21cd3.73±0.10aD2543.39±0.01a0.20±0.03a5.55±0.61bc3.64±0.08d3.65±0.05a
注:“/”表示未检测(下同)
由表5可以看出,黄桃果汁中的有机酸主要是柠檬酸和奎宁酸[17],占总有机酸总量的74.50%。黄桃果酒中有机酸种类更加丰富,主要有柠檬酸、奎宁酸、琥珀酸、乳酸和苹果酸,占总有机酸含量的86.90%~90.80%。酵母通过酒精发酵产生柠檬酸,果酒中柠檬酸含量较黄桃果汁中增加了8.55%~18.22%,是黄桃酒中含量最高的有机酸。柠檬酸具有令人愉悦的柑橘味[18],口感圆润清爽,A-33菌株发酵后果酒柠檬酸含量最高,为3.18 g/L,A-81最低有2.92 g/L。奎宁酸可作为碳源被菌株利用[19],WT-7、WT-14和WT-21发酵黄桃果酒中奎宁酸表现出明显的下降,推测黄桃来源酿酒酵母对果汁有更好的适应性。果酒中琥珀酸含量在1.03~1.55 g/L,琥珀酸带有酸味和特殊的咸苦味,在果酒成熟的过程中有助于酯类物质的形成[20]。乳酸在发酵过程中形成,是一种比较温和的有机酸,使果酒的口感更加柔和[21],菌株WT-14发酵后乳酸含量最高为1.70 g/L,A-61产生了最少的乳酸为1.03 g/L。苹果酸是酸性较强的有机酸,略带刺激性,黄桃果酒中苹果酸含量在0.76~1.03 g/L,占总有机酸的比例较少,不会对黄桃果酒造成负面影响。
表5 黄桃果酒的有机酸组分 单位:g/L
Table 5 Organic acid components of yellow peach wine
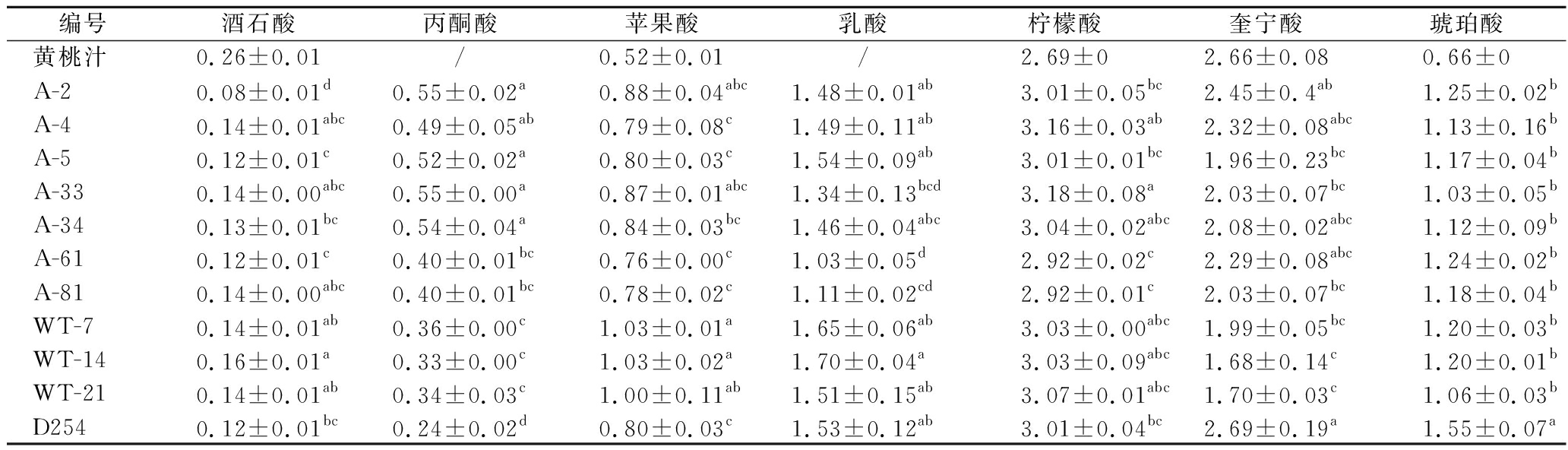
编号酒石酸丙酮酸苹果酸乳酸柠檬酸奎宁酸琥珀酸黄桃汁0.26±0.01/0.52±0.01/2.69±02.66±0.080.66±0A-20.08±0.01d0.55±0.02a0.88±0.04abc1.48±0.01ab3.01±0.05bc2.45±0.4ab1.25±0.02bA-40.14±0.01abc0.49±0.05ab0.79±0.08c1.49±0.11ab3.16±0.03ab2.32±0.08abc1.13±0.16bA-50.12±0.01c0.52±0.02a0.80±0.03c1.54±0.09ab3.01±0.01bc1.96±0.23bc1.17±0.04bA-330.14±0.00abc0.55±0.00a0.87±0.01abc1.34±0.13bcd3.18±0.08a2.03±0.07bc1.03±0.05bA-340.13±0.01bc0.54±0.04a0.84±0.03bc1.46±0.04abc3.04±0.02abc2.08±0.02abc1.12±0.09bA-610.12±0.01c0.40±0.01bc0.76±0.00c1.03±0.05d2.92±0.02c2.29±0.08abc1.24±0.02bA-810.14±0.00abc0.40±0.01bc0.78±0.02c1.11±0.02cd2.92±0.01c2.03±0.07bc1.18±0.04bWT-70.14±0.01ab0.36±0.00c1.03±0.01a1.65±0.06ab3.03±0.00abc1.99±0.05bc1.20±0.03bWT-140.16±0.01a0.33±0.00c1.03±0.02a1.70±0.04a3.03±0.09abc1.68±0.14c1.20±0.01bWT-210.14±0.01ab0.34±0.03c1.00±0.11ab1.51±0.15ab3.07±0.01abc1.70±0.03c1.06±0.03bD2540.12±0.01bc0.24±0.02d0.80±0.03c1.53±0.12ab3.01±0.04bc2.69±0.19a1.55±0.07a
2.3.3 感官分析
根据描述定量分析的关键词对黄桃果酒进行感官品评,图3显示了4个感官品评结果较好的黄桃酒,同时以商品菌D254发酵的黄桃酒为对照。果香是果酒的基本特征,通常被认为是果酒品质的重要指标,菌株WT-21在果香(香气)、丰满度(口感)有最高得分。A-2发酵的黄桃酒在花香(香气)、愉悦程度(香气)、甜(口感)、平衡(口感)、嗜好程度上均有较高得分。A-61在平衡(口感)上有较高的得分。A-34在果香(香气)、愉悦程度(香气)上与A-2有相当的得分,在丰满度(口感)上有较高得分。
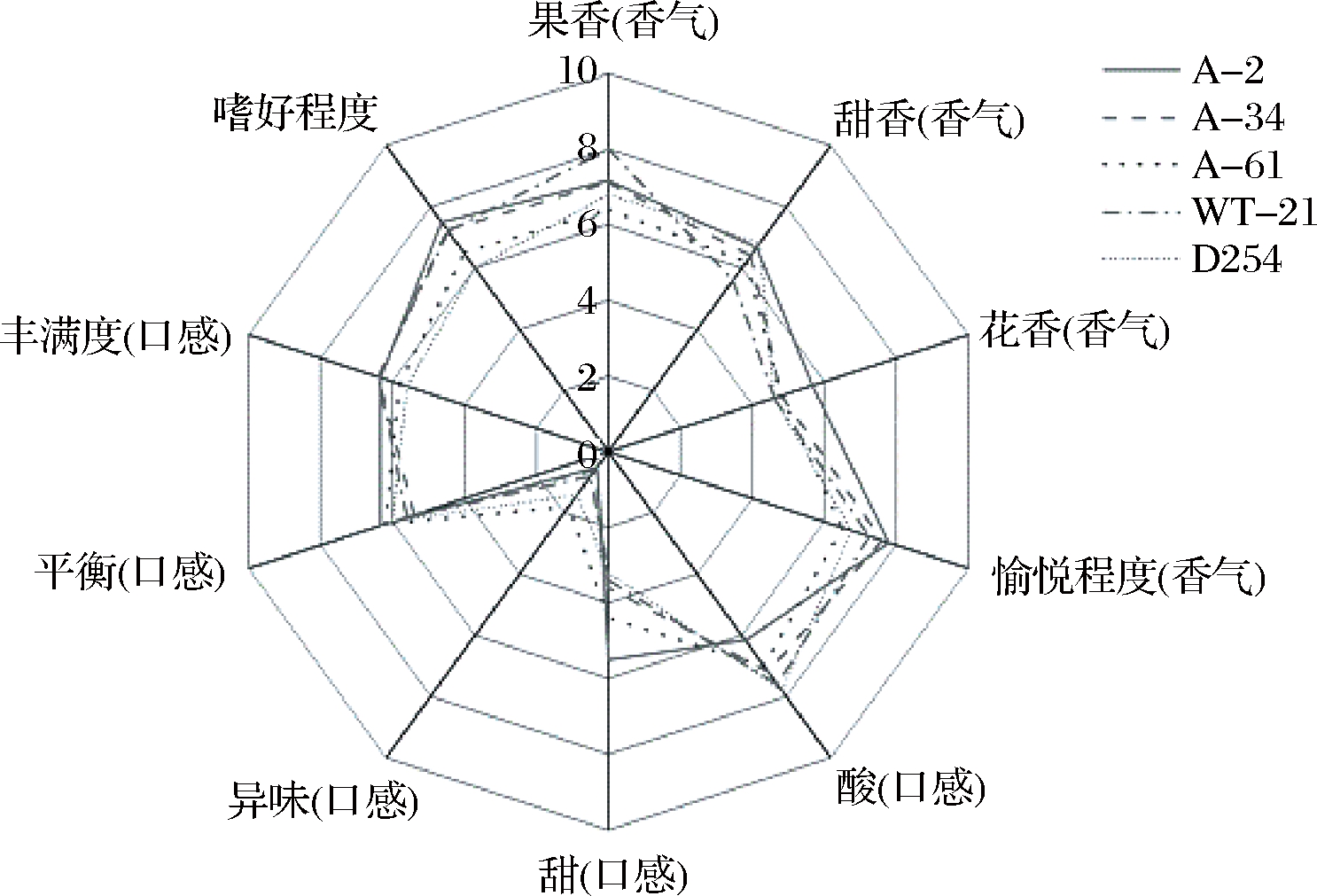
图3 酿酒酵母菌株发酵黄桃果酒的描述定量分析
Fig.3 Quantitative descriptive analysis of wines produced by Saccharomyces cerevisiae strains
2.3.4 挥发性化合物含量分析
2.3.4.1 挥发性化合物半定量分析
主要的挥发性化合物可能在发酵饮料的质量中起重要作用,通过GC-MS对黄桃果酒中的挥发性化合物进行检测,在5种黄桃酒中共检出86种挥发性化合物,其中醇类物质20种,酯类化合物28种,脂肪酸类化合物8种,萜烯/内酯类化合物9种,醛/酮/酚类化合物7种,烷烃/烯烃类化合物14种。不同菌株发酵的黄桃酒中挥发性化合物种类存在一定的差异,WT-21菌株发酵黄桃酒中检出的挥发性化合物种类最少,有67种,A-61检出的化合物种类最多有76种,A-2、A-34和D254分别检出75、72和73种挥发性化合物(数据未显示)。
所有挥发性化合物的聚类热图能够更直观的显示不同菌株发酵黄桃酒中挥发性物质含量的差异,如图4所示,WT-21菌株发酵黄桃酒中多种化合物含量高于其他菌株,如酯类化合物(乙酸乙酯、乙酸异丁酯、乳酸乙酯、乙酸己酯、2-糠酸乙酯)、醇类化合物(异戊醇、异丁醇、9-十烯-1-醇、正丙醇、1-癸醇)、萜烯/内酯类(丙位癸内酯、4-萜品醇、α-松油醇、β-癸内酯)等。D254菌株发酵黄桃酒有较多的乙酸丁酯、丁酸乙酯、4-乙酰氧基丁酸乙酯、正丁醇、癸酸甲酯等。

图4 挥发性化合物含量的聚类热图
Fig.4 Cluster heat map of volatile compound content
A-61发酵黄桃酒中有较多的2-壬醇、香茅醇、丁香酚等。菌株A-34发酵黄桃酒中芳樟醇、异戊酸乙酯、苯甲酸乙酯、大马士酮等较高。菌株A-2发酵黄桃酒中辛酸乙酯、辛酸苯甲酯、月桂酸乙酯、癸酸乙酯、辛酸异戊酯、癸酸异戊酯等较高。
2.3.4.2 挥发性化合物定量及主成分分析(principal component analysis, PCA)
挥发性化合物的半定量分析仅能说明不同菌株发酵黄桃果酒中挥发性化合物含量上的差异,但是挥发性化合物对果酒的影响更多的取决于其在果酒中的实际含量和阈值,在该研究中对黄桃果酒中35种挥发性化合物进行了定量测定,结果如表6所示。
表6 主要挥发性化合物的定量分析
Table 6 Quantitative analysis of main volatile compounds

Cas#中文名称阈值A-2A-34A-61WT-21D254醇类123-51-3异戊醇/(mg·L-1)3067.93±4.29ab85.61±2.31ab70.75±2.37ab100.15±21.01a57.25±4.07b60-12-8苯乙醇/(mg·L-1)1423.01±2.66a21.76±1.58a13.51±0.14ab18.92±4.21ab11.28±0.87b71-23-8正丙醇/(mg·L-1)914.59±0.87a13.52±0.35a13.65±0.86a17.82±3.46a17.07±1.29a78-83-1异丁醇/(mg·L-1)4032.07±0.84bc38.82±1.26ab34.25±0.09bc53.78±8.33a23.34±0.86c71-36-3正丁醇/(mg·L-1)1500.83±0.11ab0.84±0.07ab0.74±0.07b0.94±0.28ab1.42±0.15a143-08-8正壬醇/(mg·L-1)-0.76±0.02a0.63±0.06a0.79±0.18a1.12±0.28a0.89±0.02a111-27-3正己醇/(μg·L-1)8 000102.11±0.81a102.10±0.40a102.01±0.21a103.67±1.77a102.01±0.10a104-76-7异辛醇/(μg·L-1)-29.40±0.42a29.26±0.12a28.89±0.11a28.85±0.04a28.84±0.17a40716-66-3反式橙花叔醇/(μg·L-1)-6.96±1.27a6.47±0.14a3.80±0.10b2.80±0.51b1.85±0.23b总醇/(mg·L-1)139.33±8.79ab161.32±2.98ab133.84±3.17ab192.86±37.56a111.39±7.21b酯类141-78-6乙酸乙酯/(mg·L-1)12.2721.64±0.64a20.78±0.33a20.44±0.56a22.18±2.00a18.97±0.54a123-92-2乙酸异戊酯/(μg·L-1)30334.95±7.35a373.09±9.48a498.76±20.42a562.46±16.79a570.65±132.40a110-19-0乙酸异丁酯/(μg·L-1)1 600132.41±0.31b133.64±1.82b138.67±1.23b153.16±3.13a135.67±3.96b142-92-7乙酸己酯/(μg·L-1)1 5000.32±0.00a0.31±0.00a0.31±0.00a0.34±0.02a0.31±0.01a112-14-1乙酸辛酯/(μg·L-1)50 0000.23±0.00bc0.21±0.00c0.27±0.00a0.26±0.00ab0.21±0.02c103-45-7乙酸苯乙酯/(μg·L-1)2500.28±0.01a0.25±0.02a0.22±0.00a0.26±0.02a0.22±0.01a97-64-3乳酸乙酯/(mg·L-1)14 0005.52±0.27b5.47±0.03b5.23±0.01b6.61±0.03a5.36±0.03b105-54-4丁酸乙酯/(μg·L-1)20293.44±0.05bc289.65±0.60c313.98±2.24ab283.87±2.08c323.89±21.17a123-66-0己酸乙酯/(μg·L-1)1415.39±0.71a13.83±0.29a14.44±0.01a9.98±0.21b13.22±1.85ab108-64-5异戊酸乙酯/(μg·L-1)39.05±0.14ab9.29±0.53a8.6±0.10ab7.98±0.06b8.02±0.33b106-32-1辛酸乙酯/(μg·L-1)6000.15±0.02a0.1±0.01bc0.12±0ab0.07±0.01c0.08±0.01c123-29-5壬酸乙酯/(μg·L-1)1 3004.72±0.07a4.63±0.05a4.63±0.03a4.61±0.02a4.63±0.02a614-99-32-糠酸乙酯/(μg·L-1)16 00013.97±0.54a13.87±0.34a14.01±0.22a16.17±1.3a14.38±0.23a110-38-3癸酸乙酯/(μg·L-1)20014.63±3.89a10.71±1.01ab8.3±0.31ab5.59±0.72b8.02±0.81ab106-33-2月桂酸乙酯/(μg·L-1)5003.61±0.29a3.39±0.13a3.17±0.00a3.13±0.03a3.17±0.07a30673-38-2癸酸异丁酯/(μg·L-1)-1.73±0.11a1.67±0.01ab1.57±0.01ab1.52±0.02b1.5±0.02b2306-91-4癸酸异戊酯/(μg·L-1)-57.6±0.16a57.52±0.06a57.46±0.02a57.35±0.00a57.35±0.00a总酯/(mg·L-1)28.04±0.92a27.16±0.29a26.73±0.55a29.89±2.28a25.47±0.41a酚/醛96-76-42,4-二叔丁基苯酚/(μg·L-1)~200106.27±8.75a99.78±1.83a99.40±0.64a103.52±3.2a100.74±10.88a萜烯/内酯78-70-6芳樟醇/(μg·L-1)2511.64±0.54a11.86±0.51a11.82±0.08a9.02±0.45b10.45±0.10ab106-22-9(R)-(+)-β-香茅醇/(μg·L-1)10022.44±0.81a23.55±0.25a24.66±0.03a18.38±0.99b17.15±0.18b706-14-9丙位癸内酯/(μg·L-1)88114.45±0.41a114.69±0.29a114.44±0.09a115.24±1.04a114.44±0.44a705-86-2δ-癸内酯/(μg·L-1)386187.76±3.56a189.17±2.85a188.2±0.58a193.11±6.52a188.11±1.87a总萜烯/内酯/(μg·L-1)336.28±5.32a339.28±3.90a339.13±0.60a335.76±8.99a330.14±2.40a脂肪酸142-62-1己酸/(mg·L-1)0.423.97±0.08a4.01±0.35a4.35±0.09a3.85±0.23a3.97±0.08a124-07-2辛酸/(mg·L-1)0.53.97±0.39a4.05±0.52a4.52±0.02a4.32±0.54a4.34±0.24a334-48-5正癸酸/(mg·L-1)14.03±0.46a3.96±0.35a4.32±0.13a3.65±0.12a3.84±0.07a143-07-7正十二烷酸/(mg·L-1)10.31±0.04a0.28±0.02a0.27±0.02a0.26±0.01a0.26±0.02a总脂肪酸/(mg·L-1)12.28±0.98a12.30±1.24a13.46±0.06a12.08±0.90a12.42±0.41a
注:“-”表示未查到
高级醇在数量上是果酒中最大的芳香族化合物,高级醇质量浓度低于300 mg/L可以对果酒产生积极的影响[22]。黄桃果酒中高级醇含量在111.4~192.9 mg/L,异戊醇、异丁醇、2-苯基乙醇和正丙醇是黄桃果酒中含量最多的高级醇。酿酒酵母WT-21发酵黄桃果酒高级醇含量最高,相比于对照菌株D254提高了73.10%。
酯类化合物主要包括乙酸酯类和脂肪酸乙酯类。乙酸酯通过高级醇的酯化反应产生[2]。乙酸乙酯是黄桃果酒中含量最高的乙酸酯,低浓度下会增加果酒的香气复杂性,质量浓度高于150 mg/L的情况下会给葡萄酒带来难闻的气味(醋味)[12],黄桃果酒中乙酸乙酯含量在18.96~22.17 mg/L,WT-21是乙酸乙酯最高生产者,D254则是较小生产者。其次是乙酸异戊酯,菌株WT-21和D254发酵黄桃酒中乙酸异戊酯产量相对较高有0.56 mg/L,酿酒酵母A-2发酵的黄桃果酒中乙酸异戊酯产量最低为0.33 mg/L。乳酸乙酯是黄桃果酒中含量最高的脂肪酸乙酯,平均含量为5.23~6.61 mg/L,乳酸乙酯能够提高发酵饮料的果香和花香[23]。至于丁酸乙酯、己酸乙酯和异戊酸乙酯在黄桃果酒中含量较低,但其OAV>1,可能对黄桃果酒的风味带来积极的影响。
脂肪酸主要在发酵过程中形成,低水平下(<20 mg/L)这组挥发物对果酒的风味产生积极的影响,但在高浓度下会产生汗水,酸味和稀薄的味道[21]。黄桃果酒中的脂肪酸主要有正癸酸、辛酸和己酸,OAV>1,总脂肪酸含量<14 mg/L。己酸、辛酸在果酒中有很高的香气强度,并赋予果酒甜美,水果和奶酪的香气[2]。癸酸带有脂肪味,可能对果酒的香气带来负面影响[24]。果酒中的脂肪酸除了本身带有的香气之外,在阻止其酯类物质水解方面也具有重要作用。
在所有黄桃酒中都检出了其他微量挥发性化合物,例如芳樟醇(柑桔香气)、β-香茅醇、γ-癸内酯和δ-癸内酯。萜烯化合物与花香和柠檬香气有关[25],芳樟醇为酒精饮料增添了花香和果香的香气。内酯被认为是桃香气的主要贡献者,特别是γ-和δ-癸内酯被认为是特征影响化合物[26]。
挥发性化合物对果酒风味的贡献取决于OAV,OAV>1的挥发物通常被认为是能够促进葡萄酒香气的化合物[11]。通过PCA以确定不同酿酒酵母生产的黄桃果酒的风味差异,将OAV>1的13种挥发性化合物用作变量。如图5所示,前2个主成分方差的累积贡献率为69.1%,其中PC1和PC2分别解释了40.8%和28.3%的方差。所有方差都是由挥发性化合物产生的,这些化合物能够将5种黄桃酒区分开来。图5中每个酵母发酵黄桃酒的3个独立重复结果相对接近,表明样品之间的可重复性。与第一主成分呈正相关的化合物有乙酸乙酯、异戊醇、异丁醇、丙位癸内酯,WT-21发酵黄桃酒主成分得分负载在PC1正向,说明与其他菌株发酵黄桃酒相比,WT-21发酵黄桃酒与乙酸乙酯、异戊醇、异丁醇、丙位癸内酯有很强的相关性。与第二主成分呈正相关的化合物有异戊酸乙酯、苯乙醇、己酸乙酯。A-34和A-2发酵黄桃酒负载在PC2的正向,与苯乙醇、异戊酸乙酯、己酸乙酯相关性较高,其主成分得分有部分重叠,表明主要挥发性化合物含量有相似的特征。菌株A-61和D254发酵黄桃酒与丁酸乙酯、己酸、乙酸异戊酯相关性较高。
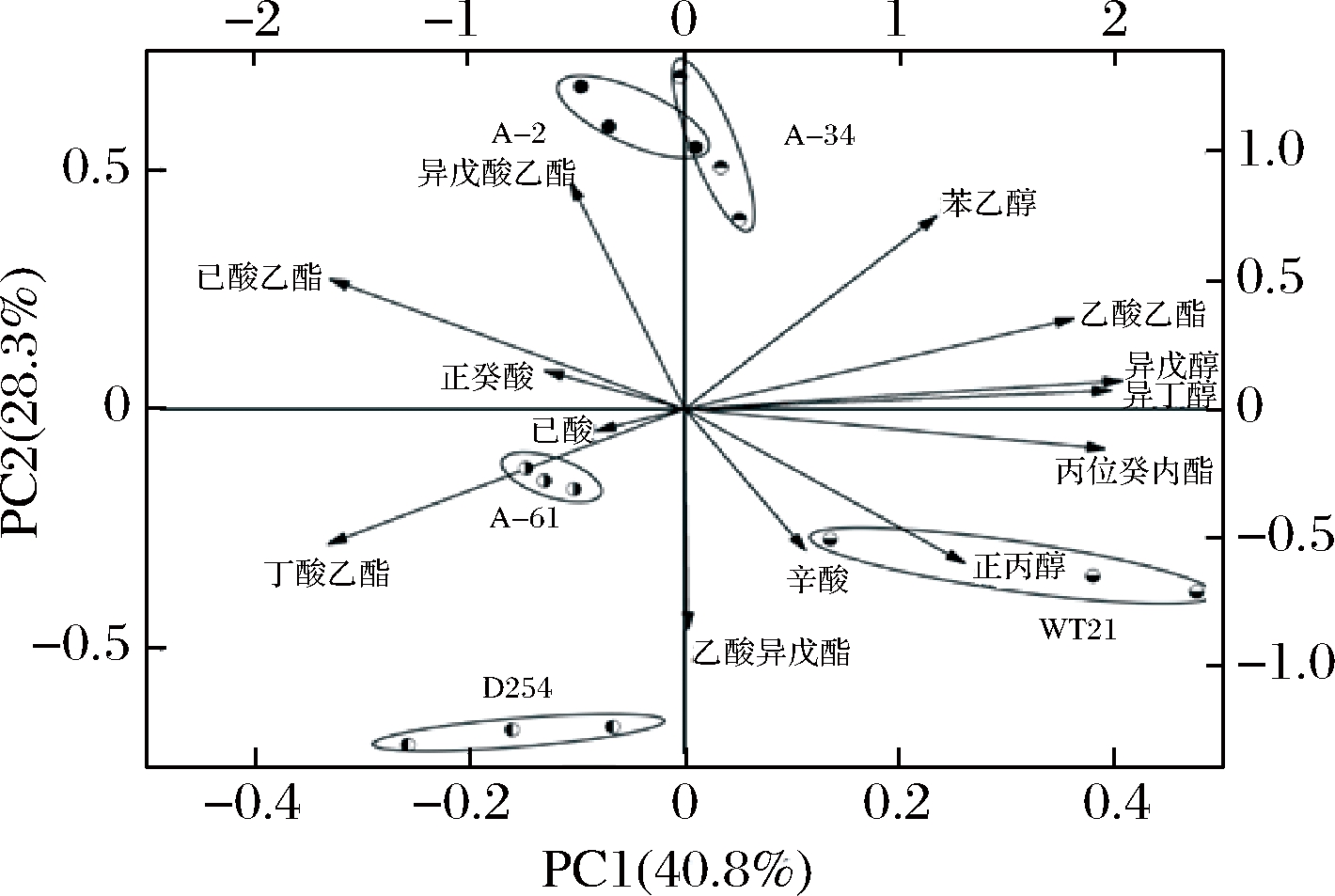
图5 主成分得分和载荷双标图
Fig.5 Loading plot and score plot of principal components analysis
2.3.5 偏最小二乘回归分析
为了揭示黄桃果酒中感官属性与挥发性化合物之间的关系,使用SIMCA 14.1软件进行了偏最小二乘回归(partial least squares,PLS)分析。由所有挥发物(X变量)和4个感官描述词(Y变量)生成的初始相关模型中61.3%的X变量解释了83.0%的感官属性变异。根据LI等[27]的研究,投影的变量重要性值(variable importance for the projection,VIP)<1的变量与解释Y变量的关系最小,因此从矩阵中删除了23个无关紧要的变量。生成了包含63种挥发性化合物和4个感官描述符的新集合,其中75.2%的X变量解释了80.7%的Y变量,如图6所示。

图6 黄桃果酒的挥发性和感官变量的偏最小二乘分析
Fig.6 Partial least squares analysis of volatility and
sensory variables of yellow peach wine
注:挥发性化合物:1-乙酸苯乙酯;2-丁酸乙酯;3-辛酸乙酯;
4-月桂酸乙酯;5-3-羟基十三酸乙酯;6-乙酸异丁酯;7-癸酸乙酯;
9-正辛醇;10-正壬酸;11-十一醇;12-异戊醇;13-正己酸乙酯;
14-乙酸异戊酯;16-癸烷;17-壬醛;18-乙酸乙酯;20-月桂酸;
21-1-壬醇;22-9-癸烯酸;25-2-十一醇;
26-(E)-7,11-二甲基-3-亚甲基-1,6,10-十二碳三烯;
27-辛酸异戊酯;28-癸酸异戊酯;30-7-辛酸乙酯;31-反式-橙花叔醇;
32-3-呋喃甲醇;33-法呢醇;34-3-甲硫基丙醇;36-六甲基环三硅氧烷;
38-八甲基环四硅氧烷;41-4-萜烯醇;42-苯乙醇;43-2-糠酸乙酯;
45-2-壬醇;46-己酸-2-苯乙酯;47-正十四烷;49-9-癸烯酸乙酯;
50-正丙醇;52-(+)-α-松油醇;53-芳樟醇;54-异丁醇;55-2-壬酮;
56-苯甲酸乙酯;58-乳酸乙酯;59-辛酸苯乙酯;60-壬烯;
61-邻苯二甲酸二丁酯;62-1-癸醇;63-戊基环丙烷;64-反式十六烷
基乙酸酯;66-(-)-4-萜品醇;69-异戊酸乙酯;73-L(-)-乳酸乙酯;
74-邻苯二甲酸二异丁酯;76-4-乙酰氧基丁酸乙酯;
77-二氢-β-紫罗兰醇;78-丙位丁内酯;80-δ-癸内酯;
81-丙位癸内酯;83-9-十烯-1-醇;84-2-甲氧基-3-(2-丙烯-1-基)-苯酚;
85-乙酸丁酯;86-乙酸己酯。感官属性:果香、花香、甜香和愉悦程度
由图6可以看出,“果香”位于第一象限,最大系数对应于18、1、54、83、58、12、34、61、47、26。“甜香”位于第三象限,最大系数对应于13、55、25、56、45、69、53、2。“花香”位于第二象限,与60、4、7、27、46、31、30、20相关性较高。“愉悦程度”负载位于正Y轴附近,与1、42、60、21、18、4、46、20、30、27、31相关性较高。PLS结果可以很好的解释从感官品评获得的黄桃酒之间的感官差异。WT-21在“果香”上有最高得分可能与乙酸乙酯(果味)、乙酸苯乙酯(玫瑰花香、果香)、乳酸乙酯(水果、奶油香气)、异戊醇(苹果白兰地香气)的较高含量有关。A-2和A-34在“花香”和“愉悦程度”的得分较高可能与月桂酸乙酯(花香、甜香、果香)、苯乙醇(玫瑰花香)、癸酸乙酯(椰子香)、1-壬醇(玫瑰、橙香)、辛酸异戊酯(水果香)、乙酸苯乙酯(玫瑰花香、果香)、辛酸苯乙酯(果香)的较高强度有关。D254在“甜香”上的较高得分可能与丁酸乙酯(草莓、苹果)、苯甲酸乙酯(水果香)有关。
3 结论
本研究基于菌株生长实验、耐受性实验、感官品评及风味组分分析,筛选获得了4株生长和发酵性能优良的酿酒酵母菌株。其中,酿酒酵母菌株WT-21在14 d内完成发酵,对黄桃果汁中的果糖、奎宁酸有很好的利用能力,发酵产生的黄桃果酒中多种酯类化合物、醇类化合物、萜烯内酯类化合物含量高于其他菌株,总醇和总酯的含量相比于商业菌株D254提高了73.1%和17.4%,在感官品评中有最高的“果香”和“丰满度”得分,这些特征使得它可以生产出具有强烈香气的黄桃果酒。菌株A-61发酵黄桃酒中甘油含量最高,为5.22 g/L,挥发性化合物种类最多有76种,在感官品评中有最高的“平衡”(口感)得分,可用于提高黄桃果酒的香气复杂性。菌株A-2和A-34发酵的黄桃果酒在“花香”和“愉悦程度”上有最高得分,多种产生花香的挥发性化合物含量高于其他菌株,可用于生产更具花香的黄桃酒。本研究提供了一种系统选育黄桃果酒酵母的方法,基于该方法筛选得到的4株酿酒酵母菌株具有各自典型的酿造品质,对特征性黄桃果酒产品开发具有重要的参考价值和较强的工业应用前景。
[1] ![]() H, VR
H, VR NOV
NOV D, OMELKOV
D, OMELKOV J.Isolation, identification and characterization of regional indigenous Saccharomyces cerevisiae strains[J].Brazilian Journal of Microbiology, 2016,47(1):181-190.
J.Isolation, identification and characterization of regional indigenous Saccharomyces cerevisiae strains[J].Brazilian Journal of Microbiology, 2016,47(1):181-190.
[2] LORENZINI M, SIMONATO B, SLAGHENAUFI D, et al.Assessment of yeasts for apple juice fermentation and production of cider volatile compounds[J].LWT, 2019,99:224-230.
[3] SETTANNI L, SANNINO C, FRANCESCA N, et al.Yeast ecology of vineyards within Marsala wine area (western sicily) in two consecutive vintages and selection of autochthonous Saccharomyces cerevisiae strains[J].Journal of Bioscience and Bioengineering, 2012,114(6):606-614.
[4] ORTIZ M J, BARRAJ N N, BAFFI M A, et al.Spontaneous must fermentation:Identification and biotechnological properties of wine yeasts[J].LWT, 2013,50(2):371-377.
N N, BAFFI M A, et al.Spontaneous must fermentation:Identification and biotechnological properties of wine yeasts[J].LWT, 2013,50(2):371-377.
[5] LIU N, QIN Y, SONG Y Y, et al.Selection of indigenous Saccharomyces cerevisiae strains in Shanshan County (Xinjiang, China) for winemaking and their aroma-producing characteristics[J].World Journal of Microbiology & Biotechnology, 2015,31(11):1 781-1 792.
[6] CAO S F, LIANG M H, SHI L Y, et al.Accumulation of carotenoids and expression of carotenogenic genes in peach fruit[J].Food Chemistry, 2017,214:137-146.
[7] VARGAS E F D, JABLONSKI A, FL RES S H, et al.Waste from peach (Prunus persica) processing used for optimization of carotenoids ethanolic extraction[J].International Journal of Food Science and Technology, 2017,52(3):757-762.
RES S H, et al.Waste from peach (Prunus persica) processing used for optimization of carotenoids ethanolic extraction[J].International Journal of Food Science and Technology, 2017,52(3):757-762.
[8] ![]() S M,
S M, ![]() M M, et al.Physicochemical, antioxidant and sensory properties of peach wine made from redhaven cultivar[J].Journal of Agricultural and Food Chemistry, 2013,61(6):1 357-1 363.
M M, et al.Physicochemical, antioxidant and sensory properties of peach wine made from redhaven cultivar[J].Journal of Agricultural and Food Chemistry, 2013,61(6):1 357-1 363.
[9] PANDO BEDRI ANA R,MANGAS ALONSO J J,SU
ANA R,MANGAS ALONSO J J,SU REZ VALLES B.Evaluation of autochthonous Saccharomyces bayanus strains under stress conditions for making ice ciders[J].LWT-Food Science and Technology, 2017,81:217-225.
REZ VALLES B.Evaluation of autochthonous Saccharomyces bayanus strains under stress conditions for making ice ciders[J].LWT-Food Science and Technology, 2017,81:217-225.
[10] VALLES B S, BEDRI ANA R P, QUEIPO A L, et al.Screening of cider yeasts for sparkling cider production (Champenoise method)[J].Food Microbiology, 2008,25(5):690-697.
ANA R P, QUEIPO A L, et al.Screening of cider yeasts for sparkling cider production (Champenoise method)[J].Food Microbiology, 2008,25(5):690-697.
[11] GAROFALO C, BERBEGAL C, GRIECO F, et al.Selection of indigenous yeast strains for the production of sparkling wines from native Apulian grape varieties[J].International Journal of Food Microbiology, 2018,285:7-17.
[12] MAURIELLO G, CAPECE A, D'AURIA M, et al.SPME-GC method as a tool to differentiate VOC profiles in Saccharomyces cerevisiae wine yeasts[J].Food Microbiology, 2009,26(3):246-252.
[13] 中华人民共和国国家质量监督检验检疫局, 中国国家标准化管理委员会.GB/T 15038—2006 葡萄酒、果酒通用分析方法[S].北京:中国标准出版社, 2007.
State Administration of Quality Supervision, Inspection and Quarantine of the People′s Republic of China, China National Standardization Administration Committee.GB/T 15038—2006 Analytical methods of wine and fruit wine[S].Beijing:China Standards Press, 2007.
[14] 中华人民共和国国家卫生和计划生育委员会. GB 5009.225—2016 食品安全国家标准 酒中乙醇浓度的测定[S]. 北京: 中国标准出版社, 2016.
State health and Family Planning Commission of the people′s Republic of China. GB/T 15038—2006 Determination of ethanol concentration in wine in national food safety standards[S]. Beijing: China Standards Press, 2016.
[15] 李凯, 王金晶, 李永仙, 等.红心火龙果果酒特征香气分析[J].食品与发酵工业,2019,45(13):217-223.
LI K, WANG J J, LI Y X, et al.Characteristic aroma components of red pitaya wine[J].Food and Fermentation Industries, 2019,45(13):217-223.
[16] SU REZ-LEPE A J, MORATA A.New trends in yeast selection for winemaking[J].Trends in Food Science & Technology, 2011,23(1):39-50.
REZ-LEPE A J, MORATA A.New trends in yeast selection for winemaking[J].Trends in Food Science & Technology, 2011,23(1):39-50.
[17] GUO C T, BI J F, LI X, et al.Antioxidant profile of thinned young and ripe fruits of Chinese peach and nectarine varieties[J].International Journal of Food Properties, 2020,23(1):1 272-1 286.
[18] VILELA A.Use of nonconventional yeasts for modulating wine acidity[J].Fermentation, 2019,5(1):27.
[19] WU B H, GENARD M, LESCOURRET F, et al.Influence of assimilate and water supply on seasonal variation of acids in peach (cv Suncrest)[J].Journal of the Science of Food and Agriculture, 2002,82(15):1 829-1 836.
[20] BARO M, FIALA J.Chasing after minerality, relationship to yeast nutritional stress and succinic acid production[J].Czech Journal of Food Sciences, 2012,36:188-193.
M, FIALA J.Chasing after minerality, relationship to yeast nutritional stress and succinic acid production[J].Czech Journal of Food Sciences, 2012,36:188-193.
[21] CHIDI B S, BAUER F F, ROSSOUW D.Organic acid metabolism and the impact of fermentation practices on wine acidity:A review[J].South African Journal of Enology and Viticulture, 2018,39(2):1-15.
[22] LIN X, HU X P, WU W Y, et al.Evaluation of the volatile profile of wax apple (Syzygium samarangense) wines fermented with different commercial Saccharomyces cerevisiae strains[J].Food Science and Biotechnology, 2019,28(3):657-667.
[23] BARBOSA E A, SOUZA M T, DINIZ R H S, et al.Quality improvement and geographical indication of cachaça(Brazilian spirit) by using locally selected yeast strains[J].Journal of Applied Microbiology, 2016,121(4):1 038-1 051.
[24] SHU Y S,CHANG Y C,TENG F S, et al.Evaluation of sequential inoculation of Saccharomyces cerevisiae and Oenococcus oeni strains on the chemical and aromatic profiles of cherry wines[J].Food Chemistry, 2013,138(4):2 233-2 241.
[25] S NCHEZ-PALOMO E, TRUJILLO M, RUIZ G A, et al.Aroma profile of malbec red wines from La Mancha region:Chemical and sensory characterization[J].Food Research International, 2017,100:201-208.
NCHEZ-PALOMO E, TRUJILLO M, RUIZ G A, et al.Aroma profile of malbec red wines from La Mancha region:Chemical and sensory characterization[J].Food Research International, 2017,100:201-208.
[26] CANO-SALAZAR J, ECHEVERR A G, CRISOSTO C H, et al.Cold-storage potential of four yellow-fleshed peach cultivars defined by their volatile compounds emissions, standard quality parameters, and consumer acceptance[J].Journal of Agricultural and Food Chemistry, 2012,60(5):1 266-1 282.
A G, CRISOSTO C H, et al.Cold-storage potential of four yellow-fleshed peach cultivars defined by their volatile compounds emissions, standard quality parameters, and consumer acceptance[J].Journal of Agricultural and Food Chemistry, 2012,60(5):1 266-1 282.
[27] LI H M, JIANG D Q, LIU W L, et al.Comparison of fermentation behaviors and properties of raspberry wines by spontaneous and controlled alcoholic fermentations[J].Food Research International, 2020,128:108 801.