壶瓶碎米荠(Cardamine hupingshanensis),又称虎耳金,是十字花科碎米荠属植物,性平、味苦,具有止咳平喘、活血等功效[1-2]。其幼嫩茎叶是一种珍稀的野菜,可作蔬菜食用。碎米荠中含有丰富的水分、蛋白质、可溶性糖、氨基酸、维生素C、纤维素以及硒[3]。其中恩施地区壶瓶碎米荠硒含量丰富,它的根、芽和叶中硒的平均含量分别可以达到2 985、3 329和2 491 mg/kg[4-5]。
植物中营养成分繁多,在提取不同成分时,有着比较复杂的传质和传热过程[6-7]。部分植物多糖已经探索出了相关提取动力学模型[8-10],但没有普遍适用于所有植物多糖的提取动力学模型。目前壶瓶碎米荠多糖的研究主要在硒多糖提取、纯化等过程的工艺优化和活性方面探究[11-13],缺少从理论上探究其提取过程的相关研究。如何提高壶瓶碎米荠多糖的提取得率对开发、生产壶瓶碎米荠多糖相关产品的成本和经济效益有很大影响。因此,建立一个可靠的壶瓶碎米荠多糖提取动力学模型是十分必要的。本文结合Fick第二扩散定律[14]对超声提取壶瓶碎米荠多糖进行建模,采用超声辅助提取壶瓶碎米荠多糖,同时, 从理论上探究壶瓶碎米荠多糖提取过程, 得到相应的提取动力学方程和相关参数,从而为壶瓶碎米荠多糖的提取提供理论依据和技术支撑。
1 材料与方法
1.1 材料与试剂
材料:壶瓶碎米荠购买于湖北恩施新塘乡,55 ℃烘干后粉碎过100目筛备用。
试剂:无水乙醇、标准葡萄糖溶液、浓硫酸、苯酚等均为分析纯。
1.2 仪器与设备
GZX-9246MBE 电热鼓风干燥箱,上海博迅医疗生物仪器股份有限公司; LD-Y500A高速万能粉碎机,上海顶帅电器有限公司; KQ-300DE 数控超声波清洗仪,昆山市超声仪器有限公司; UV-8000H 紫外-可见分光光度计,上海元析仪器有限公司;低速冷冻离心机,湖南湘仪实验室仪器开发有限公司。
1.3 提取及检测方法
1.3.1 壶瓶碎米荠多糖超声提取
多糖的提取参考相关文献[13],略有改动。将采购的壶瓶碎米荠用水洗净后于55 ℃烘干,粉碎过100目筛, 在超声辅助条件下进行提取然后通过离心、过滤、冻融、醇沉12 h,再次进行离心、过滤、干燥得到多糖粗品。在固液比1∶30的条件下,分别在超声功率120、180、240和300 W 4个水平上进行处理。同时,提取温度设为293、313、333、353K。所有试验中,提取时间设为10、20、30、40、50、60、70和80 min 8个水平。所有试验做3个平行处理。
1.3.2 多糖含量测定
壶瓶碎米荠多糖含量测定参考相关文献[13, 15]进行。以葡萄糖标准品的质量浓度值(单位:mg/mL)为横坐标(x),吸光度值为纵坐标(y),作标准曲线,计算得到方程为:y=10.405x+0.007 7(R2=0.999 1,质量浓度值为0~0.84 mg /mL时,质量浓度和吸光度值的线性关系良好)。吸取1 mL复溶后的样液,置于试管中,加1 mL 6%(体积分数)苯酚溶液,混匀,再加入浓硫酸5 mL,摇匀,以相应试剂为空白管,同时进行 15 min的沸水浴,冷却后在490 nm下测定吸光度。
1.4 壶瓶碎米荠多糖提取动力学模型建立
本试验以壶瓶碎米荠为原料,以水为溶剂,分析、探究超声提取壶瓶碎米荠多糖的提取动力学过程。壶瓶碎米荠多糖在提取过程中涉及到溶质的扩散理论[16],在提取过程主要包括溶剂浸润、内扩散和外扩散3个过程[17]。在提取过程中,壶瓶碎米荠粉末颗粒中的多糖含量在不断减少,是一个非稳态的扩散过程。因此可以利用Fick第二定律研究壶瓶碎米荠多糖提取过程[18-19]。
假设:(1)壶瓶碎米荠粉碎成均匀的球型颗粒;(2)多糖的扩散是从球型颗粒内部沿着半径方向进行的;(3)提取过程中,壶瓶碎米荠颗粒内部多糖的质量浓度不随时间改变,扩散系数也不变,整个提取过程壶瓶碎米荠内部温度一致;(4)不考虑多糖在壶瓶碎米荠颗粒表面的传质阻力。其中,设定壶瓶碎米荠粉末半径为 R,颗粒内的溶剂体积为V1提取过程中,t 时刻颗粒内距球表面为 r 处的有效成分质量浓度为 C,D表示内扩散系数。C∞为平衡浓度,C0为初始浓度。
根据Fick第二定律:
(1)
式中:![]() 表示浓度变化率,
表示浓度变化率,![]() 分别是X、Y、Z轴上的浓度梯度。
分别是X、Y、Z轴上的浓度梯度。
假定壶瓶碎米荠为球型,满足球对称扩散。
(2)
令f=Cr 边界条件为:r=0,f=0,则:依据傅里叶变换得:
(3)
(4)
因为多糖的浓度分布是无穷极分布,其高次项趋近于零,可以忽略不计,因而当式(4)中n=1,令k=π2D/R2,则得到式(5):
(C∞-C)/(C∞-C0)=(6/π2) exp(-kt)
(5)
将式(5)等号左侧分子分母同时除以C∞,并两边同时被1除且两边取对数,则得到式(6):
ln[C∞/(C∞![]()
(6)
式(5)、(6)两式为动力学模型,两个式子都能表示出壶瓶碎米荠多糖粉末颗粒的半径、提取的时间、温度与多糖浓度之间的关系。
2 结果与分析
2.1 速率常数k的求解
2.1.1 不同温度下速率常数k的求解
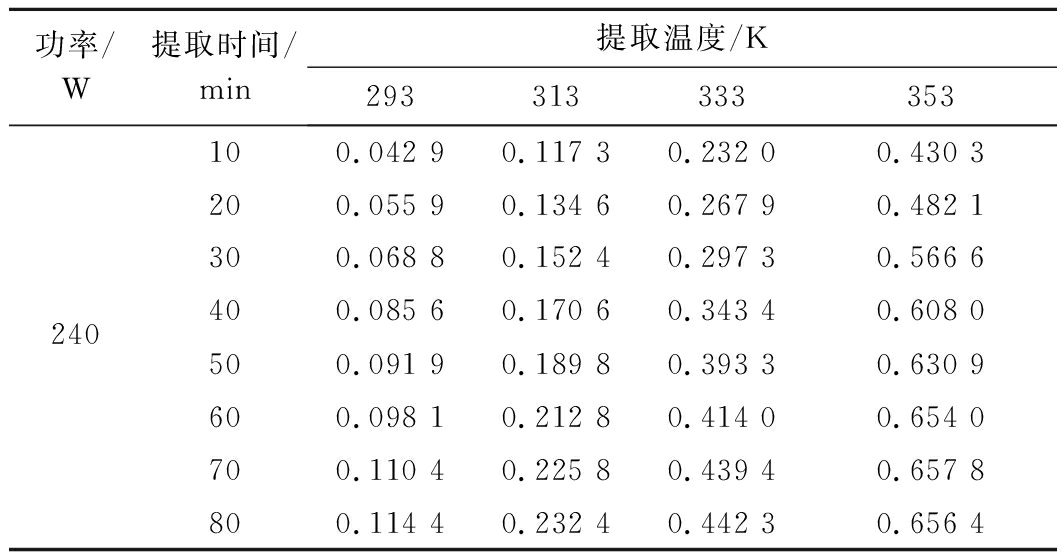
在240 W功率下进行不同温度提取壶瓶碎米荠多糖。当提取壶瓶碎米荠多糖,得到的质量浓度维持稳态或者变化较小时,这时可认定己达到提取浓度平衡状态,此时为平衡浓度。在同一功率条件下,影响多糖提取浓度的是多糖的扩散速度,影响其扩散速度的是温度的大小。由表1可以看出温度对壶瓶碎米荠多糖的提取浓度有影响:随着温度的升高,壶瓶碎米荠多糖的提取浓度增大;温度越高,提取浓度达到平衡所需时间也越短。在240 W功率下,不同温度提取壶瓶碎米荠多糖的平衡浓度如表2所示。
表1 不同温度条件下提取壶瓶碎米荠多糖的质量浓度 单位:mg/mL
Table 1 The concentration of Cardamine hupingshanensis
polysaccharide in pot under different temperature
功率/W提取时间/min提取温度/K293313333353100.042 90.117 30.232 00.430 3200.055 90.134 60.267 90.482 1300.068 80.152 40.297 30.566 6240400.085 60.170 60.343 40.608 0500.091 90.189 80.393 30.630 9600.098 10.212 80.414 00.654 0700.110 40.225 80.439 40.657 8800.114 40.232 40.442 30.656 4
表2 不同温度提取条件壶瓶碎米荠多糖的平衡浓度
Table 2 Equilibrium concentration of Cardamine hupingshanensis polysaccharide under different extraction conditions
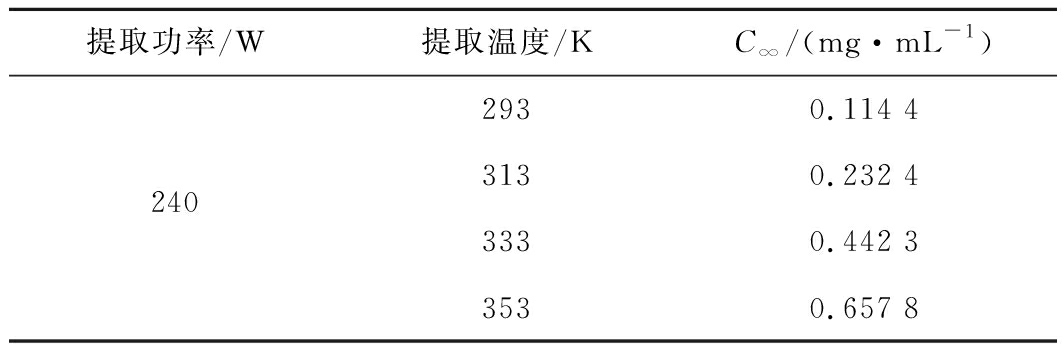
提取功率/W提取温度/KC∞/(mg·mL-1)2930.114 42403130.232 43330.442 33530.657 8
根据表1和表2的试验数据作ln(C∞/C∞-C)与提取时间t的关系图,结果见图1。
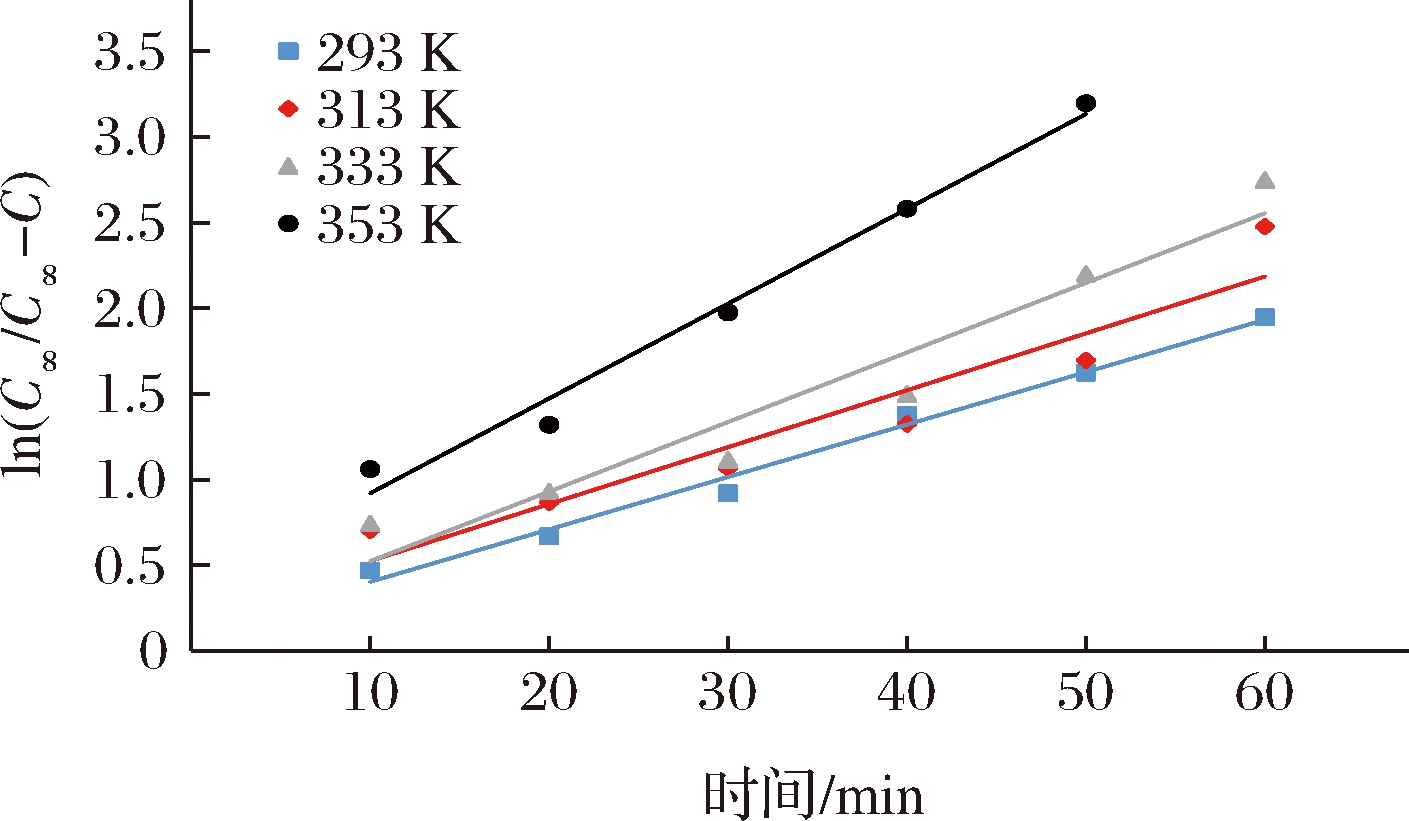
图1 240 W功率条件下不同温度ln(C∞/C∞-C)与时间的关系
Fig.1 Relationship between different temperatures ln(C∞/C∞-C) and extraction time at 240 W
由表1、表2和图1得到的直线回归方程的回归结果和相应的表观速率常数见表3。
表3 不同温度对应的提取直线回归结果
Table 3 The result of extraction linear regression at different temperatures

提取温度/K直线方程R2k/min-1293ln(C∞/C∞-C)=0.030 6t+0.097 70.988 70.030 6240 W313ln(C∞/C∞-C)=0.033 2t+0.193 40.908 40.033 2333ln(C∞/C∞-C)=0.040 6t+0.117 80.936 10.040 6353ln(C∞/C∞-C)=0.055 3t+0.367 40.983 90.055 3
从表1、表3和图1 可以看出,由动力学模型和实验数据推出的提取动力学方程式线性关系良好,其相关系数均在0.90以上。从表3可以得出在同一功率下,温度在293~353K时随着温度的升高,表观速率常数也在逐渐增大。说明温度升高有利于加快壶瓶碎米荠多糖的溶出,提高多糖提取量。
2.1.2 不同超声功率条件下速率常数k的求解
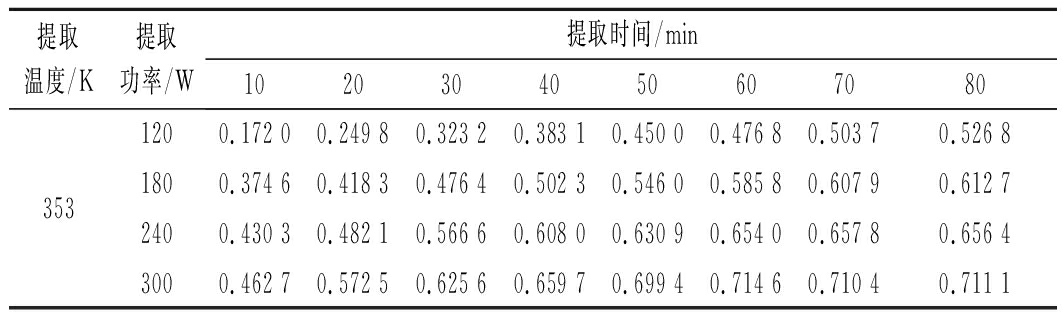
在353 K温度下,利用不同超声功率提取壶瓶碎米荠多糖,得到的多糖质量浓度如表4所示。
表4 不同功率下壶瓶碎米荠多糖质量浓度 单位:mg/mL
Table 4 The concentration of Cardamine hupingshanensis
polysaccharide in pot under different power
提取温度/K提取功率/W提取时间/min10203040506070801200.172 00.249 80.323 20.383 10.450 00.476 80.503 70.526 8 3531800.374 60.418 30.476 40.502 30.546 00.585 80.607 90.612 7 2400.430 30.482 10.566 60.608 00.630 90.654 00.657 80.656 4 3000.462 70.572 50.625 60.659 70.699 40.714 60.710 40.711 1
由表4可以看出,在同一温度、时间条件下,功率越高,提取得到的多糖浓度越大。由表4可知353K温度下进行不同功率提取壶瓶碎米荠多糖的平衡浓度,如表5所示。
表5 不同功率提取条件壶瓶碎米荠多糖的平衡浓度
Table 5 Equilibrium concentration of Cardamine hupingshanensis polysaccharide under different extraction conditions
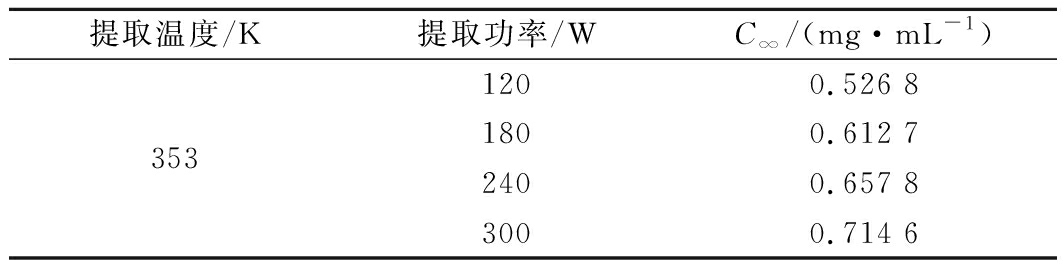
提取温度/K提取功率/WC∞/(mg·mL-1)1200.526 83531800.612 72400.657 83000.714 6
利用表4和表5 的实验数据作ln(C∞/C∞-C)与提取时间t的关系图,结果见图2。由图2得到的直线回归方程的回归结果和相应的表观速率常数见表6。
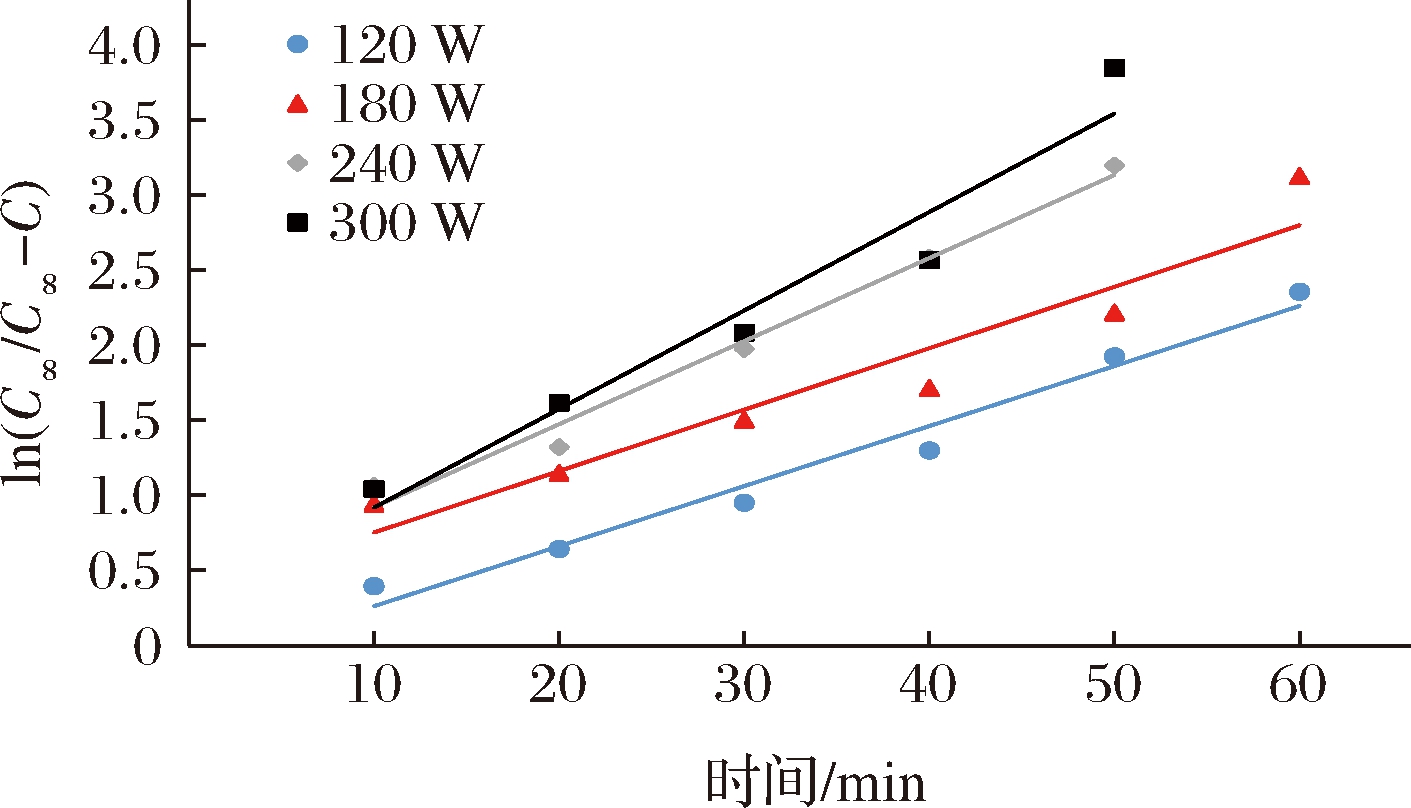
图2 353 K温度条件下不同功率ln(C∞/C∞-C)与提取时间t的关系
Fig.2 Relationship between different power ln (C∞/C ∞-C) and extraction time at 353 K
表6 不同功率对应的提取直线回归结果Table 6 extracted linear regression results of different powers

提取温度/K提取功率/W直线方程R2k/min-1120ln(C∞/C∞-C)=0.040 0t-0.138 40.975 60.040 0353180ln(C∞/C∞-C)=0.040 9t+0.343 10.921 40.040 9240ln(C∞/C∞-C)=0.055 3t+0.367 40.983 90.055 3300ln(C∞/C∞-C)=0.065 6t+0.262 40.948 30.065 6
从表4、表6和图2,推导得到的提取动力学方程模型与测得的数据结果拟合所得的方程线性关系良好,其相关系数均在0.92以上。由表6 可以看出,在同一温度下,随着功率的升高,表观速率常数逐渐增大,说明升高超声提取的功率有利于加快壶瓶碎米荠多糖的溶出,提高多糖得率。
2.2 相对萃余率的求解
壶瓶碎米荠粉末颗粒加入水中0 min时,这时C0=0,由此可设定相对萃余率Y=(C∞-C)/C∞,则公式(5)可以变换为Y=(6/π2)exp(-kt),以Y为纵坐标,提取时间t为横坐标作相对萃余率Y=(C∞-C)/C∞对提取时间 t关系图。
2.2.1 不同温度下相对萃余率的求解
由表1、表2实验数据作在同一功率下不同温度相对萃余率Y=(C∞ -C)/C∞对提取时间t关系图。由图3拟合得到的回归方程和对应的速率常数分别见表7。
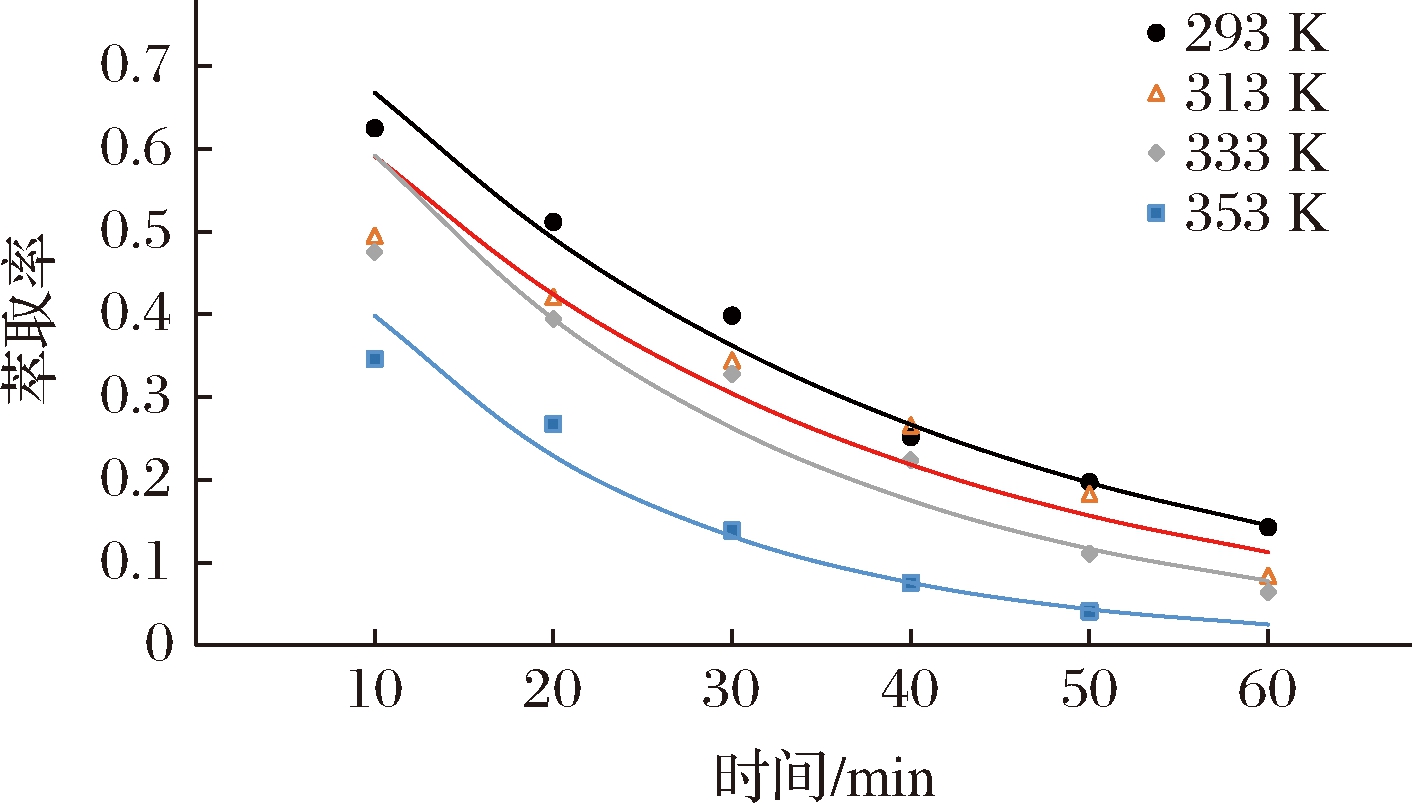
图3 240 W超声不同温度下萃余率与时间的关系
Fig.3 Relationship between extraction recovery and time at different temperatures under 240 W ultrasound
表7 不同温度下多糖相对萃余率对时间回归结果
Table 7 Time regression results of relative extraction rate of polysaccharides at different temperatures
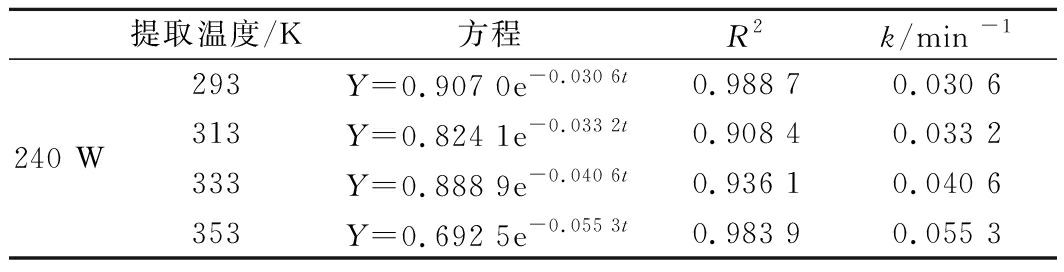
提取温度/K方程R2k/min -1293Y=0.907 0e-0.030 6t0.988 70.030 6240 W313Y=0.824 1e-0.033 2t0.908 40.033 2333Y=0.888 9e-0.040 6t0.936 10.040 6353Y=0.692 5e-0.055 3t0.983 90.055 3
由图3和表7 可以看出,在相同功率不同温度下提取多糖的过程中关于相对萃余率Y=(C∞-C)/C∞对提取时间t拟合方程,相关系数R2均在0.90以上,曲线拟合度良好。表明提取壶瓶碎米荠多糖的过程符合指数模型。由表7拟合所得方程可知,时间越长,萃余率越小;且在功率240 W下,温度越高,多糖萃余率越小,则提取率(1-Y)随着温度升高而增大。反映出温度为293~353 K时,升高温度可以加快多糖提取。
2.2.2 不同功率下相对萃余率的求解
由表4、表5实验数据作在同一温度下不同时间相对萃余率Y=(C∞-C)/C∞对提取时间t关系图。结果如图4所示。由图4拟合得到的回归方程和对应的速率常数见表8。
由图4和表8可以看出,在相同温度不同得超声功率下提取多糖的过程中关于相对萃余率Y=(C∞-C)/C∞对提取时间t拟合方程相关系数R2均在0.92以上,曲线拟合精度良好,表明壶瓶碎米荠多糖的提取过程符合指数模型。由表8拟合所得方程可知,随着时间的延长,萃余率减小;温度353 K下,功率越高,多糖萃余率越小,则提取率(1-Y)增大,反映出功率的增加可以加快多糖的提取。说明超声破坏了细胞,加大了多糖的溶出通道,从而加快多糖的溶出。
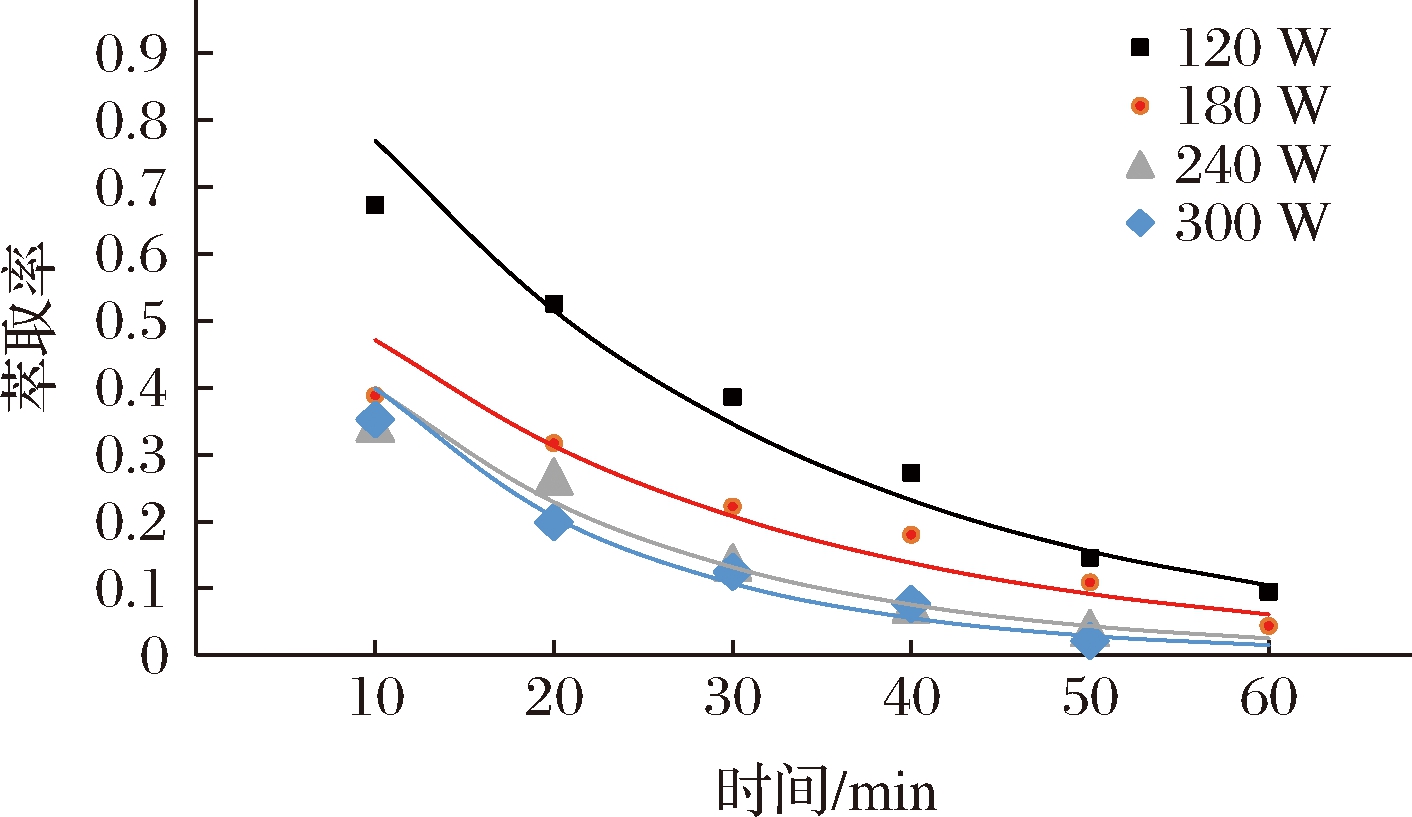
图4 353 K下不同功率下萃余率与时间的关系
Fig.4 Relationship between recovery and time at different power at 353 K
表8 不同功率下多糖相对萃余率对时间回归结果
Table 8 Regression results of relative extraction rate of polysaccharide to time under different power

提取温度/K提取功率/W方程R2k/min -1120Y=1.148 4e-0.040 0t0.975 60.040 0353180Y=0.709 6e-0.040 9t0.921 40.040 9240Y=0.692 5e-0.055 3t0.983 90.055 3300Y=0.769 1e-0.065 6t0.948 30.065 6
2.3 壶瓶碎米荠多糖提取活化能的求解
阿伦尼乌斯公式是由瑞典的阿伦尼乌斯所创立的[20]。它是化学反应速率常数随温度变化关系的经验公式,公式写作k=Aexp(-Ea/RT)。k是2.1求得的速率常数,R是摩尔气体常量等于8.314 J/(mol·K),T为温度,Ea代表活化能,A为频率因子。
将上述公式转换为lnk=lnA-(Ea/RT)。利用表3中的数据对lnk和1/T作(图5),斜率为-Ea/R。
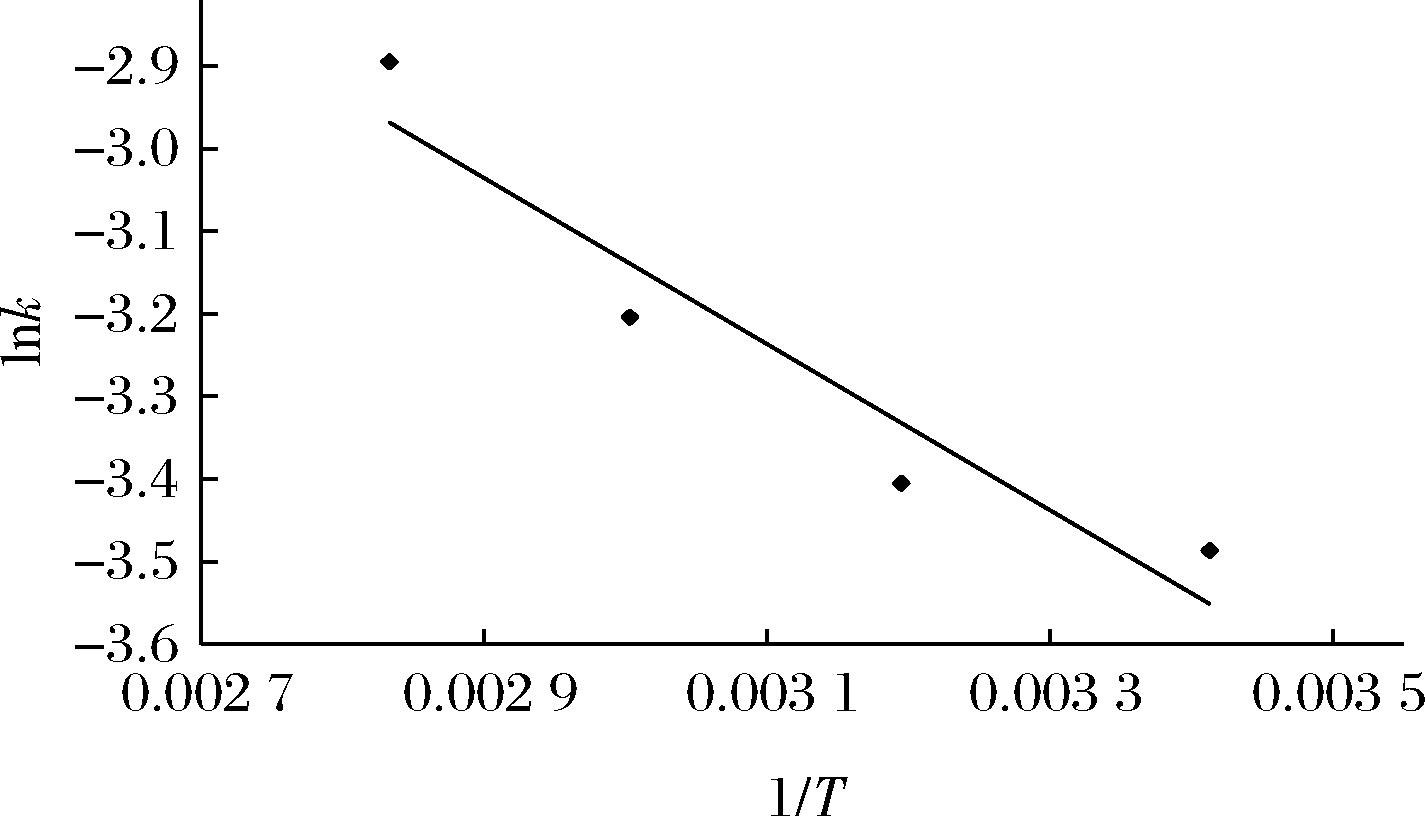
图5 壶瓶碎米荠多糖提取lnk与1/T的关系图
Fig.5 Relationship between lnk and 1/T of Cardamine hupingshanensis polysaccharide extraction
由图5可以看出,240 W时,lnk和1/T关系曲线的拟合方程为lnk=-1 005.2(-Ea/R)-0.120 5,R2=0.908 5,在240 W时lnk和1/T具有良好的相关性,但相关系数未达到0.95以上,推测导致这一问题的原因可能是超声仪器的控温系统不够稳定,温度不能保持恒定不变。根据回归方程可以计算得到240 W功率下壶瓶碎米荠多糖提取过程中的活化能Ea为8 357.232 8 J/mol。
2.4 半衰期的求解
t1/2 是指提取了平衡浓度一半时所经历的时间[21],所以这时C=C∞/2。根据式(6)可推论出t1/2=[ln2-ln(π2/6)]/k,约为t1/2=ln1.215 8/k。由表4、表6 所提供的k值可以求出t1/2,以t1/2为纵坐标,横坐标是提取多糖的温度T作图,得到图6,以t1/2为纵坐标,以提取多糖的超声功率P作图,得到图7。
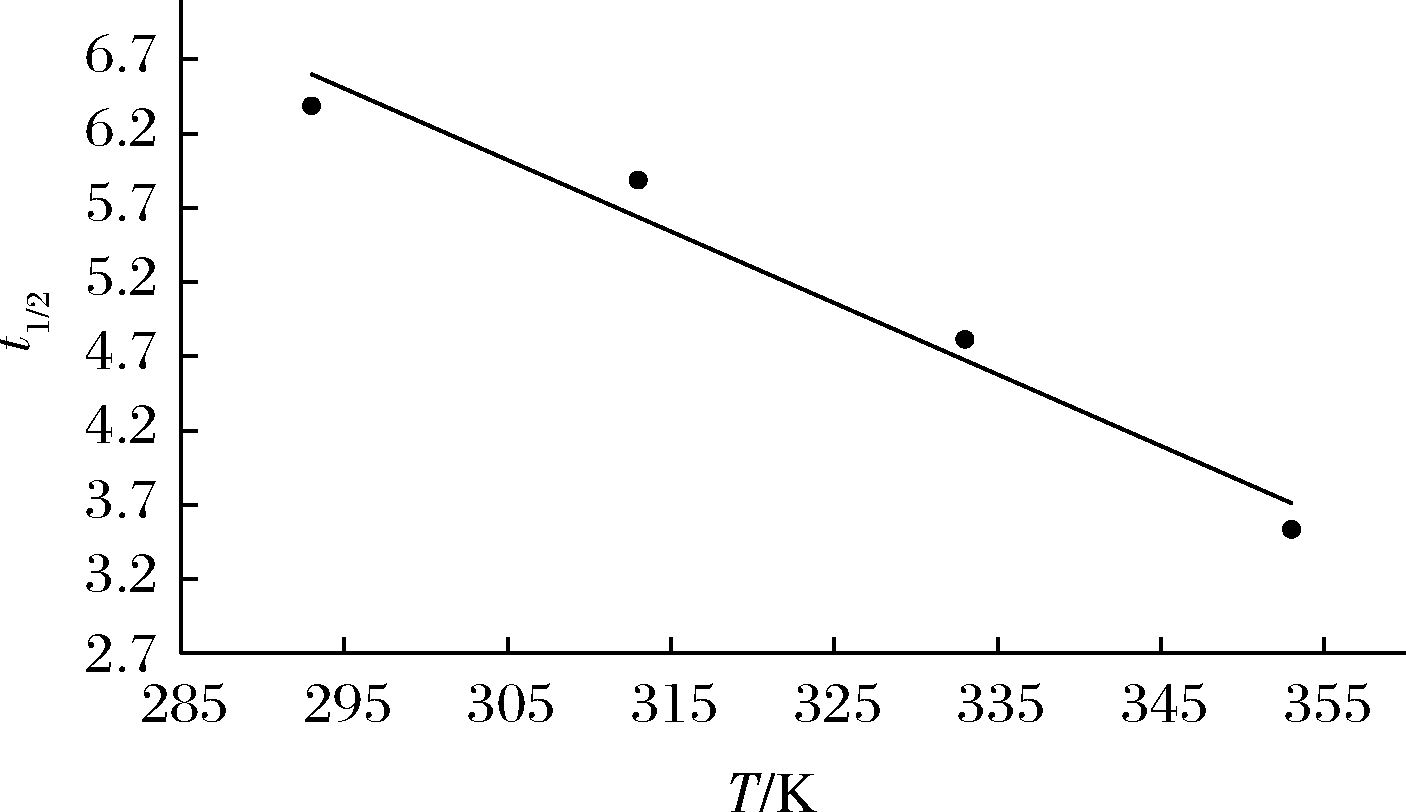
图6 t1/2 与温度的关系图
Fig.6 Relationship between t1/2 and temperature
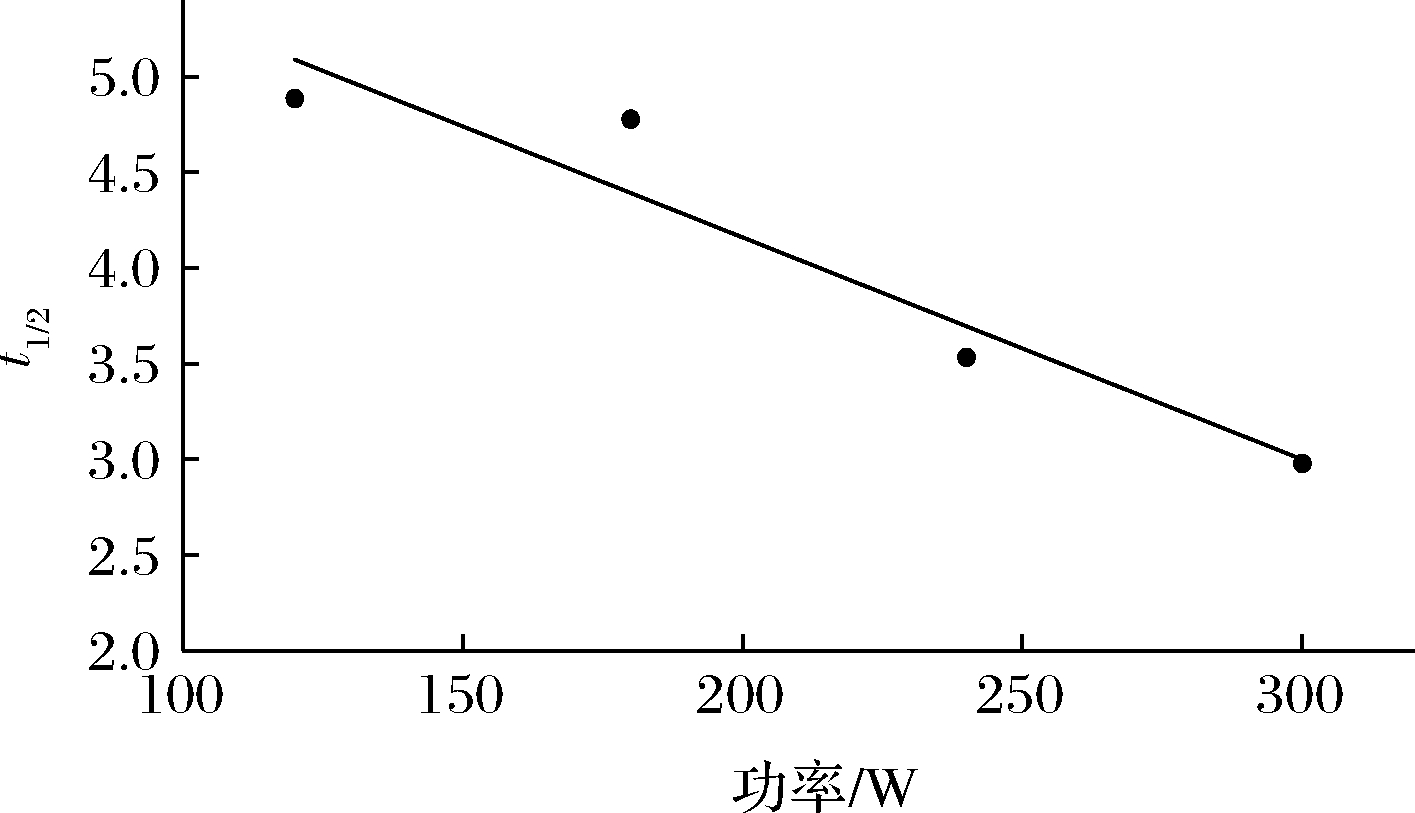
图7 t1/2 与功率的关系图
Fig.7 Relationship between t1/2and work and power
由图6、图7可以得出,353 K时t1/2与功率P关系曲线的拟合方程为t1/2=-0.011 6P-6.480 8,R2=0.917 9。240 W时,t1/2和温度关系曲线的拟合方程为t1/2=-0.048 2P+20.71, R2=0.966 9。
由此可知在同一超声功率下,多糖提取浓度达到平衡浓度一半所需时间随着温度的升高而减小。同一温度下,多糖提取浓度达到平衡浓度一半所需时间随着功率的升高而减小。达到平衡浓度一半所需时间反映了提取的效率,达到平衡浓度一半所需时间越短提取速率越快。所以温度升高、超声功率增大能够加快提取速率。
2.5 平均扩散系数的求解
整个提取过程的平均扩散系数可以通过提取速率常数k来计算。提取速率常数是与平均扩散系数(D)、物料形状和大小相关联的[22]。满足k=π2D/R2。壶瓶碎米荠多糖为球形颗粒,R=0.077 mm。由 k=π2D/R2可知,扩散系数D可以根据与速率常数、颗粒半径之间的关系函数D=kR2/π2得到。
超声提取时,整个体系的扩散系数不仅是多糖分子在水中的扩散系数Dw,还包含超声引起的扩散系数Dc。Dw主要是温度作用下的扩散,Dc为超声引起的涡流扩散系数[23]。超声作用下,温度引起的扩散作用远小于超声引起的扩散。所以忽略Dw,D=Dc[24]。多糖提取过程作D与温度关系图(图8);作D与超声功率的关系图(图9)。根据得到的回归方程可分别计算出2种不同提取方法下的有效扩散系数。
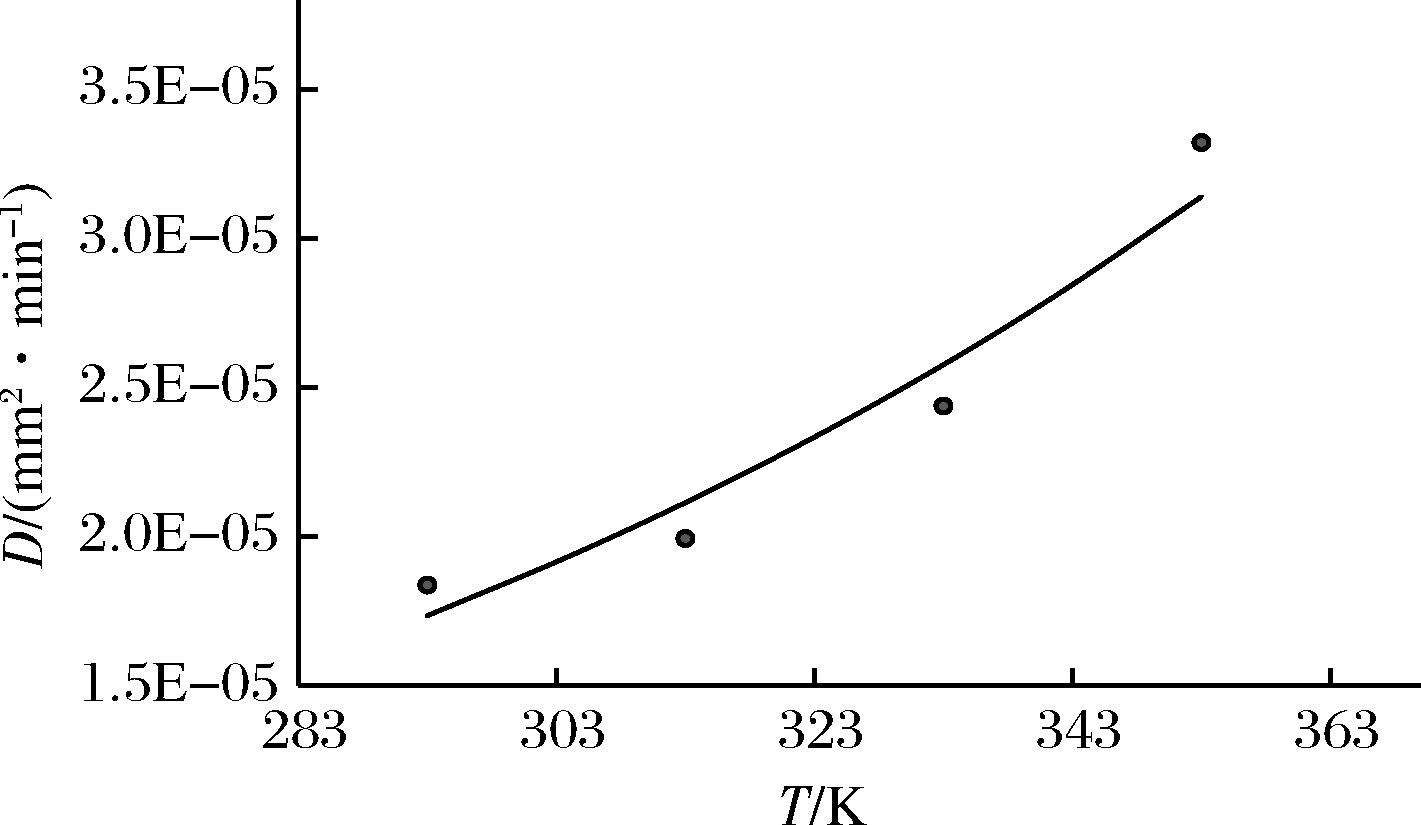
图8 平均扩散系数与温度的关系图
Fig.8 Relationship between average diffusion coefficient and temperature
由图8得到在超声功率为240 W时平均扩散系数的拟合方程为:D=9.59×10-7e0.009 9T,R2=0.937 9。由图9可以得出,在温度为353 K时平均扩散系数的拟合方程为:D=1.59×10-5e0.003P,R2=0.919 6。当温度一定,功率不同时,平均扩散系数随着功率增大而增大。当功率固定,温度不同时,平均扩散系数随着温度增大而增大。
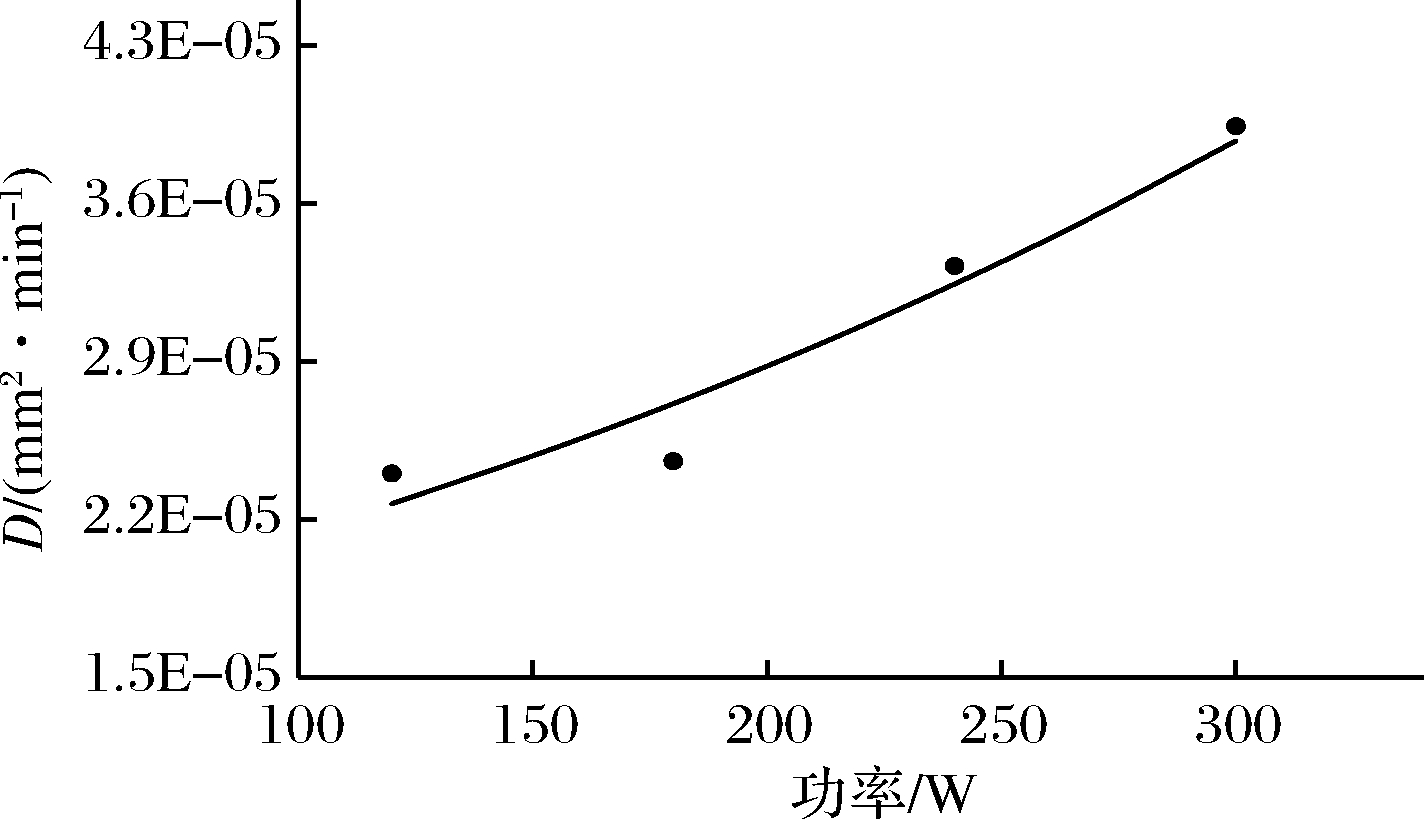
图9 平均扩散系数与功率的关系图
Fig.9 Relationship between average diffusion coefficient and work and power
3 结论
结合 Fick 第二定律,建立了超声提取壶瓶碎米荠多糖质量的动力学模型,建立的动力学模型展现出了提取壶瓶碎米荠多糖质量浓度与壶瓶碎米荠颗粒半径、时间、扩散系数之间的关系。在此基础上,以壶瓶碎米荠粉末为原料,在不同温度和超声功率下提取多糖,检测得到不同提取条件下的多糖的质量浓度。测得的多糖浓度与动力学模型方程结合,得到壶瓶碎米荠多糖提取过程中的一般方程、指数方程和相关参数。因为超声波处理可能导致颗粒微观结构的破坏[25],试验假定壶瓶碎米荠颗粒在提取过程中半径不变,且超声仪器的控温系统不够稳定等原因,会影响实验数据结果,降低相关方程的相关性,导致试验的相关系数未均达到0.95,但基本都达到了0.9,所以试验测得数据与动力学模型计算值具有一定的吻合性,求得的动力学参数可以为壶瓶碎米荠多糖提取工艺的优化提供一定的理论基础。
[1] 刘合刚, 费新贵, 陈林.华中碎米荠的生药学研究[J].时珍国药研究, 1994(3):14-15.
LIU H G, FEI X G, CHEN L.Pharmacognostical study of Cardamine urbaniana[J].Lishizhen Medicine and Materia Medica Research, 1994 (3):14-15.
[2] 石爱华, 彭祚全.堇叶碎米荠本草考证及生物学研究[J].微量元素与健康研究, 2015,32(5):61-64.
SHI A H, PENG Z Q.Textual research and biological research of Cardamine urbaniana[J].Studies of Trace Elements and Health, 2015,32(5):61-64.
[3] 曹斌.恩施碎米荠含硒蛋白分离提取、初步纯化、体外抗氧化活性研究[D].贵阳:贵州大学,2016.
CAO B.Isolation, preliminary purification and in vitro antioxidant activity of selenoprotein from Cardamine bursa Enshi[D].Guiyang:Guizhou University, 2016
[4] CUI L W, ZHAO J T, CHEN J Y, et al.Translocation and transformation of selenium in hyperaccumulator plant Cardamine enshiensis from Enshi, Hubei China[J].Plant and Soil,2018, 425(1-2):577-588.
[5] 向天勇. 恩施碎米荠的生物学特性及叶片含硒化合物研究[D].长沙:湖南农业大学, 2006.
XIANG T Y.Biological characteristics and selenium compounds in leaves of Cardamine Enshi[D].Changsha:Hunan Agricultural University, 2006.
[6] 白兴达. 半湿法玉米胚稳态挤压与浸油动力学研究[D].淄博;山东理工大学, 2017.
BAI X D.Kinetic study on steady extrusion and oil soaking of semi wet corn embryo[D].Zibo:Shandong University of Technology, 2017.
[7] 王文骏. 柑橘皮果胶超声辅助提取的作用机制研究[D].杭州:浙江大学,2018.
WANG W J.Mechanism of ultrasonic assisted extraction of pectin from citrus peel[D].Hangzhou:Zhejiang University, 2018.
[8] RICARDO P C,ALLISON L,ANDREA B,et al.Aqueous extraction of the sulfated polysaccharide ulvan from the green alga ulva rigida-kinetics and modeling[J].BioEnergy Research,2017,10(3):915-928.
[9] HU W W,YE X Q,CHANTAPAKUL T,et al.Manosonication extraction of RG-I pectic polysaccharides from citrus waste:Optimization and kinetics analysis[J].Carbohydrate Polymers,2020,235:1-10.
[10] M NICA M U,MAR
NICA M U,MAR A E DALMAU, VALERIA S E,et al.Effects of acoustic power and pH on pectin-enriched extracts obtained from citrus by-products.Modelling of the extraction process[J].Journal of the Science of Food and Agriculture,2019,99(15):6 893-6 902.
A E DALMAU, VALERIA S E,et al.Effects of acoustic power and pH on pectin-enriched extracts obtained from citrus by-products.Modelling of the extraction process[J].Journal of the Science of Food and Agriculture,2019,99(15):6 893-6 902.
[11] 张春燕. 壶瓶碎米荠含硒化合物复合提取工艺及含硒黄酮活性研究[D].恩施:湖北民族学院,2018.
ZHANG C Y.Compound extraction process of selenium containing compounds from Cardamine hupehensis and the activity of selenium containing flavonoids[D].Enshi:Hubei University for nationalities, 2018.
[12] 李瑜,马俊, 高海娜, 等.硒在堇叶碎米荠中的赋存形态及分布规律[J].中国食物与营养, 2020, 26(7):26-28.
LI Y, MA J, GAO H N, et al.Speciation and distribution of selenium in Cardamine violaceus[J].Food and Nutrition in China, 2020, 26 (7):26-28.
[13] 罗凯,黄秀芳,周毅峰,等.响应面试验优化复合酶法提取碎米荠多糖工艺及其抗氧化活性[J].食品科学, 2017, 38(4):237-242.
LUO K, HUANG X F, ZHOU Y F, et al.Optimization of extraction process and antioxidant activity of Polysaccharide from Cardamine bursa by response surface methodology[J].Food Science, 2017, 38 (4):237-242.
[14] ZHANG W N, ZHANG H L, LU C Q, et al.A new kinetic model of ultrasound-assisted extraction of polysaccharides from Chinese chive[J].Food Chemistry, 2016, 212:274-281.
[15] 刘廷丹, 杨秀娟, 邓君明, 等.苯酚-硫酸法测定蛤蚧酒中多糖含量[J].食品工业, 2018, 39(8):298-301.
LIU T D, YANG X J, DENG J M, et al.Determination of polysaccharide content in Gejie wine by phenol sulfuric acid method[J].Food Industry, 2018, 39 (8):298-301.
[16] HOU K F, ZHENG Q, LI Y R, et al.Modeling and optimization of herb leaching processes[J]. Computers and Chemical Engineering, 2000, 24(2):1 343-1 348.
[17] WANG Y G,WANG X J,ZHANG K,et al.Extraction kinetics, thermodynamics, rheological properties and anti-BVDV activity of the hot water assisted extraction of Glycyrrhiza polysaccharide.[J].Food & Function,2020,11(5):4 067-4 080.
[18] WANG Y G, ZHANG X, MA X Q, et al.Study on the kinetic model, thermodynamic and physicochemical properties of Glycyrrhiza polysaccharide by ultrasonic assisted extraction[J].Ultrasonics Sonochemistry,2019, 51:249-257.
[19] DASILVA C V,PEREIRA V J,COSTAG M N, et al.Supercritical solvent impregnation/deposition of spilanthol-enriched extracts into a commercial collagen/cellulose-based wound dressing[J].The Journal of Supercritical Fluids,2018,133(1):503-511.
[20] THERESA B, DALENE D B, MARTIN K, et al.Modeling of thermal degradation kinetics of the C-glucosyl xanthone mangiferin in an aqueous model solution as a function of pH and temperature and protective effect of honeybush extract matrix[J].Food Research International,2018,103:103-105.
[21] MICHAEL S, YUEN Y C.The kinetics and mechanism of caffeine infusion from coffee:The temperature variation of the hindrance factor[J].Journal of the Science of Food and Agriculture,1997, 74(3):416-420.
[22] ISHMAEL A.Ultrasound-assisted alkali extraction of protein from tea residue and its activity evaluation[D].Zhenjiang:Jiangsu University, 2019.
[23] 廖建庆, 王涵, 王咸鹏, 等.超声波甘草酸提取动力学模型[J].声学技术, 2018, 37(6):565-570.
LIAO J Q, WANG H, WANG X P, et al.Kinetic model of ultrasonic extraction of glycyrrhizic acid[J].Acoustic Technology, 2018, 37(6):565-570.
[24] 陆海勤,李毅花,李冬梅,等.超声协同电场提取黄花菜多糖的动力学研究[J].华南理工大学学报(自然科学版),2017,45(9):67-73;87.
LU H Q, LI Y H, LI D M, et al.Study on the kinetics of ultrasonic assisted electric field extraction of polysaccharides from day lily[J].Journal of South China University of Technology(Natural Science Edition), 2017,45 (9):67-73;87.
[25] XU Y, PAN S Y.Effects of various factors of ultrasonic treatment on the extraction yield of all- trans-lycopene from red grapefruit (Citrus paradise Macf.)[J].Ultrasonics-Sonochemistry, 2013, 20(4):1 026-1 032.