白酒是具有我国民族特色的蒸馏酒,随着消费趋势的变化和白酒的国际化,白酒低度化成为当前白酒发展的趋势[1-4]。但目前我国低度白酒风味化学理论还不完善,酒体设计、产品开发大多还是基于经验操作,优质低度白酒的生产始终存在较大的难度,成为限制我国白酒低度化发展的瓶颈之一[5]。加浆降度是低度白酒生产的重要环节,降度过程中由于酒精含量和其他风味物质含量的降低,酒体风味会发生显著变化,往往会出现风味寡淡、失去产品风格和特色等突出问题[5-6]。
白兰地、威士忌、朗姆酒等蒸馏酒通常采用加冰或加水稀释的方式饮用,对蒸馏酒降度过程中风味感官质量变化的研究也是国际蒸馏酒风味研究的重点[7-8]。蒸馏酒降度过程中风味感知的变化主要源于酒精度和风味物质含量下降。其中,由于物理化学作用和生理学作用,酒精度变化对风味感知具有重要作用。酒精度下降会导致水/乙醇基质的分子结构变化[8]。CONNER等[9]研究发现,酒精度下降时,威士忌中的长链乙酯化合物溶解度降低,在溶液中形成聚合物包裹风味物质,降低了风味物质的挥发。此外,酒精度的降低会增加风味物质的挥发性[10-13],2种效应协同作用最终影响风味物质的挥发性。酒精度变化除了通过改变风味物质的挥发性间接影响风味感知外,还会改变风味化合物的阈值,从而直接影响风味感知[8]。酒精度上升,由于其本身具有的刺激性气味,会抑制其他风味物质的感知,导致风味化合物阈值升高。而风味物质浓度下降会减少风味物质的挥发量,间接影响酒的风味轮廓。此外,风味物质间的相互作用会直接影响风味的感知[12,14-16]。因此,降度过程往往是酒精度和风味物质浓度变化协同作用造成风味轮廓变化。
为探究酒精度和风味物质含量这2个关键因素变化对白酒香气感知和风味组分挥发性的影响,本文以清香型白酒为例,分别使用超纯水和酒精水溶液稀释酒样,将感官与仪器相结合,对原酒样及其稀释酒样进行研究,以探索影响低度酒品质的关键因素。
1 材料与方法
1.1 材料与试剂
本实验的样品酒为汾酒,清香型,酒精体积分数为53%,购自品牌官方旗舰店。
乙醇(色谱级),百灵威科技有限公司(北京);超纯水由Mili-Q纯水仪(Millipore,Bedford,MA,USA)制备;C4-C9直链酮,Sigma-Aldrich贸易有限公司(上海);化合物标准品(色谱级),Sigma-Aldrich贸易有限公司(上海)、阿法埃莎化学有限公司(天津)和百灵威科技有限公司(北京)。
1.2 仪器与设备
静态顶空气相结合离子迁移谱(static headspace-gas chromatography-ion mobility spectrometry,SHS-GC-IMS):自动进样器(TurboMatrix16),美国Perkin Elmer公司;GC-2010气相色谱仪,日本Shimadzu公司;离子迁移谱模块,德国Gesellschaft für Analytische Sensorsysteme mbH。
1.3 实验方法
1.3.1 白酒样品制备
为模拟降度白酒的生产过程,将汾酒酒样Q加超纯水稀释,得到酒精体积分数为40%、30%、20%的稀释酒样,分别记为Q-40、Q-30、Q-20。此外,降度过程中,乙醇的体积分数(以下简称酒精度)以及其他风味物质的质量浓度均发生变化,为探索这2个因素分别对香气释放和感知的影响,另使用酒精度为53%的酒精水溶液稀释汾酒酒样Q,稀释比例与Q-30一致,记为Q-30E。
1.3.2 定量描述分析香气属性强度变化
1.3.2.1 品评人员培训与选拔
参照国际标准ISO 8586—2012对品评员进行筛选培训[17]。对选拔出的16位品评员(8男8女)进行为期2个月的培训。并定期测试各品评员的香气识别和样品区分能力,以适当调整培训内容与进程。
1.3.2.2 香气描述词的确认以及标度培训
首先,收集品评员对酒样的描述词,并参考白酒风味轮中的感官描述词,获得白酒品评的全部感官描述词。并通过小组讨论,定义每个描述词所代表的气味,如表1所示。采用0~15分值打分制,通过参考品建立香气强度标尺,如表1所示。使用非测试样品进行模拟训练,并利用R语言对品评员小组的重复性以及一致性进行评价,在品评小组中挑选出10位表现优异的品评员组成最终的品评小组,以进行最终的定量描述分析实验(quantitative descriptive analysis,QDA)。
表1 定量描述分析香气描述词、定义、参考样品及其评分
Table 1 List of aroma attributes,definitions,references and reference scores determined for QDA

描述词定义参考品分数果香水果成熟时所散发出来的香气含有20 mg/L己酸乙酯的水溶液10醇香白酒中醇类成分呈现的香气特征含20 mg/L异戊醇的酒精度40%的酒精水溶液8甜香白酒呈现的类似甜味感受的香气特征5 μL蜂蜜酒鼻子溶于50 mL水9酸味白酒中挥发性酸类成分所呈现的香气特征20 mg/L丁酸,20 mg/L戊酸的水溶液9清香白酒中以乙酸乙酯为主的多种成分呈现的香气特征120 mg/L乙酸乙酯,6 mg/L乳酸乙酯的水溶液7粮香高粱、大米、小麦等多种粮谷原料经发酵蒸馏使白酒呈现的类似蒸熟粮食的香气特征煮熟高粱8糠味白酒呈现的类似生谷壳等辅料的气味特征潮湿的谷壳7霉味白酒呈现的类似发霉的气味特征霉味较为典型的酒样10
1.3.2.3 样品的测试
组织者将10 mL白酒样品倒入白酒品评杯中,使用三位数的随机号码标注品评杯,并用锡纸覆盖以降低样品挥发所造成的差异。在25 ℃的环境下,按随机顺序将样品提供给品评员,每次提供3个样品,要求品评员在样品间休息30~60 s,每组样品之间休息5~10 min,以降低因嗅觉疲劳对实验结果的影响,所有样品品评3次。
1.3.3 静态顶空气相结合离子迁移谱测定风味组分挥发性变化
仪器条件:使用SHS-GC-IMS进行样品检测。将1 mL样品置于20 mL的气密瓶中,封上盖子在25 ℃下平衡8 h。用90 ℃的自动进样针吸取100 μL顶部空间气体,气体经过140 ℃的传输线到达200 ℃ GC进样口,随后进入到DB-FFAP柱(60 m×0.25 mm,0.25 μm)中,柱初始温度40 ℃,保持3 min,以4 ℃/min升至150 ℃,保持5 min,分流比为5。最后气体经过150 ℃的连接处,到达45 ℃的迁移管。利用STANDALONE软件收集数据。
化合物的定性与定量:使用C4-C9直链酮混合物计算保留指数。在与样品检测相同的条件下,根据挥发性化合物的离子迁移谱和保留指数与纯标准品进行比较,以鉴定化合物。除了与纯标准品的保留指数进行比较外,还将其与文献中报道的保留指数进行比较。使用VOCal软件计算每个目标化合物峰体积,以峰体积的大小表征顶部空间化合物浓度。
1.4 数据处理
使用R Studio对品评小组的一致性、稳定性进行评定,采用Origin 2021作图,SPSS进行相关性分析,XLSTAT进行主成分分析。
2 结果与分析
2.1 感官品评小组的建立和培训
为了保证品评结果的科学性和可靠性,在解析降度对清香型白酒香气感知的影响之前,需对品评小组的品评结果进行一致性与稳定性评估。本实验参考文献[18]中所述的方法,利用R语言对品评小组的品评结果进行方差分析。
表2结果显示“稀释样品×品评员”对香气属性变化的影响不显著,不同品评员在品评样品时,其评分无显著差异,表明品评小组在评分时具有较好的一致性。“稀释样品×重复样品”对香气属性变化的影响不显著,品评员在3次品评同一样品时,其打分无显著差异,表明品评小组在品评时具有良好的重复性。综上,品评小组的品评结果具有一致性和稳定性,表明品评小组的品评结果具有科学性和可靠性。
表2 清香型白酒的香气属性方差分析F值a
Table 2 Analysis of variance (ANOVA) F-ratios for amora attributes of Chinese light-flavor Baijiu

注:*,**,***分别代表P<0.05,P<0.01,P<0.001;a, F值是变异的来源;b,稀释样品×品评员、稀释样品×重复样品、品评员×重复样品分别表示稀释样品与品评员、稀释样品与重复样品、品评员与重复样品之间的相互作用
描述词稀释样品品评员重复样品稀释样品×品评员b稀释样品×重复样品b品评员×重复样品b果香8.9***2.2*1.21.41.01.0甜香1.45.8***0.01.41.41.0粮香27.8***7.8***1.31.51.40.8糠味6.0***1.80.50.71.00.5酸味8.3***3.6***0.81.40.31.0清香2.33.2**1.11.40.30.5霉味5.3***2.5*0.51.50.41.8*醇香21.1***5.3***2.71.20.71.1
2.2 清香型白酒降度稀释过程中香气属性变化分析
酒精度的下降会降低化合物的阈值,从而增强香气化合物的香气强度;物质浓度的下降则会降低品评员感知到的香气强度[8]。上述2种效应的叠加造成酒样香气属性的变化。但由于不同香气化合物受到2种效应的影响程度存在差异,因此各香气化合物呈现出的香气属性变化规律也存在着差异。
如表2所示,甜香、清香在降度过程中未发生显著变化,果香、粮香、糠味、酸味、霉味、醇香等6个香气属性具有显著变化。酒样在被超纯水稀释过程中(图1-a),醇香、果香、酸味强度呈现下降趋势,其余香气属性呈现上升趋势。其中,清香型白酒的不良气味——霉味和糠味香气强度在降度过程中显著突出,对清香型低度酒的品质具有不良影响。
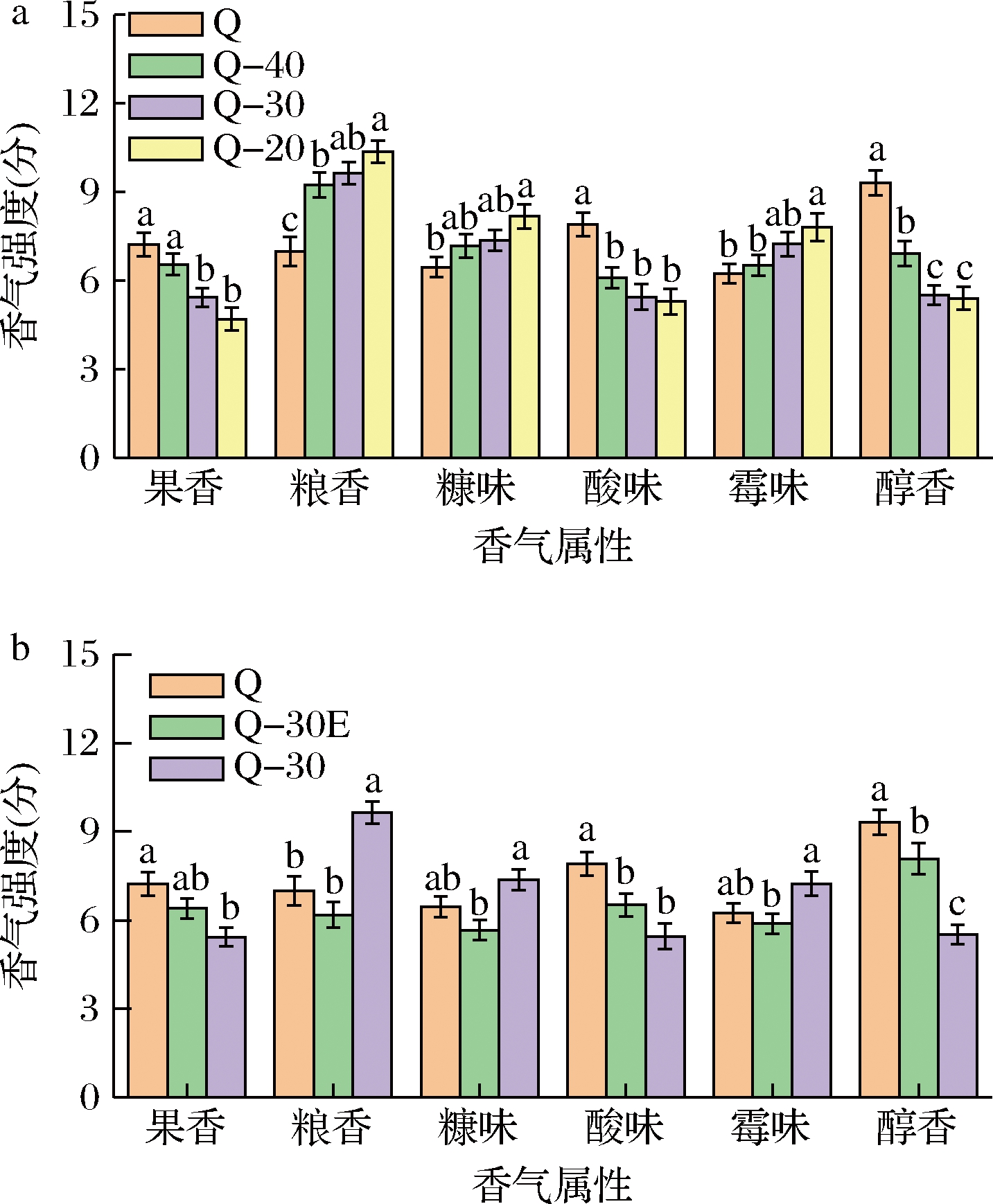
a-酒样Q,Q-40,Q-30,Q-20对比图;b-酒样Q,Q-30E,Q-30对比图
图1 清香型酒样香气属性强度柱形图
Fig.1 The intensity of aroma attribute in Chinese light-flavor Baijiu samples
注:不同字母代表显著性差异(P<0.05)
酒样Q与Q-30E酒精度相同但物质浓度不同,酒样Q-30E与Q-30物质浓度相同但酒精度不同。将3个酒样对比可发现(图1-b),当酒精度不变而物质浓度下降时,各香气属性强度变化不显著;而当物质浓度不变、酒精度降低时,果香、酸味以及醇香香气强度显著下降,粮香显著上升。这表明,在白酒降度过程中,物质浓度的变化对于香气属性强度变化的影响低于酒精度的影响。
对具有显著变化的香气属性与酒精度、物质浓度进行斯皮尔曼相关性分析(图2)。只有果香与物质浓度具有显著正相关性,其他5种香气属性均与酒精度显著相关(其中,粮香、糠味、霉味为显著负相关;酸味、醇香为显著正相关)。这说明,果香强度的变化主要受酒样中物质浓度的影响,而其他香气属性强度的变化主要取决于酒精度的变化。

图2 物质与香气属性斯皮尔曼相关性分析
Fig.2 Spearman correlation analysis between compounds and amora attributes
注:红线代表正相关,绿线代表负相关
为进一步明确酒样在稀释过程中感官特征变化,对其进行主成分分析(图3)。前2个主成分因子累计可解释数据的96.88%。各稀释酒样与原酒Q的风味轮廓差异均较大,其中,Q-40相对而言与原酒Q的香气轮廓更为接近,其香气也更怡人。而Q-20和Q-30中的糠味、霉味等不良气味较重。清香型白酒的香气特点在于“清”,随着稀释倍数的增加,其中被高酒精度掩盖的不良香气更加突出。因此,生产优质的低度清香型白酒,应注意酒精度的选择。

图3 汾酒酒样主成分分析
Fig.3 PCA of Chinese light-flavor Baijiu samples(Fenjiu)
2.3 稀释酒样风味组分挥发性变化规律
香气被感知的前提是香气化合物从溶液里挥发到空气中,其挥发量直接影响香气的强弱,因此研究酒样在稀释过程中挥发性的变化有助于解析香气属性强度变化的成因。利用SHS-GC-IMS测定稀释样品顶部空间中各风味组分的信号峰强度变化,以表征风味组分在稀释过程中挥发性的变化[19]。为模拟酒样的真实消费过程,本实验将样品置于顶空瓶内在25 ℃的环境下平衡8 h后,使用静态顶空进样[20]。
在样品稀释过程中,酒精度与物质浓度均发生变化。分别以酒精度和物质浓度为自变量,对检测到的27个香气化合物的变化进行单因素方差分析。如表3所示,稀释酒样中,随着酒精度和物质浓度改变发生显著变化的化合物分别有10个(占比37.0%)和5个(占比18.5%)。这表明,在降度过程中,化合物的挥发性受酒精度变化的影响大于物质浓度。这与QDA结论一致。此外,清香型白酒中呈现“清香”的主要物质——乙酸乙酯顶空浓度无显著变化,与之对应的是,“清香”在降度过程中香气强度也无显著变化。
表3中,共有12个化合物的顶空浓度具有显著变化。在用超纯水稀释过程中,不同的化合物顶空浓度会呈现出不同的变化趋势(图4)。

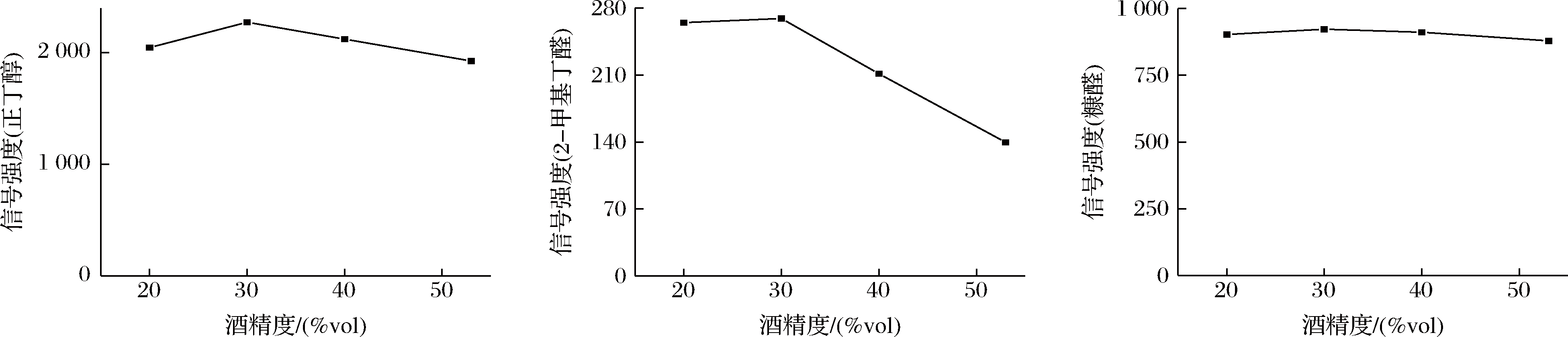
图4 用超纯水稀释的清香型酒样中香气化合物信号峰强度变化散点图
Fig.4 Scatter plots of voltage intensity of aroma compounds in Chinese light-flavor Baijiu samples diluted with ultrapure water
表3 清香型酒样中香气化合物信号峰强度变化
Table 3 The changes of voltage intensity of aroma compounds in Chinese light-flavor Baijiu samples
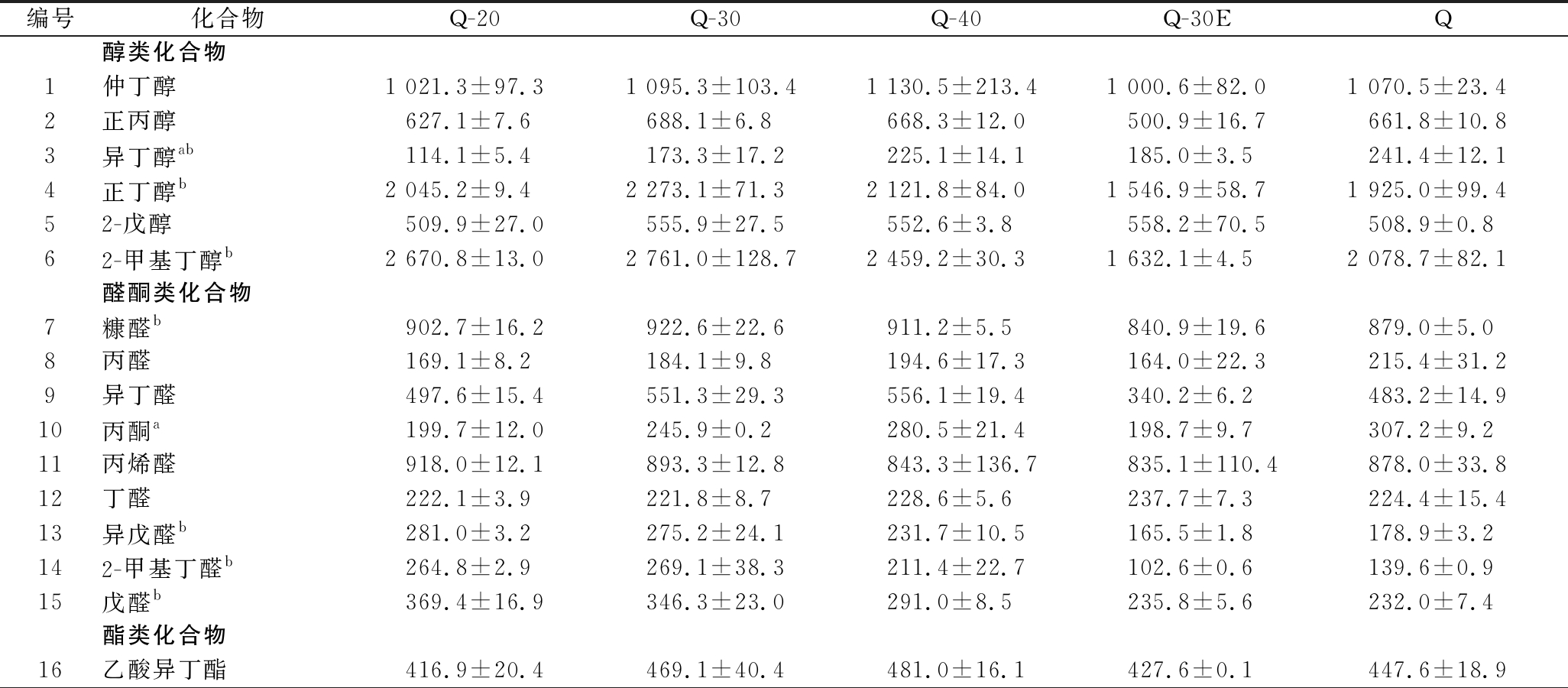
编号化合物Q-20Q-30Q-40Q-30EQ醇类化合物1仲丁醇1 021.3±97.31 095.3±103.41 130.5±213.41 000.6±82.01 070.5±23.42正丙醇627.1±7.6688.1±6.8668.3±12.0500.9±16.7661.8±10.83异丁醇ab114.1±5.4173.3±17.2225.1±14.1185.0±3.5241.4±12.14正丁醇b2 045.2±9.42 273.1±71.32 121.8±84.01 546.9±58.71 925.0±99.452-戊醇509.9±27.0555.9±27.5552.6±3.8558.2±70.5508.9±0.862-甲基丁醇b2 670.8±13.02 761.0±128.72 459.2±30.31 632.1±4.52 078.7±82.1醛酮类化合物7糠醛b902.7±16.2922.6±22.6911.2±5.5840.9±19.6879.0±5.08丙醛169.1±8.2184.1±9.8194.6±17.3164.0±22.3215.4±31.29异丁醛497.6±15.4551.3±29.3556.1±19.4340.2±6.2483.2±14.910丙酮a199.7±12.0245.9±0.2280.5±21.4198.7±9.7307.2±9.211丙烯醛918.0±12.1893.3±12.8843.3±136.7835.1±110.4878.0±33.812丁醛222.1±3.9221.8±8.7228.6±5.6237.7±7.3224.4±15.413异戊醛b281.0±3.2275.2±24.1231.7±10.5165.5±1.8178.9±3.2142-甲基丁醛b264.8±2.9269.1±38.3211.4±22.7102.6±0.6139.6±0.915戊醛b369.4±16.9346.3±23.0291.0±8.5235.8±5.6232.0±7.4酯类化合物16乙酸异丁酯416.9±20.4469.1±40.4481.0±16.1427.6±0.1447.6±18.9
续表3

注:a,随着物质浓度变化其挥发性发生显著变化的化合物;b,随着酒精度变化其挥发性发生显著变化的化合物(在α=0.05时,Fisher最小显著差异检验)
编号化合物Q-20Q-30Q-40Q-30EQ17丁酸乙酯995.1±7.81 228.2±88.01 293.6±47.2950.3±8.61 256.6±14.018乙酸异戊酯b657.7±20.5880.3±132.6897.4±115.4598.0±18.8708.8±2.119戊酸乙酯1 141.3±39.51 113.2±33.51 135.5±53.81 115.2±95.31 137.8±6.520己酸乙酯2 978.4±59.13 248.1±215.33 068.3±141.03 237.1±287.82 936.8±277.621醋酸异丙酯210.9±0.3222.0±12.9207.9±36.2193.3±27.6243.6±0.622乙酸乙酯11 982.4±22.712 948.1±107.413 388.1±190.211 718.4±67.513 299.8±95.823丙酸乙酯ab2 238.4±12.12 390.7±27.52 470.6±40.72 454.0±36.02 513.3±27.124异丁酸乙酯682.4±37.1779.6±88.5757.0±93.1663.0±19.0694.9±11.7含氮、含硫化合物252,6-二甲基吡嗪a1 893.2±10.72 350.5±129.72 754.0±159.82 360.7±2.53 003.1±21.226二甲基硫ab148.3±9.2188.9±1.2215.6±12.2192.7±9.9228.9±4.0萜烯类化合物27α-蒎烯265.8±18.7292.6±13.7295.9±40.6272.7±10.9277.1±19.9
其中,二甲基硫、异丁醇、2,6-二甲基吡嗪、丙酮、戊醛、异戊醛等6个化合物顶空浓度变化与酒精度变化显著相关(二甲基硫、异丁醇、2,6-二甲基吡嗪、丙酮为显著正相关,戊醛、异戊醛为显著负相关),且R2均大于0.87。乙酸异戊酯、2-甲基丁醇、正丁醇、2-甲基丁醛、糠醛等5个化合物随着酒精度的上升呈现先上升后下降的趋势,丙酸乙酯呈现上升趋势。
白酒中挥发性风味物质的释放不仅取决于溶液中挥发物的浓度,而且还受挥发物之间的相互作用、不挥发性物质以及酒精度的影响[9,13]。酒样被超纯水稀释过程中,酒精度的降低会增加化合物的挥发性,物质浓度的降低会减少物质的挥发量,2个效果的叠加最终使化合物的挥发性发生变化[12,14-15]。不同化合物由于其疏水性、极性、碳链长度等物理化学性质不同,其随着酒精度变化呈现出的变化也各有区别[12,21-22]。
3 结论
本文采用QDA表征了稀释过程中清香型白酒香气属性的变化规律。清香、甜香香气属性强度变化不显著,醇香、果香、酸味强度随着稀释倍数的增加而显著下降,粮香、糠味、霉味显著上升。6个具有显著变化的香气属性中仅有果香强度变化与物质浓度显著相关,其余香气属性强度变化均与酒精度变化显著相关,表明酒精度对香气属性感知的影响大于物质浓度的影响。
使用SHS-GC-IMS分析稀释过程中风味组分挥发性的变化规律,共鉴定出27种化合物,有12种化合物挥发性发生显著变化。其中,10个化合物随着酒精度改变发生显著变化,这表明化合物的挥发性受酒精度变化的影响大于物质浓度。各化合物因其具有不同的物理化学性质,而呈现出不同的变化趋势。风味化合物挥发性的变化如何影响香气感知,值得进一步研究。
[1] 刘勇. 谈低度化白酒发展现状[J].酿酒,2020,47(3):26-27.
LIU Y.A brief discussion on the development status of low-alcohol liquor[J].Liquor Making,2020,47(3):26-27.
[2] 孙西玉, 梁邦昌.中国低度白酒的历史沿革与白酒发展趋势[J].酿酒科技,2007(6):73-76.
SUN X Y,LIANG B C.The history origin of Chinese low-alcohol liquors and the development trends[J].Liquor-Making Science & Technology,2007(6):73-76.
[3] 杨孟涵.低度酒技术,厚积薄发渐成主流[N].华夏酒报,2018-12-11(A10).
YANG M H.Low-alcohol Baijiu technology has gradually become the mainstream[N].Chinese Wine News,2018-12-11(A10).
[4] 王延才.中国酒业协会第五届理事会第三次(扩大)会议2015年中国酒业工作报告[J].酿酒,2016,43(3):4-15.
WANG Y C.The 3rd (expanded) meeting of the fifth council of china wine industry association 2015 china wine industry work report[J].Liquor Making,2016,43(3):4-15.
[5] 张馨元, 徐岩,王栋,等.优质低度与高度浓香型白酒挥发性风味组分差异特征解析[J].食品与发酵工业,2020,46(15):66-71.
ZHANG X Y,XU Y,WANG D,et al.Characterization of volatile compounds in high-quality low-alcohol and high-alcohol strong-aroma type Baijiu[J].Food and Fermentation Industries,2020,46(15):66-71.
[6] 史路路, 颜雪辉,吕梅,等.低度白酒生产方式的研究进展[J].酿酒,2013,40(2):17-19.
SHI L L,YAN X H,LYU M,et al.Research progress of low alcoholic liquor production[J].Liquor Making,2013,40(2):17-19.
[7] ICKES C M,CADWALLADER K R.Effect of ethanol on flavor perception of Rum[J].Food Science & Nutrition,2018,6(4):912-924.
[8] ICKES C M,CADWALLADER K R.Effects of ethanol on flavor perception in alcoholic beverages[J].Chemosensory Perception,2017,10(4):119-134.
[9] CONNER J M,PATERSON A,PIGGOTT J R.Agglomeration of ethyl-esters in model spirit solutions and malt whiskies[J].Journal of the Science of Food and Agriculture,1994,66(1):45-53.
[10] BOELRIJKA A,BASTENB W,BURGERINGA M,et al.The effect of co-solvent on the release of key flavours in alcoholic beverages;comparing in vivo with artificial mouth-MS Nose measurements[C].The 10th Weurman Flavour Research Symposium.Beaune:2003.
[11] CONNER J M,BIRKMYRE L,PATERSON A,et al.Headspace concentrations of ethyl esters at different alcoholic strengths[J].Journal of the Science of Food and Agriculture,1998,77(1):121-126.
[12] BOOTHROYD E L,LINFORTH R S T,COOK D J.Effects of ethanol and long-chain ethyl ester concentrations on volatile partitioning in a whisky model system[J].Journal of Agricultural and Food Chemistry,2012,60(40):9 959-9 966.
[13] GOLDNER M C,ZAMORA M C,DI LEO LIRA P,et al.Effect of ethanol level in the perception of aroma attributes and the detection of volatile compounds in red wine[J].Journal of Sensory Studies,2009,24(2):243-257.
[14] PETROZZIELLO M,ASPROUDI A,GUAITA M,et al.Influence of the matrix composition on the volatility and sensory perception of 4-ethylphenol and 4-ethylguaiacol in model wine solutions[J].Food Chemistry,2014,149:197-202.
[15] VILLAMOR R R,EVANS M A, MATTINSON D S,et al.Effects of ethanol,tannin and fructose on the headspace concentration and potential sensory significance of odorants in a model wine[J].Food Research International,2013,50(1):38-45.
[16] LYTRA G,TEMPERE S,LE FLOCH A,et al.Study of sensory interactions among red wine fruity esters in a model solution[J].Journal of Agricultural and Food Chemistry,2013,61(36):8 504-8 513.
[17] International Organization for Standardization.ISO 8586—2012 Sensory analysis—General guidelines for the selection,training and monitoring of selected assessors and expert sensory assessors[S].Switzerland:International Organization for Standardization,2012.
[18] Lê S,WORCH T.Analyzing Sensory Data with R[M].New York:CRC Press,2015.
[19] WANG S Q,CHEN H T,SUN B G.Recent progress in food flavor analysis using gas chromatography-ion mobility spectrometry (GC-IMS)[J].Food Chemistry,2020,315.DOI:10.1016/j.foodchem.2019.126158.
[20] HARTMANN P J,MCNAIR H M,ZOECKLEIN B W.Measurement of 3-alkyl-2-methoxypyrazine by headspace solid-phase microextraction in spiked model wines[J].American Journal of Enology and Viticulture,2002,53(4):285-288.
[21] AZNAR M,TSACHAKI M,LINFORTH R S T,et al.Headspace analysis of volatile organic compounds from ethanolic systems by direct APCI-MS[J].International Journal of Mass Spectrometry,2004,239(1):17-25.
[22] TSACHAKI M,AZNAR M,LINFORTH R S T,et al.Dynamics of flavour release from ethanolic solutions[J].Developments in Food Science,2006,43:441-444.