低聚异麦芽糖(isomalto-oligosacchrides, IMOs)是一类聚合度通常为2~10,含有1个或多个α-1,6糖苷键的寡聚葡萄糖。其主要功能成分是异麦芽糖、异麦芽三糖(isomaltotriose, IG3)和潘糖等[1-2]。IMOs甜度低、热量低,具有低血糖指数特征;IMOs可被肠道益生菌如双歧杆菌分解利用,产生短链脂肪酸,提高人体免疫力,有研究表明,IMOs产品中IG3的成分相比于异麦芽糖更有利于人体内双歧杆菌生长,这说明了IG3为主要益生因子之一[3-5];IMOs不被龋齿链球菌利用,可以有效预防龋齿。因此IMOs被广泛应用于食品、医药和化妆品等行业。
目前,工业上主要使用以下2种方法制备IMOs。第1种方法以淀粉为原料经过淀粉酶、葡萄糖苷酶处理制备IMOs[6]:例如LEE等[7]将麦芽糖淀粉酶和α-葡萄糖转移酶复配催化玉米糖浆,可产出67.4%的IMOs,其中,IG3及聚合度更高的IMOs占比为39.7%。第2种方法以蔗糖为原料经过右旋糖酐蔗糖酶(dextransucrase, DS)单独制备IMOs或与右旋糖酐酶一同制备IMOs[8-12]:例如GOULAS等[12]使用DS和右旋糖酐酶以蔗糖为原料制备IMOs,产出聚合度为10~60的异麦芽寡糖(占比至多36%)。
KRALJ等[13]报道了1种4,6-α-葡聚糖转移酶(4,6-α-glucanotransferase,4,6-α-GT)可将直链淀粉通过转苷反应转化成右旋糖酐,产物中α-1,6糖苷键比率高达90%[13-16]。但基于底物的结构,仅4,6-α-GTs不可能将非直链淀粉类的α-1,4糖苷键高效地转化为α-1,6糖苷键连接的多聚糖[17]。据此我们提出了4,6-α-GTs和右旋糖酐酶制备IMOs的新策略,以麦芽糊精为底物,使用本实验室筛选的来源于Lactobacillus fermentum的4,6-α-葡萄糖基转移酶(4,6-α-glycosyltransferases, LfGT)合成右旋糖酐[18],使用酵母将右旋糖酐中的葡萄糖消化后冷冻干燥制成粉末,再使用具有IG3产物特异性的来源于Brevibacterium fuscum的异麦芽三糖右旋糖酐酶(isomaltotrio-dextranase, BfIMTD)降解右旋糖酐以制备IMOs的两步法工艺。本研究在第1步合成反应中添加商品化普鲁兰酶和重组表达的异普鲁兰酶(isopullulanase, IPU)与LfGT复配对合成反应进行优化,以提高中间产物右旋糖酐的产量和有效键型(α-1,6糖苷键)比率,并对降解反应中BfIMTD降解右旋糖酐的工艺进行优化,以实现富含IG3的IMOs高效制备。
1 材料与方法
1.1 实验材料
1.1.1 菌种与质粒
Escherichia coli JM109、 E.coli BL21(DE3)和Pichia pastoris KM71为本实验室保藏;目的基因合成于上海捷瑞生物工程有限公司。
1.1.2 酶与主要试剂
LfGT来源于本实验室;商品化高温淀粉酶、糖化酶及普鲁兰酶购于山东隆科特有限公司。
异麦芽糖、潘糖、G3等标准品,Sigma-Aldrich有限公司;商品化右旋糖酐20000,上海国药集团化学试剂有限公司;麦芽糊精(DE2,DE4~6和DE5~7),罗盖特精细化工有限公司;酵母,安琪生物集团有限公司。所用培养基为大肠杆菌和酵母宿主常用培养基。主要仪器包括常用摇瓶发酵、酶反应及产物检测所需仪器等。
1.2 重组菌的构建及发酵
根据研究需求,从NCBI数据库中选择B.fuscum来源的BfIMTD,及Aspergillus niger来源的IPU的氨基酸序列,由上海捷瑞生物工程有限公司对目的氨基酸序列进行表达宿主密码子优化以及基因合成,选择E.coli BL21(DE3)和pET-24a(+)作为BfIMTD的表达宿主和载体,选择P.pastoris KM71和pPIC9K作为IPU的表达宿主和载体,使用大肠杆菌宿主和毕赤酵母宿主常用发酵方法分别对BfIMTD和IPU进行重组表达,使用SDS-PAGE方法对重组酶进行分析[19-20]。
1.3 重组酶的酶活测定
使用DNS法对BfIMTD和IPU进行酶活力测定[21]。
在本研究中,在pH 7.5和45 ℃的条件下使用10 g/L商品化右旋糖酐20000作为底物反应10 min测定BfIMTD酶活力。酶活力定义:上述条件下,将1 min 水解右旋糖酐生成1 μmol的葡萄糖所需酶量定义为右旋糖酐酶的1个单位的酶活力。
在pH 3.5和30 ℃的条件下使用50 g/L普鲁兰多糖反应30 min测定IPU酶活力。酶活力定义:上述条件下,将1 min水解普鲁兰多糖生成1 μmol的葡萄糖所需酶量定义为IPU的1个单位的酶活力。
1.4 低聚异麦芽糖的制备及检测方法
1.4.1 合成右旋糖酐及中间处理的方法
将麦芽糊精溶于50 mmol/L磷酸/柠檬酸缓冲液中配制成250 g/L麦芽糊精溶液,随后加入适量LfGT及缓冲液至底物麦芽糊精终质量浓度为200 g/L,同批次可能同时或分别加入适量普鲁兰酶、IPU,通过加酶组合优化此合成步骤,在37 ℃,200 r/min条件下反应24 h。
随后加入高温淀粉酶(95 ℃, 反应30 min)和糖化酶(60 ℃,反应30 min)对合成反应液中未反应的底物及产物中的末端α-1,4糖苷键短链部分进行处理,随后煮沸灭酶。向反应液中加入50 g/L反应液的干酵母,在30 ℃条件下反应12 h消化葡萄糖。
将处理好的反应液置于-80 ℃下冷藏过夜,随后置于冷冻干燥机中进行冷冻干燥, 获得样品右旋糖酐粉末。
1.4.2 水解右旋糖酐制备IMOs的方法
将1.4.1所述样品粉末溶于50 mmol/L磷酸/柠檬酸缓冲液中,加入适量右旋糖酐酶,于37 ℃条件下反应不同时长,煮沸灭酶离心后即可获得IMOs反应液。
1.4.3 产物的HPLC检测方法
使用安捷伦1260 HPLC色谱仪对右旋糖酐(DP≥3)进行检测。检测条件为:色谱柱Agilent Hi-Plex Ca (7.7 mm×300 mm, 8 μm),柱温80 ℃,流动相为纯水,流速0.5 mL/min,进样量为10 μL。将HPLC测得三糖及以上聚合度部分视为右旋糖酐,其产量按照测得产品峰面积占所有产品的比例计算。
使用安捷伦1260 HPLC色谱仪对寡糖分子(IG3、异麦芽糖和葡萄糖等)进行检测。待测样品经纯乙腈等体积过夜沉淀后,取上清液检测,检测条件为:色谱柱Agilent ZORBAX NH2 (4.6 mm×250 mm, 5 μm),柱温35 ℃,流动相为体积分数70%~75%的乙腈,流速0.8 mL/min,进样量为10 μL。标准品(葡萄糖-麦芽七糖混合标样G1~G7、异麦芽糖、IG3等)同样品一同检测,IMOs的产量按照外标法计算得相应浓度,并结合第1步反应占比,计算得IG3两步法产率。
1.4.4 产物键型的核磁共振氢谱(1H-nuclear magnetic resonance spectra,1H-NMR)检测方法
利用AVANCE III 400 MHz数字NMR核磁共振光谱仪(Bruker Biospin International AG)测定右旋糖酐的键型比例。称取30~40 mg样品溶于500 μL D2O (D, 99.9%)中,漩涡振荡至彻底溶解后打入核磁管中进行测定,温度为60 ℃。将三甲基甲硅烷基丙酸(0.3 g/L)溶解在样品中作为内标。
2 结果与分析
2.1 合成步骤右旋糖酐的制备
本研究中使用到的底物麦芽糊精属于淀粉不同程度的水解产物,其主链为α-1,4糖苷键连接,在链上的不同部位会有不同聚合度的支链,分支处以α-1,6糖苷键为主的糖苷键连接。图1中呈现了麦芽糊精具有代表性的结构。合成步骤中使用的酶种类包括LfGT、普鲁兰酶及IPU。3种酶的主要作用分别为:(1)产生右旋糖酐:4,6-α-GTs作为合成右旋糖酐的主要酶,它能够利用淀粉的直链部分生成含有α-1,6糖苷键连接的右旋糖酐部分,但与淀粉含有支链的部位不易发生反应;(2)提高右旋糖酐产量:普鲁兰酶是一类可以水解淀粉分支的脱支酶,可将最小单位的支链从主链上水解下来,使4,6-α-GTs可以最大程度地利用淀粉质底物;(3)提高产物中α-1,6糖苷键比例:IPU可以水解普鲁兰多糖中1个或连续α-1,6糖苷键后的α-1,4糖苷键,此处IPU水解麦芽糊精或LfGT产出右旋糖酐由α-1,6糖苷键连接支链后的α-1,4糖苷键,随后LfGT利用得到的直链淀粉,最终获得α-1,6糖苷键占比更高的产物。
综上所述,本研究分别建立并优化了单酶(LfGT),双酶复配(LfGT和普鲁兰酶)以及三酶复配(LfGT、普鲁兰酶和IPU)3种生产右旋糖酐的反应体系,以获得具有更高α-1,6糖苷键右旋糖酐反应体系(图1)。
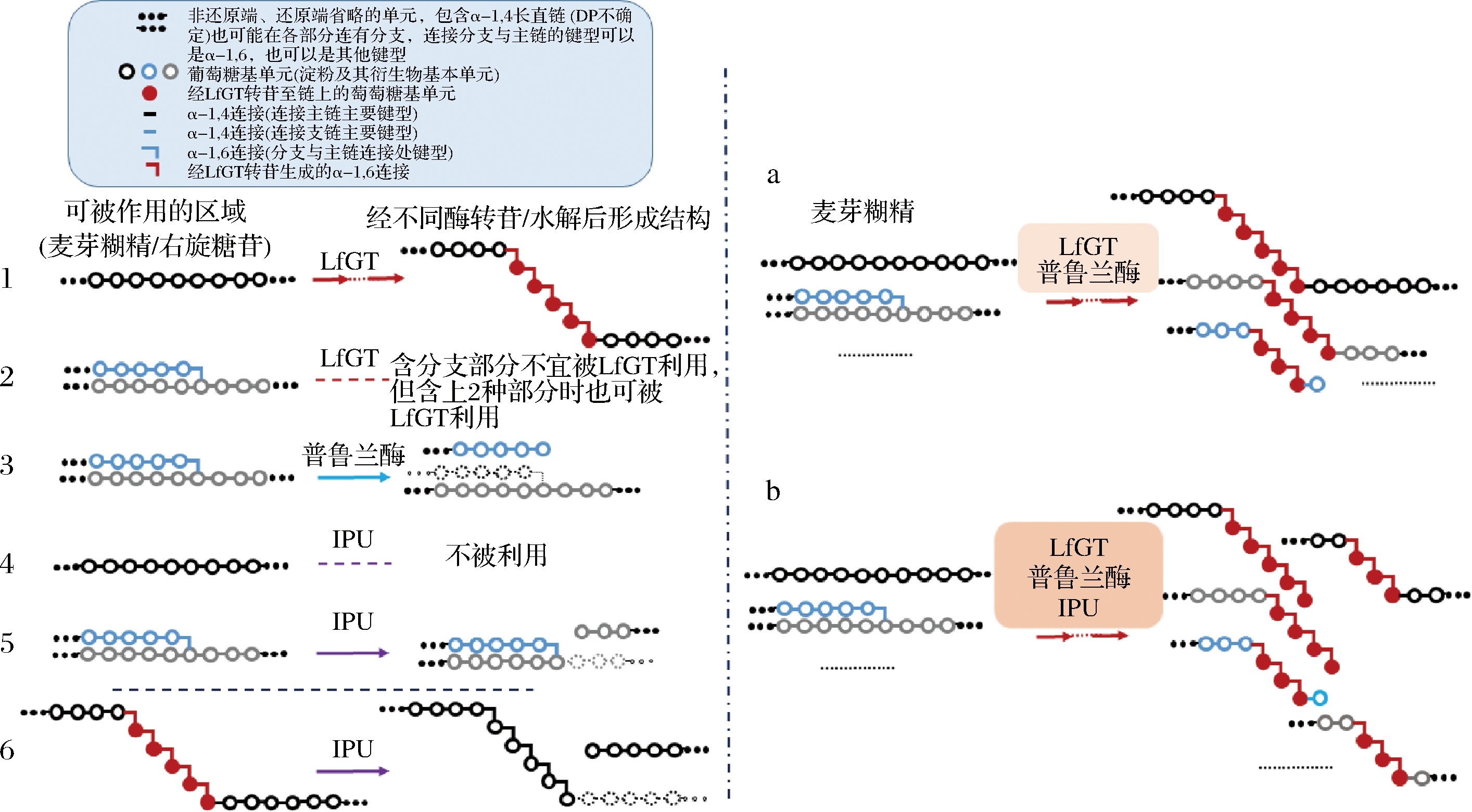
1-可与LfGT反应的底物直链区域;2-不可与LfGT反应的底物含支链的区域;3-可被普鲁兰酶水解的底物支链区域(α-1,6糖苷键);4-不可被异普
鲁兰酶水解的底物直链区域;5-可被异普鲁兰酶水解的底物上紧跟支链的α-1,4末端;6-可被异普鲁兰酶水解的LfGT产物上紧跟支链的α-1,4末端;
a-LfGT和普鲁兰酶复配产物结构;b-LfGT,普鲁兰酶和异普鲁兰酶复配产物结构
图1 合成步骤底物和产物结构简图
Fig.1 Structure of the substrate and product in the synthesis step
2.1.1 LfGT加酶量对右旋糖酐合成的影响
本实验室筛选得到L.fermentum来源的LfGT,其最适温度为37 ℃,最适pH为6.0。在LfGT的最适条件37 ℃和pH 6.0下,将200 g/L麦芽糊精(DE2)与不同加酶量的LfGT (300、400、500、800 U/g底物,以下简称U/g)反应24 h。反应结束后使用1.4.1所述方法处理反应液,以消除未被利用的底物和产物含有α-1,4糖苷键末端的部分,下述合成步骤后处理方法保持一致。使用1.4.3所述方法检测有效成分的峰面积占比来确定LfGT加酶量对合成反应效率的影响。
如图2-a所示,12.384 min和10.739 min出峰成分为本合成步骤产物右旋糖酐,16.206 min出峰为葡萄糖。如图2-b所示,当LfGT加酶量为400 U/g时,右旋糖酐的产物占比最高,约为24.5%,此时葡萄糖占比为71.5%,未被LfGT利用的麦芽糊精经高温淀粉酶和糖化酶中间处理水解为葡萄糖。产物由酵母消除葡萄糖后冷冻干燥成粉末后,称取其30~40 mg粉末溶于500 μL D2O,使用0.3 g/L TMSP作为内标一同溶于样品中进行1H-NMR检测,如图2-c所示,检测得产物中α-1,4糖苷键和α-1,6糖苷键的比例为1∶3.15,α-1,6糖苷键比率为76%。加酶量为400~800 U/g,产物右旋糖酐减少,可能是LfGT存在副反应——水解反应,在右旋糖酐产量接近平衡时,增加LfGT的加酶量,其水解反应开始起作用,水解底物麦芽糊精或生成的产物右旋糖酐,因此提高加酶量反而使得右旋糖酐产量降低。
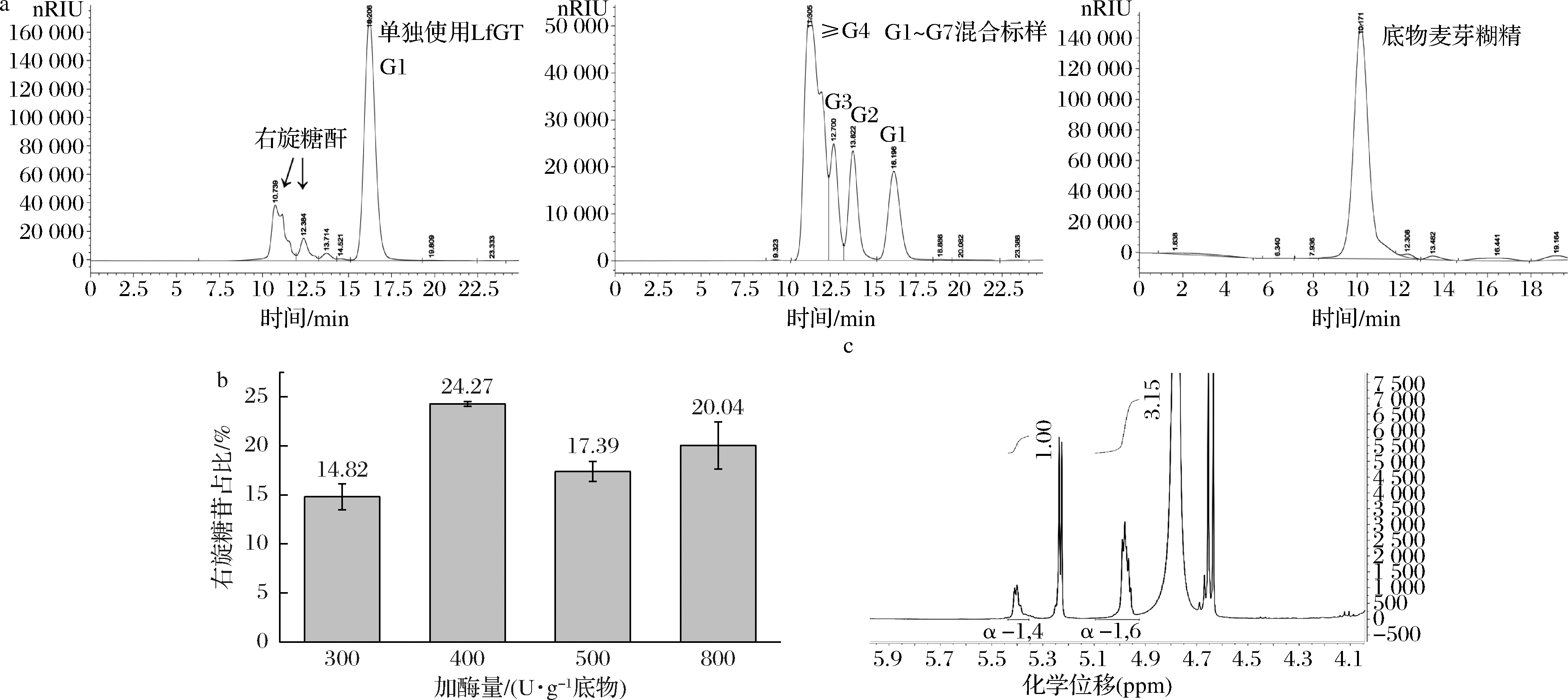
a-LfGT产物HPLC图谱(G1:葡萄糖;G2:麦芽糖;G3:麦芽三糖;≥G4:麦芽四糖~麦芽七糖);
b-LfGT加酶量对右旋糖酐产物占比的影响;c-加酶量为400 U/g时产物1H-NMR图谱
图2 单独使用LfGT产物HPLC图谱、其加酶量对右旋糖酐产物占比的影响及产物1H-NMR图谱
Fig.2 HPLC analysis of product prepared by LfGT, the effect of LfGT amount on dextran proportion and relavant 1H-NMR analysis
2.1.2 LfGT与普鲁兰酶复配对右旋糖酐合成的影响
在37 ℃和pH 6.0的条件下,依据2.1.1的探究结果使用400 U/g加酶量的LfGT进行复配优化,依照实验室研究经验使用40 U/g的普鲁兰酶进行复配。双酶复配的HPLC产物图谱如图3-a所示。同时分别使用200 g/L DE2、DE4~6和DE5~7的麦芽糊精作为底物对右旋糖酐的产量进行探究,如图3-b 所示。底物使用DE2麦芽糊精时,单独使用LfGT催化反应的右旋糖酐产物占比为24.3%,双酶复配的右旋糖酐产物占比增加了仅50%;底物使用DE4~6或DE5~7麦芽糊精时,单独使用LfGT催化反应的右旋糖酐产物占比约45%,双酶复配产出右旋糖酐占比增加了15%。双酶复配时,DE2麦芽糊精的转化程度更高。此外,利用1H-NMR检测产物的键型比例,如图3-c所示,在使用DE2的麦芽糊精时,双酶复配产物的α-1,6糖苷键比率可达89.2%。各组实验结果综合表明,利用普鲁兰酶与LfGT复配,可以进一步提高产物中右旋糖酐产量。

a-双酶复配产物HPLC图谱;b-复配组合及底物对右旋糖酐产物占比的影响;c-使用DE2麦芽糊精的双酶复配产物1H-NMR图谱
图3 双酶复配产物HPLC图谱、不同复配组合与不同DE值麦芽糊精对右旋糖酐占比的影响及双酶复配产物1H-NMR图谱
Fig.3 HPLC analysis of product prepared by two enzymes, the effect of enzyme cocktails and maltodextrins with varying DE on
dextran proportion and relevant 1H-NMR analysis
2.1.3 LfGT、普鲁兰酶与异普鲁兰酶复配对右旋糖酐合成的影响
根据AKEBOSHI等[22]、SAKANO等[23]对来源于A.niger的IPU的研究,其最适pH为3.0~3.5,最适温度为40 ℃。本研究依据相关发酵方法对IPU进行重组表达。重组表达的IPU酶活力可达691.5 U/mL,可用于制备IMOs两步法工艺。在37 ℃和pH 6.0的条件下,在2.1.2所述双酶复配的基础上使用DE2的麦芽糊精,加入IPU一同反应24 h,三酶复配的HPLC产物图谱如图4-a所示。400 U/g的IPU与LfGT和普鲁兰酶复配时右旋糖酐产物占比可达66.3%,如图4-b所示。利用1H-NMR检测不同组合产物的键型比例,如图4-c所示,三酶组合的键型比例为1∶142.3,α-1,6糖苷键的比率达到99.3%,这说明IPU的加入几乎使所有可用的α-1,4糖苷键经LfGT转糖基化为α-1,6糖苷键。α-1,6糖苷键占比更高的右旋糖酐对后续右旋糖酐酶发挥水解特性更加有效,从而直接影响IMOs的产率。

a-三酶复配产物HPLC图谱;b-三酶复配不同IPU加酶量对右旋糖酐产物占比的影响;
c-IPU加酶量为400 U/g时三酶复配产物的1H-NMR检测图谱
图4 三酶复配产物HPLC图谱、不同IPU加酶量对右旋糖酐产物占比的影响及其1H-NMR检测
Fig.4 HPLC analysis of product prepared by three enzymes, the effect of IPU amount on dextran proportion and relevant 1H-NMR analysis
2.2 降解步骤IMOs的制备
2.2.1 BfIMTD加酶量对制备IMOs的影响
依据相关方法对BfIMTD进行重组表达,测得胞外上清液的酶活力为7.8 U/mL,说明BfIMTD在大肠杆菌中表达成功。根据MIZUNO等[24]对BfIMTD的研究表明,该重组BfIMTD最适温度为45 ℃,最适pH为7.5。按照1.4.1所述方法使用酵母将产品中的葡萄糖消化,随后冷冻干燥制成粉末。在40 ℃和pH 7.5的条件下,使用上述右旋糖酐(终质量浓度为100 g/L)与BfIMTD反应4 h探究BfIMTD加酶量对产出IMOs的影响。如图5所示,BfIMTD展现其产物特异性,高效产出IG3,IG3的产率在加酶量为150 U/g时可以达到最高93.6 g/L,两步法总的IG3转化率为62.1%。

图5 BfIMTD不同加酶量对IMOs产量的影响
Fig.5 The effect of BfIMTD amount on IMOs production
2.2.2 反应时长对制备IMOs的影响
在40 ℃和pH 7.5的条件下,使用右旋糖酐溶液(终质量浓度为100 g/L)与150 U/g加酶量的BfIMTD反应。如图6所示,从反应2 h开始BfIMTD产出84.6 g/L的IG3,随后缓慢增加,在10 h时达到最高质量浓度98.3 g/L,此时两步法IG3总的转化率为65.2%,随后产率保持平缓至12 h。外切酶BfIMTD特异性产出IG3,产品符合对IMOs益生性能的要求。
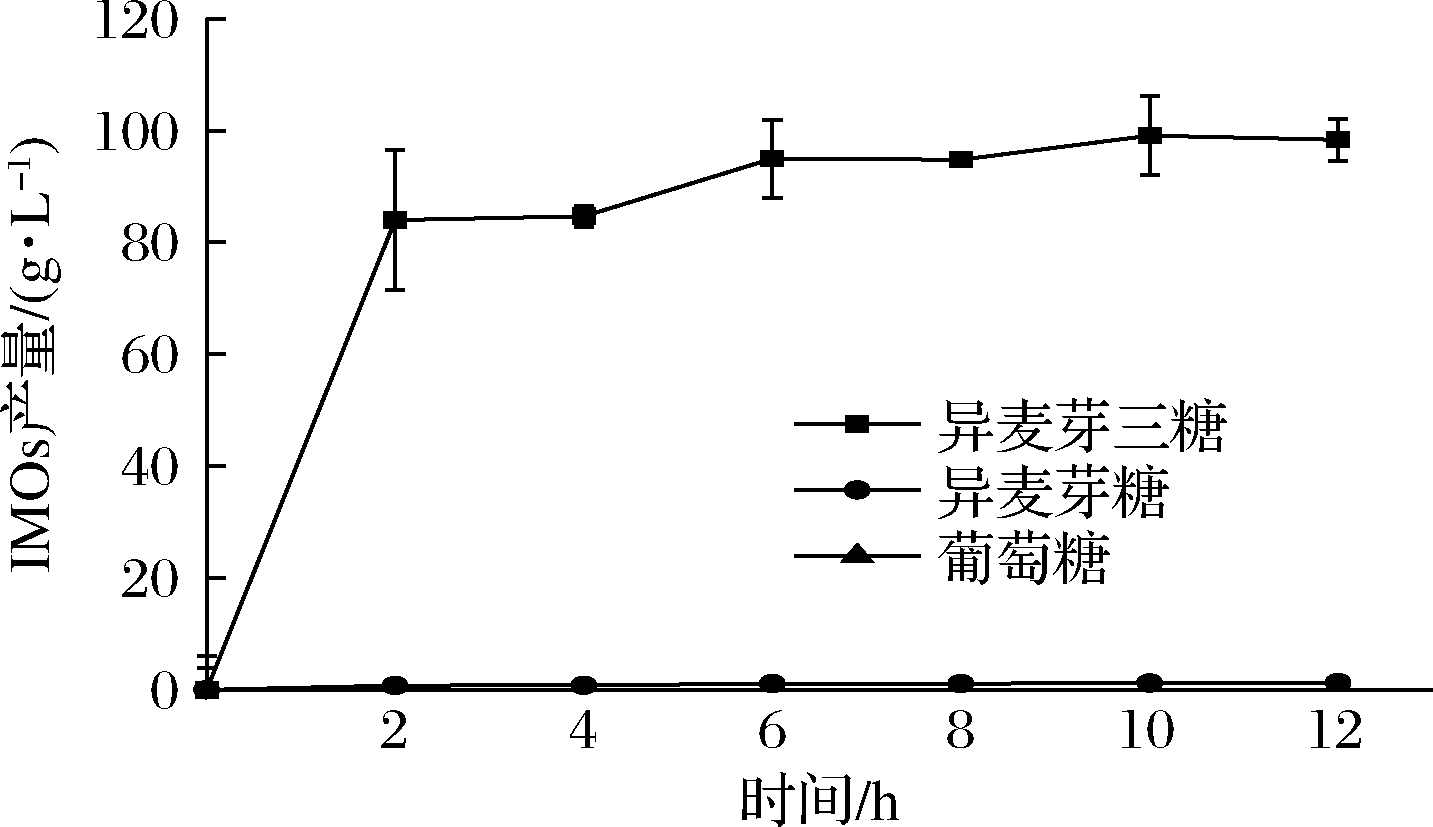
图6 反应时长对BfIMTD产出IMOs的影响
Fig.6 The effect of reaction time by BfIMTD on IMOs yield
3 结论与讨论
以淀粉酶主导制备IMOs的传统方法工艺复杂、产率低、有效成分含量低;以右旋糖酐蔗糖酶主导的制备IMOs方法成本高,且产品中含有无法被利用的葡萄糖且其产物右旋糖酐聚合度不可控。本研究开发了4,6-α-葡聚糖基转移酶和异麦芽三糖右旋糖酐酶高效制备IMOs的两步法工艺,第1步优化单酶、双酶、三酶复配体系,以提高中间产物右旋糖酐的产量和α-1,6糖苷键比率,使用普鲁兰酶和LfGT复配时,可以得到产物占比为73.1%的右旋糖酐,其α-1,6 糖苷键比率为89.2%,使用IPU、普鲁兰酶与LfGT复配催化DE2麦芽糊精,可以得到产物占比为66.3%的右旋糖酐,此时其α-1,6糖苷键比率可达99.3%;第2步对异麦芽三糖右旋糖酐酶降解右旋糖酐产出IMOs进行优化,以制备IG3占比更高的IMOs产品,使用BfIMTD降解三酶复配产出的右旋糖酐可以产出98.3 g/L的IG3,此时两步法IG3的产率为65.2%。本研究还可以在以下这些方面展开后续研究:
(1) 本研究的合成步骤后续可通过数据库挖掘或自然筛选获取能够有效利用麦芽糖、麦芽三糖的4,6-α-GTs,进一步提升右旋糖酐产率,同时对4,6-α-GTs催化的链长范围进行探究,以产出链长更可控的右旋糖酐或IMOs。
(2) 本研究的降解步骤选用的表达宿主是大肠杆菌,其表达量高、通用性好,但是IMOs主要用于食品领域,因此后续研究可选用食品安全菌枯草芽孢杆菌对所需右旋糖酐酶进行重组表达和制备研究,以满足食品工业应用需求。
[1] 王良东. 低聚异麦芽糖性质、功能、 生产和应用[J].粮食与油脂, 2008,21(4):43-47.
WANG L D.The properties, functions, production and utilizations of isomaltooligosacharide[J].Journal of Cereals and Oils, 2008,21(4):43-47.
[2] SORNDECH W, NAKORN K N, TONGTA S, et al.Isomalto-oligosaccharides:Recent insights in production technology and their use for food and medical applications[J].LWT, 2018, 95:135-142.
[3] KANEKO T, KOHMOTO T, KIKUCHI H, et al.Effects of isomaltooligosaccharides with different degrees of polymerization on human fecal bifidobacteria[J].Bioscience, Biotechnology and Biochemistry, 1994, 58(12):2 288-2 290.
[4] KOHMOTO T, FUKUI F, TAKAKU H, et al.Effect of isomalto-oligosaccharides on human fecal flora[J].Bifidobacteria and Microflora, 1988, 7(2):61-69.
[5] WU Q Q, PI X E, LIU W, et al.Fermentation properties of isomaltooligosaccharides are affected by human fecal enterotypes[J].Anaerobe, 2017, 48:206-214.
[6] SORNDECH W, SAGNELLI D, BLENNOW A, et al.Combination of amylase and transferase catalysis to improve IMO compositions and productivity[J].LWT-Food Science and Technology, 2017, 79:479-486.
[7] LEE H S, AUH J H, YOON H G, et al.Cooperative action of α-glucanotransferase and maltogenic amylase for an improved process of isomaltooligosaccharide (IMO) production[J].Journal of Agricultural and Food Chemistry, 2002, 50(10):2 812-2 817.
[8] GAN W W, ZHANG H B, ZHANG Y Q, et al.Biosynthesis of oligodextrans with different Mw by synergistic catalysis of dextransucrase and dextranase[J].Carbohydrate Polymers, 2014, 112:387-395.
[9] SHUKLA S, SHI Q, MAINA N H, et al.Weissella confusa Cab3 dextransucrase:Properties and in vitro synthesis of dextran and glucooligosaccharides[J].Carbohydrate Polymers, 2014, 101:554-564.
[10] SONG J Y, KIM Y M, LEE B H, et al.Increasing the dietary fiber contents in isomaltooligosaccharides by dextransucrase reaction with sucrose as a glucosyl donor[J].Carbohydrate Polymers, 2020, 230:115 607.
[11] HUANG S X, HOU D Z, QI P X, et al.Enzymatic synthesis of non-digestible oligosaccharide catalyzed by dextransucrase and dextranase from maltose acceptor reaction[J].Biochemical and Biophysical Research Communications, 2020, 523(3):651-657.
[12] GOULAS A K, FISHER D A, GRIMBLE G K, et al.Synthesis of isomaltooligosaccharides and oligodextrans by the combined use of dextransucrase and dextranase[J].Enzyme and Microbial Technology, 2004, 35(4):327-338.
[13] KRALJ S, GRIJPSTRA P, VAN LEEUWEN S S, et al.4,6-α-glucanotransferase, a novel enzyme that structurally and functionally provides an evolutionary link between glycoside hydrolase enzyme families 13 and 70[J].Applied and Environmental Microbiology, 2011, 77(22):8 154-8 163.
[14] BAI Y X, GANGOITI J, DIJKSTRA B W, et al.Crystal structure of 4,6-α-glucanotransferase supports diet-driven evolution of GH70 enzymes from α-amylases in oral bacteria[J].Structure, 2017, 25(2):231-242.
[15] ARD VOL A, ROVIRA C.Reaction mechanisms in carbohydrate-active enzymes:Glycoside hydrolases and glycosyltransferases.Insights from ab initio quantum mechanics/molecular mechanics dynamic simulations[J].Journal of the American Chemical Society, 2015, 137(24):7 528-7 547.
VOL A, ROVIRA C.Reaction mechanisms in carbohydrate-active enzymes:Glycoside hydrolases and glycosyltransferases.Insights from ab initio quantum mechanics/molecular mechanics dynamic simulations[J].Journal of the American Chemical Society, 2015, 137(24):7 528-7 547.
[16] LEEMHUIS H, DOBRUCHOWSKA J M, EBBELAAR M, et al.Isomalto/malto-polysaccharide, a novel soluble dietary fiber made via enzymatic conversion of starch[J].Journal of Agricultural and Food Chemistry, 2014, 62(49):12 034-12 044.
[17] BAI Y X, VAN DER KAAIJ R M, LEEMHUIS H, et al.Biochemical characterization of the Lactobacillus reuteri glycoside hydrolase family 70 GTFB type of 4,6-α-glucanotransferase enzymes that synthesize soluble dietary starch fibers[J].Applied and Environmental Microbiology, 2015, 81(20):7 223-7 232.
[18] GANGOITI J, VAN LEEUWEN S S, MENG X F, et al.Mining novel starch-converting glycoside hydrolase 70 enzymes from the nestlé culture collection genome database:The Lactobacillus reuteri NCC 2613 GtfB[J].Scientific Reports, 2017, 7(1):9 947.
[19] 宿玲恰, 张悦, 吴敬.嗜热栖热菌海藻糖合酶的分子改造及其应用[J].食品与发酵工业, 2015, 41(12):1-5.
SU L Q, ZHANG Y, WU J.Molecular modification and application of trehalose synthase from Thermus themophilus[J].Food and Fermentation Industries, 2015, 41(12):1-5
[20] 刘玲玲. β-葡萄糖苷酶转化葡萄糖制备低聚龙胆糖的研究[D].无锡:江南大学, 2009.
LIU L L.Studies on production of gentiooligosaccharide from glucose with β-glucosidase[D].Wuxi:Jiangnan University, 2009.
[21] MILLER G L.Use of dinitrosalicylic acid reagent for determination of reducing sugar[J].Analytical Chemistry, 1959, 31(3):426-428.
[22] AKEBOSHI H, KASHIWAGI Y, AOKI H, et al.Construction of an efficient expression system for Aspergillus isopullulanase in Pichia pastoris, and a simple purification method[J].Bioscience Biotechnology and Biochemistry, 2003, 67(5):1 149-1 153.
[23] SAKANO Y, HIGUCHI M, KOBAYASHI T.Pullulan 4-glucanohydrolase from Aspergillus niger[J].Archives of Biochemistry and Biophysics, 1972, 153(1):180-187.
[24] MIZUNO T, MORI H, ITO H, et al.Molecular cloning of isomaltotrio-dextranase gene from Brevibacterium fuscum var.dextranlyticum strain 0407 and its expression in Escherichia coli[J].Bioscience, Biotechnology and Biochemistry, 1999, 63(9):1 582-1 588.