亚硝酸盐广泛存在于土壤、水域及植物中[1],是一种常用的食品添加剂,乳制品、泡菜、腌腊肉等食物中含量较高[2]。这类添加剂能赋予食品良好的外观色泽和独特风味,延缓其氧化酸败,延长货架期,抑制腐败菌的生长繁殖,阻止致病菌导致的食物中毒[3]。但是若从食物中摄取过量的亚硝酸盐,会严重威胁人类健康。首先在亚硝酸盐作用下,人体亚铁血红蛋白会丧失携带氧的能力,严重时会危及生命[4-5],其次亚硝酸盐在胃内酸性环境中,会与人体内的伯胺及酰胺类物质发生亚硝化反应生成N-亚硝胺;亚硝胺类化合物是一种强致癌物质,会引起食管癌,胃癌,咽喉癌,肝癌和大肠癌等[6]。此外,亚硝酸盐还可能引发人类先天畸形,其是中枢神经系统先天畸形高发的重要原因之一[7-8]。因此,分析检测食品中亚硝酸盐的含量,无论是对食品企业的生产监督还是对消费者的饮食安全都具有极为重要的意义。
目前,用来检测食品中亚硝酸盐的方法较多[9-10],有离子色谱法[11-13]、紫外分光光度法[14-16]、催化光度法[17-18]、电化学分析法[19-22]等。其中,电化学分析法重现性差且耗时长;色谱法和光谱法仪器昂贵,分析复杂;紫外分光光度法易操作,但灵敏度较低。荧光光度法因具有检测快捷、灵敏度高、样品用量少、选择性强等优点[23-24],受到了很多研究者的关注。本文利用酸性条件下![]() 与过量的KI反应生成
与过量的KI反应生成![]() 阴离子,
阴离子,![]() 可与罗丹明6G形成离子缔合物,使得罗丹明6G发生荧光猝灭,且体系的荧光猝灭值ΔF与
可与罗丹明6G形成离子缔合物,使得罗丹明6G发生荧光猝灭,且体系的荧光猝灭值ΔF与![]() 的质量浓度呈良好的线性关系的原理建立了一种测定
的质量浓度呈良好的线性关系的原理建立了一种测定![]() 的新方法。
的新方法。
1.1.1 仪器与设备
BSA124S型电子天平,北京赛多利斯仪器系统有限公司;UV-2600型紫外-可见分光光度,日本理学公司;Cary Eclipse荧光光度计,安捷伦科技有限公司;JXL-2S-2A数显恒温水浴锅,江苏省金坛市金祥龙电子有限公司;DHG-9070A电热恒温鼓风干燥箱,上海齐欣科学仪器有限公司。
1.1.2 试剂与材料
亚硝酸钠、碘化钾、硫酸、罗丹明6G、吐温-80,均为分析纯试剂。配制储备液:0.08 g/L ![]() 溶液;0.1 mol/L KI溶液;0.1 mol/L H2SO4溶液;5×10-5mol/L罗丹明6G溶液;1.0 g/L吐温-80溶液;饱和硼砂溶液;50 g/L的硫酸锌溶液;实验用水为超纯水。
溶液;0.1 mol/L KI溶液;0.1 mol/L H2SO4溶液;5×10-5mol/L罗丹明6G溶液;1.0 g/L吐温-80溶液;饱和硼砂溶液;50 g/L的硫酸锌溶液;实验用水为超纯水。
材料:火腿肠(2种品牌),采购自超市。
在25 mL比色管中,先加适量![]() 标准溶液,然后加入2.0 mL 0.1 mol/L KI溶液稀释到10 mL,再加入2.0 mL 0.1 mol/L H2SO4溶液,在暗处放置10 min 后加入2.0 mL 5×10-5 mol/L罗丹明6G溶液和1.0 mL 1.0 g/L吐温-80溶液,最后用超纯水定容,摇匀,锡箔纸包裹保存。在477 nm的激发波下,于552 nm处测其荧光强度F,并测定不加
标准溶液,然后加入2.0 mL 0.1 mol/L KI溶液稀释到10 mL,再加入2.0 mL 0.1 mol/L H2SO4溶液,在暗处放置10 min 后加入2.0 mL 5×10-5 mol/L罗丹明6G溶液和1.0 mL 1.0 g/L吐温-80溶液,最后用超纯水定容,摇匀,锡箔纸包裹保存。在477 nm的激发波下,于552 nm处测其荧光强度F,并测定不加![]() 的试剂空白荧光强度值为F0、计算荧光猝灭值ΔF=F0-F,并以ΔF对
的试剂空白荧光强度值为F0、计算荧光猝灭值ΔF=F0-F,并以ΔF对![]() 质量浓度作图,通过得到的标准曲线确定样品中
质量浓度作图,通过得到的标准曲线确定样品中![]() 含量。
含量。
准确称取捣碎且混匀的火腿肠样品10.00 g于烧杯中,加入6 mL饱和硼砂溶液,搅拌均匀,再加入60 mL 80 ℃热水。置沸水浴中加热15 min取出,边搅拌边加入5 mL 50 g/L的硫酸锌溶液,以沉淀蛋白质。冷却至室温,转入1 L容量瓶中,用水定容,摇匀。静置15 min,弃去上层脂肪,清液用滤纸过滤,弃去初滤液10 mL,收集其余滤液存于试剂瓶中作为分析试液,进行样品分析[13-14]。
实验表明,在477 nm激发光照射下,KI-罗丹明6G在552 nm出现最强荧光发射,当溶液中存在![]() 时,
时,![]() 与体系中的KI反应生成
与体系中的KI反应生成![]() 与罗丹明6G分子形成离子络合物,使其荧光猝灭,不同浓度
与罗丹明6G分子形成离子络合物,使其荧光猝灭,不同浓度![]() 对KI-罗丹明6G体系荧光强度的影响见图1,可明显看出随着
对KI-罗丹明6G体系荧光强度的影响见图1,可明显看出随着![]() 浓度的增大,KI-罗丹明6G体系的荧光强度逐渐减弱。本实验选用477 nm作为荧光激发波长,在552 nm处测定体系荧光淬灭值ΔF,以达到对
浓度的增大,KI-罗丹明6G体系的荧光强度逐渐减弱。本实验选用477 nm作为荧光激发波长,在552 nm处测定体系荧光淬灭值ΔF,以达到对![]() 的定量分析。
的定量分析。
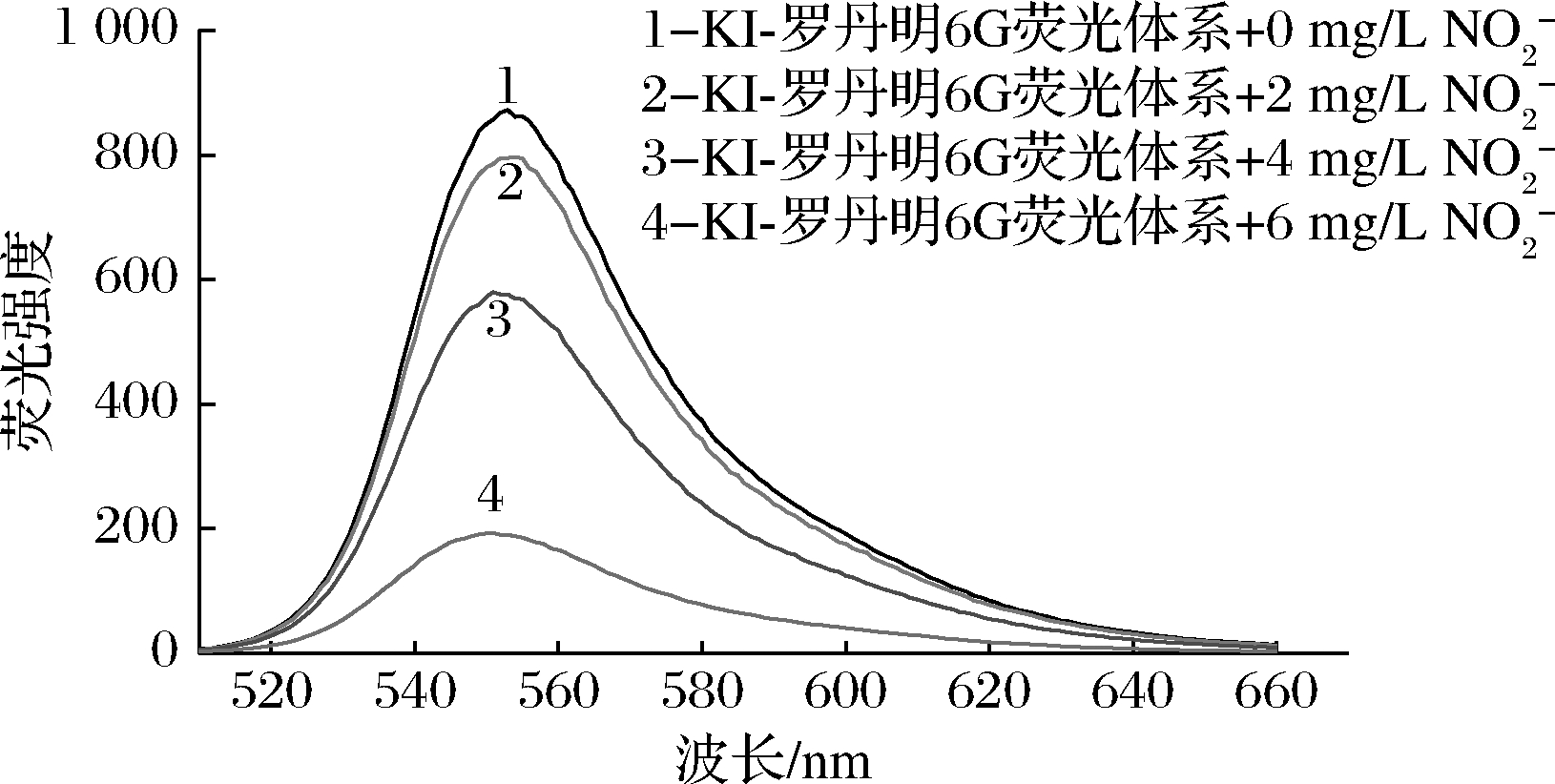
图1 不同浓度的![]() 存在时KI -罗丹明6G的荧光强度
存在时KI -罗丹明6G的荧光强度
Fig.1 Fluorescence spectra of KI-rhodamine 6G with
different concentration of ![]()
2.2.1 H2SO4用量对测定结果的影响
按1.2中的实验方法,保证其他条件不变,改变0.1 mol/L H2SO4的加入量分别为0.5、1.0、1.5、2.0、2.5、3.0 mL,测定罗丹明6G的荧光猝灭情况,结果如图2-a所示。当H2SO4加入量为2.0 mL时,体系荧光猝灭值ΔF最大;随着硫酸加入量的增大,荧光猝灭值ΔF有所减小。故实验选择0.1 mol/L H2SO4加入量为2.0 mL。
2.2.2 KI用量对体系测定结果的影响
固定其他条件及0.1 mol/L H2SO4用量2.0 mL不变,改变0.1 mol/L KI溶液的加入量分别为0.5、1.0、1.5、2.0、2.5 mL,按1.2实验方法测定试液荧光猝灭值,结果如图2-b所示。当KI加入量为2.0 mL时,体系荧光猝灭值ΔF最大,反应最灵敏,故实验选择0.1 mol/L KI加入量为2.0 mL。
2.2.3 吐温-80用量对体系测定结果的影响
由于离子缔合物具有疏水性,为使其稳定地存在于水溶液中,通常加入表面活性剂,吐温-80可用于罗丹明光度分析的研究[15]。固定其他条件不变,硫酸、碘化钾用量为上述讨论的最佳用量,改变1.0 g/L吐温-80加入量分别为0、0.5、1.0、1.5、2.0 mL,体系荧光猝灭值ΔF如图2-c所示。吐温-80加入量为0.5 mL时,体系的荧光猝灭值ΔF最大。故实验选择1.0 g/L吐温-80加入量为0.5 mL。
2.2.4 罗丹明6G用量对体系测定结果的影响
在上述实验确定的硫酸、碘化钾、吐温-80最佳用量的基础上,分别考察了5×10-5 mol/L罗丹明6G加入量为1.0、1.5、2.0、2.5、3.0 mL时,体系荧光猝灭值ΔF的变化,结果如图2-d所示。当罗丹明6G加入量为2.0 mL时,体系的荧光猝灭值ΔF最大,故实验选择5×10-5 mol/L罗丹明6G加入量为2.0 mL。
2.2.5 反应时间对体系测定结果的影响
确定上述讨论的最佳条件不变,按照1.2实验方法,使KI-罗丹明6G荧光体系及![]() 罗丹明6G样品液同时反应5、10、15、20、25 min后测定其荧光强度,以考察反应时间对体系荧光猝灭值的影响,结果如图2-e所示。反应15 min后,体系荧光猝灭值ΔF基本不再有显著增大,这说明
罗丹明6G样品液同时反应5、10、15、20、25 min后测定其荧光强度,以考察反应时间对体系荧光猝灭值的影响,结果如图2-e所示。反应15 min后,体系荧光猝灭值ΔF基本不再有显著增大,这说明![]() 罗丹明6G荧光猝灭反应可以在15 min之内完成。但考虑到长期光照可能会引起空气中的氧气将KI缓慢氧化,因此选定测定最佳时间为反应15~30 min完成。
罗丹明6G荧光猝灭反应可以在15 min之内完成。但考虑到长期光照可能会引起空气中的氧气将KI缓慢氧化,因此选定测定最佳时间为反应15~30 min完成。

a-0.1 mol/L H2SO4用量对体系荧光猝灭值的影响;b-0.1 mol/ L KI溶液用量对体系荧光猝灭值的影响;c-0.1 g/L吐温-80
用量对体系荧光猝灭值的影响;d-5×10-5 mol/L罗丹明6G用量对体系荧光猝灭值的影响;e-反应时间对体系荧光猝灭值的影响
图2 实验条件优化
Fig.2 Optimization of experimental conditions
综上各单因素实验可知,0.1 mol/L H2SO4用量为2.0 mL,0.1 mol/L KI用量为2.0 mL,1.0 g/L吐温-80加入量为0.5 mL,5×10-5 mol/L罗丹明6G加入量为2.0 mL,反应时间为15~30 min时体系的荧光猝灭程度最大,即为测定![]() 最佳条件。
最佳条件。
准确配制质量浓度20、40、60、80、100、120、140、160、180、200、220、240、260、280 μg/L的![]() 标准溶液,在选定的最佳实验条件下,按照1.2实验方法分别测定加入上述NO2标准溶液4.0 mL时体系的荧光猝灭情况。以荧光猝灭值ΔF对
标准溶液,在选定的最佳实验条件下,按照1.2实验方法分别测定加入上述NO2标准溶液4.0 mL时体系的荧光猝灭情况。以荧光猝灭值ΔF对![]() 质量浓度作图得工作曲线,如图3所示。
质量浓度作图得工作曲线,如图3所示。![]() 质量浓度在30~240 μg/L时与体系的荧光强度猝灭值呈良好的线性关系,线性回归方程为:ΔF = 1.944 4ρ-25.178,相关系数r= 0.997 5。按IUPAC估算该方法的检出限为23.3 μg/L。同时,对加入160 μg/L
质量浓度在30~240 μg/L时与体系的荧光强度猝灭值呈良好的线性关系,线性回归方程为:ΔF = 1.944 4ρ-25.178,相关系数r= 0.997 5。按IUPAC估算该方法的检出限为23.3 μg/L。同时,对加入160 μg/L ![]() 标准溶液的试液进行11次平行测定,其相对标准偏差(relative standard deviation,RSD)为2.7%。
标准溶液的试液进行11次平行测定,其相对标准偏差(relative standard deviation,RSD)为2.7%。
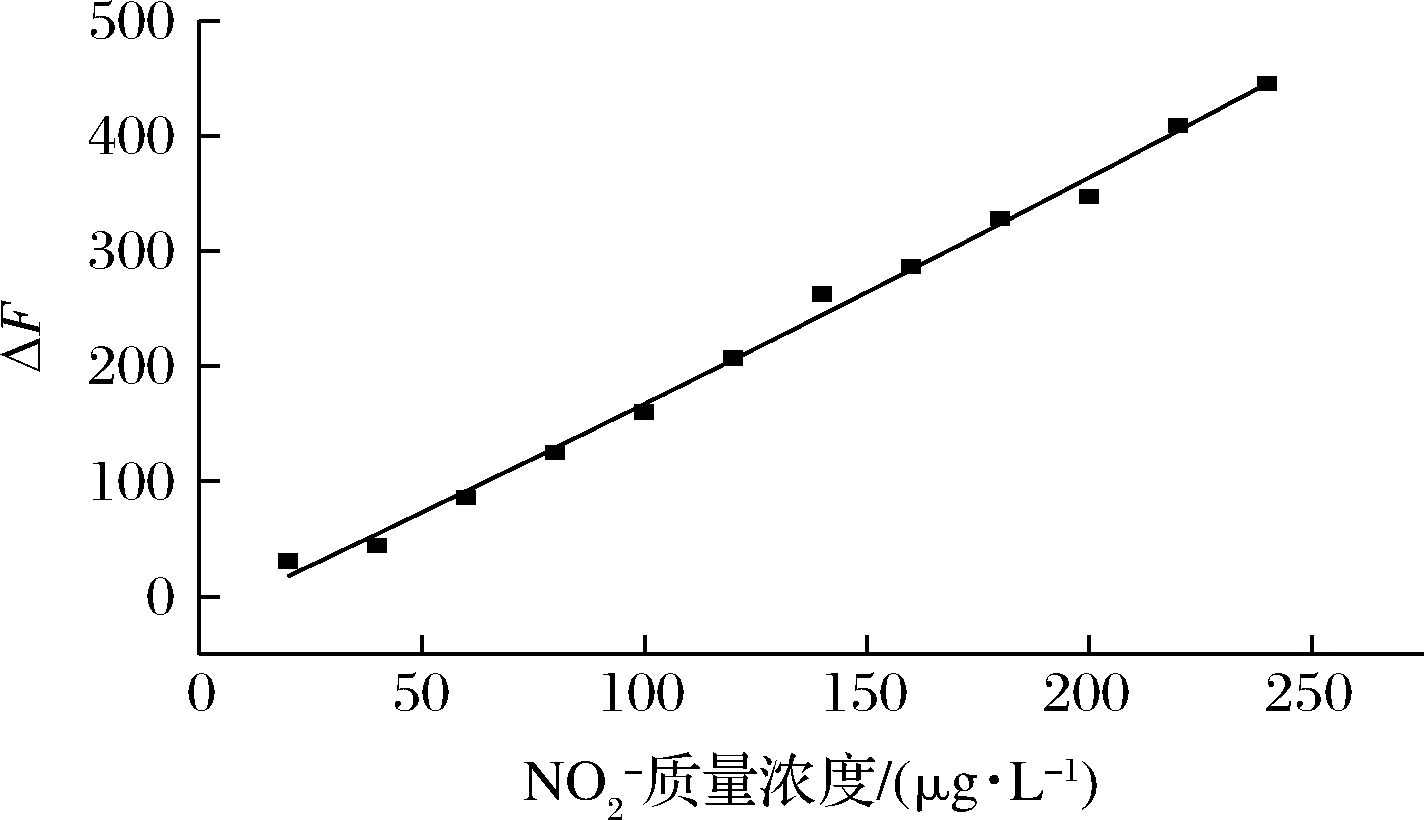
图3 标准曲线
Fig.3 Calibration curves
在优化的实验条件下,选择![]() 标准溶液,考察了一些常见组分对体系测定结果的影响。按照1.2实验方法,分别测定了上述共存离子对罗丹明6G的荧光猝灭情况。结果表明,当相对误差≤±5%时,共存离子质量浓度可允许的倍数为:1 000倍的
标准溶液,考察了一些常见组分对体系测定结果的影响。按照1.2实验方法,分别测定了上述共存离子对罗丹明6G的荧光猝灭情况。结果表明,当相对误差≤±5%时,共存离子质量浓度可允许的倍数为:1 000倍的![]() 倍的
倍的![]() 倍的Cd2+;200倍的Ni2+、Al3+、Zn2+;100倍的
倍的Cd2+;200倍的Ni2+、Al3+、Zn2+;100倍的![]() 倍的Fe3+,说明该方法的选择性较好。
倍的Fe3+,说明该方法的选择性较好。
按照1.3方法将2种火腿肠样品各处理3份,移取处理好的火腿肠样品溶液参照1.2实验方法测定其荧光猝灭值ΔF,确定样品中亚硝酸盐的含量。为了检验该方法的准确度,同时也采用国标比色法进行对比测定,并做加标回收率试验,结果如表1所示。采用该方法测定2种火腿肠样品中亚硝酸盐含量分别为11.18、18.72 mg/kg,测定值与比色法检测结果基本一致,所测回收率为95.5%~105.3%,表明该方法具有较高的准确度与精密度,可用于实际样品分析。
表1 火腿肠中亚硝酸盐分析结果(n=3)
Table 1 Analytical results of nitrite in ham sausage (n=3)

样品测定值/样品亚硝酸盐含量/(mg·kg-1)加标量/测定值/回收率/%RSD/%(μg·L-1)本方法比色法(μg·L-1)(μg·L-1)样品1187.218.7217.8530.0218.8105.32.2样品2111.811.1812.5020.0130.995.53.4
本实验基于酸性溶液中,![]() 与过量的KI反应生成
与过量的KI反应生成![]() 阴离子,
阴离子,![]() 可与罗丹明6G形成离子缔合物,并使罗丹明6G发生荧光猝灭的原理,建立了一种KI-罗丹明6G荧光猝灭法检测
可与罗丹明6G形成离子缔合物,并使罗丹明6G发生荧光猝灭的原理,建立了一种KI-罗丹明6G荧光猝灭法检测![]() 的新方法。该方法灵敏度高,选择性好,测定快速且准确,为食品中亚硝酸盐含量的测定提供了依据。采用该方法测定2种市售火腿肠样品中亚硝酸盐含量分别为11.18、18.72 mg/kg,与国标法检测结果基本一致,所测回收率为95.5%~105.3%,测定效果良好。
的新方法。该方法灵敏度高,选择性好,测定快速且准确,为食品中亚硝酸盐含量的测定提供了依据。采用该方法测定2种市售火腿肠样品中亚硝酸盐含量分别为11.18、18.72 mg/kg,与国标法检测结果基本一致,所测回收率为95.5%~105.3%,测定效果良好。
[1] 马卓能, 黎奕锋, 祁巧茹, 等.模拟胃条件下不同配搭食物中亚硝酸盐含量变化研究[J].现代预防医学, 2014, 41(3):426-428.
MA Z N, LI Y F, QI Q R, et al.Research of change of nitrite content in different supplements of food under the condition of simulated stomach[J].Modern Preventive Medicine, 2014, 41(3):426-428.
[2] 张会亮, 苗贝贝, 黄传峰, 等.液相色谱-串联质谱法测定火腿肠和咸菜中亚硝酸盐含量[J].食品安全质量检测学报, 2018, 9(20):5 313-5 318.
ZHANG H L, MIAO B B, HUANG C F, et al.Determination of nitrite in ham sausage and pickles by liquid chromatography-tandem mass spectrometry[J].Journal of Food Safety and Quality, 2018, 9(20):5 313-5 318.
[3] 夏远, 高玉敏, 张国龙, 等.内蒙古医科大学新华校区周围市售香肠和火腿肠中亚硝酸盐含量的测定[J].食品安全质量检测学报, 2016, 7(12):4 904-4 907.
XIA Y, GAO Y M, ZHANG G L, et al.Determination of nitrite concentration in the commercial sausage and ham from Xinhua district of Inner Mongolia medical university[J].Journal of Food Safety and Quality, 2016, 7(12):4 904-4 907.
[4] BRENDER J D, OLIVE J M, FELKNER M, et al.Dietary nitrites and nitrates, nitrosatable drugs, and neural tube defects[J].Epidemiology(Cambridge,Mass.), 2004(15):330-336.
[5] 谢燕丹, 刘零怡, 楼乔明, 等.加工蔬菜中亚硝酸盐的消除技术研究进展[J].食品与发酵工业, 2016, 42(8):279-286.
XIE Y D, LIU L Y, LOU Q M, et al.Advances on nitrite-eliminating in vegetable processing[J].Food and Fermentation Industries, 2016, 42(8):279-286.
[6] 钱文文, 辛宝.α-萘胺显色法测定5种市售火腿肠中亚硝酸盐含量[J].食品安全导刊, 2016(24):91-92.
QIAN W W, XIN B.Determination of nitrite content in five kinds of ham sausage by α-naphthalamine colorimetric method[J].China Food Safety Magazine, 2016(24):91-92.
[7] CROEN L A, TODOROFF K, SHAW G M.Maternal exposure to nitrate from drinking water and diet and risk for neural tube defects[J].American Journal of Epidemiology, 2001, 153(4):325-331.
[8] CEDERGREN M I, SELBING A J, LÖFMAN O, et al.Chlorination by products and nitrate in drinking water and risk for congenital cardiac defects[J].Environmental Research, 2002, 89(2):124-130.
[9] 杜红霞, 贺稚非, 李洪军.食品中亚硝酸盐检测技术研究进展[J].肉类研究, 2006,20(1):41-45;7.
DU H X, HE Z F, LI H J.Study on the development of nitrite′s detective technology in foods[J].Meat Research, 2006,20(1):41-45;7.
[10] 赵静, 王娜, 冯叙桥, 等.蔬菜中硝酸盐和亚硝酸盐检测方法的研究进展[J].食品科学, 2014, 35(8):42-49.
ZHAO J, WANG N, FENG X Q, et al.Advances in detection methods for nitrate and nitrite in vegetables[J].Food Science, 2014, 35(8):42-49.
[11] 蔡荟梅, 侯如燕, 高柱, 等.离子色谱法测定茶叶中的硝酸盐和亚硝酸盐[J].茶叶科学, 2012, 32(2):95-99.
CAI H M, HOU R Y, GAO Z, et al.Determination of nitrate and nitrite in tea by ion chromatography[J].Journal of Tea Science, 2012, 32(2):95-99.
[12] 韩春霞, 梁立娜, 范慧红.离子色谱法测定达肝素钠中的亚硝酸根[J].药物分析杂志, 2011, 31(11):2 171-2 173.
HAN C X, LIANG L N, FAN H H.Determination of nitrite in dalttparin sodium by ion chromatography[J].Chinese Journal of Pharmaceutical Analysis, 2011, 31(11):2 171-2 173.
[13] 战旭梅, 刘靖, 刘萍.高效液相色谱法测定香肠中亚硝酸盐含量[J].食品与机械, 2014, 30(6):72-74.
ZHAN X M, LIU J, LIU P.Determination of nitrite in sausage by high pressure liquid chromatography[J].Food & Machinery,2014, 30(6):72-74.
[14] 聂峰, 吴迎春, 陈德径, 等.一种新的食品中亚硝酸盐含量测定方法研究[J].食品科学, 2009, 30(4):221-223.
NIE F, WU Y C, CHEN D J, et al.A new determination method of nitrite in foods[J].Food Science, 2009, 30(4):221-223.
[15] 龚建康, 田维贵, 叶坪.市售香肠中亚硝酸盐含量的测定[J].昭通学院学报, 2018, 40(5):29-33.
GONG J K, TIAN W G, YE P.Determination of nitrite content from the commercial sausage[J].Journal of Zhaotong University, 2018, 40(5):29-33.
[16] CHERIAN T, NARAYANA B.A new system for the spectrophotometric determination of trace amounts of nitrite in environmental samples[J].Journal of the Brazilian Chemical Society, 2006, 17(3):577-581.
[17] 胡卫平, 董学芝, 何智娟.甲基紫动力学催化光度法测定火腿肠中痕量亚硝酸根[J].分析试验室, 2005, 24(1):59-62.
HU W P, DONG X Z, HE Z J.Determination of trace nitrite by catalytic spectrophotometric method with methyl violet[J].Chinese Journal of Analysis Laboratory, 2005, 24(1):59-62.
[18] 熊海涛. 催化光度法检测香肠与小青菜中的亚硝酸盐含量[J].食品工业, 2014, 35(8):277-280.
XIONG H T.Detection of trace nitrite in sausage and small greens with catalytic spectrophotometry[J].The Food Industry, 2014, 35(8):277-280.
[19] 陈晓东, 郭培源.基于主成分分析法提取高光谱图像特征检测香肠亚硝酸盐含量[J].肉类研究, 2016, 30(12):22-27.
CHEN X D, GUO P Y.Detection of nitrite in sausages based on feature extraction of hyperspectral images using principal component analysis[J].Meat Research, 2016, 30(12):22-27.
[20] YILMAZ Ü T, SOMER G.Determination of trace nitrite by direct and indirect methods using differential pulse polarography and application[J].Journal of Electroanalytical Chemistry, 2008, 624(1-2):59-63.
[21] 汪雪, 李辉, 吴敏, 等.石墨烯壳聚糖金纳米粒子修饰电极同时测定亚硫酸根和亚硝酸根[J].分析化学, 2013, 41(8):1 232-1 237.
WANG X, LI H, WU M, et al.Simultaneous electrochemical determination of sulphite and nitrite using a gold nanoparticle/graphene-chitosan modified electrode[J].Chinese Journal of Analytical Chemistry, 2013, 41(8):1 232-1 237.
[22] ZHANG Y M, HUANG H P, XU L.A novel electrochemical sensor based on Au-Dy2 (WO4)3 nanocomposites for simultaneous determination of uric acid and nitrite[J].Chinese Journal of Analytical Chemistry, 2020, 48(3):e20 032-e20 037.
[23] 王益林, 陆建平, 汤艳荣, 等.罗丹明6G荧光猝灭法测定中草药中微量铁[J].分析试验室, 2008, 27(7):109-111.
WANG Y L, LU J P, TANG Y R, et al.Determination of iron in chinese herbal medicine based on fluorescence quenching of rhodamine 6G[J].Chinese Journal of Analysis Laboratory, 2008, 27(7):109-111.
[24] 王丹, 罗红群, 李念兵.碘化物-罗丹明6G体系共振瑞利散射法测定痕量铅[J].环境化学, 2005, 24(1):97-100.
WANG D, LUO H Q, LI N B.Resonance Rayleigh scattering method for the determination of trace lead with iodide-rhodamine 6G system[J].Environmental Chemistry, 2005, 24(1):97-100.