香气是影响茶叶品质的一个重要属性,主要由茶叶中的挥发性物质所决定[1-2]。挥发性物质的形成受多种因素的影响,如品种、生长环境、加工工艺等[3]。根据加工方式和品质特征的不同,茶叶可分为绿茶、白茶、黄茶、乌龙茶、红茶和黑茶六大类[4],不同的茶类具有明显不同的香气特征。目前,国内外学者对此做了大量的研究,研究重点多集中在香气化合物的鉴定和不同茶类香气差异的分析上[5-6]。BALDERMANN等[7]对来自不同国家和地区的绿茶、乌龙茶和红茶进行分析,发现随着发酵程度的增加,挥发性化合物的含量随之增加。WANG等[8]的研究表明,不同类型的茶叶其香气组成和含量差异很大,可利用挥发性化合物的聚类分析对不同的茶叶进行分类。YE等[9]通过对生熟2种普洱茶的香气化合物进行分析,指出甲氧酚类化合物和醇类衍生物可作为普洱生茶和熟茶的鉴别标记物。鉴于大多数研究所采用的样品来自不同原料,难免会存在例如品种或生长环境等所带来的干扰,对结果造成很大的影响。因此,本研究采用同一来源的梅占品种鲜叶加工六大茶类,通过气相色谱质谱联用(gas chromatography-mass spectrometry,GC-MS)技术对样品中的挥发性化合物进行检测,通过方差分析、主成分分析(principal component analysis,PCA)和正交偏最小二乘判别分析(orthogonal partial least squares discriminant analysis,OPLS-DA)等化学计量学方法对GC-MS数据进行降维和筛选,找出区分不同茶类的标志性化合物,通过计算化合物气味活性值(odor activity value,OAV)和香气特征影响值(aroma character impact value,ACI)评价各挥发性化合物对成茶香气的贡献度,以此探究六大茶类香气形成的差异,可为茶叶的定向加工与品质调控提供依据,更好地指导生产,充分发挥各茶类的风味优势。
1 材料与方法
1.1 材料与试剂
茶鲜叶:茶树品种梅占(Camellia sinensis var.Meizhan)在我国具有较大栽培面积,且具有产量高、制得成茶品质优良的特点。但目前该品种主要用于加工乌龙茶,很少用于加工其他茶类,且鲜有关于该品种制得成茶香气的报道,因此,本研究采用梅占品种一芽二叶鲜叶进行六大茶类的加工,鲜叶于2018年9月采自重庆市巴南区南润茶厂。
试剂:C8~C23正构烷烃混合物(99%),美国Supelco公司;癸酸乙酯(99%),美国Sigma公司;正己醛(98%)、甲基戊烯酮(95%)、叶醇(98%)、乙基苯(99%)、γ-丁内酯(99%)、苯甲醛(99%)、己酸(98%)、(E,E)-2,4-庚二烯醛(98%)、苯甲醇(98%)、芳樟醇氧化物Ⅰ(97%)、芳樟醇(98%)、苯乙醇(98%)、乙酸苄酯(98%)、水杨酸甲酯(99%)、α-松油醇(98%)、癸醛(98%)、β-环柠檬醛(95%)、橙花醇(98%)、香叶醇(98%)、吲哚(99%)、(Z)-己酸-3-己烯酯(99%)、己酸己酯(98%)、β-石竹烯(90%)、丁酸苯乙酯(98%)、香叶基丙酮(98%)、十二醇(99%)、二氢猕猴桃内酯(98%)、(E)-橙花叔醇(95%),日本TCI株式会社;NaCl(分析级),成都科隆化学试剂公司。
1.2 仪器与设备
QP2010Plus气相色谱质谱联用仪,日本岛津公司;溶剂辅助风味蒸发(solvent assisted flavor evaporation,SAFE)装置,日本桐山制作所;超纯水发生器,美国Millipore公司;SHZ-D(Ⅲ)型循环水真空泵,上海邦西仪器科技有限公司;氮吹仪,天津恒奥科技发展有限公司;FB224电子分析天平,上海舜宇恒平科学仪器有限公司;HWS-26电热恒温水浴锅,上海齐欣科学仪器有限公司。
1.3 方法
1.3.1 样品制备
按照图1的工艺流程进行样品制备。
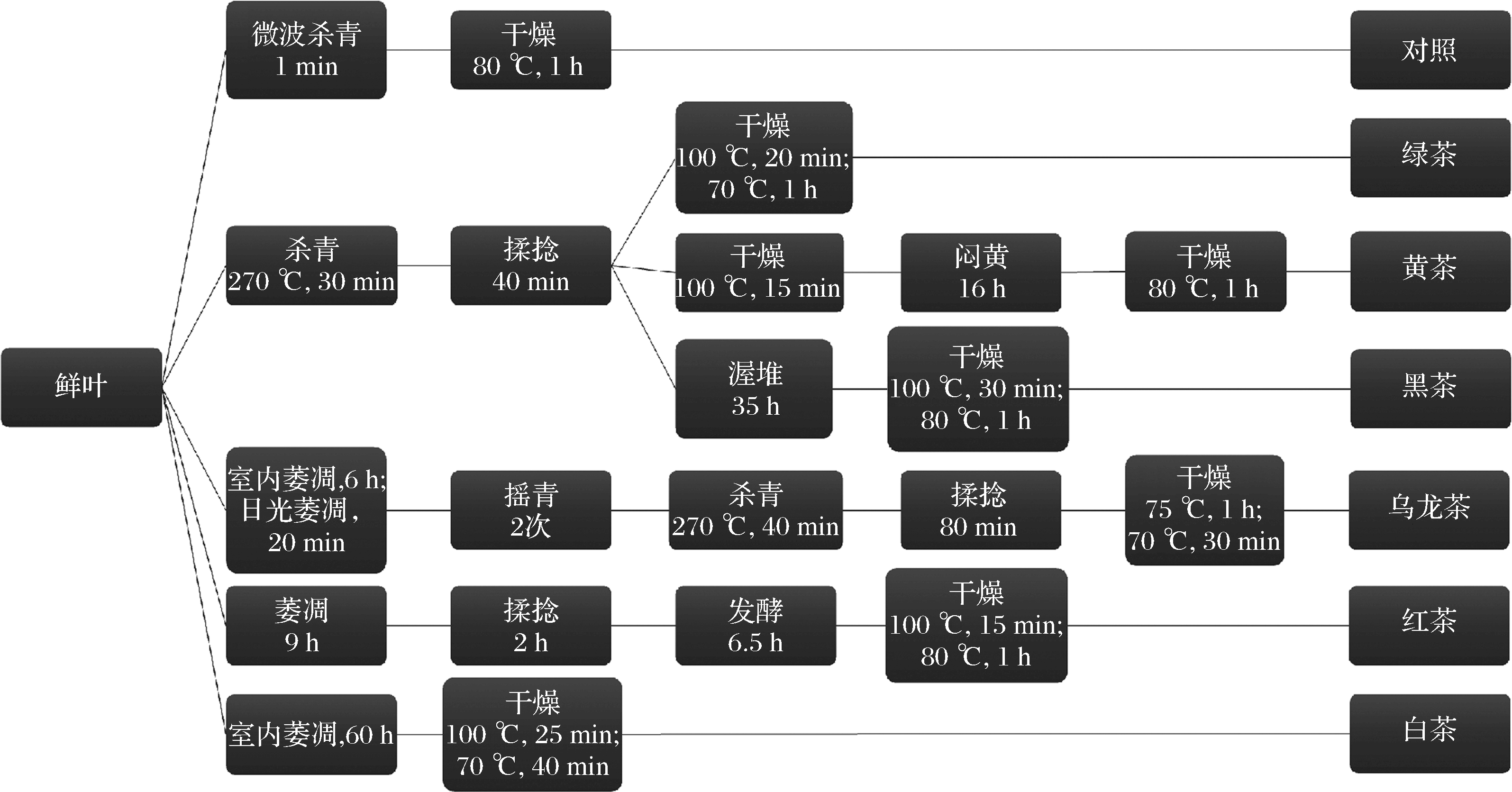
图1 对照及六大茶类样品制备流程图
Fig.1 Flow chart illustrating the different stages in the manufacture of six teas and control sample
1.3.2 SAFE提取茶样挥发性成分
精确称取9.000 g粉碎后的茶样,置于100 mL具塞锥形瓶,分3次加入二氯甲烷进行萃取:第1次加入40 mL萃取3 h,第2次加入30 mL萃取13 h,第3次加入30 mL萃取1 h,合并3次的提取液,过滤。将滤液转移至SAFE装置进行除杂,具体操作参照文献[10]。萃取液经旋转蒸发仪蒸发浓缩至2 mL左右,再用氮吹仪继续浓缩至0.4 mL,封口后置于-40 ℃冰箱备用。
1.3.3 GC-MS分析
GC条件:色谱柱为DB-5MS(30 m×0.25 mm×0.25 μm)石英毛细管柱;进样口温度为250 ℃;柱箱升温程序:初始温度40 ℃,以5 ℃/min升至130 ℃,然后以10 ℃/min升至150 ℃,再以3 ℃/min升至180 ℃,保持1 min,最后以10 ℃/min升至260 ℃,保持3 min;载气为氦气(纯度>99.999%);流速1.0 mL/min;进样量1.0 μL;进样模式不分流,溶剂延迟4 min。
MS条件:电子离子源;能量70 eV;离子源温度250 ℃;接口温度250 ℃;质量扫描范围:40~400 m/z。
1.3.4 定性定量分析
定性方法:运用NIST8.LIB和NIST8 s.LIB标准谱库对GC-MS质谱数据进行检索,保留相似度大于80的化合物,参考LIAO等[11]的方法,利用正构烷烃(C8~C23)测量计算保留指数(retention index,RI),结合文献报道及标准品比对,对挥发性化合物进行定性。
定量方法:外标法定量,取一系列已知浓度梯度的香气标准品,在相同的条件下检测,取得标准曲线方程和回归系数R2如表1所示。表中列出化合物的含量计算均用其对应标准曲线,未列出化合物含量采用癸酸乙酯的标准曲线进行计算。
表1 挥发性化合物标准曲线
Table 1 Standard curves of volatile compounds detected in tea samples

序号保留指数标曲R2化合物线性范围/ng1<800y=328 898x-264 2870.999 2 正己醛1~5002830y=859 375x+323 3550.996 1甲基戊烯酮1~1003849y=2×106x-374 1490.997 8乙基苯1~1004869y=658 915x-472 7320.995 8叶醇1~1005900y=432 162x+694 1490.996 4γ-丁内酯5~1006964y=502 934x-1 414 8330.997 7苯甲醛5~50071 014y=229 166x-184 2560.991 5(E,E)-2,4-庚二烯醛1~10081 033y=231 531x-139 9430.993 2 苯甲醇1~10091 071y=59 747x-1 114 8310.997 0芳樟醇氧化物Ⅰ1~100101 089y=59 7474x-1 114 8310.997 0芳樟醇氧化物Ⅱ1~100111 105y=576 840x-134 8040.993 8 芳樟醇1~500121 113y=253 625x-255 8080.994 3苯乙醇5~500131 162y=626 261x-298 3820.991 4乙酸苄酯1~100141 170y=956 836x-135 1120.997 1芳樟醇氧化物Ⅲ1~100151 175y=956 836x-135 1120.997 1芳樟醇氧化物Ⅳ1~100161 188y=698 188x-221 9780.993 7(Z)-3-己烯基丁酯1~100171 190y=310 123x + 152 1660.990 2水杨酸甲酯5~500181 195y=768 730x-180 8890.991 1α-松油醇1~100191 209y=937 068x+387 5380.990 3癸醛1~100201 221y=709 435x-183 7640.990 1β-环柠檬醛1~100211 229y=383 971x-254 3740.995 7橙花醇1~100221 245y=290 746x-468 810 0.999 8香叶醇1~1 000231 302y=412 106x+2 146 3000.999 2 吲哚5~100241 387y=743 913x-283 5730.997 9己酸叶醇酯1~100251 392y=600 099x+264 1190.995 1己酸己酯1~100261 398y=1 040 008x-233 4280.996 9癸酸乙酯1~1 000271 409y=106x-575 0270.999 2β-石竹烯1~100281 425y=106x+3 000 0000.998 7丁酸苯乙酯1~100291 450y=285 483x-24 3050.997 2香叶基丙酮1~100301 459y=106x-781 4340.999 3十二醇5~100311 513y=1 143 648x-114 8390.992 4 二氢猕猴桃内酯1~100321 534y=320 998x-140 3050.999 0(E)-橙花叔醇1~100
1.3.5 OAV及ACI的计算
OAV为化合物浓度与文献报道的水中香气阈值的比值。ACI根据公式(1)计算:
(1)
式中:ACI,香气特征影响值,%;Ci,香气化合物i的浓度,μg/g;Ti,香气化合物i的阈值,mg/kg;Oi,香气化合物i的香气活度值。
1.3.6 数据分析
所有实验均重复3次,数据采用SPSS 18.0统计软件进行单因素方差分析,P<0.05 认为存在显著性差异。
2 结果与分析
2.1 六大茶类挥发性化合物的GC-MS分析
由表2和图2可知,对照样品中检测到挥发性化合物51种,绿茶中53种,白茶中64种,黄茶中69种,乌龙茶中74种,红茶中64种,黑茶中58种,所有样品共计检测到132种挥发性化合物,其中醇类38种、酮类15种、醛类14种、酯类31种、酸类5种、碳氢类24种和其他类5种。随着鲜叶加工成不同种类的成茶,挥发性化合物的种类和含量都有着不同程度的增加。白茶的挥发性化合物总量是最高的,其余依次是红茶、黄茶、乌龙茶、绿茶、黑茶和对照。
表2 对照和六大茶类样品中检出挥发性化合物的含量 单位:μg/g
Table 2 The content of volatile compounds detected in the control samples and six categories of teas

序中文名保留时间/保留指数对照绿茶白茶黄茶乌龙茶红茶黑茶号min计算文献1环戊酮4.273789.87671.16±0.12------22,3-丁二醇4.292790.6782--0.89±0.12b0.32±0.06a-0.27±0.01a-3正己醛4.408795.4802--4.09±0.13----4甲基戊烯酮4.415795.7797---0.71±0.02---52-己醇4.657805.88004.27±0.51e3.73±0.52de2.52±0.09c6.16±0.44f3.18±0.16d0.69±0.04a1.33±0.13b62-环戊烯酮5.07823.0834.90.62±0.10------7叶醇5.592844.8855--3.06±0.31b-0.33±0.03a--8乙基苯5.708849.6855.50.37±0.139正己醇5.891857.2865--1.42±0.22----10丁酸6.108866.3840--0.11±0.02----11四氢糠醇6.124866.98530.04±0.00a0.11±0.02b-1.06±0.06e0.23±0.02d0.16±0.02c-12庚醛6.721891.89130.10±0.02a0.13±0.02a-0.39±0.07b---13(E)-2-己烯醇6.792894.8879----0.14±0.01--14γ-丁内酯6.921900.1917--0.72±0.07----153-甲基-4-庚酮8.13943.2932-0.07±0.00-----16苯甲醛8.35951.09640.26±0.01a0.50±0.02a3.26±0.33d1.04±0.17b0.46±0.04a1.88±0.19c0.28±0.01a17己酸8.807967.3977----0.98±0.07a2.75±0.27b-182-甲基-3-辛酮9.001974.29850.04±0.00------19甲基庚烯酮9.01973.8986-0.07±0.00a0.20±0.01c0.31±0.05d0.19±0.01c0.19±0.04c0.12±0.00b20正癸烯9.198980.5988.80.07±0.01a0.25±0.04b0.36±0.07c0.64±0.06d0.33±0.02c-0.09±0.01a21(E,E)-2,4-庚二烯醛9.8091 002.81 008----0.42±0.02--222-乙基己醇10.2691 017.51 0291.02±0.13cd1.37±0.25d-3.43±0.65e1.12±0.03cd0.72±0.22bc0.48±0.08ab23苯甲醇10.4351 023.81 0210.86±0.09a2.59±0.26ab60.63±6.06d7.01±0.70b5.27±0.47ab48.87±4.89c1.65±0.16ab24N-甲基吡咯烷酮10.6331 030.41 034----0.03±0.01b0.02±0.01a-25苯乙醛10.7251 032.81 0410.02±0.00a0.05±0.01b0.15±0.03c0.06±0.00b0.13±0.01c0.14±0.03c-26罗勒烯10.8121 035.81 0370.40±0.05c0.59±0.01d0.06±0.00a0.65±0.12d0.83±0.03e0.14±0.02b0.04±0.00a27γ-己内酯10.9331 040.41 036--0.21±0.04----28呋喃酮11.0971 045.91 053---0.22±0.00---292-乙酰基吡咯11.2661 051.61 059---0.20±0.04---30苯乙酮11.3611 054.71 0620.02±0.00a0.04±0.00c0.04±0.00bc0.20±0.02d0.04±0.00bc0.03±0.00ab0.03±0.00ab31芳樟醇氧化物Ⅰ11.561 061.41 0670.45±0.02a3.83±0.38c14.21±1.40e6.04±0.47d2.51±0.06b5.36±0.54d0.45±0.05a32双戊烯11.7721 068.51 028-0.09±0.01a3.38±0.31b---0.04±0.0033芳樟醇氧化物Ⅱ12.031 076.91 0860.25±0.01a1.22±0.12b7.12±0.71e2.29±0.25c1.14±0.02b3.28±0.33d0.20±0.03a34芳樟醇12.4051 089.61 1011.49±0.15a5.15±0.52b19.61±1.96d8.60±0.83c4.11±0.01b4.96±0.50b0.08±0.01a35二氢芳樟醇12.51 092.81 1061.49±0.26c1.42±0.22bc1.47±0.11c6.11±0.34e1.08±0.06ab4.15±0.33d0.98±0.06a36苯乙醇12.7671 101.81 112--26.57±0.21c36.85±3.68d13.08±0.87b64.13±6.41e2.39±0.12a372-乙基-5-(1-甲基乙烯基)-1,3-环己烯13.2951 119.71 1120.09±0.01------38(3E,5E)-2,6-二甲基-1,3,5,7-辛四烯13.3011 119.91 130-0.08±0.01a-0.08±0.01a---39甲酸辛酯13.351 121.61 110-0.07±0.01a-0.20±0.02b---40L-薄荷醇13.4241 124.11 172----0.07±0.01--412,3-二氢-3,5二羟基-6-甲基-4(H)-吡喃-4-酮13.6151 130.61 130---1.46±0.26---42馬鞭烯醇13.961 142.31 145-0.04±0.01a-0.13±0.00b---43(Z)-6-壬烯-1-醇13.9841 143.11 171--0.04±0.01----44乙酸苄酯14.2331 151.51 172--0.03±0.00----45(E,Z)-2,6-壬二烯醇14.3071 154.01 160--0.02±0.00----46辛酸14.3991 157.11 152----0.02±0.00--47芳樟醇氧化物Ⅲ14.5311 160.81 1630.57±0.04a3.04±0.30c7.34±0.70e4.83±0.48d2.13±0.04b7.08±0.71e0.53±0.02a48芳樟醇氧化物Ⅳ14.6531 165.11 1630.21±0.03a1.16±0.12b5.26±0.53e2.81±0.28c0.09±0.01b4.43±0.40d0.22±0.01a49(E)-2-壬醛14.8061 170.91 168-0.11±0.00b-0.38±0.01c--0.05±0.00a50萘14.9131 174.61 179---0.39±0.01d0.18±0.00b0.26±0.02c0.06±0.01a51(E)-2,6-二甲基-3,7-辛二烯-2,6-二醇15.0251 178.41 176--3.66±0.40----
续表2
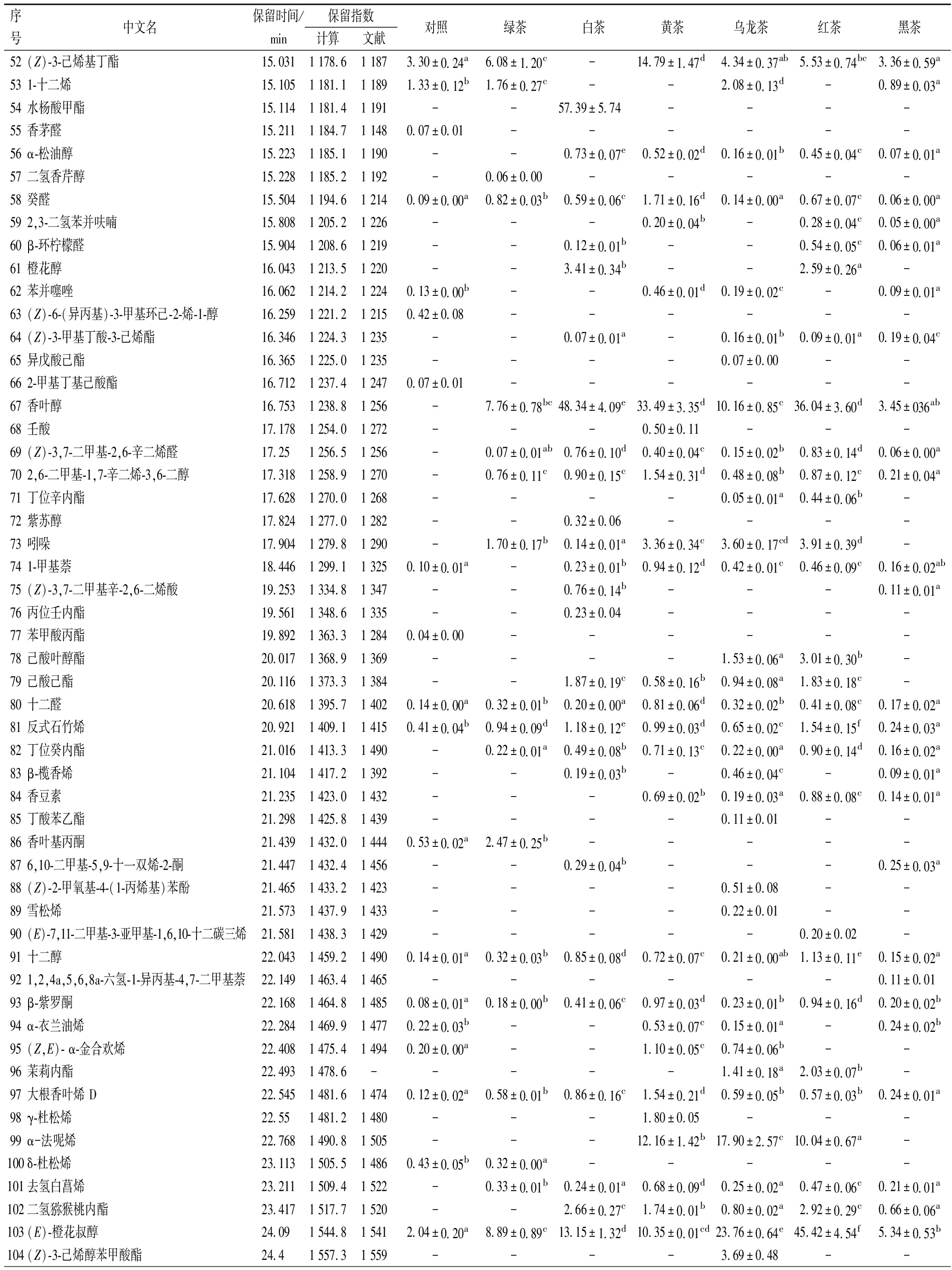
序中文名保留时间/保留指数对照绿茶白茶黄茶乌龙茶红茶黑茶号min计算文献52(Z)-3-己烯基丁酯15.0311 178.61 1873.30±0.24a6.08±1.20c-14.79±1.47d4.34±0.37ab5.53±0.74bc3.36±0.59a531-十二烯15.1051 181.11 1891.33±0.12b1.76±0.27c--2.08±0.13d-0.89±0.03a54水杨酸甲酯15.1141 181.41 191--57.39±5.74----55香茅醛15.2111 184.71 1480.07±0.01------56α-松油醇15.2231 185.11 190--0.73±0.07e0.52±0.02d0.16±0.01b0.45±0.04c0.07±0.01a57二氢香芹醇15.2281 185.21 192-0.06±0.00-----58癸醛15.5041 194.61 2140.09±0.00a0.82±0.03b0.59±0.06c1.71±0.16d0.14±0.00a0.67±0.07c0.06±0.00a592,3-二氢苯并呋喃15.8081 205.21 226---0.20±0.04b-0.28±0.04c0.05±0.00a60β-环柠檬醛15.9041 208.61 219--0.12±0.01b--0.54±0.05c0.06±0.01a61橙花醇16.0431 213.51 220--3.41±0.34b--2.59±0.26a-62苯并噻唑16.0621 214.21 2240.13±0.00b--0.46±0.01d0.19±0.02c-0.09±0.01a63(Z)-6-(异丙基)-3-甲基环己-2-烯-1-醇16.2591 221.21 2150.42±0.08------64(Z)-3-甲基丁酸-3-己烯酯16.3461 224.31 235--0.07±0.01a-0.16±0.01b0.09±0.01a0.19±0.04c65异戊酸己酯16.3651 225.01 235----0.07±0.00--662-甲基丁基己酸酯16.7121 237.41 2470.07±0.01------67香叶醇16.7531 238.81 256-7.76±0.78bc48.34±4.09e33.49±3.35d10.16±0.85c36.04±3.60d3.45±036ab68壬酸17.1781 254.01 272---0.50±0.11---69(Z)-3,7-二甲基-2,6-辛二烯醛17.251 256.51 256-0.07±0.01ab0.76±0.10d0.40±0.04c0.15±0.02b0.83±0.14d0.06±0.00a702,6-二甲基-1,7-辛二烯-3,6-二醇17.3181 258.91 270-0.76±0.11c0.90±0.15c1.54±0.31d0.48±0.08b0.87±0.12c0.21±0.04a71丁位辛内酯17.6281 270.01 268----0.05±0.01a0.44±0.06b-72紫苏醇17.8241 277.01 282--0.32±0.06----73吲哚17.9041 279.81 290-1.70±0.17b0.14±0.01a3.36±0.34c3.60±0.17cd3.91±0.39d-741-甲基萘18.4461 299.11 3250.10±0.01a-0.23±0.01b0.94±0.12d0.42±0.01c0.46±0.09c0.16±0.02ab75(Z)-3,7-二甲基辛-2,6-二烯酸19.2531 334.81 347--0.76±0.14b---0.11±0.01a76丙位壬内酯19.5611 348.61 335--0.23±0.04----77苯甲酸丙酯19.8921 363.31 2840.04±0.00------78己酸叶醇酯20.0171 368.91 369----1.53±0.06a3.01±0.30b-79己酸己酯20.1161 373.31 384--1.87±0.19c0.58±0.16b0.94±0.08a1.83±0.18c-80十二醛20.6181 395.71 4020.14±0.00a0.32±0.01b0.20±0.00a0.81±0.06d0.32±0.02b0.41±0.08c0.17±0.02a81反式石竹烯20.9211 409.11 4150.41±0.04b0.94±0.09d1.18±0.12e0.99±0.03d0.65±0.02c1.54±0.15f0.24±0.03a82丁位癸内酯21.0161 413.31 490-0.22±0.01a0.49±0.08b0.71±0.13c0.22±0.00a0.90±0.14d0.16±0.02a83β-榄香烯21.1041 417.21 392--0.19±0.03b-0.46±0.04c-0.09±0.01a84香豆素21.2351 423.01 432---0.69±0.02b0.19±0.03a0.88±0.08c0.14±0.01a85丁酸苯乙酯21.2981 425.81 439----0.11±0.01--86香叶基丙酮21.4391 432.01 4440.53±0.02a2.47±0.25b-----876,10-二甲基-5,9-十一双烯-2-酮21.4471 432.41 456--0.29±0.04b---0.25±0.03a88(Z)-2-甲氧基-4-(1-丙烯基)苯酚21.4651 433.21 423----0.51±0.08--89雪松烯21.5731 437.91 433----0.22±0.01--90(E)-7,11-二甲基-3-亚甲基-1,6,10-十二碳三烯21.5811 438.31 429-----0.20±0.02-91十二醇22.0431 459.21 4900.14±0.01a0.32±0.03b0.85±0.08d0.72±0.07c0.21±0.00ab1.13±0.11e0.15±0.02a921,2,4a,5,6,8a-六氢-1-异丙基-4,7-二甲基萘22.1491 463.41 465------0.11±0.0193β-紫罗酮22.1681 464.81 4850.08±0.01a0.18±0.00b0.41±0.06c0.97±0.03d0.23±0.01b0.94±0.16d0.20±0.02b94α-衣兰油烯22.2841 469.91 4770.22±0.03b--0.53±0.07c0.15±0.01a-0.24±0.02b95(Z,E)- α-金合欢烯22.4081 475.41 4940.20±0.00a--1.10±0.05c0.74±0.06b--96茉莉内酯22.4931 478.6-----1.41±0.18a2.03±0.07b-97大根香叶烯 D22.5451 481.61 4740.12±0.02a0.58±0.01b0.86±0.16c1.54±0.21d0.59±0.05b0.57±0.03b0.24±0.01a98γ-杜松烯22.551 481.21 480---1.80±0.05---99α-法呢烯22.7681 490.81 505---12.16±1.42b17.90±2.57c10.04±0.67a-100δ-杜松烯23.1131 505.51 4860.43±0.05b0.32±0.00a-----101去氢白菖烯23.2111 509.41 522-0.33±0.01b0.24±0.01a0.68±0.09d0.25±0.02a0.47±0.06c0.21±0.01a102二氢猕猴桃内酯23.4171 517.71 520--2.66±0.27c1.74±0.01b0.80±0.02a2.92±0.29c0.66±0.06a103(E)-橙花叔醇24.091 544.81 5412.04±0.20a8.89±0.89c13.15±1.32d10.35±0.01cd23.76±0.64e45.42±4.54f5.34±0.53b104(Z)-3-己烯醇苯甲酸酯24.41 557.31 559----3.69±0.48--
续表2
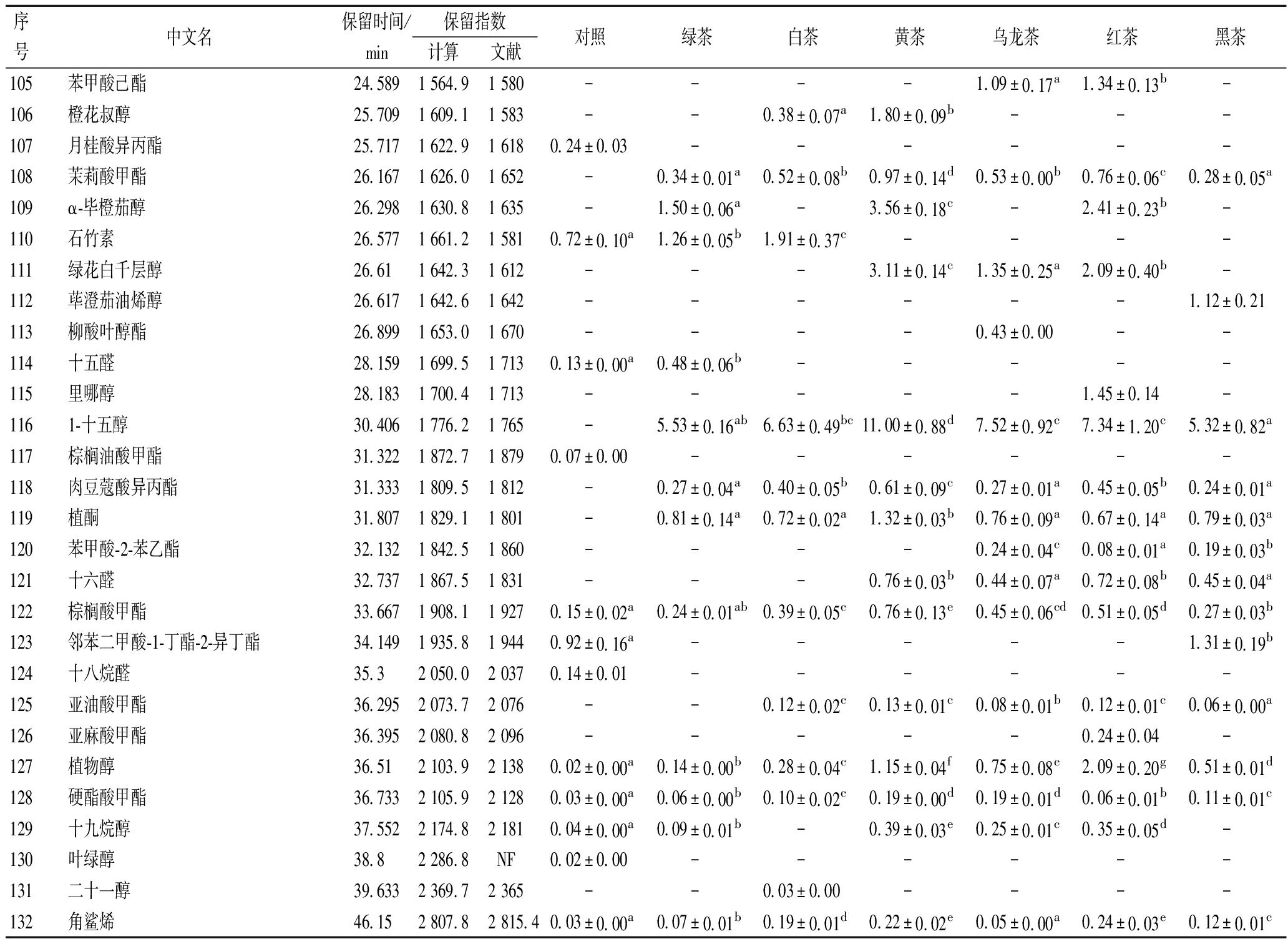
序中文名保留时间/保留指数对照绿茶白茶黄茶乌龙茶红茶黑茶号min计算文献105苯甲酸己酯24.5891 564.91 580----1.09±0.17a1.34±0.13b-106橙花叔醇25.7091 609.11 583--0.38±0.07a1.80±0.09b---107月桂酸异丙酯25.7171 622.91 6180.24±0.03------108茉莉酸甲酯26.1671 626.01 652-0.34±0.01a0.52±0.08b0.97±0.14d0.53±0.00b0.76±0.06c0.28±0.05a109α-毕橙茄醇26.2981 630.81 635-1.50±0.06a-3.56±0.18c-2.41±0.23b-110石竹素26.5771 661.21 5810.72±0.10a1.26±0.05b1.91±0.37c----111绿花白千层醇26.611 642.31 612---3.11±0.14c1.35±0.25a2.09±0.40b-112荜澄茄油烯醇26.6171 642.61 642------1.12±0.21113柳酸叶醇酯26.8991 653.01 670----0.43±0.00--114十五醛28.1591 699.51 7130.13±0.00a0.48±0.06b-----115里哪醇28.1831 700.41 713-----1.45±0.14-1161-十五醇30.4061 776.21 765-5.53±0.16ab6.63±0.49bc11.00±0.88d7.52±0.92c7.34±1.20c5.32±0.82a117棕榈油酸甲酯31.3221 872.71 8790.07±0.00------118肉豆蔻酸异丙酯31.3331 809.51 812-0.27±0.04a0.40±0.05b0.61±0.09c0.27±0.01a0.45±0.05b0.24±0.01a119植酮31.8071 829.11 801-0.81±0.14a0.72±0.02a1.32±0.03b0.76±0.09a0.67±0.14a0.79±0.03a120苯甲酸-2-苯乙酯32.1321 842.51 860----0.24±0.04c0.08±0.01a0.19±0.03b121十六醛32.7371 867.51 831---0.76±0.03b0.44±0.07a0.72±0.08b0.45±0.04a122棕榈酸甲酯33.6671 908.11 9270.15±0.02a0.24±0.01ab0.39±0.05c0.76±0.13e0.45±0.06cd0.51±0.05d0.27±0.03b123邻苯二甲酸-1-丁酯-2-异丁酯34.1491 935.81 9440.92±0.16a-----1.31±0.19b124十八烷醛35.32 050.02 0370.14±0.01------125亚油酸甲酯36.2952 073.72 076--0.12±0.02c0.13±0.01c0.08±0.01b0.12±0.01c0.06±0.00a126亚麻酸甲酯36.3952 080.82 096-----0.24±0.04-127植物醇36.512 103.92 1380.02±0.00a0.14±0.00b0.28±0.04c1.15±0.04f0.75±0.08e2.09±0.20g0.51±0.01d128硬酯酸甲酯36.7332 105.92 1280.03±0.00a0.06±0.00b0.10±0.02c0.19±0.00d0.19±0.01d0.06±0.01b0.11±0.01c129十九烷醇37.5522 174.82 1810.04±0.00a0.09±0.01b-0.39±0.03e0.25±0.01c0.35±0.05d-130叶绿醇38.82 286.8NF0.02±0.00------131二十一醇39.6332 369.72 365--0.03±0.00----132角鲨烯46.152 807.82 815.40.03±0.00a0.07±0.01b0.19±0.01d0.22±0.02e0.05±0.00a0.24±0.03e0.12±0.01c
注:“-”表示未检出;NF表示未查阅到相关信息;同一行不同字母表示具有显著性差异(P<0.05)
醇类是所有茶类中含量最高的一类化合物,尤以红茶(83.38%)和白茶(72.96%)中醇类化合物的比例最高,其中苯甲醇的含量在茶叶加工过程中显著增加,其在绿茶、白茶、黄茶、乌龙茶、红茶和黑茶中的含量分别为对照(0.86 μg/g)的3.01、70.46、8.14、6.13、56.79和1.91倍,二氢香芹醇为绿茶的特有成分,里哪醇为红茶的特有成分,荜澄茄油烯醇为黑茶的特有成分。苯乙醇和α-松油醇存在于发酵茶中,在对照和绿茶中均没有检测到。14种醛类化合物中,香茅醛仅在对照中检测到,(E,E)-2,4-庚二烯醛只在乌龙茶中检测到。C6和C9醇类和醛类是茶叶“清新”气味的主要来源[3],这类化合物如正己醛、正己醇、(Z)-6-壬烯-1-醇、(E,Z)-2,6-壬二烯醇等仅在白茶中检测到。β-紫罗酮存在于所有样品中,与对照相比,其在六类茶中的积累量均明显增加,且存在显著性差异,黄茶中的含量最高(0.97 μg/g),分别为绿茶、白茶、乌龙茶、红茶和黑茶的5.39、2.37、4.22、1.03和4.85倍,具有清新花香属性的香叶基丙酮只在绿茶中检测到。酯类化合物的种类仅次于醇类,且在白茶(20.52%)中的比例最高,其中水杨酸甲酯(57.39 μg/g)是白茶中含量最高的化合物,且为白茶的特有成分。对照和绿茶中均没有检测到酸类化合物,其余茶类中酸类化合物的含量也很低(0.11~2.75 μg/g)。碳氢类化合物中含量最高的物质为α-法呢烯,仅在黄茶(12.16 μg/g)、乌龙茶(17.9 μg/g)和红茶(10.04 μg/g)中检测到。其他类化合物中,吲哚存在于黑茶外的5种茶中,2-乙酰基吡咯仅在黄茶中检测到。
杀青是绿茶加工过程中的关键工序,其能促进茶叶中类胡萝卜素香气前体和脂肪酸类香气前体的降解,形成香叶基丙酮、(Z)-茉莉酮、橙花叔醇、庚醛、癸醛等芳香物质,促进绿茶香气的形成[12-14]。白茶的关键加工工序是萎凋,萎凋过程伴随着失水和缓慢氧化,糖苷类水解产生的苯乙醇、香叶醇、苯甲醇、芳樟醇及其氧化物、正己醛、2-己醇、水杨酸甲酯等主要的呈香物质显著增加[8,15]。β-紫罗酮是对茶叶香气起关键作用的一种类胡萝卜素衍生物,不仅可以来源于发酵阶段的酶促氧化,还可以由干燥阶段的热作用催化产生[13,16]。黄茶经历了杀青、长时间闷黄和2次干燥过程,所有种类的挥发性化合物都有较高水平的积累量,其中庚醛、β-紫罗酮的含量远高于其他茶类,而且还积累了一些含氮类挥发性化合物,如吲哚、2-乙酰基吡咯和苯并噻唑,均是美拉德反应的产物[14]。乌龙茶的萎凋和摇青工艺是其香气品质形成的关键,摇青过程持续的机械损伤增强了相关基因的表达,导致茉莉内酯的大量积累[17]。α-法呢烯和(E)-橙花叔醇都是以类胡萝卜素为前体的香气化合物,其含量的大量增加可能是由于日光萎凋过程中的光氧化促进了类胡萝卜素的水解[18]。红茶的加工过程涉及到多种挥发性化合物的形成途径[19],在揉捻和发酵阶段,经机械破碎的叶片组织释放水解酶类到细胞壁或胞腔中,挥发性化合物的形成通道被激活,产生关键挥发性成分,如:单萜醇(芳樟醇、氧化芳樟醇和香叶醇)、芳香醇(苯甲醇和苯乙醇)、β-紫罗酮和β-环柠檬醛等,促进红茶香气的形成[3,13]。与其他茶类相比,红茶中的酸类化合物含量较高,这是由于醇类化合物的羟基不稳定,易氧化成醛,进一步氧化成酸,这一现象在红茶的发酵阶段尤为普遍[20]。黑茶中的挥发性化合物含量是六大茶类中最低的,与对照相比,仅有小部分化合物含量增加,如香叶醇、β-环柠檬醛、十二醛和丁位癸内酯,其余化合物含量均下降或没有显著性变化,原因是在温度、湿度、水分和氧气的共同作用下,较长时间的渥堆过程使得一部分挥发性化合物发生了降解和氧化,导致其含量发生了显著的下降[21]。
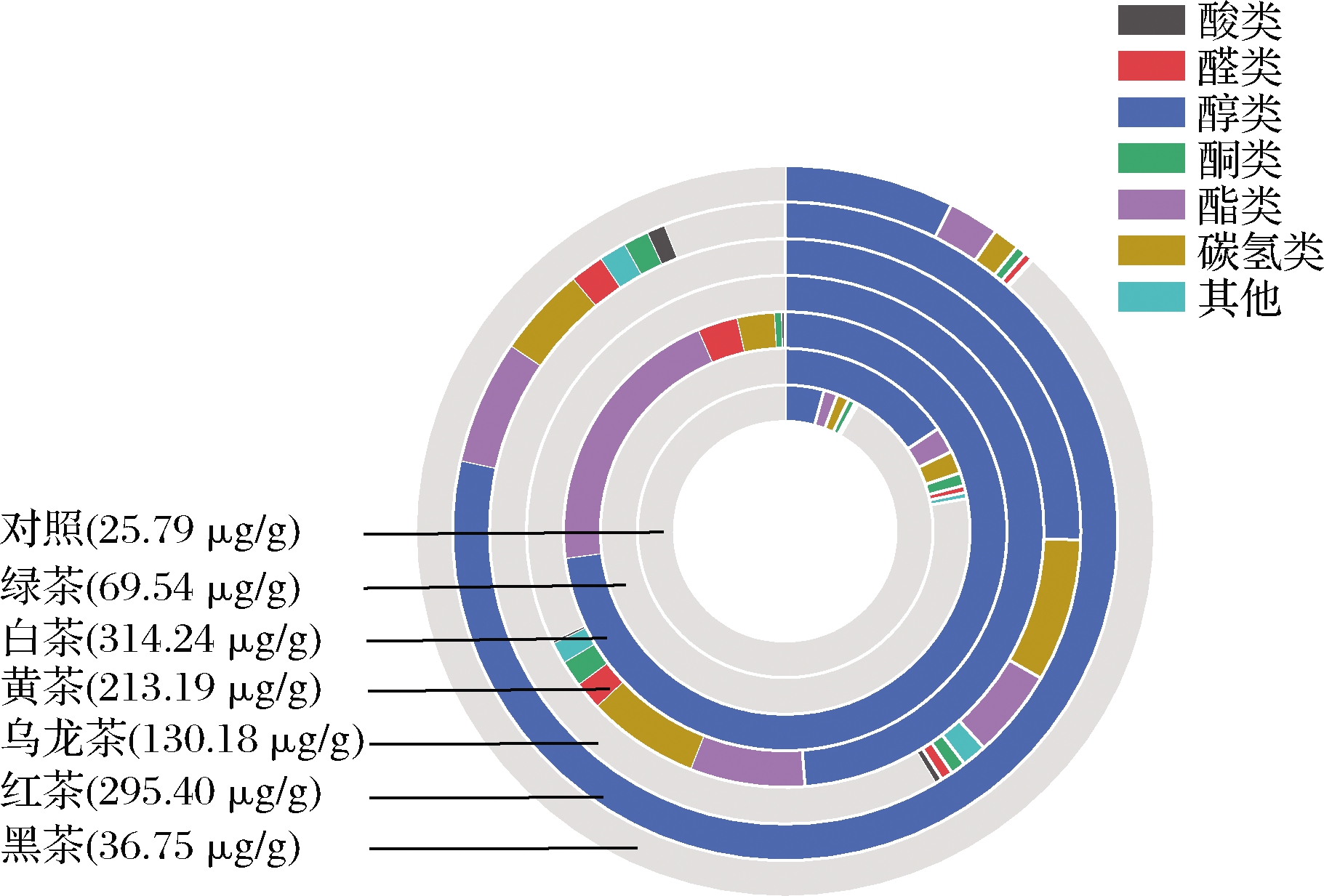
图2 对照和六大茶类中各类别挥发性化合物的含量
Fig.2 The contents of different chemical classes of volatile compounds in the control sample and six categories of teas
2.2 六大茶类32种共有挥发性化合物的聚类热图分析
与对照相比,不同的加工方式不仅导致各茶类特有成分的生成,而且共有成分的含量也发生了很大的变化。六大茶类共有成分32种,文献报道为81种[14],二者相同组分有17种,造成这一差异的原因可能有:(1)茶树品种不同:其鲜叶内香气前体的种类、含量及相关酶活性的差异导致成茶香气化合物的差异[22-23];(2)工艺参数的差异:虽都采用六大茶类的典型加工工艺进行茶叶的加工,但同类型加工工艺中如时间、温度等参数不同仍会对成茶挥发性化合物造成很大的影响[24];(3)提取方法的差异:不同的提取方法对挥发性化合物的提取率不同,且在提取过程中还可能存在挥发性化合物的损耗,导致最终结果的不同[25]。
对32种共有挥发性化合物进行聚类热图分析,如图3所示,各茶类挥发性化合物之间的差异显著,且32种共有成分被聚为四类。第一类包括2-己醇和罗勒烯,其在不发酵和部分发酵茶中的含量较高,显著高于在全发酵的红茶和黑茶中的含量。第二类包括苯乙酮、植酮、2,6-二甲基-1,7-辛二烯-3,6-二醇、癸醛、大根香叶烯D、十二醛、去氢白菖烯、甲基庚烯酮、1-十五醇、茉莉酸甲酯、肉豆蔻酸异丙酯、棕榈酸甲酯和硬脂酸甲酯。这些化合物在对照中的含量很低或没有,说明主要是在加工过程中产生的,具有清香属性的甲基庚烯酮在白茶和黄茶中的含量较高,具有花果香气的癸醛和十二醛在黄茶和红茶中的含量较高。茉莉酸甲酯作为半发酵茶中一种重要的脂肪酸衍生物[26],具有茉莉样香气,在乌龙茶中有较高的积累量。第三类化合物包括苯甲醇、苯甲醛、芳樟醇
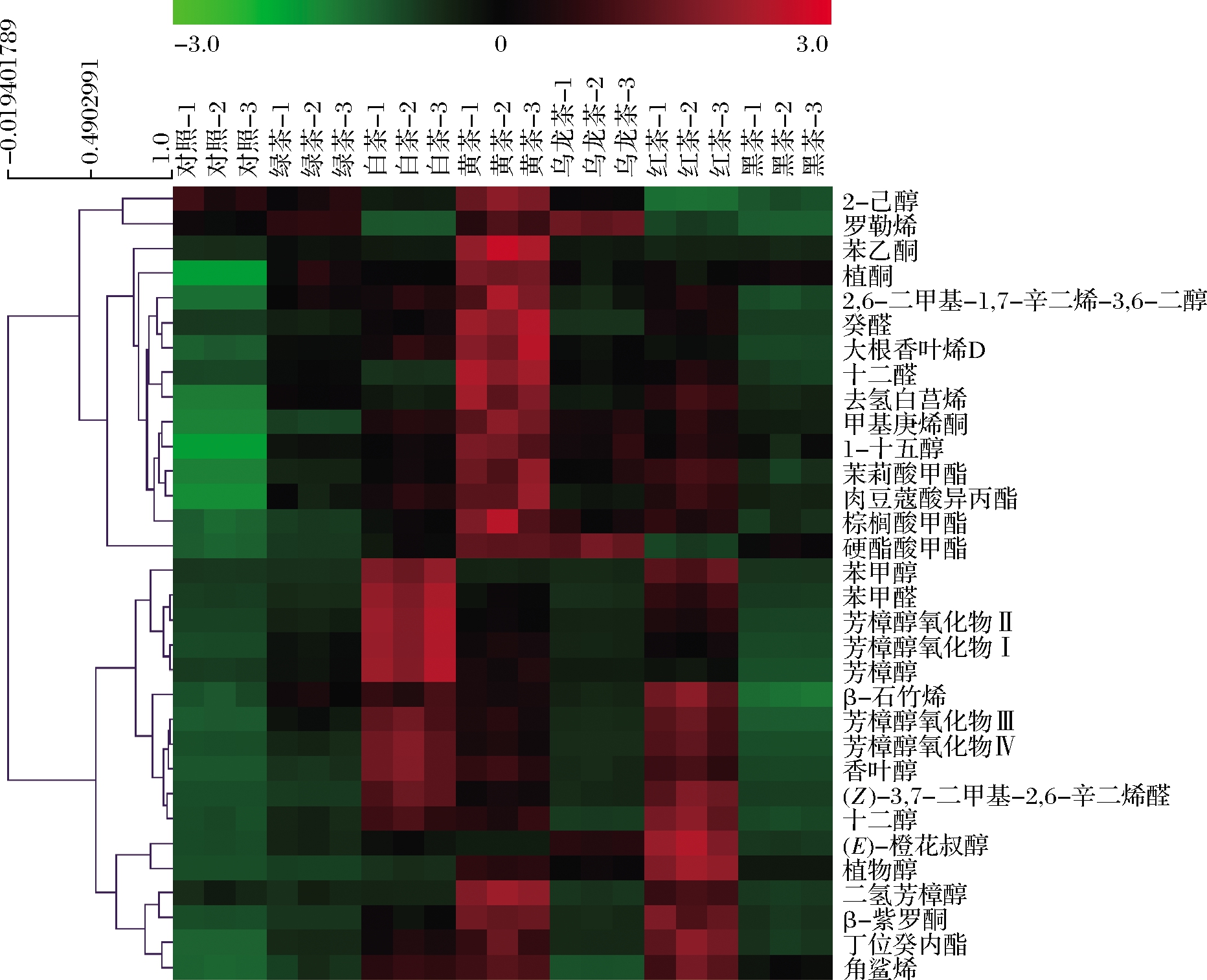
图3 对照和六大茶类样品中32种共有挥发性化合物的 聚类热图分析
Fig.3 Hierarchical clustering analysis of the 32 common volatile compounds in the control sample and six categories of teas
及其氧化物、β-石竹烯、香叶醇、(Z)-3,7-二甲基-2,6-辛二烯醛和十二醇,单萜醇和芳香醇主要来源于糖苷类水解,其在红茶和白茶中的含量显著高于其他茶类,如香叶醇在白茶中的含量最高,分别是绿茶、黄茶、乌龙茶、红茶和黑茶的6.29、1.56、4.80、1.35和14.13倍。第4类化合物包括(E)-橙花叔醇、植物醇、二氢芳樟醇、β-紫罗酮、丁位癸内酯和角鲨烯,具有甜花香属性的(E)-橙花叔醇在红茶和乌龙茶中的含量极为丰富,带有花香属性的β-紫罗酮和带有果香属性的丁位癸内酯在红茶和黄茶中的含量显著高于其他茶类。
2.3 六大茶类32种共有挥发性化合物的主成分分析
对六大茶类32种共有成分数据进行主成分分析,前3个主成分累计方差贡献率达89%,可以基本代表所有变量信息。图4-a为对照和6种茶在PC1和PC2上的得分图,从图中可以看出每种茶之间差异明显,分离度和样品间的重复性均较好。绘制32种共有成分在PC1 vs PC2、PC2 vs PC3和PC1 vs PC3上的载荷图(图4-b~图4-d)。从图中可以看出各物质与3个主成分的相关性,较高的载荷量表明其对主成分的影响较大。肉豆蔻酸异丙酯、丁位癸内酯、茉莉酸甲酯、角鲨烯、2,6-二甲基-1,7-辛二烯-3,6-二醇、香叶醇、β-紫罗酮、十二醇、甲基庚烯酮、芳樟醇氧化物Ⅲ在PC1上有较大载荷量,苯甲醇、罗勒烯、苯乙酮、2-己醇、苯甲醛、十二醛、硬酯酸甲酯、芳樟醇氧化物Ⅱ和(Z)-3,7-二甲基-2,6-辛二烯醛在PC2上有较大载荷量,植物醇、(E)-橙花叔醇、芳樟醇、芳樟醇氧化物Ⅰ、2-己醇在PC3上有较大载荷量,表示各个样品在PC1、PC2、PC3上得分的差异主要由以上物质贡献。

a-样品在PC1和PC2上的得分图;b-32种共有成分在PC1和PC2上的载荷图;c-32种共有成分在PC2和PC3上的载荷图; d-32种共有成分在PC1和PC3上的载荷图
图4 对照和六大茶类中32种共有挥发性化合物的主成分分析图
Fig.4 PCA score and loading plot derived from 32 common volatile compounds of the control sample and six categories of teas
注:图中数字代表列于表2中的挥发性化合物编号
2.4 六大茶类32种共有挥发性化合物的正交偏最小二乘判别分析
利用正交偏最小二乘判别分析对六大茶类的32种共有挥发性化合物进行识别分析,计算出OPLS-DA变量重要性因子(variable important for the projection,VIP), 共筛选出10种化合物(VIP>1),分别是罗勒烯(VIP:1.422 62)、硬脂酸甲酯(VIP:1.342 33)、(E)-橙花叔醇(VIP:1.253 54)、β-石竹烯(VIP:1.134 8)、植物醇(VIP:1.095 7)、甲基庚烯酮(VIP:1.080 5)、角鲨烯(VIP:1.067 42)、2-己醇(VIP:1.062 21)、植酮(VIP:1.056 88)、芳樟醇(VIP:1.050 38)和芳樟醇氧化物Ⅰ(VIP:1.000 71),对茶叶的分类鉴别具有重要贡献。
2.5 六大茶类活性香气化合物的OAV和ACI分析
OAV值是化合物含量与其阈值之比,通常认为OAV>1的化合物对香气有较大贡献。ACI的提出用来表征香气特征影响指数[27],ACI值越大,说明该化合物对样品香气的贡献程度越高。查阅文献[11,28-31]计算出各样品中化合物的 OAV和ACI值,如表3所示,OAV>1 的化合物共计32种。其中芳樟醇及其氧化物在所有样品中的OAV值和ACI值都很高,说明其对各样品香气构成皆有着重要贡献。此外,呈现花香的十二醛、β-石竹烯、β-紫罗酮等化合物虽然在各个样品中的含量不高,但由于其阈值较低,所以其OAV值均大于1,也具有较高的香气贡献度。除对照和绿茶外,苯乙醇在其他5种茶中的含量均较高,但由于其较高的阈值,故仅在红茶中苯乙醇的OAV>1。这充分说明了挥发性化合物含量的高低并不等同于其对香气的贡献程度[14]。
表3 样品中关键化合物的OAV和ACI值
Table 3 OAV and ACI of the key compounds responsible for the samples
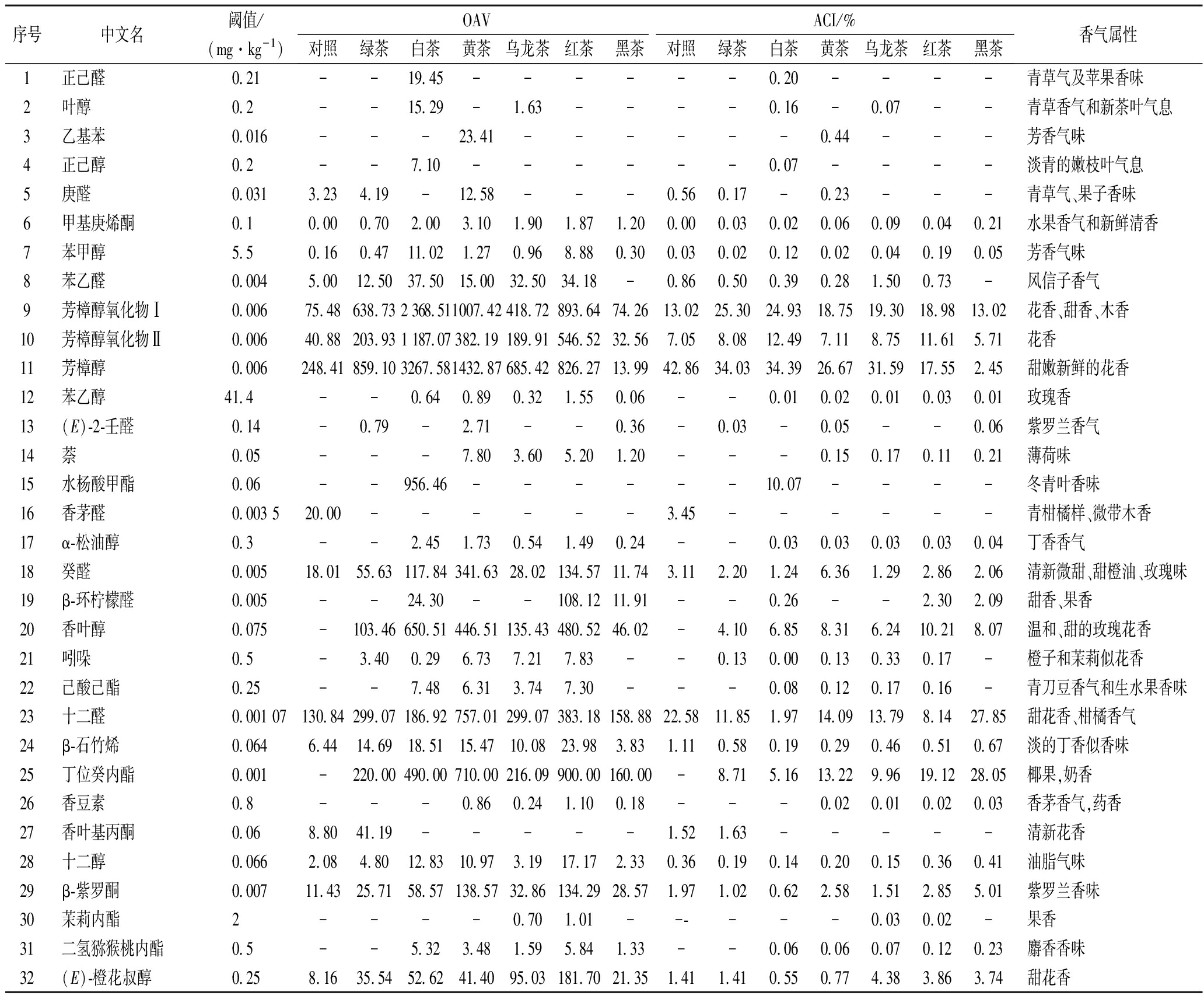
序号中文名阈值/(mg·kg-1)OAVACI/%对照绿茶白茶黄茶乌龙茶红茶黑茶对照绿茶白茶黄茶乌龙茶红茶黑茶香气属性1正己醛0.21--19.45------0.20----青草气及苹果香味2叶醇0.2--15.29-1.63----0.16-0.07--青草香气和新茶叶气息3乙基苯0.016---23.41------0.44---芳香气味4正己醇0.2--7.10------0.07----淡青的嫩枝叶气息5庚醛0.0313.234.19-12.58---0.560.17-0.23---青草气、果子香味6甲基庚烯酮0.10.000.702.003.101.901.871.200.000.030.020.060.090.040.21水果香气和新鲜清香7苯甲醇5.50.160.4711.021.270.968.880.300.030.020.120.020.040.190.05芳香气味8苯乙醛0.0045.0012.5037.5015.0032.5034.18-0.860.500.390.281.500.73-风信子香气9芳樟醇氧化物Ⅰ0.00675.48638.732 368.511007.42418.72893.6474.2613.0225.3024.9318.7519.3018.9813.02花香、甜香、木香10芳樟醇氧化物Ⅱ0.00640.88203.931 187.07382.19189.91546.5232.567.058.0812.497.118.7511.615.71花香11芳樟醇0.006248.41859.103267.581432.87685.42826.2713.9942.8634.0334.3926.6731.5917.552.45甜嫩新鲜的花香12苯乙醇41.4--0.640.890.321.550.06--0.010.020.010.030.01玫瑰香13(E)-2-壬醛0.14-0.79-2.71--0.36-0.03-0.05--0.06紫罗兰香气14萘0.05---7.803.605.201.20---0.150.170.110.21薄荷味15水杨酸甲酯0.06--956.46------10.07----冬青叶香味16香茅醛0.003 520.00------3.45------青柑橘样、微带木香17α-松油醇0.3--2.451.730.541.490.24--0.030.030.030.030.04丁香香气18癸醛0.00518.0155.63117.84341.6328.02134.5711.743.112.201.246.361.292.862.06清新微甜、甜橙油、玫瑰味19β-环柠檬醛0.005--24.30--108.1211.91--0.26--2.302.09甜香、果香20香叶醇0.075-103.46650.51446.51135.43480.5246.02-4.106.858.316.2410.218.07温和、甜的玫瑰花香21吲哚0.5-3.400.296.737.217.83--0.130.000.130.330.17-橙子和茉莉似花香22己酸己酯0.25--7.486.313.747.30---0.080.120.170.16-青刀豆香气和生水果香味23十二醛0.001 07130.84299.07186.92757.01299.07383.18158.8822.5811.851.9714.0913.798.1427.85甜花香、柑橘香气24β-石竹烯0.0646.4414.6918.5115.4710.0823.983.831.110.580.190.290.460.510.67淡的丁香似香味25丁位癸内酯0.001-220.00490.00710.00216.09900.00160.00-8.715.1613.229.9619.1228.05椰果,奶香26香豆素0.8---0.860.241.100.18---0.020.010.020.03香茅香气,药香27香叶基丙酮0.068.8041.19-----1.521.63-----清新花香28十二醇0.0662.084.8012.8310.973.1917.172.330.360.190.140.200.150.360.41油脂气味29β-紫罗酮0.00711.4325.7158.57138.5732.86134.2928.571.971.020.622.581.512.855.01紫罗兰香味30茉莉内酯2----0.701.01------0.030.02-果香31二氢猕猴桃内酯0.5--5.323.481.595.841.33--0.060.060.070.120.23麝香香味32(E)-橙花叔醇0.258.1635.5452.6241.4095.03181.7021.351.411.410.550.774.383.863.74甜花香
注:“-”表示未检出
绿茶中带有青味、清花香属性化合物的OAV值较高,如庚醛、癸醛、香叶基丙酮等,说明清花香属性在绿茶中占主要优势。白茶中OAV值较高的化合物为具有清新气味和甜花香的化合物,如正己醛、甲基庚烯酮、水杨酸甲酯、香叶醇等,被认为是新鲜白茶中的主要呈香物质[32-33]。黄茶中带有青香、果香、花香的化合物皆有较高的OAV值,如庚醛、癸醛、十二醛和β-紫罗酮,说明黄茶中各香气属性较均衡。(E)-橙花叔醇、吲哚等具花香属性的化合物在乌龙茶中的OAV值均较高,且ACI值远大于在其他茶类中的,是乌龙茶中普遍存在的特征香气化合物[7]。红茶中具有典型花果香气的苯甲醇、β-环柠檬醛、香叶醇、丁位癸内酯和具有紫罗兰香气的β-紫罗酮的OAV值均较高,多种香气化合物协调作用,塑造红茶的典型风味。黑茶中OAV和ACI值最高的化合物为呈现果香属性的十二醛和丁位癸内酯,芳樟醇及其氧化物的ACI值相较其他茶类有明显降低,癸醛、β-环柠檬醛等化合物在塑造黑茶的香型方面也起到关键作用。各类茶的香气构成中优势化合物存在较大差异,导致各自具有明显不同的香气类型。
3 结论
在本研究中,由GC-MS分析结果可知,同一品种鲜叶加工成的六大茶类,因加工工艺不同,其挥发性化合物含量及组成存在较大差异。各茶类共有成分32种,绿茶特有成分5种,白茶13种,黄茶7种,乌龙茶10种,红茶和黑茶各3种,结合OPLS-DA筛选出的罗勒烯、(E)-橙花叔醇、β-石竹烯等10种VIP>1的共有挥发性化合物,可作为区分各茶类的标志性化合物。
OAV和ACI分析表明,芳樟醇及其氧化物在对照和所有茶类中的OAV和ACI值均很高,说明其可能是该品种的特征属性。绿茶和白茶为不发酵和轻发酵茶,化合物组成较相似,皆带有一定清香属性,但白茶甜香更显;黄茶因经历了较长时间的闷黄过程,香气化合物积累更丰富,带有青香、花香、果香化合物的OAV值均较高;乌龙茶萎凋和摇青阶段导致带有花香属性的化合物大量积累,其在成茶中的OAV和ACI值均较高;红茶发酵过程积累了大量香气化合物,以花香和果香化合物占主要优势;黑茶渥堆过程导致大量带有清新气味化合物的水解,带有果香属性的化合物逐渐凸显,在成茶中具有最高的ACI值,从而表现出明显不同的香气轮廓。
对茶叶整体香气起主要贡献作用的化合物大多属于各类茶的共有成分,即主要香气组分有很大的重合度,差别主要在于各类茶中占主要优势的关键香气化合物比例不同,导致各自的香气贡献度不同,从而造成其香气表型的差异。
[1] 宛晓春. 茶叶生物化学[M].北京:中国农业出版社, 2003.
WAN X C.Tea Biochemistry[M].Beijing:China Agriculture Press, 2003.
[2] SUSANNE B, YANG Z Y, KATSUNO T, et al.Recent studies of the volatile compounds in tea[J].Food Research International, 2013, 53(2):585-599.
[3] ZHENG X Q, LI Q S, XIANG L P, et al.Recent advances in volatiles of teas[J].Molecules, 2016, 21(3):1-12.
[4] ZHENG W J, WAN X C, BAO G H.Brick dark tea:A review of the manufacture, chemical constituents and bioconversion of the major chemical components during fermentation[J].Phytochemistry Reviews, 2015, 14(3):499-523.
[5] GUO X Y, HO C T, SCHWAB W, et al.Aroma compositions of large-leaf yellow tea and potential effect of theanine on volatile formation in tea[J].Food Chemistry, 2018, 280:73-82.
[6] YENER S, JOSE A S, PABLO M G, et al.Rapid and direct volatile compound profiling of black and green teas (Camellia sinensis) from different countries with PTR-ToF-MS[J].Talanta, 2016, 152:45-53.
[7] BALDERMANN S, YANG Z Y, KATSUNO T.Discrimination of green, oolong, and black teas by GC-MS analysis of characteristic volatile flavor compounds[J].American Journal of Analytical Chemistry, 2014, 5(9):620-632.
[8] WANG K B, LIU F, LIU Z H, et al.Comparison of catechins and volatile compounds among different types of tea using high performance liquid chromatograph and gas chromatograph mass spectrometer[J].International Journal of Food Science and Technology, 2011, 46(7):1 406-1 412.
[9] YE Jing, WANG W G, HO C T, et al.Differentiation of two types of pu-erh teas by using an electronic nose and ultrasound-assisted extraction-dispersive liquid-liquid microextraction-gas chromatography-mass spectrometry[J].Analytical Methods, 2016, 8:593-604.
[10] 肖凌, 毛世红, 童华荣.3种香型凤凰单丛茶挥发性成分分析[J].食品科学, 2018, 39(20):233-239.
XIAO L, MAO S H, TONG H R.Analysis on volatile components of three types of Fenghuang Dancong tea[J].Food Science, 2018, 39(20):233-239.
[11] LIAO X L, YAN J N, WANG B, et al.Identification of key odorants responsible for cooked corn-like aroma of green teas made by tea cultivar “Zhonghuang 1”[J].Food Research International, 2020, 136:109355.
[12] HAN Z X, RANA M M, LIU G F, et al.Green tea flavour determinants and their changes over manufacturing processes[J].Food Chemistry, 2016, 212:739-748.
[13] HO C T, ZHENG X, LI S M.Tea aroma formation[J].Food Science and Human Wellness, 2015, 4(1):9-27.
[14] FENG Z H, LI Y F, LI M, et al.Tea aroma formation from six model manufacturing processes[J].Food Chemistry, 2019, 285:347-354.
[15] 李凤娟. 白茶的滋味、香气和加工工艺研究[D].杭州:浙江大学, 2012.
LI F J.Studies on the taste, aroma and processing of white tea[D].Hangzhou:Zhejiang University, 2012.
[16] 宛晓春, 夏涛.茶树次生代谢[M].北京:科学出版社, 2015.
WAN X C, XIA T.Tea Plant Secondary Metabolism[M].Beijing:Science Press, 2015.
[17] ZENG L T, ZHOU Y, FU X M, et al.Biosynthesis of jasmine lactone in tea (Camellia sinensis) leaves and its formation in response to multiple stresses[J].Journal of Agricultural and Food Chemistry, 2018, 66(15):3 899-3 909.
[18] KAWAKANI M, KOBAYASHI A.“Carotenoid-derived aroma compounds in tea.” in Carotenoid-Derived Aroma Compounds[M].Washington, DC:American Chemical Society, 2001.
[19] WU H L, HUANG W J, CHEN Z J, et al.GC-MS-based metabolomic study reveals dynamic changes of chemical compositions during black tea processing[J].Food Research International, 2019, 120:330-338.
[20] 赵常锐, 宁井铭, 丁勇, 等.祁红毛茶初制过程中香气成分变化的研究[J].安徽农业大学学报, 2010, 37(3):471-477.
ZHAO C R, NING J M, DING Y, et al.Changes of aroma constituents of Qimen raw black tea during processing[J].Journal of Anhui Agricultural University, 2010, 37(3):471-477.
[21] CAO L T, GUO X M, LIU G J, et al.A comparative analysis for the volatile compounds of various Chinese dark teas using combinatory metabolomics and fungal solid-state fermentation[J].Journal of Food and Drug Analysis, 2018, 26(1):112-123.
[22] 康受姈. 不同茶树品种、生产季节和加工方法对茶叶挥发性化合物的影响[D].杭州:浙江大学, 2016.
KANG S L.Effects of tea cultivar, growing season and processing method on volatiles of tea leaves[D].Hangzhou:Zhejiang University, 2016
[23] TAKEO T, MAHANTA P K.Comparison of black tea aromas of orthodox and CTC tea and of black teas made from different varieties[J].Journal of Food and Agricultural, 1983, 34(3):307-310.
[24] 汪蓓, 舒娜, 陆安霞, 等.不同杀青温度对绿茶香型形成的影响[J].食品与发酵工业, 2020, 46(4):197-203.
WANG B, SHU N, LU A X, et al.Aroma formation of green tea effected by different pan-fire temperature[J].Food and Fermentation Industries, 2020, 46(4):197-203.
[25] 郭向阳, 宛晓春.茶叶香气提取方法[J].食品安全质量检测学报, 2019, 10(15):4 869-4 876.
GUO X Y, WAN X C.Extraction methods of tea aroma[J].Journal of Food Safety and Quality, 2019, 10(15):4 869-4 876.
[26] KOBAYASHI A,KAWAMURA M, YAMAMOTO Y, et al.Methyl epijasmonate in the essential oil of tea[J].Agricultural and Biological Chemistry, 1988, 52(9):2 299-2 303.
[27] YANG X G.Aroma constituents and alkylamides of red and green huajiao (Zanthoxylum bungeanum and Zanthoxylum schinifolium)[J].Journal of Agricultural and Food Chemistry, 2008, 56(5):1 689-1 696.
[28] VAN GEMERT L J.Compilations of Odour Threshold Values in Air, Water and Other Media[M].The Netherlands:Oliemans Punter & Partners BV, 2003.
[29] PINO J A, MESA J.Contribution of volatile compounds to mango (Mangifera indica L.) aroma[J].Flavour and Fragrance Journal, 2006, 21(2):207-213.
[30] 苗潇潇, 李美萍, 李平, 等.HS-SPME-GC-O-MS分析玫瑰花露中的易挥发性成分[J].食品科学, 2016, 37(12):156-162.
MIAO X X, LI M P, LI P, et al.Analysis of volatile compounds in rose hydrolat by headspace solid-phase micro extraction and gas chromatography-olfactometry-mass spectrometry[J].Food Science, 2016, 37(12):156-162.
[31] ENGEL K H, FLATH R A, BUTTERY R G, et al.Investigation of volatile constituents in nectarines.1.Analytical and sensory characterization of aroma components in some nectarine cultivars[J].Journal of Agricultural and Food Chemistry, 1988, 36(3):549-553.
[32] CHEN Q C, ZHE Y, YAN H, et al.Identification of aroma composition and key odorants contributing to aroma characteristics of white teas[J].Molecules, 2020, 25(24):6 050.
[33] 刘琳燕, 周子维, 邓慧莉, 等.不同年份白茶的香气成分[J].福建农林大学学报(自然科学版), 2015, 44(1):27-33.
LIU L Y, ZHOU Z W, DENG H L, et al.Analysis of the aromatic components in white tea produced in different years[J].Journal of Fujian Agriculture and Forestry University (Natural Science Edition), 2015, 44(1):27-33.