糖是日常生活中的需求品,但是目前糖的过量食用问题已经开始威胁到人类的健康,过量食用糖会增加肥胖、高血压以及糖尿病等的患病风险[1]。这使得许多国家纷纷开始了减糖行动,例如美国、英国和法国针对含糖饮料进行糖征税,丹麦针对巧克力、冰激凌等产品制定的“肥胖税”,这些减糖政策的制定都取得了积极的效果[2]。目前我国在健康中国行动中也对减糖提出了明确的要求,其中提到要尽快研制儿童食品添加蔗糖摄入的限量指导,提倡人群降低蔗糖的摄入量,鼓励选择用天然甜味物质和甜味剂替代蔗糖生产食品和饮料,尽可能地使超重、肥胖以及一些心脑血管疾病的风险降低。糖精是最早应用于食品工业代糖的甜味剂,但由于糖精的食用对人体有害无益,所以糖精逐渐被淘汰,取而代之的是以阿斯巴甜为代表的人工甜味剂。这类人工甜味剂在人体内很难被转化,所以可以认为是无热量的糖,目前也仍然在食品工业中被广泛使用。但是随着人们的不断探索研究,以甜菊糖苷为代表的一类绿色、健康的天然甜味剂引起了人们的注意,甜菊糖苷的热量仅为蔗糖的1/3,但甜度为蔗糖的几百倍,是众多糖尿病和高血压患者的最佳选择。目前甜菊糖苷已经开始应用于烘焙、乳制品、饮料等产品的生产中,其中在2019年全球推出的饮料新品中,新型甜味剂甜菊糖苷的使用量已经仅次于三氯蔗糖和安赛蜜。由此可见,甜菊糖苷具有很好的发展前景。
甜菊糖是一种天然存在于甜叶菊中的甜味剂,即甜菊烯二萜苷,通常被称为甜菊糖苷[3]。这种甜味剂的应用最早起源于南美洲巴拉圭原住居民,甜菊糖苷在20世纪30年代由法国的两位化学家从甜叶菊中成功分离。20世纪70年代日本开始从南美洲引进菊科植物甜叶菊并成功种植,后来甜菊糖开始作为一种甜味剂应用于日本食品工业。随后不久,我国从日本引进了甜叶菊并试种成功[4]。甜叶菊中的甜味成分统称为甜菊糖苷[5],甜菊糖苷的种类繁多,主要包括莱鲍迪苷A族、莱鲍迪苷C族、莱鲍迪苷F族等,另外杜香苷A等也属于甜菊糖苷类化合物[6]。2008年高纯度的甜菊糖苷和莱鲍迪苷A通过了美国GRAS的安全认证;2011年甜菊糖苷已被进出口委员会(Committee on Import and Export,CODEX)采用,使其能作为食品添加剂使用并出版了食品使用标准;另外甜菊糖苷也通过了欧盟的安全性审查,并开始能够作为甜味剂在欧盟地区使用;随后中国、新加坡、马来西亚等国家也开始将甜菊糖苷纳入可使用甜味剂行列;2013年莱鲍迪苷A作为最常见的甜菊糖苷类化合物开始成为了世界的主流,并且开始在全球的主要国家中使用;2018年至今,素有“下一代甜菊糖”之称的莱鲍迪苷M,由于其口感最接近于蔗糖,开始慢慢取代莱鲍迪苷A成为世界的主流。
甜菊糖苷类化合物的化学结构中均具有一个相同的基本骨架——内-贝壳杉烯酸(ent-kaurenoic acid)结构。具有甜味的甜菊糖苷化合物都是一些具有ent-kaurane骨架的二萜苷;另外,甜菊糖苷的甜度还与其化学结构有一定的关系,杨全花[7]根据各甜菊糖苷化合物的甜度值范围得到的甜度大小顺序:Ⅱ型骨架>Ⅲ型骨架>Ⅰ型骨架>Ⅴ型骨架>Ⅳ型骨架(图1)。甜菊糖苷中最常见的2种化合物为莱鲍迪苷 A和甜菊苷(stevioside,St)。以蔗糖为标准,甜菊糖苷的相对甜度为150~300倍,而莱鲍迪苷A的相对甜度位于各甜菊糖苷类化合物之首,大约是250~450倍。另外,低热量也是甜菊糖苷的一个显著特点。由此可见,甜菊糖苷是蔗糖等传统甜味剂的一种天然优良替代品。

a-Ⅰ型;b-Ⅱ型;c-Ⅲ型;d-Ⅳ型;e-Ⅴ型
图1 甜菊糖苷5种骨架结构图
Fig.1 Five kinds of skeleton structures of stevioside
1 甜菊糖苷及其衍生物(甜菊糖及其衍生物制备技术与结构分析)
甜菊糖苷类化合物的种类繁多,目前已经发现甜菊糖苷类化合物30多种[6],主要包括较常见的甜菊苷和莱鲍迪苷A、逐渐成为世界主流的莱鲍迪苷M和莱鲍迪苷D以及含量较低的莱鲍迪苷R和莱鲍迪苷S等,这些甜菊糖苷的基本骨架大致相同,不同之处在于取代基上化学结构的不同。另外人们对于甜菊糖苷的衍生物甜菊醇、异甜菊醇也不断地进行研究。甜菊糖苷及其衍生物不仅表现出了可应用于食品工业的优良性质,也表现出特殊的生理功能。
1.1 甜菊糖苷的提取方法
目前已发现的甜菊糖苷化合物的提取技术主要包括热水提取、超声辅助提取、酶法、大孔树脂吸附法等,其中大孔树脂吸附法的应用最多;随着提取技术的不断进步,近年来还出现了利用快速固液动态萃取法[8]、双水相体系提取法[9]及超临界萃取法[10]等方法提取甜菊糖苷。虽然目前针对甜菊糖苷提取的方法较多,但这些提取方法并不适用于所有的甜菊糖苷种类,每种方法仅适用于其特定的范围。几种主要的提取方法的适用甜菊糖苷范围如表1所示。
表1 甜菊糖苷的主要提取方法及其适用种类
Table 1 Main extraction methods of stevioside and its applicable species

提取方法适用甜菊糖苷种类快速固液动态萃取法甜菊苷、莱鲍迪苷A[8]超临界流体萃取甜菊苷、莱鲍迪苷A[10]超滤甜菊苷、莱鲍迪苷A[11]加压热水提取甜菊苷、莱鲍迪苷A[12]微波辅助提取甜菊苷、莱鲍迪苷A[13]DES-UAE法甜菊苷、莱鲍迪苷A[14]大孔吸附树脂莱鲍迪苷A[15]高速逆流色谱甜菊苷、莱鲍迪苷A、莱鲍迪苷C[16-17]高速剪切均质萃取法甜菊糖苷、莱鲍迪苷A、莱鲍迪苷C[18]
因为甜菊苷和莱鲍迪苷A是甜菊糖苷类化合物中最常见的2种化合物,所以多数的甜菊糖苷提取方法主要是针对这2种甜菊糖苷。
1.2 甜菊糖苷及其衍生物
甜菊糖苷类化合物主要包括甜菊糖苷及其衍生物,主要分为自然界提取和已有的甜菊糖苷生物转化以及利用基因工程技术获得。由自然界提取而来的甜菊糖苷类化合物主要包括莱鲍迪苷A、莱鲍迪苷B、莱鲍迪苷C和莱鲍迪苷D等;由已有的甜菊糖苷生物转化而来的主要是指甜菊糖苷的衍生物甜菊醇和异甜菊醇等;而利用基因工程技术获取的甜菊糖苷类化合物主要是指莱鲍迪苷M。
由表2可以看出,甜菊糖苷及其衍生物的化学结构的不同之处在于它们的基本骨架上R1、R2位置上的取代基不同。甜度居于各甜菊糖苷化合物之首的是莱鲍迪苷A,其相对甜度为250~450倍,莱鲍迪苷A与甜菊苷的结构相似,不同之处只是多了一个葡萄糖部分[20]。莱鲍迪苷D与莱鲍迪苷A结构类似,通过一系列的体外实验也可以证明两者具有相似性,且实验证明莱鲍迪苷D的安全性较高可以应用于食品中[21]。衍生物甜菊醇和异甜菊醇的分子质量较所列甜菊糖苷的分子质量低,它们主要是来源于甜菊糖苷在碱性或酸性条件下的水解,经水解之后分别生成ent-kaurane二萜甜菊醇或ent-beyerane二萜异甜菊醇[22]。
表2 甜菊糖苷及其衍生物归纳表[3,19]
Table 2 Summary of stevioside and its derivatives

甜菊糖及其衍生物种类分子式R1R2相对甜度甜菊苷C38H60O18β-Glcβ-Glc-β-Glc(2→1)250~300甜菊糖苷C32H50O13Hβ-Glc-β-Glc(2→1)100~125莱鲍迪苷AC44H70O23β-Glcβ-Glc-β-Glc(2→1)|β-Glc-(3→1)250~450莱鲍迪苷BC38H60O18Hβ-Glc-β-Glc(2→1)|β-Glc-(3→1)300~350莱鲍迪苷CC44H70O22β-Glcβ-Glc-β-Rha(2→1)|β-Glc-(3→1)50~120莱鲍迪苷DC50H80O28β-Glc-β-Glc(2→1)β-Glc-β-Glc(2→1)|β-Glc-(3→1)200~300莱鲍迪苷EC44H70O23β-Glc-β-Glc(2→1)β-Glc-β-Glc(2→1)150~300莱鲍迪苷FC43H68O22β-Glcβ-Glc-β-Xyl(2→1)|β-Glc-(3→1)250~300莱鲍迪苷MC56H90O33β-Glc-β-Glc(2→1)|β-Glc-(3→1)β-Glc-β-Glc(2→1)|β-Glc-(3→1)200~350莱鲍迪苷NC56H90O32β-Glc-α-Rha(2→1)|β-Glc-(3→1)β-Glc-β-Glc(2→1)|β-Glc-(3→1)-莱鲍迪苷RC43H68O22---莱鲍迪苷SC44H70O22---莱鲍迪苷GC38H60O18β-Glcβ-Glc-β-Glc(3→1)-莱鲍迪苷HC50H80O27β-Glcβ-Glc-β-Rha(2→1)-β-Glc(3→1)|β-Glc-(3→1)-莱鲍迪苷IC50H80O28β-Glc-β-Glc(3→1)β-Glc-β-Glc(2→1)|β-Glc-(3→1)-莱鲍迪苷JC50H80O27β-Glc-β-Rha(2→1)β-Glc-β-Glc(2→1)|β-Glc-(3→1)-莱鲍迪苷KC50H80O27β-Glc-β-Glc(2→1)β-Glc-β-Rha(2→1)|β-Glc-(3→1)-莱鲍迪苷LC50H80O28β-Glcβ-Glc-β-Glc(2→1)-β-Glc(6→1)|β-Glc-(3→1)-杜香苷AC38H60O17β-Glcβ-Glc-β-Rha(2→1)50~120杜香苷BC38H60O17Hβ-Glc-β-Rha(2→1)|β-Glc-(3→1)40~60甜菊醇C20H30O3---异甜菊醇C20H30O3---
注:Glc,glucose;Rha,rhamnose;Xyl,xylose
1.2.1 莱鲍迪苷A
莱鲍迪苷A(rebaudioside A),化学式为C44H70O23,基本骨架R1和R2位置的取代基分别为β-Glc、β-Glc-[β-Glc(3-1)]-β-Glc(2-1),分子质量为967.88 g/mol。莱鲍迪苷A是甜菊糖苷中的主要成分,也是甜菊糖苷中最稳定的成分[23];目前莱鲍迪苷A的提纯和精制工艺手段主要包括:高效液相色谱法、薄层色谱法、膜分离法、毛细管电泳法、液滴逆流分配层析法、超临界萃取法、重结晶法[24]。莱鲍迪苷A与其他的甜菊糖苷相比显示出更多的甜味和可口的味道,欧洲、美国、中国、韩国、巴西等地已批准莱鲍迪苷A作为一种甜味剂使用,但由于莱鲍迪苷A与一些已投入使用的甜味剂相比仍存在口感不佳的问题,这使得它在国内并没有太高的热度。

图2 莱鲍迪苷A结构示意图
Fig.2 Structure of rebaudioside A
莱鲍迪苷A具有特殊的生理功能。一些研究表明,莱鲍迪苷A具有较强的降血糖作用[25], 它对2型糖尿病可能具有治疗效果,并对胰岛β细胞产生胰岛素有直接影响[20]。莱鲍迪苷A的血液动力学效应研究中发现,在血压正常或正常平均动脉压较低的健康个体中,每日摄入1 000 mg/kg体重莱鲍迪苷A后,平均动脉压或心率未观察到显著变化[26],说明莱鲍迪苷A也具有一定的抗高血压作用,对人体的血压水平影响较小。莱鲍迪苷A还可以增强胰岛素的产生,从而起到调节血糖的作用,具有健康的糖调节活性[3]。莱鲍迪苷A对TPA诱导的小鼠炎症反应也有很强的抑制作用,表明其具有一定的抗癌作用[27-28]。另外SARAVANAN等[29]的研究结果表明,抗脂质过氧化、抗高血脂和抗氧化也是天然低热量甜味剂莱鲍迪苷A的一些重要特性。
1.2.2 甜菊苷
甜菊苷(stevioside),分子式为C38H60O18,其在基本骨架R1和R2位置的取代基分别为β-Glc、β-Glc-β-Glc(2→1),相对甜度为250~300倍。甜菊苷是甜叶菊植物中主要的ent-kaurene型二萜糖苷之一,在南美洲、日本和中国等地甜菊苷已被商业用于许多食品的增甜,但不足之处是它具有一定的苦涩余味。目前甜菊苷的提取方法与莱鲍迪苷A基本相同,主要包括微波辅助提取、超临界流体萃取和加压热水提取等。
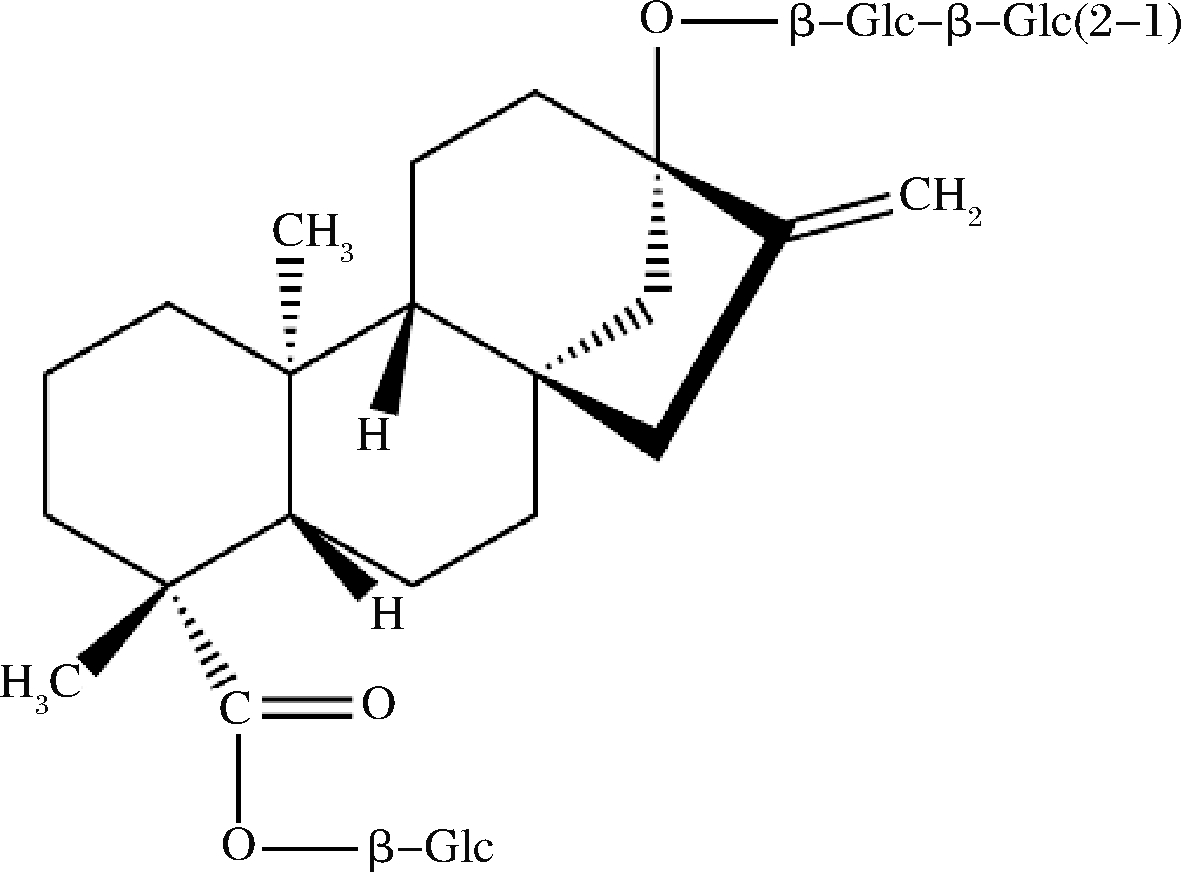
图3 甜菊苷结构示意图
Fig.3 Structure of stevioside
甜菊苷具有一定的抗炎作用,是一种胃保护剂,它可以阻断钙通道抑制平滑肌收缩,减少虹鳟鱼组胺引起的胃异常,是减少组胺引起的酸分泌和抑制胃蛋白酶作用的潜在原因[30]。甜菊苷具有利尿功能和引起血管舒张,使血浆容量下降。一些基于人类的研究也表明,甜菊糖苷影响心血管系统,导致低血压,缩短收缩时间,从而减少中风的发生;临床试验表明甜菊苷可以降低收缩压和舒张压[3]。一些体内和体外研究也表明,甜菊苷具有降血糖的作用,其机制主要是增加了胰岛素分泌[31]。另外与莱鲍迪苷A相同的是,甜菊苷也具有抗癌活性[32]。
1.2.3 莱鲍迪苷D
莱鲍迪苷D(rebaudioside D),分子式C50H80O28,其在基本骨架R1和R2位置的取代基分别为β-Glc-β-Glc(2→1)、β-Glc-[β-Glc-(3→1)]-β-Glc(2→1),相对甜度居于200~300倍范围,是甜叶菊植物中含量较少的一种甜菊糖苷类化合物。
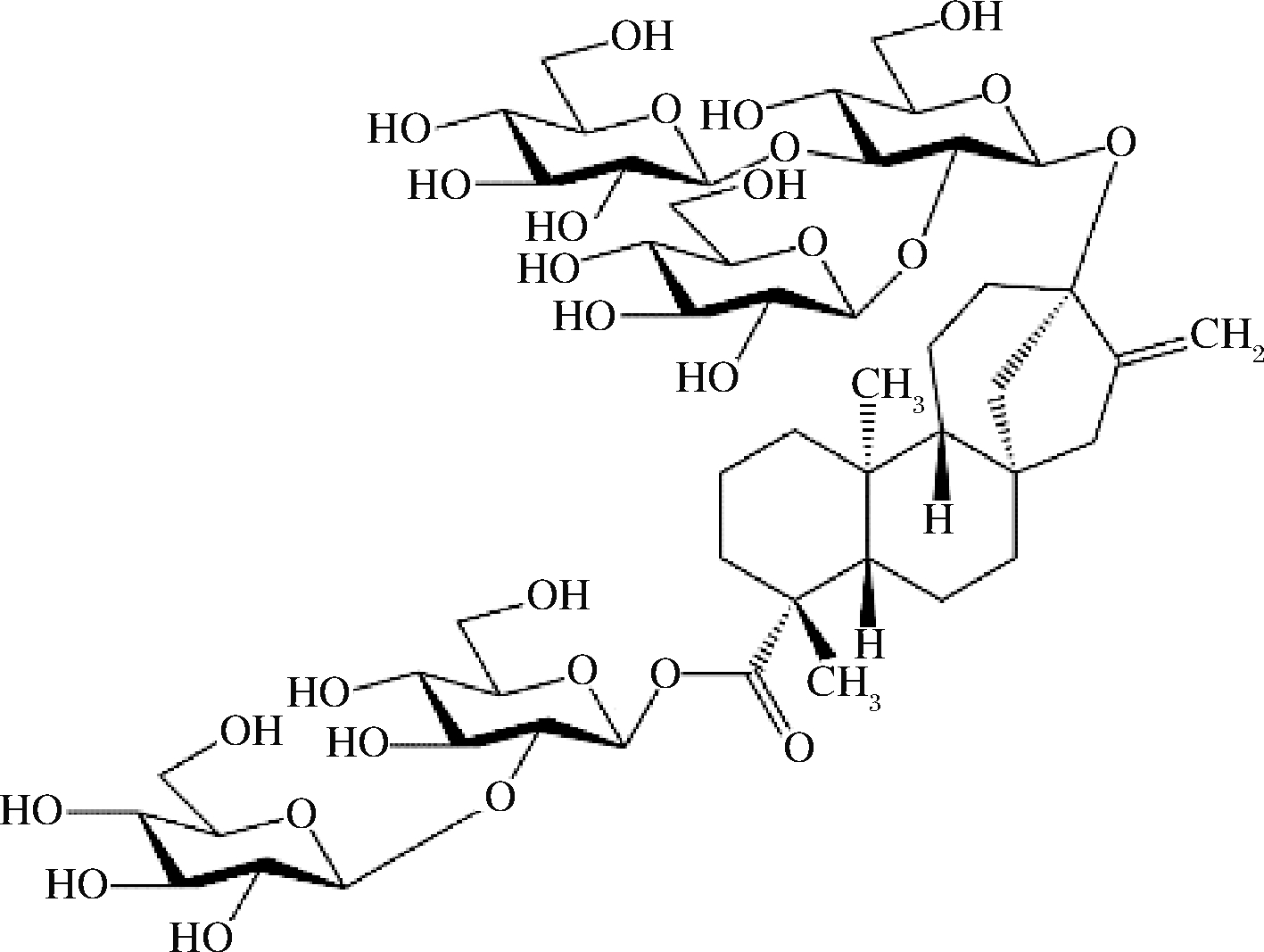
图4 莱鲍迪苷D结构图
Fig.4 Structure of rebaudioside D
莱鲍迪苷D的代谢和毒性与莱鲍迪苷A相似,但是莱鲍迪苷D的代谢途径较长,肠道吸收率低;在体外实验中,莱鲍迪苷A和莱鲍迪苷D溶液在模拟胃液和小肠液中表现出相似的稳定性,容易被从盲肠收集的肠道细菌水解[21]。
1.2.4 莱鲍迪苷M
莱鲍迪苷M(rebaudioside M),分子式为C56H90O33,β-Glc-[β-Glc-(3→1)]-β-Glc(2→1)是其基本骨架R1和R2位置的取代基,相对甜度为200~350倍。莱鲍迪苷M的结构如图5所示。
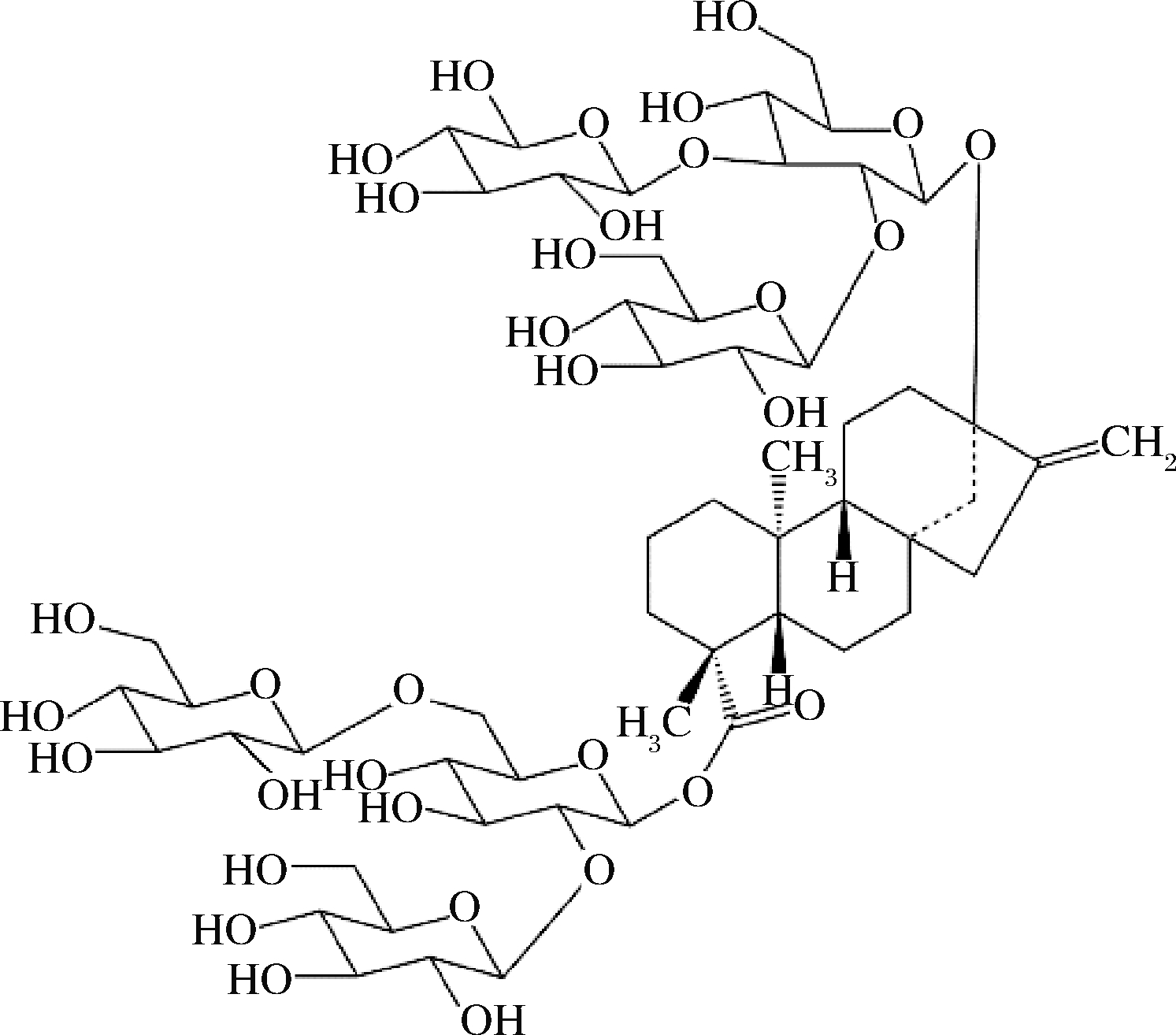
图5 莱鲍迪苷M结构图
Fig.5 Structure of rebaudioside M
2014年PRAKASH等报道出一种新的甜菊糖苷类化合物——rebaudioside M[33]。莱鲍迪苷M甜味干净,略带苦涩味或甘草味,口感方面最接近于蔗糖。在pH 4~8溶液中莱鲍迪苷M最稳定,pH<2明显不稳定,此外莱鲍迪苷M的稳定性还会随着温度的升高而降低;其稳定性与莱鲍迪苷A非常相似[34]。此外,莱鲍迪苷M被美国食品和药物管理局认为是安全的。
莱鲍迪苷M在自然界中的含量很少,其主要有3种获取途径,第1种途径主要是利用转基因酵母从甜叶菊提取物中获得,具有纯度高的优点;第2种途径主要是从葡萄糖被基因工程技术改造过的酵母发酵获得,但是最终获得的莱鲍迪苷M不再属于天然来源;第3种途径是通过不断地改良育种来选育出莱鲍迪苷M含量较高的甜叶菊种类,从而能够提取出大量的莱鲍迪苷M。
1.2.5 甜菊醇、异甜菊醇
甜菊醇(steviol)和异甜菊醇(isosteviol),分子式均为C20H30O3,两者的分子质量为318.2 g/mol,是甜菊糖苷化合物的衍生物。两者的结构如图6所示。
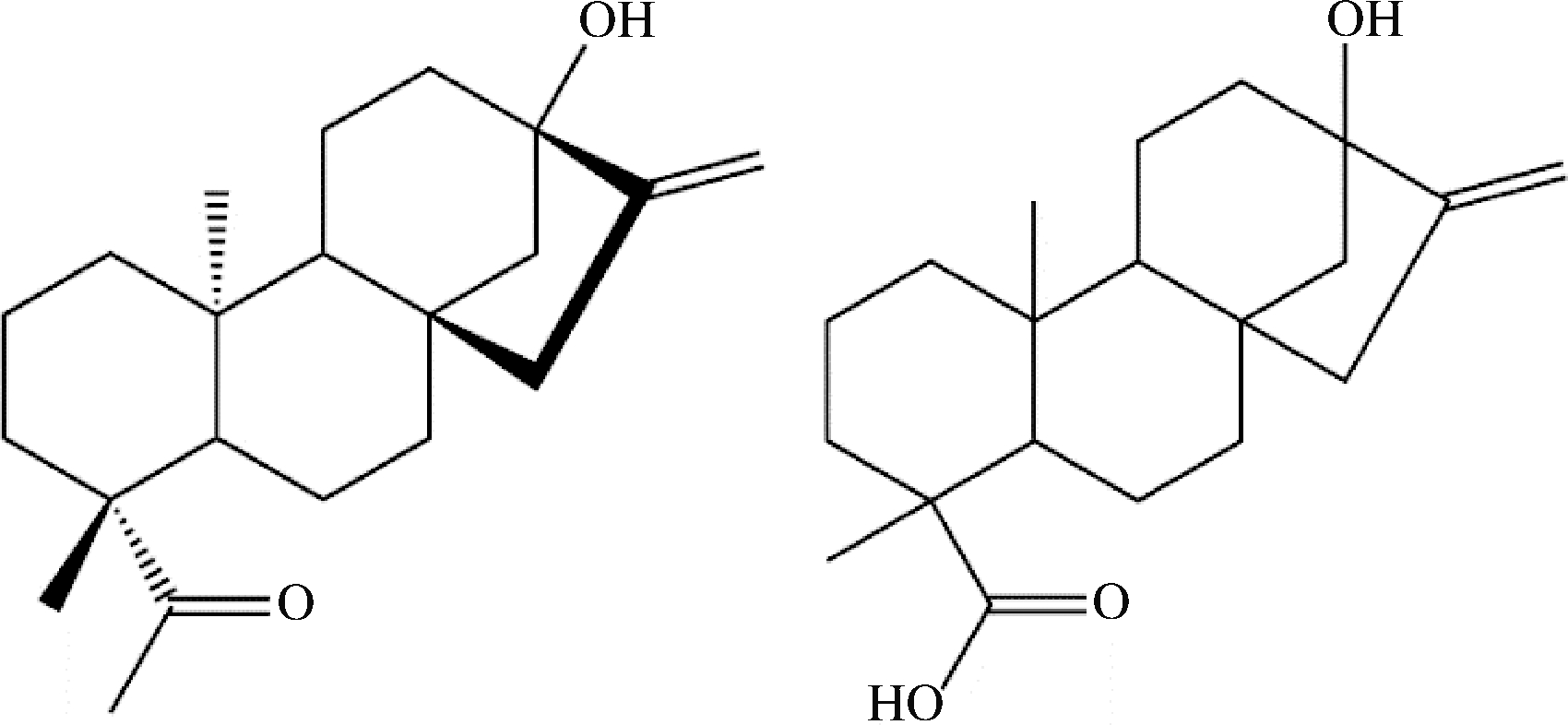
图6 甜菊醇(左)和异甜菊醇(右)结构图
Fig.6 Structures of steviol (left) and isosteviol (right)
甜菊醇具有抗炎、降低血糖的生理功能,它可直接作用刺激胰岛β细胞和INS-1细胞分泌胰岛素[34-35];另外甜菊醇对结肠上皮细胞还具有抗感染的效力。异甜菊醇可以抑制血管紧张素II诱导的细胞增殖和内皮素I的分泌,它还可以减少活性氧的生成,起到一定的抗氧化作用[23]。
2 甜菊糖苷在食品工业中的应用
在食品工业中蔗糖是最常见的甜味剂,但蔗糖的大量使用会导致餐后血糖的升高,会引起人体肥胖和增加心脑血管疾病的患病风险;鉴于这些问题的存在,人们开始寻求新的甜味剂来替代传统甜味剂在食品工业上的应用。甜菊糖被誉为“人类第三代健康糖源”,是一种纯天然、低热量、高甜度、高安全性的物质,被发现可以有效的替代传统甜味剂,作为一种健康甜味剂应用于食品工业。目前甜菊糖苷已经应用于烘焙、饮料、乳制品、糖果等产品中。
2.1 甜菊糖苷在烘焙产品中的应用
烘焙产品主要是指蛋糕、面包、点心等。在烘焙产品的制作中,糖是不可缺少的成分。其中最常见的是蔗糖在烘焙产品中的应用,它的参与可以改善产品的质地口感等,但蔗糖的长期大量食用会显著增加肥胖、龋齿、心血管疾病的患病风险。而甜菊糖苷作为一种新型天然甜味剂,其自身具有的热量低、甜度高的特点,可以有效地改善这种现状。除此之外,甜菊糖苷热稳定性也很高,它在整个烘焙过程中能保持其稳定性,并且可以加热到200 ℃,在烹调过程中既不发酵也不发生褐变反应,能够很好地保持产品风味、降低热量,使延长产品的货架期成为了可能,拓宽了烘焙的应用领域[36]。KARP等[37]将甜菊糖苷取代巧克力松饼中20%的蔗糖, 松饼的可可风味和甜味口感均有所提升。
2.2 甜菊糖苷在饮料中的应用
果汁饮料、碳酸饮料等饮料产品中均含有大量糖,长期饮用均会造成肥胖现象的不断增加。考虑到这些不良影响的存在,众多的饮料公司开始在饮料制作过程中添加甜菊糖苷作为甜味剂,如莱鲍迪苷A已被全球最大的果汁饮料经销商可口可乐公司应用于饮料的制作中[19],在可口可乐推出的Coca Cola Life中使用甜菊糖作为甜味剂,成功地达到了减低热量的效果;雀巢也开始在水果饮料Sanpellegrino 中加入甜菊糖来取代 40% 的白糖;百事可乐也推出了添加甜菊糖的产品七喜;另外目前市场上一些比较常见的饮料小茗同学、农夫山泉的茶Π等也开始使用甜菊糖苷来代替部分糖从而降低产品的甜度。虽然很多饮料公司都开始研发使用甜菊糖苷的新产品,但均有因新配方而丧失消费者的风险。目前在饮料市场中应用最多的为甜菊苷和莱鲍迪苷A,它们的加入既可以达到低热量的效果,又能起到增甜的作用,最重要的是有效地降低了肥胖等不良现象的发生几率。例如桃子汁由甜叶菊(160 mg/L)和蔗糖(56 g/L)混合配制而成,与含有9%蔗糖的对照样品相比,在不影响产品感官品质的情况下,可使热量减少25%[30]。
2.3 甜菊糖苷在乳制品中的应用
乳制品主要包括液体乳、冰激凌、干酪等乳制品,由于甜菊糖苷在经过热处理后能保持其稳定性,因此成为乳制品的合适选择[30]。在乳制品中,冰激凌是很受欢迎的冷冻乳制品之一,在冰激凌的制作过程中,它的质地、黏度、口味均会受到甜味剂的影响,冰激凌生产中最常使用的甜味剂是蔗糖,但由于蔗糖对健康的影响,人们开始将甜菊糖苷应用于冰激凌生产中。有研究表明,使用甜菊糖苷和蔗糖的混合物生产的冰激凌比只是用甜菊糖苷生产的冰激凌具有更好的感官评分[38-39];另外,人们在一些酸奶产品中也发现甜菊糖苷与蔗糖混合使用会具有更好的口感。徐泽琦等[40]的甜菊糖苷低糖大豆发酵酸奶研究中用甜菊糖苷替代30%蔗糖发酵4 h后,不仅口感气味色泽都较好,而且有更高的营养价值,适用于糖尿病病人、患有口腔龋齿的人食用。
2.4 甜菊糖苷改性研究
尽管甜菊糖苷是一种天然来源的甜味剂,并且具有低热高甜、性质稳定等优点,但是它的甜味与白砂糖或糖醇类相比依然存在差异,有轻微的苦味以及较差的余味,尤其是应用在热冲调产品中余味会越发明显,通过改性的方法改善甜菊糖苷的味质是目前甜味剂公司共同努力的方向。主要的改性方法有化学修饰法、酶促修饰法和微生物转化法。
2.4.1 化学修饰法
化学修饰法指通过化学反应改变甜菊苷的分子结构,从而改变其理化性质和感官品质,主要是通过改变连接在配基上的糖基来改善甜菊糖的味质。化学修饰法因反应条件苛刻,合成步骤较多,加上安全原因,目前已很少研究。
2.4.2 酶促修饰法
酶促修饰法是指通过酶的转糖基作用或水解作用,在甜菊糖苷中引入葡萄糖基以期改善其味质。采用的酶包括环糊精葡萄糖基转移酶、β-半乳糖苷酶、糊精葡聚糖酶等,采用该方法制备的产物是葡萄糖基甜菊糖苷,属于食用香料,甜菊糖苷经过上述酶法改性以后虽然味质得到了改善,但是相对甜度也会明显降低,一般改性后产物的相对甜度是白砂糖的50~150倍左右。
2.4.3 微生物转化法
微生物转化法是指利用微生物代谢过程对甜菊苷进行转化,目前的研究大多数是利用微生物体内的酶对甜菊糖苷进行改性,DE等[41]筛选了一株真菌Gibberella fujikuroi,用以甜菊苷Stv为唯一碳源的培养基诱导该真菌产酶,实现了将甜菊苷Stv部分转化成味质更好的RA。用麸皮培养基对棘孢曲霉进行固体发酵,得到的酶液能够在10 h内以沉淀析出的形式把甜菊糖中的Stv和莱鲍迪苷C全部转化成甜菊醇(SV),通过这样的方法使得体系中味质更好的RA得以有效富集[42]。
3 展望
我国是世界上的第二食糖大国,但近年来由于糖的食用带来的健康问题逐渐引起了人们的重视,“无糖”“低卡”已经成为了人们的健康追求。为了满足消费者的需求,必须不断地研究出新的甜味剂来改善现状。甜菊糖苷作为一种绿色健康的新型甜味剂,具有低热量、高甜度的优点既解决了传统甜味剂的缺点,又满足了消费者在口感上的要求,它可以有效地替代传统甜味剂,达到人们对于健康追求的食用要求,具有很大的发展前景。
[1] 陆婉瑶,王健,孟庆佳,等.减糖产品现状与发展趋势分析[J].甘蔗糖业,2020,49(4):83-91.
LU W Y,WANG J,MENG Q J,et al.Analysis of current situation and development trend of sugar reducing products[J].Sugarcane and Canesugar,2020,49 (4):83-91
[2] 米玉倩,吴静,梁晓峰.欧美国家减糖政策分析及其对我国慢性病防控的启示[J].中国卫生事业管理,2017,34(4):247-248;251.
MI Y Q,WU J,LIANG X F.Enlightenment from the sugar reduction policy at abroad on control and prevention of chronic diseases in China[J].Chinese Health Service Management,2017,34(4):247-248;251.
[3] MATHUR S, BULCHANDAN N, PARIHAR S, et al.Critical Review on Steviol Glycosides:Pharmacological,Toxicological and Therapeutic Aspects of High Potency Zero Caloric Sweetener[J].International Journal of Pharmacology,2017,13(7):916-928.
[4] 丰雪. 甜菊糖苷的提取及莱鲍迪苷A的分离纯化研究[D].南昌:南昌大学,2012.
FENG X.Study on extraction of stevio glycosides and purification of rebaudioside A[D].Nanchang:Nanchang University,2012.
[5] 陈俊名. 甜菊糖苷的体外代谢及生物活性研究[D].无锡:江南大学,2019.
CHEN J M.In vitro metabolism and biological activity of steviol glycosides[D].Wuxi:Jiangnan University,2019.
[6] WÖLWER-R U.The leaves of Stevia rebaudiana (Bertoni),their constituents and the analyses thereof:a review.[J].Journal of Agricultural and Food Chemistry,2012,60(4):886-895.
[7] 杨全花. 甜叶菊化学成分、含量及其甜度的研究[D].北京:北京化工大学,2012.
YANG Q H.Analysis of the chemical constituents and its properties of Stevia rebaudiana[D].Beijing:Beijing University of Chemical Technology,2012
[8] GALLO M,VITULANO M,ANDOLFI A,et al.Rapid Solid-Liquid Dynamic Extraction (RSLDE):a New Rapid and Greener Method for Extracting Two Steviol Glycosides (Stevioside and Rebaudioside A) from Stevia Leaves[J].Plant Foods for Human Nutrition,2017,72(2):141-148.
[9] ABOLGHASEMBEYK T, SHAHRIARI S, SALEHIFAR M.Extraction of stevioside using aqueous two-phase systems formed by choline chloride and K3PO4[J].Food and Bioproducts Processing,2017,102:107-115.
[10] AMEER K, CHUN B S, KWON J H.Optimization of supercritical fluid extraction of steviol glycosides and total phenolic content from Stevia rebaudiana (Bertoni) leaves using response surface methodology and artificial neural network modeling[J].Industrial Crops and Products,2017,109:672-685.
[11] MART NEZ-ALVARADO J C,TORRESTIANA-S
NEZ-ALVARADO J C,TORRESTIANA-S NCHEZ B,AGUILAR-USCANGA M G.Isolation of steviol glycosides by a two-step membrane process operating under sustainable flux[J].Food and Bioproducts Processing,2017,101:223-230.
NCHEZ B,AGUILAR-USCANGA M G.Isolation of steviol glycosides by a two-step membrane process operating under sustainable flux[J].Food and Bioproducts Processing,2017,101:223-230.
[12] ![]() ,BARBA F J,GRANATO D,et al.Galanakis,Zoran Herceg,Verica Dragovi?-Uzelac,Predrag Putnik.Pressurized hot water extraction (PHWE) for the green recovery of bioactive compounds and steviol glycosides from Stevia rebaudiana Bertoni leaves[J].Food Chemistry,2018,254:150-157.
,BARBA F J,GRANATO D,et al.Galanakis,Zoran Herceg,Verica Dragovi?-Uzelac,Predrag Putnik.Pressurized hot water extraction (PHWE) for the green recovery of bioactive compounds and steviol glycosides from Stevia rebaudiana Bertoni leaves[J].Food Chemistry,2018,254:150-157.
[13] ![]() ,MARAS M,BARBA F J,et al.Innovative technologies for the recovery of phytochemicals from Stevia rebaudiana Bertoni leaves:A review[J].Food Chemistry,2018,268:513-521.
,MARAS M,BARBA F J,et al.Innovative technologies for the recovery of phytochemicals from Stevia rebaudiana Bertoni leaves:A review[J].Food Chemistry,2018,268:513-521.
[14] MILANI G,VIAN M,CAVALLUZZI M M,et al.Ultrasound and deep eutectic solvents:An efficient combination to tune the mechanism of steviol glycosides extraction.[J].Ultrasonics Sonochemistry,2020,69:105225.
[15] LIU Y F,DI D L,BAI Q Q,et al.Preparative separation and purification of rebaudioside a from steviol glycosides using mixed-mode macroporous adsorption resins.[J].Journal of Agricultural and Food Chemistry,2011,59(17):9 629-9 636.
[16] HUANG X Y,FU J F,DI D L.Preparative isolation and purification of steviol glycosides from Stevia rebaudiana Bertoni using high-speed counter-current chromatography[J].Separation and Purification Technology,2010,71(2):220-224.
[17] LIU Y,WANG G,HUANG X,et al.Use of O-carboxymethyl chitosan in high-speed counter-current chromatography:a novel additive for a biphasic solvent system[J].New Journal of Chemistry,2014,38(3):1 150-1 157.
[18] XU S H,WANG G Y,GUO R L,et al.Extraction of steviol glycosides from Stevia rebaudiana (Bertoni) leaves by high-speed shear homogenization extraction[J].Journal of Food Processing and Preservation,2019,43(12):e14250.
[19] CASTRO-MUOZ R,D AZ-MONTES E,CASSANO A,et al.Membrane separation processes for the extraction and purification of steviol glycosides:An overview[J].Critical Reviews in Food Scicence and Nutrition,2021,61(13):2 152-2 174.
AZ-MONTES E,CASSANO A,et al.Membrane separation processes for the extraction and purification of steviol glycosides:An overview[J].Critical Reviews in Food Scicence and Nutrition,2021,61(13):2 152-2 174.
[20] GUPTA E,PURWAR S,SUNDARAM S,et al.Stevioside and rebaudioside A-predominant ent-kaurene diterpene glycosides of therapeutic potential:A review[J].Czech Journal of Food Sciences,2017,34(4):281-299.
[21] NIKIFOROV A I,RIHNER M O,EAPEN A K,et al.Metabolism and toxicity studies supporting the safety of rebaudioside D[J].International Journal of Toxicology,2013,32(4):261-273.
[22] WANG M W,LI H,XU F X,et al.Diterpenoid lead stevioside and its hydrolysis products steviol and isosteviol:Biological activity and structural modification[J].European Journal of Medicinal Chemistry,2018,156:885-906.
[23] SINGH D P,KUMARI M,PRAKASH H G,et al.Phytochemical and pharmacological importance of stevia:A calorie-free natural sweetener[J].Sugar Tech,2019,21(2):227-234.
[24] 孙传范, 李进伟.甜菊糖苷研究进展[J].食品科学,2010,31(9):338-340.
SUN C F,LI J W.Research progress of stevioside[J].Food science,2010,31(9):338-340
[25] SARAVANAN R,VENGATASH B K.V,RAMACHANDRAN V.Effect of Rebaudioside A,a diterpenoid on glucose homeostasis in STZ-induced diabetic rats[J].Journal of Physiology and Biochemistry,2012,68(3):421-431.
[26] MAKI K C,CURRY L L,REEVES M S,et al.Chronic consumption of rebaudioside A,a steviol glycoside,in men and women with type 2 diabetes mellitus[J].Food and Chemical Toxicology,2008,46(suppl 7):S47-S53.
[27] RASKOVIC A,JAKOVLJEVIC V,MIKOV M,et al.Joint effect of commercial preparations of Stevia rebaudiana Bertoni and sodium monoketocholate on glycemia in mice[J].European Journal of Drug Metabolism and Pharmacokinetics,2004,29(2):83-86.
[28] YASUKAWA K,KITANAKA S,SEO S.Inhibitory effect of stevioside on tumor promotion by 12-O-tetradecanoylphorbol-13-acetate in two-stage carcinogenesis in mouse skin[J].Biological & Pharmaceutical Bulletin,2002,25(11):1 488-1 490.
[29] SARAVANAN R,RAMACHANDRAN V.Modulating efficacy of Rebaudioside A,a diterpenoid on antioxidant and circulatory lipids in experimental diabetic rats[J].Environmental Toxicology and Pharmacology,2013,36(2):472-483.
[30] GANDHI S,GANDHI S,GAT Y,et al.Natural sweeteners:Health benefits of Stevia[J].Foods and Raw Materials,2018,6(2):392-402.
[31] SALEHI B, L PEZ M D, MART
PEZ M D, MART NEZ-L
NEZ-L PEZ S,et al,Stevia rebaudiana Bertoni bioactive effects:From in vivo to clinical trials towards future therapeutic approaches[J].Phytotherapy Research,2019,33(11):2 904-2 917.
PEZ S,et al,Stevia rebaudiana Bertoni bioactive effects:From in vivo to clinical trials towards future therapeutic approaches[J].Phytotherapy Research,2019,33(11):2 904-2 917.
[32] PRAKASH I, MARKOSYAN A, BUNDERS C.Development of next generation Stevia sweetener:Rebaudioside M[J].Foods,2014,3(1):162-175.
[33] PURKAYASTHA S,BHUSARI S,PUGH G,et al.In vitro metabolism of rebaudioside E under anaerobic conditions:Comparison with rebaudioside A[J].Regulatory Toxicology and Pharmacology,2015,72(3):646-657.
[34] JEPPESEN P B,GREGERSEN S,ALSTRUP K K,et al.Stevioside induces antihyperglycaemic,insulinotropic and glucagonostatic effects in vivo:Studies in the diabetic Goto-Kakizaki (GK) rats.[J].Phytomedicine,2002,9(1):9-14.
[35] JEPPESEN P B,GREGERSEN S,POULSEN C R,et al.Stevioside acts directly on pancreatic beta cells to secrete insulin:Actions independent of cyclic adenosine monophosphate and adenosine triphosphate-sensitive K+-channel activity[J].Metabolism:Clinical and Experimental,2000,49(2):208-214.
[36] PANPATIL V V,POLASA K.Assessment of stevia (Stevia rebaudiana)-natural sweetener:A review[J].Journal of Food Science and Technology -Mysore-,2008,45(6):467-473.
[37] KARP S, WYRWISZ J, KUREK M A, et al.Combined use of cocoa dietary fibre and steviol glycosides in low-calorie muffins production[J].International Journal of Food Science & Technology,2017,52(4):944-953.
[38] OZDEMIR C,ARSLANER A,OZDEMIR S,et al.The production of ice cream using Stevia as a sweetener[J].Journal of Food science and Technology,2015,52(11):7 545-7 548.
[39] ALIZADEH M,AZIZI-LALABADI M,KHEIROURI S.Impact of using stevia on physicochemical,sensory,rheology and glycemic index of soft ice cream[J].Food and Nutrition Sciences,2014,5(4):390-396.
[40] 徐泽琦, 周芳,李雪琪,等.甜菊糖苷低糖大豆发酵酸奶的工艺研究[J].农产品加工,2019(20):29-32.
XU Z Q,ZHOU F,LI X Q,et al.Study on the technology of low sugar soybean yoghurt fermentation with Stevia glycoside[J].Farm Products Processing,2019 (20):29-32
[41] DE OLIVEIRA B H,PACKER J F,CHIMLLI M,et al.Enzymatic modification of stevioside by cell-free extract of Gibberella fujikuroi[J].Journal of Biotechnology,2007,131(1):92-96.
[42] 马迎迎,陈育如,张伟娜,等.棘孢曲霉转化甜菊糖为甜菊醇及纯化莱鲍迪苷A[J].微生物学报,2014,54(1):62-68.
MA Y Y,CHEN Y R,ZHANG W N,et al.Biological conversion of stevioside to steviol by Aspergillus aculeatus and the purification of rebaudioside A[J].Acta Microbiologica Sinica,2014,54(1):62-68.