非酶褐变反应是没有酶参与的褐变反应,广泛存在于食品的热处理和贮存过程,可赋予食物特殊的风味,加深食物的颜色,对食品品质的评价有非常重要的影响。非酶褐变反应主要包括Maillard反应[1-2]、焦糖化反应和L-抗坏血酸(L-ascorbic acid, ASA)非酶褐变。其中Maillard反应主要是还原糖与氨基酸、蛋白质之间的反应,其本质是羰基-氨基发生一系列的复杂反应。焦糖化反应是糖类化合物(尤其是单糖)在无水条件下加热或用稀酸溶液处理,通过脱水、缩合等多步反应最终生成褐色物质的反应[3]。L-抗坏血酸又称维生素C,具有隐性羰基及类糖结构,它不仅自身可以发生非酶褐变,还可以与氨基酸、蛋白质发生Maillard反应[4-5],同时L-抗坏血酸还可作为天然抗氧化剂或添加剂应用于食品的加工生产过程。L-抗 坏血酸的降解可为食物带来特别的风味与色泽,但如果反应条件不当,也会产生一些有害物质,危害人类健康。
研究基于L-抗坏血酸的非酶褐变反应,可以更好且有效地把控食品品质,对食品的生产加工及贮存有非常重要的指导意义。本文围绕L-抗坏血酸非酶褐变过程进行了综述,主要从其自降解过程的特点、与氨基酸Maillard反应生成的风味物质、褐变过程和反应动力学特征等方面进行了叙述。本文旨在为食品工业中基于L-抗坏血酸的非酶褐变研究提供参考。
1 L-抗坏血酸自降解非酶褐变反应
食品加工或贮存过程,L-抗坏血酸的降解可分为有氧降解和无氧降解。在现实情况中,这两种降解途径可能同时存在。
1.1 L-抗坏血酸无氧降解
HUELIN[6]研究了L-抗坏血酸在不同pH水溶液中降解生成二氧化碳的含量;FINHOLT等[7]研究了L-抗坏血酸在不同pH环境下的无氧降解速率;KURATA 等[8]提出了L-抗坏血酸在酸性环境下降解生成糠醛的反应机理;SMOOT等[9]在研究葡萄柚汁中L-抗坏血酸的浓度变化时,发现在无氧条件下,L-抗坏血酸基本不会生成脱氢抗坏血酸,而是逐步降解生成糠醛;何平等[10]研究了L-抗坏血酸在注射液中的降解;VERNIN等[11]研究发现,L-抗坏血酸在无溶剂条件下加热到300 ℃或在丙二醇中加热到180 ℃,最终会降解生成糠醛。
L-抗坏血酸的无氧降解主要经过水解、脱羧、脱水和成环等步骤,其主要机理如图1所示[8,10-12]。
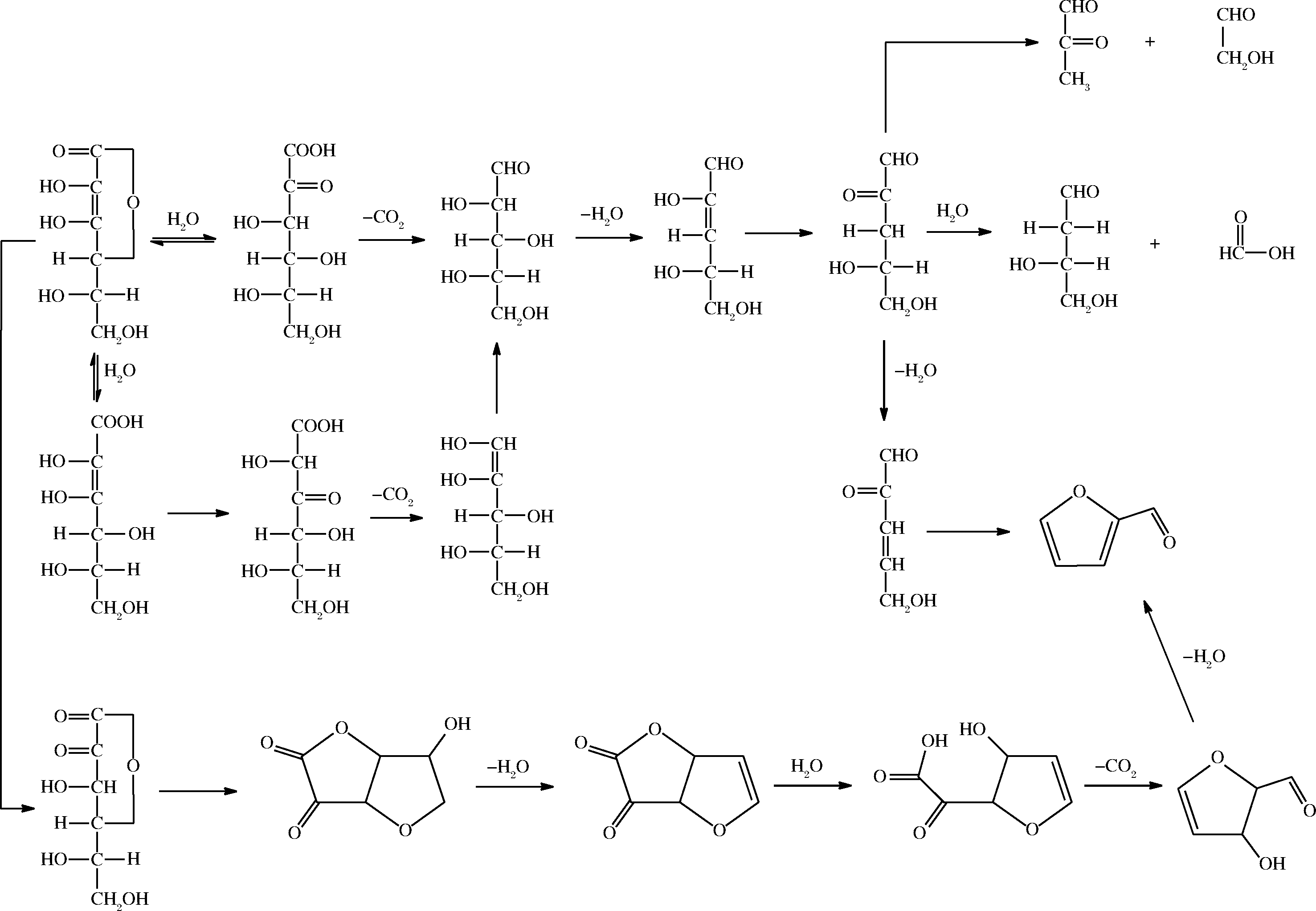
图1 L-抗坏血酸的无氧降解
Fig.1 Non-oxidative degradation of ASA
在无氧情况下,L-抗坏血酸首先经过水解、脱羧形成戊糖,然后戊糖进一步脱水、烯醇互变生成二羰基化合物,高活性的二羰基化合物在不同的反应条件下,降解生成小分子物质或环化生成糠醛。
1.2 L-抗坏血酸有氧降解
文献报道[13-15],在有氧条件下,L-抗坏血酸首先氧化生成脱氢抗坏血酸,然后经水解开环生成2,3-二酮-L-古洛酸,其反应路径如图2所示。
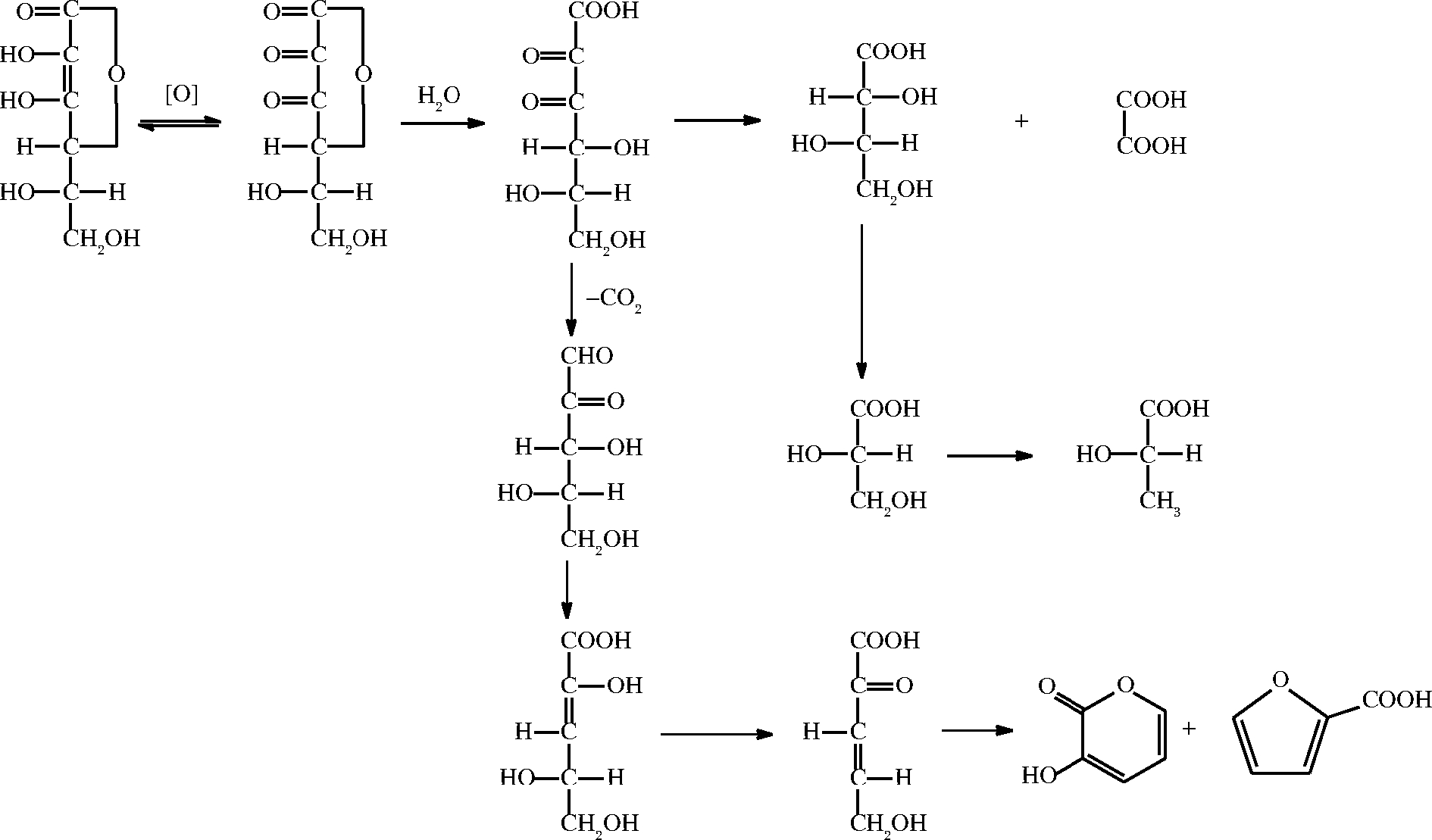
图2 L-抗坏血酸的有氧降解
Fig.2 Oxidative degradation of ASA
早期人们研究发现,L-抗坏血酸在中性和碱性条件下降解的最终产物为草酸、乳酸等有机酸[13]。KIMOTO 等[14]对脱氢抗坏血酸的降解产物进行了分析,发现其降解产物包含2-糠酸、3-羟基-2-吡喃酮、5-甲基-3,4-二羟基戊酮等;SOLOMON等[16]研究氧气对L-抗坏血酸降解的影响发现溶解氧对脱氢抗坏血酸的形成有着显著影响;SAWAMURA等[17]、DEUTSCH[18]研究发现脱氢抗坏血酸和2,3-二酮-L-古洛酸是其降解中间物质,这些中间产物会进一步反应生成小分子;YUAN等[15]用HPLC检测了L-抗坏血酸在酸性条件下的降解产物。
1.3 L-抗坏血酸降解动力学研究
关于L-抗坏血酸的动力学研究,学者们一般认为L-抗坏血酸在溶液中首先电离出质子,然后再降解生成各种无色活性中间体,最后各种高活性物质相互缩合生成褐色大分子。不同反应条件下L-抗坏血酸的自降解动力学特征见表1。
表1 不同条件下L-抗坏血酸的自降解动力学
Table 1 The self-degradation kinetics of ASA under different conditions
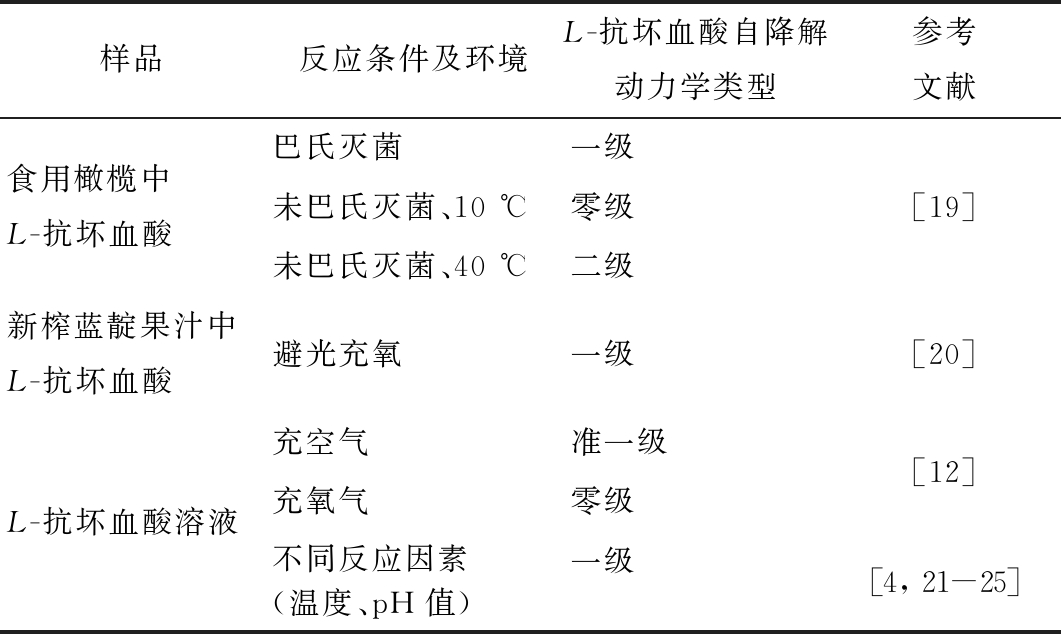
样品反应条件及环境L-抗坏血酸自降解动力学类型参考文献食用橄榄中L-抗坏血酸巴氏灭菌未巴氏灭菌、10 ℃未巴氏灭菌、40 ℃一级零级二级[19]新榨蓝靛果汁中L-抗坏血酸避光充氧一级[20]L-抗坏血酸溶液充空气充氧气不同反应因素(温度、pH值)准一级零级一级[12][4, 21-25]
MONTA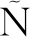 O等[19]研究发现经巴氏灭菌的食用橄榄中L-抗坏血酸的降解动力学符合一级动力学特征;而未经过巴氏灭菌处理的产品,在不同温度下有不同动力学特征。舒晓明等[12]研究了在空气和氧气条件下L-抗坏血酸降解动力学行为。郭庆启等[20]研究了新榨蓝靛果汁里L-抗坏血酸的降解动力学特征,发现在避光充氮时,其降解符合一级动力学特征。GRUDIC等[21]使用循环伏安法研究了L-抗坏血酸的降解动力学,发现其降解符合准一级动力学特征。李亚等[4,22]研究了不同反应参数对L-抗坏血酸降解和生成的影响。此后,林杨栋等[23]、余科等[24-25]分别研究了中性、碱性条件下L-抗坏血酸自降解动力学行为,并提出了L-抗坏血酸自降解的动力学方程。
O等[19]研究发现经巴氏灭菌的食用橄榄中L-抗坏血酸的降解动力学符合一级动力学特征;而未经过巴氏灭菌处理的产品,在不同温度下有不同动力学特征。舒晓明等[12]研究了在空气和氧气条件下L-抗坏血酸降解动力学行为。郭庆启等[20]研究了新榨蓝靛果汁里L-抗坏血酸的降解动力学特征,发现在避光充氮时,其降解符合一级动力学特征。GRUDIC等[21]使用循环伏安法研究了L-抗坏血酸的降解动力学,发现其降解符合准一级动力学特征。李亚等[4,22]研究了不同反应参数对L-抗坏血酸降解和生成的影响。此后,林杨栋等[23]、余科等[24-25]分别研究了中性、碱性条件下L-抗坏血酸自降解动力学行为,并提出了L-抗坏血酸自降解的动力学方程。
2 L-抗坏血酸/氨基酸Maillard反应
L-抗坏血酸因为具有潜在的羰基组分且与人们生活息息相关,因此近些年来,研究基于L-抗坏血酸的Maillard反应成为了另一研究热点。
2.1 L-抗坏血酸与氨基酸非酶褐变
L-抗坏血酸与氨基酸发生Maillard反应,反应底物首先会发生裂解生成小分子化合物,这些小分子化合物没有颜色但具有很高的反应活性。这些高活性化合物易与其他小分子醛酮或含氮、硫化合物发生反应,生成挥发性物质,而这些挥发性物质进一步反应生成褐色大分子化合物。
2.1.1 无色中间体的生成
Maillard反应的前期反应会生成一些含共轭结构的小分子化合物,这些化合物在紫外区294 nm处有特殊吸收峰[26]。对于无色中间体的检测,大多采用紫外-可见光分光光度法进行分析检测。无色中间体的系列研究如表2所示。
表2 L-抗坏血酸/氨基酸Maillard反应无色中间体的生成
Table 2 The formation of un-colorful intermediate products from Maillard reaction between ASA and amino acid

底物研究内容结论参考文献L-脯氨酸/丙氨酸+L-抗坏血酸pH对无色中间体生成的影响pH为5~6时,无色中间体吸光度值最高[27-28]L-谷氨酸/天冬氨酸+L-抗坏血酸底物比例对无色中间体生成的影响L-抗坏血酸含量对无色中间体生成影响较大[5,29-30]L-半胱氨酸+L-抗坏血酸时间与温度对无色中间体生成的影响延长时间、升高温度均能使无色中间体增加[31]甘氨酸+L-抗坏血酸pH与温度对无色中间体生成的影响pH为4.5,反应温度为130~150 ℃有利于无色中间体生成[32]L-苏氨酸/色氨酸+ L-抗坏血酸时间与温度对无色中间体生成的影响相较于其他氨基酸,L-苏氨酸与L-色氨酸对反应时间和温度更敏感[32]
邓启辉等[27-28]研究了不同pH条件下,L-抗坏血酸与L-脯氨酸、L-丙氨酸的反应,发现当体系溶液pH为5~6时,无色中间体的吸光度值达到最大;ZHOU等[5,29-30]研究了不同质量浓度的L-抗坏血酸/L-谷氨酸、L-天冬氨酸在碱性环境中的反应,发现L-抗坏血酸浓度的影响更大;唐乐攀[31]研究了L-抗 坏血酸与L-半胱氨酸的反应;李亚[32]研究了不同pH值下(4.5、 6.8、8.0、9.5)L-抗坏血酸与甘氨酸的反应,发现不同pH值对褐变影响较大,之后她又研究了L-抗坏血酸与L-苏氨酸、L-色氨酸以及3种碱性氨基酸的反应;余科[33]用过量浓度法研究了L-抗坏血酸与甘氨酸的反应。
2.1.2 褐色物质的生成
褐色物质的生成主要发生在L-抗坏血酸/氨基酸Maillard反应后期,其产物也是采用紫外-可见光分光光度法进行检测。褐色物质的系列研究如表3所示。
表3 L-抗坏血酸/氨基酸Maillard反应褐色物质的生成
Table 3 The formation of browning products from Maillard reaction between ASA and amino acid
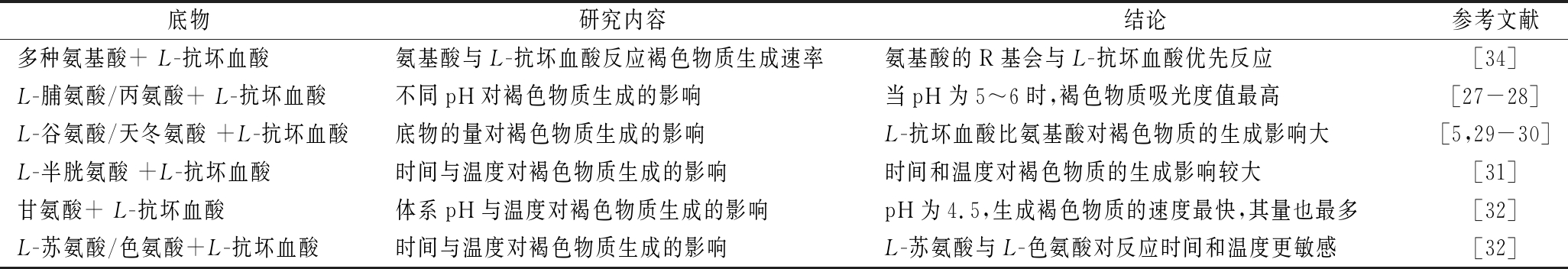
底物研究内容结论参考文献多种氨基酸+ L-抗坏血酸氨基酸与L-抗坏血酸反应褐色物质生成速率氨基酸的R基会与L-抗坏血酸优先反应[34]L-脯氨酸/丙氨酸+ L-抗坏血酸不同pH对褐色物质生成的影响当pH为5~6时,褐色物质吸光度值最高[27-28]L-谷氨酸/天冬氨酸 +L-抗坏血酸底物的量对褐色物质生成的影响L-抗坏血酸比氨基酸对褐色物质的生成影响大[5,29-30]L-半胱氨酸 +L-抗坏血酸时间与温度对褐色物质生成的影响时间和温度对褐色物质的生成影响较大[31]甘氨酸+ L-抗坏血酸体系pH与温度对褐色物质生成的影响pH为4.5,生成褐色物质的速度最快,其量也最多[32]L-苏氨酸/色氨酸+L-抗坏血酸时间与温度对褐色物质生成的影响L-苏氨酸与L-色氨酸对反应时间和温度更敏感[32]
李任强等[34]研究了L-抗坏血酸与碱性氨基酸、芳香族氨基酸的Maillard反应;邓启辉等[27-28]研究发现当体系pH为5~6时,褐色物质有最大吸光度值;较高浓度的L-抗坏血酸与L-谷氨酸、L-天冬氨酸在碱性条件下更有利于褐色物质的生成[5,29-30];唐乐攀[31]的研究发现,L-抗坏血酸与L-半胱氨酸反应生成的褐色物质在较高温度时速率较大;李亚[32]发现L-抗坏血酸与甘氨酸在pH值为4.5时,生成褐色物质速率最快,同时她发现L-苏氨酸与L-色氨酸对反应温度和时间较为敏感;余科[33]的研究发现酸性环境更有利于褐色物质的生成。
2.2 L-抗坏血酸与氨基酸Maillard反应风味物质研究
关于L-抗坏血酸/氨基酸Mailalrd反应,一般认为在加热条件下,L-抗坏血酸首先降解生成乙醛、丙酮醛、丙酮醇、1,2-二羰基和1,3-二羰基等一系列小分子化合物[35-36],如图3所示。

图3 L-抗坏血酸的降解
Fig.3 The self-degradation reaction of ASA
对于L-抗坏血酸降解反应生成挥发性小分子化合物主要利用固相微萃取-气相色谱-质谱技术进行分析检测。这些小分子化合物反应活性高,与氨基酸降解生成的小分子物质(一般为—NH2)进一步反应生成挥发性物质。如与不含硫氨基酸反应主要生成吡嗪及吡嗪类衍生物;与含硫氨基酸反应生成的挥发性物质比较复杂,此时不仅有吡嗪及吡嗪类衍生物,还会有噻唑及噻唑类衍生物或噻吩类化合物生成。
2.2.1 L-抗坏血酸与不含硫氨基酸的Maillard反应
学者对L-抗坏血酸与不含硫氨基酸的Maillard反应路径研究如图4所示[36-37]。
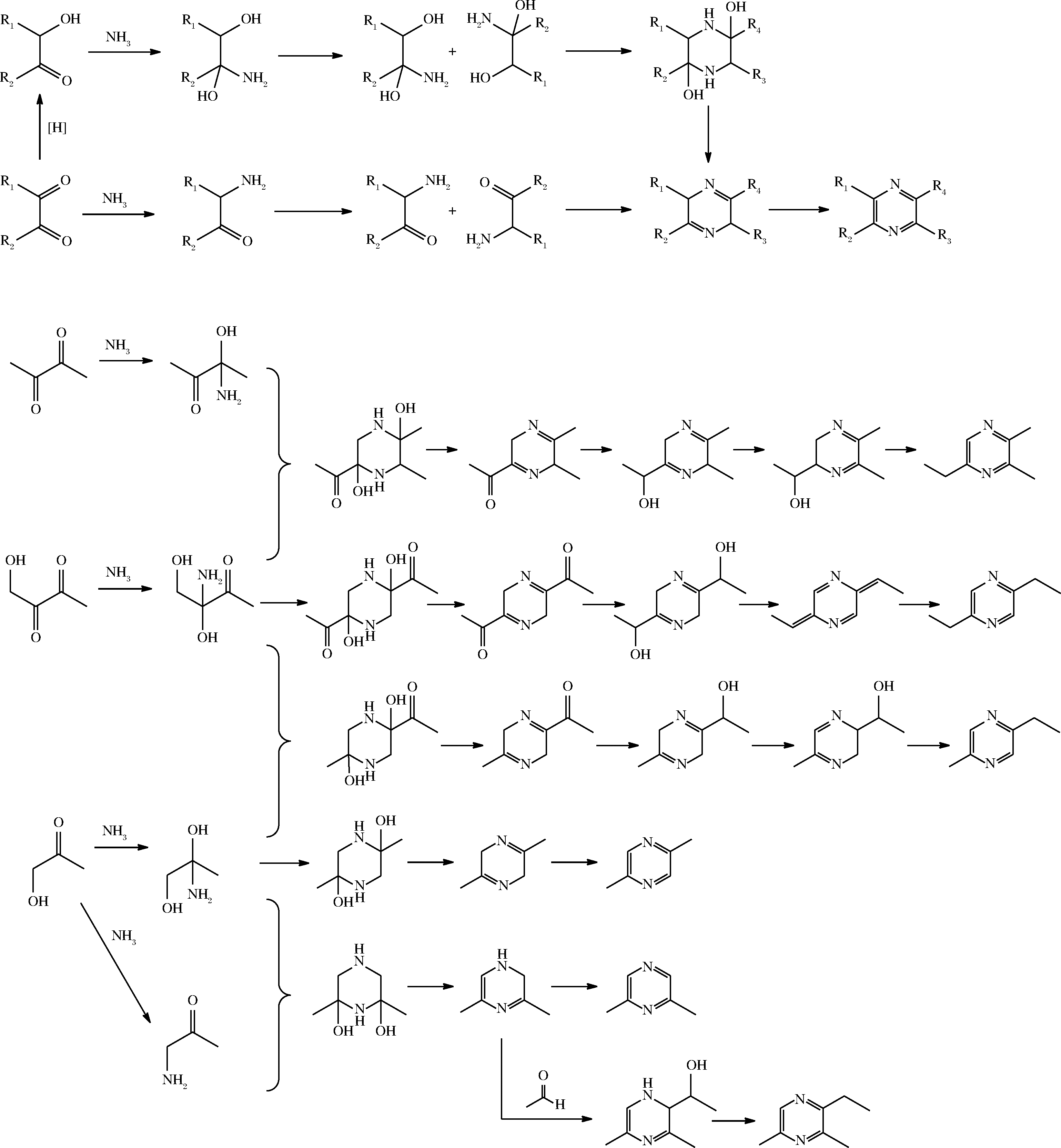
图4 L-抗坏血酸/氨基酸Maillard反应中吡嗪类化合物的形成
Fig.4 The formation of pyrazine from Maillard reaction between ASA and amino acid
ADAMS等[38]研究了L-抗坏血酸与多种氨基酸反应生成吡嗪的反应;YU等[39-40]对比研究了不同pH条件下L-抗坏血酸与L-丙氨酸的反应,还研究了L-抗坏血酸与L-丝氨酸、L-苏氨酸的反应,发现挥发性物质大多为烷基吡嗪,另外还有一些呋喃类和醛类化合物;TAN等[41]对比研究了L-抗坏血酸与L-谷氨酸、L-天冬氨酸Maillard反应,提出了吡嗪可能的生成机理,并用同位素标记法进行研究[36];李亚[32]发现溶液的pH值对挥发性物质种类与形成有显著影响;ZHOU等[29]报道过量的L-抗坏血酸会促进挥发性物质的生成。
2.2.2 L-抗坏血酸与含硫氨基酸Maillard反应
YU等[42]报道了L-抗坏血酸与L-半胱氨酸的反应,发现挥发性物质主要为噻吩、噻唑、吡嗪、噻吩并噻吩类及噻吩酮;LUO等[43]研究了尿素对L-抗坏血酸与L-蛋氨酸反应的影响,刘应煊等[44-45]研究了肌肽和尿素对L-抗坏血酸和L-半胱氨酸反应的影响;YU等[35]使用13C标记的L-抗坏血酸与L-半胱氨酸反应,提出了含硫香味化合物的形成机理;YANG等[46]研究了不同pH条件下L-抗坏血酸与L-蛋氨酸Maillard反应形成香味化合物的机制;谭志伟等[47]研究了水分含量对L-抗坏血酸与L-半胱氨酸Maillard反应形成挥发性物质的影响。L-抗坏血酸与含硫氨基酸(主要为L-半胱氨酸)Maillard反应,硫化合物的生成如图5所示。
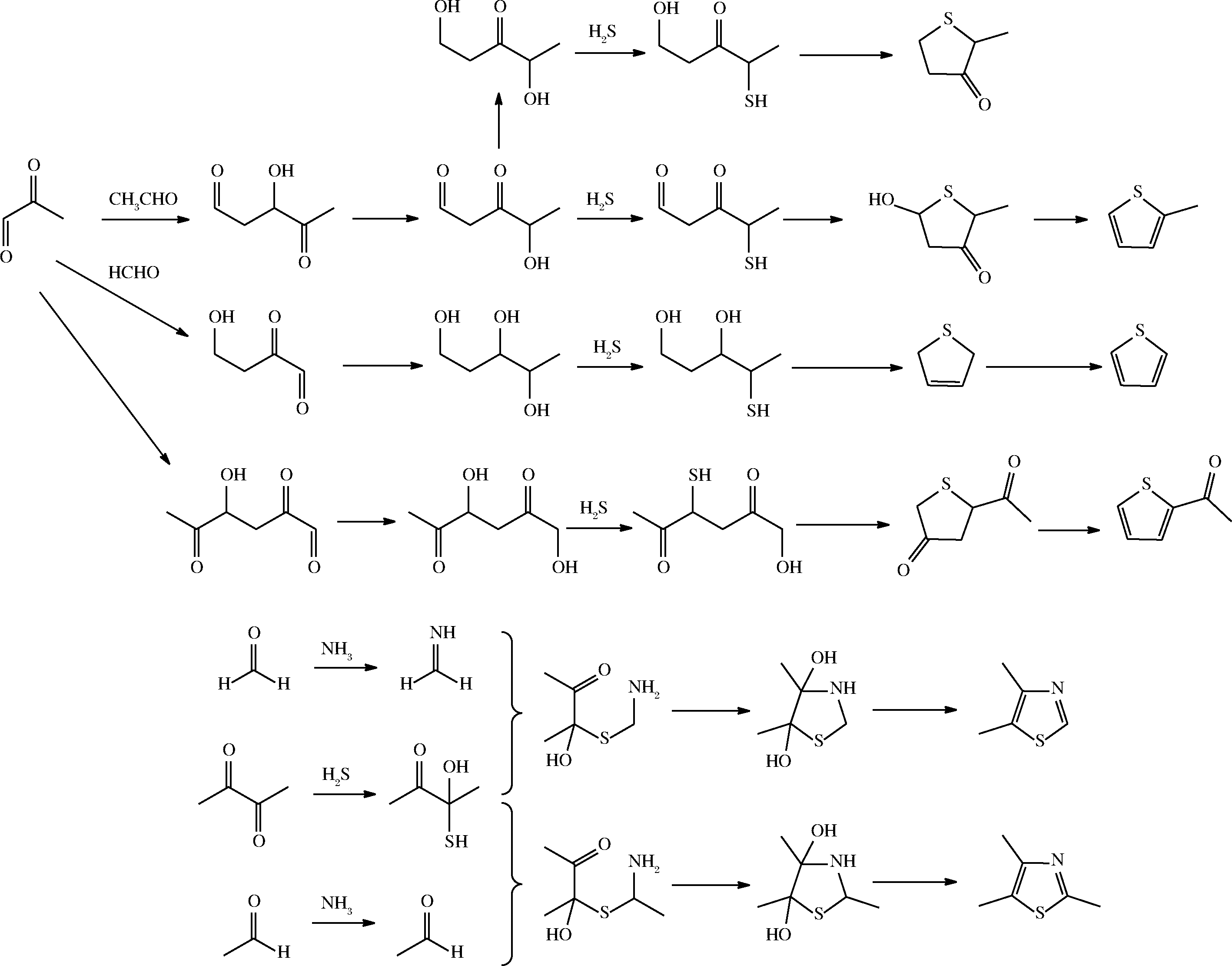
图5 L-抗坏血酸/氨基酸Maillard反应硫化物的形成
Fig.5 The formation of sulfide from Maillard reaction between ASA and amino acid
2.3 L-抗坏血酸与氨基酸反应动力学
L-抗坏血酸/氨基酸Maillard反应的动力学研究,可以让人们更好地预测与把控食品质量。研究者主要对底物消耗、无色中间体和褐色物质的生成动力学特征进行了研究。L-抗坏血酸/氨基酸Maillard反应动力学研究模型如图6所示。

图6 L-抗坏血酸/氨酸酸动力学模型
Fig.6 The kinetics model of Maillard reaction between ASA and amino acid
一般认为L-抗坏血酸和氨基酸经第一步降解分别生成中间产物,其中L-抗坏血酸的中间产物可以进一步反应生成无色中间体,而氨基酸的中间产物需要与L-抗坏血酸的中间产物共同反应生成无色中间体,这些无色中间体在反应的最后阶段发生一系列复杂反应,最终生成褐变产物。研究发现氨基酸自降解褐变较难发生,一般忽略不计。L-抗坏血酸/氨基酸反应动力学研究如表4所示。
表4 L-抗坏血酸/氨基酸反应动力学
Table 4 The kinetics of reaction between ASA and amino acids

注:-表示未见报道
底物动力学特征L-抗坏血酸/氨基酸无色中间体褐色物质挥发性物质参考文献L-半胱氨酸+L-抗坏血酸一级/一级零级零级无固定等级[31]L-谷氨酸/天冬氨酸+L-抗坏血酸-/-零级零级无固定等级[30]甘氨酸+L-抗坏血酸-/一级零级零级无固定等级[32-33]
研究发现[30-32],底物的消耗大多遵循一级动力学特征,总体表现为二级动力学特征,而挥发性物质的生成动力学较为复杂,无色中间体和褐色物质的生成符合零级或准零级反应动力学特征。用经典过量浓度法研究基于L-抗坏血酸与氨基酸Maillard反应动力学表明[33,48-49],褐色物质的生成也符合零级动力学特征。同时研究发现L-抗坏血酸/氨基酸反应中褐色物质的生成需经过一个诱导期,在诱导期内主要生成物为无色中间体。
3 L-抗坏血酸非酶褐变反应产物对食品的影响
3.1 积极影响
非酶褐变反应,尤其是Maillard反应在食品中广泛存在,其产物具有抗氧化作用[27-28]。抗氧化物主要为类黑精,其为Maillard反应后期形成的一类结构复杂、聚合度不等的高分子混合物。研究表明,类黑精具有抗氧化、抗菌、抗肿瘤、降血糖等生物活性。除了抗氧化作用外,Maillard反应还可以改善食品的品质[50]。
3.2 消极影响
2002年,人们首次报道了丙烯酰胺的形成机理,认为在食品热加工过程中,食品中的天冬酰胺与羰基化合物发生Maillard反应也会形成丙烯酰胺。而丙烯酰胺具有潜在的致癌风险,同时具有神经毒性、基因毒性和生殖毒性。另外,在食品热加工过程中,伴随着Maillard反应的发生,会生成5-羟甲基糠醛。在一些动物模型和体外细胞模型实验中发现,5-羟甲基糠醛在体内和体外会转化成磺酸氧甲基糠醛和5-氯甲基糠醛,而这两种物质同时也具有强致癌性和基因毒性。Maillard反应的后期也会形成晚期糖基化末端产物,研究发现它们与糖尿病以及各种肾脏、血管疾病等都有着一定的联系。
关于L-抗坏血酸参与的Maillard反应,需待食品研究工作者做进一步的研究与探讨,完善Maillard反应在食品工业中的应用价值。
[1] HODGE J E.Dehydrated foods, chemistry of browning reactions in model systems[J].Journal of Agricultural and Food Chemistry, 1953, 1(15):928-943.
[2] MARTINS S I F S, JONGEN W M F, VAN BOEKEL M A J S.A review of Maillard reaction in food and implications to kinetic modelling[J].Trends in Food Science and Technology, 2000, 11(9-10):364-373.
[3] 汪东风, 孙丽平, 张莉.非酶褐变反应的研究进展[J].农产品加工(学刊), 2006(10):9-19.
WANG D F, SUN L P, ZHANG L.Reseach progress on nonenzymatic browning reaction[J].Academic Periodical of Farm Products Processing, 2006(10):9-19.
[4] 李亚, 杨艳, 余爱农, 等.L-抗坏血酸自降解过程的非酶褐变反应动态研究[J].食品工业科技, 2016, 37(4):117-122;127.
LI Y, YANG Y, YU A N, et al.The process and dynamic research for the non-enzymatic browning reaction about the self-degradation of L-ascorbic acid [J].Science and Technology of Food Industry, 2016, 37(4):117-122;127.
[5] 周永妍, 李亚, 余爱农.抗坏血酸/谷氨酸Maillard反应体系中间产物和褐变程度的研究[J].湖北民族学院学报(自然科学版), 2015, 33(1):80-84.
ZHOU Y Y, LI Y, YU A N.Study on the intermediate product and browning intensity from ascorbic acid /glutamic model system[J].Journal of Hubei University for Nationalities(Natural Science Edition), 2015, 33(1):80-84.
[6] HUELIN F E.Studies on the anaerobic decomposition of ascorbic acid[J].Journal of Food Science, 1953, 18(1-6):633-639.
[7] FINHOLT P, PAULSSEN R B, HIGUCHI T.Rate of anaerobic degradation of ascorbic acid in aqueous solution[J].Journal of Pharmaceutical Sciences, 1963, 52(10):948-954.
[8] KURATA T, SAKURAI Y.Degradation of L-ascorbic acid and mechanism of nonenzymic browning reaction[J].Agricultural and Biological Chemistry, 1967, 31(1):170-184.
[9] SMOOT J M, NAGY S.Effects of storage temperature and duration on total vitamin C content of canned single-strength grapefruit juice[J].Journal of Agricultural and Food Chemistry, 1980, 28(2):417-421.
[10] 何平, 殷恭宽.抗坏血酸在注射液中的降解途径[J].药学学报, 1986, 21(9):686-691.
HE P, YIN G K.The pathway for the anaerobic degradation of ascorbic acid in neutral injection[J].Acta Pharmaceutica Sinica, 1986, 21(9):686-691.
[11] VERNIN G, CHAKIB S, ROGACHEVA S M, et al.Thermal decomposition of ascorbic acid[J].Carbohydrate Research, 1997, 305(1):1-15.
[12] 舒晓明, 蒋露, 史焱, 等.抗氧剂L-抗坏血酸在水溶液中氧化反应速率常数的测定[J].华西药学杂志, 2005, 20(6):507-509.
SHU X M, JIANG L, SHI Y, et al.Determination of oxidation rate constant of antioxidant L-ascorbic acid in aqueous solution[J].West China Journal of Pharmaceutical Sciences, 2005, 20(6):507-509.
[13] KAMIYA S.Studies on the decomposition of L-ascorbic acid.Part XIV[J].Journal of the Agricultural Chemical Society of Japan, 1960, 34(1):13-16.
[14] KIMOTO E, TANAKA H, OHMOTO T, et al.Analysis of the transformation products of dehydro-L-ascorbic acid by ion-pairing high-performance liquid chromatography[J].Analytical Biochemistry, 1993, 214(1):38-44.
[15] YUAN J P, CHEN F.Degradation of ascorbic acid in aqueous solution[J].Journal of Agricultural and Food Chemistry, 1998, 46(12):5 078-5 082.
[16] SOLOMON O, SVANBERG U, SAHLSTRÖM A.Effect of oxygen and fluorescent light on the quality of orange juice during storage at 8 ℃[J].Food Chemistry, 1995, 53(4):363-368.
[17] SAWAMURA M, TAKEMOTO K, MATSUZAKI Y, et al.Identification of two degradation products from aqueous dehydroascorbic acid[J].Journal of Agricultural and Food Chemistry, 1994, 42(5):1 200-1 203.
[18] DEUTSCH J C.Ascorbic acid oxidation by hydrogen peroxide[J].Analytical Biochemistry, 1998, 255(1):1-7.
[19] MONTA O A, CASADO F J, REJANO L, et al.Degradation kinetics of the antioxidant additive ascorbic acid in packed table olives during storage at different temperatures[J].Journal of Agricultural and Food Chemistry, 2006, 54(6):2 206-2 210.
O A, CASADO F J, REJANO L, et al.Degradation kinetics of the antioxidant additive ascorbic acid in packed table olives during storage at different temperatures[J].Journal of Agricultural and Food Chemistry, 2006, 54(6):2 206-2 210.
[20] 郭庆启, 张娜, 王硕, 等.蓝靛果汁维生素C热降解动力学的研究[J].食品工业科技, 2012, 33(8):179-182.
GUO Q Q, ZHANG N, WANG S, et al.Thermal degradation dynamic of vitamin C in Ionicera edulis Turcz juice[J].Science and Technology of Food Industry, 2012, 33(8):179-182.
[21] GRUDIC V V, BLAGOJEVIC N Z, VUKASINOVIC-PESIC V L, et al.Kinetics of degradation of ascorbic acid by cyclic voltammetry method[J].Chemical Industry and Chemical Engineering Quarterly, 2015, 21(2):351-357.
[22] LI Y, YANG Y, YU A N, et al.Effects of reaction parameters on self-degradation of L-ascorbic acid and self-degradation kinetics[J].Food Science and Biotechnology, 2016, 25(1):97-104.
[23] 林扬栋, 余科, 汪汝浩, 等.碱性条件下L-抗坏血酸自降解的非酶褐变研究[J].化学研究与应用, 2017, 29(9):1 311-1 319.
LIN Y D, YU K, WANG R H, et al.The non-enzymatic brown of self-degradation reaction of L-ascorbic acid under alkanline conditions[J].Chemical Research and Application, 2017, 29(9):1 311-1 319.
[24] 余科, 张雅玲, 杨艳, 等.响应面法优化L-抗坏血酸降解的工艺条件[J].化学与生物工程, 2018, 35(11):26-30.
YU K, ZHANG Y L, YANG Y, et al.Optimization in degradation process of L-ascorbic acid by response surface methodology[J].Chemistry and Bioengineering, 2018, 35(11):26-30.
[25] 余科, 杨艳, 余爱农, 等.中、碱性条件下L-抗坏血酸自降解非酶褐变过程动力学研究[J].化学研究与应用, 2019, 31(6):1 013-1 020.
YU K, YANG Y, YU A N, et al.Self-degradation reaction kinetics of L-ascorbic acid under neutral and alkaline condition[J].Chemical Research and Application, 2019, 31(6):1 013-1 020.
[26] BILLAUD C, BRUN-MÉRIMÉE S, LOUARME L, et al.Effect of glutathione and Maillard reaction products prepared from glucose or fructose with glutathione on polyphenoloxidase from apple—I:Enzymatic browning and enzyme activity inhibition[J].Food Chemistry, 2004, 84(2):223-233.
[27] 邓启辉, 余爱农, 王发松, 等.pH对L-抗坏血酸与L-脯氨酸/ L-丙氨酸Maillard反应产物抗氧化活性的影响[J].精细化工, 2010, 27(10):1 016-1 019;1 034.
DENG Q H, YU A N, WANG F S, et al.Antioxidative activity of maillard reaction products from a L-ascorbic acid and L-proline/ L-alanine model system as influenced by pH[J].Fine Chemicals, 2010, 27(10):1 016-1 019;1 034.
[28] 邓启辉. L-抗坏血酸/ 氨基酸模式体系中Maillard反应产物的抗氧化活性研究[D].恩施:湖北民族学院, 2011.
DENG Q H.Study on Antioxidative activity of maillard reaction products from L-ascorbic acid/ amino acid model systems[D].Enshi:Hubei University for Nationalities, 2011.
[29] ZHOU Y Y, LI Y, YU A N.The effects of reactants ratios, reaction temperatures and times on Maillard reaction products of the L-ascorbic acid/ L-glutamic acid system[J].Food Science and Technology, 2016, 36(2):268-274.
[30] 周永妍. 抗坏血酸/ 酸性氨基酸体系非酶褐变反应研究[D].恩施:湖北民族学院, 2015.
ZHOU Y Y.Study on non-enzymic browning reaction from ascorbic acid/ acidic amino acid model system[D].Enshi:Hubei University for Nationalities, 2015.
[31] 唐乐攀. 抗坏血酸/ 半胱氨酸体系非酶褐变反应动力学研究[D].恩施:湖北民族学院, 2014.
TANG L P.Study on kinetics of nonenzymic browning reaction from ascorbic acid/ cysteine model system[D].Enshi:Hubei University for Nationalities, 2014.
[32] 李亚. L-抗坏血酸/ 中性和碱性氨基酸非酶褐变反应研究[D].恩施:湖北民族学院, 2016.
LI Y.Study on Non-enzymic browning reaction from L-ascorbic acid/ neutral and basic amino acid systems[D].Enshi:Hubei University for Nationalities, 2016.
[33] 余科. L-抗坏血酸/ 氨基酸非酶褐变反应的化学行为研究[D].恩施:湖北民族大学, 2019.
YU K.Chemical behavior of the non-enzymatic browning reaction in L-ascorbic acid/ amino acid systems[D].Enshi:Hubei Minzu University, 2019.
[34] 李任强, 江凤仪, 方玲, 等.维生素C与氨基酸褐变反应的研究[J].食品工业科技, 2002,23(11):32-34.
LI R Q, JIANG F Y, FANG L, et al.Study on the chemical reaction between vitamin C and amino acids[J].Science and Technology of Food Industry, 2002,23(11):32-34.
[35] YU A N, TAN Z W, WANG F S.Mechanism of formation of sulphur aroma compounds from L-ascorbic acid and L-cysteine during the Maillard reaction[J].Food Chemistry, 2012, 132(3):1 316-1 323.
[36] YU A N, TAN Z W, WANG F S.Mechanistic studies on the formation of pyrazines by Maillard reaction between L-ascorbic acid and L-glutamic acid[J].LWT-Food Science and Technology, 2013, 50(1):64-71.
[37] YU A N, TAN Z W, SHI B A.Influence of the pH on the formation of pyrazine compounds by the Maillard reaction of L-ascorbic acid with acidic, basic and neutral amino acids[J].Asia-Pacific Journal of Chemical Engineering, 2012, 7(3):455-462.
[38] ADAMS A, KIMPE N D.Formation of pyrazines from ascorbic acid and amino acids under dry-roasting conditions[J].Food Chemistry, 2009, 115(4):1 417-1 423.
[39] YU A N, DENG Q H.Volatiles from the Maillard reaction of L-ascorbic acid and L-alanine at different pHs[J].Food Science and Biotechnology, 2009, 18(6):1 495-1 499.
[40] YU A N, ZHANG A D.The effect of pH on the formation of aroma compounds produced by heating a model system containing L -ascorbic acid with L-threonine/ L-serine[J].Food Chemistry, 2010, 119(1):214-219.
[41] TAN Z W, YU A N.Volatiles from the Maillard reaction of L-ascorbic acid with L-glutamic acid/ L-aspartic acid at different reaction times and temperatures[J].Asia-Pacific Journal of Chemical Engineering, 2012, 7(4):563-571.
[42] YU A N, ZHANG A D.Aroma compounds generated from thermal reaction of L-ascorbic acid with L-cysteine[J].Food Chemistry, 2010, 121(4):1 060-1 065.
[43] LUO S, ZHOU H Y, WANG L, et al.Effects of urea on the formation of perfume compounds by ascorbic acid-methionine model reaction[J].Advanced Materials Research, 2011, 396-398:182-187.
[44] 刘应煊, 余爱农, 肖儒兰.肌肽对抗坏血酸-半胱氨酸模式反应形成香味化合物的影响[J].食品工业科技, 2012, 33(4):122-127;131.
LIU Y X, YU A N, XIAO R L.Effect of carnosine on aroma compounds generation from Maillard reaction of ascorbic acid and cysteine[J].Science and Technology of Food Industry, 2012, 33(4):122-127;131.
[45] 刘应煊, 余爱农.尿素对抗坏血酸-半胱氨酸模式反应形成香味化合物的影响[J].精细化工, 2011, 28(8):780-786;790.
LIU Y X, YU A N.Effect of urea on aroma compounds generated from maillard reaction of L-cysteine with L-ascorbic acid[J].Fine Chemicals, 2011, 28(8):780-786;790.
[46] YANG X Z, YU A N.Aroma compounds generated from L-ascorbic acid and L-methionine during the Maillard reaction[J].Advanced Materials Research, 2013, 781-784:1 811-1 817.
[47] 谭志伟, 余爱农, 刘应煊.水分含量对L-抗坏血酸/ L-半胱氨酸Maillard反应体系中挥发性产物的影响[J].食品科学, 2014, 35(10):132-138.
TAN Z W, YU A N, LIU Y X.Effect of water content on generation of volatile compounds from maillard reaction of L-ascorbic acid and L-cysteine[J].Food Science, 2014, 35(10):132-138.
[48] YANG Y, LI Y, FENG L, et al.The effects of reaction parameters on the non-enzymatic browning reaction between L-ascorbic acid and glycine[J].International Journal of Food Engineering, 2021, 17(1):49-56.
[49] YU A N, ZHOU Y Y, YANG Y N.Kinetics of browning and correlations between browning degree and pyrazine compounds in L -ascorbic acid/ acidic amino acid model systems[J].Food Chemistry, 2017, 221:1 678-1 684.
[50] 高维, 刘刚.抗坏血酸对蛋白基美拉德反应产物的性质影响[J].食品科技, 2016, 41(5):244-247.
GAO W, LIU G.Effect of ascorbic acid on properties of protein Maillard reaction products[J].Food Science and Technology, 2016, 41(5):244-247.