黄茶是我国特有的茶类,由绿茶演变而来。其初加工与绿茶相似,为杀青、闷黄、干燥3道基本工序。闷黄是黄茶加工特有的工序,也是影响黄茶品质的关键环节,对黄茶、黄汤、黄叶及醇厚鲜爽滋味品质的形成至关重要[1]。闷黄是指将杀青叶趁热堆积,使茶坯在湿热条件下发生热化学变化,使叶子转变为黄色,形成黄茶叶底黄,汤色黄,干茶也显黄亮的品质特征[2]。黄茶闷黄过程中,茶叶内部发生以非酶促湿热化学反应为主的一系列化学反应,叶内多酚类、多糖、蛋白质、叶绿素等发生氧化、裂解、水解等系列反应,形成较多的简单儿茶素、可溶性糖、游离氨基酸等品质成分和少量的茶黄素,叶绿素锐减,进而形成黄茶特有的品质特征[3]。已有研究表明,黄茶具有一定的营养和药理保健价值[4-6],受到越来越多消费者的青睐,黄茶产业日渐壮大。
黄茶制作技术要求高,闷黄程度难以掌控。目前,在大生产条件下对黄茶发酵的程度判断均以叶色、香气等感官因子作为评价指标,即依靠制茶人员的感官经验,而人的感官判断存在许多局限,对提高黄茶质量极为不利。茶叶中存在的多元氧化还原体系如醌酚氧化还原体系、抗坏血酸氧化还原体系等对茶叶品质形成影响极大[7]。LUXIMON-RAMMA等[8]发现生化成分的含量是决定茶叶品质的关键。电化学技术(包括电导率和氧化还原反应在内)已广泛用于水质分析、酿酒业、电位滴定等领域,目前在茶叶加工方面也有应用研究。肖纯等[9]和陈宗道等[10]的研究表明,红茶发酵过程中发酵叶的电导率和氧化还原电位与发酵质量有明确的应变关系,通过对发酵过程中电导率和氧化还原电位的测定可实现发酵程度的传感。张其生[11]通过研究发现红碎茶发酵过程中,发酵叶茶汤pH呈规律性下降趋势。但在黄茶闷黄过程中的研究鲜见报道,特别是对黄茶电化学参数与品质相关性的研究尚未见报道。本实验采用电化学技术结合感官审评和理化成分测定的方法,探究黄茶闷黄过程中闷黄叶茶汤的电化学参数(pH、电导率、氧化还原电位)、感官品质和主要理化成分的变化规律,在电化学参数测定中设置2个温度,即常温(冷泡)和冲泡温度(热泡),冷泡是反映闷黄叶本身的物质成分含量或物理化学性质,热泡是反映冲泡温度对闷黄叶物质成分含量或物理化学性质的影响。本研究对黄茶闷黄过程中电化学参数与品质的相关性进行分析,初步探讨黄茶闷黄适度的科学判断指标,为黄茶的加工提供更现实可靠的理论依据。
1 材料与方法
1.1 试验材料
制茶原料:2019年春夏季福鼎大白品种一芽二叶鲜叶,在我校教学茶厂和杨何茶厂开展实验。
1.2 仪器、设备与试剂
1.2.1 仪器与设备
6CCB-80/12型理条机,雅安市名山区山峰茶机厂;6CR-40型茶叶揉捻机,雅安市名山区山峰茶机厂;SPX-250生化恒温培养箱,上海申贤恒温设备厂;TASI-8601型红外测温仪,苏州特安斯电子有限公司;PHS-3B型酸度计,上海虹益仪器仪表有限公司;DDSJ-308A型电导率仪,上海精密科学仪器有限公司;BS-124S型微量电子分析天平,上海仪电分析仪器有限公司;DHG-9245A型鼓风式电热恒温干燥箱,上海齐欣科学仪器有限公司;UV-2300紫外-可见分光光度计,上海天美科学仪器有限公司;微波炉,美的集团;茶叶审评杯碗。
1.2.2 主要试剂
茚三酮、酒石酸钾钠、氧化亚锡、福林酚、硫酸亚铁、碱式乙酸铅、乙醇、蒽酮、硫酸、丙酮、乙醚、氯仿、正丁醇等试剂,均为分析纯。
1.3 实验方法
1.3.1 茶样制作与取样
1.3.1.1 黄茶制作方法
参照资料[12-13]与黄小茶加工工艺并结合预实验结果确定黄茶工艺流程和工艺参数。
表1 黄茶加工工艺流程及参数
Table 1 The processing process and parameters of yellow tea

工艺流程工艺参数鲜叶福鼎大白品种一芽二叶初展,5 kg摊放室温25~28 ℃,时间6 h杀青采用理条机杀青,260~270 ℃,时间5 min揉捻趁热揉捻5 min闷黄白纱布包裹,湿坯闷黄,叶温45 ℃,闷黄时间13 h干燥温度70 ℃,时间3 h,烘至足干
1.3.1.2 取样方法
从揉捻结束(闷黄0 h)开始第一次取样,编号为0, 然后每隔1 h 取样1次,编号为1~13,每次所取茶样马上分为Q、W 2份,Q样直接用于电化学参数的测定,W样按干燥工艺进行干燥,用于茶叶理化成分测定和感官审评。
1.3.2 闷黄叶电化学参数测定
由于闷黄过程中闷黄叶含水量会有轻微变化,为了统一质量,将所取用于测定电化学参数的闷黄叶进行微波快速干燥。
闷黄叶茶汤pH值测定[14]:称取2份闷黄叶各3.0 g,分别放入2个250 mL的锥形瓶,分别用150 mL的热水(100 ℃)和150 mL的冷水[室温(25±2) ℃]冲泡5 min,茶样冲泡后,用脱脂棉过滤茶渣,冷却至室温,并测定茶汤的pH值[15]。
闷黄叶茶汤电导率测定[14]:称取2份闷黄叶各3.0 g,分别放入2个250 mL的锥形瓶,分别用150 mL的热水(100 ℃)和150 mL的冷水[室温(25±2) ℃]冲泡5 min,茶样冲泡后,用脱脂棉过滤茶渣,冷却至室温,并测定茶汤的电导率。
闷黄叶茶汤氧化还原电位测定[14]:称取2份闷黄叶各3.0 g,分别放入2个250 mL的锥形瓶,分别用150 mL的热水(100 ℃)和150 mL的冷水[室温(25±2) ℃]冲泡5 min,茶样冲泡后,用脱脂棉过滤茶渣,冷却至室温,并测定茶汤的氧化还原电位。
1.3.3 理化成分测定方法
用120 ℃,1 h烘箱快速法测定茶叶含水量[16];用全量法测定水浸出物总量;茶多酚总量采用福林酚试剂比色法测定[17];用紫外光分光光度法测定咖啡碱含量[18-19];游离氨基酸含量采用茚三酮比色法测定[20];用系统分析法测定茶色素含量[20];用蒽酮-硫酸法测定可溶性糖含量[21-22];用香荚兰素比色法测定儿茶素含量[23]。
1.3.4 感官审评方法
参照茶叶感官审评国家标准GB/T 23776—2018《茶叶感官审评方法》[24]进行。由5名高级评茶师分别对茶样的外形、汤色、香气、滋味和叶底进行评分,满分为100分,以上5项并分别按照25%、10%、25%、30%、10%的比率计算感官审评总分。
1.3.5 数据分析及处理
采用Excel软件对试验数据进行统计,所有数据均以平均数±标准差表示,方差分析和相关性分析采用SPSS 22.0软件[25]完成,电化学参数与感官品质及电化学参数与理化成分的相关性分析均采用双变量相关分析方法。
2 结果与分析
2.1 黄茶闷黄过程中电化学参数随闷黄时间的变化规律
黄茶闷黄过程中,随着闷黄时间的延长,闷黄叶茶汤pH、电导率和氧化还原电位均发生了不同程度的变化,结果如图1所示。
由图1可知,随着闷黄时间的延长,闷黄叶茶汤冷泡和热泡pH均呈现降低的变化趋势,推测原因可能是闷黄过程中有机酸的积累使pH降低;其中冷泡pH在闷黄0~4 h阶段快速降低,4 h后降低趋势减缓;热泡pH在闷黄0~2 h阶段快速降低,2 h后降低趋势减缓;推测其原因可能是由于热泡过程中茶叶中的物质浸出的速度比冷泡快。

a-闷黄叶冷泡茶汤pH;b-闷黄叶热泡茶汤pH;c-闷黄叶冷泡茶汤电导率;d-闷黄叶热泡茶汤电导率;e-闷黄叶冷泡茶汤氧化还原电位;f-闷黄叶热泡茶汤氧化还原电位
图1 黄茶闷黄过程中闷黄叶电化学参数的动态变化
Fig.1 The dynamic changes of the electrochemical parameters of yellow tea during yellowing process
黄茶闷黄过程中,闷黄叶茶汤电导率的变化波动较多,且无明显变化规律。根据电导原理,电导率变化主要取决于物质中电解质带电分子的多少和活度。茶叶内含物根据其电化学性质可分为三类:(1)电解质,如氨基酸和无机盐等;(2)分子带电荷的胶体物质,如蛋白质等;(3)非电解质,即既不显示胶体性质也不具电解质性质的物质[9]。黄茶闷黄过程中,不同阶段发生不同的反应,一方面随着多酚类物质的氧化,电导率上升,另一方面,氧化后的多酚类物质进一步与氨基酸等物质缩合,使电导率下降。经比较后发现,同一闷黄时间下,冷泡电导率值明显低于热泡电导率;推测其原因可能是由于热水冲泡的闷黄叶浸出物质比冷水冲泡的闷黄叶浸出物质量多且种类更为丰富。
氧化还原电位是溶液中所有物质氧化还原性的宏观体现,氧化还原电位为正表示溶液显氧化性,为负表示溶液显还原性,氧化还原电位越高表示氧化性越强,越低表示还原性越强[26]。黄茶闷黄过程中,闷黄叶茶汤冷泡氧化还原电位和热泡氧化还原电位随着闷黄时间的延长均呈现升高的变化趋势,其中冷泡氧化还原电位在闷黄0~2 h阶段快速升高,2 h后升高趋势减缓;热泡氧化还原电位在闷黄0~2 h和5~6 h阶段升高幅度较大,其他阶段升高趋势较缓;推测其原因可能是闷黄前期湿热作用使多酚类等物质发生氧化、裂解、水解等系列反应进程较快,氧化还原电位升高幅度较大。
2.2 黄茶闷黄过程中主要理化成分的变化规律
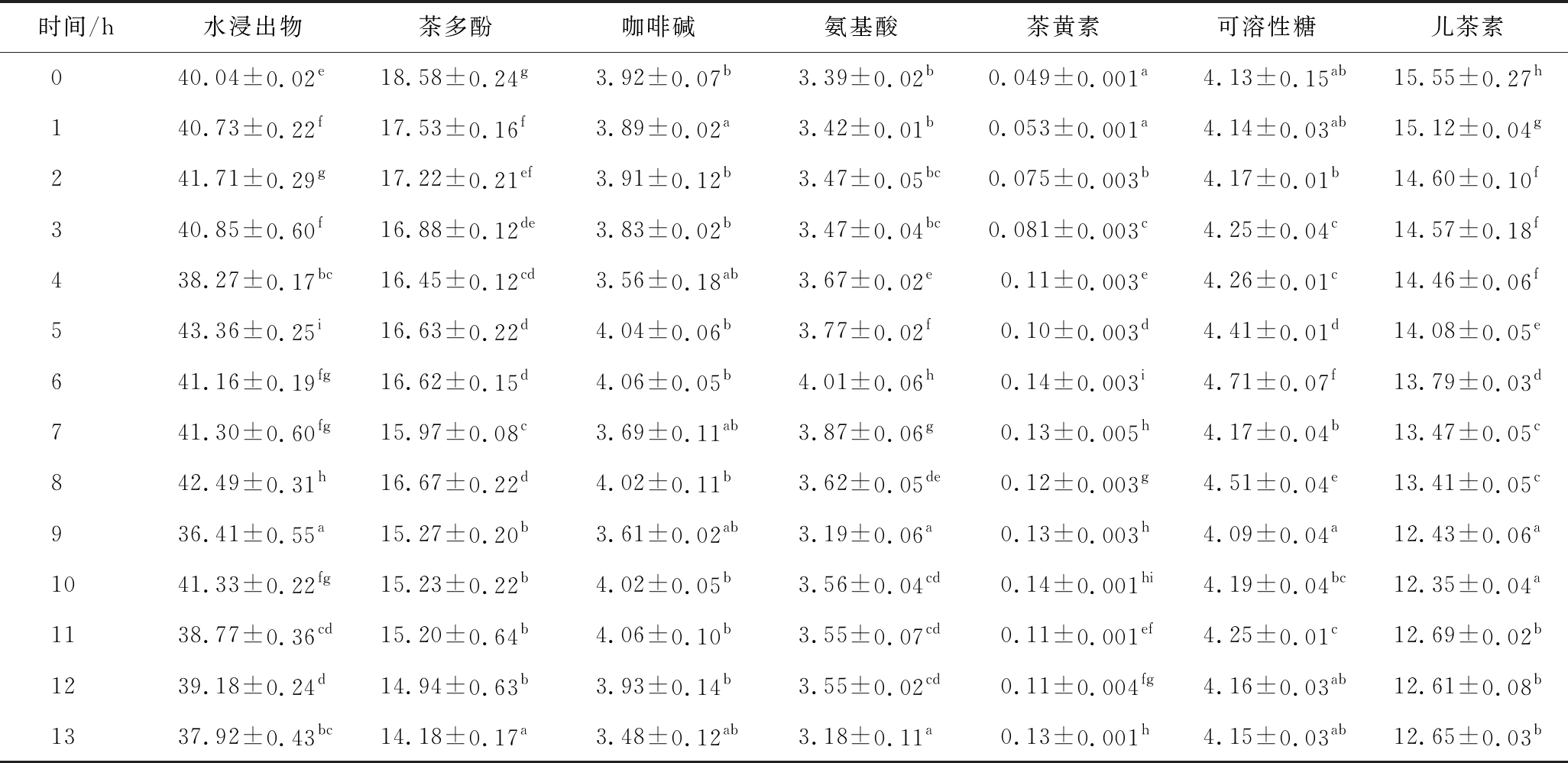
黄茶闷黄过程中,黄茶内含物质发生不同程度的变化,主要理化成分随闷黄时间的变化如表2所示。由表2可知,闷黄过程中茶多酚和儿茶素的含量随闷黄时间的延长呈下降的趋势,茶多酚是形成茶汤滋味的重要成分,在闷黄过程中茶多酚总量降低,同时也降低了茶汤的苦味和涩味,这是黄茶有别于绿茶的重要原因之一。氨基酸、茶黄素和可溶性糖含量呈现先增加后减少的趋势,且均在闷黄6 h时含量最高,在强烈的湿热作用下,蛋白质水解成游离氨基酸,后期氨基酸发生氧化含量减少;茶多酚自然氧化为茶黄素;多糖类物质在湿热作用下发生转化,为茶汤品质提供甜味和醇厚度。咖啡碱作为茶汤苦味的贡献物质,含量变化较小,但波动较多;水浸出物的变化也波动较多,无明显变化规律。
表2 主要理化成分检测结果 单位:%
Table 2 Main physical and chemical components determination record
注:同一竖列不同字母表示在P<0.05水平有显著差异
时间/h水浸出物茶多酚咖啡碱氨基酸茶黄素可溶性糖儿茶素040.04±0.02e18.58±0.24g3.92±0.07b3.39±0.02b0.049±0.001a4.13±0.15ab15.55±0.27h140.73±0.22f17.53±0.16f3.89±0.02a3.42±0.01b0.053±0.001a4.14±0.03ab15.12±0.04g241.71±0.29g17.22±0.21ef3.91±0.12b3.47±0.05bc0.075±0.003b4.17±0.01b14.60±0.10f340.85±0.60f16.88±0.12de3.83±0.02b3.47±0.04bc0.081±0.003c4.25±0.04c14.57±0.18f438.27±0.17bc16.45±0.12cd3.56±0.18ab3.67±0.02e0.11±0.003e4.26±0.01c14.46±0.06f543.36±0.25i16.63±0.22d4.04±0.06b3.77±0.02f0.10±0.003d4.41±0.01d14.08±0.05e641.16±0.19fg16.62±0.15d4.06±0.05b4.01±0.06h0.14±0.003i4.71±0.07f13.79±0.03d741.30±0.60fg15.97±0.08c3.69±0.11ab3.87±0.06g0.13±0.005h4.17±0.04b13.47±0.05c842.49±0.31h16.67±0.22d4.02±0.11b3.62±0.05de0.12±0.003g4.51±0.04e13.41±0.05c936.41±0.55a15.27±0.20b3.61±0.02ab3.19±0.06a0.13±0.003h4.09±0.04a12.43±0.06a1041.33±0.22fg15.23±0.22b4.02±0.05b3.56±0.04cd0.14±0.001hi4.19±0.04bc12.35±0.04a1138.77±0.36cd15.20±0.64b4.06±0.10b3.55±0.07cd0.11±0.001ef4.25±0.01c12.69±0.02b1239.18±0.24d14.94±0.63b3.93±0.14b3.55±0.02cd0.11±0.004fg4.16±0.03ab12.61±0.08b1337.92±0.43bc14.18±0.17a3.48±0.12ab3.18±0.11a0.13±0.001h4.15±0.03ab12.65±0.03b
2.3 黄茶闷黄过程中感官品质的变化规律
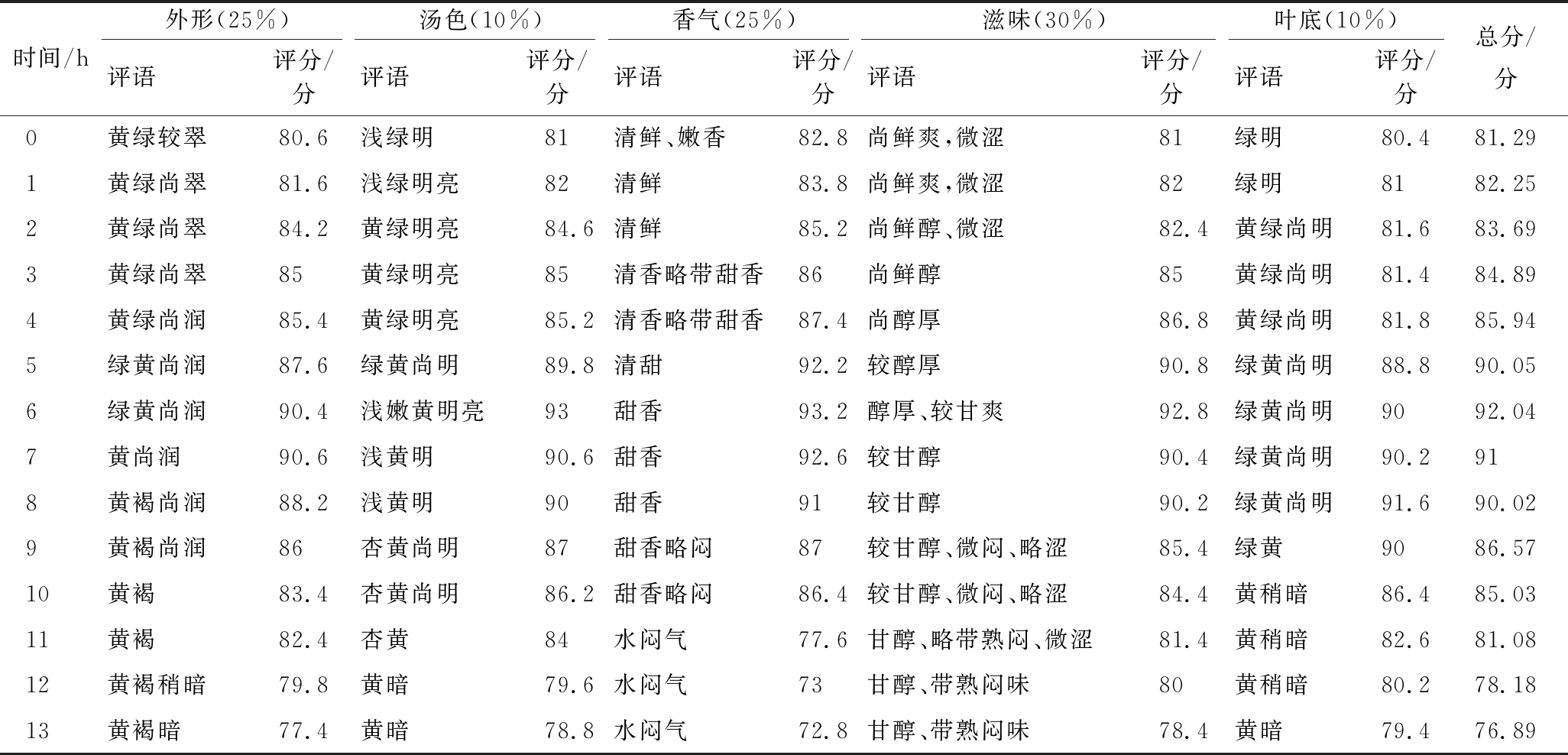
闷黄是形成黄茶黄汤黄叶及醇厚鲜爽滋味品质的关键工序[1],表3显示了黄茶闷黄过程茶叶样品感官审评结果。由表3可以看出,茶叶样品的感官评价得分随着闷黄时间的延长而逐渐增加,当闷黄时间为6 h时达到最高点,此时黄茶基本达到“三黄”的品质特征,随着闷黄时间的延长,感官审评得分在6 h后逐渐下降,9 h后,黄茶干茶和叶底色泽开始变暗,香气带水闷味,滋味变涩或带熟闷味;至闷黄13 h,黄茶干茶和叶底色泽呈现黄褐色且发暗,滋味带严重的熟闷味。以上结果表明,黄茶适宜的闷黄时间是6 h。
表3 闷黄叶闷黄过程中感官品质变化
Table 3 The sensory quality changes of yellowing leaves during yellowing process
时间/h外形(25%)汤色(10%)香气(25%)滋味(30%)叶底(10%)评语 评分/分评语评分/分评语评分/分评语评分/分评语评分/分总分/分0黄绿较翠80.6浅绿明81清鲜、嫩香82.8尚鲜爽,微涩81绿明80.481.291黄绿尚翠81.6浅绿明亮82清鲜83.8尚鲜爽,微涩82绿明8182.252黄绿尚翠84.2黄绿明亮84.6清鲜85.2尚鲜醇、微涩82.4黄绿尚明81.683.693黄绿尚翠85黄绿明亮85清香略带甜香86尚鲜醇85黄绿尚明81.484.894黄绿尚润85.4黄绿明亮85.2清香略带甜香87.4尚醇厚86.8黄绿尚明81.885.945绿黄尚润87.6绿黄尚明89.8清甜92.2较醇厚90.8绿黄尚明88.890.056绿黄尚润90.4浅嫩黄明亮93甜香93.2醇厚、较甘爽92.8绿黄尚明9092.047黄尚润90.6浅黄明90.6甜香92.6较甘醇90.4绿黄尚明90.2918黄褐尚润88.2浅黄明90甜香91较甘醇90.2绿黄尚明91.690.029黄褐尚润86杏黄尚明87甜香略闷87较甘醇、微闷、略涩85.4绿黄9086.5710黄褐83.4杏黄尚明86.2甜香略闷86.4较甘醇、微闷、略涩84.4黄稍暗86.485.0311黄褐82.4杏黄84水闷气77.6甘醇、略带熟闷、微涩81.4黄稍暗82.681.0812黄褐稍暗79.8黄暗79.6水闷气73甘醇、带熟闷味80黄稍暗80.278.1813黄褐暗77.4黄暗78.8水闷气72.8甘醇、带熟闷味78.4黄暗79.476.89
2.4 黄茶闷黄过程中电化学参数与品质的相关性分析
2.4.1 黄茶闷黄过程中电化学参数与感官品质的相关性分析
综合感官品质和理化成分发现,黄茶闷黄合适的时间是6 h。为了更准确地探究电化学变化与感官品质的相关关系,本实验选取闷黄前7 h的闷黄叶茶汤电化学参数与感官审评各因子得分和审评总分进行相关性分析,分析结果如表4所示。
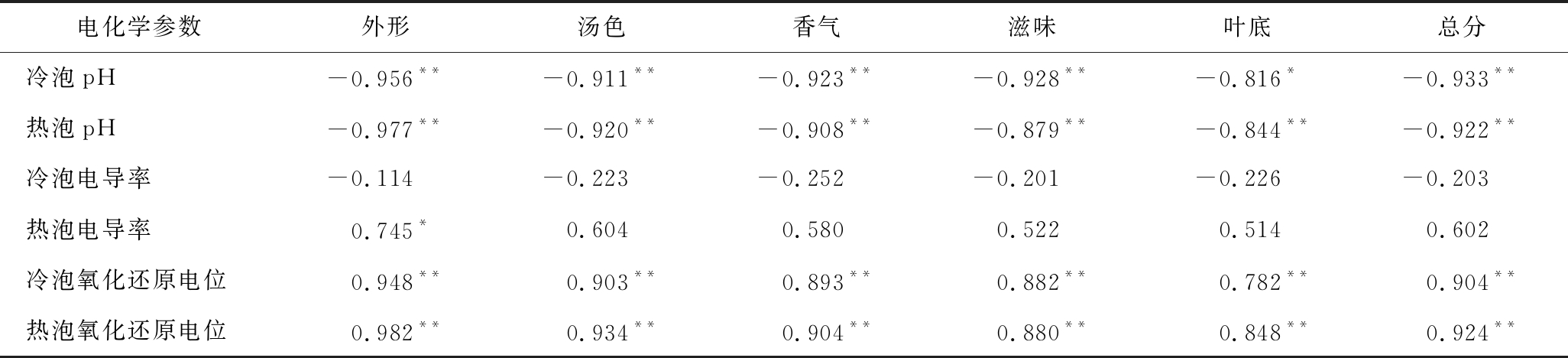
由表4可知,闷黄叶茶汤pH与各感官因子和总分之间呈极显著负相关(P<0.01),其中冷泡pH与外形、汤色、香气、滋味、叶底、感官审评总分得分的相关系数分别达到-0.956、-0.911、-0.923、-0.928、-0.816、 -0.933;热泡pH与外形、汤色、香气、滋味、叶底、感官审评总分得分的相关系数分别达到-0.977、-0.920、-0.908、-0.879、-0.844、-0.922;推断茶汤pH会影响到茶叶的外形、汤色、香气、滋味和叶底,在一定条件下,茶汤pH值越低,茶叶感官品质越好。
表4 电化学参数与感官品质的相关性分析
Table 4 Correlation analysis between electrochemical parameters and sensory quality
注:*表示差异显著(P<0.05),**表示差异极显著(P<0.01)
电化学参数外形汤色香气滋味叶底总分冷泡pH-0.956**-0.911**-0.923**-0.928**-0.816*-0.933**热泡pH-0.977**-0.920**-0.908**-0.879**-0.844**-0.922**冷泡电导率-0.114-0.223-0.252-0.201-0.226-0.203热泡电导率0.745*0.6040.5800.5220.5140.602冷泡氧化还原电位0.948**0.903**0.893**0.882**0.782**0.904**热泡氧化还原电位0.982**0.934**0.904**0.880**0.848**0.924**
闷黄叶茶汤氧化还原电位与各感官因子和总分之间呈极显著正相关(P<0.01),其中冷泡氧化还原电位与外形、汤色、香气、滋味、叶底、感官审评总分得分的相关系数分别达到0.948、0.903、0.893、0.882、0.782、0.904;热泡氧化还原电位与外形、汤色、香气、滋味、叶底、感官审评总分得分的相关系数分别达到0.982、0.934、0.904、0.880、0.848、0.924;猜测茶汤氧化还原电位会影响到茶叶的外形、汤色、香气、滋味和叶底,在一定条件下,茶汤氧化还原电位越高,茶叶感官品质越好。
闷黄叶茶汤电导率与各感官因子和总分均不具有显著相关关系。
通过对比各电化学参数与感官评分的相关性发现,与感官审评总分相关性最大的是茶汤冷泡pH,相关系数为-0.933,其次为热泡氧化还原电位和热泡pH,相关系数分别为0.924、-0.922,可见,茶汤pH值和热泡氧化还原电位与黄茶感官审评关系密切,能在一定程度上反映茶叶品质的优劣。
2.4.2 黄茶闷黄过程中电化学参数与理化成分的相关性分析
本实验对闷黄叶茶汤冷泡和热泡pH、电导率、氧化还原电位6个电化学参数与水浸出物含量、茶多酚含量、咖啡碱含量、氨基酸含量、茶黄素含量、可溶性糖含量和儿茶素含量7个理化成分的含量进行了相关性分析,分析结果如表5所示。
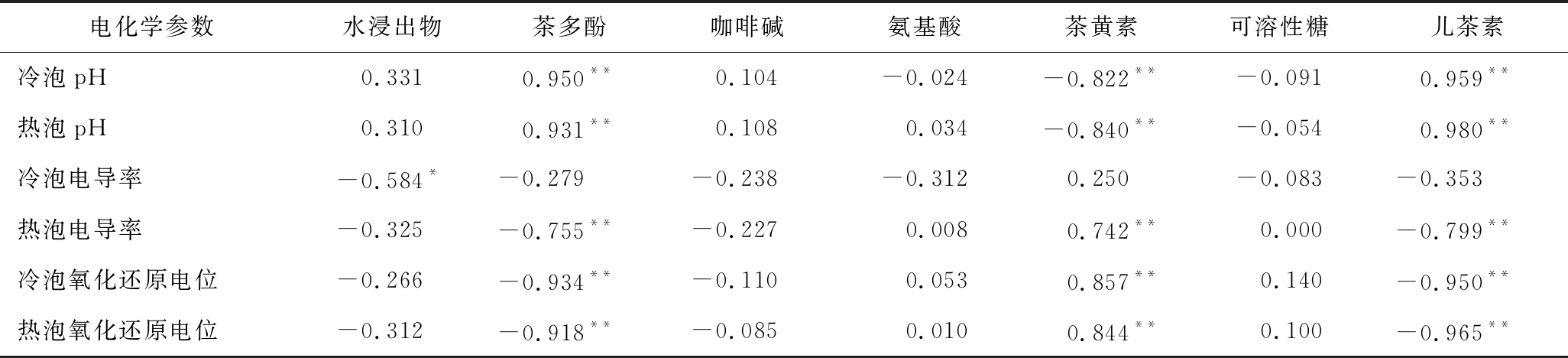
由表5可知,闷黄叶茶汤冷泡电导率与水浸出物呈显著负相关,相关系数为-0.584;闷黄叶茶汤冷泡和热泡pH均与茶多酚含量呈极显著正相关,相关系数分别为0.950、0.931,多酚类物质发生氧化、裂解影响着茶汤pH;闷黄叶茶汤热泡电导率、冷泡和热泡氧化还原电位均与茶多酚呈极显著负相关,相关系数分别为-0.755、-0.934、-0.918,多酚类物质在闷黄过程中生成新的物质,使得茶汤氧化还原电位升高。闷黄叶茶汤冷泡和热泡pH均与茶黄素呈极显著负相关,相关系数分别为-0.822、-0.840,多酚类的氧化和茶黄素含量的增加使得茶汤pH降低;闷黄叶茶汤热泡电导率、冷泡和热泡氧化还原电位均与茶黄素呈极显著正相关,相关系数分别为0.742、0.857、0.844,茶黄素含量的增加使得茶汤热泡电导率和氧化还原电位升高。闷黄叶茶汤冷泡和热泡pH均与儿茶素呈极显著正相关,相关系数分别为0.959、0.980, 猜测茶汤pH的降低或许与儿茶素的氧化和异构化有关;闷黄叶茶汤热泡电导率、冷泡和热泡氧化还原电位均与儿茶素呈极显著负相关,相关系数分别为-0.799、-0.950、-0.965,这或许是儿茶素闷黄过程中被大量氧化所致。
表5 电化学参数与理化成分的相关性分析
Table 5 Correlation analysis between electrochemical parameters and physicochemical components
电化学参数水浸出物茶多酚咖啡碱氨基酸茶黄素可溶性糖儿茶素冷泡pH0.3310.950**0.104-0.024-0.822**-0.0910.959**热泡pH0.3100.931**0.1080.034-0.840**-0.0540.980**冷泡电导率-0.584*-0.279-0.238-0.3120.250-0.083-0.353热泡电导率-0.325-0.755**-0.2270.0080.742**0.000-0.799**冷泡氧化还原电位-0.266-0.934**-0.1100.0530.857**0.140-0.950**热泡氧化还原电位-0.312-0.918**-0.0850.0100.844**0.100-0.965**
由以上分析结果可看出,闷黄叶茶汤电化学参数与茶多酚、茶黄素和儿茶素均呈极显著相关关系。
通过对比各电化学参数与理化成分的相关性发现,与理化成分相关性较大的是茶汤pH和氧化还原电位,其中冷泡和热泡茶汤pH和氧化还原电位与儿茶素的相关度最大,相关系数分别为0.959、0.980、-0.950、-0.965,然后是茶多酚和茶黄素,茶多酚。茶黄素和儿茶素是黄茶的主要品质成分,表明茶汤pH值和氧化还原电位能反映黄茶茶多酚、茶黄素和儿茶素含量的变化,能在一定程度上反映茶叶品质的优劣。
3 讨论与结论
钱园凤[14]通过研究红茶发酵过程发现,发酵叶茶汤pH随着发酵叶氧化程度的增加呈下降趋势,而发酵叶茶汤电导率无明显变化规律。汪东风[7]研究发现,发酵叶茶汤氧化还原电位随着发酵叶氧化程度的增加呈上升趋势。本实验结果表明,黄茶闷黄过程中,闷黄叶茶汤电化学参数随着闷黄时间的延长均发生了不同程度的变化,其中闷黄叶茶汤冷泡和热泡pH随着闷黄时间的延长均呈现降低的变化规律,冷泡和热泡氧化还原电位随着闷黄时间的延长均呈现升高的变化规律,冷泡和热泡电导率的变化波动较多,无明显变化规律,这与钱园凤[14]和汪东风等[7]研究结果基本一致;茶多酚和儿茶素的含量随闷黄时间的延长呈下降的变化趋势,氨基酸、茶黄素和可溶性糖含量呈先增加后减少的变化趋势,而水浸出物和咖啡碱含量波动较大,无明显变化规律;闷黄过程前期,茶样的感官审评得分逐渐升高,达到最大值后下降,审评总分较高茶样的闷黄时间集中在5~8 h,其中闷黄6 h茶样的感官审评总分最高。
通过将闷黄叶茶汤pH、电导率和氧化还原电位与干茶感官审评分数和主要理化成分进行相关性分析发现,与干茶感官品质相关性较高的电化学参数为冷泡pH、热泡pH、冷泡氧化还原电位和热泡氧化还原电位。pH是水溶液最重要的理化参数之一,凡涉及水溶液的自然现象、化学变化和生产过程均与pH值有关[27]。茶汤的pH由游离的氢离子和氢氧根离子的浓度决定,总体上,茶汤中游离的氢离子多于游离的氢氧根离子,故茶汤通常呈微酸性。已有研究显示,茶汤中含有的主要酸性物质为各种羧酸(苹果酸、柠檬酸、脂肪酸等)、某些氨基酸、维生素C、皂苷和茶黄素等,含有的呈碱性的物质主要为咖啡碱和部分芳香物质等[11,28],冷泡和热泡茶汤pH值与感官审评分数之间呈极显著负相关,而冷泡和热泡茶汤氧化还原电位与感官审评分数呈极显著的正相关关系,表明一定时间内,pH值越低的茶汤,氧化还原电位越高,该茶叶感官品质越好。闷黄过程中,多酚类物质在湿热条件下发生非酶性自动氧化,使得具有苦涩滋味的酯型儿茶素发生降解而转化为简单儿茶素,并且产生了爽口的茶黄素,这是形成黄茶醇和鲜爽滋味的重要原因[29]。本实验中,茶多酚、儿茶素和茶黄素含量与闷黄叶茶汤冷泡和热泡pH、冷泡和热泡氧化还原电位和热泡电导率均呈极显著的相关关系,其中闷黄叶茶汤冷泡和热泡pH值与茶多酚和儿茶素含量呈极显著正相关,与茶黄素含量呈极显著负相关,说明当茶叶中茶多酚和儿茶素含量越高、茶黄素含量越低,茶汤pH值越大。茶汤冷泡和热泡氧化还原电位与茶多酚含量、儿茶素含量呈极显著负相关,与茶黄素含量呈极显著正相关关系,说明当茶叶中茶多酚与儿茶素含量越低、茶黄素含量越高,则茶汤氧化还原电位值越大。热泡茶汤电导率与茶多酚和儿茶素含量呈极显著负相关,与茶黄素含量呈极显著正相关,说明当茶叶中茶多酚与儿茶素含量越低,茶黄素含量越高,茶汤电导率的值越大。
综上所述,茶汤电化学参数与感官品质和主要品质成分茶多酚和儿茶素及茶黄素均呈高度的相关性,可作为评价茶叶品质的方式之一,结果可为提高闷黄适度判定的便捷性和准确性提供一定的数据参考,对推动黄茶市场发展和黄茶生产的标准化具有重要意义。
[1] 陈斌. 黄茶加工工艺[J].农村新技术, 2008(12):68-69.
CHEN B.Yellow tea processing technology [J].New Rural Technology, 2008(12):68-69.
[2] 宛晓春. 茶叶生物化学[M].北京:中国农业出版社, 2008.
WAN X C.Tea Biochemistry [M].Beijing:China Agriculture Press, 2008.
[3] 张娇, 梁壮仙, 张拓, 等.黄茶加工中主要品质成分的动态变化[J].食品科学, 2019, 40(16):200-205.
ZHANG J, LIANG Z X, ZHANG T, et al.Dynamic changes of main quality components during yellow tea processing[J].Food Science, 2019, 40(16):200-205.
[4] TENG Y, LI D X, GURUVAIAH P, et al.Dietary supplement of large yellow tea ameliorates metabolic syndrome and attenuates hepatic steatosis in db/db mice[J].Nutrients, 2018, 10(1):75.
[5] KUJAWSKA M, EWERTOWSKA M, IGNATOWICZ E, et al.Evaluation of safety and antioxidant activity of yellow tea (Camellia sinensis) extract for application in food[J].Journal of Medicinal Food, 2016, 19(3):330-336.
[6] GRANATO D, GREVINK R, ZIELINSKI A A F, et al.Analytical strategy coupled with response surface methodology to maximize the extraction of antioxidants from ternary mixtures of green, yellow, and red teas (Camellia sinensis var.sinensis)[J].Journal of Agricultural and Food Chemistry, 2014, 62(42):10 283-10 296.
[7] 汪东风. 茶汤氧还体系电位值的测定[J].茶业通报, 1993,15(4):3-5.
WANG D F.Determination of potential value of oxygen return system in tea decoction [J].Journal of Tea Business, 1993,15(4):3-5.
[8] LUXIMON-RAMMA A, BAHORUN T, CROZIER A, et al.Characterization of the antioxidant functions of flavonoids and proanthocyanidins in Mauritian black teas[J].Food Research International, 2005, 38(4):357-367.
[9] 肖纯, 陈宗道.红茶发酵程度的传感技术研究[J].茶业通报, 1989,11(2):40-44.
XIAO C, CHEN Z D.Study on sensing technology of fermentation degree of black tea [J].Journal of Tea Business, 1989,11(2):40-44.
[10] 陈宗道, 肖纯.红茶发酵指示仪的研制[J].茶叶, 1988,14(4):22-24.
CHEN Z D, XIAO C.Development of black tea fermentation indicator [J].Chaye Journal of Tea, 1988,14(4):22-24.
[11] 张其生. “发酵”叶象与茶汤pH值的初步探讨[J].茶业通报, 1981,3(2):54-56.
ZHANG Q S.Preliminary study on pH value of “fermented” leaf weasel and tea decoction [J].Journal of Tea Business, 1981,3(2):54-56.
[12] 夏涛. 制茶学[M].3版.北京:中国农业出版社, 2016.
XIA T.Tea Making[M].3rd Edition.Beijing:China Agriculture Press, 2016.
[13] 张明露, 彭玙舒, 尹杰.不同闷黄时间和温度对黄茶品质的影响[J].耕作与栽培, 2018(3):12-14.
ZHANG M L, PENG Y S, YIN J.Effects of different piling time and temperature during processing on the quality of yellow tea[J].Tillage and Cultivation, 2018(3):12-14.
[14] 钱园凤. 工夫红茶发酵适度判定方法研究[D].北京:中国农业科学院, 2013.
QIAN Y F.Study on the judgment method of optimum fermentation of Congou black tea [D].Beijing:Chinese Academy of Agricultural Sciences, 2013.
[15] 叶庆生. 红茶萎凋发酵中多酚氧化酶、过氧化物酶同工酶的活性变化与儿茶素、茶黄素组分的消长[J].安徽农学院学报.1986, 13(2):19-29.
YE Q S. Study on the activity-variation of ppo-, po-isoenzymes and the growth and decline of catechin, tf components during withering and fermentation of black tea[J]. Journal of Anhui Agricultural University, 1986, 13(2): 19-29.
[16] 张正竹. 茶叶生物化学实验教程[M].北京:中国农业出版社,2009.
ZHANG Z Z.Tea Biochemistry Experiment Tutorial [M].Beijing:China Agriculture Press, 2009.
[17] 国家市场监督管理总局, 中国国家标准化管理委员会.GB/T 8313—2018 茶叶中茶多酚和儿茶素类含量的检测方法[S].北京:中国标准出版社, 2018.
State Administration for Market Regulation, Standardization Administration of China.GB/T 8313—2018 Method for determination of polyphenols and catechins in tea[S].Beijing:China Standards Press, 2018.
[18] 黄意欢. 茶学实验技术[M].北京:中国农业出版社, 1997.
HUANG Y H.Experimental Technology of Tea Science [M].Beijing:China Agriculture Press, 1997.
[19] BELAY A, TURE K, REDI M, et al.Measurement of caffeine in coffee beans with UV/vis spectrometer[J].Food Chemistry, 2008, 108(1):310-315.
[20] 钟萝. 茶叶品质理化分析[M].上海:上海科学技术出版社, 1989.
ZHONG L.Physicochemical Analysis of Tea Quality [M].Shanghai:Shanghai Science and Technology Press, 1989.
[21] 傅博强, 谢明勇, 聂少平, 等.茶叶中多糖含量的测定[J].食品科学, 2001,22(11):69-73.
FU B Q, XIE M Y, NIE S P, et al.Method simplified in assaying tea polysaccharide [J].Food Science, 2001,22(11):69-73.
[22] 王黎明, 夏文水.蒽酮-硫酸法测定茶多糖含量的研究[J].食品科学, 2005,26(7):185-188.
WANG L M, XIA W S.Determination of TPS by improvement of anthrone-sulfuric acid method[J].Food Science, 2005,26(7):185-188.
[23] 魏毅, 王娟, 罗杰英.香荚兰素比色法测定茶多酚口含片中儿茶素含量[J].中国中药杂志, 1999,24(6):347.
WEI Y, WANG J, LUO J Y.Determination of catechins in tea polyphenols oral tablets by vanillin colorimetry [J].China Journal of Chinese Materia Medica, 1999,24(6):347.
[24] 陆松侯, 施兆鹏.茶叶审评与检验[M].3版.北京:中国农业出版社, 2001.
LU S H, SHI Z P.Tea Evaluation and Inspection[M].Third Edition.Beijing:China Agriculture Press, 2001.
[25] 冯成志, 贾凤芹.社会科学统计软件SPSS教程[M].北京:清华大学出版社, 2009.
FENG C Z, JIA F Q.Social Science Statistical Software SPSS Tutorial [M].Beijing:Tsinghua University Press, 2009.
[26] 李坚. 葡萄酒的氧化程度对酒质的影响及其判别模型的构建[D].长沙:湖南农业大学, 2017.
LI J. The influence of oxidation degree of wine on its quality and the construction of its discriminant model[D].Changsha:Hunan Agricultural University, 2017.
[27] 李发美. 分析化学[M].7版.北京:人民卫生出版社, 2011:38, 178-192.
LI F M.Analytical Chemistry[M].7th Edition.Beijing:People′s Medical Publishing House, 2011:38, 178-192.
[28] 郭桂义, 葛国平.不同茶类茶汤pH值的研究[J].食品科技, 2012, 37(5):74-76.
GUO J Y, GE G P.Preliminary on pH of different tea liquor [J].Food Science and Technology, 2012, 37(5):74-76.
[29] 龚永新, 蔡烈伟, 蔡世文, 等.闷堆对黄茶滋味影响的研究[J].茶叶科学, 2000, 20(2):110-113.
GONG Y X, CAI L W, CAI S W, et al.Study on the effect of stack-cover process on the taste of yellow tea [J].Journal of Tea Science, 2000, 20(2):110-113.