表1 流动相梯度洗脱程序
Table 1 Mobile phase gradient elution procedure

时间/minA[0.1%(体积分数)甲酸-水]B(乙腈)0.0195515753037.195540stopstop
由于预期寿命的增加和人口的变化,神经退行性疾病的发病率逐年升高[1]。氧化应激是神经退行性相关疾病的主要触发因子[2-3]。过量的多不饱和脂肪酸,高有氧率,过渡金属的存在以及抗氧化酶活性的降低使大脑容易受到氧化损伤[2]。多酚是植物中天然存在的微量营养素,是植物体内必需的生理化合物[4],具有抗氧化、抗炎等特性,已有较多研究证明了多酚的神经保护作用[5-7]。
小米是中国北方及西北地区的传统谷物之一,富含多酚类物质,具有良好的抗氧化性[8]。DYKES等[9]综述了国内外各种小米中所含有的多酚类物质,小米中的酚类化合物主要存在于小米的果皮、种皮和糊粉层中,分为两类:羟基苯甲酸和羟基肉桂酸。根据国内外各种小米品种中酚类化合物成分及含量的相关研究可知,小米多酚化合物主要为酚酸类和菊花黄酮类[10]。
目前我国对小米的研究还主要集中在其化学成分的分析及营养成分的分析,而对其多酚类活性成分及功效研究较少。延莎等[11]以6种不同米色小米为原料提取小米多酚并探讨其多酚提取物的抗氧化性。结果表明,6种不同米色小米多酚提取物在5种抗氧化实验中均具有较好的体外抗氧化活性, 且多酚总量与抗氧化性具有显著相关性, 所以总酚含量越高,其小米的抗氧化性越好。
本研究对2种产地小米进行了多酚的提取和成分分析,并通过过氧化氢(H2O2)处理 SH-SY5Y 建立神经细胞氧化应激模型,探究2种小米多酚对神经细胞氧化损伤的保护作用,为深入开发小米资源进行应用研究提供理论基础。
金小米,缘谷缘粮农业科技有限公司;桃花小米,张家口坤记商贸有限公司;乙醇、石油醚、三氯甲烷、没食子酸、碳酸钠(Na2CO3)、Folin-Ciocateu试剂、过氧化氢(H2O2),国药化学试剂有限公司(上海);DMEM-F12培养基、胰酶、MTT细胞增殖及细胞毒性检测试剂盒,碧云天生物技术有限公司。
型号电饭煲,美的集团有限公司;型号冻干机,宁波新芝生物科技股份有限公司;型号高速多功能磨粉机,上海菲力博宝业公司;200目筛,台州三门跃阳筛网厂;磁力搅拌器,上海梅颖浦仪器仪表制造有限公司;低温高速离心机,天美仪拓实验室设备(上海)有限公司;型号旋转蒸发器,上海亚荣生化仪器厂;涡旋振荡器,美国Scientific Industries公司;紫外分光光度计,尤尼柯(上海)仪器有限公司;色谱仪器,岛津LC-30A;质谱仪器, AB Sciex Triple TOF 5600+;HH-W-600水浴锅,金坛市江南仪器厂;BSC-1300IIA2型超净工作台,江苏净化设备有限公司;MCO-20AIC型CO2 细胞培养箱,日本三洋公司;酶标仪,美国伯腾仪器有限公司。
1.3.1 小米多酚提取与纯化
将金小米和桃花小米按料液比1∶1.2(g∶mL)煮熟,冷却至室温后冻干48 h,用高速多功能磨粉机粉碎机研磨后过200目筛。再将小米粉按料液比1∶10溶于80%(体积分数)乙醇中。在60 ℃恒定搅拌下浸提2 h,得到乙醇提取液。以3 500 r/min 离心10 min后,使用旋转蒸发仪50 ℃,80 r/min浓缩,得到乙醇浓缩液[12]。加入与乙醇浓缩液等体积石油醚萃取,取下层溶液;再加入等体积三氯甲烷萃取,取上层溶液;再加入等体积乙酸乙酯萃取3次,取乙酸乙酯相合并,使用旋转蒸发仪35 ℃,80 r/min浓缩,得乙酸乙酯浓缩液;使用冷冻干燥机冻干48 h得纯化小米多酚并在4 ℃下贮存备用[8]。
1.3.2 总酚含量的测定
采用 Folin-Ciocalteau法测总酚[13]。准确地称取没食子酸标准品0.011 g,用蒸馏水溶解后定容至100 mL,得到标准液质量浓度为0.11 mg/mL。准确吸取0、0.4、0.6、0.8、1.0、1.2、1.4 mL置于25 mL 的棕色试管中,取小米多酚复溶液0.5 mL,加蒸馏水至6.0 mL,然后分别加入福林酚试剂 0.5 mL,涡旋5 s,8 min后加入1.5 mL 200 g/L的Na2CO3溶液,充分混合后定容,常温避光放置2 h,以不加标准液的6.0 mL 蒸馏水为空白对照,760 nm下测定吸光值,每个样品平行测定3次。根据标准曲线以没食子酸作为对照样品计算样品中总多酚含量。
1.3.3 小米多酚组分分析
取小米复溶液1 mL于2 mL离心管内,放入高速离心机中1 300 r/min离心10 min,过0.22 um微孔滤膜后装入1.5 mL自动进样瓶内,得到小米提取物样品。同样条件得到空白对照样品。将样品放入 4 ℃冰箱保存,在分析前取出(保存时间不能超过24 h)。
采用高效液相-色谱分析[14-15],色谱柱为C18(1.8 μm,2.1 mm×100 mm);柱温35 ℃;流速0.3 mL/min;进样量3 μL;流动相采用乙腈-0.1%(体积分数)甲酸水溶液的梯度洗脱程序,见表1。
表1 流动相梯度洗脱程序
Table 1 Mobile phase gradient elution procedure

时间/minA[0.1%(体积分数)甲酸-水]B(乙腈)0.0195515753037.195540stopstop
质谱离子化模式为电喷雾正离子模式,离子源电压分别为5 500 V,离子源温度为600 ℃,去簇电压(declustering voltage,DP) 分别为100 V,碰撞能量(collision energy,CE)分别为35 eV,碰撞能量扩展(collision energy expansion,CES)分别为15 eV;离子化模式为电喷雾负离子模式,离子源电压分别为-4 500 V,离子源温度为500 ℃,DP分别为100 V, CE分别为-35 eV,CES别为15 eV。雾化气体为氮气,辅助气1为60 PSI,辅助气2为50 PSI,气帘气为40 PSI。一级质谱母离子扫描范围为50~1 000,信息依赖采集设置响应值超过100 cps的6个最高峰进行二级质谱扫描,离子扫描范围为50~1 000。
1.3.4 SH-SY5Y 神经细胞的培养
SH-SY5Y 神经细胞在补充有10%胎牛血清(体积分数)的 DMEM-F12 培养基中培养,并在实验前在 37 ℃下在5%(体积分数)CO2的细胞培养箱中培养至对数期,用于后续实验。
1.3.5 细胞活力的测定
通过3-(4,5-二甲基噻唑-2-基)-2,5- 二苯基四唑溴化物[3-(4,5-dimethyl-2-thiazolyl)-2,5-diphenyl-2H-tetrazolium bromide,MTT]细胞增殖及细胞毒性测试评估小米多酚对 H2O2诱导的细胞损伤的细胞保护活性[8]。96孔板处理后的SH-SY5Y细胞加入MTT。代谢活跃的细胞将黄色四唑盐MTT裂解成紫色的甲瓒晶体。将形成的甲瓒溶解,用酶标仪在570 nm 处测量吸光度。结果以对照组的百分比表示。具体方法以MTT细胞增殖及细胞毒性测定试剂盒生产说明书为依据。
1.3.6 建立 H2O2 诱导的氧化应激模型
将生长密度达到90%的 SH-SY5Y 神经细胞用胰蛋白酶消化成单细胞悬液,并按5×103个细胞/孔接种于96孔板中,1个孔加入100 μL细胞,全反式维甲酸(tretinoin,RA)诱导分化48 h。采用H2O2 毒性试验,测定H2O2的IC50值。再通过检测细胞活性,确定小米多酚对于由H2O2引起的氧化应激具有作用的浓度。
1.3.7 小米多酚处理细胞
小米多酚储备液:金小米和桃花小米浓缩液,添加时根据多酚含量用培养基稀释成所需浓度,并过滤除菌。
共处理:小米多酚和H2O2同时加入培养15 h。
预处理:先用小米多酚与细胞培养12 h后更换H2O2培养15 h。
1.3.8 统计学分析 细胞试验的数据统计分析用
使用Graph Pad Prism 8.0.2(graph pad software,San Diego,CA,USA)和SPSS 17.0(IBM corporation,Armonk,NY,USA)进行分析。2组间的差异采用t检验进行评估。P≤0.05为差异有统计学意义。
以没食子酸质量浓度为横坐标、吸光度为纵坐标建立没食子酸标准曲线,回归方程为 y=85.28x+0.033 61(R2=0.996 3),线性范围0~0.006 16 mg/mL。
根据标准曲线测得金小米的质量浓度为1.23 mg/mL,占总提取物的15.57%,桃花小米的质量浓度为1.27 mg/mL,占总提取物的57.26%,桃花小米的酚类含量高于金小米。
本实验定性检测出28种多酚类化合物,其中金小米中20种,桃花小米中8种,包含12种黄酮类化合物和其他物质,如木质素、酚酸、色素、单宁、非黄酮酚类等。与XIANG等[16]测定结果相似,鉴定出的20种酚类化合物包括黄酮类化合物和酚酸化合物。朱俊玲等[17]也在小米多酚中检测出黄酮类物质。如表2和表3所示,金小米中厚朴三酚、刺苞菊苷、水仙苷、香叶木苷含量较高,桃花小米中厚朴三酚、毛兰素、5,8-二羟基葛根素、10-姜酚、奎宁酸含量较高。
表2 金小米多酚成分 单位:%
Table 2 Polyphenol constituents of golden millet
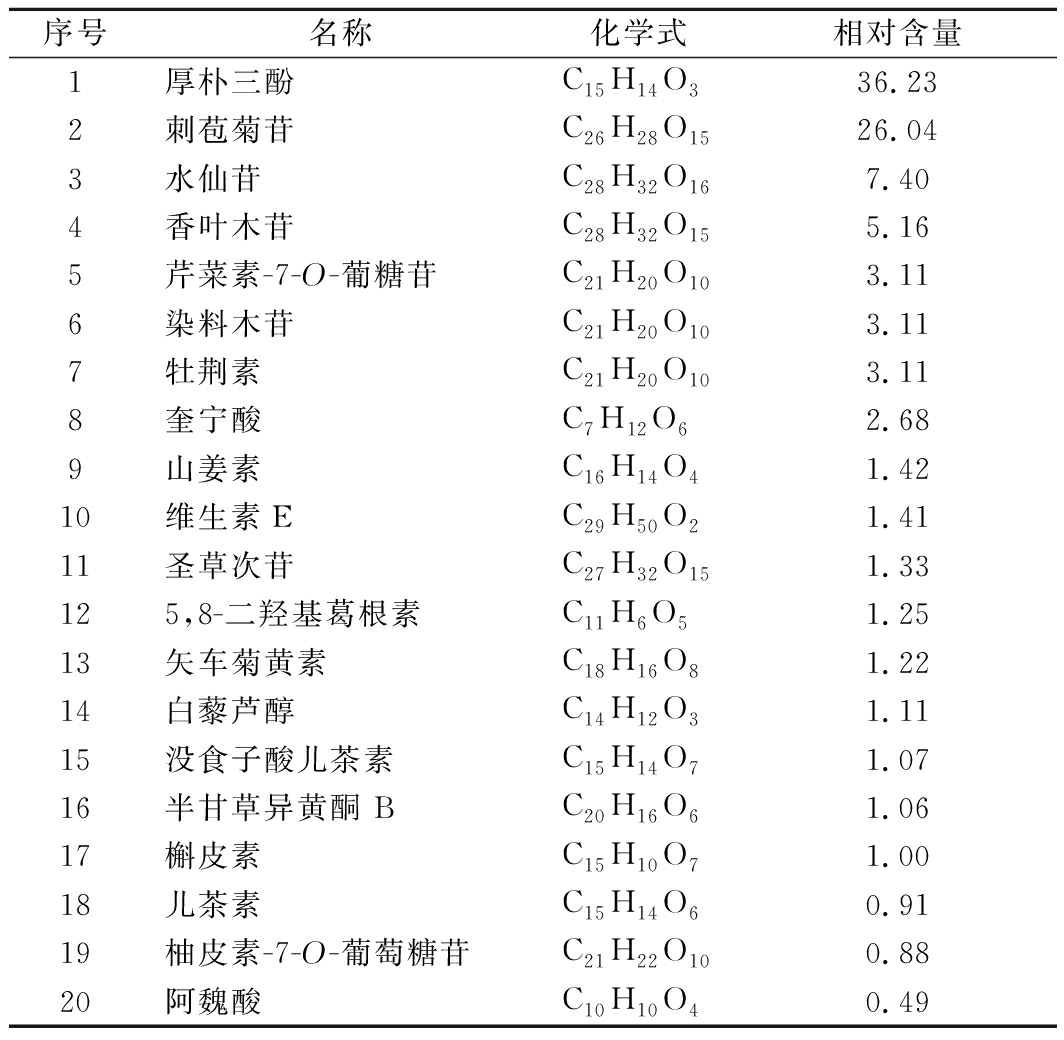
序号名称化学式相对含量1厚朴三酚C15H14O336.23 2刺苞菊苷C26H28O1526.04 3水仙苷C28H32O167.40 4香叶木苷C28H32O155.16 5芹菜素-7-O-葡糖苷C21H20O103.11 6染料木苷C21H20O103.11 7牡荆素C21H20O103.11 8奎宁酸C7H12O62.68 9山姜素C16H14O41.42 10维生素EC29H50O21.41 11圣草次苷C27H32O151.33 125,8-二羟基葛根素C11H6O51.25 13矢车菊黄素C18H16O81.22 14白藜芦醇C14H12O31.11 15没食子酸儿茶素C15H14O71.07 16半甘草异黄酮 BC20H16O61.06 17槲皮素C15H10O71.00 18儿茶素C15H14O60.91 19柚皮素-7-O-葡萄糖苷C21H22O100.88 20阿魏酸C10H10O40.49
表3 桃花小米多酚成分 单位:%
Table 3 Polyphenol constituents of peach flower millet
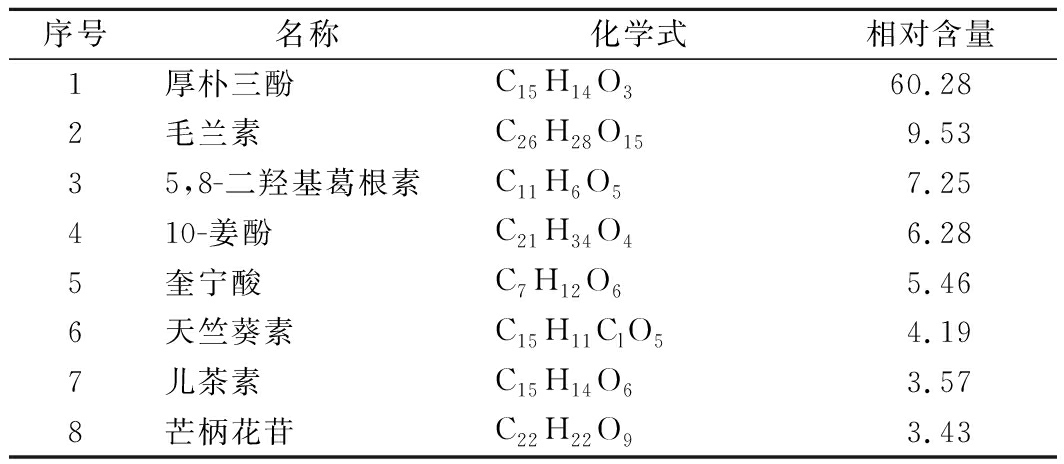
序号名称化学式相对含量1厚朴三酚C15H14O360.28 2毛兰素C26H28O159.53 35,8-二羟基葛根素C11H6O57.25 410-姜酚C21H34O46.28 5奎宁酸C7H12O65.46 6天竺葵素C15H11ClO54.19 7儿茶素C15H14O63.57 8芒柄花苷C22H22O93.43
目前关于黄酮类(牡荆素、槲皮素等)抗氧化[18]、抗炎[19]、抗血脂[20]、抗癌[21]等研究十分广泛,刺苞菊苷、染料木苷、水仙苷等研究较少。香叶木苷因其溶解度和生物利用度也鲜有研究[22],厚朴三酚几乎没有相关研究。
SH-SY5Y 细胞起源于神经母细胞瘤,通常被RA诱导分化,以获得更多神经元样特性,包括神经突生长和形态学改变,以模拟研究中的神经元反应,促进细胞生存和减少凋亡[23]。对H2O2处理浓度的研究显示,当利用 300 μmol/L H2O2处理 SH- SY5Y 15 h 后,SH-SY5Y 的细胞活力显著下降到对照组的50%(图1)。
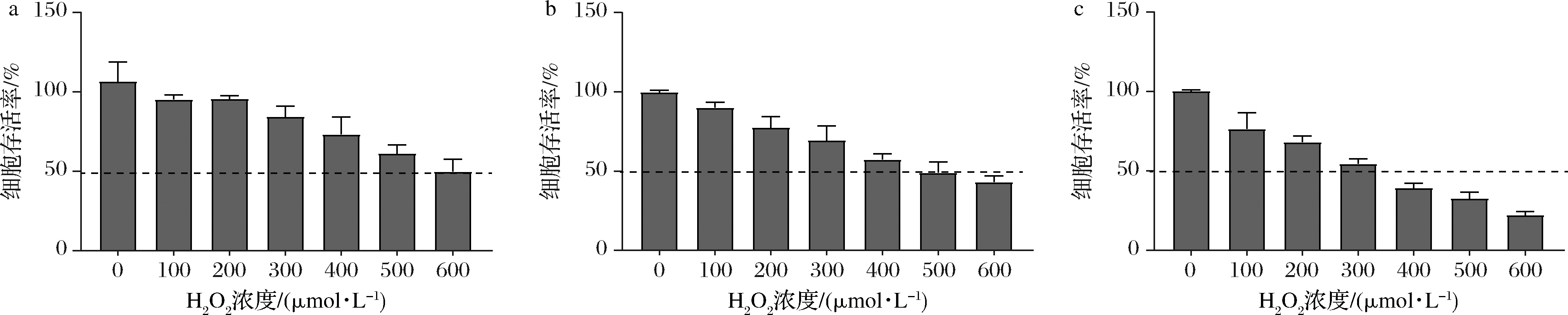
a-H2O2作用5 h;b-H2O2作用10 h;c-H2O2作用15 h
图1 不同时间和H2O2作用浓度对细胞存活率的影响
Fig.1 Effects of different time and concentration of H2O2 on cell viability
用不同质量浓度(100、200、300、400、500、600 μg/mL)的小米多酚对 SH-SY5Y 细胞进行处理,对照组为不经H2O2和小米多酚处理的正常培养细胞,细胞存活率记100%。分别评价小米多酚预处理和共处理对神经细胞的保护作用,共处理的方式为SH-SY5Y在RA诱导48 h后小米多酚和H2O2同时加入培养15 h,预处理则是SH-SY5Y在RA诱导48 h后先用小米多酚与细胞培养12 h后更换H2O2培养15 h。
结果如图2所示,与对照组相比,H2O2处理(100 μmol/L)组细胞生存力显著受到损伤。由图2-a和图2-c可以看出,共处理的方式下,小米多酚对于神经细胞的保护作用并不显著。图2-b和图2-d中,小米多酚预处理下,200~300 μg/mL的小米多酚对 H2O2损伤的SH-SY5Y具有保护作用(P<0.05)。而当小米多酚质量浓度增加到400 μg/mL以上时,细胞生存力反而下降,这可能是由于多酚类物质在高浓度下对细胞产生了毒性作用。不论是金小米还是桃花小米,预处理方式下细胞的生存率总是优于共处理,吴枝娟等[24]在阿魏酸(ferulic acid,FA)对阿霉素诱导H9c2心肌细胞损伤的研究中FA预处理组细胞生存率均高于相同剂量FA共处理组,这与本研究相一致。推测这其中的原因可能是预处理的方式使细胞活力增强,增殖更多从而提高了细胞的抵御能力。

a-金小米与H2O2共处理;b-金小米预处理;c-桃花小米与H2O2共处理;d-桃花小米预处理
图2 小米多酚对H2O2处理的SH-SY5Y细胞生存力的影响
Fig.2 Effects of millet polyphenol on the viability of SH-SY5Y cells treated with H2O2
注:*表示P<0.05;**表示P<0.01
虽然金小米的总酚含量较低,但是金小米中酚的种类较多且含有像荆素、维生素E、白藜芦醇、槲皮素、FA等抗氧化及自由基清除能力较强的酚类[25],牡荆素可通过激活PI3K/Akt信号通路保护多巴胺能神经元免受MPP+/mptp诱导的神经毒性[26]。白藜芦醇通过抑制NF-κB信号通路对Aβ42诱导的星形胶质细胞和小胶质细胞炎症的抑制作用[27]。而桃花小米中酚类种类较少,且其生物活性不如金小米中的酚类。
通过对金小米和桃花小米总酚提取及含量检测,发现桃花小米酚类含量更高,但金小米中酚类化合物种类较多。2种小米的多酚中厚朴三酚含量最高,但是目前几乎没有关于厚朴三酚的研究,作为小米多酚中重要的成分,其研究价值不应被忽略。H2O2诱导的SH-SY5Y细胞氧化应激模型显示2种小米多酚浓度在 200~300 μg/mL 内都可以提高H2O2处理的SH-SY5Y细胞的存活率,证明小米多酚对氧化应激状态下的神经细胞具有一定的保护作用。小米多酚预处理的保护作用优于共处理,其具体原因值得进一步研究。
[1] SKOVRONSKY D M, LEE V M Y, TROJANOWSKI J Q.Neurodegenerative diseases:New concepts of pathogenesis and their therapeutic implications[J].Annual Review of Pathology:Mechanisms of Disese, 2006, 1:151-170.
[2] CHEIGNON C, TOMAS M, BONNEFONT-ROUSSELOT D, et al.Oxidative stress and the amyloid beta peptide in Alzheimer′s disease[J].Redox Biology, 2018, 14:450-464.
[3] LIN M T, BEAL M F.Mitochondrial dysfunction and oxidative stress in neurodegenerative diseases[J].Nature, 2006, 443(7 113):787-795.
[4] SILVA R F M, ![]() L.Polyphenols from food and natural products:Neuroprotection and safety[J].Antioxidants (Basel), 2020, 9(1):61.
L.Polyphenols from food and natural products:Neuroprotection and safety[J].Antioxidants (Basel), 2020, 9(1):61.
[5] ABIB R T, PERES K C, BARBOSA A M, et al.Epigallocatechin-3-gallate protects rat brain mitochondria against cadmium-induced damage[J].Food Chemical Toxicology, 2011, 49(10):2 618-2 623.
[6] EL-MISSIRY M A, OTHMAN A I, EL-SAWY M R, et al.Neuroprotective effect of epigallocatechin-3-gallate (EGCG) on radiation-induced damage and apoptosis in the rat Hippocampus[J].International Journal of Radiation Biology, 2018, 94(9):798-808.
[7] CHUNG W G, MIRANDA C L, MAIER C S.Epigallocatechin gallate (EGCG) potentiates the cytotoxicity of rotenone in neuroblastoma SH-SY5Y cells[J].Brain Research, 2007, 1 176:133-142.
[8] LI S, XIAN F R, GUAN X, et al.Neural protective effects of millet and millet polyphenols on high-fat diet-induced oxidative stress in the brain[J].Plant Foods for Human Nutrition, 2020, 75(2):208-214.
[9] DYKES L, ROONEY L W.Sorghum and millet phenols and antioxidants[J].Journal of Cereal Science, 2006, 44(3):236-251.
[10] 田志琴. 小米多酚类活性物质的提取及抗氧化性研究[D].郑州:河南工业大学, 2011.
TIAN Z Q.The studies on extraction and antioxidant activities of foxtail millet ployphenol[D].Zhengzhou:He′nan University of Technology, 2011.
[11] 延莎, 祁鹏煜, 张苏慧,等.不同米色小米多酚提取物的体外抗氧化活性[J].中国粮油学报, 2017, 32(10):33-38;44.
YAN S, QI P Y, ZHANG S H, et al.Antioxidant activity of polyphenol extracts from different beige millet in vitro[J].Journal of the Chinese Cereals and Oils Association, 2017, 32(10):33-38;44.
[12] DEWANTO V, WU X Z, LIU R H.Processed sweet corn has higher antioxidant activity[J].Journal of Agricultural and Food Chemistry, 2002, 50(17):4 959-4 964.
[13] BOX J D.Investigation of the folin-ciocalteau phenol reagent for the determination of polyphenolic substances in natural waters[J].Water Research, 1983, 17(5):511-525.
[14] ZHA H H, CAI Y P, YIN Y D, et al.SWATH to MRM:Development of high-coverage targeted metabolomics method using SWATH technology for biomarker discovery[J].Analytical Chemistry, 2018, 90(6):4 062-4 070.
[15] LUO P, YIN P Y, ZHANG W J, et al.Optimization of large-scale pseudotargeted metabolomics method based on liquid chromatography-mass spectrometry[J].Journal of Chromatography A, 2016, 1 437:127-136.
[16] XIANG J L, APEA-BAH F B, NDOLO V U, et al.Profile of phenolic compounds and antioxidant activity of finger millet varieties[J].Food Chemistry, 2019, 275:361-368.
[17] 朱俊玲, 梁凯, 闫巧珍,等.小米多酚的分离纯化及其组分分析[J].中国粮油学报 2021, 36(2):34-40.
ZHU J L, LIANG K, YAN Q Z, et al.Isolation, purification and component analysis of polyphenols from millet [J].Journal of the Chinese of Cereals and Oils Association, 2021, 36(2):34-40.
[18] PENG Y, GAN R Y, LI H B, et al.Absorption, metabolism, and bioactivity of vitexin:Recent advances in understanding the efficacy of an important nutraceutical[J].Critical Reviews in Food Science and Nutrition, 2021, 61(6):1 049-1 064.
[19] YAHAYA M A F, ZOLKIFFLY S Z I, MOKLAS M A M, et al.Possible epigenetic role of vitexin in regulating neuroinflammation in alzheimer′s disease[J].Journal of Immunology Research, 2020:9469210.
[20] LEI X B, YANG Y.Vitexin and an HMG-Co a reductase inhibitor prevent the risks of atherosclerosis in high-fat atherogenic diet fed rats[J].Journal of King Saud University - Science, 2020, 32(3):2 088-2 095.
[21] ZHANG G N, LI D Y, CHEN H, et al.Vitexin induces G2/M-phase arrest and apoptosis via Akt/mTOR signaling pathway in human glioblastoma cells[J].Molecular Medicine Reports, 2018, 17(3):4 599-4 604.
[22] 艾凤伟, 佟雷, 杨开勇,等.甲基-β-环糊精对香叶木苷的增溶作用[J].中国实验方剂学杂志 2012, 18(7):41-43.
AI F W, TONG L, YANG K Y, et al.Solubilization effect of methyl-β-cyclodextrin on diosmin[J].Chinese Journal of Experimental Formulae, 2012, 18(7):41-43.
[23] CHEUNG Y T, LAU W K W, YU M S, et al.Effects of all-trans-retinoic acid on human SH-SY5Y neuroblastoma as in vitro model in neurotoxicity research[J].Neuro Toxicology, 2009, 30(1):127-135.
[24] 吴枝娟, 余靖, 王瑞幸, 等.阿魏酸预处理对阿霉素诱导H9c2心肌细胞损伤的保护作用[J].中国药理学通报 2014,30(8):1 059-1 065.
WU Z J, YU J, WANG R X, et al.Protective effect of ferulic acid on doxorubicin induced cellular injury in H9c2 myocardial cells[J].Chinese Pharmacological Bulletin 2014,30(8):1 059-1 065.
[25] AGATI G, AZZARELLO E, POLLASTRI S, et al.Flavonoids as antioxidants in plants:Location and functional significance[J].Plant Science, 2012, 196:67-76.
[26] HU M, LI F M, WANG W D.Vitexin protects dopaminergic neurons in MPTP-induced Parkinson′s disease through PI3K/Akt signaling pathway[J].Drug Design Development and Therapy, 2018, 12:565-573.
[27] ZHAO H F, WANG Q, CHENG X J, et al.Inhibitive effect of resveratrol on the inflammation in cultured astrocytes and microglia induced by Abeta1-42[J].Neuroscience, 2018, 379:390-404.