纳米乳液(nanoemulsion),又称微乳液(microemulsion),是由水、油、表面活性剂和助表面活性剂等自发形成,粒径为1~100 nm的热力学稳定、各向同性,透明或半透明的均相分散体系。一般来说,纳米乳液分为3种类型:水包油型纳米乳液(oil in water, O/W)、油包水型纳米乳液(water in oil, W/O)以及双连续型纳米乳液(B.C)。与传统乳液相比,纳米乳液具有传统乳液不可比拟的优势,比如颜色透明、负载的生物活性物质生物利用度高、物理稳定性优异,可用于婴儿食品、功能饮料等多种特殊食品的制备[1-2]。随着功能性食品的不断发展,搭载可防治癌症、高血压、肥胖和心血管系统等慢性疾病的生物活性物质食品越来越受到学术界的关注。然而,长链n-3多不饱和脂肪酸 (long chain n-3 poly unsaturated fatty acids, LC n-3 PUFA)、类胡萝卜素、共轭亚油酸、辅酶Q10等大多数具有特殊功能的生物脂质均为弱水溶性物质,很难被直接融入亲水性食品或饮料中,通常需借助传输系统整合至食品体系[3-4]。
由于缺乏利用食品级原料制备具有特殊功能纳米乳液的研究,纳米乳液的潜在优势一直未能很好的体现在食品工业中。近年来纳米科技及胶体科学的快速发展,不断涌现出制备纳米乳液和提高稳定性的新技术和新方法,这些进步使得优化设计具有特定功能和用途的纳米乳液成为可能[5-6]。针对该领域的研究现状,本文综述了近年来在LC n-3 PUFA纳米乳液特点、制备方法以及功能应用等的最新研究成果,希望对食品及饮料工业中应用负载LC n-3 PUFA食品纳米乳液的合理设计与制备有所启示。
1 负载LC n-3 PUFA食品纳米乳液的特点
在功能食品及饮料市场快速发展的当下,食品工业对在食品体系中有效包埋与传输(如生物活性物质、风味物质及天然色素等)功能性物质的需求逐渐增加。这其中大部分物质例如LC n-3 PUFA、植物甾醇、共轭亚油酸、类胡萝卜素、姜黄素及维生素A、D、E、K等均为脂溶性物质,很难被直接整合入以水为主体的食品或饮料中,通常需要被包埋于可均匀分散在水相中的胶体传输系统中[7]。此外,大部分功能饮料需外观透明或轻微的浑浊,这限制了可用于负载脂溶性生物活性物质传输系统的种类,因为传输系统中的载体微粒尺寸需足够小以至于不散射自然光(r≪λ)。以纳米乳液为载体的传输系统有望克服以上问题,成功负载脂溶性生物活性物质并有效整合在食品或饮料中。
传统的水包油乳液(r>100 nm)已在传统食品或饮料产品中被广泛用于包埋脂溶性活性物质,如富含二十碳五烯酸(eicosapentaenoic acid, EPA)、二十二碳六烯酸(docosahexaenoic acid, DHA)、维生素A、D的鱼油和酸奶等[8-9]。然而纳米乳液(r<100 nm)有着众多优于传统乳液的潜在优势,尤其在一些特殊食品中的应用。纳米乳液通常能抵抗因颗粒聚集和重力作用导致的乳液不稳定现象,并且纳米乳液中的纳米颗粒因尺寸较小而不易散射自然光,因此更适合于对外观清澈度有较高要求的食品,尤其是功能饮料的生产[2]。通过结构化设计,纳米乳液可形成高黏度、胶状类浓缩乳液,可实现在保证口感的同时显著降低油的用量,因此可用于酸奶等对食品流变性质有不同需求的食品,或针对肥胖患者的低脂食品[10]。纳米乳液可显著提高其所负载活性物质的生物利用度,因此可用于包埋和传递某些对人体生物利用度低的生物活性物质[11]。纳米乳液的功能性很大程度上取决于体系中纳米颗粒的结构特性,如纳米颗粒的浓度、组成、粒径分布、电荷及物理状态等,而这些特性主要由构建纳米乳液原料固有的特性及制备方法决定。LC n-3 PUFA纳米乳液对食品储存稳定性的影响见表1。
表1 LC n-3 PUFA纳米乳液对食品储存稳定性的影响
Table 1 Effects of LC n-3 PUFA nanoemulsion on food storage stability

活性组分食品体系货架期非纳米乳液体系纳米乳液体系参考文献肉桂油苹果汁2 h褐变48 h褐变[12]巴兹尔精油黄秋葵3 d15 d[13]柠檬醛菠萝9 d12 d[14]乳酸菌素酸奶20 d40 d[15]迷迭香、鼠尾草香精油虹鳟鱼17 d21 d[16]壳聚糖火鸡肉片6 d9 d[17]八角茴香腌肉8 d16 d[18]壳聚糖角油虹鳟鱼丸3 d12 d[19]牛至精油和柑橘纤维低脂奶酪13 d24 d[20]
2 负载LC n-3 PUFA纳米乳液的制备方法
2.1 传统纳米乳液的制备方法
通常,纳米乳液可经高能量和低能量2种制备方法实现[21]。高能量方法利用机械装置,产生可破坏或掺杂油水相的高强度作用力,实现乳液尺寸纳米化,这类机械装置包括高压真空均质机,微射流均质机和超声仪等。高能量方法虽然是食品工业目前制备纳米乳液的基本方法,但有很多局限,比如高昂的设备安装维护费用及高能耗损失,最主要的是该类方法不能有效制备食品纳米乳液。低能量方法制备纳米乳液是利用乳化剂的特殊性质,在混合的表面活性剂-油-水(surfactant-oil-water, SOW)三相体系,通过改变SOW组成或环境条件,最终自发形成纳米乳液[22]。基于低能量技术的纳米乳液制备方法主要包括自乳化及相转变两大类[23]。低能量纳米乳液制备方法具有设备简单、成本低、低能耗损失等优势,该方法可用于对高黏度油脂制备纳米乳液,且一旦形成后对环境的稳定性影响较小[24]。
自乳化方法源于制药领域,用于制备自乳化纳米药物传输系统,近年来开始应用于食品领域,以制备负载脂溶性生物活性物质的纳米乳液[25]。尽管自乳化方法制备纳米乳液的机制尚未完全阐明,但普遍公认的机理(图1)是在磁力搅拌下,将含有水溶性表面活性剂的油相与水混合。由于这种运动,水分散物质由油相转变为水相,导致界面不稳定,小油滴自发形成。为了产生小的乳状液滴,两相界面处的紊流应该被触发,并且辅助表面活性剂如乙醇、丙酮和丙二醇也被激活[26]。自乳化方法依赖于油和表面活性剂自身性质、界面应力、油和表面活性剂比例,及助溶剂用量和种类。油是自乳化方法中的关键因素,可用该方法制备纳米乳液的脂质包括中链甘油三脂或脂肪酸酯,而表面活性剂通常需要有较高亲水疏水平衡值,如食品级表面活性剂吐温和司盘系列中部分组成,或双亲性磷脂分子。这种方法的主要缺点是需要使用大量的合成表面活性剂[27]。

图1 自乳化方法制备纳米乳液机制
Fig.1 Preparation mechanism of nano-emulsion by self-emulsification method
2.2 负载LC n-3 PUFA食品纳米乳液低能量技术制备方法
通过低能量方法,虽可得到食品级纳米乳液,但其制备过程主要依靠经验方法,比如在油与食品级表面活性剂被确定的前提下,通过改变乳化条件实现乳液尺寸的纳米化。此外,所制备的纳米乳液是否能满足对预期食品或饮料外观、流变学等功能性的需求只能在反复试验后得到确认,这种方式不仅浪费资源,常常也得不到理想结果。纳米乳液是由单个纳米颗粒组成,因此纳米乳液最终的功能性质将由纳米颗粒的浓度、组成、相貌形态、大小分布、表面电荷及物理状态等结构特性决定。为了能在不同的低能量方法中正确选择实现食品功能要求的方法及SOW组成,建立纳米乳液-固体分散体结构功能关系将至关重要,这样可实现按需定制食品纳米乳液工业。因此,通过建立乳液纳米颗粒自身微观结构特性与纳米乳液整体外观、稳定性及流变学特性等宏观功能特性间关系,是优化低能量方法,合理设计具有特定功能和用途食品纳米乳液的有效保证。
相转变方法可以通过改变体系不同温度、盐离子浓度或pH等环境条件下表面活性剂性质,包括其分子曲率、构相和相对溶解度的变化实现。常见的相转变方法包括相转变温度、组成相转变和突变相转变等,但目前仅组成相转变和突变相转变2种方法可实现对食品级表面活性剂及食用油制备食品纳米乳液。组成相转变方法是基于非离子表面活性剂的自发曲率变化引起的温度诱导相变。它的形成是通过改变环境pH或盐离子浓度,促使表面活性剂分子曲率或相对溶解度的改变,并最终形成纳米乳液(图2)。
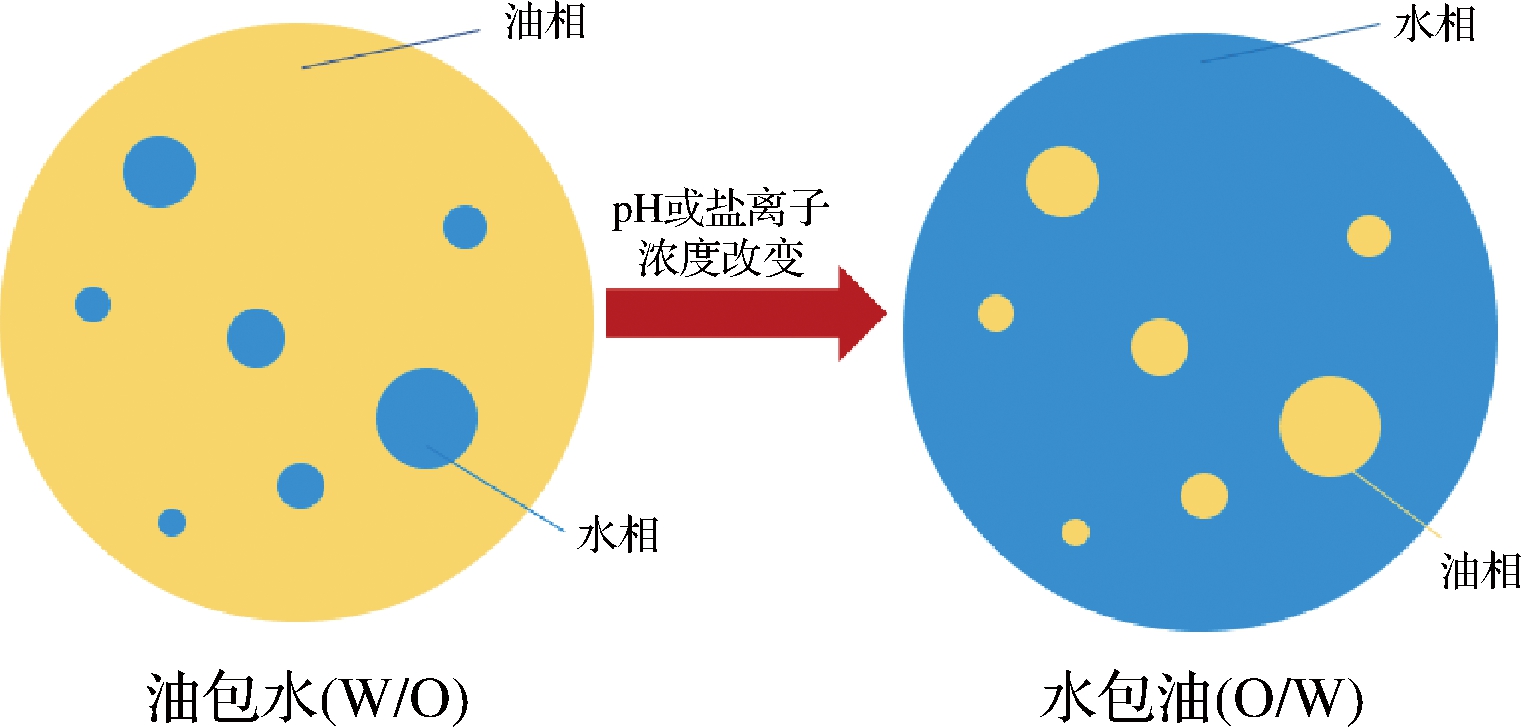
图2 组成相转变方法制备纳米乳液机制
Fig.2 Preparation of nanoemulsion mechanism by phase transformation method
在低温下,对温度敏感的表面活性剂具有亲水性和正的自发曲率,但随着温度的升高,它们变得更加疏水性和负的自发曲率[28]。HESSIEN等[29]采用吐温-80和司盘80,首先在高盐条件下制备了油包水乳液,通过向该体系添加水以降低体系盐离子浓度以改变表面活性剂分子曲率,使其在油水界面达到亲疏水平衡,继续添加将实现水包油纳米乳液。由于聚合物链脱水,聚氧乙烯等非离子表面活性剂经过连续的快速冷却和加热过程,在高温下具有亲脂性,在低温下具有亲水性。因此,水包油纳米乳液在低温条件下更稳定,而油包水纳米乳液在高温条件下更稳定。组成相转变方法是一种低成本的方法,容易扩大规模,通过控制温度从而产生所需的液滴尺寸。主要的缺点是它局限于非离子表面活性剂,可能需要大量的乳化剂[30]。
与组成相转变不同,突变相转变方法是通过改变表面活性剂-油-水组成比例来形成纳米乳液。如图3所示,在搅拌的状态下通过向特定表面活性剂与油的混合体系缓慢加入水,首先形成油包水普通乳液,增加水的量形成油水彼此交织的双连续相,持续加水最终将形成水包油纳米乳液。该方法的作用机制是当水的添加量超过一临界点时,最初油包水系统中形成的层状液晶结构会因水浓度的增加而膨胀,最终导致油包水结构的破裂并达到相转变点,形成水包油纳米乳液[31]。

图3 突变相转变方法制备纳米乳液机制
Fig.3 Mechanism of nano emulsion prepared by mutant phase transformation method
纳米乳液体系为热力学不稳定系统,通常会因奧氏熟化而造成体系物理不稳定。此外改变环境存储条件时,其稳定性也会发生改变,比如低温贮藏通常会出现沉淀。因此需改善技术,从而提高纳米乳液体外稳定性,并保持其自身高生物利用度特性。固体分散技术是将研究对象以分子、胶态、微晶等状态均匀分散在某一固体载体物质中,通过不同干燥技术,最终制成无定形固体分散体。固体分散技术最早用于增加难溶性药物的溶解度和溶出速率,同时延缓和控制药物释放[32]。此外,固体分散技术能够增加药物的稳定性,提高药物的生物利用度,因此被广泛应用于各种药物剂型的制备。运用固体分散技术所制备的纳米乳液固体分散体将同时具备纳米乳液的高生物利用率,及固体分散体的高溶解性和高稳定性。通过固体分散技术制备的纳米乳液固体分散体,一方面在体外可存储于各种低温状态并保持其物化稳定性,另一方面能有效保护生物活性物质顺利通过胃液,并经胃液及胃的蠕动下再次生成粒径<200 nm的微乳液进入人体小肠消化系统。这些细小微乳液的形成能有效增加其表面积,从而使其负载的生物活性物质能被肠壁细胞有效吸收,最终获得生物活性物质一致和可重复的生物利用度。
3 负载LC n-3 PUFA纳米乳液的应用
纳米乳液可以通过覆盖一层保护壁材料,封装必需脂肪酸、维生素、多肽、抗氧化剂、矿物质和益生菌等多种生物活性化合物,防止活性成分在食物中蒸发、化学反应或迁移,并在加工和储存时保持其稳定性,广泛应用于食品加工、生物、医药等多个领域[33]。
3.1 纳米乳液在食品体系中的涂层保护应用
纳米乳液包封亲脂成分可提高其处理和使用的便利性,促进其与产品的结合,通过改善亲脂化合物的性质增加生物利用度,控制其释放的速度或位置,保护其免受化学降解。深海鱼油含有大量的EPA和DHA 脂肪酸,具有众多生物活性并对多种疾病有预防作用,比如对心血管系统疾病、婴儿脑部与视力发育及部分癌症等有明显改善作用。由于人体自身不能有效合成EPA及DHA,因此需从外界食品中摄取,比如添加DHA的婴儿奶粉[34]。LC n-3 PUFA因其不完全水溶性及化学不稳定性,而不能作为直接食物原料。目前在食品中添加LC n-3 PUFA的方法是以经高压均质、干燥获得LC n-3 PUFA粉体为食品原料,添加入食品中。这一现有工艺最大的问题不仅是能耗高,而且由于LC n-3 PUFA化学稳定性差,极易发生脂肪氧化。有研究表明经高压均质后,由于机械操作过程温度的影响,包埋LC n-3 PUFA的乳液已开始氧化,这样的制备工艺必将影响其货架期。采用低能量制备的纳米乳液,并采用温和喷雾干燥条件配合最优固化剂,将纳米乳液固体分散,可保持LC n-3 PUFA化学稳定性。此外,纳米乳液在不同果蔬、粮油及肉制品的保鲜或稳定性中已显示出较好的效果,不仅对产品储藏期间的微生物种群数量、生化反应、生理褐变、氧化稳定性起到积极作用,而且应用领域也日趋广泛。具体应用及影响效果见表2。
表2 纳米乳液在食品体系的应用及其影响效果
Table 2 Application and effect of nano-emulsion in food system

食品加工类型液滴尺寸对产品的影响保质期文献来源甜瓜-蜜瓜放入纳米乳剂中浸泡1 min,干燥30 min10~20 nm对沙门菌和李斯特菌的抑菌活性降低3.5~7.7 lg CFU/g-[35]果汁-苹果、芒果等采用微流态化法制备黑孜然和姜黄精油纳米乳11~43 nm未经高温消毒的果汁在环境温度下保存状态稳定7 d[36]苹果汁通过微流态化制备纳米乳液,并将其加入到苹果汁中60~82 mm通过抑制多酚活性抑制褐变达48 h褐变推迟48 h[37]鲜切苹果采用转子-静相均质法制备Nopal胶浆纳米乳液,将切好的果核苹果浸入纳米乳液中涂覆<200 nm果胶甲基酯酶活性降低,多酚氧化酶活性降低65%,减少褐变21 d[36]圣女果用高压均质法制备的纳米乳液与海藻酸钠溶液混合,浸在番茄上形成涂层176.8 m减少总细菌计数<4.5 lg CFU/g,未包衣番茄的细菌载量为>6 lg CFU/g14 d[38]秋葵荚将超声纳米乳剂喷淋到秋葵表面<100 nm与对照相比,色泽、质地和整体可接受性较好,对真菌病原体有较高的抑制作用15 d[13]芹菜用超声法制备纳米乳液,将新鲜芹菜浸入纳米乳液中226~546 nm在60 min内,单核增生李斯特菌数量减少50%,细菌减少5个lg CFU/g7 d[39]虹鳟鱼将鱼片浸入超声波制备的纳米乳液59~112 nm提高鱼肉质量,减缓微生物生长21 d[16]鲜切牛肉通过超声处理,加入增塑剂,形成浸入肉中的涂层基141.2~145.1 nm与未包膜肉相比,总活菌计数分别减少了4.14和5.71 lg CFU/g8 d[40]鸡饼纳米乳由相反相组成,并掺入其中180~200 nm抑制脂肪氧化,感官特性稳定24周[41]鸡肉片用姜黄素-肉桂精油纳米乳液(CCN)、姜黄素-大蒜精油纳米乳液(CGN)、姜黄素-向日葵油纳米乳液(CSN)和果胶配制,将肉片浸入包覆的乳液中130 nm总细菌生长减少了97.8%,CCN、CGN和CSN分别减少了95.1%、72.9%和42.6%12 d[42]全脂牛奶采用高压匀浆器制备纳米乳,并加入全脂牛奶中471 nm60 min内自由基清除的潜力为11%,在储存期结束时没有阶段性分离10 d[43]松糕红洋葱皮提取液以海藻酸钠溶解,并加入蛋糕混合物8.3~13.6 nm在66~80 ℃烘烤后保持稳定,具有更高的感官可接受性-[44]
3.2 纳米乳液在食品体系中的功效维护应用
纳米乳液的另一个优势是能提高其负载活性物质的生物利用度,因此LC n-3 PUFA的生物活性也可能因其承载体纳米乳液自身特性,而显著提高[45]。从营养学的角度,提高具有特殊营养功能活性物质的生物利用度,有利于其生物活性在人体的利用,但目前并不清楚纳米乳液负载生物活性物质生物利用度的过度提高,是否会对人体造成负面影响[46]。纳米乳液系统在提高食品基质中疏水化合物的溶解度、生物利用度和功能性方面具有更高的潜力。封装还有助于通过提供亲水涂层或机械应力增加脂溶性成分的溶解度,如脂溶性维生素(β-胡萝卜素),天然香料(辣椒素、柠檬醛)和某些抗氧化剂(白藜芦醇)。目前,对LC n-3的每日推荐用量是650~1 000 mg,而过多食用可能导致因血小板聚集造成的出血不止。理论上,纳米乳液负载的LC n-3 PUFA因可能的生物利用度提高而对人体产生类似出血不止的剂量将低于其被普通食品负载所需的剂量[47]。因此,目前建立的LC n-3 PUFA每日推荐量可能不再适用于其被纳米尺寸载体负载的食品或饮料,在固化纳米乳液等纳米食品进入市场前,应对其所负载生物活性物质的生物利用度进行系统评价[48]。
4 展望
低能量方法制备食品纳米乳液并最终固化,是纳米技术中最为便捷的可用于重塑食品功能的途径。我国对功能性食品纳米乳液的研究处于起步阶段,尤其对负载生物活性脂质纳米乳液固体分散自身物性及对生物利用度的改变和评价的研究相对较少,在将其成功应用于食品工业之前,仍有一些瓶颈亟待解决:如何选择高效的工艺过程,利用食品级原料制备纳米乳液;如何合理设计纳米乳液颗粒,使其负载的功能物质获得特殊的功能性;如何成功的将负载功能物质的纳米乳液整合进入食品主体,在不同储藏条件下保持物理稳定,并不影响食品固有品质;如何正确评估负载功能物质纳米乳液的生物利用度等都是该领域未来亟待解决的问题。选择低能量制备方法及相关固体分散技术的研究不仅将对相关领域研究提供新的思路,所取得的研究成果对于开发安全无毒、负载其他生物活性脂质的食品纳米乳液及固体分散体也将具有借鉴意义,为我国食品工业功能食品领域在国际市场上的拓展提供新的解决途径。
[1] HOSSEINI S F, RAMEZANZADE L, MCCLEMENTS D J.Recent advances in nanoencapsulation of hydrophobic marine bioactives:Bioavailability, safety, and sensory attributes of nano-fortified functional foods[J].Trends in Food Science & Technology, 2021, 109:322-339.
[2] GHAYOUR N, HOSSEINI S M H, ESKANDARI M H, et al.Nanoencapsulation of quercetin and curcumin in casein-based delivery systems[J].Food Hydrocolloids, 2019, 87:394-403.
[3] 夏天航, 魏子淏, 马磊, 等.负载虾青素的油凝胶纳米乳液的构建及体外消化研究[J].食品与发酵工业, 2021, 47(9):1-7.
XIA T H, WEI Z H, MA L, et al.The development and its digestion study of astaxanthin-loaded oleogel-based nanoemulsions in vitro[J].Food and Fermentation Industries, 2021, 47(9):1-7.
[4] DELSHADI R, BAHRAMI A, MCCLEMENTS D J, et al.Development of nanoparticle-delivery systems for antiviral agents:A review[J].Journal of Controlled Release, 2021, 331:30-44.
[5] ZHOU H L, ZHENG B J, MCCLEMENTS D J. Encapsulation of lipophilic polyphenols in plant-based nanoemulsions: Impact of carrier oil on lipid digestion and curcumin, resveratrol and quercetin bioaccessibility[J]. Food & Function, 2021, 12(8):3 420-3 432.
[6] ZHOU H L, ZHENG B J, MCCLEMENTS D J.Encapsulation of lipophilic polyphenols in plant-based nanoemulsions:Impact of carrier oil on lipid digestion and curcumin, resveratrol and quercetin bioaccessibility[J].Food & Function, 2021, 12(8):3 420-3 432.
[7] SEHL A, COUЁDELO L, VAYSSE C, et al.Intestinal bioavailability of n-3 long-chain polyunsaturated fatty acids influenced by the supramolecular form of phospholipids[J].Food & Function, 2020, 11(2):1 721-1 728.
[8] THANATUKSORN P, KAWAI K, HAYAKAWA M, et al.Improvement of the oral bioavailability of coenzyme Q10 by emulsification with fats and emulsifiers used in the food industry[J].LWT - Food Science and Technology, 2009, 42(1):385-390.
[9] NIU Z G, ACEVEDO-FANI A, MCDOWELL A, et al.Nanoemulsion structure and food matrix determine the gastrointestinal fate and in vivo bioavailability of coenzyme Q10[J].Journal of Controlled Release, 2020, 327:444-455.
[10] SHEN J C, PAN X M, BHATIA S R.Self-assembly and thermoreversible rheology of perfluorocarbon nanoemulsion-based gels with amphiphilic copolymers[J].Colloids and Surfaces B:Biointerfaces, 2021, 202:111641.
[11] WANG Q, WEI H H, DENG C F, et al.Improving stability and accessibility of quercetin in olive oil-in-soy protein isolate/pectin stabilized O/W emulsion[J].Foods (Basel, Switzerland), 2020, 9(2):123.
[12] XU J, MUKHERJEE D, CHANG S K C.Physicochemical properties and storage stability of soybean protein nanoemulsions prepared by ultra-high pressure homogenization[J].Food Chemistry, 2018, 240:1 005-1 013.
[13] GUNDEWADI G, RUDRA S G, SARKAR D J, et al.Nanoemulsion based alginate organic coating for shelf life extension of okra[J].Food Packaging and Shelf Life, 2018, 18:1-12.
[14] PRAKASH A, BASKARAN R, VADIVEL V.Citral nanoemulsion incorporated edible coating to extend the shelf life of fresh cut pineapples[J].LWT, 2020, 118:108851.
[15] VAISHANAVI S, PREETHA R.Soy protein incorporated nanoemulsion for enhanced stability of probiotic (Lactobacillus delbrueckii subsp.bulgaricus) and its characterization[J].Materials Today:Proceedings, 2021, 40:S148-S153.
[16] OZOGUL Y, YUVKA ![]() UCAR Y, et al.Evaluation of effects of nanoemulsion based on herb essential oils (rosemary, laurel, thyme and sage) on sensory, chemical and microbiological quality of rainbow trout (Oncorhynchus mykiss) fillets during ice storage[J].LWT, 2017, 75:677-684.
UCAR Y, et al.Evaluation of effects of nanoemulsion based on herb essential oils (rosemary, laurel, thyme and sage) on sensory, chemical and microbiological quality of rainbow trout (Oncorhynchus mykiss) fillets during ice storage[J].LWT, 2017, 75:677-684.
[17] KEYKHOSRAVY K, KHANZADI S, HASHEMI M, et al.Chitosan-loaded nanoemulsion containing Zataria multiflora Boiss and Bunium persicum Boiss essential oils as edible coatings:Its impact on microbial quality of Turkey meat and fate of inoculated pathogens[J].International Journal of Biological Macromolecules, 2020, 150:904-913.
[18] LIU Q, ZHANG M, BHANDARI B, et al.Effects of nanoemulsion-based active coatings with composite mixture of star anise essential oil, polylysine, and nisin on the quality and shelf life of ready-to-eat Yao meat products[J].Food Control, 2020, 107:106771.
[19] SHOKRI S, PARASTOUEI K, TAGHDIR M, et al.Application an edible active coating based on chitosan- Ferulago angulata essential oil nanoemulsion to shelf life extension of rainbow trout fillets stored at 4 ℃[J].International Journal of Biological Macromolecules, 2020, 153:846-854.
[20] ARTIGA-ARTIGAS M, ACEVEDO-FANI A, MART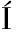 N-BELLOSO O.Improving the shelf life of low-fat cut cheese using nanoemulsion-based edible coatings containing oregano essential oil and mandarin fiber[J].Food Control, 2017, 76:1-12.
N-BELLOSO O.Improving the shelf life of low-fat cut cheese using nanoemulsion-based edible coatings containing oregano essential oil and mandarin fiber[J].Food Control, 2017, 76:1-12.
[21] CHEN W Y, JU X R, ALUKO R E, et al.Rice bran protein-based nanoemulsion carrier for improving stability and bioavailability of quercetin[J].Food Hydrocolloids, 2020, 108:106042.
[22] WANG Q, REN Y R, DING Y P, et al.The influence of pH and enzyme cross-linking on protein delivery properties of WPI-beet pectin complexes[J].Food Research International, 2018, 105:678-685.
[23] PEREIRA S F, BARROSO A, MOUR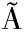 O R H V, et al.A low energy approach for the preparation of nano-emulsions with a high citral-content essential oil[J].Molecules (Basel, Switzerland), 2021, 26(12):3666.
O R H V, et al.A low energy approach for the preparation of nano-emulsions with a high citral-content essential oil[J].Molecules (Basel, Switzerland), 2021, 26(12):3666.
[24] GLEDOVIC A, JANOSEVIC LEZAIC A, NIKOLIC I, et al.Polyglycerol ester-based low energy nanoemulsions with red raspberry seed oil and fruit extracts:Formulation development toward effective in vitro/in vivo bioperformance[J].Nanomaterials (Basel, Switzerland), 2021, 11(1):217.
[25] HANDA M, UJJWAL R R, VASDEV N, et al.Optimization of surfactant- and cosurfactant-aided pine oil nanoemulsions by isothermal low-energy methods for anticholinesterase activity[J].ACS Omega, 2020, 6(1):559-568.
[26] BAHUGUNA A, RAMALINGAM S, KIM M.Formulation, characterization, and potential application of nanoemulsions in food and medicine.In Nanotechnology for food, agriculture, and environment[M].Cham:Springer,2020:39-61.
[27] AZMI N A N, ELGHARBAWY A A M, MOTLAGH S R, et al.Nanoemulsions:factory for food, pharmaceutical and cosmetics[J].Processes, 2019, 7(9):617.
[28] JIANG T, LIAO W, CHARCOSSET C.Recent advances in encapsulation of curcumin in nanoemulsions:A review of encapsulation technologies, bioaccessibility and applications[J].Food Research International, 2020, 132:109035.
[29] HESSIEN M, SINGH N, KIM C, et al.Stability and tunability of O/W nanoemulsions prepared by phase inversion composition[J].Langmuir, 2011, 27(6):2 299-2 307.
[30] ESPITIA P J P, FUENMAYOR C A, OTONI C G.Nanoemulsions:synthesis, characterization, and application in bio-based active food packaging[J].Comprehensive Reviews in Food Science and Food Safety, 2019, 18(1):264-285.
[31] MARTIN-PI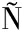 ERO M J, MU
ERO M J, MU OZ J, ALFARO-RODRIGUEZ M C.Improvement of the rheological properties of rosemary oil nanoemulsions prepared by microfluidization and vacuum evaporation[J].Journal of Industrial and Engineering Chemistry, 2020, 91:340-346.
OZ J, ALFARO-RODRIGUEZ M C.Improvement of the rheological properties of rosemary oil nanoemulsions prepared by microfluidization and vacuum evaporation[J].Journal of Industrial and Engineering Chemistry, 2020, 91:340-346.
[32] LI Y, MEI L, GUAN X Y, et al.Ellagic acid solid dispersion:Characterization and bioactivity in the hydroxyl radical oxidation system[J].Food Research International, 2021, 142:110184.
[33] 王强, 李琳, 鞠兴荣, 等.多尺度结构变化与食品品质功能调控研究进展[J].中国食品学报, 2022, 22(1):1-11.
WANG Q, LI L, JU X R, et al.Research progress on multi-scale structure change and quality function of food[J].Journal of Chinese Institute of Food Science and Technology, 2022, 22(1):1-11.
[34] ALI M, IMRAN M, KHAN M K, et al.Functional and oxidative quality characterization of spray-dried omega-3-enriched milk powder[J].Journal of Food Quality, 2021, 2021:6693960.
[35] PAUDEL S K, BHARGAVA K, KOTTURI H.Antimicrobial activity of cinnamon oil nanoemulsion against Listeria monocytogenes and Salmonella spp.on melons[J].LWT, 2019, 111:682-687.
[36] FRANKLYNE J S, IYER S, EBENAZER A, et al.Essential oil nanoemulsions:Antibacterial activity in contaminated fruit juices[J].International Journal of Food Science & Technology, 2019, 54(9):2 802-2 810.
[37] XU J, ZHOU L, MIAO J Y, et al.Effect of cinnamon essential oil nanoemulsion combined with ascorbic acid on enzymatic browning of cloudy apple juice[J].Food and Bioprocess Technology, 2020, 13(5):860-870.
[38] PIROZZI A, DEL GROSSO V, FERRARI G, et al.Edible coatings containing oregano essential oil nanoemulsion for improving postharvest quality and shelf life of tomatoes[J].Foods (Basel, Switzerland), 2020, 9(11):1605.
[39] D VILA-RODR
VILA-RODR GUEZ M, L
GUEZ M, L PEZ-MALO A, PALOU E, et al.Antimicrobial activity of nanoemulsions of cinnamon, rosemary, and oregano essential oils on fresh celery[J].LWT, 2019, 112:108247.
PEZ-MALO A, PALOU E, et al.Antimicrobial activity of nanoemulsions of cinnamon, rosemary, and oregano essential oils on fresh celery[J].LWT, 2019, 112:108247.
[40] GHANI S, BARZEGAR H, NOSHAD M, et al.The preparation, characterization and in vitro application evaluation of soluble soybean polysaccharide films incorporated with cinnamon essential oil nanoemulsions[J].International Journal of Biological Macromolecules, 2018, 112:197-202.
[41] DE CARLI C, MORAES-LOVISON M, PINHO S C.Production, physicochemical stability of quercetin-loaded nanoemulsions and evaluation of antioxidant activity in spreadable chicken p tés[J].LWT, 2018, 98:154-161.
tés[J].LWT, 2018, 98:154-161.
[42] ABDOU E S, GALHOUM G F, MOHAMED E N.Curcumin loaded nanoemulsions/pectin coatings for refrigerated chicken fillets[J].Food Hydrocolloids, 2018, 83:445-453.
[43] GOLFOMITSOU I, MITSOU E, XENAKIS A, et al.Development of food grade O/W nanoemulsions as carriers of vitamin D for the fortification of emulsion based food matrices:A structural and activity study[J].Journal of Molecular Liquids, 2018, 268:734-742.
[44] MAHMOUD K F, HAMMOUDA A Z, ALI H S, et al.Efficiency of red onion peel extract capsules on obesity and blood sugar[J].Pakistan Journal of Biological Sciences:PJBS, 2021, 24(1):99-111.
[45] MITRUS O, ![]() M, LOSADA-BARREIRO S, et al.Targeting antioxidants to interfaces:Control of the oxidative stability of lipid-based emulsions[J].Journal of Agricultural and Food Chemistry, 2019, 67(11):3 266-3 274.
M, LOSADA-BARREIRO S, et al.Targeting antioxidants to interfaces:Control of the oxidative stability of lipid-based emulsions[J].Journal of Agricultural and Food Chemistry, 2019, 67(11):3 266-3 274.
[46] KALININA I, POTOROKO I, NENASHEVA A, et al.Prospects for the application of taxifolin based nanoemulsions as a part of sport nutrition products[J].Human Sport Medicine, 2019,19(1):100-107.
[47] SHAFIQ M, ANJUM S, HANO C, et al.An overview of the applications of nanomaterials and nanodevices in the food industry[J].Foods (Basel, Switzerland), 2020, 9(2):148.
[48] CHEN Z J, HAN S, ZHOU S P, et al.Review of health safety aspects of titanium dioxide nanoparticles in food application[J].NanoImpact, 2020, 18:100224.