在全球浓缩果汁消费量中浓缩苹果汁占比最大,而我国是最大的生产国和出口国[1-3]。在浓缩苹果汁生产工艺中,浓缩步骤尤为重要[4-5]。传统的浓缩方式有蒸发浓缩、冷冻浓缩、膜浓缩等,其中运用最为广泛的是膜浓缩[6],膜技术中有纳滤、超滤、反渗透膜等[7]。安晓婵等[8]研究发现在常压下实现热敏料液低温浓缩,且膜通量和热效率均较适宜的液隙式膜蒸馏方法,并对11 °Brix的澄清苹果汁进行了浓缩试验;也有研究采用超滤、反渗透技术浓缩黑果枸杞花青素,并根据浓缩前后可溶性固形物含量的变化规律,确定最佳工艺条件[9]。传统的膜浓缩属于压力推动膜过程[10],均需要加压,存在严重的膜污染。正渗透技术是一种新型膜分离技术,具有无需外加压力、低膜污染等优点[11-12]。正渗透膜主要有三醋酸纤维素(cellulose triacetate,CTA)膜和薄膜复合材料(thin film composite,TFC)膜2种。CTA拥有良好的亲水性、耐氯性且简单易得[13]。TFC具有高渗透选择性且更薄,可减少浓差极化[14]。正渗透膜由活性层和支撑层组成[15]。当活性层朝向原料液(active layer-feed solution,AL-FS)时为正渗透模式(forward osmosis,FO),活性层朝向汲取液(active layer-draw solution,AL-DS)时为压力延迟渗透模式(pressure retarded osmosis,PRO)[16],有研究通过在聚砜支撑层背面构建碳纳米管(carbon nanotubes,CNT)抗污染层,在支撑层表面界面聚合制备高性能聚酰胺复合正渗透膜,并应用于果汁浓缩[17]。目前,正渗透技术浓缩苹果汁尚在实验室阶段,没有形成工业生产模式,主要是由于正渗透浓缩过程中的反向渗透扩散(reverse solute flux,RSF)问题没有解决。RSF是汲取液溶质穿过正渗透膜进入原料液(即果汁)中,从而降低了浓缩果汁的质量,还会引起浓差极化[18-19]。弄清在正渗透浓缩苹果汁过程中汲取液溶质反向扩散规律,将会极大推动正渗透技术在浓缩苹果汁行业的应用和新型汲取液开发,从而有利于解决我国果汁浓缩技术瓶颈等重大问题[20]。
苹果汁成分复杂,主要有糖类、小分子酚类和维生素等物质,糖类影响液体的流动性,也影响正渗透过程的浓缩性能,为了深入探究正渗透浓缩苹果汁技术中汲取液的选择和RSF规律,本研究将苹果汁中几种主要糖抽象出来形成模拟苹果汁,探究各种汲取液浓缩模拟果汁的可行性和对RSF的影响,以期寻找更适合苹果汁浓缩过程的膜操作模式、汲取液浓度及汲取液的选择。
1 材料与方法
1.1 实验仪器及药品
1.1.1 材料与试剂
氯化钠、D(-)-果糖、D(+)-无水葡萄糖、蔗糖、无水乙酸钠、无水柠檬酸钠,国药集团化学试剂有限公司。
1.1.2 仪器与设备
台式电导率仪、pH计,梅特勒-托利多仪器(上海)有限公司;电子天平,美国新诺双杰;蠕动泵,兰格恒流泵有限公司;正渗透装置(有机玻璃反应器),私人订制;TFC正渗透膜,国初科技(厦门)有限公司。
1.2 实验装置及实验方法
1.2.1 实验装置
实验装置主要由压力泵、正渗透装置组成(图1)。正渗透装置包括2个完全相同的腔室,原料液室和汲取液室,2个腔室由FO膜隔开。FO膜使用的是TFC膜,两室通过硅胶软管与两边的储水罐相连。原料液的贮水罐放在1个通过计算机监测的电子天平上,方便测量数据。汲取液室的硅胶软管通过压力泵和储水罐相连。压力泵主要是控制流速。

图1 正渗透装置示意图
Fig.1 Schematic diagram of forward osmosis device
1.2.2 实验方法
利用果汁成分中所含糖类的相对含量为葡萄糖3.1 g/100 g、果糖5.5 g/100 g、蔗糖1.5 g/100 g,分别配制成3种糖混合溶液、葡萄糖溶液、果糖溶液、蔗糖溶液构建模拟果汁体系,设置泵的转速为90 r/min进行正渗透浓缩实验。
1.2.2.1 不同糖度溶液作为原料液以及膜活性层朝向对浓缩性能的影响
利用1 000 mL的4 mol/L的NaCl溶液作为汲取液,混合糖溶液、葡萄糖溶液、果糖溶液、蔗糖溶液作为原料液,改变膜朝向进行FO模式和PRO模式的实验,2 min后测定汲取液质量、10 min后测定汲取液的电导率、pH、糖度,汲取液一侧的贮水罐放在1个通过计算机监测的电子天平上,记录2 min内的增加质量和22、72 h的累积增加质量,再通过监测贮水罐中质量的增加计算水通量。通过比较浓缩后果汁的糖度与原果汁的糖度计算浓缩倍数。根据汲取液浓度和电导率关系制作标准曲线,再通过公式(1)计算得到水通量,通过公式(2)计算得到RSF等。
水通量[L/(m2·h),LMH]计算如公式(1)所示:
(1)
式中:t,时间,h;mt,F,在t时刻缓冲罐和罐中原料液的质量,g;S,FO膜的表面积,m2;ρ,水的密度,g/L。
RSF指基于汲取液中汲取液溶质向原料液室的净迁移量,一般用Js表示。反向渗透通量[RSF,g/(m2·h),gMH]计算如公式(2)所示:
(2)
式中:Vf,D,汲取液/阴极液的最终体积,L;Vi,D,汲取液/阴极液的初始体积,L;Cf,D,汲取液/阴极液的最终质量浓度,g/L;Ci,D,汲取液/阴极液的初始质量浓度,g/L。
果汁浓缩倍数由果汁中的固形物含量白利糖度表示(degrees brix,符号°Bx),浓缩倍数的计算如公式(3)所示:
浓缩倍数![]()
(3)
1.2.2.2 功能性汲取液对正渗透浓缩果汁的影响
在PRO模式下,原料液为混合糖溶液,分别以2 mol/L醋酸钠、4 mol/L醋酸铵、2 mol/L柠檬酸钠为汲取液测定功能性汲取液对正渗透浓缩果汁的影响。利用计算机监测的电子天平记录汲取液2 min的质量变化和22、48以及72 h的累计质量变化。前2 h,每隔10 min测定汲取液的pH、电导率、糖度变化。通过监测贮水罐中质量的增加计算水通量。通过比较浓缩后果汁的糖度与原果汁的糖度计算浓缩倍数。根据汲取液浓度和电导率关系制作标准曲线,再通过公式(2)计算得到RSF等。
2 结果与分析
2.1 不同糖度溶液作为原料液以及膜活性层朝向对浓缩性能的影响
2.1.1 水通量
为了研究苹果汁中糖成分对浓缩的影响,针对浓缩苹果汁中3种糖类(果糖、葡萄糖、蔗糖)[21],模拟了果汁体系并进行相关实验。浓缩苹果汁中,果糖含量>葡萄糖含量>蔗糖含量,按含量比例配成果糖溶液、葡萄糖溶液、蔗糖溶液以及3种糖混合溶液(55 g/100 g的果糖,31 g/100 g的葡萄糖,15 g/100 g的蔗糖)作为原料液。FO膜为非对称膜,支撑层面对原料液,活性层面对汲取液为PRO模式,反之为FO模式。
图2为不同膜操作形式以及不同糖溶液作为原料液时膜汲水能力的试验结果。其中,图2-a、图2-c为PRO模式,可以发现蔗糖溶液作为原料液时膜汲水能力最强,果糖和葡萄糖次之,混合糖最弱。蔗糖溶液作为原料液时,2 min平均吸水量为0.95 g,120 min时汲水量为58.02 g;混合糖溶液作为原料液时,2 min平均吸水量为0.39 g,120 min时汲水量为23.25 g。由于正渗透浓缩是以膜两侧溶液渗透压差为驱动力,实现物质分离,在温度一定时,溶液的渗透压力与溶液的浓度成正比,混合糖的浓度大,渗透压高,膜两侧的渗透压差降低。图2-b、图2-d为FO模式,与PRO模式结果类似。
对比图2-a和图2-b,混合糖、葡萄糖、果糖、蔗糖溶液作为原料液时,120 min的汲水量在PRO模式下分别为23.25、41.22、35.76、58.02 g,FO模式下分别为8.72、23.94、12.44、26.56 g;图2-e中,混合糖、葡萄糖、果糖、蔗糖溶液作为原料液时,PRO模式22 h的汲水量分别为(155.18±15.52)、(305.84±27.53)、(260.30±23.43)、(309.64±27.87)g,FO模式下分别为(76.60±6.51)、(164.58±14.15)、(92.44±8.32)、(208.26±17.91)g,由此发现,PRO模式下的吸水量整体都大于FO模式。对比图2-c和图2-d,120 min内,混合糖、葡萄糖、果糖、蔗糖溶液作为原料液时,PRO模式下的水通量分别为10.00~18.00、20.00~30.00、10.00~20.00、30.00~35.00 LMH,而FO模式下的水通量分别为1.00~8.00、10.00~20.00、5.00~10.00、10.00~15.00 LMH,发现PRO模式下的水通量整体都大于FO模式。由于2种操作模式下的膜两侧本体溶液的浓度差相同,则可能是FO模式下存在更明显的浓差极化从而导致浓缩过程中性层两侧的渗透压差降低,有效推动力降低。

a-PRO模式下吸水量;b-FO模式下吸水量;c-PRO模式下水通量;d-FO模式下水通量;e-22 h累积汲水量
图2 不同膜操作形式以及不同糖度溶液作为原料液对汲水能力的影响
Fig.2 Effect of different sugar feed solutions on water extraction capacity in different membrane modes
2.1.2 反向溶质扩散
由图3可知,在PRO模式下,4种不同糖度的反向渗透通量都随着时间的增加而减小,在120 min时,最高的反向渗透通量为混合糖,为100.00~167.70 gMH,最低的反向渗透通量为蔗糖,为50.00~100.00 gMH,由图3-a可知,蔗糖反向渗透通量始终小于另外3种;在FO模式下,4种糖度的反向渗透通量也随着时间的增加而减小,在120 min时,最高的反向渗透通量为混合糖,为167.72~377.18 gMH,最低的反向渗透通量为蔗糖,为133.95~233.46 gMH(图3-b),结果与PRO模式相同。由于反向渗透通量越高,水通量越小,则正渗透浓缩果汁效率越低。在120 min内,PRO模式下最高的反向渗透比FO模式下最低的反向渗透通量都要低。在120 min以内,PRO模式下的反向渗透百分比始终低于FO模式下的反向渗透百分比,而最终22 h时,PRO模式下反向渗透通量更少。说明PRO模式下与RO模式相比,反向渗透通量越小,水通量越大,更有利于浓缩果汁。在PRO模式中,0~120 min,葡萄糖的反向渗透通量增长幅度最低,蔗糖次之,混合糖最高;而反渗百分比中,最高反渗百分比为(0.19±0.018)%,相比FO模式要小得多。反向渗透在PRO模式下的影响是较小的。22 h时,PRO模式下蔗糖的反向渗透通量最低。葡萄糖的反向渗透通量越低,水通量越大,在浓缩果汁过程中对正渗透影响越小。
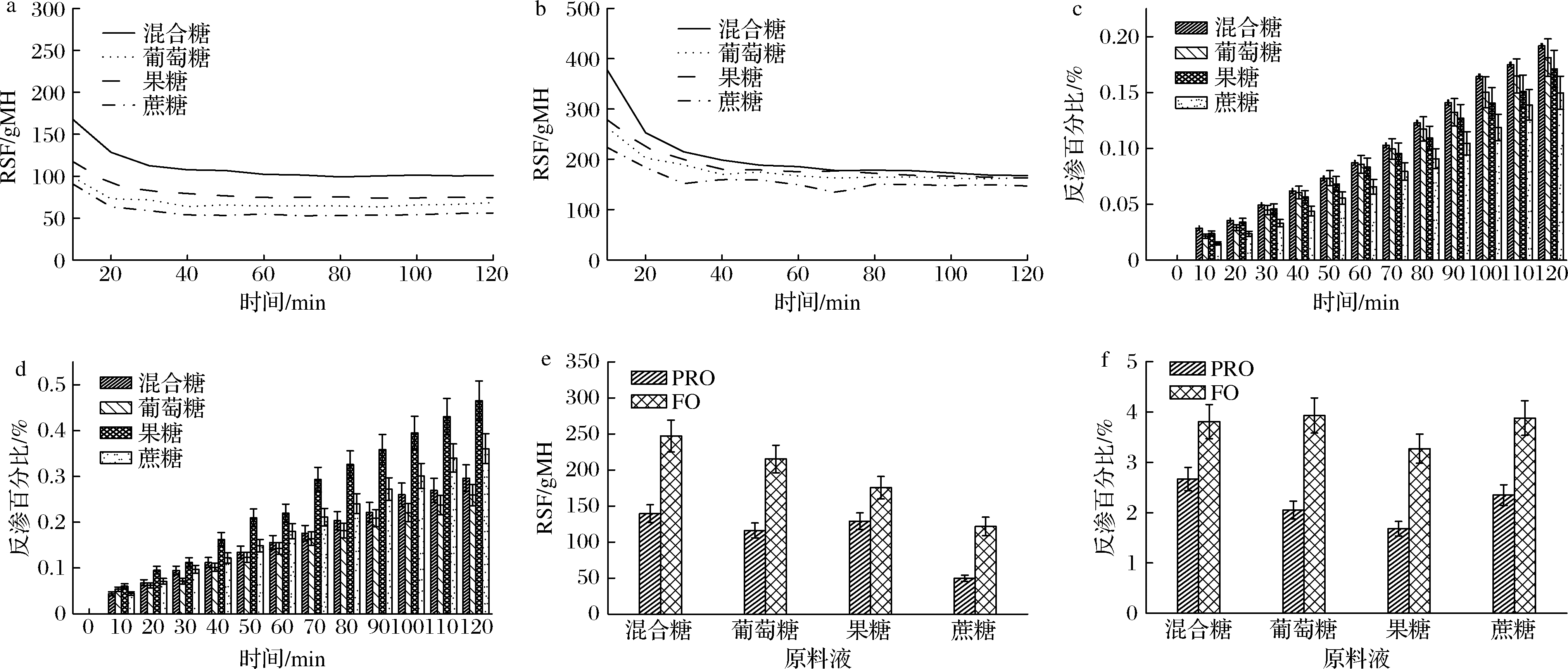
a-PRO模式下RSF;b-FO模式下RSF;c-PRO模式下反渗百分比;d-FO模式下反渗百分比;e-22 h累计反向渗透通量;f-22 h累计反向渗透百分比
图3 不同模式下不同糖度溶液作为原料液对反向溶质扩散的影响
Fig.3 Effect of different sugar content solutions as feed solution on reverse solute flux in different membrane modes
2.1.3 pH
检测混合糖、葡萄糖、果糖和蔗糖原料液在反应前2 h的pH值,发现不论是在FO模式还是PRO模式下,原料液的pH数值始终在6.0附近波动。说明在正渗透浓缩模拟果汁体系中,膜两侧pH变化不大,大致都在6.0左右,这可能是因为膜两侧的溶液pH相差不大并且都接近于中性。因此,NaCl汲取液不会对模拟果汁体系的pH产生影响,实际果汁体系中维生素和酸性小分子等物质在正渗透膜侧穿梭可能会导致pH的变化,在今后实际体系的研究中需继续对pH进行检测。

图4 不同模式以及不同糖度溶液作为原料液的pH
Fig.4 pH of different modes and different sugar content solutions as feed solution
2.2 功能性汲取液对正渗透浓缩果汁的影响
反向渗透的溶质源自于汲取液,汲取液的性质决定了反渗溶质的性质和反向扩散系数。汲取液是正渗透技术中至关重要的一部分,是决定正向渗透过程的核心因素。无机汲取液中氯化钠凭借其高溶解度、高渗透压及价格低廉,成为目前应用最广泛的汲取液,但是由于氯离子和钠离子的离子半径较小,反向溶质扩散现象比较严重。有机汲取液能够获得较高的水通量和较低的双向溶质扩散[22]。基于汲取液调控是控制反向溶质扩散的主要途径之一,反向溶质扩散无法彻底消除易造成苹果汁溶液盐度或杂质积累以及苹果汁易被氧化而发生褐变,因此使用稳定剂类、抗氧化剂类功能性汲取液,利用反向扩散溶质将功能因子缓释添加到浓缩中的苹果汁中,强化浓缩苹果汁稳定性。醋酸钠在食品中可用作稳定剂和pH调节剂,可缓和不良气味并防止变色及改善风味,其在水中溶解度约为5.60 mol/L,由于实际操作中较难达到最高溶解度,故选择4 mol/L浓度来进行实验;柠檬酸钠在食品、饮料工业中用作防腐剂和稳定剂,有螯合金属离子的功能,起到抗氧化的效果,其在25 ℃常温下水中溶解度为720 g/L,即2.45 mol/L,实际操作中较难达到最高溶解度,故选择2 mol/L浓度进行实验。
2.2.1 吸水量
由图5分析4 mol/L氯化钠(无机汲取液)和4 mol/L醋酸钠(有机阴离子汲取液)分别作为汲取液时,水通量、实时吸水量以及72 h的吸水量,对比发现4 mol/L醋酸钠作为汲取液时,水通量值略高于4 mol/L氯化钠汲取液。图5-b和图5-c中,4 mol/L醋酸钠作为汲取液时,2 min平均吸水量为0.42 g,120 min时汲水量为24.95 g,72 h的汲水量为(436.21±42.75)g;4 mol/L氯化钠作为汲取液时,2 min平均吸水量为0.39 g,120 min时汲水量为23.25 g,72 h的汲水量为(368.26±33.11)g。因此醋酸钠作为汲取液时吸水量较氯化钠高,膜的汲水能力较氯化钠强,有机溶质中引入电荷能增加渗透压[23],且有机离子汲取液可以有效降低反应器中盐度的积累。
再对比图5中2 mol/L醋酸钠溶液和2 mol/L柠檬酸钠溶液分别作为汲取液时2 h内的水通量、吸水量以及72 h的吸水量,发现相同摩尔浓度的柠檬酸钠汲取液和醋酸钠汲取液在前2 h时产生的水通量接近。2 mol/L醋酸钠作为汲取液时,2 min平均吸水量为0.26 g,120 min时汲水量为15.88 g,72 h的汲水量为(363.54±28.36)g;2 mol/L柠檬酸钠作为汲取液时,2 min平均吸水量为0.28 g,120 min时汲水量为16.94 g,72 h的汲水量为(330.03±30.02)g。但在72 h柠檬酸钠汲取液的吸水量更大,说明柠檬酸钠汲取液汲水的持续性更好,可以在长时间内保持较高的水通量。
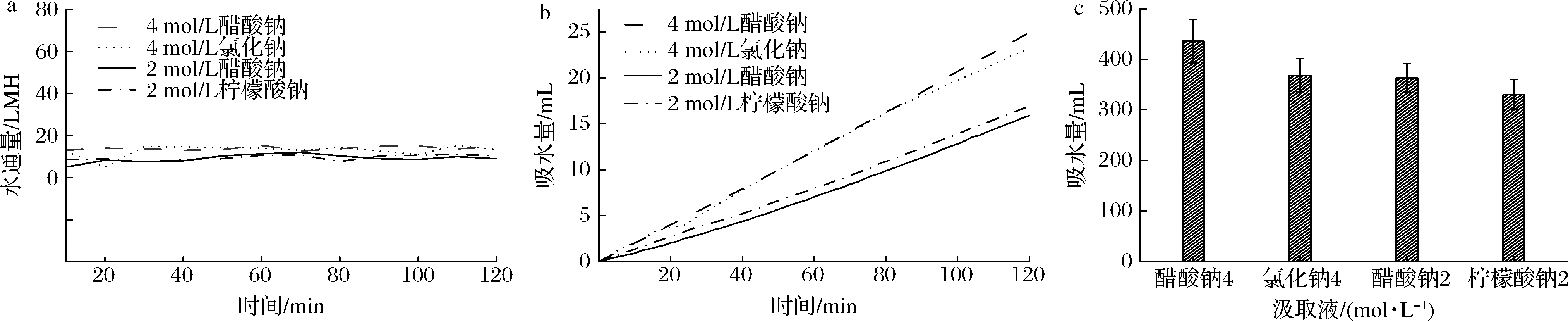
a-水通量;b-吸水量;c-72 h累积吸水量
图5 功能性汲取液对浓缩果汁的影响
Fig.5 Effect of functional draw solution on concentrated apple juice
2.2.2 糖度和pH
图6-a为PRO模式下不同功能性汲取液的原料液的初始和72 h最终糖度,4 mol/L醋酸钠作为汲取液时,初始糖度为(5.3±0.5)°Baume,72 h试验后糖度为(7.0±0.6)°Baume,浓缩倍数约为1.4;2 mol/L醋酸钠作为汲取液时,初始糖度为(5.1±0.4)°Baume,72 h试验后糖度为(6.3±0.6)°Baume,浓缩倍数为1.2;2 mol/L柠檬酸钠作为汲取液时,初始糖度为(5.2±0.47)°Baume,72 h试验后糖度为(7.0±0.6)°Baume,浓缩倍数约为1.4。因此柠檬酸钠作为汲取液时浓缩倍数较大,更适用于浓缩苹果汁。
图6-b为PRO模式下不同功能性汲取液中,72 h内pH变化。当氯化钠作为汲取液时,72 h时pH为(5.92±0.011),与其他几种汲取液比较,pH变化较小,而2 mol/L醋酸钠变化较大,72 h时为(6.76±0.13)。不同汲取液,pH不同,但是pH之差都<1,表明功能性汲取液对pH的影响较小,但是不可忽略。
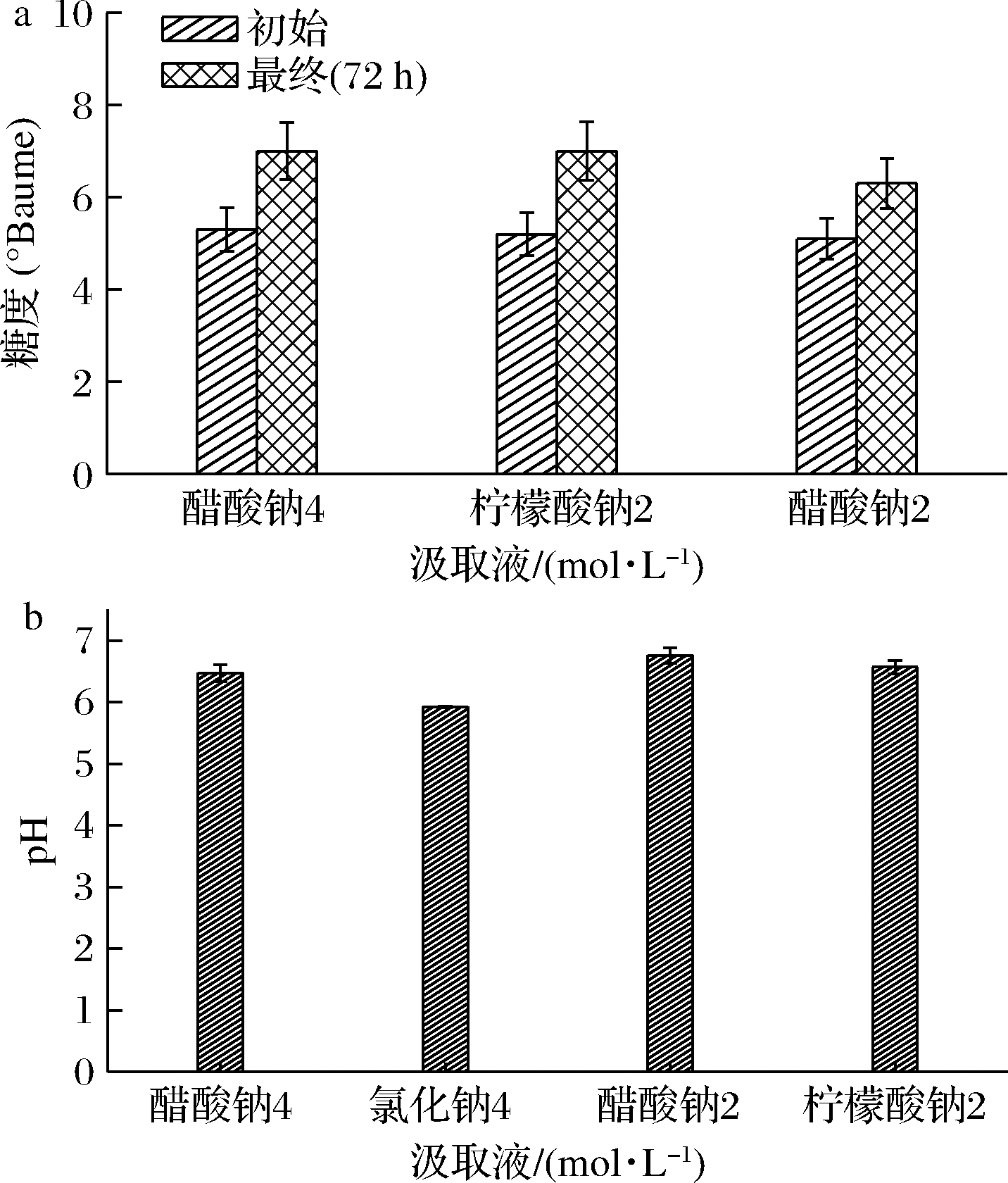
a-糖度;b-pH
图6 不同功能性汲取液下模拟苹果汁的状态
Fig.6 The condition of simulated apple juice with different functional draw solution
2.2.3 反向溶质扩散
如图7所示,在120 min内,4 mol/L醋酸钠汲取液和4 mol/L氯化钠汲取液的反向渗透通量都随时间的增加而减小,但氯化钠的增幅比醋酸钠高;氯化钠的反渗百分比始终比醋酸钠高,但是都没有超过0.2%。在120 min时,氯化钠的反向渗透通量为100.66 gMH,而醋酸钠为63.57 gMH。即醋酸钠比氯化钠总体反向通量小,水通量大,更有利于浓缩果汁;而在120 min内,2 mol/L醋酸钠和2 mol/L柠檬酸钠反向渗透通量都在增加,但是醋酸钠的增幅更大;而醋酸钠的反渗百分比较柠檬酸钠高,但没有超过0.05%。在120 min时,醋酸钠的反向渗透通量为34.15 gMH,柠檬酸钠为19.79 gMH。整体来看,柠檬酸钠比醋酸钠的反向渗透通量更小,有利于水通量的增加,提高正渗透浓缩果汁的效率。

a-醋酸钠和氯化钠的RSF;b-醋酸钠和柠檬酸钠的RSF;c-醋酸钠和氯化钠的反渗百分比;d-醋酸钠和柠檬酸钠的反渗百分比
图7 不同功能性汲取液对反向溶质扩散的影响
Fig.7 Effects of different functional draw solution on reverse solute flux
3 结论
在不同糖度溶液作为原料液以及膜活性层朝向对浓缩性能的影响的探讨中,主要探究水通量、吸水量、反向溶质扩散、pH的变化。在混合糖、葡萄糖、果糖和蔗糖原料液中,葡萄糖原料液最有利于果汁浓缩,蔗糖原料液最次,果汁是一个混合体系,在不改变原料液中糖度的基础上,增加原料液中葡萄糖的比重,即可让果汁的浓缩率提高。而在膜朝向的实验中,相较而言,PRO模式比FO模式更有利于果汁浓缩。在PRO模式下功能性汲取液对正渗透浓缩果汁的影响的探讨中,运用了醋酸钠、柠檬酸钠、氯化钠作为功能性汲取液,通过水通量、吸水量、反向溶质扩散、糖度来进行比较,得到柠檬酸钠的反向渗透通量更小,有利于水通量的增加,最有利于正渗透浓缩果汁的效率,氯化钠最次。
[1] 刘英杰.中国苹果产业经济研究[D].北京:中国农业大学,2005.
LIU Y J.Apple industry in China[D].Beijing:China Agricultural University,2005.
[2] 秦泰. 中国苹果汁国际竞争力研究[D].杨凌:西北农林科技大学,2007.
QIN T.On the international competitiveness of apple juice in China[D].Yangling:Northwest Agriculture & Forestry University,2007.
[3] 陈芳, 曾令琴,葛毅强,等.浓缩苹果汁中农药残留去除方法的研究现状及展望[J].食品与发酵工业,2005,31(9):66-69.
CHEN F,ZENG L Q,GE Y Q,et al.Review on methods to reduce the residue of pesticides in concentrated apple juice[J].Food and Fermentation Industries,2005,31(9):66-69.
[4] 赵光远. 混浊苹果汁的研制及其储藏稳定性的研究[D].无锡:江南大学,2005.
ZHAO G Y.Studies on producing cloudy apple juice and storage stability of the products[D].Wuxi:Jiangnan University,2005.
[5] 韦建平. 陕西及全国浓缩苹果汁产业发展的现状与对策[D].杨凌:西北农林科技大学,2005.
WEI J P.Current situation and countermeasure for the development of Shaanxi and countrywide apple juice concentrate[D].Yangling:Northwest Agriculture & Forestry University,2005.
[6] 白小鸣, 王华,曾小峰,等.果汁浓缩技术概述[J].食品与发酵工业,2014,40(7):131-135.
BAI X M,WANG H,ZENG X F,et al.New advances of fruit juice concentration technology[J].Food and Fermentation Industries,2014,40(7):131-135.
[7] 王轩, 毕金峰,刘璇,等.高新技术在浓缩苹果汁加工中应用进展[J].食品与发酵工业,2012,38(6):139-143.
WANG X,BI J F,LIU X,et al.Research progress on application of innovative technologies in concentrated cider processing[J].Food and Fermentation Industries,2012,38(6):139-143.
[8] 安晓婵, 张翔宇,周宗尧,等.构建高性能复合正渗透膜及其在果汁浓缩中的应用[J].膜科学与技术,2018,38(4):99-106.
AN X C,ZHANG X Y,ZHOU Z Y,et al.Fabrication of high performance thin film composite forward osmosis membranes and its application for juice concentration[J].Membrane Science and Technology,2018,38(4):99-106.
[9] 于佳男, 陈东,曹莹莹,等.液隙式膜蒸馏常压低温浓缩果汁研究[J].包装与食品机械,2020,38(4):1-4.
YU J N,CHEN D,CAO Y Y,et al.Research on low temperature concentration of juice at normal pressure based on liquid gap membrane distillation[J].Packaging and Food Machinery,2020,38(4):1-4.
[10] 杨方威, 冯叙桥,曹雪慧,等.膜分离技术在食品工业中的应用及研究进展[J].食品科学,2014,35(11):330-338.
YANG F W,FENG X Q,CAO X H,et al.Application in the food industry and development of membrane separation technology[J].Food Science,2014,35(11):330-338.
[11] 林红军, 陈建荣,陆晓峰,等.正渗透膜技术在水处理中的应用进展[J].环境科学与技术,2010,33(S2):411-415.
LIN H J,CHEN J R,LU X F,et al.Application progresses of forward osmosis process in water treatment[J].Environmental Science & Technology,2010,33(S2):411-415.
[12] 胡群辉, 邹昊,姜莹,等.正渗透膜分离关键技术及其应用进展[J].膜科学与技术,2014,34(5):109-115.
HU Q H,ZOU H,JIANG Y,et al.Research progress of the key techniques and applications for forward osmosis[J].Membrane Science and Technology,2014,34(5):109-115.
[13] 魏新渝. 高耐氯性复合反渗透膜的制备研究[D].天津:天津大学,2010.
WEI X Y.Preparation of composite RO membrane with high chlorine resistance[D].Tianjin:Tianjin University,2010.
[14] 刘富. PVDF、PVC微孔膜亲水化改性的研究[D].杭州:浙江大学,2007.
LIU F.Hydrophilic modification of PVDF、PVC microporous membranes[D].Hangzhou:Zhejiang University,2007.
[15] 唐媛媛, 徐佳,陈幸,等.正渗透脱盐过程的核心——正渗透膜[J].化学进展,2015,27(7):818-830.
TANG Y Y,XU J,CHEN X,et al.Core of forward osmosis for desalination——forward osmosis membrane[J].Progress in Chemistry,2015,27(7):818-830.
[16] 王毅, 谢朝新,周宁玉,等.三醋酸纤维(CTA)正渗透膜活性层朝向对正渗透过程的影响[J].四川环境,2014,33(2):17-24.
WANG Y,XIE C X,ZHOU N Y,et al.Study on the influence of the orientation of the CTA membrane for osmosis(FO) process[J].Sichuan Environment,2014,33(2):17-24.
[17] 李悦, 拜淑娟,高庆超,等.膜浓缩技术制备黑果枸杞花青素的工艺研究[J].食品研究与开发,2019,40(7):130-136.
LI Y,BAI S J,GAO Q C,et al.Preparation of anthocyanin in Lycium ruthenicum Murr by membrane concentration technique[J].Food Research and Development,2019,40(7):130-136.
[18] 黄维菊, 褚良银,陈文梅,等.微滤膜分离过程强化研究新进展[J].食品与发酵工业,2005,31(9):131-135.
HUANG W J,CHU L Y,CHEN W M,et al.Recent development in the research about enhancement of micro-filtration membrane separation processes[J].Food and Fermentation Industries,2005,31(9):131-135.
[19] 刘蕾蕾. 三醋酸纤维素正渗透膜的制备与性能研究[D].青岛:中国海洋大学,2010.
LIU L L.Studies on preparation and performance of cellulose triacetate forward osmosis membrane[D].Qingdao:Ocean University of China,2010.
[20] 谢朋, 张忠国,孙涛,等.正渗透过程中汲取质反向渗透研究进展[J].化工进展,2015,34(10):3 540-3 550.
XIE P,ZHANG Z G,SUN T,et al.Research progress of reverse draw solute permeation in forward osmosis process[J].Chemical Industry and Engineering Progress,2015,34(10):3 540-3 550.
[21] 李开, 曾鸣,宋昊,等.浓缩果汁中游离糖的组成分析[J].食品研究与开发,2019,40(16):129-134.
LI K,ZENG M,SONG H,et al.Composition analysis of free sugars in concentrated juices[J].Food Research and Development,2019,40(16):129-134.
[22] HAMDAN M,SHARIF A O,DERWISH G,et al.Draw solutions for forward osmosis process:Osmotic pressure of binary and ternary aqueous solutions of magnesium chloride,sodium chloride,sucrose and maltose[J].Journal of Food Engineering,2015,155:10-15.
[23] 杨晓璇. 抗生素分离与藻酸盐浓缩脱水正渗透试验研究[D].北京:北京建筑大学,2020.
YANG X X.Experimental study on separation of antibiotics and concentration of alginate by forward osmosis[D].Beijing:Beijing University of Civil Engineering and Architecture,2020.