副干酪乳杆菌(Lactobacillus paracasei)广泛存在于干酪、发酵乳、泡菜等发酵食品,以及人体的口腔、肠道之中,兼性厌氧,不运动不产生芽胞,具备长久的安全使用历史,已被列入我国《可用于食品菌种名单》和欧盟安全资格认定(EU Safety Qualification,QPS)名单中。研究表明L.paracasei等益生菌的功能性和安全性特征在菌株水平具有特异性[1-4]。目前已有多株商业化菌株在乳制品、固体饮料制品、保健食品等领域广泛应用,其在功能性、安全性等方面存在较大差异。L.paracaseiK56和ET-22是分别分离自儿童和成人肠道的益生菌,耐胃酸和耐肠液性能良好,具有调节免疫、缓解肠道炎症、平衡肠道菌群、缓解便秘等功效,在发酵乳、固体饮料及保健食品等领域具有广泛的应用潜力[5-7]。
副干酪乳杆菌所属的乳杆菌属(Lactobacillus)作为一类重要的益生菌资源,在全球健康食品工业中占据着重要地位。乳杆菌属分类学地位已发生重要变迁,原乳杆菌属被重新划分为25个属,本研究中涉及的L.paracasei变迁为副干酪乳酪杆菌(Lacticaseibacillus paracasei)[8],考虑到新分类单元的应用存在过渡期,本项目研究仍沿用之前的乳杆菌属国际分类体系。新的分类方法更精确的描述了菌种的共同特征,有助于乳杆菌属在各领域的研发创新和资源挖掘与利用,有助于促进相关产品的政府监管和国际贸易发展,将对我国相关法规和乳制品行业应用产生深远的影响。
益生菌产品形式丰富多样,对益生菌在菌株水平的准确鉴定是确保其功能开发和安全性研究的重要前提,但目前国内外关于益生菌菌株水平鉴定的技术方法和明确判定标准仍处于起步阶段,建立完善的菌株水平鉴定技术体系是行业发展的重点趋势。益生菌菌株水平鉴定通常在菌种水平鉴定的基础上开展[9],菌种水平分类学地位的确认通过多相鉴定进行,通常包括菌落菌体形态、生理生化特征分析(如:VITEK、API、BIOLOG)、基质辅助激光解析电离飞行时间质谱(matrix-assisted laser desorption ionization time-of-flight mass spectrometry,MALDI-TOF MS)等表型鉴定方法,以及16S rRNA基因、pheS/atpD功能基因、平均核苷酸一致性(average nucleotide identity,ANI)分析等基因型鉴定方法[10-13]。基于全基因组测序(whole genome sequencing,WGS)的单核苷酸多态性(single nucleotide polymorphism,SNP)分析和多位点测序分型(multi-site sequencing for typing,MLST)分析技术凭借其全面的遗传信息和较高的分辨率成为菌株分型鉴定的可靠方法[14-17],但目前仍缺乏WGS技术用于益生菌菌株鉴定的判定标准。本研究针对副干酪乳杆菌L.paracasei K56和ET-22,通过形态学、生理生化等表型鉴定技术,结合WGS、MLST技术、单核苷酸多态性分析等分子生物学技术,开展L.paracasei菌株水平鉴定研究,实现了L.paracasei K56和ET-22菌株水平区分,通过菌株水平鉴定实现益生菌的精准溯源,为产品质量控制提供可靠的技术标准,同时为政府监管、行业标准法规制定提供技术参考,对促进益生菌在食品行业更加安全和广泛的应用具有重要意义。
1 材料和方法
1.1 实验材料
1.1.1 实验菌株
副干酪乳杆菌L.paracasei K56和ET-22,内蒙古伊利实业集团股份有限公司;模式菌株Lactobacillus casei CICC 6117T和Lactobacillus paracasei JCM 8130T,中国工业微生物菌种保藏管理中心。其他7株参考菌株分离自有明确菌株声称的乳饮料、滴剂及菌剂等产品。菌株具体信息见表1。
表1 菌株信息
Table 1 Information of selected strains
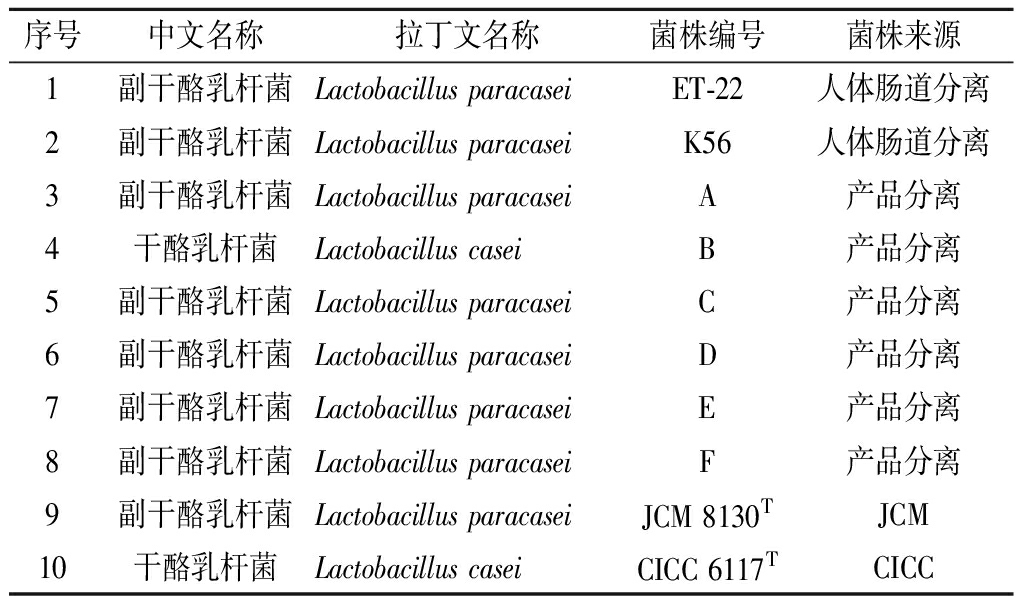
序号中文名称拉丁文名称菌株编号菌株来源1 副干酪乳杆菌Lactobacillus paracaseiET-22人体肠道分离2 副干酪乳杆菌Lactobacillus paracaseiK56人体肠道分离3 副干酪乳杆菌Lactobacillus paracaseiA产品分离4 干酪乳杆菌Lactobacillus caseiB产品分离5 副干酪乳杆菌Lactobacillus paracaseiC产品分离6 副干酪乳杆菌Lactobacillus paracaseiD产品分离7 副干酪乳杆菌Lactobacillus paracaseiE产品分离8 副干酪乳杆菌Lactobacillus paracaseiF产品分离9 副干酪乳杆菌Lactobacillus paracaseiJCM 8130TJCM10 干酪乳杆菌Lactobacillus caseiCICC 6117TCICC
1.1.2 实验仪器
ECLIPSE 80i光学显微镜,尼康仪器(上海)有限公司;隔水式培养箱,上海一恒科学仪器有限公司;Hitachi SU8010扫描电镜,日立高新技术(上海)国际贸易有限公司;BAL-TEC SCD005喷金-离子溅射仪;MALDI-TOF MS仪,德国布鲁克公司;BGISEQ-500高通量基因测序仪、BGIDL-50全自动样本加载系统,深圳华大智造科技有限公司;微量可调移液器、小型台式冷冻离心机,德国Eppendorf公司;高压灭菌锅,日本HIRAYAMA公司;Q800R2超声打断仪,美国Sonicator公司;Qubit 3.0核酸荧光定量仪,赛默飞世尔科技(中国)有限公司。
1.1.3 实验试剂
MRS琼脂、强化梭菌培养基,美国BD公司;API 50 CHL培养基、API 50 CHL试验条,法国生物梅里埃公司;革兰氏染色液、0.85%生理盐水,北京陆桥技术股份有限公司;厌氧产气袋,日本三菱化学公司;溶菌酶、RNase A溶液、GoldView、琼脂糖,北京全式金生物技术有限公司;高通量测序试剂套装BGISEQ-500RS(PE100)、MGIEasy通用DNA文库制备试剂套装,深圳华大智造科技有限公司;Qubit®dsDNA HS Assay Kit、Qubit®ssDNA Assay Kit,赛默飞世尔科技(中国)有限公司;细菌基因组DNA提取试剂盒E.Z.N.A.®Bacterial DNA Kit,Omega Bio-tek公司。
1.2 实验方法
1.2.1 形态学观察
采用4区划线法将菌株K56和ET-22接种于MRS培养基平皿,于36 ℃厌氧条件下培养48 h后,观察记录菌落特征,并进行革兰氏染色观察记录菌体特征。菌株K56和ET-22经无菌生理盐水漂洗后用戊二醛固定过夜,将漂洗后的菌体加入到滤纸包中,乙醇梯度脱水,二氧化碳临界点干燥后,将样品放置到喷金-离子溅射仪中进行喷金,使用扫描电镜进行菌体特征观察。
1.2.2 API分析
将菌株K56和ET-22接种于MRS培养基平皿中,在36 ℃厌氧条件下培养24 h,用无菌棉签挑取足量菌落加入API 50 CHL培养基中制得混浊度相当于3 McFarland的菌悬液,接种API 50 CHL实验条,于36 ℃厌氧培养24~48 h后,加入附加试剂判读结果。试验条判读结果使用数据库API 50 CHL V3.0进行鉴定。
1.2.3 MALDI-TOF MS鉴定
采用甲酸萃取法制备检测样本,分别挑取培养皿中各菌株菌体,混匀于300 μL超纯水中,添加900 μL无水乙醇充分振荡,离心菌体并去除上清液,完全去除乙醇后,用50 μL 70%甲醇重悬菌体细胞,再加入50 μL乙腈,通过移液枪反复吹打混合悬液;将制备的悬液按照MALDI-TOF MS检测规程进行鉴定分析,确定菌株种水平分类学地位。
1.2.4 WGS及分析
1.2.4.1 菌株DNA提取及测序
按照细菌基因组DNA提取试剂盒E.Z.N.A.®Bacterial DNA Kit操作规程提取各菌株基因组DNA,使用MGIEasy通用DNA文库制备试剂套装进行建库,将符合出库标准的文库按照BGISEQ-500RS高通量测序试剂套装的说明书完成DNA纳米球的制备、加载和上机测序。使用SOAPnuke v1.5.6对下机原始数据进行过滤,去除接头序列、PCR重复序列、和低质量碱基序列(Phred得分<20),利用SPAdes v3.11.0进行序列拼接,获得组装基因组序列[18-19]。
1.2.4.2 菌株ANI分析
以模式菌株Lactobacillus paracasei subsp. paracasei JCM 8130T(GCF_000829035.1)、Lactobacillus paracasei subsp. tolerans DSM 20258T(GCF_001436485.1)为参考菌株,利用fastaANI(v 1.3)软件对测序菌株进行ANI分析。
1.2.4.3 基于WGS的多基因序列位点分析(whole genome multilocus sequence typing,wgMLST)
使用Prodigal 2.6.3预测样品基因组序列中的编码基因,获得编码基因的核酸序列与蛋白质序列。利用CD-HIT v4.6.6对编码基因进行聚类分析,提取各样品中均存在的共有基因。采用TreeBeST(v 1.9.2)的PHYML(最大似然法)算法构建系统进化树,bootstraps参数设置为1 000。
1.2.4.4 SNP分析
通过MUMmer 比对软件,将每个样品与参考序列进行比对,筛选潜在SNP位点。提取参考序列SNP位点两边各100 bp序列,用BLAT将提取的序列和组装结果进行比对,进行SNP位点验证。采用BLAST、TRF、Repeatmask软件预测重复序列位点,过滤去除重复区SNP,最后得到可靠的SNP。
2 结果与分析
2.1 形态学观察
菌株K56在MRS培养基上36 ℃厌氧培养48 h,菌落白色、圆形,表面湿润,不透明,边缘整齐(图1-a);光学显微镜下观察,菌体呈杆状,(0.4~0.5)μm×(0.9~3.2)μm,单个或成对排列,革兰氏阳性(图1-b)。扫描电镜观察,菌体呈杆状,菌体呈杆状,(0.4~0.5)μm×(0.9~1.8)μm,单个或成对排列(图1-c)。菌株K56的菌落和菌体形态符合副干酪乳杆菌特征[20]。

a-菌落形态;b-菌体显微形态;c-菌体扫描电镜形态
图1 菌株K56菌落和菌体形态
Fig.1 Colony and morphology of strain K56
菌株ET-22在MRS培养基上36 ℃厌氧培养48 h,菌落白色、圆形,表面湿润,不透明,边缘整齐(图2-a);光学显微镜下观察,菌体呈杆状,(0.5~0.6)μm×(0.9~2.7)μm,单个或成对排列,革兰氏阳性(图2-b)。扫描电镜观察,菌体呈杆状,(0.5~0.6)μm×(1.2~3.1)μm,单个或成对排列(图2-c)。菌株ET-22的菌落和菌体形态符合副干酪乳杆菌特征。
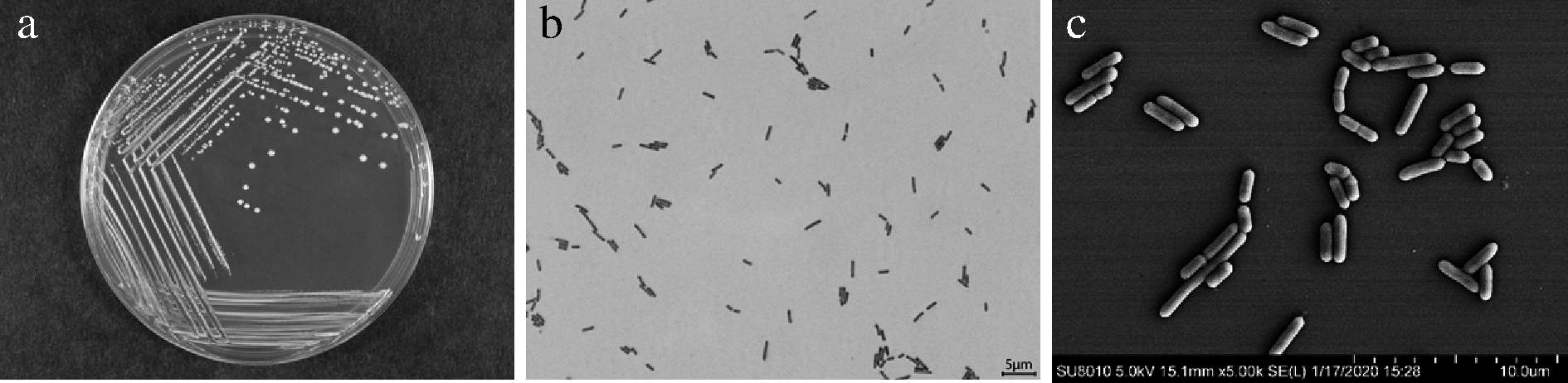
a-菌落形态;b-菌体显微形态;c-菌体扫描电镜形态
图2 菌株ET-22菌落和菌体形态
Fig.2 Colony and morphology of strain ET-22
2.2 API鉴定结果
菌株K56和ET-22的API生理生化结果如表2所示。菌株K56经API 50 CHL系统鉴定为副干酪乳杆菌副干酪亚种,鉴定百分率为99.7%,T值为0.54;菌株ET-22经API 50 CHL系统鉴定为副干酪乳杆菌副干酪亚种(Lactobacillus paracasei subsp.paracasei),鉴定百分率为89.0%,T值为0.43。
API微生物鉴定系统根据微生物对各种生理条件、生化指标代谢反应进行分析,并将结果转化为软件可识别的数据进行聚类分析,与已知的参比菌株数据库进行比较,最终实现对未知菌株的鉴定[21],其结果与数据库中收录的菌株种类与数量密切相关,本研究中目标菌株K56和ET-22鉴定至亚种水平,与鉴定系统中生理生化反应及数据库中菌株收集的数量有关,API鉴定系统提供的代谢特征还可为后续菌株功能开发提供有效支撑。
表2 菌株K56和ET-22的API分析结果
Table 2 API analysis results of strain K56 and ET-22

K56ET-22K56ET-22K56ET-22K56ET-22甘油--赤藓糖醇--D-阿拉伯糖--L-阿拉伯糖--D-核糖++D-木糖--L-木糖--侧金盏花醇++wβ-甲基-D-木糖苷--D-半乳糖++D-葡萄糖++D-果糖++D-甘露糖++L-山梨糖++L-鼠李糖--卫矛醇--肌醇--甘露醇++山梨醇++α-甲基-D-甘露糖苷--α-甲基-D-葡萄糖苷+w+wN-乙酰葡糖胺++苦杏仁苷++w熊果苷++七叶灵++水杨苷++D-纤维二糖++D-麦芽糖++D-乳糖++wD-蜜二糖--D-蔗糖+w+wD-海藻糖++菊糖--D-松三糖--D-棉子糖--淀粉--糖原--木糖醇--D-龙胆二糖++D-土伦糖++D-来苏糖--D-塔格糖++D-岩藻糖--L-岩藻糖--D-阿拉伯醇--L-阿拉伯醇--葡萄糖酸钾+w+2-酮基-葡萄糖酸盐--5-酮基-葡萄糖酸盐--
注:“+”,阳性;“-”,阴性
2.3 菌株K56和ET-22及参考菌株MALDI-TOF MS鉴定
本研究通过MALDI-TOF MS鉴定,确定菌株K56、ET-22和参考菌株的种水平分类学地位。MALDI-TOF是近年来新兴的微生物快速鉴定系统,通过检测微生物核糖体等高丰度稳定表达的特征蛋白指纹图谱,与已知微生物菌种蛋白指纹图谱数据库比对分析后,进行快速菌种鉴定,该方法已进入国家标准GB/T 33682—2017[10],在工业微生物(含乳杆菌属和双歧杆菌属)菌种鉴定方面有较好的应用效果[22]。本研究应用的MALDI-TOF MS数据库中目前包含119种乳杆菌属菌株图谱,其中副干酪乳杆菌数据有15株,通过MALDI-TOF MS鉴定表明,各试验菌株与数据库中标准菌株核糖体蛋白图谱的鉴定比对值达到2以上,专属菌株及参考菌株均鉴定为副干酪乳杆菌Lactobacillus paracasei(表3),干酪乳杆菌Lactobacillus casei CICC 6117T鉴定为干酪乳杆菌Lactobacillus casei,其中干酪乳杆菌Lactobacillus casei B经鉴定为副干酪乳杆菌Lactobacillus paracasei,这种随科技进步导致的分类学地位变迁是常见的现象,也表明了益生菌菌株分类学的进步和规范化发展。鉴定结果具有较高的可信度,进一步表明目标菌株K56和ET-22及相关参考菌株具备准确的种水平分类学地位。
2.4 ANI分析
对菌株K56、ET-22和参考菌株进行WGS分析,测序结果显示试验菌株测序深度大于300×,全基因组序列Q30均在90%以上,满足后续组装及分析要求。ANI于2007年由GORIS等[12]提出,通过比较大量模式菌株的两两基因组指出2个基因组序列之间的整体相似性,ANI值95%~96%与DNA-DNA杂交值的70%相对应,可作为细菌物种鉴定的有效方法。选取模式菌株L.paracasei subsp. paracasei JCM 8130T(ref1)和L.paracasei subsp. tolerans DSM 20258T(ref2)的全基因组序列作为参考序列进行ANI分析。结果表明,不同L.paracasei菌株与模式菌株全基因组序列的ANI值均达到95%以上(表4),其中菌株ET-22-D1和K56-D1为目标菌株的原始菌株,菌株ET-22-D2和K56-D2分别为对应菌株传代培养5代的菌株。符合同菌种分类学地位的评判标准,菌株K56和ET-22及相关参考菌株均鉴定为副干酪乳杆菌(L.paracasei)。
表3 不同L.paracasei菌株的MALDI-TOF MS鉴定结果
Table 3 MALDI-TOF MS results of different L.paracasei strains
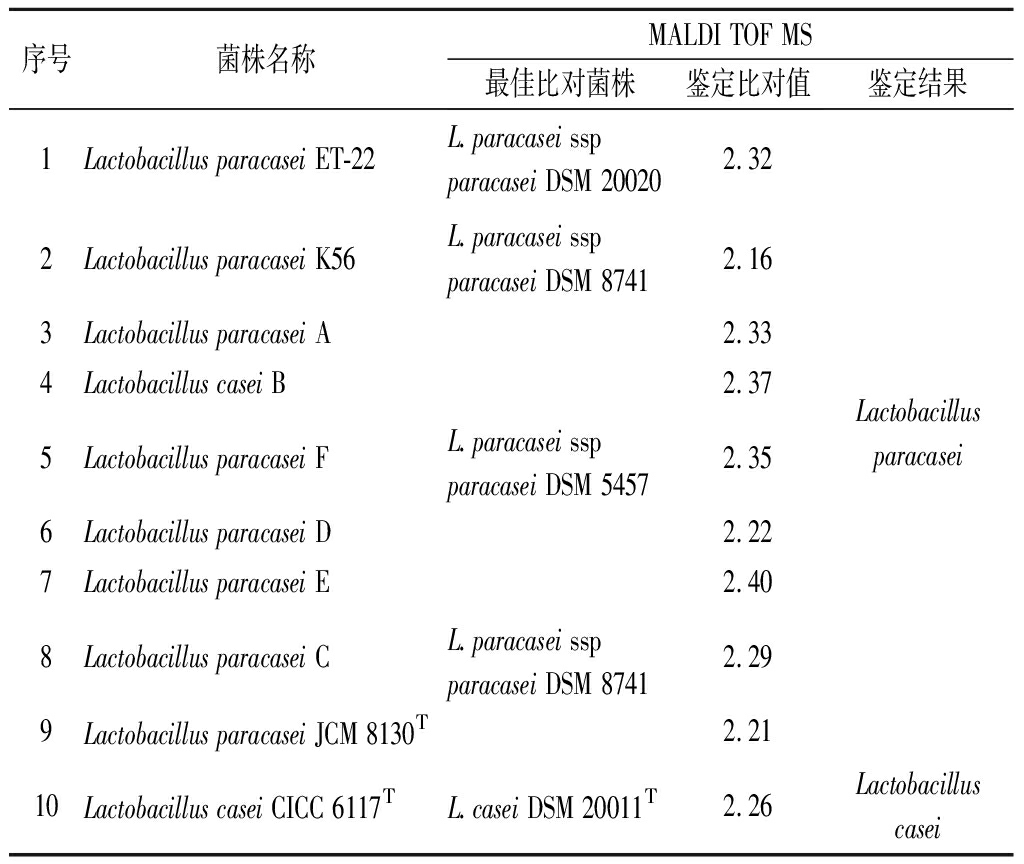
序号菌株名称MALDI TOF MS最佳比对菌株鉴定比对值鉴定结果1Lactobacillus paracasei ET-22L.paracasei ssp paracasei DSM 200202.322Lactobacillus paracasei K56L.paracasei ssp paracasei DSM 87412.163Lactobacillus paracasei A2.334Lactobacillus casei B2.375Lactobacillus paracasei FL.paracasei ssp paracasei DSM 54572.356Lactobacillus paracasei D2.227Lactobacillus paracasei E2.408Lactobacillus paracasei CL.paracasei ssp paracasei DSM 87412.299Lactobacillus paracasei JCM 8130T2.21Lactobacillus paracasei10Lactobacillus casei CICC 6117TL.casei DSM 20011T2.26Lactobacillus casei
注:鉴定对比值在2.00~3.00时表明鉴定结果为高可信度鉴定
表4 不同L.paracasei的ANI分析结果
Table 4 ANI analysis results of different L.paracasei strains
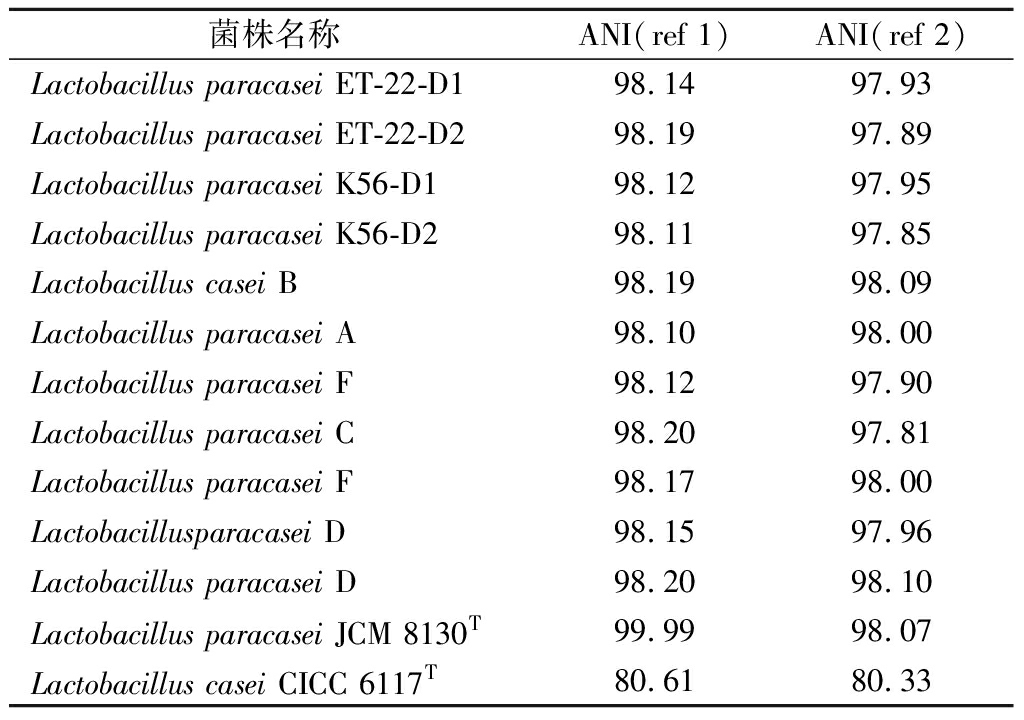
菌株名称ANI(ref 1)ANI(ref 2)Lactobacillus paracasei ET-22-D198.1497.93Lactobacillus paracasei ET-22-D298.1997.89Lactobacillus paracasei K56-D198.1297.95Lactobacillus paracasei K56-D298.1197.85Lactobacillus casei B98.1998.09Lactobacillus paracasei A98.1098.00Lactobacillus paracasei F98.1297.90Lactobacillus paracasei C98.2097.81Lactobacillus paracasei F98.1798.00Lactobacillusparacasei D98.1597.96Lactobacillus paracasei D98.2098.10Lactobacillus paracasei JCM 8130T99.9998.07Lactobacillus casei CICC 6117T80.6180.33
综上,结合形态学、生理生化(API)、MALDI-TOF MS和WGS ANI方法对菌株K56和ET-22种水平分类学地位进行了鉴定。通过MALDI-TOF MS和WGS ANI可得到目标菌株K56和ET-22及相关参考菌株明确的菌种水平分类学地位,形态学、生理生化(API)虽然不能对菌株进行精确鉴定,但其提供的菌株形态及代谢特征可为后续菌株功能开发、高密度培养、高效制造等提供有效支撑。
2.5 wgMLST分析
经过wgMLST分析得到各L.paracasei菌株的核心基因共有1 701个(图3),以共有基因为基础,开展wgMLST分析(图4)。系统发育分析结果表明,菌株K56和ET-22的序列分别处于同一分支,系统发育中Bootstrap值达99%以上,具备更近的亲缘关系,该方法可有效区分菌株K56和ET-22与本研究中的其他参考菌株。MLST是基于多位点序列分型的菌株分型方法,是一种基于核酸序列测定的微生物分型方法,通过串联多个基因内部片段序列,对菌株的等位基因进行多样性的比较,通过不同的序列型分析菌株间的关系,在流行病学监测和进化研究方面有较广泛的应用。传统的MLST方法依托PCR扩增少数持家基因进行序列分析,由于选择的基因数量较少,可能不能得到较好的菌株区分效果[23-24]。wgMLST方法主要通过对菌株间的所有共有基因进行差异分析和系统发育分析来实现菌株分型鉴定。DURANTI等[16]对18株青春双歧杆菌(Bifidobacterium adolescentis)进行全基因测序和wgMLST分析,结果表明通过对872个共有基因的进行差异分析和系统发育分析,不同株青春双歧杆菌(B.adolescentis)可得到良好区分。本研究中通过全基因组序列数据分析,选取专属菌株和参考菌株的1 701个共有基因进行系统发育分析,可将目标菌株K56和ET-22与参考菌株进行有效区分。
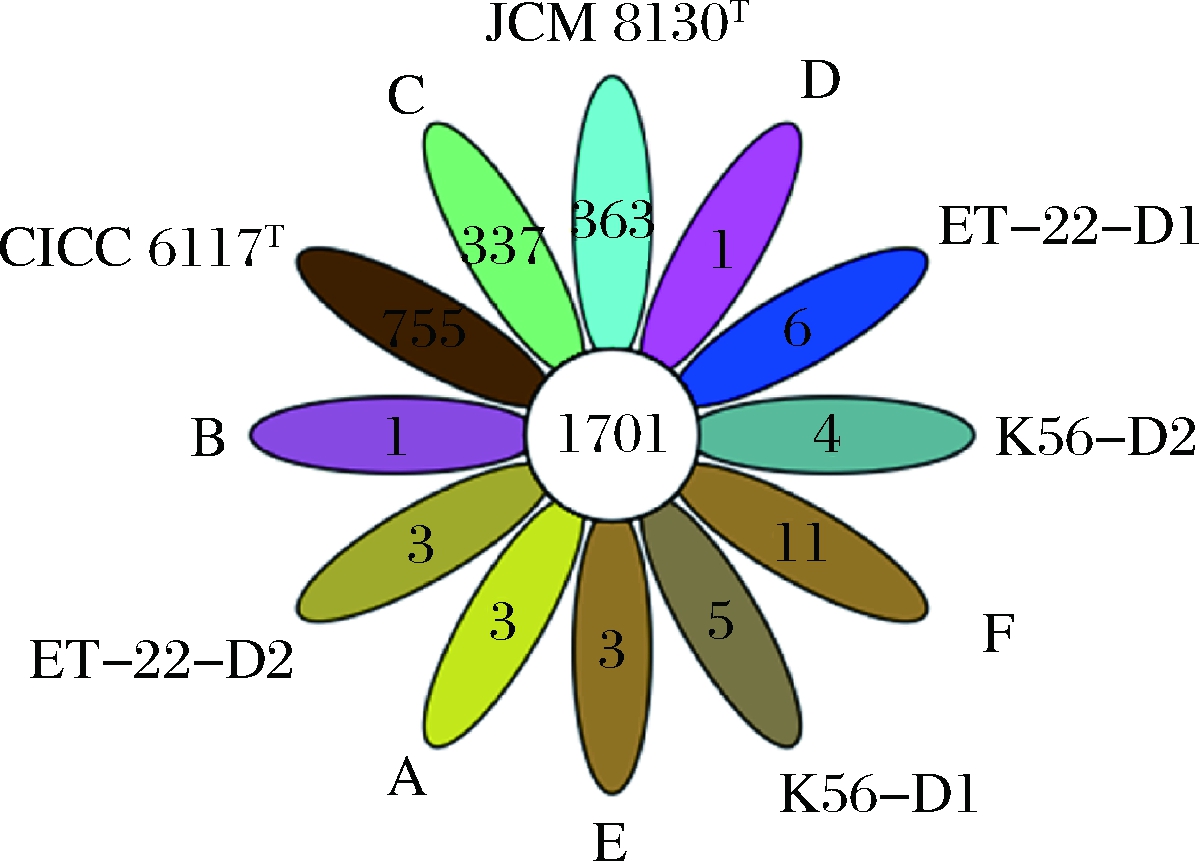
图3 实验菌株序列的共有基因分布
Fig.3 Distribution of common genes in experimental strains

图4 基于wgMLST的L.paracasei系统发育分析
Fig.4 Phylogenetic analysis of L.paracasei strains based on wgMLST
2.6 SNP分析
单核苷酸多态性主要是指在基因组水平上由单个核苷酸的变异所引起的DNA序列多态性,具备数量丰富、分辨率高、覆盖基因组范围大、遗传稳定等特点,可作为较稳定的遗传标记应用于微生物菌株的分型溯源分析[25]。分别以副干酪乳杆菌K56和ET-22的基因组序列为参考,SNP分析结果如表5和表6所示。
表5 L.paracasei K56及参考菌株的SNP分析结果
Table 5 SNP analysis results of L.paracasei K56 and reference strains

菌株SNPLactobacillusparacasei K56-D10(ref)Lactobacillusparacasei K56-D2103Lactobacillusparacasei ET-22-D1357Lactobacillusparacasei ET-22-D2335Lactobacillusparacasei A167Lactobacilluscasei B167Lactobacillusparacasei C32 010Lactobacillusparacasei D129Lactobacillusparacasei E134Lactobacillusparacasei F163Lactobacillusparacasei JCM 8130T29 426Lactobacilluscasei CICC 6117T78 805
表6 L.paracasei ET-22及参考菌株的SNP分析结果
Table 6 SNP analysis results of L.paracasei ET-22 and reference strains

菌株SNPLactobacillus paracasei ET-22-D10(ref)Lactobacillusparacasei ET-22-D249Lactobacillusparacasei K56-D1333Lactobacillusparacasei K56-D2276Lactobacillusparacasei A225Lactobacilluscasei B266Lactobacillusparacasei C31 167Lactobacillusparacasei D245Lactobacillusparacasei E262Lactobacillusparacasei F274Lactobacillusparacasei JCM 8130T28 778Lactobacilluscasei CICC 6117T79 258
菌株K56基因序列与参考序列相比,其SNP差异为103,其余副干酪乳杆菌菌株与参考基因组的SNP差异均大于129,菌株ET-22基因序列与参考序列相比,其SNP差异为49,其余副干酪乳杆菌菌株与参考基因组的SNP差异均大于225。表明菌株K56和ET-22可与8株副干酪乳杆菌菌株良好区分。基于SNP差异的系统发育分析也显示K56和ET-22的基因序列分别聚集在同一分支,可与其他菌株进行明显区分(图5~图6)。通过对大肠埃希氏菌(Escherichia coli)、单增李斯特氏菌(Listeria monocytogenes)等致病菌的SNP分析研究表明,21个SNP差异是判断同一菌株的标准之一[25],SNP分析在益生菌领域的研究主要包括乳杆菌、双歧杆菌等不同菌株的分型分析,但目前还未有关于益生菌同株的评判标准,该方法的判定标准与目标菌株及参考菌株的种类与数量密切相关,基于目前的菌株数量及数据结果分析,SNP分析可有效实现Lactobacillus paracasei K56和ET-22的株水平分型及鉴定。
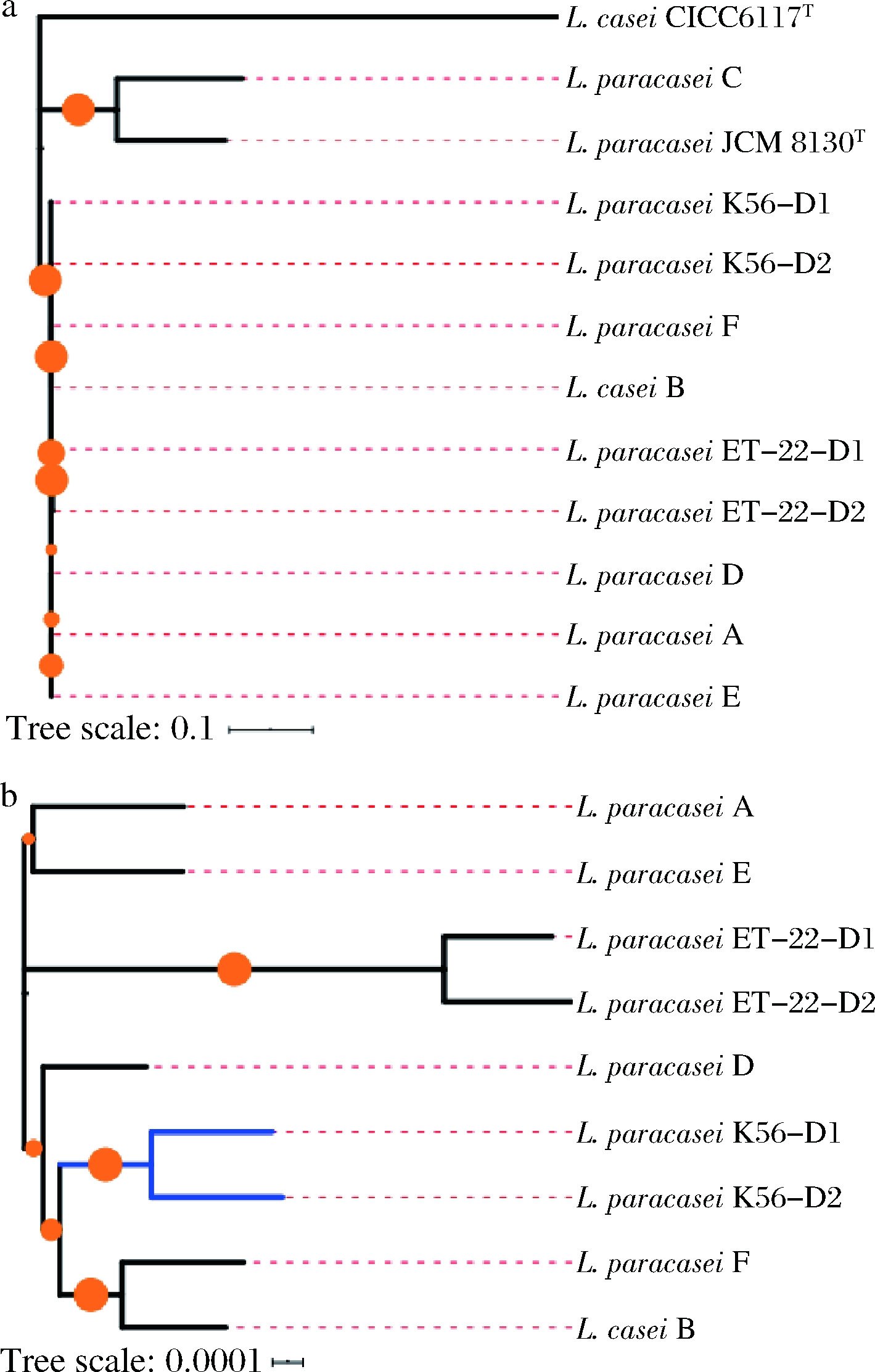
图5 基于SNP的副干酪乳杆菌L. paracasei K56系统发育分析
Fig.5 Phylogenetic analysis of L. paracasei K56 and reference strains based on wg SNP

图6 基于SNP的副干酪乳杆菌L.paracasei ET-22 系统发育分析
Fig.6 Phylogenetic analysis of L.paracasei ET-22 and reference strains based on SNP
3 结论
本研究通过形态学、生理生化(API)、MALDI-TOF鉴定和WGS ANI方法可将菌株K56和ET-22鉴定为副干酪乳杆菌L. paracasei;进一步通过SNP和wgMLST可有效区分副干酪乳杆菌L. paracasei K56和ET-22与本研究中的其他菌株。本研究L.paracasei K56和ET-22菌株水平鉴定的技术流程,为益生菌菌株水平的精确鉴定技术体系的构建提供了有效数据支撑和实践。wgSNP和wgMLST作为分辨率较高的益生菌菌株水平鉴定技术,其适用范围、判定标准与研究涵盖的目标菌株、参考菌株数量密切相关。随着试验菌株样本量的不断扩充,建立的益生菌菌株水平鉴定流程和评价标准将更具代表性、覆盖度和统计学意义。
[1] FAO/WHO.Joint FAO/WHO Working Group Report on Drafting Guidelines for the Evaluation of Probiotics in Food[R].London,Ontario,Canada,April 30 and May 1,2002.
[2] 中国卫生部,可用于食品的菌种名单[Z].2010,65号.
Ministry of Health,P.R.China,List of strains that can be used for food[Z].2010,No.65.
[3] IPA.guidelines to qualify a microorganism to be termed as “probiotic”.International Probiotics Association(IPA)[Z].2017.1
[4] 中国食品科学技术学会益生菌分会.益生菌的科学共识(2020年版)[J].中国食品学报,2020(5):303-307.
Probiotics Society of the Chinese Institute of Food Science and Technology.Scientific consensus on probiotics(2020)[J].Journal of Chinese Institute of Food Science and Technology,2020,20(5):303-307.
[5] 赵雯,刘伟贤,洪维鍊,等.副干酪乳杆菌K56在缓解肠道炎症方面的新应用:中国,CN110892940A[P].2020-03-20.
ZHAO W,LIU W X,HONG W L,et al.New use of Lactobacillus paracasei K56 in inhibiting intestinal inflammation:China,CN110892940A[P].2020-03-20.
[6] 洪维鍊,刘伟贤,赵雯,等.一种具有缓解肠道炎症功能的副干酪乳杆菌ET-22:中国,CN110893195A[P].2020-03-20.
HONG W L,LIU W X,ZHAO W,et al.A Lactobacillus paracasei ET-22 that can inhibit intestinal inflammation:China,CN110893-195A[P].2020-03-20.
[7] 洪维鍊,刘伟贤,赵雯,等.一种具有免疫调节功能的副干酪乳杆菌ET-22:中国,CN110964658A[P].2020-04-07.
HONG W L,LIU W X,ZHAO W,et al.A Lactobacillus paracasei ET-22 with the ability of immunoregulation:China,CN110964658A[P].2020-04-07.
[8] ZHENG J S,WITTOUCK S,SALVETTI E,et al.A taxonomic note on the genus Lactobacillus:Description of 23 novel genera,emended description of the genus Lactobacillus Beijerinck 1901,and union of Lactobacillaceae and Leuconostocaceae[J].International Journal of Systematic and Evolutionary Microbiology,2020,70(4):2 782-2 858.[LinkOut]
[9] HELLER K J,BOCKELMANN W,BROCKMANN E,et al.Identification of probiotics at strain level-Guidance document[J].Bulletin of the International Dairy Federation,2013,462:5-8.
[10] 国家农业标准化监测与研究中心.GB/T 33682—2017 基质辅助激光解析电离飞行时间质谱鉴别微生物方法通则[S].北京:中国标准出版社,2017.
National Monitoring and Research Center for Agricultural Standardization.GB/T 33682—2017 General microorganism identification method with matrix-assisted laser desorption/ionization time of flight mass spectrometry[S].Beijing:China Standards Press,2017.
[11] KIM M,OH H S,PARK S C,et al.Towards a taxonomic coherence between average nucleotide identity and 16S rRNA gene sequence similarity for species demarcation of prokaryotes[J].International Journal of Systematic and Evolutionary Microbiology,2014,64(Pt 2):346-351.
[12] GORIS J,KONSTANTINIDIS K T,KLAPPENBACH J A,et al.DNA-DNA hybridization values and their relationship to whole-genome sequence similarities[J].International Journal of Systematic and Evolutionary Microbiology,2007,57(Pt 1):81-91.
[13] RICHTER M,ROSSELLO-MORA R.Shifting the genomic gold standard for the prokaryotic species definition[J].PNAS,2009,106(45):19 126-19 131.
[14] MOROVIC W,HIBBERD A A,ZABEL B,et al.Genotyping by PCR and high-throughput sequencing of commercial probiotic products reveals composition biases[J].Frontiers in Microbiology,2016,7:1747.
[15] INGLIN R C,MEILE L,STEVENS M J A.Clustering of Pan-and core-genome of Lactobacillus provides novel evolutionary insights for differentiation[J].BMC Genomics,2018,19(1):1-15.
[16] DURANTI S,MILANI C,LUGLI G A,et al.Evaluation of genetic diversity among strains of the human gut commensal Bifidobacterium adolescentis[J].Scientific Reports,2016,6:23971.
[17] MILANI C,DURANTI S,LUGLI G A,et al.Comparative genomics of Bifidobacterium animalis subsp.lactis reveals a strict monophyletic bifidobacterial taxon[J].Applied and Environmental Microbiology,2013,79(14):4 304-4 315.
[18] CHEN Y X,CHEN Y S,SHI C M,et al.SOAPnuke:A MapReduce acceleration supported software for integrated quality control and preprocessing of high-throughput sequencing data[J].Gigascience,2018,7(1):1-6.
[19] BANKEVICH A,NURK S,ANTIPOV D,et al.SPAdes:A new genome assembly algorithm and its applications to single-cell sequencing[J].Journal of Computational Biology,2012,19(5):455-477.
[20] GOODFELLOW M,KAMPFER P,BUSSE H J,et al.Bergey’s manual of systematic bacteriology,Second Edition[M].New York:Springer,2012:504.
[21] 段永翔.API鉴定系统及其在细菌学检验中的应用[J].现代预防医学,2004,31(5):729-731.
DUAN Y X.API identification system and its application in bacteriological test[J].Modern Preventive Medicine,2004,31(5):729-731.
[22] 范铁男,邹积宏,卢行安,等.基质辅助激光解吸电离飞行时间质谱技术作为常见益生菌菌种鉴定辅助工具的研究[J].中国微生态学杂志,2010,22(11):970-973.
FAN T N,ZOU J H,LU X A,et al.MALDI-TOF mass spectrometry as an assistant tool for identification of common probiotics[J].Chinese Journal of Microecology,2010,22(11):970-973.
[23] CHAN M S,MAIDEN M C J,SPRATT B G.Database-driven Multi Locus Sequence Typing(MLST) of bacterial pathogens[J].Bioinformatics,2001,17(11):1 077-1 083.
[24] MAIDEN M C J,VAN RENSBURG M J J,BRAY J E,et al.MLST revisited:The gene-by-gene approach to bacterial genomics[J].Nature Reviews Microbiology,2013,11(10):728-736.
[25] PIGHTLING A W,PETTENGILL J B,LUO Y,et al.Interpreting whole-genome sequence analyses of foodborne bacteria for regulatory applications and outbreak investigations[J].Frontiers in Microbiology,2018,9:1482.