硒被认为是继铁、锌、碘后人体严重缺少的第4种营养元素,调查显示全球约15%人口缺硒[1]。中国营养学会报告显示,我国居民每日硒总摄入量仅为26~32 μg,远低于60 μg/d的推荐摄入量[2]。随着人们健康意识及对食品营养要求的日益提高,食用富硒农产品被认为是安全、有效的补硒方式[3]。全球近一半的人口以稻米为主食[4],作为最大的稻米生产国和消费国[5],我国有60%的居民每天食用大米[6]。硒在机体内的生物利用度很大程度上取决于膳食中硒的存在形态[7]。富硒大米中硒是以硒代蛋氨酸(selenomethinonine,SeMet)、甲基硒代半胱氨酸(methylselenocysteine,MeSeCys)、硒代半胱氨酸(selenocysteine,SeCys)等有机硒,以及亚硒酸盐[selenite,Se(IV)]等无机硒组成[8]。与无机硒相比,SeMet、SeCys和MeSeCys更容易被机体消化吸收、具有更高生物利用度[9-10]。因此,科学评价富硒大米中硒对人体的营养效应,科学指导富硒大米的加工和健康消费尤为重要。
由于硒化合物的不稳定性和挥发性[11],蒸煮、油炸等常用烹饪方法会增加食物中的硒损失、改变其形态及生物利用度[12]。FIDELIS等[13]发现每100 g煮熟的大米中硒含量同未蒸煮相比降低了18.3 μg。KHANAM等[14]发现高压熟化后大米硒含量下降了3.72%。其他加工方式会导致富硒大米硒含量的降低[7-15]。LU等[16]研究表明常用家庭烹饪方法会导致谷物中损失高达46.9%的SeMet。加工过程中硒形态的变化会影响硒的生物利用度[17-18],微波、加压熟化处理后,大米中硒生物可利用度显著降低(P<0.05)[14]。然而以上研究均是基于单方面分析富硒大米的硒损失、形态或生物利用度,没有系统研究不同加工方式对富硒大米的影响。本文以重庆市江津区中山镇种植的富硒大米渝香203为实验对象,比较分析大米加工常见的不同方式(常压蒸煮、高压蒸煮、微波及挤压处理)对富硒大米中硒损失及硒形态的影响,同时通过体外模拟消化探究不同加工方式对富硒大米硒生物利用度及消化后各形态硒含量的影响,通过以上研究为富硒米类食品的制作和生产提供理论参考,推动富硒产业优质健康发展。
1 材料与方法
1.1 材料与试剂
富硒大米由重庆市江津区储备粮有限公司提供,产地为重庆市江津区中山镇,品种为渝香203,加工精度为精碾。
胃蛋白酶(CAS:9001-75-6)、胰酶(CAS:8049-47-6)、链霉蛋白酶E(CAS:9036-06-06),北京索莱宝科技有限公司;猪胆盐、α-淀粉酶,北京奥博星生物技术有限公司;亚硒酸根标准物质(GBW10032,浓度0.543 μmol/g)、硒代蛋氨酸标准溶液(GBW10034,浓度0.499 μmol/g)、甲基-硒代半胱氨酸标准溶液(GBW10088,浓度0.433 μmol/g),中国计量科学研究院;(NH4)2HPO4(CAS:7783-28-0)、三羟甲基氨基甲烷(CAS:77-86-1),上海麦克林生化科技有限公司;甲醇(色谱纯),上海阿拉丁生化科技股份有限公司;乙酸(色谱纯),重庆市钛新化工有限公司;硝酸、盐酸,成都市科隆化学品有限公司;除特别标注外,其余所用化学试剂均为分析纯。
1.2 仪器与设备
LS-50H立式压力蒸汽灭菌锅器,江阴滨江医疗设备有限公司;MAS-ⅡPLUS常压微波合成/萃取反应工作站,上海新仪微波化学科技有限公司;WLG10A实验用微型双锥螺杆挤出机,上海新硕精密机械有限公司;KQ-400DB数控超声波清洗器,昆山市超声仪有限公司;SY-10真空冷冻干燥机,北京松源华兴科技发展有限公司;PB-10酸度计,德国Sartorius公司;CHA-B水浴恒温振荡器,常州亚特实验仪器有限公司;DW-ZW128超低温冷冻储存箱,中科美菱低温科技股份有限公司;Centrifuge5804R离心机,德国Eppendorf公司;HCJ-1型磁力搅拌水浴锅,常州恩培仪器制造有限公司;FP6多通道原子荧光分光光度计,北京普析通用仪器责任有限公司;1260 Infinity II液相色谱系统、ICP-MS 7700x电感耦合等离子体质谱仪、Poroshell 120SB-C18液相色谱柱(4.6 mm×250 mm,4 μm),美国Agilent公司。
1.3 实验方法
1.3.1 富硒大米加工方式
富硒大米样品采用以下不同加工方式处理后冷冻干燥粉碎成粉,-80 ℃冷冻保存,备用。
1.3.1.1 常压蒸煮
参照周小理等[19]的方法略作修改,大米样品淘洗3次,水与样品比例1.3∶1(质量比,下同),浸泡30 min,蒸煮20 min,焖制5 min。
1.3.1.2 高压蒸煮
参照KHANAM等[14]的方法略作修改,大米样品淘洗3次,水与样品比例2∶1,浸泡30 min,温度120 ℃,压力100 kPa,高压蒸煮10 min,焖制20 min。
1.3.1.3 微波加工
参照KHANAM等[14]的方法略作修改,大米样品淘洗3次,水与样品比例4.5∶1,浸泡30 min,温度100 ℃,功率350 W,微波处理10 min。
1.3.1.4 挤压加工
参照陈怡岑等[20]的方法略作修改,富硒大米样品粉碎成粉,含水量调至30%,双螺杆挤压处理,螺杆转速40 r/min,挤压温度100 ℃。
1.3.2 硒含量测定
参照GB 5009.93—2017《食品安全国家标准 食品中硒的测定》第一法氢化物原子荧光光谱法,略作修改。准确称取样品0.5~1 g(精确至0.000 1 g),置于消化管中,加入5 mL硝酸,封口后冷消化过夜,沸水浴8 h,自然冷却后加入2.5 mL 50%(体积分数,下同)盐酸溶液,转移入25 mL容量瓶中,并用超纯水定容至刻度线,定容后的样品用101型滤纸过滤,原子荧光分光光度计测定,同时做空白对照。
1.3.3 有机硒含量测定
参照李志全等[21]的方法略作修改,称取样品0.5 g(精确到0.000 1 g)于50 mL带塞刻度试管中,加入20 mL 50%盐酸溶液,涡旋混匀,超声波处理45 min,沸水浴30 min取出自然冷却,定容至25 mL,脱脂棉过滤后,取10 mL滤液,消解后使用原子荧光分光光度计测定硒含量,测定值为无机硒含量,总硒减无机硒即为有机硒含量。
1.3.4 生物利用度测定
参照龚如雨[7]的方法略作修改。
体外模拟胃消化过程:称取0.5 g(精确到0.000 1 g)样品于50 mL离心管,加入10 mL模拟胃液(10 g/L胃蛋白酶,0.15 mol/L NaCl,pH 2.0),37 ℃恒温水浴振荡器振荡4 h,消化后样品3 500 r/min离心,取上清液,0.45 μm滤膜过滤,样品储存于-20 ℃,待测,每个样品做3个平行。
体外模拟肠消化过程:胃消化完成后,用饱和NaHCO3溶液调节消化液pH至7.5;加入10 mL模拟肠液(30 g/L胰酶、15 g/L淀粉酶、10 g/L胆盐、0.15 mol/L NaCl),样品混匀,37 ℃水浴振荡4 h,3 500 r/min离心,取上清液,0.45 μm滤膜过滤,样品储存于-20 ℃,待测,每个样品做3个平行。体外模拟胃肠富硒大米硒的生物利用度用公式(1)计算:
生物利用度![]()
(1)
1.3.5 硒形态测定
参照NY/T 3556—2020《粮谷中硒代半胱氨酸和硒代蛋氨酸的测定 液相色谱-电感耦合等离子体质谱法》标准略作修改,取粉碎后的样品1 g(精确至0.000 1 g)于50 mL离心管,加入10 mL三羟甲基氨基甲烷-盐酸缓冲液,室温40 W超声30 min,加入25 mg链霉蛋白酶E,漩涡混匀,置于37 ℃恒温振荡器中振荡酶解20 h,5 000 r/min、4 ℃离心10 min。取2 mL上清液于10 mL容量瓶,加流动相[40 mmol/L (NH4)2HPO4,体积分数为30%甲醇,pH 6.8]定容至刻度线,过0.22 μm滤膜后测定硒形态。
液相色谱条件:流动相流速1.0 mL/min,进样量50 μL,读数时间15~20 min。电感耦合等离子体质谱条件:采集质量数78,积分时间1.0 s,采集模式为时间积分,采样深度6.4 mm,高频等离子体发射功率1 550 W,载气流量1.02 L/min,载气补偿气流量0.11 L/min,蠕动泵转速0.3 r/s。
1.3.6 数据统计分析
所有实验指标重复测定3次,结果以平均值±标准差表示,实验数据采用Statistix 9软件,基于Tukey HSD法进行0.05水平显著性分析;采用GraphPad Prism 7.00软件用于所有实验结果的图形绘图。
2 结果与分析
2.1 富硒大米硒含量
对实验所用的富硒大米硒含量进行测定,其中总硒含量为263.90 μg/kg,有机硒含量为212.14 μg/kg,有机硒占大米中总硒的比例为80.42%。参照GB/T 22499—2008 《富硒稻谷》中规定的加工大米硒含量要求(40~300 μg/kg),该样品达到国家富硒标准。
2.2 加工方式对富硒大米总硒含量的影响
富硒大米通过常压蒸煮、高压蒸煮、微波及挤压处理4种常用的方式处理,测定处理后各样品中的总硒含量如表1所示,所有处理方式均会造成大米中硒含量的损失,常压蒸煮、微波及高压蒸煮3种方式损失较小,挤压处理后的样品硒损失较大,硒含量仅为150.27 μg/kg,与未处理的大米相比总硒含量有显著性差异(P<0.05),高压处理损失率仅为1.78%,微波处理损失率为4.21%,常压蒸煮损失率为3.26%,而挤压处理导致硒的损失率高达到43.05%。
表1 不同加工方式处理后富硒大米中的总硒含量
Table 1 Total selenium content in selenium-enriched rice treated with different processing methods
加工方式未处理常压蒸煮微波蒸煮高压处理挤压处理总硒含量/(μg·kg-1)263.90±15.61a255.31±7.06a252.82±21.22a259.19±27.14a150.27±3.39b
注:同行不同字母表示组间差异显著(P<0.05)
LIU等[22]发现水洗会降低大米中的矿物质含量。大米在蒸煮前都会进行清洗处理,这一过程会导致大米糊粉层和外胚乳的硒损失。因为各形态硒的不稳定性和挥发性,加工处理会造成硒形态的改变及损失[17]。KHANAM等[14]的研究表明,压力加热能显著降低大米中的硒含量(由148 μg/kg降至142.5 μg/kg)。因为蒸煮过程中所有水都被大米吸收,不同蒸煮工艺对富硒大米中总硒水平无显著性差异(P>0.05)[23],与本文研究结果一致。ADEBOWALE等[24]的研究表明热稳定性的矿物质不受挤压蒸煮的影响,但刘志东等[25]的研究表明挤压处理会造成南极磷虾粉中钙、铁等矿物质的损失。GRANT等[26]研究发现硒具有挥发性,以二甲基硒或二甲基二硒的形式从植物中挥发,由此推测挤压过程中较大的压力使大米中硒形成挥发性化合物[27],导致硒的损失。
2.3 加工方式对富硒大米硒形态的影响
通过酶法提取,高效液相色谱电感耦合等离子体法测定硒形态,比较样品与标品的峰面积得到样品中的硒形态及含量。如表2所示,富硒大米中最主要的硒形态为SeMet,未处理样品中SeMet的含量为187 μg/kg,占总硒70.86%,其次含有4.98%的Se(IV),还含有少量的MeSeCys,占总硒的1.32%。该结果与SUN等[23]研究类似,大米中主要的硒形态为SeMet,占总硒的83%~84%,其次是MeSeCys,占总硒的6.2%,还含有少量的Se(IV)及SeCys。
SeMet可以非特异性地代替蛋氨酸与蛋白质结合,形成硒结合蛋白,在蛋白质的正常周转过程中逐步释放到机体中,不断满足机体对硒的需求,富硒谷物中的SeMet被认为是长期补充硒的良好来源[16]。加工处理会导致富硒大米中主要硒形态SeMet有较大变化,由表2可得加工处理会显著减少大米中的SeMet含量,其中常压和微波处理对SeMet的影响较大,与未处理样品相比,常压和微波分别造成了17.28%和17.74%的损失,而高压和挤压造成的损失分别为11.17%和8.45%。有研究表明,在加工过程中SeMet常转换为硒代蛋氨酸-硒氧化物[15],由于硒化合物的不稳定性,蒸煮、煮沸、煎炸等常用的家庭烹饪方法均会导致谷物中SeMet的损失,最高损失可达46.9%[16];富硒大米中Se(IV)在微波、高压及挤压处理中完全损失,常压处理后还有部分保留。除SeMet外,其他非蛋白氨基酸主要存在于细胞壁中,不存在于蛋白质中[28],所以加工过程易损失;常压和挤压处理样品中,MeSeCys含量与未处理样品无显著差异(P>0.05),高压处理后含量降低,微波处理会使MeSeCys含量增加。AMOAKO等[29]的研究表明,加热会使酵母SeMet通过二甲基二烯酰亚胺等媒介形成MeSeCys,因此推测加工过程中MeSeCys含量升高是因为发生了硒形态的转换。
表2 富硒大米不同加工方式处理后主要硒形态及含量
Table 2 The main selenium forms and contents of selenium-enriched rice with different processing methods

加工方式硒形态各形态含量/(μg·kg-1)占有机硒比例/%占样品总硒比例/%常压蒸煮MeSeCys3.40±0.05b1.60±0.021.29±0.02Se(Ⅳ)6.81±0.63-2.58±0.24SeMet154.68±1.52C72.93±0.7258.61±0.58微波蒸煮MeSeCys4.61±0.35a2.17±0.161.75±0.13Se(Ⅳ)未检出--SeMet153.82±0.64C72.52±0.3058.29±0.24高压处理MeSeCys2.79±0.02c1.32±0.011.06±0.01Se(Ⅳ)未检出--SeMet166.11±3.48B78.31±1.6462.94±1.32挤压处理MeSeCys3.52±0.08b1.66±0.041.33±0.03Se(Ⅳ)未检出--SeMet171.19±8.21B80.71±3.8768.87±3.11未处理MeSeCys3.48±0.30b1.64±0.141.32±0.11Se(Ⅳ)13.15±1.16-4.98±0.44SeMet187.00±2.60A88.17±1.2370.86±0.98
注:同列肩标不同大写和小写字母分别表示不同加工方式处理后富硒大米中MeSeCys和SeMet含量差异显著(P<0.05)
2.4 加工方式对硒生物利用度的影响
不同加工方式处理富硒大米,硒在模拟体外胃肠消化过程中的生物利用度如图1所示,未处理样品胃消化硒生物利用度仅为30.79%,常压蒸煮方式最高,为38.38%,显著高于未处理样品,高压处理样品与未处理样品相比没有显著差异(P>0.05),挤压处理样品胃消化硒生物利用度为26.85%,显著低于未处理样品,这是由于挤压处理造成硒损失较大。肠道消化硒生物利用度与胃消化相比有明显提高,未处理样品的生物利用度由30.79%增加到45.69%,提升了14.90%,这与ZHANG等[18]的研究结果一致,与胃消化相比,大米样品中硒生物利用度在肠道消化后提升了13%,硒在肠道阶段的生物可利用度高于胃阶段,本文研究发现高压和常压处理使样品中更多的硒在肠消化过程释放。大米中硒主要存在于胚乳细胞的蛋白质中,在胃的酸性环境中,大米蛋白发生变性和部分展开,使大米中部分硒被释放,肠消化过程中,肠液中的胰酶和胆盐使大米中多糖和蛋白质被进一步分解为单糖和小肽(或游离氨基酸),促使大米中更多硒被释放,生物利用度增大[22-23]。

图1 不同加工方式处理富硒大米体外胃肠消化生物利用度
Fig.1 In vitro gastrointestinal digestion bioavailability of selenium-enriched rice with different processing methods 注:用不同的小写字母和大写字母分别表示样品在不同加工 处理后胃和肠道生物利用度有显著差异(P<0.05)
加工会改变富硒大米中硒的生物利用度,加工样品胃肠消化物中硒的生物利用度由高到低依次为:常压>高压>微波>挤压。常压、高压及微波处理后的样品硒生物利用度都显著高于未处理样品(P<0.05),说明这3种处理方式均利于人体对富硒大米中硒的吸收利用,常压处理后硒的利用率最高,比未处理样品高29.30%。相关研究发现,水煮、微波及压力烹饪对菌类和蔬菜中的硒生物利用度有促进作用[14,30]。硒生物利用度与硒含量、硒形态及食物中其他成分变化有关[14,17-18],加工会改变大米中主要大分子淀粉和蛋白的结构,影响大米中硒的生物利用度[30]。挤压处理造成的硒损失较大,生物利用度偏低,微波处理对SeMet含量的影响较大,处理后样品中硒的生物利用度较低。
2.5 加工方式对富硒大米体外消化后硒形态的影响
将不同加工方式处理的富硒大米样品进行体外模拟胃肠消化,测定消化液中的硒形态见表3,富硒大米经胃肠消化后主要的硒形态为MeSeCys和SeMet,Se(Ⅳ)经过胃肠消化后未检出,与KHANAM等[14]的研究结果一致,富硒大米加工处理后体外胃肠消化液中主要检出的形态为SeMet。
表3 不同加工方式处理富硒大米体外胃肠消化后 各形态硒含量
Table 3 Selenium forms after in vitro gastrointestinal digestion of selenium-enriched rice with different processing methods

加工方式硒形态各形态含量/(μg·kg-1)占消化液中总硒的比例/%常压蒸煮MeSeCys0.30±0.046.99±1.04Se(Ⅳ)未检出-SeMet1.85±0.0743.66±1.62微波蒸煮MeSeCys0.38±0.0211.31±0.64Se(Ⅳ)未检出-SeMet1.82±0.0753.46±2.08高压处理MeSeCys0.25±0.016.04±0.07Se(Ⅳ)未检出-SeMet1.67±0.0140.70±0.08挤压处理MeSeCys0.33±0.059.97±1.54Se(Ⅳ)未检出-SeMet1.88±0.1157.03±3.41未处理MeSeCys1.55±0.1245.65±3.43Se(Ⅳ)未检出-SeMet1.63±0.0547.98±1.43
富硒大米经4种方式加工处理后胃肠消化液中SeMet含量均高于未处理样品,MeSeCys含量与未处理样品相比均显著减少,说明常压、高压、微波及挤压处理有利于富硒大米中SeMet在消化过程中的释放和利用。食品中的硒在酶、光、热、压力等因素的作用下会发生转化和损失,硒化合物会通过酶途径或非酶途径相互转化。MeSeCys可被裂解酶降解形成挥发性甲基硒醇,或进一步转移到二甲基硒化物中,这可能是导致硒化合物在食品加工过程中的降解、挥发损失的原因[28]。SeMet在食物中以蛋白质组成形式存在,因此在加工过程中相对稳定[28]。
2.6 加工方式对富硒大米中SeMet生物利用度的影响
SeMet为富硒大米中最主要的硒形态,是最易被机体利用的形态[16],在膳食硒的代谢过程中,SeMet可替代蛋白质中的蛋氨酸,与组织中蛋白质发生结合,在组织蛋白的转换中转化为硒蛋白[10],或可转化为SeCys,在机体发挥其生理功能。不同加工方式处理富硒大米中SeMet的生物利用度体外模拟结果如图2所示,其中未处理样品中SeMet生物利用度为34.70%,加工处理可以提升大米中SeMet的生物利用度。挤压处理样品中SeMet的利用度为43.19%,高压处理后为42.27%,常压和微波处理后分别为47.49%和46.69%,常压处理生物利用度最高,与未处理相比提高了12.79%,与KHANAM等[14]的研究结果一致。加工会使食物中的基质发生改变,影响与基质结合的矿物质的利用,本文4种加工处理均有助于样品中SeMet在消化过程的释放,会对大米中主要硒形态的利用产生一定的积极作用。值得注意的是,虽然挤压处理会造成总硒生物利用度偏低,但SeMet的利用度在挤压处理后显著高于未处理样品,且处理后有利于大米中SeMet的利用。

图2 不同加工方式处理富硒大米SeMet生物利用度
Fig.2 Bioavailability of SeMet in selenium- enriched rice treated by different processing methods 注:不同字母表示组间差异显著(P<0.05)
3 结论
本文通过常压、微波、高压及挤压处理对富硒大米进行加工处理,探究不同加工方式对富硒大米中硒含量、形态及生物利用度的影响,结果表明,挤压处理导致硒损失43.05%,常压、高压、微波处理不会对硒含量产生显著影响(P<0.05);4种加工方式均降低了大米中SeMet的含量,Se(IV)经微波、高压及挤压处理后完全损失,微波处理会使MeSeCys含量增加;体外模拟胃肠消化实验结果发现,常压、高压加工处理能够显著提高富硒大米样品胃肠消化后总硒生物利用度;4种加工方式均可提高富硒大米中SeMet的生物利用度,有助于样品中SeMet在消化过程的释放,对大米中主要硒形态的生物利用产生一定的积极作用。综上所述,常压和高压蒸煮方式对富硒大米总硒含量及形态影响较小,有利于机体对硒的吸收利用。本研究为富硒大米在常见米制品加工方式及体外消化过程中硒损失、形态及生物利用度变化情况提供数据支撑。
[1] LIDON F C, OLIVEIRA K, RIBEIRO M M, et al.Selenium biofortification of rice grains and implications on macronutrients quality[J].Journal of Cereal Science, 2018, 81:22-29.
[2] 胡婷, 吴文良, 赵桂慎, 等.我国富硒农产品及食品标准体系发展与展望[J].中国标准化, 2019(11):136-144.
HU T, WU W L, ZHAO G S, et al.Development and prospect of selenium-enriched agricultural products and foods standards in China[J].China Standardization, 2019(11):136-144.
[3] ZHANG L Q, SONG H X, GUO Y B, et al.Benefit-risk assessment of dietary selenium and its associated metals intake in China (2017-2019):Is current selenium-rich agro-food safe enough?[J].Journal of Hazardous Materials, 2020, 398:123224.
[4] ZHANG Z H, GAO S P, CHU C C.Improvement of nutrient use efficiency in rice:Current toolbox and future perspectives[J].Theoretische Und Angewandte Genetik, 2020, 133(5):1 365-1 384.
[5] YAO B M, CHEN P, SUN G X.Distribution of elements and their correlation in bran, polished rice, and whole grain[J].Food Science & Nutrition, 2020, 8(2):982-992.
[6] TANG D, CHENG Z K.From basic research to molecular breeding—Chinese scientists play a central role in boosting world rice production[J].Genomics, Proteomics & Bioinformatics, 2018, 16(6):389-392.
[7] 龚如雨. 大米中硒的赋存形态及其生物可利用度研究[D].南昌:南昌大学, 2018.
GONG R Y.Speciation of selenium in rice and its bioaccessibility[D].Nanchang:Nanchang University, 2018.
[8] SUN G X, LIU X, WILLIAMS P N, et al.Distribution and translocation of selenium from soil to grain and its speciation in paddy rice (Oryza sativa L.)[J].Environmental Science & Technology, 2010, 44(17):6 706-6 711.
[9] FAIRWEATHER-TAIT S J, COLLINGS R, HURST R.Selenium bioavailability:Current knowledge and future research requirements[J].The American Journal of Clinical Nutrition, 2010, 91(5):1 484S-1 491S.
[10] HU T, HUI G F, LI H F, et al.Selenium biofortification in Hericium erinaceus (lion’s mane mushroom) and its in vitro bioaccessibility[J].Food Chemistry, 2020, 331:127287.
[11] D’AMATO R, REGNI L, FALCINELLI B, et al.Current knowledge on selenium biofortification to improve the nutraceutical profile of food:A comprehensive review[J].Journal of Agricultural and Food Chemistry, 2020, 68(14):4 075-4 097.
[12] RAYMAN M P.Food-chain selenium and human health:Emphasis on intake[J].The British Journal of Nutrition, 2008, 100(2):254-268.
[13] FIDELIS R R, CAMPESTRINI R, MARTINEZ R A S, et al.Physiological quality of rice in the function of selenium doses[J].Revista De Agricultura Neotropical, 2018, 5(3):30-38.
[14] KHANAM A, PLATEL K.Bioaccessibility of selenium, selenomethionine and selenocysteine from foods and influence of heat processing on the same[J].Food Chemistry, 2016, 194:1 293-1 299.
[15] VICENTE-ZURDO D, G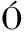 MEZ-G
MEZ-G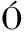 MEZ B, PÉREZ-CORONA M T, et al.Impact of fish growing conditions and cooking methods on selenium species in swordfish and salmon fillets[J].Journal of Food Composition and Analysis, 2019, 83:103275.
MEZ B, PÉREZ-CORONA M T, et al.Impact of fish growing conditions and cooking methods on selenium species in swordfish and salmon fillets[J].Journal of Food Composition and Analysis, 2019, 83:103275.
[16] LU X Q, HE Z S, LIN Z Q, et al.Effects of Chinese cooking methods on the content and speciation of selenium in selenium bio-fortified cereals and soybeans[J].Nutrients, 2018, 10(3):317.
[17] PYRZYNSKA K, SENTKOWSKA A.Selenium in plant foods:Speciation analysis, bioavailability, and factors affecting composition[J].Critical Reviews in Food Science and Nutrition, 2021, 61(8):1 340-1 352.
[18] ZHANG R, LI Y H, XU Y F, et al.Effects of dietary supplements on the bioaccessibility of Se, Zn and Cd in rice:Preliminary observations from in vitro gastrointestinal simulation tests[J].International Journal of Environmental Research and Public Health, 2020, 17(14):4978.
[19] 周小理, 王惠, 周一鸣, 等.不同烹煮方式对米饭食味品质的影响[J].食品科学, 2017, 38(11):75-80.
ZHOU X L, WANG H, ZHOU Y M, et al.Influence of different cooking methods on eating quality of rice[J].Food Science, 2017, 38(11):75-80.
[20] 陈怡岑, 何欢, 李万军, 等.粮谷重制米挤压工艺的优化[J].食品工业, 2019, 40(12):21-26.
CHEN Y C, HE H, LI W J, et al.Optimization of extrusion process for grain remaking rice[J].Food Industry, 2019, 40(12):21-26.
[21] 李志全, 龚国珍.食品中有机硒无机硒的检测[J].检验检疫学刊, 2019, 29(3):47-48.
LI Z Q, GONG G Z.Determination of organic selenium and inorganic selenium in food[J].Journal of Inspection and Quarantine, 2019, 29(3):47-48.
[22] LIU K L, ZHENG J B, CHEN F S.Effects of washing, soaking and domestic cooking on cadmium, arsenic and lead bioaccessibilities in rice[J].Journal of the Science of Food and Agriculture, 2018, 98(10):3 829-3 835.
[23] SUN G X, VAN DE WIELE T, ALAVA P, et al.Bioaccessibility of selenium from cooked rice as determined in a simulator of the human intestinal tract (SHIME)[J].Journal of the Science of Food and Agriculture, 2017, 97(11):3 540-3 545.
[24] ADEBOWALE A A, KAREEM S T, SOBUKOLA O P, et al.Mineral and antinutrient content of high quality cassava-tigernut composite flour extruded snack[J].Journal of Food Processing and Preservation, 2017, 41(5):e13125.
[25] 刘志东, 陈勇, 曲映红, 等.挤压加工对南极磷虾粉营养组分的影响[J].海洋渔业, 2016, 38(3):311-319.
LIU Z D, CHEN Y, QU Y H, et al.Effect of pressing processing on the nutritional components of Antarctic krill powder[J].Marine Fisheries, 2016, 38(3):311-319.
[26] GRANT T D, MONTES-BAY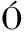 N M, LEDUC D, et al.Identification and characterization of Se-methyl selenomethionine in Brassica juncea roots[J].Journal of Chromatography A, 2004, 1026(1-2):159-166.
N M, LEDUC D, et al.Identification and characterization of Se-methyl selenomethionine in Brassica juncea roots[J].Journal of Chromatography A, 2004, 1026(1-2):159-166.
[27] KIELISZEK M.Selenium-fascinating microelement, properties and sources in food[J].Molecules, 2019, 24(7):1 298.
[28] MO H, LI G, WEI X.Benefit and risk of selenium supplement[J].Agro Food Industry Hi Tech, 2013, 24(4):4-6.
[29] AMOAKO P O, KAHAKACHCHI C L, DODOVA E N, et al.Speciation, quantification and stability of selenomethionine, S-(methylseleno)cysteine and selenomethionine Se-oxide in yeast-based nutritional supplements[J].Journal of Analytical Atomic Spectrometry, 2007, 22(8):938.
[30] ZHOU F, PENG Q, WANG M, et al.Influence of processing methods and exogenous selenium species on the content and in vitro bioaccessibility of selenium in Pleurotus eryngii[J].Food Chemistry, 2021, 338:127661.