合成高分子化合物制成的各类材料因较好的包装性能故而被广泛使用,但由于其降解难且废弃后产生的污染问题,正逐渐影响到生态环境。明胶(gelatin,GEL)可从食品加工废物中获得,其主要成分为蛋白质,通常由胶原经过物理、化学降解或热变性得到。作为一种具有良好的组织相容性、生物降解性和生物相容性的天然高分子材料[1],GEL有望应用于肉制品和水产品包装、医学材料和农业覆膜等方面[2-5],是食品包装材料的一种可持续替代品。GEL膜具有一定的阻隔性能,但因其易溶于水且机械性能较差无法满足不同情况的需要,因此有必要对其进行复合或改性[6]。
交联改性是提高GEL膜性能的一种重要手段,利用醛类的醛基和GEL链上的氨基之间发生席夫碱反应形成共价键,使界面相互作用最大化,改变复合材料的整体理化性质[7]。戊二醛是目前GEL常用的化学交联改性剂,可在较短时间内有效交联GEL,有效改善其机械性能和水中的稳定性能[8],但由于戊二醛具有一定的细胞毒性且易挥发,气味刺激,因此限制了其在食品包装上的应用。二醛基纤维素(dialdehyde cellulose,DAC)是高碘酸钠选择性氧化纤维素的产物,广泛应用于医疗行业[9-10],可利用大分子链上的醛基和GEL分子链上的氨基之间发生席夫碱反应形成碳氮双键共价键,因此有望通过交联改善材料的整体理化性质[7]。
本研究通过向GEL溶液中添加不同质量分数水溶性DAC制备DAC/GEL复合膜,并对其化学、力学、透湿、透氧、热稳定性和溶解性能进行表征,探究交联剂DAC添加量对复合膜的影响,确定DAC/GEL复合膜最佳的配比方案,以期为其在食品绿色包装材料的应用提供参考。
1 材料与方法
1.1 材料与试剂
纤维素粉、高碘酸钠(均为分析纯),上海麦克林生化科技有限公司;GEL(化学纯),国药集团化学试剂有限公司。
1.2 仪器与设备
Spectrum100傅立叶变换红外光谱仪,珀金埃尔默公司;SCW-500电子拉力机、W3/060水蒸气透过率测试系统、C230H氧气透过率测试系统,济南兰光公司;Theta·Flex水接触角测定仪,上海大昌华嘉公司;TGA550热重分析仪,美国TA公司;SU8020扫描电镜(scanning electron microscope,SEM),日本日立公司。
1.3 实验方法
二醛纤维素/明胶复合膜的制备通过溶剂蒸发法制备二醛基纤维素交联的明胶复合膜(D-GEL)。取10 g GEL溶于90 g去离子水,45 ℃下搅拌均匀,形成质量分数为10%的GEL溶液。利用高碘酸钠对纤维素的选择性氧化制备2,3-DAC溶液。将纤维素粉和高碘酸钠溶于去离子水中,在常温下避光搅拌反应72 h,产物用去离子水纯化后于100 ℃加热溶解[11],最后高转速下离心去除杂质,得到DAC溶液。分别将占GEL干重0%、1%、5%、10%、15%和20%的DAC溶液加入到GEL溶液中,将此共混液于30 ℃水浴中磁力搅拌均匀。将共混液倒在直径为12 cm×12 cm方形培养皿内,干燥后得到DAC/GEL复合膜,记为D-GEL。将不同DAC占比的复合膜依次命名为GEL、1%D-GEL、5%D-GEL、10%D-GEL、15%D-GEL和20%D-GEL。
1.3.2 D-GEL性能测定及表征
1.3.2.1 红外光谱分析
称取0.01 g干燥D-GEL粉末,与1.00 g干燥的KBr一同放入研钵中研磨混匀,取0.1 g研磨后的粉末,平铺在模具中置于压片机内,抽气加压2 min左右后压制成片。将样品压片放入傅里叶红外光谱仪中进行扫描测定,扫描次数:32次,分辨率:4 cm-1,扫描范围:500~4 000 cm-1。
1.3.2.2 SEM
将复合膜进行冷冻干燥,对冷冻干燥的样品表面喷金,采用场发射SEM以3.00 kV的加速电压对薄膜进行表面和横截面的形貌分析。
1.3.2.3 透光性
将10 mm×50 mm的D-GEL复合膜置于紫外-可见分光光度计中,在200~800 nm以1 nm/s的扫描速度测量复合膜的透光性[12]。
1.3.2.4 拉伸强度
参照标准GB 13022—91 《塑料薄膜拉伸性能试验方法》。首先测量复合膜的厚度,每张膜随机测量10个点取算数平均值。将膜裁成100 mm×15 mm的长条,用电子拉力机的夹具夹紧试样的两端,使试样的长轴与夹具中心连线重合,测试距离和速度分别为50 mm和25 mm/s。每种复合膜样品的抗拉强度做3次平行实验,结果取平均值。
1.3.2.5 断裂伸长率
参照标准GB 13022—91 《塑料薄膜拉伸性能试验方法》。将膜裁成100 mm×15 mm的长条,用电子拉力机的夹具夹紧试样的两端,测试距离和速度分别为50 mm和25 mm/s。每种复合膜样品的断裂伸长率分别做3次平行实验,结果取平均值。
1.3.2.6 透湿性能
将复合膜裁剪为直径7 cm的圆片,测量其厚度,每张膜随机测量10个点取平均值。将10 mL蒸馏水加入透湿杯中,正确组装透湿杯并盖紧杯盖,将夹有样品的透湿杯放入透湿测试系统中,输入各腔室复合膜的厚度,设置温度25 ℃,湿度50%,启动测试。试验每隔2 h称量1次重量,共称量8次,每种DAC浓度的样品测试3组平行数据,结果取平均值[13]。
1.3.2.7 透氧性能
参照标准GB 1037—88《塑料薄膜和片材透水蒸气性试验方法 杯式法》。将复合膜裁剪为直径10 cm的圆片,并在相应的位置打孔。测量薄膜厚度,每张膜取均匀分布的10点,取平均值。将裁剪好的样品薄膜装入测试系统中,设置N2、O2的压力分别为0.25、0.1 MPa,温度、湿度分别为23 ℃,50%,启动测试。实验每隔8 h测试1次,共测3次,每种DAC浓度的样品测试3组平行数据,结果取平均值。
1.3.2.8 溶胀度
将D-GEL薄膜裁剪成3 cm×3 cm的试样条,在40 ℃环境下烘干至恒重并测量试样条重量,将试样条放入容器内并加入去离子水直至没过试样条,浸泡24 h,用滤纸吸干试样条表面多余的水分后再次称量试样条重量,每种DAC浓度的样品测试3组平行数据,结果取平均值[14]。薄膜的水溶性计算如公式(1)所示:
(1)
式中:Q为薄膜的水溶性,%;W0为样品浸泡前的质量,g;W1为样品浸泡后的质量,g。
1.3.2.9 溶解度
将D-GEL薄膜裁剪成3 cm×3 cm的试样条,在40 ℃环境下烘干至恒重并测量试样条重量,将试样条放入容器内并加入去离子水直至没过试样条,浸泡24 h后捞出,再在40 ℃环境下烘干至恒重并记录重量,每种DAC浓度的样品测试3组平行数据,结果取平均值[14]。薄膜的溶解度计算如公式(2)所示:
(2)
式中:S为薄膜的溶解度,%;W0为样品浸泡前的质量,g;W1为样品浸泡后的质量,g。
1.3.2.10 亲水性
采用水静态接触角测量法。在材料表面滴加10 μL超纯水,通过滴形分析仪将薄膜表面的液滴放大投影到屏幕上,并测量液滴边缘切线与相界面的夹角,通过测量夹角的大小来分析薄膜的亲水性[15]。
1.3.2.11 热稳定性能
剪取8~10 mg复合膜,放入氧化铝坩埚中,在氮气环境下进行热重测试,气流速率设置为50 mL/min,升温速率为10 ℃/min,测试温度为50~600 ℃。
1.4 数据处理与分析
采用Excel 2016和IBM SPSS Statistics 26软件进行数据分析,并通过 Duncan多重检验法检验显著性,P<0.05为差异显著。使用Origin 8.0软件制图。
2 结果与分析
2.1 D-GEL的表征
食品包装薄膜的颜色至关重要,其直接影响产品外观及消费者的可接受度。图1为不同DAC浓度制得D-GEL薄膜的外观形貌图。由图1可知,无论是否添加DAC,薄膜透明度均良好,表面光洁平整,这说明DAC与GEL溶液在成膜过程中具有良好的相容性。随着DAC添加量的增加,所制得的复合膜表现出淡黄色,但其透明度依然非常好。

图1 不同DAC含量的D-GEL复合膜的外观形貌图
Fig.1 Visual photos of the D-GEL composite films with different DAC content
图2是D-GEL薄膜的透光率曲线,透光率的大小可用来反映复合膜对不同光线的阻隔能力及薄膜体系内各部分的相容性。当加入DAC后,薄膜在可见光区(400~780 nm)的透光率出现小幅度的下降,但不影响其整体透光度,这从图1中可以很明显地看出,可能是由于DAC的加入使GEL的原始结构遭到破坏,光在非晶区及晶区界面产生散射,光通路发生改变[16]。图2-B为复合膜在紫外光区UV-A(315~400 nm)、UV-B(280~315 nm)和UV-C(200~280 nm)3个区域的阻光性能,如图所示,纯GEL膜在UV-A、UV-B、UV-C区域的透光率分别有90.4%、79.3%和48.3%,而15%D-GEL在UV-A、UV-B和UV-C区域的透光率降至53.8%、9.0%和9.5%,分别降低了36.6%、70.3%和38.8%,说明DAC的加入可增强复合膜材料对紫外线的阻隔能力,可能是因为DAC与GEL反应后生成了一些可以吸收或反射紫外光线的基团,导致薄膜对紫外线的阻隔性能加强,当DAC添加量达到饱和后,继续添加破坏薄膜原有的致密结构,导致20%D-GEL阻隔性下降。
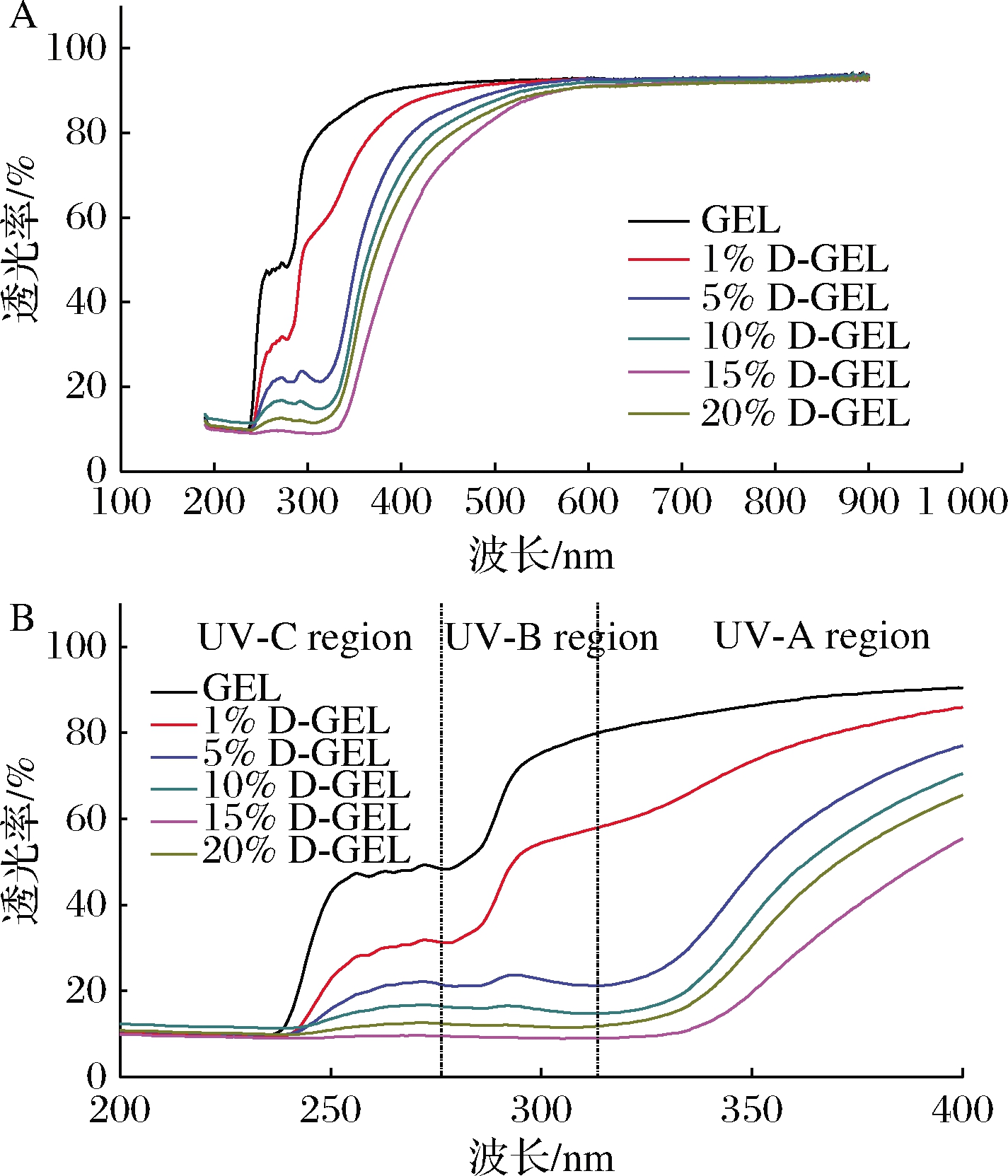
A-200~800 nm;B-UV-A、UV-B、UV-C区域
图2 D-GEL复合膜在200~800 nm及UV-A、UV-B、 UV-C区域的透光性
Fig.2 The transmittance of D-GEL composite films at 200~800 nm and UV-A, UV-B, UV-C region
傅里叶红外光谱技术可以作为一种直接评价纤维素氧化后结构变化的方法。图3为纯GEL、DAC及D-GEL的红外光谱图,其中GEL特征峰分别位于1 657、1 534和1 241 cm-1,分别代表酰胺I带、Ⅱ带和Ⅲ带[17]。DAC的特征峰位于2 945、1 733和1 641 cm-1,代表—CHO中C![]() O的非对称谱峰[18-19]。DAC与GEL的交联反应主要是GEL上的氨基与DAC上的醛基发生反应,形成席夫碱结构C
O的非对称谱峰[18-19]。DAC与GEL的交联反应主要是GEL上的氨基与DAC上的醛基发生反应,形成席夫碱结构C![]() N,其吸收峰在1 690~1 630 cm-1,与GEL酰胺I带处的特征峰重叠,形成了1 664 cm-1的新峰[20],1 610 cm-1处可能为C
N,其吸收峰在1 690~1 630 cm-1,与GEL酰胺I带处的特征峰重叠,形成了1 664 cm-1的新峰[20],1 610 cm-1处可能为C![]() N的伸缩振动峰。由图3可知,复合后DAC在1 641和1 733 cm-1处的特征峰消失,GEL酰胺I带的特征峰从1 657移动到1 664 cm-1,酰胺Ⅱ带的特征峰从1 534移动到1 535 cm-1,酰胺Ⅲ带未发生移动,说明DAC与GEL产生了有效的交联。
N的伸缩振动峰。由图3可知,复合后DAC在1 641和1 733 cm-1处的特征峰消失,GEL酰胺I带的特征峰从1 657移动到1 664 cm-1,酰胺Ⅱ带的特征峰从1 534移动到1 535 cm-1,酰胺Ⅲ带未发生移动,说明DAC与GEL产生了有效的交联。

A-红外光谱全谱分析;B-红外光谱1 200~2 000 cm-1波谱分析
图3 DAC、GEL和D-GEL的红外光谱分析
Fig.3 Fourier transform infrared spectroscopy of DAC, GEL and D-GEL
图4为纯GEL薄膜与D-GEL复合薄膜的SEM照片。由图4可知,复合前后薄膜表面均光滑平整且无明显纹路,横断面致密连续,DAC加入后并没有出现明显的分相,说明GEL与DAC具有良好的相容性。复合后薄膜表面出现少量白色晶体,可能是因为DAC在交联过程中,由于其分子间作用力而产生的聚集现象;复合后断面也更为粗糙,可能的原因是由于交联后产生共价键使得薄膜形成了新的网状结构。

A-GEL的SEM图;B-D-GEL的SEM图;C-GEL横截面SEM图; D-D-GEL横截面SEM图
图4 GEL和D-GEL的SEM图及GEL和D-GEL的 横截面SEM图
Fig.4 SEM images of GEL and D-GEL;cross section SEM images of GEL and D-GEL
2.2 D-GEL的力学性能
力学性能是衡量包装材料物理性质的重要指标,薄膜的拉伸强度直接决定其能否对食品提供完整的物理保护。D-GEL复合膜的拉伸强度和断裂伸长率如图5所示。随着DAC添加量的增加,复合膜的力学性能呈现先增后减的趋势,其原因可能是由于GEL上的氨基与DAC的醛基发生席夫碱反应形成共价键,增加了分子内部链间的联系;当DAC的添加量达到饱和状态后,继续添加会降低聚合物基质的内聚力,降低薄膜强度[21]。实验组中添加了10% DAC制得的复合膜的力学性能最好,在拥有一定抗拉伸强度的同时维持了较好的断裂伸长率,其抗拉强度和断裂伸长率分别比纯GEL膜增加了45.9%和19.7%,5%以上的DAC添加量能显著够提高薄膜的拉伸强度(P<0.05)。杨斯乔等[22]研究甲壳素对GEL薄膜的影响,在添加0.5%的甲壳素后复合膜的拉伸强度为20 MPa左右,随着添加继续呈现波浪状的下降趋势。曹蓓等[23]以环氧氯丙烷作为羟丙基纤维素和GEL的交联剂制备复合膜,当GEL占比达到50%时,复合膜拉伸强度为29.43 MPa,断裂伸长率为8.28%,之后随GEL占比减小均而不断降低。相比于其他交联改性剂,DAC的添加能使GEL薄膜的拉伸强度得到较大的提升,满足日常使用的需求。

A-拉伸强度;B-断裂伸长率
图5 不同DAC含量的D-GEL复合膜的拉伸强度 和断裂伸长率
Fig.5 Tensile strength and elongation at break of D-GEL composite films with different DAC content
注:不同小写字母表示差异显著(P<0.05)(下同)
2.3 D-GEL的水中溶胀度、溶解度以及水接触角
GEL固有的亲水性在很大程度上限制了其作为食品包装材料的应用。物理交联、热处理或戊二醛等方法都可以用来增强GEL膜的阻水性[24],DAC作为一种绿色材料可以取代有一定毒性的戊二醛作为交联剂。图6是D-GEL复合膜的溶胀度和溶解性,可以看出DAC的添加能显著减小复合膜的溶胀度和溶解度(P<0.05),5%的DAC添加量可使其分别降低86.3%和65.3%。因此,DAC能够提高GEL薄膜在水中的稳定性,是一种有效的交联剂。杨斯乔等[22]在GEL中加入0%~20%甲壳素后测量其溶胀度(吸水率),所有实验组在浸泡12 h后溶胀度均在400%以上,说明DAC比甲壳素能更有效地改善GEL薄膜在水中的稳定性。裴莹等[25]制备的纳米纤维素晶须/GEL复合膜,薄膜初始溶胀度为378%,并随着纳米纤维素晶须的加入而不断减小,当晶须含量为15%时复合膜溶胀度最低,降至为95%,与本实验结果差别不大。
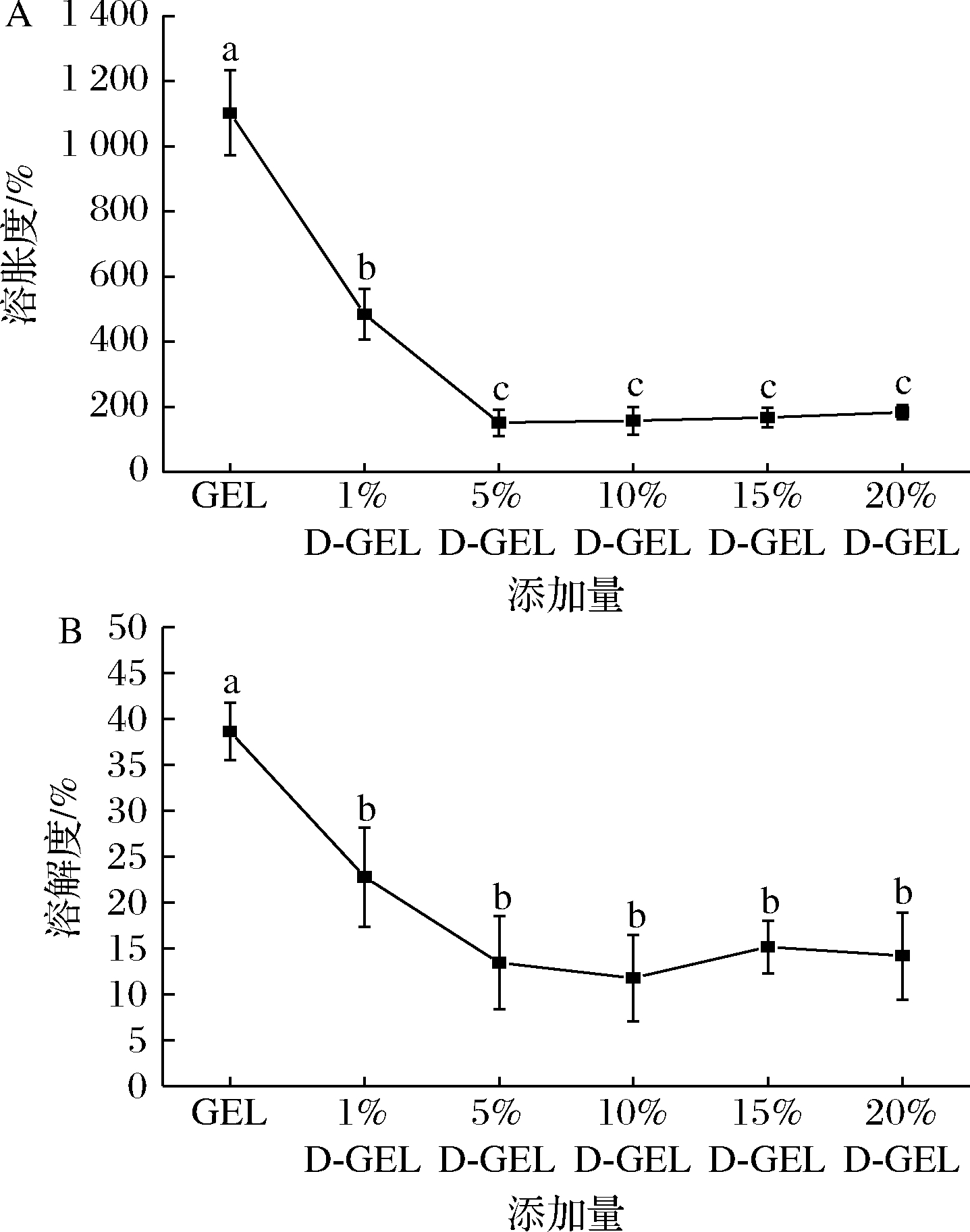
A-溶胀度;B-溶解度
图6 不同含量DAC的D-GEL复合膜的溶胀度和溶解度
Fig.6 Swelling capacity and solubility of D-GEL composite films with different DAC content
亲水性即材料对水分子的亲和力,是决定聚合物材料适用性的重要因素,通常通过水滴与膜表面接触的接触角度来确定,角度越小代表材料亲水性越好。图7是水滴在D-GEL复合膜表面的图像,由图7可知,DAC的加入使复合膜亲水性出现不同程度的减小,随着DAC添加量的增大,水接触角增大,说明复合膜抵抗水分子渗透的能力增强。

A-GEL;B-1%D-GEL;C-5%D-GEL;D-10%D-GEL; E-15%D-GEL;F-20%D-GEL
图7 不同含量DAC的D-GEL复合膜表面的水接触角图
Fig.7 Images of water contact angles on the surface of D-GEL composite films with different DAC content
2.4 D-GEL的阻隔性能
阻隔性能是食品包装薄膜的另一项重要指标,主要指针对水蒸气和氧气的阻隔率,较强的阻隔性能有利于延长食品的货架期。D-GEL复合膜的透湿系数如图8所示,DAC的加入能够显著降低GEL膜的水蒸气透过系数(P<0.05),其中10%D-GEL水蒸气透过系数最低,与GEL相比降低了13.6%,20%次之,15%D-GEL的透过系数有略微升高,可能的原因是过量的DAC会减弱其分子间作用力,导致阻隔性降低,而继续添加DAC后,其在原有的复合膜上形成了1层新的膜,限制了水蒸气的通过。张金丽等[26]向鱼鳞GEL中添加纳米银颗粒制备复合膜,其透湿系数随纳米银颗粒的添加而减小,与本实验结果差别不大。
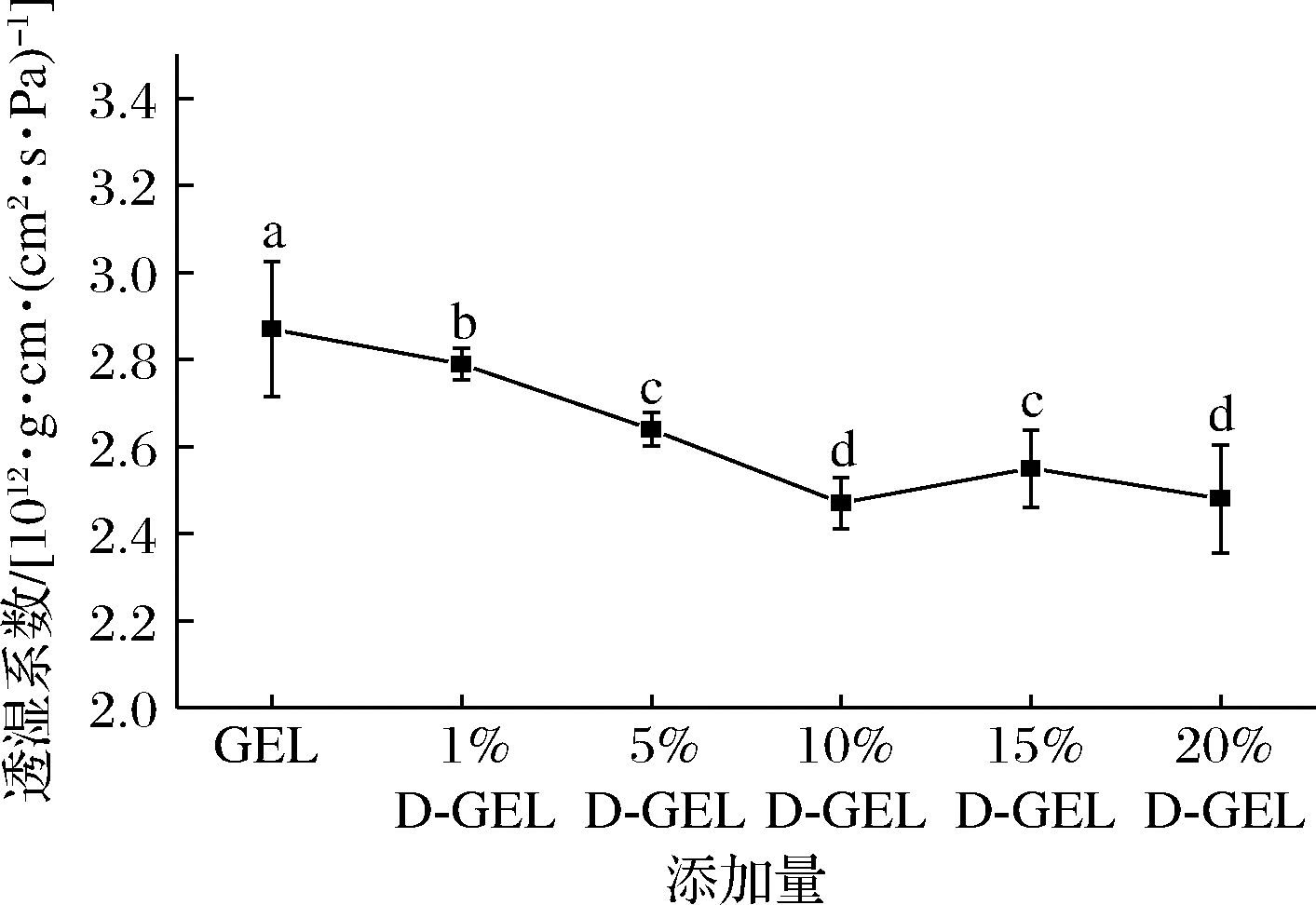
图8 不同含量DAC的D-GEL复合膜的透湿系数
Fig.8 Water vapor permeability of D-GEL composite films with different DAC content
图9是D-GEL复合膜的透氧系数,当添加20%DAC时,复合膜透氧系数相比原先下降18.5%(P>0.05)。DAC的加入可以提高GEL内部分子间的作用力和紧密度,从而使得水蒸气和氧气分子在膜内所经过的路径变得更加复杂,延长其扩散时间[27],增加复合膜的阻隔性能。
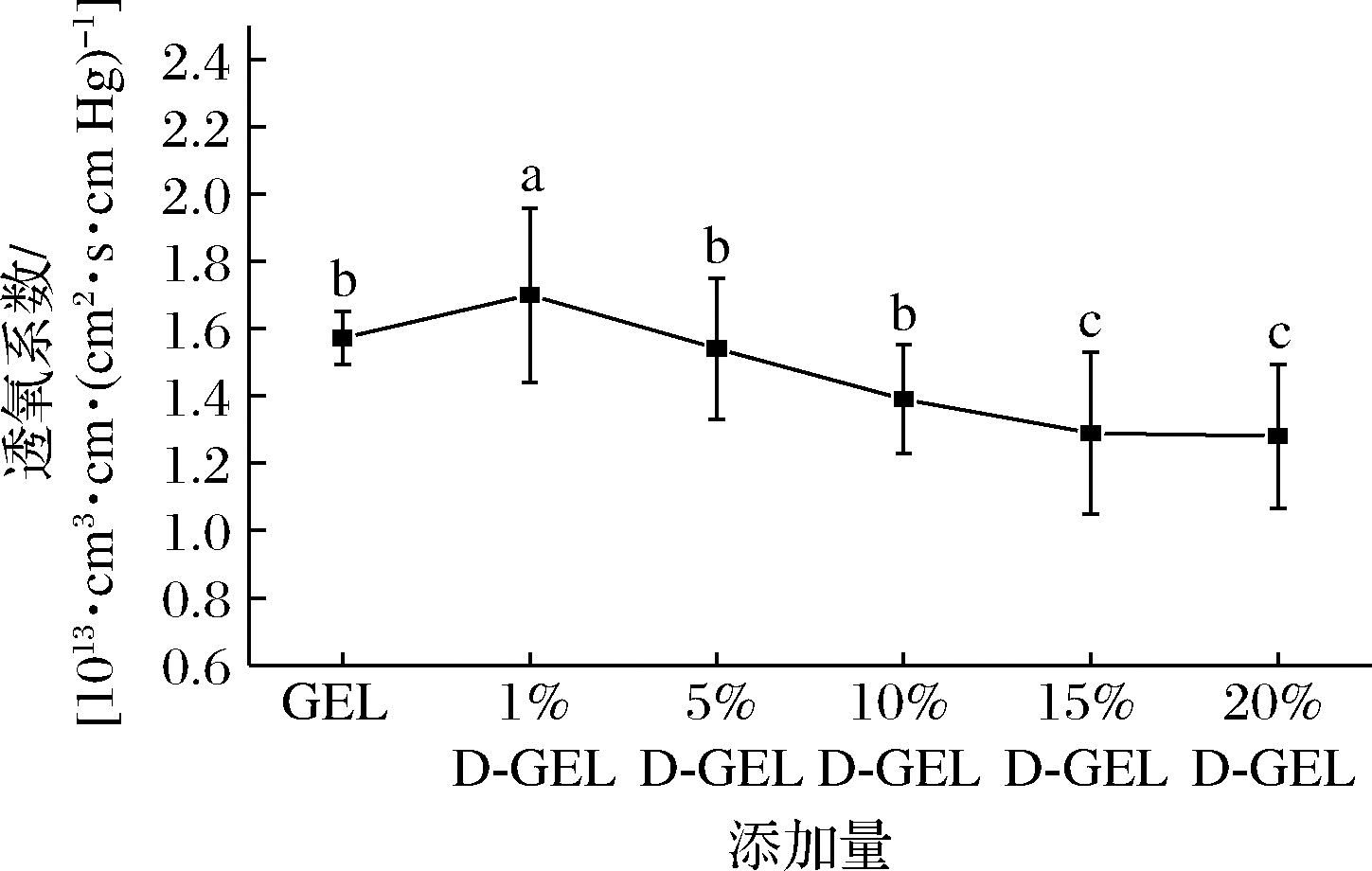
图9 不同含量DAC的D-GEL复合膜的透氧系数
Fig.9 Oxygen permeability of D-GEL composite films with different DAC content
2.5 D-GEL的热稳定性能
图10为D-GEL复合膜的热重分析曲线。质量损失第1阶段是25~240 ℃,损失约为20%,该温度下主要是薄膜中的水分、挥发性物质和一些作用力较弱的化学键断裂或蒸发,25~50 ℃下复合膜质量损失在10%以内,说明其在常温下热稳定性能良好。240~470 ℃为质量损失第2阶段,该阶段质量从80%降到了20%,DAC的大分子链和GEL中的肽键发生了热分解[28];10%D-GEL和20%D-GEL的热分解曲线较纯GEL膜发生了左移,说明交联会使复合膜的热分解温度降低。470~600 ℃为质量损失第3阶段,该阶段材料基本完全碳化。D-GEL的热重曲线较GEL发生了左移,表明复合后GEL膜的热稳定性略微下降,可能的原因是交联生成的席夫碱稳定性较差,在高温下易分解。总的来说,DAC的添加对GEL材料的热稳定性没有太大的影响。可能是由于新生成的席夫碱键虽然能加强DAC与GEL之间界面的结合力[29],但其在一定温度下不稳定所导致的。
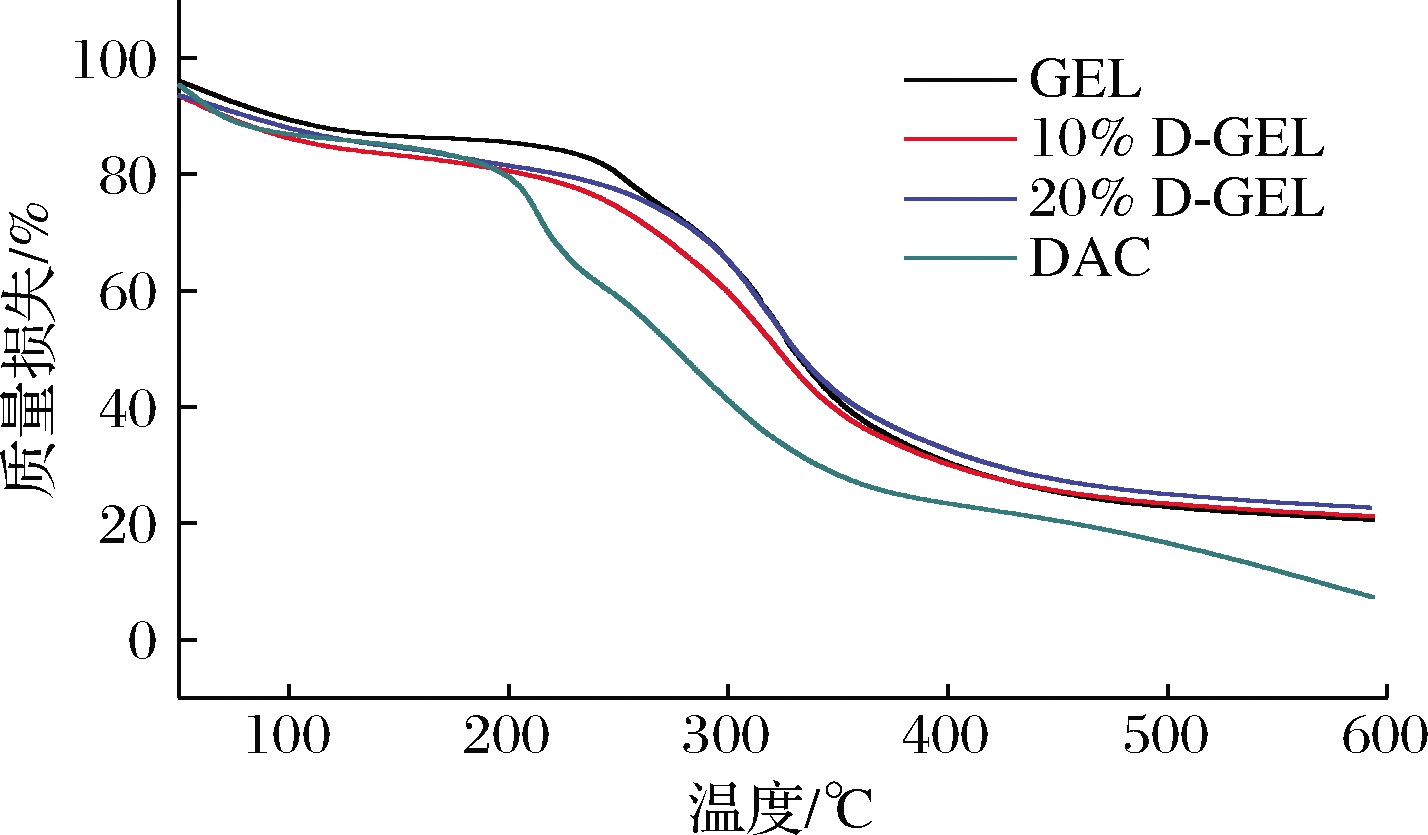
图10 GEL、DAC及D-GEL的热重分析曲线
Fig.10 Thermogravimetric analysis curves of GEL, DAC and D-GEL
3 结论
DAC与GEL溶液在成膜过程中具有良好的相容性,随着DAC浓度的增加,复合膜对可见光的透过率几乎无影响,但其对紫外线的屏蔽能力显著增强,其力学性能先增后减,10%D-GEL力学性能最好,拉伸强度和断裂伸长率较纯GEL膜分别增加了45.9%和19.7%。交联后D-GEL复合膜在水中稳定性明显提高,仅1%DAC的加入就可使其溶胀度和溶解度分别下降618.3%和15.9%。20%D-GEL的阻隔性能最好,水蒸气和氧气透过系数分别下降了13.6%和18.5%,DAC对改善GEL薄膜的热稳定性能无明显作用。
[1] 郭允, 杨硕晔.明胶的应用研究进展[J].河南职工医学院学报, 2013, 25(2):228-230.
GUO Y, YANG S Y.Research progress of gelatin application[J].Journal of Henan Medical College for Staff and Workers, 2013, 25(2):228-230.
[2] CHANG T.Artificial Cells:Biotechnology, Nanomedicine, Regenerative Medicine, Blood Substitutes, Bioencapsulation, and Cell/Stem Cell Therapy[M].Singapore:World Scientific, 2007.
[3] 缪进康. 明胶及其在科技领域中的利用[J].明胶科学与技术, 2009, 29(1):28-49;51.
MIAO J K.Utilization of gelatin on sci-technical areas[J].The Science and Technology of Gelatin, 2009, 29(1):28-49;51.
[4] 王碧, 刘凯, 张良英.2,4-D在明胶/壳聚糖微球中的包埋与释放[J].内江师范学院学报, 2008, 23(6):57-60.
WANG B, LIU K, ZHANG L Y.2, 4-D embedded in and release from gelatin/chitosan microsphere[J].Journal of Neijiang Normal University, 2008, 23(6):57-60.
[5] 任佳欣, 遇世友, 许锡凯, 等.可食性蛋白膜在食品包装中的应用研究进展[J].食品工业科技, 2020, 41(9):320-326.
REN J X, YU S Y, XU X K, et al.Application research progress of edible protein film in food packaging[J].Science and Technology of Food Industry, 2020, 41(9):320-326.
[6] 王毅虎, 卢伟鹏, 张兵, 等.明胶膜改性的研究进展[J].明胶科学与技术, 2013, 33(3):143-146.
WANG Y H, LU W P, ZHANG B, et al.Research progress on modification of gelatin film[J].The Science and Technology of Gelatin, 2013, 33(3):143-146.
[7] KWAK H W, LEE H, PARK S, et al.Chemical and physical reinforcement of hydrophilic gelatin film with di-aldehyde nanocellulose[J].International Journal of Biological Macromolecules, 2020, 146:332-342.
[8] 王雄清, 代敏, 郭文宇, 等.戊二醛-明胶-纳米SiO2复合膜的抑菌试验研究[J].江苏农业科学, 2009,37(1):218-220.
WANG X Q, DAI M, GUO W Y, et al.Study on antibacterial effect of the glutaraldehyde/gelatin/nano-SiO2 composite membrane[J].Jiangsu Agricultural Sciences, 2009,37(1):218-220.
[9] YAGI M, KATO S, NISHITOBA T, et al.Effects of chitosan-coated dialdehyde cellulose, a newly developed oral adsorbent, on glomerulonephritis induced by anti-Thy-1 antibody in rats[J].Nephron, 1998, 78(4):433-439.
[10] BLAIR S D, BACKHOUSE C M, HARPER R, et al.Comparison of absorbable materials for surgical haemostasis[J].British Journal of Surgery, 1988, 75(10):969-971.
[11] YAN G H, ZHANG X Q, LI M Z, et al.Stability of soluble dialdehyde cellulose and the formation of hollow microspheres:Optimization and characterization[J].ACS Sustainable Chemistry & Engineering, 2019, 7(2):2 151-2 159.
[12] KUMAR R, KUMARI S, RAI B, et al.Effect of nano-cellulosic fiber on mechanical and barrier properties of polylactic acid (PLA) green nanocomposite film[J].Materials Research Express, 2019, 6(12):125108.
[13] SRINIVASA P C, RAMESH M N, THARANATHAN R N.Effect of plasticizers and fatty acids on mechanical and permeability characteristics of chitosan films[J].Food Hydrocolloids, 2007, 21(7):1 113-1 122.
[14] TIAN X Z, YAN D D, LU Q, et al.Cationic surface modification of nanocrystalline cellulose as reinforcements for preparation of the chitosan-based nanocomposite films[J].Cellulose, 2017, 24(1):163-174.
[15] 殷好勇, 金振声, 张顺利, 等.在玻璃的TiO2涂膜上有机物分子的吸附及光催化分解对水接触角的影响[J].感光科学与光化学, 2001, 19(2):81-87.
YIN H Y, JIN Z S, ZHANG S L, et al.Influence of adsorption and photocatalytic decomposition of organic compounds on water contact angle on TiO2 coated glass[J].Photographic Science and Photochemistry, 2001, 19(2):81-87.
[16] 程珊, 王稳航, 滕安国, 等.羧甲基纤维素强化胶原纤维膜的制备及其性能分析[J].食品科学, 2019, 40(3):194-201.
CHENG S, WANG W H, TENG A G, et al.Preparation and property analysis of carboxymethyl cellulose-reinforced collagen fiber film[J].Food Science, 2019, 40(3):194-201.
[17] 于淑池, 赖卓慧.金鲳鱼骨明胶的提取工艺及性质研究[J].食品研究与开发, 2020, 41(3):159-165.
YU S C, LAI Z H.Study on extraction technology and properties of gelatin from golden pompano bones[J].Food Research and Development, 2020, 41(3):159-165.
[18] 李列琴, 陈雪峰, 刘宁, 等.苹果渣氧化纤维素的制备及表征[J].食品与发酵工业, 2018, 44(2):129-134.
LI L Q, CHEN X F, LIU N, et al.Preparation and characterization of apple pomace oxidized cellulose[J].Food and Fermentation Industries, 2018, 44(2):129-134.
[19] 郑学晶, 李俊伟, 刘捷, 等.双醛淀粉改性明胶膜的制备与性能研究[J].中国皮革, 2011, 40(23):28-31;36.
ZHENG X J, LI J W, LIU J, et al.Preparation and properties of dialdehyde starch modified gelatin films[J].China Leather, 2011, 40(23):28-31;36.
[20] 吴立军. 有机化合物波谱解析[M].3版.北京:中国医药科技出版社, 2009.
WU L J.Spectral Analysis of Organic Compounds[M].3 rd ed.Beijing:China Medical Science Press, 2009.
[21] 包俊青, 唐亚丽, 卢立新, 等.肉桂醛对明胶基肠衣膜的性能影响[J].食品科学, 2019, 40(14):1-6.
BAO J Q, TANG Y L, LU L X, et al.Effect of cinnamaldehyde on the performance of gelatin-based edible casing[J].Food Science, 2019, 40(14):1-6.
[22] 杨斯乔, 李海朝.甲壳素-明胶复合膜性能研究[J].食品研究与开发, 2019, 40(18):44-51.
YANG S Q, LI H C.Properties of chitin-gelatin composite membrane[J].Food Research and Development, 2019, 40(18):44-51.
[23] 曹蓓, 靳杜娟, 李亦然.羟丙基纤维素/明胶复合膜的制备及性能表征[J].塑料科技, 2020,48(2):42-46.
CAO B, JIN D J, LI Y R.Preparation and performance characterization of hydroxypropyl cellulose/gelatin composite films[J].Plastics Science and Technology, 2020,48(2):42-46.
[24] BABIN H, DICKINSON E.Influence of transglutaminase treatment on the thermoreversible gelation of gelatin[J].Food Hydrocolloids, 2001, 15(3):271-276.
[25] 裴莹, 徐高强, 李玉辉, 等.纳米纤维素晶须/明胶复合膜的制备与结构及性能[J].高分子材料科学与工程, 2017, 33(8):45-49.
PEI Y, XU G Q, LI Y H, et al.Fabrication, structure and properties of cellulose nanowhiskers/gelatin composite film[J].Polymer Materials Science & Engineering, 2017, 33(8):45-49.
[26] 张金丽, 陈子和, 陈燕婷, 等.Ag NPs改性鱼鳞明胶-琼脂复合膜的制备及性能[J].精细化工, 2020, 37(12):2 496-2 503;2 509.
ZHANG J L, CHEN Z H, CHEN Y T, et al.Preparation and properties of nanoparticles modified fish scale gelatin-agar composite films silver[J].Fine Chemicals, 2020, 37(12):2 496-2 503;2 509.
[27] 刘幸幸. 壳聚糖/植物蛋白复合包装膜的制备与性能研究[D].杭州:浙江理工大学, 2012.
LIU X X.Preparation and study of chitosan/plant protein composite packageing film[D].Hangzhou:Zhejiang Sci-Tech University, 2012.
[28] ![]() A, SIONKOWSKA A.The effect of UV radiation on the values of thermal parameters of collagen containing β-carotene[J].Polymer Degradation and Stability, 1999, 65(1):87-90.
A, SIONKOWSKA A.The effect of UV radiation on the values of thermal parameters of collagen containing β-carotene[J].Polymer Degradation and Stability, 1999, 65(1):87-90.
[29] 林凤采, 汪雪琴, 杨旋, 等.一步法制备双醛基微纤化纤维素及其明胶复合膜[J].化工进展, 2018, 37(4):1 522-1 528.
LIN F C, WANG X Q, YANG X, et al.One-step synthesis of dialdehyde microfibrillated cellulose and its composite film with gelatin[J].Chemical Industry and Engineering Progress, 2018, 37(4):1 522-1 528.