人参(Panax ginseng C.A.Mey.)是一种来自五加科(Araliaceae)人参属的多年生草本植物[1],至今已有两千年的药用历史。根据现代研究表明,人参具有免疫调节、抗肿瘤、抗衰老等药理作用,可用于心脑血管系统、免疫系统及神经系统等疾病的治疗,同时能够改善记忆力,降疲劳,有益于人体健康[2-7]。目前,人参作为一种极具药用价值的名贵中药材,已成为全球最畅销的中草药产品之一,越来越广泛的应用于各种食品、保健品和药品中。其中,人参皂苷作为人参的主要生物活性成分,到目前为止,已经从中鉴定出超过150种人参皂苷,包括Rh1,Rs1,Rh2,Rk2,Rf,Rg3等[8]。由于其存在复杂结构及较长合成路径的难题,人工合成人参皂苷非常困难[9-10]。基于此,如何提高人参种质品质以及促进人参皂苷成分的体外生物合成等成为科研工作者研究的热点问题,而转录组学研究方法可以为人参皂苷生物合成提供大量的候选基因,并为后期的研究奠定基础。
20世纪90年代,各种组学技术日新月异,作为生物信息学的前沿研究手段,转录组学是发展最早,应用最广泛的技术之一[11],在一定程度上对基因的研究模式产生了影响,将基因组学带入了一个新的高速发展时期。近年来,随着技术的飞速发展和不断更新,转录组研究取得了巨大进步,尤其是在研究特定组织或特定生理条件下表达的基因信息,采用转录组测序技术可以高效、简便、快速的进行获取,对于人参药用植物研究中发现功能基因、分析代谢途径以及阐明调控机理具有重要意义[12]。基于此,本文通过文献的查阅和整理,对转录组学研究方法、新技术及在挖掘人参皂苷生物合成途径相关基因应用上的研究进展进行综述,以期为人参的深入研究提供有价值的参考。
1 转录组学研究方法
转录组这一概念是在1995年VELCULESCU等[13]对酵母菌基因表达进行研究时首次提出的。转录组狭义上通常是指细胞中所有参与蛋白质翻译的信使RNA(messenger RNA,mRNA)[14]。转录组学以样品中的全部转录本为研究对象,从群体水平上研究功能基因的表达水平及转录调控规律。已经在生物前沿研究,如动植物基础研究、微生物、临床诊断和中药产品研发等领域得到了越来越广泛的应用[15-18]。目前,转录组学研究技术主要分为两大类,一类是以杂交方法为基础的微阵列技术,另一类是以测序为基础的转录组测序技术,两种技术在人参皂苷合成代谢的研究中都有应用。
1.1 微阵列基因芯片技术
微阵列基因芯片技术最早是在1991年由FODORS等首次提出,是当时影响最深远的重大科技进展之一[19]。该技术是将核酸片段作为分子探针,使其固定于载玻片等载体支持物上,与荧光标记的样品进行杂交,通过杂交信号强弱,获得样品相关的生物信息[20]。但是,该技术在应用过程中仍然存在许多不足,如基因芯片技术存在假阳性,特异性低,检测系统灵敏度低,样品制备繁琐,使用成本较高等,限制了其应用的普及。
1.2 转录组测序技术
1.2.1 表达序列标签技术、基因表达序列分析技术及大规模平行测序技术
目前转录组测序技术是人参转录组学分析研究的重要手段,根据其技术发展水平可分为三阶段,即第一代测序技术、第二代测序技术和第三代测序技术[21]。最开始发展起来的表达序列标签技术、基因表达序列分析技术和大规模平行测序技术都为转录组学研究中的第一代测序技术,主要以Sanger测序方法为基础,从整体水平研究动植物组织中生物表达信息,其基本原理是将mRNA反转录的互补DNA (complementary DNA,cDNA)两端的一段序列作为序列标签来反映基因的表达水平[22]。最初,研究人员使用Sanger方法对转录组进行测序,并通过序列分析比对来研究参与人参皂苷生物合成途径的基因[23]。但是,这些传统的测序方法由于成本高、耗时长,测序通量低等缺点已不是人参转录组测序的最佳分析方法[24-25]。
1.2.2 RNA-Seq技术
转录组学的第二代测序技术,即RNA-Seq技术可以直接对没有基因信息物种的转录组进行分析,更深入的获得几乎所有转录本信息[26],弥补了非模式植物转录组研究中缺乏基因组信息的不足,基于转录组研究可以进行基因组映射,有助于研究基因的表达情况。该技术具有更高的检测通量,更高的分辨率、灵敏度,以及更广的检测范围等优势,也是目前深入研究人参转录组应用最广的转录组测序方法[27]。RNA-seq测序的平台主要包括Roche公司的焦磷酸测序平台、Illumina公司的Illumina/Solexa平台和Applied Biosystems公司的SOLID平台[28-29]。这3种测序平台中的Illumina/Solexa平台展现出显著优势,具有所需样品量少、测序通量大、准确率高、测序费用低的优点。它的不足,如序列有效读长较短、运行时间较长也在逐步改善,成为当前人参转录组研究的首选测序平台。随着第二代测序技术的应用,在解析人参皂苷合成途径、代谢网络和基因间相互作用方面不断取得新进展。
1.3 纳米孔单分子测序技术和单分子实时测序
与第一、二代测序技术相比,第三代纳米孔单分子测序技术和单分子实时测序能对全长转录组进行研究,在新转录本发现上具有明显优势,其具有无需PCR扩增、测序通量高、超长读长和所需样品量少等优点[30-31]。但是,由于第三代测序技术存在测序信号弱的缺点,易导致碱基识别过程中产生随机错误,增加了测序成本等难题,目前仍处于优化阶段[32-33]。
2 转录组学的前沿新技术
2.1 单细胞转录组测序技术
随着第一、第二、第三代测序技术的不断更替和发展,目前,转录组测序已经不限制于组织和器官样本的研究,单细胞转录组测序(single-cell RNA sequencing,scRNA-Seq)技术的出现,实现了对单细胞样本的分析,可以通过从单个细胞中提取转录组数据来分析基因表达异质性。这使我们能够对每个细胞进行区分和表征,揭示细胞动态过程,从而识别稀有细胞群,是转录组研究的技术性突破。单细胞转录组测序技术是由TANG等在2009年对小鼠的单个卵裂球细胞进行转录组研究时首次创立并应用[34],研究中scRNA-Seq技术可以大幅度提升基因检测通量,为扩大细胞数量和兼容实现高通量RNA测序开辟了一条新途径。此后,单细胞RNA测序技术不断得到改良和开发,在过去十年中,单细胞转录组测序技术在样本收集、单细胞捕获、条形码反转录、cDNA扩增、文库制备、测序和生物信息学分析方面不断取得新进展,测序成本大大降低,有效信息量获取逐渐增加,实验效率显著增强,已成为转录组学研究的强大工具[35-38]。单细胞RNA-seq技术在小鼠和人类的单细胞研究中正处于快速发展阶段,先后应用于胚胎早期发育、组织器官发育、免疫学及肿瘤疾病等领域[39-42]。然而,对植物的单细胞分析仍处在初始阶段,目前见于拟南芥、玉米、水稻、杨树、番茄和花生等模式植物、农产品或经济作物的研究中。主要通过高分辨率单细胞转录图谱,发现细胞异质性,用于鉴定植物细胞类型,解析细胞发育轨迹,挖掘参与植物发育的候选基因等[43-44]。预期未来在人参等药用植物活性成分的生物合成机理解析方面具有较大的应用空间。
2.2 空间转录组技术
在2020年,空间转录组技术被Nature杂志推选为年度最有价值的新技术,无一不证明空间转录组技术应用的重要性。空间转录组技术是将组织学成像和RNA测序相结合,以同时定量和定位细胞的基因表达,可视化识别组织区域中RNA分子的图谱[45],主要包括显微切割技术、原位捕获技术、原位杂交技术和原位测序技术。随着这些技术的不断发展和完善,检测的通量、转录本数目和空间分辨率等不断提高,空间转录组技术已成为一种实现新型生物学分析的手段[46-47]。相较于在哺乳动物组织应用中的不断发展,空间转录组在植物上的研究并不多见,由于植物组织切片中细胞壁、叶绿体和液泡等细胞结构的存在,使转录分析复杂化,为空间转录组研究带来挑战[48]。该技术在植物中应用是通过获得高分辨率的位置信息,解析植物细胞类型特异性基因表达情况,阐述细胞的独特空间发育轨迹,可用于实现作物的改良[49]。目前,空间转录组技术在挖掘人参皂苷生物合成基因的应用研究还未见相关报道。由于植物细胞壁结构的存在,使大量细胞从组织中分离出来难度较高,但若能突破细胞解离困难的限制,将这两种前沿新技术在人参转录组研究中进行应用,有望获取大量细胞异质性信息及空间位置信息,解析人参组织在特定空间位置中各类细胞的分化轨迹和功能基因的特异性表达,将会为揭示人参次级代谢物的生物合成途径提供新蓝图。
3 人参皂苷生物合成的相关基因
如何获取大量人参植物的主要活性成分人参皂苷已成为科研工作者研究的热点。转录组测序技术的出现,为大规模生产人参皂苷成分,揭示人参皂苷生物合成途径提供了重要的基因资源。同时,随着转录组学技术的发展,转录组学同其他组学(如代谢组学、蛋白质组学和基因组学等)的多组学联用技术在人参植物研究领域中也得到了广泛应用,通过多组学的整合分析,实现对人参功能分子表达模式精确量化,多视角阐述人参次级代谢物多样性合成的复杂分子机制,为筛选影响人参次级代谢物合成的相关基因提供了有利手段和新思路。目前,已有许多科研工作者研究人参皂苷生物合成途径的相关文献,对其合成路径也有了大体的推断,见图1。其生物合成过程中大约有20余步连续的酶促反应,但是只有少数参与该过程的酶基因被克隆,如角鲨烯环氧化物酶(squalene epoxidase,SE)[50]、达玛烯二醇-Ⅱ合酶(dammarenediol-Ⅱ synthase,DS)[51],β-淀粉样蛋白合酶(beta-amyrin synthase,β-AS)[52]、UDP-葡萄糖基转移酶(UDP-glycosyltransferase,UGT)[53]和细胞色素P450(cytochrome P450s,CYPs)[54]等。因此,应用转录组学技术或联合其他组学技术挖掘参与人参中次级代谢物合成途径涉及的相关基因,对提高人参药材品质及人参皂苷产量具有深远意义。
3.1 参与第一阶段合成反应的基因
据研究,人参皂苷的生物合成过程需要通过3个阶段。第一阶段是基于自身的甲羟戊酸(mevalonate,MVA)途径和甲基赤藓醇磷酸(methyl erythritol phosphate,MEP)途径代谢产生异戊烯基二磷酸(isopentenyl pyrophosphate,IPP)和二甲丙烯二磷酸(dimethylallyl pyrophosphate,DMAPP),是人参皂苷前体物质的合成阶段[55-56]。3-羟基-3-甲基戊二酸单酰辅酶A还原酶(3-hydroxy-3-methyl glutaryl coenzyme A reductase,HMGR)作为上游的关键限速酶,是MVA通路中的调节靶点,HMGR表达上调可以影响人参中人参皂苷的合成效率,在人参皂苷生物合成的第一阶段发挥重要的作用[57]。XUE等[58]采用第二代测序技术,对人参不同部位样品进行了测序分析,研究发现,有380个参与人参皂苷生物合成以及编码MEP途径和MVA途径酶的基因,通过基因表达谱分析,2-C-甲基-D-赤藓糖醇4-磷酸胞苷酰转移酶 (2-C-methyl-D-erythritol 4-phosphate cytidylyl transferase,IspD)可能是MEP途径合成人参皂苷的关键酶。并首次揭示MEP途径的基因转录丰度与人参根中MVA途径的基因转录丰度相似,这是第一次根据人参样品的转录组数据鉴定整个途径中的所有基因,为人参皂苷代谢途径研究提供了新的生物信息。此外,ZHANG等[59]采用代谢组学及转录组学联用技术,分别对人参各部位的人参皂苷含量进行测定,对人参周皮、皮部、中柱组织进行测序研究,组装了182 881个独立基因,通过加权基因共表达网络分析(weighted correlation network analysis,WGCNA)发现其中有21 178个独立基因与人参皂苷的含量呈正相关,MVA通路中的大多数转录本在3个组织中均有不同程度的表达。与萜类合成相关的HMGR,磷酸甲羟戊酸激酶(phosphomevalonate kinase,PMK),异戊烯二磷酸δ异构酶(isopentenyl-diphosphate delta-isomerase,IDI)在人参周皮中的表达量明显高于人参皮部和中柱的表达量,该表达谱的异同有助于提高对人参皂苷在不同组织中合成、积累和运输调控网络的理解。
3.2 参与第二阶段合成反应的基因
第二阶段为三萜骨架生物合成阶段,包括人参皂苷C骨架延长和母核苷元形成。首先IPP和DMAPP在法尼基焦磷酸合酶(farnesyl diphosphate synthase,FPS)作用下,发生缩合反应生成法尼基焦磷酸(farnesyl diphosphate,FPP),之后FPP在法尼基焦磷酸合成酶(squalene synthase,SS)催化下生成鲨烯,在此过程将母核苷元C骨架分别延长至15碳和30碳,其中FPS和SS是鲨烯结构合成中发挥重要作用酶基因[60]。之后鲨烯在SE作用下合成2,3-氧化鲨烯,在此基础上,母核苷元骨架环化过程中的关键酶基因DS和β-AS的催化反应直接影响人参皂苷苷元的类型和最终结构,分别形成为达玛烷型人参皂苷的四环骨架及齐墩果烷型人参皂苷。刘璐[61]在课题研究中,对人参代谢表达谱进行了分析,基于基因的差异性表达,从单基因数据集中鉴定出15个FPS,16个SE,9个β-As和85个UGTs,确定了相关候选基因。结果表明,多种关键基因的表达影响着人参皂苷的代谢途径,对于促进多种单体人参皂苷的生物合成具有重要意义。YIN等[62]首次将不同年龄段人参的人参皂苷生物合成途径中关键基因酶活性变化,基因表达与人参皂苷含量之间的关系进行了研究。结果发现,在2~4年参龄的人参中DS基因表达迅速增加,在4~6年基因表达保持稳定,并且DS酶活性与人参皂苷含量显著相关。为我们提出了一种通过鉴定人参皂苷合成途径中相关基因表达,酶活性与人参皂苷含量相关分析方法来识别人参根年龄的潜在新策略。另有相关研究通过采用“基因-皂苷含量”、“基因-基因”关联分析的方法,以达到获得参与人参皂苷生物合成候选基因的目的。王康宇等[63]基于人参转录组数据,对人参的候选基因PgDof表达量与单体皂苷和总皂苷含量及人参皂苷生物合成关键酶基因进行相关分析,获得了与关键酶基因,如SE2_4、FPS_22、CYP716A53v2_1、DS_1、β-AS_6等互作显著,得到了影响人参皂苷生物合成的重要候选基因PgDof-14-1,为挖掘候选基因提供了新思路。

a-MVA途径、MEP途径、三萜骨架生物合成及母核苷元的后修饰过程;b-部分三萜皂苷的生物合成途径
图1 人参皂苷生物合成途径及相关酶
Fig.1 Ginsenoside biosynthesis pathway and related enzymes
注:虚线箭头为省略途径;?为暂未阐明的酶;Glc:β-D-glucopyranosyl
3.3 参与第三阶段合成反应的基因
第三阶段是人参皂苷合成母核苷元的后修饰阶段,细胞色素P450和糖基转移酶(glyeosyltransferase,GT)已被证明在人参皂苷生物合成的最后步骤中起重要作用。在细胞色素P450和GT作用下,达玛烯二醇发生羟基化和糖基化,在相应母核苷元C-3位、C-6位和C-20位进行修饰,可生成不同类型人参皂苷,这个过程的反应会对人参皂苷的生物学性质和功能产生影响。ZHAO等[64]利用转录组测序技术鉴定出100个PgCYP基因,经突变关联分析发现,有6个PgCYP基因与人参皂苷生物合成显著相关,确定为人参皂苷生物合成的候选基因,此发现为人参育种和人参皂苷生物合成研究提供了一套PgCYP基因SNP/InDel标记。在合成途径中,细胞色素P450的表达情况也使不同活性成分皂苷在不同组织中具有不同含量。WEI等[65]综合化学和转录组学对人参不同组织皂苷含量和关键酶基因进行分析,研究发现,地下组织中人参皂苷Re、Rb2、Rc、Rg1、Rd、R1、和Rb1的含量高于地上组织。地下和地上组织中分别有482个和882个独立基因,经鉴定有75种不同表达的CYPs转录本。采用实时荧光定量(real time quantitative PCR,RT-qPCR)验证分析,CYP716A47表达与地上组织人参皂苷Rc和Rb2的含量显著相关。CYP716A47基因在地上组织中表达丰富,特别是在花中,其表达量比根部高31.5倍。CYP716A53v2基因主要与地下组织中人参皂苷Rd、Rb1、R1,Rg1和Re含量相关表达。这些研究为进一步研究人参皂苷合成、运输和积累的机制提供了关键基因。
相较于参与第一、二阶段合成反应中研究较为清晰的酶类,对人参皂苷糖基转移酶的了解较少。糖基转移酶是介导最终PPD型和PPT型皂苷生物合成中糖基化过程的酶,特定的基因家族UGT的表达情况丰富了皂苷的多样性,然而,只有少数UGT因其底物特异性而被表征,并且许多在次级代谢物合成途径中起关键作用的UGTs尚未被鉴定出来,这阻碍了皂苷多样性的合成。KANG等[66]对茉莉酸甲酯(methyl jasmonate,MeJA)处理的不同时间段的人参不定根的UGT相关基因表达进行转录组研究,确定了11个候选UGT基因,包括8个新的UGT基因(Pg_S4174.10、Pg_S2390.5、Pg_S6708.3、Pg_S0804.16、Pg_S5977.4、Pg_S5521.1、Pg_S0245.36、Pg_S2351.7)和3个先前研究表征过的UGT基因(Pg_S4493.1,Pg_S4157.4和Pg_S4174.7)。同时,联合代谢组学分析人参皂苷含量的时间依赖性变化,发现经MeJA处理引发了丙二酰化人参皂苷Rb1、Rb2、Rb3、Rc、Rd和七叶胆苷XVⅡ含量的增加,通过代谢分析和系统发育分析显示,这些候选UGT基因与人参皂苷生物合成密切相关,有助于人参皂苷的糖基化。KHOROLRAGCHAA等[67]使用焦磷酸测序法从人参EST数据库中筛选了12种可能参与三萜类化合物合成的UDP-糖基转移酶,评估UGT(PgUGT)基因在4年生人参(花蕾,叶子,茎和根)组织中以及加茉莉酸酯衍生物处理的不定根的特异性表达。结果表明,与花蕾和茎相比,叶和根组织中大多数PgUGT显示出较高的转录水平,与人参叶和根含有大量的次级代谢物相关。茉莉酸酯衍生物处理的人参不定根转录组测序结果发现,PgUGTs转录水平较未处理的对照组相比显著提高,其中,PgUGT1基因和PgUGT2基因对茉莉酸酯衍生物特别敏感。LI等[68]利用454焦磷酸测序技术研究了人参的根茎叶花组织的转录谱,发现105 522个人参独立基因,其中223个独立基因参与人参皂苷骨架的合成。根据注释结果预测了可能参与到人参皂苷合成途径的326个潜在的细胞色素P450和129个潜在的UDP糖基转移酶序列,这些基因的发现将有助于人参皂苷生物合成的分子机制研究。KIM等[69]通过转录组测序技术对MeJA诱导人参毛状根培养物的转录谱进行研究,筛选出与人参皂苷生物合成相关的差异表达UGTs基因PG07029G02、PG07020C06和PG07025D04等。通过鉴定最终确定实现人参皂苷Rh2到Rg3转化的UGRh2GT基因。此外,WANG等[70]基于转录组研究,采用基因表达和性状关联分析方法,筛选出7个与人参皂苷Rg3生物合成相关的基因,这些基因在MeJA诱导下的表达序列为FPS→UGT71A27_2,CYP339→PgRb3S03→PgRb3S10→PgRb3S01,该序列可能代表了Rb3合成和转运的物质代谢过程,为人参皂苷Rb3的合成机理研究提供了理论依据。
4 展望
随着测序技术的不断完善,转录组学技术成为获得人参大规模基因资源的热点研究技术,已在参与不同阶段人参皂苷生物合成反应过程中基因的发现上取得了一定成就。但是,现阶段的这些研究成果仅限于对选定的人参组织进行整体转录组测序,获得的是细胞群体中单个基因的平均表达水平,未能从单细胞水平对其进行深层次了解。随着新技术的发展,单细胞转录组和空间转录组技术在动植物的研究中取得了成功的经验,若将这些前沿技术整合应用于人参植物的研究,有望在单细胞层面上获得基因在空间位置中的差异表达信息,发现细胞间的异质性,了解不同类型细胞功能、细胞谱系发育轨迹,挖掘参与人参皂苷生物合成途径的相关基因。同时,多组学联用是获得药用植物综合全面生物学信息的有效途径,将前沿转录组学技术同蛋白质组学和代谢组学技术联用,从多角度对人参生物学信息进行分析,通过转录组学的前沿技术掌握人参植物的细胞空间位置及基因表达信息,明确参与人参皂苷生物合成途径相关基因的差异表达情况,再联合应用蛋白质组学和代谢组学的相关技术,从蛋白质组学水平研究人参代谢物和人参皂苷生物合成相关基因翻译调控关系,从代谢组学水平分析人参中人参皂苷成分变化。最终确定人参皂苷合成途径及关联酶,探究参与人参中人参皂苷生物合成路径的调控位点,揭示人参皂苷合成机制,为大规模提高人参皂苷产量与活性提供一个新的方向。
[1] 国家药典委员会.中华人民共和国药典:一部[M].北京:中国医药科技出版社,2020:8.
Chinese Pharmacopoeia Commission.Pharmacopoeia of the People's Republic of China:Volume I [M].Beijing:China Pharmaceutical Science and Technology Press,2020:8.
[2] ZHOU P,XIE W J,HE S B,et al.Ginsenoside Rb1 as an anti-diabetic agent and its underlying mechanism analysis[J].Cells,2019,8(3):204.
[3] FAN W X,HUANG Y L,ZHENG H,et al.Ginsenosides for the treatment of metabolic syndrome and cardiovascular diseases:Pharmacology and mechanisms[J].Biomedicine &Pharmacotherapy,2020,132:110915.
[4] YANG Y J,LI S S,HUANG H,et al.Comparison of the protective effects of ginsenosides Rb1 and Rg1 on improving cognitive deficits in SAMP8 mice based on anti-neuroinflammation mechanism[J].Frontiers in Pharmacology,2020,11:834.
[5] LEUNG K W,WONG A S T.Pharmacology of ginsenosides:A literature review[J].Chinese Medicine,2010,5:20..
[6] KIM S K,PARK J H.Trends in ginseng research in 2010[J].Journal of Ginseng Research,2011,35(4):389-398.
[7] 张春枝,安利佳,金凤燮.人参皂苷生理活性的研究进展[J].食品与发酵工业,2002,28(4):70-74.
ZHANG C Z,AN L J,JIN F X.Progress on the research of physiological function of ginsenosides[J].Food and Fermentation Industries,2002,28(4):70-74.
[8] TIAN M L,LI L N,ZHENG R R,et al.Advances on hormone-like activity of panax ginseng and ginsenosides[J].Chinese Journal of Natural Medicines,2020,18(7):526-535.
[9] 李晓军,张万斌,高栓虎.复杂天然产物全合成:化学合成与生物合成结合的策略[J].有机化学,2018,38(9):2 185-2 198.
LI X J,ZHANG W B,GAO S H,et al.Total synthesis of complex natural products:Combination of chemical synthesis and biosynthesis strategies[J].Chinese Journal of Organic Chemistry,2018,38(9):2 185-2 198.
[10] 张涛,王冠,张维维,等.温度调控对人参皂苷积累及其关键酶基因表达的影响[J].中草药,2020,51(19):5 035-5 040.
ZHANG T,WANG G,ZHANG W W,et al.Effects of temperature regulation on ginsenoside accumulation and gene expression of key enzymes[J].Chinese Traditional and Herbal Drugs,2020,51(19):5 035-5 040.
[11] LOCKHART D J,WINZELER E A.Genomics,gene expression and DNA arrays [J].Nature,2000,405(6 788):827-836.
[12] 李小白,向林,罗洁,等.转录组测序(RNA-seq)策略及其数据在分子标记开发上的应用[J].中国细胞生物学学报,2013,35(5):720-726;740.
LI X B,XIANG L,LUO J,et al.The strategy of RNA-seq,application and development of molecular marker derived from RNA-seq[J].Chinese Journal of Cell Biology,2013,35(5):720-726;740.
[13] VELCULESCU V E,ZHANG L,ZHOU W,et al.Characterization of the yeast transcriptome[J].Cell,1997,88(2):243-251.
[14] COSTA V,ANGELINI C,DE FEIS I,et al.Uncovering the complexity of transcriptomes with RNA-Seq [J].Journal of Biomedicine and Biotechnology,2010,2010:853916.
[15] 陈易欣,罗群.转录组学技术在急性肾损伤中的应用进展[J].生命的化学,2021,41(10):2 228-2 233.
CHEN Y X,LUO Q.Application progress of transcriptomics technology in acute kidney injury[J].Chemistry of Life,2021,41(10):2 228-2 233.
[16] 赵乐,孟祥晨.转录组测序技术在植物乳杆菌细菌素合成研究中的应用研究进展[J].乳业科学与技术,2021,44(5):32-37.
ZHAO L,MENG X C.A review of the application of transcriptome sequencing in research on bacteriocin synthesis by Lactobacillus plantarum[J].Journal of Dairy Science and Technology,2021,44(5):32-37.
[17] 肖宇辰,吉日木图,伊丽,等.转录组学在骆驼科动物中的应用研究进展[J].家畜生态学报,2019,40(6):1-6.
XIAO Y C,JIRIMUTU,YI L,et al.Research progress on the application of transcriptomics in the Camelidae[J].Journal of Domestic Animal Ecology,2019,40(6):1-6.
[18] S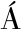 NCHEZ-VIDA
NCHEZ-VIDA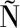 A D I,RAJWANI R,WONG M S.The use of omic technologies applied to traditional Chinese medicine research[J].Evidence-Based Complementary and Alternative Medicine,2017,2017:6359730.
A D I,RAJWANI R,WONG M S.The use of omic technologies applied to traditional Chinese medicine research[J].Evidence-Based Complementary and Alternative Medicine,2017,2017:6359730.
[19] SCHENA M,SHALON D,DAVIS R W,et al.Quantitative monitoring of gene expression patterns with a complementary DNA microarray[J].Science,1995,270(5235):467-470.
[20] 赵圣明,赵岩岩,马汉军,等.转录组学在抑菌机制中的应用研究进展[J].食品与发酵工业,2017,43(7):264-269.
ZHAO S M,ZHAO Y Y,MA H J,et al.Applications of transcriptomics in research of antimicrobial mechanism[J].Food and Fermentation Industries,2017,43(7):259-264.
[21] 李玉梅,李书娴,李向上,等.第三代测序技术在转录组学研究中的应用[J].生命科学仪器,2018,16(S1):114-121;113.
LI Y M,LI S X,LI X S,et al.Transcriptome studies with the third-generation sequencing technology[J].Life Science Instruments,2018,16(S1):114-121;113.
[22] SANGER F,NICKLEN S,COULSON A R.DNA sequencing with chain-terminating inhibitors[J].Proceedings of the National Academy of Sciences,1977,74(12):5 463-5 467.
[23] 张振乾,谭太龙,肖钢,等.基因表达系列分析法(SAGE)的改进及其在植物功能基因组研究中的应用[J].基因组学与应用生物学,2009,28(6):1 204-1 210.
ZHANG Z Q,TAN T L,XIAO G,et al.The modification of serial analysis of gene expression (SAGE) and its application in plant functional genome research[J].Genomics and Applied Biology,2009,28(6):1 204-1 210.
[24] 陈杰.大规模平行测序技术(MPSS)研究进展[J].生物化学与生物物理进展,2004,31(8):761-765.
CHEN J.A novel gene identification approach:Massively parallel signature sequencing[J].Progress in Biochemistry and Biophysics,2004,31(8):761-765.
[25] 刘厚伯,上官艳妮,潘胤池,等.RNA-Seq在药用植物研究中的应用[J].中草药,2019,50(21):5 346-5 354.
LIU H B,SHANGGUAN Y N,PAN Y C,et al.Applications of RNA-Seq technology on medicinal plants[J].Chinese Traditional and Herbal Drugs,2019,50(21):5 346-5 354.
[26] MELÉ M,FERREIRA P G,REVERTER F,et al.The human transcriptome across tissues and individuals[J].Science,2015,348(6 235):660-665.
[27] 刘伟,郭光艳,秘彩莉.转录组学主要研究技术及其应用概述[J].生物学教学,2019,44(10):2-5.
LIU W,GUO G Y,BEI C L.A summary of the main research techniques of transcriptology and their applications[J].Biology Teaching,2019,44(10):2-5.
[28] SHENDURE J,JI H.Next-generation DNA sequencing[J].Nature Biotechnology,2008,26(10):1 135-1 145.
[29] BRANTON D,DEAMER D W,MARZIALI A,et al.The potential and challenges of nanopore sequencing[J].Nature Biotechnology,2008,26(10):1 146-1 153.
[30] VAN DIJK E L,JASZCZYSZYN Y,NAQUIN D,et al.The third revolution in sequencing technology[J].Trends in Genetics:TIG,2018,34(9):666-681.
[31] 卢鹏,金静静,李泽锋,等.基于第三代测序技术的基因组组装方法及其在烟草中的应用 [J].烟草科技,2018,51(2):87-94.
LU P,JIN J J,LI Z F,et al.Genome assembly based on the third-generation sequencing technology and its application in tobacco [J].Tobacco Science &Technology,2018,51(2):87-94.
[32] RHOADS A,AU K F.PacBio sequencing and its applications[J].Genomics,Proteomics &Bioinformatics,2015,13(5):278-289.
[33] TANG F C,BARBACIORU C,WANG Y Z,et al.mRNA-Seq whole-transcriptome analysis of a single cell[J].Nature Methods,2009,6(5):377-382.
[34] PICELLI S,BJÖRKLUND ![]() K,FARIDANI O R,et al.Smart-seq2 for sensitive full-length transcriptome profiling in single cells[J].Nature Methods,2013,10(11):1 096-1 098.
K,FARIDANI O R,et al.Smart-seq2 for sensitive full-length transcriptome profiling in single cells[J].Nature Methods,2013,10(11):1 096-1 098.
[35] KLEIN A M,MAZUTIS L,AKARTUNA I,et al.Droplet barcoding for single-cell transcriptomics applied to embryonic stem cells[J].Cell,2015,161(5):1 187-1 201.
[36] GIERAHN T M,WADSWORTH M H,HUGHES T K,et al.Seq-Well:Portable,low-cost RNA sequencing of single cells at high throughput[J].Nature Methods,2017,14(4):395-398.
[37] HAN X P,WANG R Y,ZHOU Y C,et al.Mapping the mouse cell atlas by microwell-seq[J].Cell,2018,172(5):1 091-1 107.e17.
[38] XUE Z G,HUANG K,CAI C C,et al.Genetic programs in human and mouse early embryos revealed by single-cell RNA sequencing[J].Nature,2013,500(7 464):593-597.
[39] TREUTLEIN B,BROWNFIELD D G,WU A R,et al.Reconstructing lineage hierarchies of the distal lung epithelium using single-cell RNA-seq[J].Nature,2014,509(7 500):371-375.
[40] BJÖRKLUND ![]() K,FORKEL M,PICELLI S,et al.The heterogeneity of human CD127+ innate lymphoid cells revealed by single-cell RNA sequencing[J].Nature Immunology,2016,17(4):451-460.
K,FORKEL M,PICELLI S,et al.The heterogeneity of human CD127+ innate lymphoid cells revealed by single-cell RNA sequencing[J].Nature Immunology,2016,17(4):451-460.
[41] VENTEICHER A S,TIROSH I,HEBERT C,et al.Decoupling genetics,lineages,and microenvironment in IDH-mutant gliomas by single-cell RNA-seq[J].Science,2017,355(6 332):eaai8478.
[42] CHEN Y,TONG S F,JIANG Y Z,et al.Transcriptional landscape of highly lignified poplar stems at single-cell resolution[J].Genome Biology,2021,22(1):319.
[43] WANG Y,HUAN Q,LI K,et al.Single-cell transcriptome atlas of the leaf and root of rice seedlings[J].Journal of Genetics and Genomics,2021,48(10):881-898.
[44] ZHANG L L,CHEN D S,SONG D L,et al.Clinical and translational values of spatial transcriptomics[J].Signal Transduction and Targeted Therapy,2022,7:111.
[45] ![]() P L,SALM
P L,SALM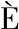 N F,VICKOVIC S,et al.Visualization and analysis of gene expression in tissue sections by spatial transcriptomics[J].Science,2016,353(6 294):78-82.
N F,VICKOVIC S,et al.Visualization and analysis of gene expression in tissue sections by spatial transcriptomics[J].Science,2016,353(6 294):78-82.
[46] 孙佳鑫,苏依拉·其木格,刘芳远等.空间转录组的发展与展望[J].生命的化学,2021,41(10):2 196-2 203.
SUN J X,SUYILA Q,LIU F Y,et al.The development and prospect of space transcriptomics[J].Chemistry of Life,2021,41(10):2 196-2 203.
[47] 危莹,张小丹,胡苗苗,等.空间转录组技术研究进展[J].生物化学与生物物理进展,2022,49(3):561-571.
WEI Y,ZHANG X D,HU M M,et al.Advances in spatial transcriptome technologies[J].Progress in Biochemistry and Biophysics,2022,49(3):561-571.
[48] COSGROVE D J.Growth of the plant cell wall[J].Nature Reviews Molecular Cell Biology,2005,6(11):850-861.
[49] MORENO-VILLENA J J,ZHOU H R,GILMAN I S,et al.Spatial resolution of an integrated C4+CAM photosynthetic metabolism[J].bioRxiv,2021.DOI:10.1101/2021.11.25.470062.
[50] HAN J Y,IN J G,KWON Y S,et al.Regulation of ginsenoside and phytosterol biosynthesis by RNA interferences of squalene epoxidase gene in Panax ginseng[J].Phytochemistry,2010,71(1):36-46.
[51] HAN J Y,KWON Y S,YANG D C,et al.Expression and RNA interference-induced silencing of the dammarenediol synthase gene in Panax ginseng[J].Plant and Cell Physiology,2006,47(12):1 653-1 662.
[52] KUSHIRO T,SHIBUYA M,EBIZUKA Y.β-amyrin synthase:Cloning of oxidosqualene cyclase that catalyzes the formation of the most popular triterpene among higher plants[J].European Journal of Biochemistry,1998,256(1):238-244.
[53] JUNG S C,KIM W,PARK S C,et al.Two ginseng UDP-glycosyltransferases synthesize ginsenoside Rg3 and rd[J].Plant and Cell Physiology,2014,55(12):2 177-2 188.
[54] HAN J Y,HWANG H S,CHOI S W,et al.Cytochrome P450 CYP716A53v2 catalyzes the formation of protopanaxatriol from protopanaxadiol during ginsenoside biosynthesis in Panax ginseng[J].Plant and Cell Physiology,2012,53(9):1 535-1 545.
[55] AUGUSTIN J M,KUZINA V,ANDERSEN S B,et al.Molecular activities,biosynthesis and evolution of triterpenoid saponins[J].Phytochemistry,2011,72(6):435-457.
[56] ZHAO Y J,LI C.Biosynthesis of plant triterpenoid saponins in microbial cell factories[J].Journal of Agricultural and Food Chemistry,2018,66(46):12 155-12 165.
[57] GU W,GENG C,XUE W D,et al.Characterization and function of the 3-hydroxy-3-methylglutaryl-CoA reductase gene in Alisma Orientale (Sam.) Juz.and its relationship with protostane triterpene production[J].Plant Physiology and Biochemistry:PPB,2015,97:378-389.
[58] XUE L,HE Z L,BI X C,et al.Transcriptomic profiling reveals MEP pathway contributing to ginsenoside biosynthesis in Panax ginseng[J].BMC Genomics,2019,20(1):383.
[59] ZHANG J J,SU H,ZHANG L,et al.Comprehensive characterization for ginsenosides biosynthesis in ginseng root by integration analysis of chemical and transcriptome[J].Molecules (Basel,Switzerland),2017,22(6):889.
[60] CA YENDO A,DE COSTA F,T DA COSTA C,et al.Biosynthesis of plant triterpenoid saponins:Genes,enzymes and their regulation[J].Mini-Reviews in Organic Chemistry,2014,11(3):292-306.
[61] 刘璐.多组学分析越南人参皂苷类成分的代谢差异及生物合成[D].昆明:云南中医药大学,2021.
LIU L.Study on metabolic differences and biosynthesis of ginsenosides from Vietnamese ginseng based on multi-omics analysis[D].Kunming:Yunnan University of Traditional Chinese Medicine,2021.
[62] YIN J X,ZHANG D H,ZHUANG J J,et al.Study on the correlation between gene expression and enzyme activity of seven key enzymes and ginsenoside content in ginseng in over time in Ji′an,China[J].International Journal of Molecular Sciences,2017,18(12):2682.
[63] 王康宇,郭彦秀,马翀,等.吉林人参Dof基因家族的鉴定及表达模式分析[J].中国中药杂志,2022,47(1):62-71.
WANG K Y,GUO Y X,MA C,et al.Transcriptome-wide identification and expression pattern analysis for Dof gene family in Panax ginseng from Jilin[J].China Journal of Chinese Materia Medica,2022,47(1):62-71.
[64] ZHAO M Z,LIN Y P,WANG Y F,et al.Transcriptome analysis identifies strong candidate genes for ginsenoside biosynthesis and reveals its underlying molecular mechanism in Panax ginseng C.A.Meyer[J].Scientific Reports,2019,9:615.
[65] WEI G F,WEI F G,YUAN C,et al.Integrated chemical and transcriptomic analysis reveals the distribution of protopanaxadiol-and protopanaxatriol-type saponins in Panax notoginseng[J].Molecules (Basel,Switzerland),2018,23(7):1773.
[66] KANG K B,JAYAKODI M,LEE Y S,et al.Identification of candidate UDP-glycosyltransferases involved in protopanaxadiol-type ginsenoside biosynthesis in Panax ginseng[J].Scientific reports,2018,8:11744.
[67] KHOROLRAGCHAA A,KIM Y J,RAHIMI S,et al.Grouping and characterization of putative glycosyltransferase genes from Panax ginseng Meyer[J].Gene,2014,536(1):186-192.
[68] LI C F,ZHU Y J,GUO X,et al.Transcriptome analysis reveals ginsenosides biosynthetic genes,microRNAs and simple sequence repeats in Panax ginseng C.A.Meyer[J].BMC Genomics,2013,14:245.
[69] KIM O,BANG K,KIM Y C,et al.Upregulation of ginsenoside and gene expression related to triterpene biosynthesis in ginseng hairy root cultures elicited by methyl jasmonate[J].Plant Cell,Tissue and Organ Culture (PCTOC),2009,98(1):25-33.
[70] WANG K Y,ZHANG Z X,LI S K,et al.Transcriptome-wide analysis for ginsenoside Rb3 synthesis-related genes and study on the expression of methyl jasmonate treatment in Panax ginseng[J].Life (Basel,Switzerland),2021,11(5):387.