大豆分离蛋白(soy protein isolate,SPI)聚集体结构无序,二硫键含量低[1],其制备的凝胶类产品难以产生富有弹性和韧性的口感质构。蛋清蛋白(egg albumin,EA)二硫键含量丰富,可作为SPI热致凝胶形成过程中游离巯基的供体[2]。本团队前期已经通过机械性能、持水力、微观形貌等指标对二者形成的复合凝胶进行了研究,分析了影响复合凝胶形成的几个内部因素。但不同外部条件的加入,可使复合体系二硫键的形成产生新变化[3],目前该类研究报道有限。基于多种手段可以影响蛋白质的物理化学特性和功能特性,因此探索不同的还原剂、离子强度、多糖、热处理等方式对每种蛋白质在最终网络中的贡献,进而揭示诱导凝胶二硫键形成的因素并阐明其对复合凝胶网络结构特性的影响具有一定意义。
本文基于以上思路,通过添加还原剂NaHSO3和Na2SO3、盐离子NaCl、多糖刺槐豆胶和结冷胶以及进行不同的热处理程序来摸索能够从外部影响大豆蛋白/蛋清蛋白(SPI+EA)复合凝胶性能的因素,分析不同条件下单一SPI体系和SPI+EA复合体系凝胶的状态,并用巯基含量的变化研究热处理对EA的影响,以进一步阐明蛋白质在不同加工条件下的聚集机制[4-5],从而为选择性混合SPI与EA的进一步实验提供思路和理论基础。
1 材料与方法
1.1 实验材料
EA,Sigma公司;低温脱脂大豆粕,山东御馨生物科技公司;NaCl、Na2SO3、NaHSO3、刺槐豆胶,上海源叶生物科技有限公司;结冷胶,郸城财鑫糖业有限责任公司;其他试剂皆为分析纯。
1.2 仪器与设备
CR22G高速冷冻离心机,日本Hitachi公司;Alpha-4冷冻干燥机,德国Christ公司;RW 20顶置式搅拌器,德国IKA公司;T25分散均质机,德国IKA公司;Zeiss EVO18台式扫描电子显微镜,德国Carl Zeiss;Genesys 10 s分光光度计,美国Therom Fisher公司;5943万能材料试验机,美国INSTRON公司。
1.3 实验方法
1.3.1 还原剂浓度及种类
配制质量分数15%的SPI+EA复合溶液[V(SPI)∶V(EA)=4∶1]10 mL于小烧杯,加入适量的去离子水和1 mol/L的NaHSO3、Na2SO3溶液使其最终浓度分别为1、5、10、50、100、200 mmol/L,SPI+EA复合溶液浓度为10%(质量分数)。测定成胶性、持水性(water-holding capacity,WHC)并观察微观结构[2]。
1.3.2 离子强度
配制质量分数15%的SPI+EA复合溶液[V(SPI)∶V(EA)=4∶1] 10 mL于小烧杯,加入适量的去离子水和2 mol/L NaCl溶液使其最终浓度分别为10、20、50、100、200、500 mmol/L,SPI+EA复合溶液浓度为10%(质量分数)。测定成胶性、持水性并观察微观结构[2]。
1.3.3 热处理程序
配制质量分数10%的SPI+EA复合溶液[V(SPI)∶V(EA)=4∶1],移取8 mL于10 mL小烧杯并调pH 5.5,置于95 ℃水浴5、10、15、30、45 min,冷却至室温观察和测定成胶性、持水性并观察微观结构[2]。
1.3.4 多糖种类
配制质量分数15%质量分数的SPI+EA复合溶液[V(SPI)∶V(EA)=4∶1] 10 mL于小烧杯,加入适量的去离子水和质量分数0.9%的刺槐豆胶、结冷胶溶液,使刺槐豆胶、结冷胶溶液最终质量分数分别为0.015%、0.03%、0.06%、0.15%、0.3%,SPI+EA复合溶液为10%(质量分数)。测定成胶性、持水性并观察微观结构[2]。
1.3.5 还原剂、盐离子及多糖复合体系
将1 mol/L NaHSO3溶液、2 mol/L NaCl溶液、质量分数为0.9%的结冷胶溶液及适量去离子水加入了质量分数15%的SPI+EA复合溶液[V(SPI)∶V(EA)=4∶1]中,使3种溶液体系中各自保持NaHSO3溶液1 mmol/L、NaCl溶液100 mmol/L和结冷胶溶液0.15%,考察复合影响。另设对照组质量分数质量分数10%纯SPI溶液和质量分数10% SPI+EA复合溶液。测定成胶性、持水性并观察微观结构[2]。
2 结果与分析
2.1 还原剂浓度及种类
加入不同浓度和种类还原剂加热后所形成的凝胶硬度、持水性和实物图见图1。试验条件下,加入NaHSO3溶液的凝胶硬度随着其加入浓度的增加,呈短暂升高后下降趋势,但加入了Na2SO3溶液的凝胶硬度随着其加入浓度的增加而逐渐下降,趋势明显,在同种浓度下,加入NaHSO3溶液的凝胶硬度比加入了Na2SO3溶液的凝胶硬度更高。同浓度的Na2SO3比NaHSO3对凝胶结构的破坏程度更大。该作用推断为还原剂具有能够减弱蛋白质分子内二硫键的形成、降低蛋白质凝胶性的作用, 进而降低蛋白质分子形成稳定的胶体网络结构, 使产品更易于分散有关[6]。加入NaHSO3或者Na2SO3的复合凝胶的持水性较高但无特定的趋势。在浓度相同时,加入NaHSO3比加入Na2SO3对体系持水性影响更具优势。试验条件范围内,凝胶的硬度与持水性无明显关系。加入不同浓度和种类还原剂的SPI+EA凝胶微观结构如图2所示。
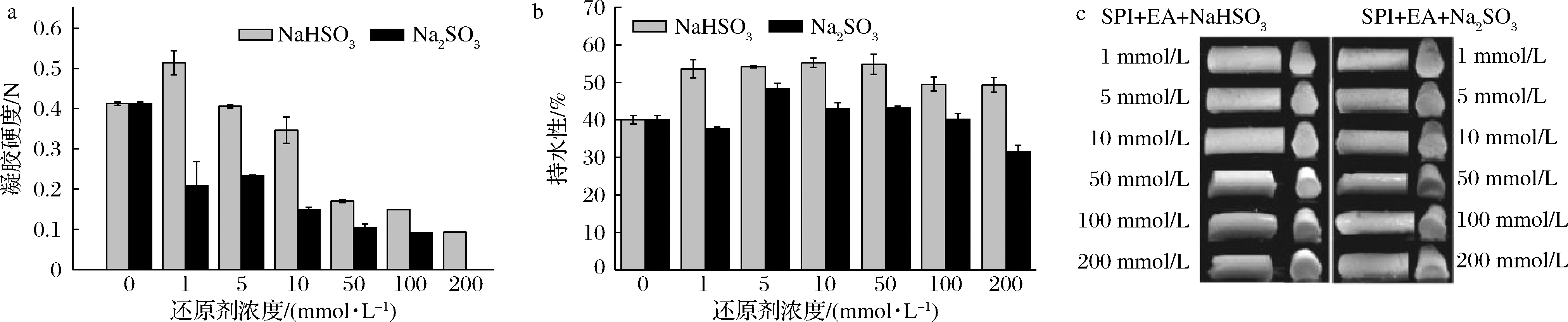
a-凝胶硬度;b-持水性;c-实物图
图1 加入不同浓度和种类还原剂的SPI+EA凝胶硬度和持水性
Fig.1 Hardness and water holding capacity of SPI+EA gels with different concentrations and kinds of reducing agents

a-1 mmol/L NaHSO3;b-1 mmol/L Na2SO3;c-5 mmol/L NaHSO3;d-5 mmol/L Na2SO3;e-10 mmol/L NaHSO3;f-10 mmol/L Na2SO3;g-50 mmol/L NaHSO3;h-50 mmol/L Na2SO3;i-100 mmol/L NaHSO3;j-100 mmol/L Na2SO3
图2 加入不同浓度和种类还原剂的SPI+EA凝胶微观结构
Fig.2 Microstructure of SPI+EA gels with different concentrations and kinds of reducing agents
随着还原剂浓度的增加,凝胶微观结构未联结的粒子数增多,导致凝胶结构松散,硬度低以及易变形(200 mmol/L还原剂形成的凝胶结构太过松软,无法切片固定)。加入Na2SO3后样品网络结构更不清晰,因而其机械强度降低、硬度下降,微结构呈疏松状。低浓度的NaHSO3的加入会使得凝胶硬度增强,然后随着其浓度的升高凝胶硬度逐渐下降,微结构渐呈疏松状。
2.2 离子强度
10%~15%的SPI+EA加入不同浓度盐溶液后加热后所形成的凝胶硬度、持水性和实物图见图3。盐浓度10~100 mmol/L内,复合凝胶的结构和质地表现为紧致,形态无差别,盐离子浓度≥200 mmol/L后凝胶逐渐松软、硬度明显降低。500 mmol/L NaCl溶液的凝胶体系无法形成直立圆柱体。数据揭示,试验条件下盐浓度提高,对凝胶的质构产生先正后负的影响[7-9]。盐浓度10~100 mmol/L内,凝胶硬度随浓度增加,表明盐溶液中和了蛋白质表面的电荷,蛋白质分子间相互吸引作用增强,分子迅速聚集形成硬的凝胶。盐离子浓度500 mmol/L后,蛋白质出现盐溶现象,凝胶强度也出现下降[7-9]。数据表明,凝胶的持水性整体改变不明显。加入不同浓度盐溶液的SPI+EA凝胶微观结构见图4。

a-凝胶硬度;b-持水性;c-实物图
图3 加入不同浓度盐溶液的SPI+EA凝胶硬度和持水性
Fig.3 Hardness and water holding capacity of SPI+EA gels with different concentrations of saline solution

a-10 mmol/L;b-20 mmol/L;c- 50 mmol/L;d-100 mmol/L;e-200 mmol/L;f-500 mmol/L
图4 加入不同浓度盐溶液的SPI+EA凝胶微观结构
Fig.4 Microstructure of SPI+EA gels with different concentrations of saline solution
凝胶微观结构随盐浓度增加从疏松过渡为致密,未联结的粒子数减少,凝胶微观结构有很大改善。其他样品颗粒聚集形成网络,盐浓度为500 mmol/L的凝胶结构柱网络结构消失,蛋白形成一片状,导致其凝胶强度下降,持水性提高。因此,低浓度的盐离子的加入可以增加凝胶的硬度,一定程度提高凝胶持水性,但浓度较高时将又降低凝胶硬度且提高持水性[7-9]。
2.3 热处理程序
10%~15%的SPI+EA经过不同热处理程序后加热所形成的凝胶硬度、持水性和实物图如图5所示。试验条件下,蛋白有更多机会及充足时间打开原有二硫键并生成更多的二硫键,随加热时间延长凝胶硬度和持水性逐渐升高,凝胶微观结构未联结的颗粒趋于减少,紧致性稍有增加。持水性和微观结构都组间差别不明显。加热时间对凝胶持水性和微观结构的影响并非主要因素[10-12]。经过不同热处理程序后加热所形成的凝胶微观结构见图6。

a-凝胶硬度;b-持水性;c-实物图
图5 经过不同热处理程序后SPI+EA凝胶硬度和持水性
Fig.5 Hardness and water holding capacity of SPI+EA gels with different heat treatment

a-加热5 min;b-加热10 min;c-加热15 min;d-加热30 min;e-加热45 min
图6 经过不同热处理程序后SPI+EA凝胶微观结构
Fig.6 Microstructure of SPI+EA gels with different heat treatment
2.4 不同的多糖
10%~15%的SPI+EA加入不同浓度和种类多糖后所形成的凝胶硬度、持水性和实物图见图7。在多糖浓度0.015%~0.3%(质量分数)内,随着刺槐豆胶浓度升高,凝胶硬度增加且结构趋于完善紧致;随结冷胶的浓度的上升,凝胶形成的孔隙增加且影响凝胶的硬度,形态不再良好完整。这与文献报道的浓度对结冷胶形成的凝胶的质构影响较大相一致[13]。加结冷胶溶液的体系相比于加入刺槐豆胶溶液的体系的持水性能更具优势,0.3%时结冷胶体系的持水性达到了74.8%。当刺槐豆胶和结冷胶量少的时候,蛋白部分空间被挤,但在整个体系占主导地位,使蛋白网络的密度反而增加,导致了复合凝胶的强度和持水性增加[14-15]。但是当结冷胶浓度较高时,蛋白和多糖的关系相反,多糖占主导地位,使蛋白的网络不连续,凝胶强度变弱,体系水分含量上升[14-15]。加入不同浓度和种类多糖后所形成的凝胶微观结构见图8。

a-凝胶硬度;b-持水性;c-实物图
图7 加入不同浓度和种类多糖的SPI+EA凝胶硬度和持水性
Fig.7 Hardness and water holding capacity of SPI+EA gels with different concentrations and kinds of polysaccharide

a-0.015%刺槐豆胶;b-0.015%结冷胶;c-0.03%刺槐豆胶;d-0.03%结冷胶;e-0.06刺槐豆胶;f-0.06%刺槐豆胶;g-0.15%结冷胶;h-0.15%刺槐豆胶;i-0.3%结冷胶;j-0.3%刺槐豆胶
图8 加入不同浓度和种类多糖的SPI+EA凝胶微观结构
Fig.8 Microstructure of SPI+EA gels with different concentrations and kinds of polysaccharide
随着多糖浓度的增加,微观结构从疏松过渡为致密,未联结的粒子数减少,形成片状[9]。相同浓度下,加入结冷胶比加入刺槐豆胶形成的凝胶结构更致密、硬度相对较高,但高浓度结冷胶会导致形成的凝胶内部孔隙较多并降低其硬度。
2.5 还原剂、盐离子及多糖复合体系
10%~15%的SPI+EA单独/复合加入了1 mmol/L NaHSO3、 100 mmol/L NaCl、 0.15%结冷胶的凝胶硬度、持水性和实物图见图9。纯10%(质量分数)SPI 形成的凝胶结构最疏松、硬度最低,SPI+EA复合凝胶结构明显变得完整紧致、硬度明显提高,100 mmol/L NaCl提升复合体系的硬度优于1 mmol/L NaHSO3,质量分数0.15%结冷胶能够显著提升复合体系的硬度。在同时加入了1 mmol/L NaHSO3、100 mmol/L NaCl和0.15%结冷胶的混合组中,SPI+EA复合凝胶体系的硬度提高效果最好,其持水性相比于未添加的原体系改变良好[9]。单独/复合加入了不同浓度的还原剂、盐和多糖的凝胶微观结构见图10。
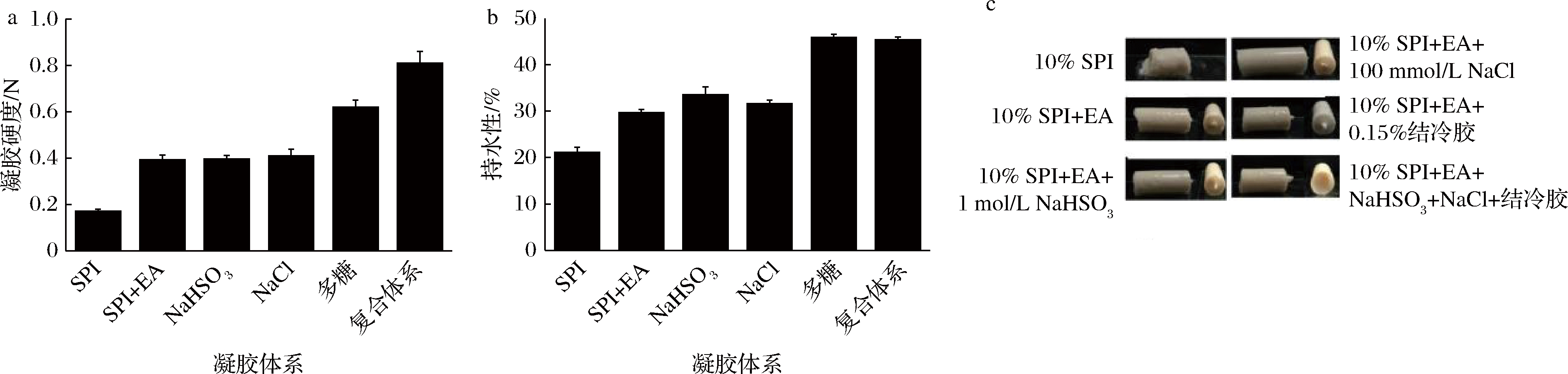
a-凝胶硬度;b-持水性;c-实物图
图9 加入多糖复合体系不同还原剂、盐和多糖的凝胶硬度和持水性
Fig.9 Hardness and water holding capacity of SPI+EA gels with saline solution, reducing agents and polysaccharide

a-10% SPI;b-10% SPI+EA;c-1 mmol/L NaHSO3;d-100 mmol/L NaCl;e-0.15%结冷胶;f-NaHSO3+NaCl+结冷胶
图10 单独/复合加入不同浓度还原剂、盐和多糖的凝胶微观结构
Fig.10 Microstructure of SPI+EA gels with different concentrations of saline solution, reducing agents and polysaccharide
单独/混合加入NaHSO3、NaCl、结冷胶的复合体系的微观结构相比与纯SPI或SPI+EA复合体系更加致密,未联结的颗粒数减少,因素的作用叠加使多条件复合凝胶的硬度达到最高,显著增加凝胶的持水性。
二硫键的形成对复合体系成胶性能的影响,如表1所示。
表1 游离巯基、总巯基及二硫键含量[14-16]
Table 1 The content of free thiol, the total sulphur and disulfide bond
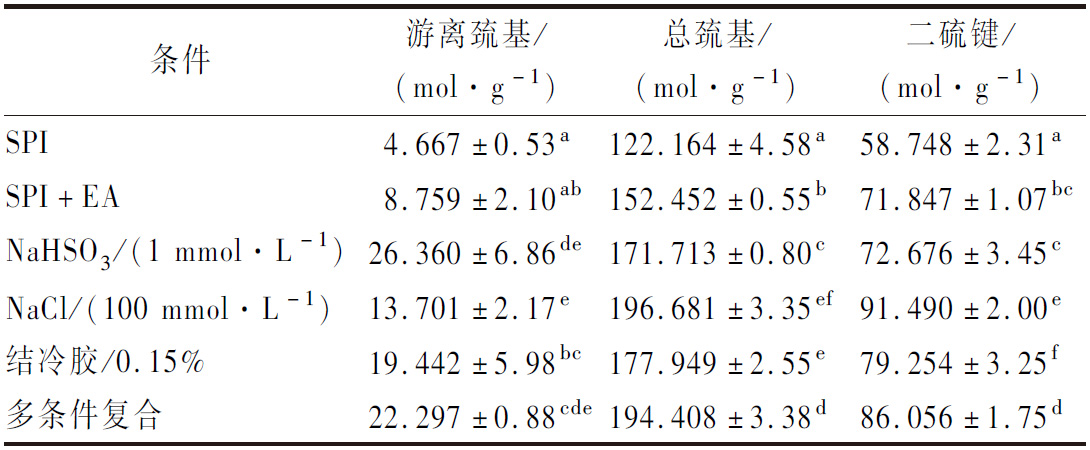
条件游离巯基/(mol·g-1)总巯基/(mol·g-1)二硫键/(mol·g-1)SPI4.667±0.53a122.164±4.58a58.748±2.31aSPI+EA8.759±2.10ab152.452±0.55b71.847±1.07bcNaHSO3/(1 mmol·L-1)26.360±6.86de171.713±0.80c72.676±3.45cNaCl/(100 mmol·L-1)13.701±2.17e196.681±3.35ef91.490±2.00e结冷胶/0.15%19.442±5.98bc177.949±2.55e79.254±3.25f多条件复合22.297±0.88cde194.408±3.38d86.056±1.75d
从二硫键含量可知,SPI溶液中的二硫键含量较少,EA的加入可以提高复合体系中二硫键的含量,在还原剂低浓度时复合凝胶内二硫键的含量增加甚微。加入NaCl和结冷胶会显著增加复合体系中二硫键的含量,从而导致随着加入溶液浓度的增加,凝胶强度逐渐增强的现象。在同时添加了NaHSO3、NaCl和结冷胶的体系中,二硫键的含量显著增加。
3 结论与讨论
低还原剂浓度利于复合凝胶蛋白网络增加,低浓度还原剂与游离巯基形成氧化还原对,或是打开了一些原有分子内的二硫键,最终形成了更强的网络。而还原剂浓度较高时,新形成的二硫键被打断,网络得不到增强,反而减弱了凝胶强度,但持水性得到了增加[5]。蛋白分子表面有亲水、带电基团,提供分子间的斥力,提高体系的离子强度将该作用屏蔽或削弱,聚集程度提高,最终凝胶强度增加。当盐浓度增加到一定程度时,蛋白质出现盐溶现象,凝胶强度也出现下降,但盐溶时持水性会显著提高[7-9]。热处理时间短时,诸多促使凝胶形成的相互作用都没生成,随时间延长,蛋白有更多机会及充足时间打开原有二硫键并生成更多的二硫键,凝胶强度和持水性也随之提高。添加多糖目的为通过微观相分离的办法增加凝胶的强度[17]。加入盐离子和结冷胶都会增加复合凝胶中二硫键的含量,还原剂的影响并不明显,在多条件复合的条件下可以明显获得最佳硬度和持水性的凝胶[14-15]。
[1] WANG C H, DAMODARAN S.Thermal gelation of globular proteins:Influence of protein conformation on gel strength[J].Journal of Agricultural & Food Chemistry, 1991, 39(3):433-438.
[2] 杨娟, 罗玮倩, 何曼源.大豆蛋白/蛋清蛋白复合凝胶特性的研究[J].食品与发酵工业, 2021, 47(6):134-138.
YANG J, LUO W Q, HE M Y.Study on the characteristics of soy protein/egg white protein composite gelatin[J].Food and Fermentation Industries, 2021, 47(6):134-138.
[3] HATAHET F, BOYD D, BECKWITH J.Disulfide bond formation in prokaryotes:History, diversity and design[J].Biochimica et Biophysica Acta (BBA) - Proteins and Proteomics, 2014, 1 844(8):1 402-1 414.
[4] WANG K Q, LUO S Z, ZHONG X Y, et al.Changes in chemical interactions and protein conformation during heat-induced wheat gluten gel formation[J].Food Chemistry, 2017, 214:393-399.
[5] ZOU L F, FU Y, SHEN K, et al.Sulfur-sulfur bond dissociation enthalpies:A high-level ab initio study[J].Journal of Molecular Structure:THEOCHEM, 2007, 807(1-3):87-92.
[6] 黄群, 杨万根, 金永国, 等.鸭蛋清蛋白凝胶质构特性影响因素研究[J].食品科学, 2014, 35(15):68-71.
HUANG Q, YANG W G, JIN Y G,et al.Factors influencing texture properties of duck egg white protein gel[J].Food Science, 2014, 35(15):68-71.
[7] LI J H, ZHANG M Q, CHANG C H, et al.Molecular forces and gelling properties of heat-set whole chicken egg protein gel as affected by NaCl or pH[J].Food Chemistry, 2018, 261:36-41.
[8] ![]() M, NISHINARI K, HANDA A.Ca2+-induced eggwhite isolate gels with various microstructure[J].Food Science and Technology Research, 2014, 20(6):1 207-1 212.
M, NISHINARI K, HANDA A.Ca2+-induced eggwhite isolate gels with various microstructure[J].Food Science and Technology Research, 2014, 20(6):1 207-1 212.
[9] WANG W J, SHEN M Y, LIU S C, et al.Gel properties and interactions of Mesona blumes polysaccharide-soy protein isolates mixed gel:The effect of salt addition[J].Carbohydrate Polymers, 2018, 192:193-201.
[10] GUO J, YANG X Q, HE X T, et al.Limited aggregation behavior of β-conglycinin and its terminating effect on glycinin aggregation during heating at pH 7.0[J].Journal of Agricultural & Food Chemistry, 2012, 60(14):3 782-3 791.
[11] VAN DER PLANCKEN I, VAN LOEY A, HENDRICKX M E G.Changes in sulfhydryl content of egg white proteins due to heat and pressure treatment[J].Journal of Agricultural & Food Chemistry, 2005, 53(14):5 726-5 733.
[12] LAMBRECHT M A, ROMBOUTS I, DE KETELAERE B, et al.Prediction of heat-induced polymerization of different globular food proteins in mixtures with wheat gluten[J].Food Chemistry, 2017, 221:1 158-1 167.
[13] 许怀远, 任向妍, 王垚.结冷胶产品凝胶特性的影响因素研究[J].食品科技, 2009, 34(11):263-268.
XU H Y, REN X Y, WANG Y.Study on affecting factors for gel properties of gellan gum[J].Food Science and Technology, 2009, 34(11):263-268.
[14] HOGG P J.Disulfide bonds as switches for protein function[J].Trends in Biochemical Sciences, 2003, 28(4):210-214.
[15] VISSCHERS R W, DE JONGH H H J.Disulphide bond formation in food protein aggregation and gelation[J].Biotechnology Advances, 2005, 23(1):75-80.
[16] 阮奇珺. 大豆蛋白热诱导二硫键连接物的形成及巯基变化亚基水平研究[D].无锡:江南大学, 2015.
RUAN Q J.Subunit level study on heat induced disulfide linked products and sulfhydryl change of soy protein[D].Wuxi:Jiangnan University, 2015.
[17] HANDA A, TAKAHASHI K, KURODA N, et al.Heat-induced egg white gels as affected pH[J].Journal of Food Science, 1998, 63(3):403-407.