高尿酸血症(hyperuricemia,HUA)是一种因人体嘌呤代谢紊乱以及尿酸排泄失常从而导致的血尿酸含量显著高于正常值的慢性临床综合症,HUA患病率逐年上升并且常常伴发多种系统性疾病[1]。HUA不仅是痛风发病的基础阶段,而且容易诱导糖尿病、高血压、尿酸盐肾病等慢性病[2],长期高尿酸水平对人体血管、心脏以及肾脏均会造成一系列不良后果[3]。当前,HUA的治疗预防措施主要有利用外源药物作用以及限制饮食中嘌呤物质的摄入量两种途径[2]。临床上的降尿酸药物大部分依赖于黄嘌呤氧化酶抑制剂(别嘌呤醇)以及促尿酸排泄药(苯溴马隆)等,虽然降尿酸药物药效明显,但极易引起过敏反应、胃肠道反应以及肝功能损害等毒副作用和病人耐受性差等问题,长期使用会引起人体严重的不良反应[4-5]。另外,由于高嘌呤食物众多,如红肉、海鲜类、肝脏类、禽类、啤酒等,目前很难通过限制饮食来控制HUA的发生[6],此外,食品添加剂中的鲜味剂也属于嘌呤类物质[7]。因此,HUA患者还必须控制饮食中鲜味剂的摄取,这些使患者追求良好风味的饮食习惯受到很大影响。因此,亟待寻找新的途径方法来降低HUA人群血液中的尿酸,探索一种新型的、毒副作用低、且具有一定食源性的HUA治疗与预防途径具有重要的意义。
乳酸菌以无毒、无害、无副作用的特点,在临床治疗和预防代谢性肠道疾病方面日益引起高度重视[8],并在有效调节胃肠道代谢功能方面展现出宽阔的临床应用前景和市场潜力。高原藏区具有夏季强紫外线、低温、低压以及缺氧等多种极端气候环境,其中保存了丰富的微生物菌种资源,并对人体产生诸多有益的影响。本文主要围绕HUA尤其是藏区HUA的发病特点、乳酸菌对HUA的作用及机制以及目前藏区防治HUA的现状进行综述,旨在为筛选降尿酸乳酸菌、开发功能食品以及防治HUA提供新思路。
1 HUA及藏区HUA的特点
1.1 HUA的发病特点
HUA是一种血液中尿酸升高的代谢性疾病,主要指人体血浆尿酸浓度连续≥420 μmol/L(男性)或360 μmol/L(女性)的状态[9]。HUA的发病因素比较复杂,遗传发病因素比如转运尿酸及代谢过程相关的尿酸酶、转运蛋白及其与炎症反应相关的酶因子占主要发病因素[10],此外,还与生活环境、餐食搭配、工作节奏及某些慢性病如痛风、慢性肾病、糖尿病等[11]外界因素密切相关。
人体内尿酸的排泄减少或(和)合成增多均可能导致HUA疾病的发生。如图1所示[12],尿酸作为嘌呤代谢的最终产物,能够通过多方面因素调节其水平并使其在人体中保持动态平衡。机体产生尿酸的途径主要有内源性与外源性两种,大多数生成的尿酸为内源性尿酸,主要源于体内核酸以及嘌呤类物质的代谢,占体内尿酸代谢总量的80%~90%[13];外源性尿酸的产生主要源于富含嘌呤食物的过量摄入,LARIO等[14]调查结果发现,过量摄入红肉、酒精饮料及高果糖食物均与HUA发生密切相关,这些因素已被明确作为HUA和痛风的一些危险因素。尿酸转化需要相关酶的参与,任何酶的异常都会导致尿酸水平异常,遗传因素诱导的HUA多由合成尿酸酶或转移尿酸酶分解功能异常引发[15]。而在临床实践中,90%的HUA患者的病因与肾脏尿酸的排泄功能下降有关,患者体内尿酸约有2/3经肾脏随尿液排泄,其余通过胃及肠道排出[12]。当血尿酸通过肾小球滤过膜时,将近90%的过滤尿液被重新吸收,并主要依赖于尿酸转运蛋白[16],经肾小管的重吸收作用最后再循环流入血液,而其余的血尿酸(10%)通过肾小球滤过最终从尿液中彻底排出[17]。
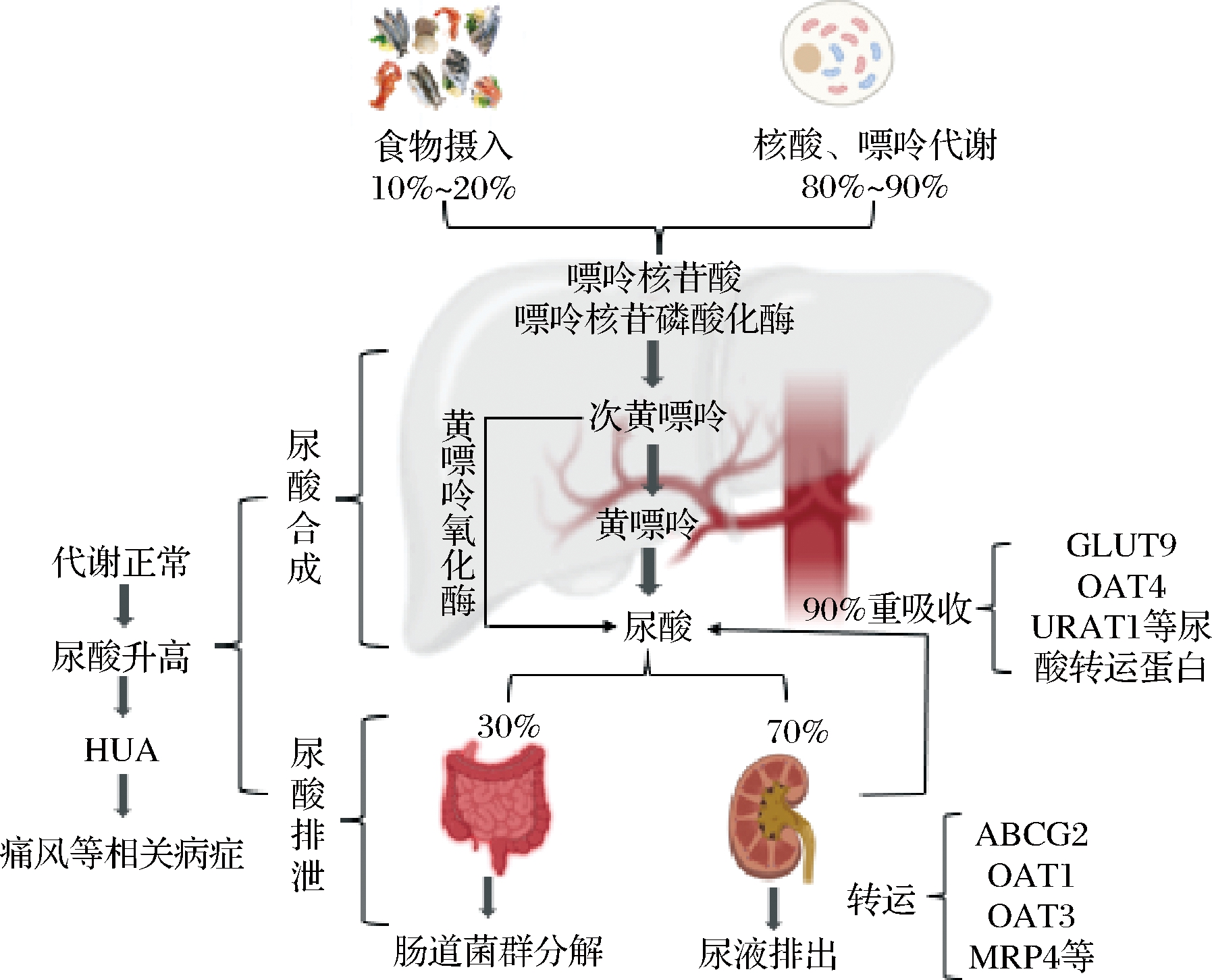
图1 尿酸代谢过程[12]
Fig.1 Uric acid metabolism process[12]
1.2 藏区HUA的特点
高原藏区HUA疾病多发,这主要由于长期以来,受风俗习惯、宗教民族的影响,藏区的居民日常餐食都以牛羊肉、酥油茶以及动物的头、蹄、肝、肺为主,这些食物嘌呤类物质含量较多。此外,因藏区的地域特征,牧民长期缺乏新鲜蔬菜水果的摄入且喜好饮酒,酒中的乙醇刺激机体肾脏合成大量乳酸从而阻碍肾脏的排泄功能,并且乙醇积累能显著增加嘌呤的生物合成代谢速度,使体内嘌呤的含量增多,从而诱发HUA疾病[18]。高原藏区寒冷环境下会直接刺激人体关节组织局部深层微血管壁的收缩,同时低氧气环境中,为有效保证关节各个组织内部供氧需求,血液按需分配到各处,人体容易出现体内红细胞数量增多[19],导致血液黏稠度增加,局部血流速度减缓,从而导致尿酸盐沉积引发HUA[20];另有研究发现,高原藏族HUA发病率人群明显高于平原地区[21],这可能与藏区高海拔、低氧影响人们肾脏和肝功能的原因有关。此外,缺氧环境下NO含量逐渐增多,NO能够与体内尿酸盐直接发生作用引起尿酸盐的沉积产物增多,生成不稳定的亚硝化尿酸代谢产物,从而诱发HUA以及慢性痛风的病症[22]。
2 藏区防治HUA的现状及进展
史恒等[23]通过调查研究发现,藏区居民HUA患病率为16.86%,其中男性患病率为23.84%,女性患病率为11.42%,西藏18岁以上居民HUA患病率高于全国平均水平。目前,关于藏区防治HUA的手段主要有西药、中医药治疗、藏医藏药三方面。
2.1 西药防治
目前人们广泛采用西药治疗HUA。黄嘌呤氧化酶(xanthine oxidase,XO)能够将人体内的黄嘌呤与次黄嘌呤氧化,形成尿酸与黄嘌呤。为有效抑制尿酸的增加,通过抑制XO的活性来实现,在药物研发过程中,以XO活性的抑制作为药物研发的重要靶点[24]。现阶段临床医学治疗通常采用别嘌醇类药物,然而在实际临床应用中发现某些患者对药物不耐受。大多数HUA患者主要是因尿酸排泄不畅而引发疾病。因此,促进尿酸排泄的药物在一定程度上更适用于高尿酸血症患者的治疗[25]。临床医学中应用的苯溴马隆能够有效抑制肾小管对尿酸的重吸收,使血尿酸浓度能够迅速降低,尿酸排泄速度加快[26]。但此类药物的长期服用也会导致患者产生不良反应,主要表现在对人体肝脏的损伤[27]。
2.2 中医药治疗
由于西医中用于治疗HUA的药物对患者具有多重副作用,大大降低了药物应用的价值。从中医角度讲,针灸通过刺激病变局部或者特定腧穴,发挥疏通经络、调和气血、平衡阴阳的作用,从而达到通则不痛,以此用于治疗HUA疾病的发生[28]。李博[29]利用穴位埋线治疗腹型肥胖HUA患者30例,治疗3个疗程后,显效率为66.7%,总有效率为93.3%,结果表明穴位埋线与针刺均能显著降低血尿酸和腹围。苗兵[28]采用针刺结合自拟中药方医治HUA患者30例,临床数据表明,针药结合总有效率达93.33%,高于中药对照组,有效降低了血尿酸、血脂。
除了针灸用于干预治疗HUA外,现代中医在传统药方的基础上对HUA症状患者也具有一定的疗效。并且许多中药有一药多效、作用靶点宽泛的优势,在HUA治疗中具有较高的研究应用价值[30]。梁谋等[31]以健脾温肾,渗湿泄浊研究出固本泄浊方,对HUA患者治疗8周后,发现固本泄浊方能够有效降低尿酸,且改善身重、便溏等中医症状积分,对肝肾功能无影响。徐红等[32]通过结合多年临床经验,研究出了芪苓颗粒,给大鼠灌胃连续14 d,经代谢组学检测发现该中药方不仅减少尿酸含量,还能促进糖脂代谢,且对代谢器官损伤小。朱娟[33]运用糖肾灌肠方每次保持灌肠30 min以上,与西医治疗相比较,发现糖肾灌肠方能有效降低尿酸及空腹血糖,减少微量蛋白尿。
2.3 藏医藏药防治
藏医藏药是藏区特有的治疗各种病症的有效手段,目前用于治疗HUA疾病临床疗效较好的藏药有:十味乳香胶囊、二十五味儿茶丸、二十五味驴血丸等[30]。然而藏药在使用的过程中重金属含量偏高,长期使用会对HUA患者的肝肾功能造成不同程度的损害。
2.4 乳酸菌对HUA的防治
乳酸菌作为人体肠道内正常菌群,能够调控人体血脂、血糖等代谢过程。已有研究表明,某些乳酸菌可以通过降解或者吸收核苷竞争性减少肠道上皮对核苷的吸收,从而减少尿酸的生成[34],在治疗HUA上具有药物治疗无可比拟的优点。曲以之等[35]研究发现,口服乳酸菌能够在肠道中分解由食物带入体内的大量嘌呤,该研究证明乳酸菌具有有效降低嘌呤摄入和提高分解血清尿酸的能力。LI等[36]在体外利用高效液相色谱的方法评价了55株乳酸菌对鸟苷和肌苷的降解作用,经驯化后的植物乳杆菌DM9218-A表现出较强的鸟苷和肌苷降解能力,且使高尿酸血症大鼠的血尿酸浓度显著降低;杨殿斌[37]通过分离研究得到1株植物乳杆菌,证实其具有快速吸收肌苷、鸟苷的代谢能力,并通过干预嘌呤代谢通路以降低体内尿酸的过量产生。日本研究学者发现1株能够快速高效分解嘌呤核苷的新型乳酸菌,该菌能够在人体肠道中吸收并降解食物中的嘌呤核苷,进而降低人体血尿酸含量[38]。日本明治公司的YAMADA等[39]通过体外放射性同位素标记实验、动物实验和人群实验等研究手段对格氏乳杆菌PA-3进行了大量研究,经过筛选得到多株具有快速高效降解嘌呤核苷能力的乳酸菌,其中格氏乳杆菌PA-3对嘌呤具有较强吸收能力,能够有效降低大鼠肠道对嘌呤的吸收,并能够显著降低大鼠和人的尿酸水平。日本明治株式会社的PA-3产品已成功投入商业化开发使用,而目前我国利用乳酸菌研究其对HUA疾病的防治尚处于起步阶段[40]。对于HUA重症患者而言,仅单一益生菌治疗难以很快见效,还必须与其他治疗药物同时配合使用,从而才能快速有效消除炎症并从胃肠道及其微生态系统的根源上调节、抑制各种炎症的反复发生。目前将益生菌用于降尿酸、缓解早期HUA的临床实例相对较少,因此需要在临床上进一步验证利用乳酸菌保健食品对缓解HUA及痛风患者的实际应用疗效。
3 乳酸菌对HUA的作用及机制
近年来,乳酸菌对HUA的预防调控机制是国内外学者的研究热点。乳酸菌主要通过有效改善患者肠道内细菌微环境,调节患者肠道新陈代谢平衡等生理功能进而有效降低患者体内血尿酸的累积,能够对HUA以及慢性痛风病症等起到间接性的预防治疗作用。金方等[41]研究发现干酪乳杆菌ZM15能够在体外降解核苷酸与核苷,并通过给大鼠腹腔注射氧嗪酸钾及高嘌呤饮食建立HUA模型,推测可能是通过与肠道上皮细胞竞争吸收相应核苷酸与核苷使模型大鼠的血尿酸水平显著降低。叶泽[34]和WU等[42]从传统发酵制品浆水中筛选并获得了具有降解尿酸的发酵乳杆菌JL-3,研究其对HUA小鼠模型的血尿酸浓度、尿酸的排出以及对小鼠肠道菌群结构和功能的影响。结果说明,JL-3能够定植在小鼠肠道中并提高肠道菌群降解尿酸的能力;同时JL-3能够主要通过增加尿酸在肠道中的排泄来降低血尿酸浓度,并降低了由高血尿酸引起的一些炎症反应。
人体肠道菌群失调是HUA的特征之一,肠道菌群失调可影响尿酸代谢导致机体血尿酸水平升高[43],从而促进了HUA的发病率。目前,越来越多的研究和临床调查表明HUA的发生与肠道菌群原生结构和数量的改变有关,HUA发病患者与正常人群相比,其体内肠道菌群存在差异性的变化[44]。任科雨等[45]研究了青岛地区30例HUA患者的肠道菌群,结果发现,HUA患者相较健康人群存在菌群失调现象,任科雨等研究还发现肠道菌群分解酶对尿酸的分解能力与某些乳酸菌(双歧杆菌、乳酸杆菌)含量成正相关,而与其他菌属无关。黄胜男等[46]通过利用高嘌呤饲料喂养鹌鹑4周来建立HUA模型,结果发现鹌鹑体内的肠道菌群黄嘌呤氧化酶活性以及尿酸水平较正常鹌鹑组显著增高,通过对鹌鹑进行抗菌药物干预后肠道菌群得到改善,尿酸趋向正常水平。该研究结果表明肠道菌群对尿酸代谢以及HUA具有一定的调控作用。
乳酸菌本身具有完整的嘌呤代谢合成途径,更重要的是由于其内部含有一种尿酸氧化酶,能够进一步将人体内尿酸氧化为尿囊素。此外,人体肠道是嘌呤类化合物的吸收部位,乳酸菌主要在肠道中通过摄取和降解嘌呤类化合物来延缓HUA,其中,降解能力主要依赖菌体内以及其代谢产物发挥作用。因此,减少肠道对尿酸的吸收和抑制肝脏中尿酸的形成是控制血清中尿酸浓度的有利途径。YU等[47]研究发现,患有HUA的大鼠经应用药物注射治疗降低尿酸后对其肠道益生菌群代谢结构发生明显改变,且益生菌对于降尿酸受体代谢异常大鼠具有一定的免疫调控抑制作用[48]。有研究表明,通过服用别嘌呤醇等药物能够抑制尿酸的合成或产生,并且能够有效对抗HUA患者胃肠道菌群结构发生变化[49]。这为HUA发病提供了新的治疗思路:以多种降低血尿酸药物治疗为主,辅以生物免疫疗法从而有效改善HUA患者的肠道菌群。
4 结论与展望
由尿酸代谢异常引发的HUA主要原因是高嘌呤、高热量饮食的过量摄入以及人体尿酸排泄代谢能力的降低。肠道内部菌群结构和数量的改变会引起尿酸代谢发生异常,反之,尿酸代谢异常也会改变肠道菌群结构,目前,两者之间互作的分子反应机制还有待进一步深入研究,从而为调节尿酸代谢提供新的科学见解。同时,我国藏区居民痛风性风湿关节炎逐渐向高度低龄化、发病时间长、病损程度重、致残率高等趋势发展,严重影响藏区居民的生活质量,而目前运用乳酸菌治疗HUA的研究尚处于起步阶段。为此,从当地纯手工发酵的乳制品中筛选不同来源的乳酸菌,充分利用当地乳酸菌资源治疗HUA是一个新的突破口,以期对HUA及痛风性关节炎患者的治疗起到一定的作用,同时对填补我国乳酸菌种质资源库具有重要意义。
[1] GLIOZZI M, MALARA N, MUSCOLI S, et al.The treatment of hyperuricemia[J].International Journal of Cardiology, 2016, 213:23-27.
[2] LIU J, ZHANG H, DONG Z, et al.Mendelian randomization analysis indicates serum urate has a causal effect on renal function in Chinese women[J].International Urology and Nephrology, 2017, 49(11):2 035-2 042.
[3] VILLIGER A, SALA F, SUTER A, et al.In vitro inhibitory potential of Cynara scolymus, Silybum marianum, Taraxacum officinale, and Peumus boldus on key enzymes relevant to metabolic syndrome[J].Phytomedicine, 2015, 22(1):138-144.
[4] 岳静静. 芒果苷元降尿酸药效验证及其药代动力学研究[D].广州:广东药科大学, 2017.
YUE J J.Study on the anti-hyperuricemia effect of norathyriol and its pharmacokinetics[D].Guangzhou:Guangdong Pharmaceutical University, 2017.
[5] ZHANG Y Y, LI Q, WANG F Z, et al.A zebrafish (Danio rerio) model for high-throughput screening food and drugs with uric acid-lowering activity[J].Biochemical and Biophysical Research Communications, 2019, 508(2):494-498.
[6] VILLEGAS R, XIANG Y B, ELASY T, et al.Purine-rich foods, protein intake, and the prevalence of hyperuricemia:The Shanghai Men's Health Study[J].Nutrition, Metabolism and Cardiovascular Diseases, 2012, 22(5):409-416.
[7] 王勇, 朱莉萍, 闫秋成.高效液相色谱法测定鸡精中呈味核苷酸含量[J].发酵科技通讯, 2010, 39(4):16-17.
WANG Y, ZHU L P, YAN Q C.Determination of flavorable nucleotide in chicken essence by HPLC[J].Fermentation Technology Newsletter, 2010, 39(4):16-17.
[8] YAMANAKA H, TANIGUCHI A, TSUBOI H, et al.Hypouricaemic effects of yoghurt containing Lactobacillus gasseri PA-3 in patients with hyperuricaemia and/or gout:A randomised, double-blind, placebo-controlled study[J].Modern Rheumatology, 2019, 29(1):146-150.
[9] DUSKIN-BITAN H, COHEN E, GOLDBERG E, et al.The degree of asymptomatic hyperuricemia and the risk of gout.A retrospective analysis of a large cohort[J].Clinical Rheumatology, 2014, 33(4):549-553.
[10] 裴芳, 裴华, 夏中华, 等.高尿酸血症和痛风的表观遗传学研究进展[J].生理科学进展, 2019, 50(3):175-180.
PEI F, PEI H, XIA Z H, et al.Research progress of epigenetics in hyperuricemia and gout[J].Progress in Physiological Sciences, 2019, 50(3):175-180.
[11] 孙琳, 王桂侠, 郭蔚莹.高尿酸血症研究进展[J].中国老年学杂志, 2017, 37(4):1 034-1 038.
SUN L, WANG G X, GUO W Y.Research progress of hyperuricemia[J].Chinese Journal of Gerontology, 2017, 37(4):1 034-1 038.
[12] 孙泽锐,王宣军,盛军.高尿酸血症研究进展[J].云南民族大学学报(自然科学版),2021,30(2):135-142;156.
SUN Z R, WANG X J, SHENG J. Research progress in hyperuricemia[J]. Journal of Yunnan Minzu University(Natural Sciences Edition), 2021,30(2):135-142;156.
[13] 邓娟, 贾红.高尿酸血症的流行病学研究现状[J].医学综述, 2014, 20(6):972-975.
DENG J, JIA H.Epidemiological research status of hyperuricemia[J].Medical Recapitulate, 2014, 20(6):972-975.
[14] LARIO B A, VALDIVIELSO J.Hiperuricemia y gota:el papel de la dieta[J].Nutricion Hospitalaria, 2014, 29(4):760-770.
[15] 张新军. 高尿酸血症的发病机制与分型诊断[J].中国心血管杂志, 2010, 15(6):418-420.
ZHANG X J.Pathogenesis and classification of hyperuricemia[J].Chinese Journal of Cardiovascular Medicine,2010, 15(6):418-420.
[16] 胡小华, 张黎明.尿酸代谢途径的研究进展[J].临床肾脏病杂志, 2019, 19(12):935-937.
HU X H, ZHANG L M.Progress in research on uric acid metabolism pathway[J].Journal of Clinical Nephrology, 2019, 19(12):935-937.
[17] XU L Q, SHI Y F, ZHUANG S G, et al.Recent advances on uric acid transporters[J].Oncotarget, 2017, 8(59):100 852-100 862.
[18] 关宝生. 痛风和高尿酸血症的人群流行病学研究及hOATl基因变异的分子生物学研究[D].佳木斯:佳木斯大学, 2011.
GUAN B S.Population epidemiology of gout and hyperuricemia and molecular biology of hOATl gene variation[D].Jiamusi:Jiamusi University, 2011.
[19] 梁萍. 高原地区部队年轻人原发性痛风高发因素的调查及临床分析[J].临床医药文献电子杂志, 2020, 7(26):172-173.
LIANG P.Investigation and clinical analysis of high incidence factors of primary gout in young troops in plateau area[J].Electronic Journal of Clinical Medical Literature, 2020, 7(26):172-173.
[20] 潘媛, 徐立, 时乐, 等.痛风性关节炎的发生与尿酸盐结晶沉积[J].安徽医药, 2009, 13(11):1 305-1 307.
PAN Y, XU L, SHI L, et al.Incidence of gouty arthritis and crystallization of uric acid sodium deposition[J].Anhui Medical and Pharmaceutical Journal, 2009, 13(11):1 305-1 307.
[21] 杨聪, 吕国治, 刘云祥, 等.西藏林芝地区藏族健康体检人群高尿酸血症分析[J].华南国防医学杂志, 2009, 23(6):10-11;33.
YANG C, LV G Z, LIU Y X, et al.Hyperuricemia in tibetans undergoing health examination in Linzhi district in tiebet[J].Military Medical Journal of South China, 2009, 23(6):10-11;33.
[22] 王辉, 彭超, 刘勇, 等.探讨高原环境下痛风性关节炎的临床特点[J].西藏医药, 2018, 39(01):36-38.
WANG H, PENG C, LIU Y, et al.To investigate the clinical characteristics of gouty arthritis in high altitude environment[J].Tibetan Medicine, 2018, 39(01):36-38.
[23] 史恒, 于跃, 白国霞, 等.西藏居民高尿酸血症患病现况分析[J].世界最新医学信息文摘, 2019, 19(63):299;302.
SHI H, YU Y, BAI G X, et al.Analysis of prevalence of high uric acidemia in Tibetan residents[J].World Latest Medicine Information, 2019, 19(63):299;302.
[24] 郭诗韵, 马丽.糖尿病肾病与高尿酸血症的关系研究进展[J].新疆中医药, 2019, 37(2):157-160.
GUO S Y, MA L.Research progress on the relationship between diabetic nephropathy and hyperuricemia[J].Xinjiang Journal of Traditional Chinese Medicine, 2019, 37(2):157-160.
[25] 唐子猗, 青玉凤.降尿酸药物治疗高尿酸血症及痛风的现状及研究进展[J].中华风湿病学杂志, 2019,23(3):199-204.
TANG Z Y, QING Y F.Current status and research progress of uric acid-lowering drugs in the treatment of hyperuricemia and gout[J].Chinese Journal of Rheumatology, 2019,23(3):199-204.
[26] 范廷婷, 钟梦诗, 罗彩凤, 等.乳腺癌术后患者心理弹性和积极应对方式对自我形象的影响研究[J].护士进修杂志, 2019, 34(2):122-125.
FAN T T, ZHONG M S, LUO C F, et al.Effect of resilience and positive coping strategies on self image for patients after breast cancer surgery[J].Journal of Nurses Training, 2019, 34(2):122-125.
[27] 张雷, 闫成芸, 许净, 等.高尿酸血症与冠心病相关性的研究进展[J].河南大学学报(医学版), 2018, 37(2):82-85;89.
ZHANG L, YAN C Y, XU J, et al.Research progress on the relationship between hyperuricemia and coronary heart disease[J].Journal of Henan University (Medical Science), 2018, 37(2):82-85;89.
[28] 苗兵. 针刺结合降尿酸方防治高尿酸血症的临床研究[J].黑龙江医学, 2016, 40(9):853-854.
MIAO B.Clinical study on prevention and treatment of hyperuricemia by acupuncture combined with lowering uric acid prescription[J].Heilongjiang Medical Journal, 2016, 40(9):853-854.
[29] 李博. 穴位埋线对腹型肥胖患者高尿酸血症的影响[D].广州:广州中医药大学, 2010.
LI B.Clinical analysis on acupoint catgut-embedding therapy for abdominal obesity[D].Guangzhou:Guangzhou University of Chinese Medicine, 2010.
[30] 王辉, 刘勇.高原痛风性关节炎的治疗研究进展[J].西藏医药, 2018, 39(3):141-144.
WANG H, LIU Y.Progress in the treatment of gouty arthritis at high altitude[J].Tibetan Medicine, 2018, 39(3):141-144.
[31] 梁谋, 钟建, 魏清兰, 等.固本泄浊方治疗无症状高尿酸血症的临床观察及安全性评价[J].江西中医药, 2018, 49(6):32-34.
LIANG M, ZHONG J, WEI Q L, et al.Clinical observation and safety evaluation of Guben Xiezhuo Prescription in the treatment of asymptomatic hyperuricemia[J].Jiangxi Journal of Traditional Chinese Medicine, 2018, 49(6):32-34.
[32] 徐红, 罗恒, 陈坚翱.基于代谢组学对中药芪苓颗粒治疗高尿酸血症的疗效及安全性评价[J].中华中医药杂志, 2017, 32(10):4 644-4 647.
XU H, LUO H, CHEN J N.Evaluation of the efficacy and safety of traditional Chinese compound Qiling Granules in the treatment of hyperuricemia based on metabonomics[J].China Journal of Traditional Chinese Medicine and Pharmacy, 2017, 32(10):4 644-4 647.
[33] 朱娟. 糖肾灌肠方对糖尿病肾病合并高尿酸患者的临床疗效观察[D].乌鲁木齐:新疆医科大学, 2016.
ZHU J.Clinical efficacy Tangshen Enema of diabetic nephropathy with hyperuricemia patients[D].Urumqi:Xinjiang Medical University, 2016.
[34] 叶泽. 益生菌对高尿酸血症小鼠血清尿酸水平的影响及机制[D].兰州:兰州大学, 2019.
YE Z.Effect and mechanism of probiotics on mouse with hyperuricemia serum uric acid level[D].Lanzhou:Lanzhou University, 2019.
[35] 曲以之, 袁杰利.痛风及微生态防治的相关进展[J].中国微生态学杂志, 2011, 23(4):372-374.
QU Y Z, YUAN J L.Microbial control of gout and related developments[J].Chinese Journal of Microecology, 2011, 23(4):372-374.
[36] LI M, YANG D B, MEI L, et al.Screening and characterization of purine nucleoside degrading lactic acid bacteria isolated from Chinese sauerkraut and evaluation of the serum uric acid lowering effect in hyperuricemic rats[J].PLoS One, 2014, 9(9):e105577.
[37] 杨殿斌. 降血尿酸乳酸菌筛选及乳杆菌对高血尿酸血症大鼠作用的研究[D].大连:大连医科大学, 2013.
YANG D B.The screening of Lactobacillus reduced blood uric acid and Lactobacillus’ effect in hyperuricemia rat model[D].Dalian:Dalian Medical University, 2013.
[38] KANO H, YAMADA N, SAITO C, et al.Lactobacillus gasseri PA-3, but not L.gasseri OLL2996, reduces the absorption of purine nucleosides in rats[J].Nucleosides, Nucleotides & Nucleic Acids, 2018, 37(6):353-360.
[39] YAMADA N, SAITO C, MURAYAMA-CHIBA Y, et al.Lactobacillus gasseri PA-3 utilizes the purines GMP and guanosine and decreases their absorption in rats[J].Nucleosides, Nucleotides & Nucleic Acids, 2018, 37(5):307-315.
[40] 麻菊美, 赵伟睿, 胡升, 等.高效降解嘌呤核苷乳酸菌的筛选及特性研究[J].食品与生物技术学报, 2019, 38(4):8-14.
MA J M, ZHAO W R, HU S, et al.Isolation of a lactic acid bacterium with high ability of purine nucleoside-decomposing and evaluation of its probiotic properties[J].Journal of Food Science and Biotechnology, 2019, 38(4):8-14.
[41] 金方, 杨虹.降血尿酸益生菌株的筛选和降血尿酸机理的探索[J].微生物学通报, 2018, 45(8):1 757-1 769.
JIN F, YANG H.Isolation of hypouricemic probiotics and exploration their effects on hyperuricemic rats[J].Microbiology China, 2018, 45(8):1 757-1 769.
[42] WU Y, YE Z, FENG P Y, et al.Limosilactobacillus fermentum JL-3 isolated from “Jiangshui” ameliorates hyperuricemia by degrading uric acid[J].Gut Microbes, 2021, 13(1):1897211.
[43] 林璋, 祖先鹏, 谢海胜, 等.肠道菌群与人体疾病发病机制的研究进展[J].药学学报, 2016, 51(6):843-852.
LIN Z, ZU X P, XIE H S, et al.Research progress in mechanism of intestinal microorganisms in human diseases[J].Acta Pharmaceutica Sinica, 2016, 51(6):843-852.
[44] 玛依娜·卡哈尔, 孙玉萍, 孜来古丽·米吉提, 等.维吾尔族与汉族人群肠道菌群与高尿酸血症关系的研究[J].新疆医科大学学报, 2014, 37(4):419-422.
KAHAER M, SUN Y P, MIJITI Z, et al.A research on the relationship between hyperuricemia and fecal microbiota in two ethnic populations[J].Journal of Xinjiang Medical University, 2014, 37(4):419-422.
[45] 任科雨,勇春明,金延春,等.青岛地区高尿酸血症患者的肠道菌群分析[J].中国医师杂志, 2014, 16(12):1 649-1 656.
REN K Y, YONG C M, JIN Y C, et al.Intestinal microflora analysis of hyperuricemia patients in Qingdao[J].Chinese Journal of Medical Doctors, 2014, 16(12):1 649-1 656.
[46] 黄胜男, 林志健, 张冰, 等.肠道菌群结构变化与高尿酸血症发生的关系[J].北京中医药大学学报, 2015, 38(7):452-456.
HUANG S N, LIN Z J, ZHANG B, et al.Correlation between structural shifts of gut microbiota and hyperuricemia in quails[J].Journal of Beijing University of Traditional Chinese Medicine, 2015, 38(7):452-456.
[47] YU Y R, LIU Q P, LI H C, et al.Alterations of the gut microbiome associated with the treatment of hyperuricaemia in male rats[J].Frontiers in Microbiology, 2018, 9:2233.
[48] ![]() M,
M,  ONIEWSKI I, VAN HEMERT S, et al.Dose-dependent effects of multi species probiotic supplementation on the lipopolysaccharide (LPS) level and cardiometabolic profile in obese postmenopausal women:a 12-week randomized clinical trial [J].Nutrients, 2018, 10(6):773-.
ONIEWSKI I, VAN HEMERT S, et al.Dose-dependent effects of multi species probiotic supplementation on the lipopolysaccharide (LPS) level and cardiometabolic profile in obese postmenopausal women:a 12-week randomized clinical trial [J].Nutrients, 2018, 10(6):773-.
[49] ETANI R, KATAOKA T, KANZAKI N, et al.Difference in the action mechanism of radon inhalation and radon hot spring water drinking in suppression of hyperuricemia in mice[J].Journal of Radiation Research, 2016, 57(3):250-257.