吞咽障碍是指从口腔吞咽或运输食物和水到胃部时发生困难的一种症状[1]。吞咽障碍会引发脱水、营养不良和吸入性肺炎,导致身体免疫力下降,并且有感染更多疾病的风险[2]。吞咽障碍人群治疗方法通常以患者为中心,分为行为型、内科型和外科型3种基本类型,行为型也被认为是首要的也是最简单的治疗方法[3]。一个重要的行为疗法就是利用食品增稠剂产品改变饮食质地,包括增加食团的表观黏度和内聚性[4-5],使食团通过咽部的速度减慢,这样能够给予咽部足够的反应时间,有利于患者的安全吞咽,减少误吸风险[6]。
目前,用于吞咽障碍人群饮食的增稠剂产品主要有淀粉基增稠剂和胶基增稠剂[7]。淀粉基增稠剂由改性淀粉组成,它可以有效提高吞咽困难患者的吞咽安全性和效率[8]。但是淀粉基增稠剂会产生令人不适的“淀粉味”,使患者的吞咽欲望下降[9],此外,人口腔中的α-唾液淀粉酶会导致淀粉水解,可能会使淀粉的增稠效果下降[10]。胶基增稠剂是由亲水胶体组成,一般含有黄原胶(xanthan gum, XG)。黄原胶具有降低吞咽障碍病人误吸风险所必需的流变特性:剪切稀化和优良的增稠能力[1]。另外,黄原胶无色无味且质地光滑,有着较多的亲水侧链,比其他亲水胶体的水合速度更快[11]。黄原胶和瓜尔豆胶(guar gum, GG)具有协同增效作用,既能生成弱凝胶也可以达到节省原材料的目的[12],并且瓜尔豆胶在结肠中能够被活性细菌发酵产生短链脂肪酸,对肠道健康具有一定的保护作用[13]。
在吞咽障碍患者饮食中,表观黏度是一个十分重要的流变参数[10]。2002年,美国饮食协会发布了国家吞咽障碍饮食方案(National Dysphagia Diet, NDD),该方案以25 ℃下50 s-1剪切速率下的表观黏度值为标准,将液态食物分为4个等级:稀薄型(1~50 mPa·s)、花蜜型(51~350 mPa·s)、蜂蜜型(351~1 750 mPa·s)、布丁型(> 1 750 mPa·s),方便不同吞咽障碍程度的患者选择不同的食物等级进行治疗[14]。该方案虽然有一定的局限性,但表明了表观黏度对吞咽障碍患者安全吞咽的影响。此外,其他流变特性,如假塑性、黏弹性和屈服应力,也与液态食物的口感和安全吞咽有一定的相关性[1, 10]。因此,需要对增稠剂在相关液体食品中的流变性质及其影响因素进行系统的研究。
目前,已有少量文献报道了胶基增稠剂在常温液体食品中(如牛奶、果汁和运动饮料等)的流变学性质[15],但考虑吞咽障碍增稠剂主要面向的是老年人或术后患者,因此,研究其在高蛋白热饮中的应用具有现实意义。在我国,豆浆和牛奶因营养丰富而深受消费者的喜爱,是常见的蛋白饮品。本文以黄原胶和瓜尔豆胶为主要原料的胶基增稠剂为研究对象,通过分析温度、pH、蛋白饮料种类(豆浆、脱脂牛奶和高脂牛奶)等对其流变性质的影响,以期阐明胶基增稠剂在蛋白热饮中的应用特点,为胶基增稠剂在吞咽障碍人群的临床使用提供建议和指导。
1 材料与方法
1.1 材料和设备
黄原胶,斯比凯可(山东)生物制品有限公司;瓜尔豆胶,丹尼斯克(中国)有限公司;复配增稠剂S,主要原料为黄原胶和瓜尔豆胶,上海民和生物科技有限公司;柠檬酸、柠檬酸钠,上海源叶生物科技有限公司;豆浆,永和食品有限公司;高脂牛奶,光明优+纯牛奶(脂肪含量为6%),光明乳业股份有限公司;德国兰雀脱脂牛奶,广州杰钬商贸有限公司;实验用水均为去离子水。
Discoery HR-3流变仪,美国TA仪器公司。
1.2 实验方法
1.2.1 样品配制
1.2.1.1 不同比例的黄原胶-瓜尔豆胶(XG-GG)混合物的配制
配制质量浓度为3 g/L的XG-GG混合溶液,混合溶液中黄原胶和瓜尔豆胶质量比为10∶0、9∶1、7∶3、5∶5、3∶7、1∶9、0∶10。在室温下,以磁力搅拌器500 r/min搅拌4 h后,放入冰箱,4 ℃水合8 h,以确保混合溶液表观黏度不再变化。
1.2.1.2 10 g/L增稠剂S的配制
准确称量100 mg增稠剂S溶解于10 mL水中,在室温下,以磁力搅拌器500 r/min搅拌4 h后,放入冰箱,4 ℃水合8 h,以确保混合溶液表观黏度不再变化。
1.2.1.3 不同pH增稠剂S的配制
准确称量100 mg增稠剂S粉末溶解于柠檬酸-柠檬酸钠缓冲溶液中,以磁力搅拌器500 r/min转速搅拌4 h后,放入冰箱,4 ℃水合8 h。样品的最终pH为1.92、3.34、4.55、5.63、6.38、8.70。
1.2.1.4 增稠豆浆和增稠牛奶(高脂和脱脂)的配制
用豆浆、脱脂牛奶和高脂牛奶溶解增稠剂S粉末,使每种蛋白饮料增稠流食质量浓度为10、20 g/L。在室温下,以磁力搅拌器500 r/min搅拌6 h后,放入冰箱,4 ℃水合8 h。
1.2.2 稳态剪切扫描(flow sweep)测试
使用Discoery HR-3流变仪对不同比例下的XG-GG混合物在常温下(25 ℃)进行稳态剪切速率扫描测试,并测定质量浓度为10 g/L增稠剂S在不同温度(20、40、60、80 ℃)和不同pH(1.92、3.34、4.55、5.63、6.38、8.70)的表观黏度以及增稠蛋白饮料(豆浆、高脂牛奶和脱脂牛奶)在常温下(25 ℃)的表观黏度。
样品测试均采用不锈钢平板(直径40 mm,测试间隙1 000 μm),剪切速率:0.1~1 000 s-1[16]。
选择Power-law模型拟合稳态流变曲线[15],如公式(1)所示:
σ=Kγn
(1)
式中:σ,剪切应力,Pa;γ,剪切速率,s-1;K,稠度系数,Pa·sn;n,流动行为指数,无量纲。
由公式(1)中K和n计算得到公式(2),从而可以计算50 s-1剪切速度下的表观黏度值η50。
η50=K·50n-1
(2)
1.2.3 振幅(oscillation amplitude)和频率(oscillation frequency)扫描测试
使用Discoery HR-3流变仪对增稠蛋白饮料(豆浆、高脂牛奶和脱脂牛奶)进行振幅扫描测试,振幅扫描范围(γ0)为0.1%~300.0%,角频率为10 rad/s[17];参照NISHINARI等[16]的方法对不同比例下的XG-GG混合物进行频率扫描测试,测定XG、GG和增稠剂S在不同温度(20、40、60、80 ℃)和不同pH(1.92、3.34、4.55、5.63、6.38、8.70)的动态频率流变特性以及增稠蛋白饮料(豆浆、高脂牛奶和脱脂牛奶)在常温下(25 ℃)的动态频率流变特性,频率0.1~10.0 Hz,应变值为2.0%,该值在线性黏弹区范围内。
样品测试均采用不锈钢平板(直径40 mm,测试间隙1 000 μm)。
1.2.4 温度扫描测试(flow temperature ramp)
使用Discoery HR-3流变仪对蛋白饮料和增稠蛋白饮料进行20~80 ℃的表观黏度温度扫描测试,升降温速率均为5 ℃/min,升温结束后保留180 s,然后开始降温程序,剪切速率为50 s-1[18]。对样品裸露部分涂上一层硅油并用防蒸罩密封,防止水分蒸发。
样品测试均采用不锈钢平板(直径40 mm,测试间隙1 000 μm)。
1.2.5 多糖胶体无相互作用理论值计算
参照RAZAI等[19]和JO等[12]的方法,对XG-GG共混物体系无相互作用理论值φ进行计算,如公式(3)所示:
φ=ω1AXG+ω2AGG
(3)
式中:φ,共混物体系无相互作用理论值;ω1,XG在共混体系中总质量的比值;ω2,GG在共混体系中总质量的比值;AXG,XG单组分参数值;AGG,GG单组分参数值。
1.2.6 数据统计分析
采用TA instruments Trios进行数据采集、处理和拟合模式分析。所有的样品均为3次重复试验,结果用平均值±标准差表示,并用SPSS 17.0软件中的ANOA对数据进行显著性分析(P<0.05)。
2 结果与分析
2.1 XG和GG复配体系的流变特性研究
2.1.1 不同比例的XG-GG混合物的稳态剪切速率扫描和动态频率扫描
图1-a为不同比例下的XG-GG混合物的表观黏度与剪切速率的关系图。图中显示样品表观黏度均随着剪切速率的增加而减少,呈现剪切稀化特征。剪切稀化行为的产生是由于剪切作用破坏了多糖分子缠结的空间网状结构,且分子缠结的破坏速度大于缠结的恢复速度,造成了表观黏度的下降[20]。当黄原胶和瓜尔豆胶的比例为5∶5时,体系的表观黏度达到最大值,说明黄原胶和瓜尔豆胶之间存在协同相互作用。GRISEL等[21]认为可能是黄原胶的无序链段和半乳甘露聚糖的光滑区发生了相互作用,使得空间网状结构得到增强导致的。
动态黏弹性与多糖的品质息息相关,也能反应多糖内部的三维网状结构[18]。图1-b和图1-c显示不同复配比下XG-GG混合体系的G′、G″和tan δ(G″/G′)随角频率变化趋势。结果显示:黄原胶与瓜尔豆胶配比为5∶5时,复配体系的G′和G″均最大,其次是1∶9;样品的tan δ在低频下均大于1,说明其偏黏性特征,随着角频率的增大,tan δ值开始降低,并最终低于1,说明样品在高频下更偏弹性特征。
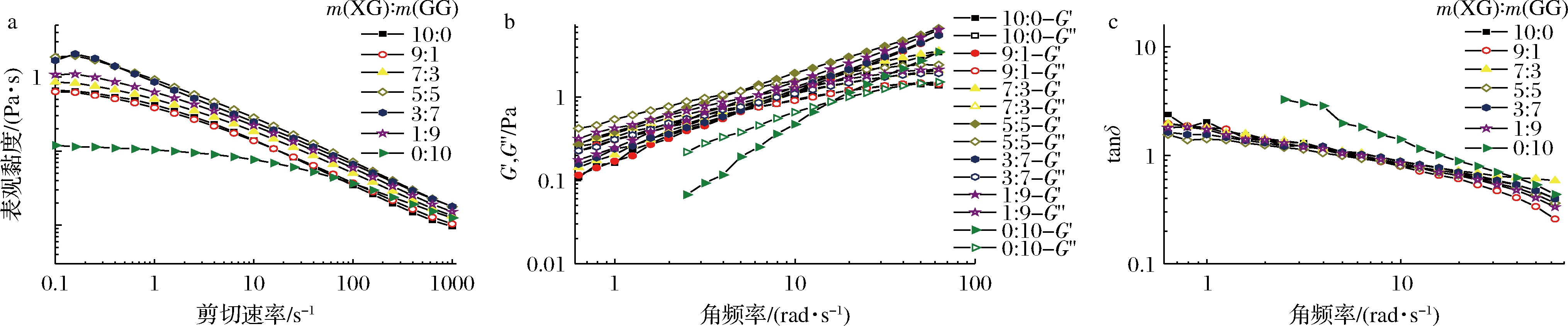
a-表观黏度;b-G′,G″;c-tan δ
图1 不同比例的XG-GG混合物的稳态和动态流变图
Fig.1 Steady-state and dynamic rheological diagrams of XG-GG mixtures in different mixing ratios
通过幂率模型Power-law计算得出每条曲线的稳态流变参数,如表1所示,其中K是指稠度系数,表示流体流动的难易程度,K值越高,说明流动越困难,而n值是一个没有量纲的参数,当n<1时,说明流体是具有剪切稀化特征的非牛顿流体,且n值越小,剪切稀化程度越高[22]。样品的n值处于0.40~0.56,远小于1,剪切稀化特征较明显。
表1 不同比例的XG-GG混合物的稳态和动态流变参数
Table 1 Steady and dynamic rheological parameters of XG-GG mixtures in different mixing ratios
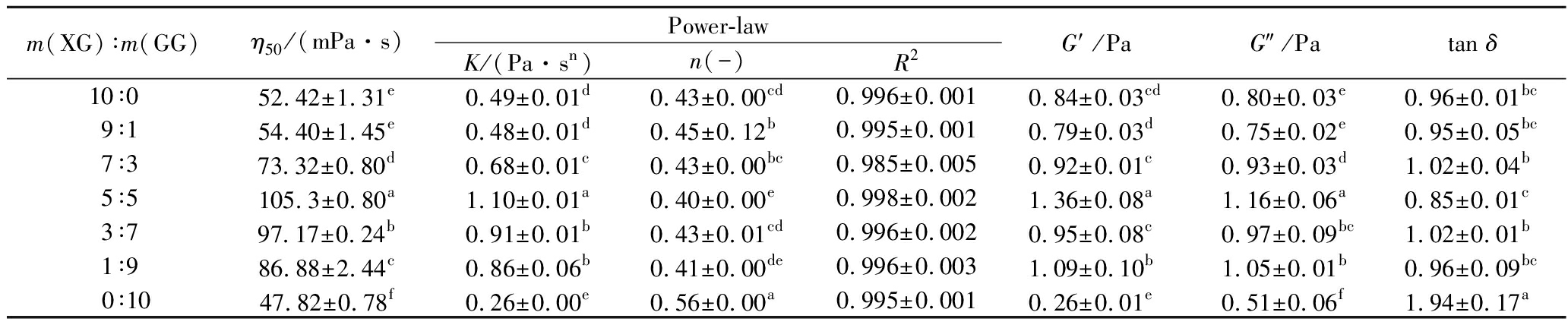
m(XG)∶m(GG)η50/(mPa·s)Power-lawK/(Pa·sn)n(-)R2G′ /PaG″ /Patan δ10∶052.42±1.31e0.49±0.01d0.43±0.00cd0.996±0.0010.84±0.03cd0.80±0.03e0.96±0.01bc9∶154.40±1.45e0.48±0.01d0.45±0.12b0.995±0.0010.79±0.03d0.75±0.02e0.95±0.05bc7∶373.32±0.80d0.68±0.01c0.43±0.00bc0.985±0.0050.92±0.01c0.93±0.03d1.02±0.04b5∶5105.3±0.80a1.10±0.01a0.40±0.00e0.998±0.0021.36±0.08a1.16±0.06a0.85±0.01c3∶797.17±0.24b0.91±0.01b0.43±0.01cd0.996±0.0020.95±0.08c0.97±0.09bc1.02±0.01b1∶986.88±2.44c0.86±0.06b0.41±0.00de0.996±0.0031.09±0.10b1.05±0.01b0.96±0.09bc0∶1047.82±0.78f0.26±0.00e0.56±0.00a0.995±0.0010.26±0.01e0.51±0.06f1.94±0.17a
注:表中不同字母表示同一列存在显著性差异(P<0.05),(下同)
剪切稀化对吞咽障碍的人群的饮食有积极作用,有研究表明高剪切稀化程度有利于减少吞咽障碍人群的误吸风险[16],较低的n值也能降低多糖在口腔中的黏稠感,增强口感舒适度[12]。当复配比例为5∶5时,n值达到最小值,假塑性特征最明显,同时,K和η50值也达到最大值,且远大于单独的黄原胶和瓜尔豆胶,有研究表明,较高的K和η50值能有效降低多糖在咽部的流动速度,减少误吸风险[4]。与单独的黄原胶和瓜尔豆胶相比,复配体系表现出的流动性能更佳。此外,表1显示不同比例下的XG-GG混合物在1.0 Hz下的G′、G″和tan δ。结果显示:复配比例为5∶5时,复配体系的G′和G″均最大,tan δ值最小,表明黄原胶和瓜尔豆胶在黏弹性方面也具有较强的协同增效作用。
2.1.2 黄原胶和瓜尔豆胶的协同相互作用
为了较为直观地观察出黄原胶和瓜尔豆胶是否具有协同作用及其最佳的复配比,将稳态和动态流变参数(K,η50,G′和G″)绘制成二元混合物中黄原胶所占比例的函数,如图2所示。图2中实线部分为二元混合物测量的实际值,虚线部分为二元混合物无相互作用的理论值。在不同的复配比下,测量值和理论值若出现正偏差,即测量值>理论值,证明体系存在协同增效作用;若出现负偏差,即测量值<理论值,证明体系存在拮抗作用。结果显示:当复配比例为9∶1时,K、η50和G′出现的正偏差并不明显,甚至G″出现了负偏差(拮抗作用),这可能是由于瓜尔豆胶的含量较低,黄原胶的无序链段与瓜尔豆胶光滑区的结合机会减少,使得协同作用不显著;除了9∶1外,K、η50、G′和G″测量的实际值与无相互作用的理论值均出现显著的正偏差,说明在稳态流变和黏弹性方面,黄原胶和瓜尔豆胶存在较为显著的协同相互作用,且最佳复配比为5∶5。
综上研究可知,黄原胶和瓜尔豆胶具有协同作用,且最佳复配比为5∶5,因此,选用黄原胶和瓜尔豆胶为主要原料,并用5∶5作为复配比,开发出了一种适用于吞咽障碍人群饮食增稠剂——增稠剂S,并将其作为研究对象做后续研究。
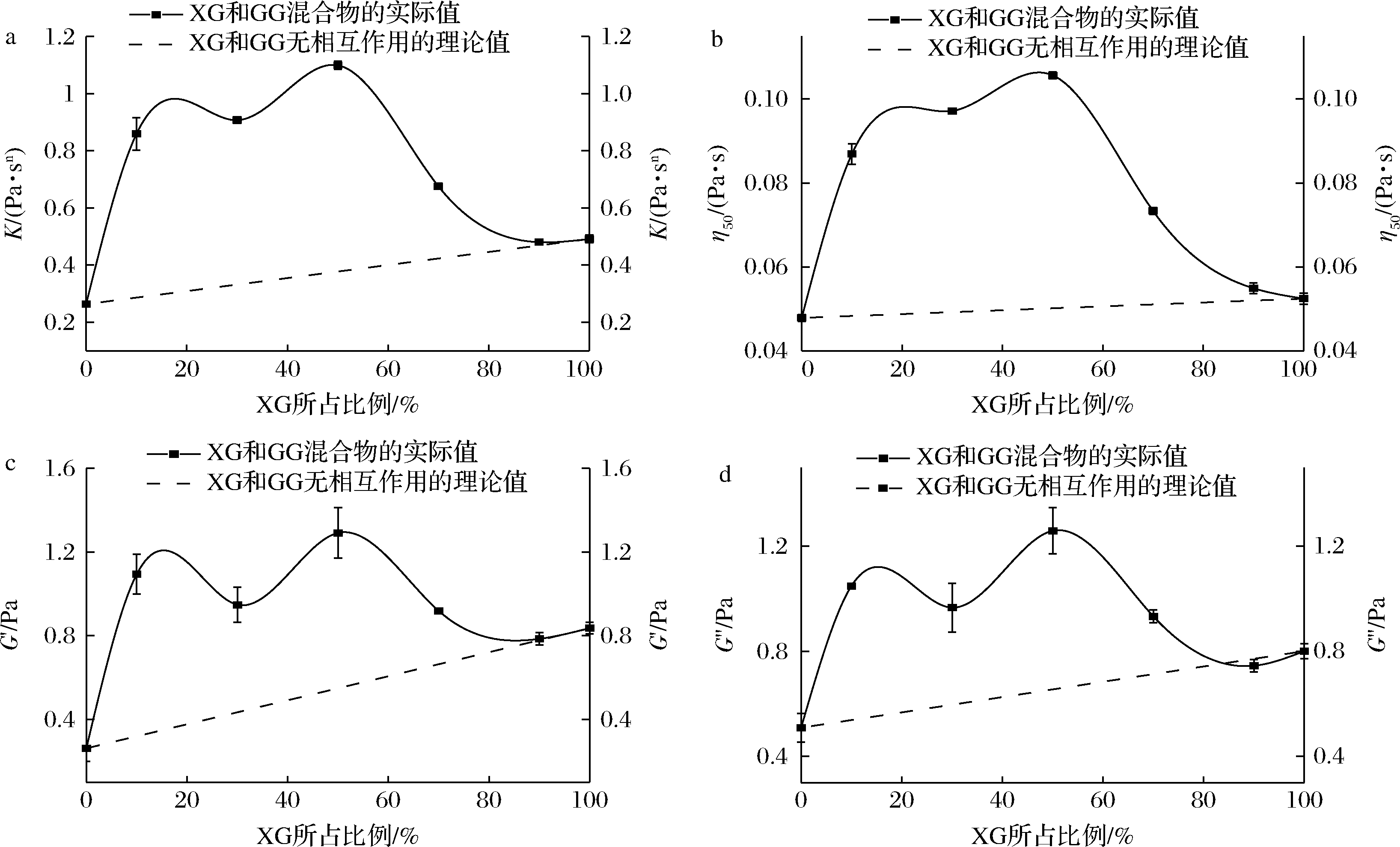
a-K;b-η50;c-G′;d-G″
图2 混合物的稳态和动态流变参数和黄原胶含量的关系
Fig.2 Plots of steady and dynamic shear rheological parameters ersus XG content of binary gum mixtures
2.2 温度和pH对增稠剂S溶液表观黏度和黏弹性的影响
温度对食品胶体的流变性质有一定影响。图3-a为不同温度下增稠剂S的稳态流变特性曲线。结果显示:样品的表观黏度随着剪切速率的增加均降低,呈现出明显假塑性特征,这是因为黄原胶具有刚性棒状结构和高分子质量,瓜尔豆胶具有长而刚性的链[12,23];低剪切速率下(0.1~1.0 s-1),增稠剂S在不同温度下的表观黏度差异显著(P<0.05),这是因为随着温度的升高,特别是在60、80 ℃时,黄原胶的大部分有序构象转变成无序构象,黄原胶和瓜尔豆胶分子运动加剧,胶体分子链间的摩擦力减少,导致增稠剂S的表观黏度迅速降低[24]。但在50 s-1下,20、40 ℃的表观黏度无显著性差异,到60 ℃时,表观黏度稍微下降,80 ℃的表观黏度下降显著。考虑到高于60 ℃的液体会对吞咽障碍患者口腔和咽部造成烫伤,提高患癌风险[25],因此认为吞咽障碍患者吞咽液体一般不超过60 ℃。而增稠剂S在20~60 ℃具有良好的热稳定性,因此增稠剂S在热水中也适用。
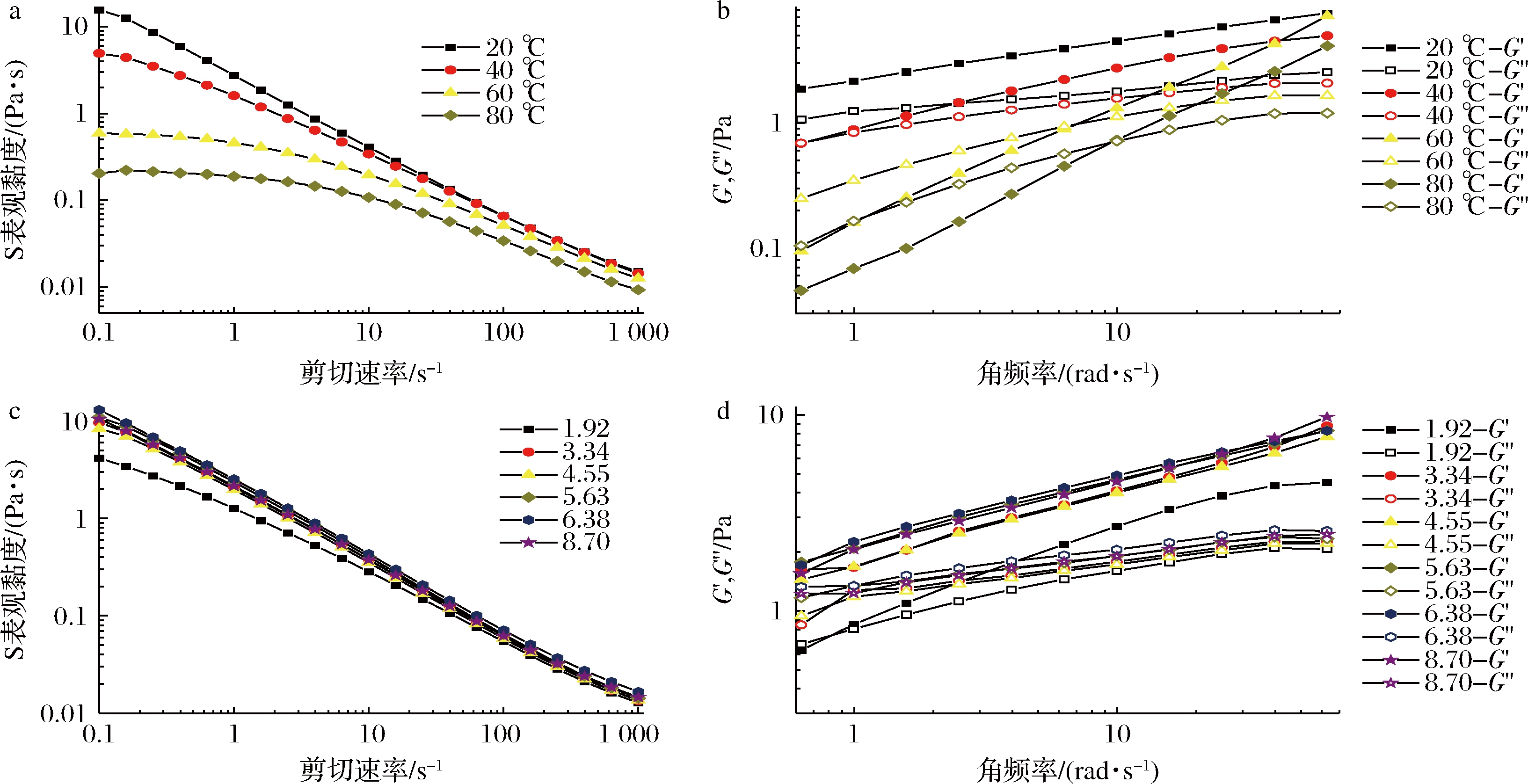
a-温度对表观黏度的影响;b-温度对G′,G″的影响;c-pH对表观黏度的影响;d-pH对G′,G″的影响
图3 温度和pH对增稠剂S的表观黏度、G′和G″的影响
Fig.3 Effect of temperature and pH on apparent iscosity, G′ and G″ of thickener S
胶体的黏弹性与内聚性有一定的相关性,而胶体的内聚性能够使其在吞咽的时候避免液珠分散,降低误吸风险[26]。因此,研究温度对增稠剂弹性模量和黏性模量的影响。图3-b中可以看出,随着温度的升高,增稠剂S的模量逐渐降低。在20和40 ℃时,增稠剂S的G′ 始终大于 G″,此时的溶液更偏弹性性质。当温度为60和80 ℃时,低频率下的G′ 小于G″,随着振动频率的增大,弹性模量和黏性模量出现交点,此时损耗正切值tan δ =1,为溶胶与弱凝胶的分界点,随着振动频率的继续增大,G′>G″。CHUN等[27]在研究黄原胶的动态黏弹性时也发现了类似的现象,认为是胶体的分子链解纠缠的滞后性使分子链形成了空间网络结构,造成了在低频下表现出液体性质而在高频下表现出弹性体性质。此外,温度的升高会使交点往高频率方向移动,说明温度升高对增稠剂S中的黄原胶和瓜尔豆胶网状结构造成了破坏[24]。
本文研究了pH值在1.92~8.70的增稠剂流变行为的变化,因为市场上常见的饮料都在此范围内,比如豆浆、牛奶、果汁和茶等。由图3-c可知,在所测pH范围内样品溶液均表现剪切稀化的假塑性特征。当pH为1.92时,增稠剂S的表观黏度稍有下降,而其他pH下的增稠剂S的表观黏度曲线几乎重叠在一起。据报道,黄原胶具有较强的pH稳定性,但在极低的pH值下(pH<2),黄原胶表面的电荷密度发生变化, 黄原胶分子之间的缔合受到影响,且在强酸性条件下黄原胶分子会发生一定程度的水解,造成表观黏度下降[28]。而我们发现,当pH为1.92~8.70时,瓜尔豆胶的表观黏度和黏弹模量无显著性差异(文中未展示),说明在强酸条件下(pH 1.92),增稠剂S表观黏度的下降是由于黄原胶结构被破坏导致复配体系的协同作用减弱。
在图3-d中,样品的G′和G″曲线斜率均为正值,且G′大于G″,即tan δ<1,表现为弱凝胶行为。在一些研究报道中,tan δ<1被视为吞咽障碍人群食品的流变学标准[12]。图中pH对G′和G″的影响呈现出和表观黏度相似的规律。在极端pH值(1.92)下,溶液的弹性模量相对较低,说明该酸性条件下,黄原胶水解导致其与瓜尔豆胶形成的内部网状结构发生了破坏。在pH值为3.34~8.70,溶液的G′和G″几乎没有变化,说明在此范围内,XG-GG复配体系的黏弹性具有较强稳定性。
2.3 蛋白饮料对增稠剂S溶液表观黏度和黏弹性的影响
2.3.1 增稠蛋白饮料的稳态流变特性、黏弹性和屈服应力
图4为增稠剂S增稠蛋白饮料的稳态流变特性曲线图。结果显示,样品的表观黏度均具有强剪切稀化的特征;随着浓度的增加,样品的表观黏度逐渐增加。表2中比较了在25 ℃下增稠剂S增稠豆浆和牛奶的流变参数差异(K、n和η50值)。整体而言,拟合的相关系数(R2)非常高,为0.992~0.999。同一食品饮料基质,随着增稠剂浓度的增大,η50和K值逐渐增大,n值逐渐减少,说明增加浓度会增加增稠饮料的表观黏度和剪切稀化程度。同一增稠剂浓度,不同食品基质中,高脂牛奶的η50最大,因为脂肪使其水相中的增稠剂浓度更高[29]。同一增稠剂浓度,高脂牛奶的n最小,说明增稠高脂牛奶的剪切稀化程度最高。另外,在质量浓度10和20 g/L下,增稠脱脂牛奶和增稠豆浆的K值和η50无显著差异。不同食品基质中增稠剂S表现出不同的稳态流变性质是由于增稠剂S与不同的大分子(如大豆蛋白、酪蛋白、脂肪等)发生相互作用导致的。
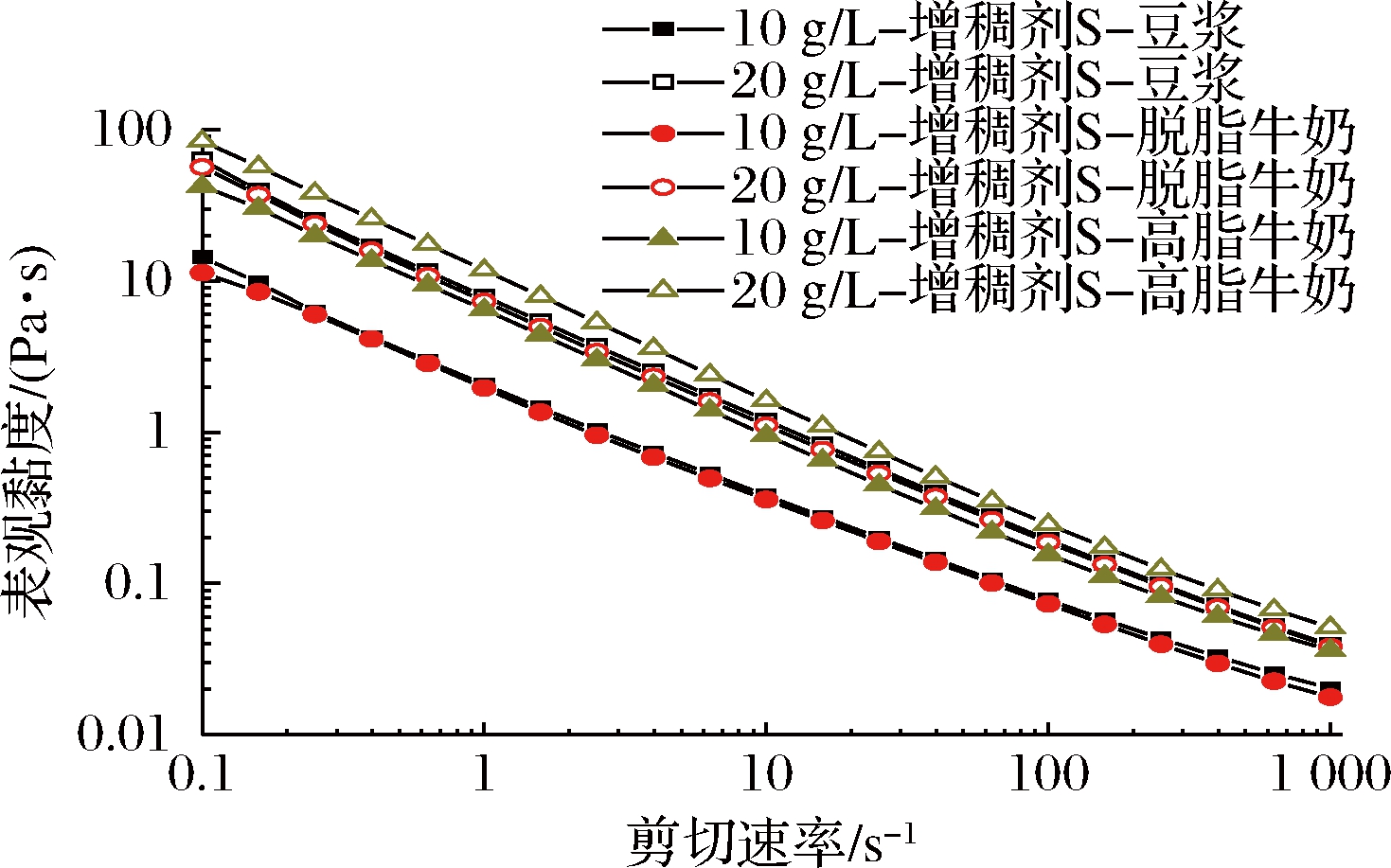
图4 增稠剂S增稠豆浆、脱脂牛奶和高脂 牛奶的稳态流变特性
Fig.4 Steady state rheology, iscoelasticity and elastic stress of thickened soybean milk, skimmed milk and high-fat milk with thickener S
表2 不同浓度的增稠剂在蛋白饮料中的稳态流变参数(25 ℃)
Table 2 Steady-state rheological parameters of different concentrations of thickeners in protein beerages (25 ℃)
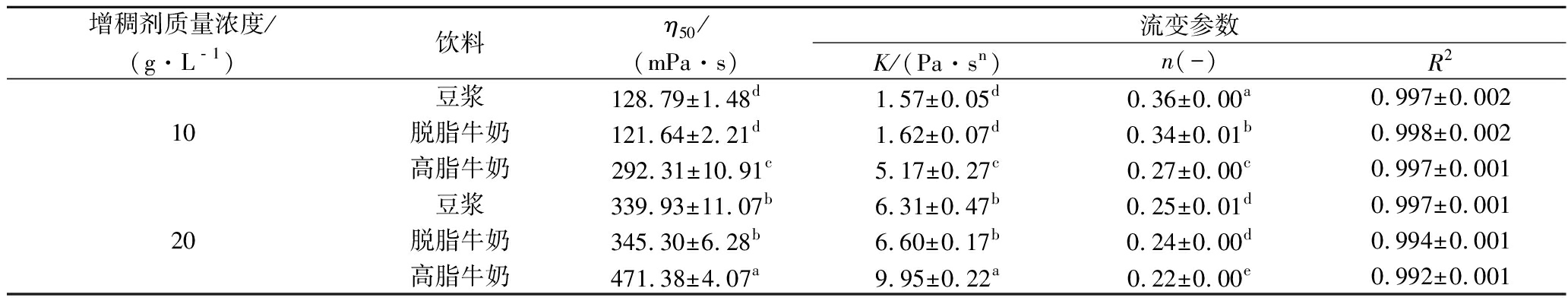
增稠剂质量浓度/(g·L﹣1)饮料η50/(mPa·s)流变参数K/(Pa·sn)n(-)R210豆浆128.79±1.48d1.57±0.05d0.36±0.00a0.997±0.002脱脂牛奶121.64±2.21d1.62±0.07d0.34±0.01b0.998±0.002高脂牛奶292.31±10.91c5.17±0.27c0.27±0.00c0.997±0.00120豆浆339.93±11.07b6.31±0.47b0.25±0.01d0.997±0.001脱脂牛奶345.30±6.28b6.60±0.17b0.24±0.00d0.994±0.001高脂牛奶471.38±4.07a9.95±0.22a0.22±0.00e0.992±0.001
图5-a展示动态应变对不同蛋白增稠饮料的黏弹性的影响。结果显示,3种增稠蛋白饮料都具有较宽的线性黏弹区(0.1%~20.0%),表明系统中存在较强的物理纠缠网络,在一定应变范围内(0.1%~20.0%)能抵抗变形,当应变继续增大,物理纠缠网络被破坏,弹性模量降低;在线性黏弹区内,3种增稠蛋白饮料的G′大于G″,即tan δ<1,表现出类固体特征;弹性模量的大小:高脂牛奶>脱脂牛奶>豆浆,说明增稠高脂牛奶具有强的物理纠缠网络结构,增稠的效果最好。
屈服应力是与材料内部网络结构有关的重要流变学表征参数,已经被认为是吞咽困难食物的“流变学准则”[17]。屈服应力表示流体开始流动时所需要的最小剪切力,如果施加的力在屈服应力之下,则舌头不能移动食团[1,30]。图5-b显示质量浓度为20 g/L增稠剂增稠不同蛋白饮料的弹性应力(弹性模量/动态应变)与动态应变的关系,曲线最大值为样品的屈服应力。增稠豆浆、增稠脱脂牛奶和增稠高脂牛奶的屈服应力分别为920.67、1 073.49、1 567.16 Pa,说明增稠高脂牛奶内部具有最强的物理纠缠网络结构,需要较大的剪切力才能克服其内部结构。
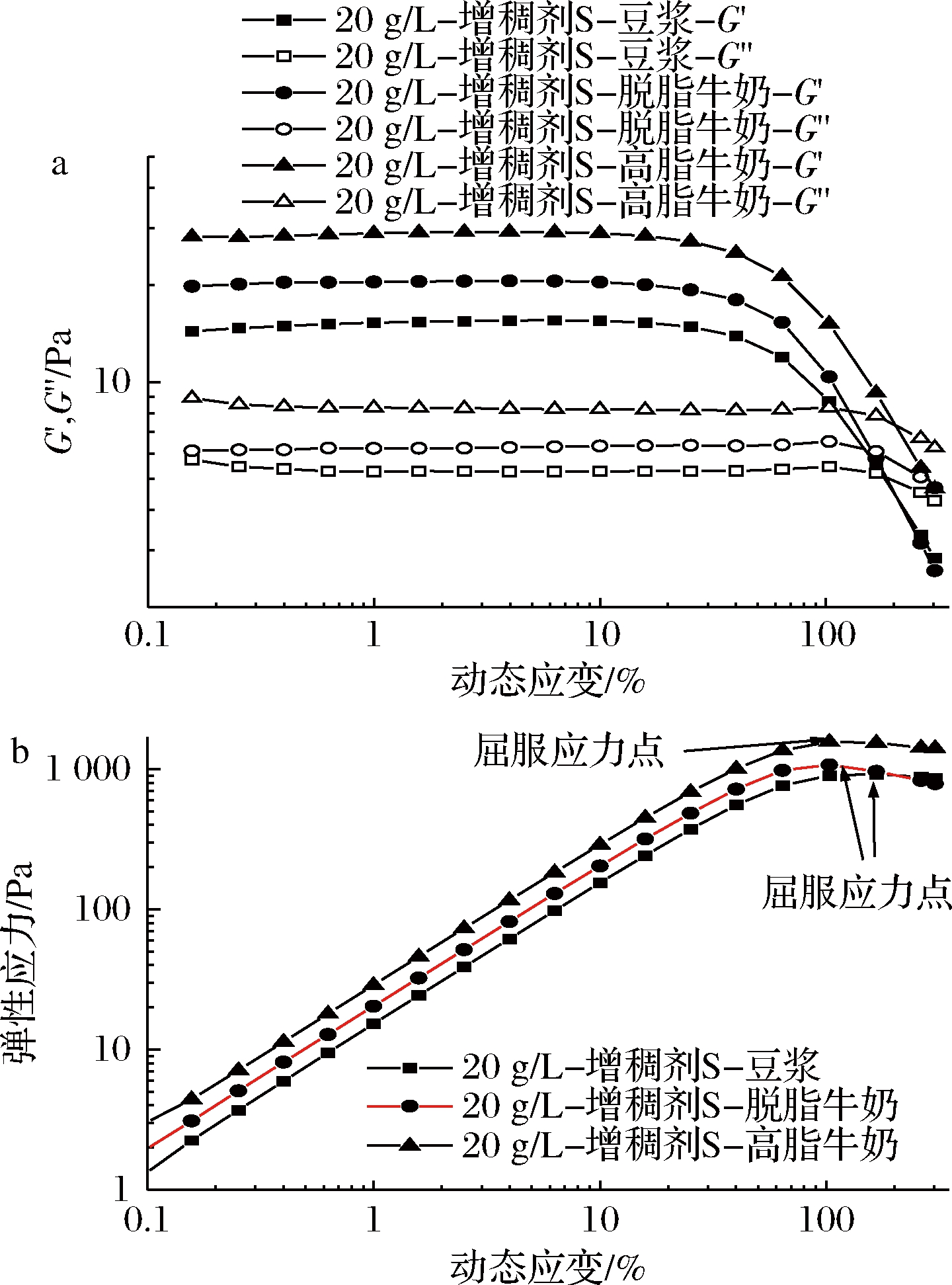
a-黏弹性;b-屈服应力
图5 增稠剂S增稠豆浆、脱脂牛奶和高脂牛奶的 黏弹性和屈服应力
Fig.5 iscoelasticity and elastic stress of thickened soybean milk, skimmed milk and high-fat milk with thickener S
综上,说明食品增稠剂在不同的食品基质中表现出不同的流变特性,吞咽障碍患者使用食品增稠剂辅助吞咽时,应该考虑到食品基质的种类对食品增稠剂增稠效果的影响。
2.3.2 温度对增稠蛋白饮料表观黏度的影响
在中国,热豆浆和热牛奶深受人们喜爱,因此研究温度对蛋白热饮的流变性质的影响是非常有现实意义的。由图6-a可知,表观黏度最大的是增稠高脂牛奶,其次是增稠脱脂牛奶,最低的是增稠豆浆。增稠豆浆表观黏度随着温度的增加逐渐减少,这是因为温度升高,分子运动加剧,分子间的部分氢键被破坏,溶液更易流动。但在增稠牛奶时,脱脂和高脂的升温曲线均会出现表观黏度增加的明显拐点(曲线一阶导数的零点),其中高脂牛奶在46 ℃附近出现拐点,脱脂牛奶在56 ℃附近出现拐点,这说明是否出现拐点与脂肪的含量无关,但猜测脂肪可能使拐点向低温区移动。KHOURYIEH等[31]研究温度对黄原胶和瓜尔豆胶的相互作用影响时,发现当温度升高至黄原胶的构象转变温度时,黄原胶无序化程度增强,黄原胶和瓜尔豆胶会发生更多的相互作用,使表观黏度增加,这可能是增稠牛奶出现拐点的原因。但是,从图6-b中可看出,黄原胶和瓜尔豆胶增稠高脂牛奶均出现表观黏度增加的拐点,拐点出现的位置在42~45 ℃。而图6-c中不添加任何胶体的高脂牛奶升温曲线并没有出现拐点,这说明黄原胶和瓜尔豆胶两种胶体都可能与牛奶中的一些大分子物质(酪蛋白、乳清蛋白等)发生了相互作用,并不是简单的黄原胶和瓜尔豆胶协同作用增强使得体系表观黏度增加[32]。

a-增稠剂S增稠蛋白饮料;b-XG-GG增稠高脂牛奶;c-高脂牛奶
图6 10 g/L的增稠蛋白饮料及高脂牛奶的表观黏度随温度变化的关系
Fig.6 Apparent iscosity of thickened protein beerages with thickeners S, XG and GG and high-fat milk ersus temperature concentration of 10 g/L
当温度降低时,断裂的氢键重新形成,增稠豆浆和增稠牛奶的表观黏度开始增加,甚至超过了升温时的表观黏度,表现出滞后性,这是由于降温有利于氢键的重新形成和分子结构的重新调整,使得流体在剪切过程中受到更多的阻力[33]。
3 结论与讨论
本文研究了黄原胶和瓜尔豆胶复配体系的流变特性,发现黄原胶和瓜尔豆胶存在协同增效作用,最佳复配比为5∶5,并以此复配比开发出一种适用于吞咽障碍人群饮食胶基增稠剂S。在此基础上,研究了温度、pH和蛋白饮料基质对吞咽障碍胶基增稠剂S流变性质的影响。研究发现:由于原料黄原胶和瓜尔豆胶的共同作用,胶基增稠剂S具有良好的温度、pH稳定性;增稠高脂牛奶的表观黏度η50最高、n值最低;从20 ℃升温到80 ℃过程中,质量浓度为10 g/L的增稠剂S在蛋白热饮中的表观黏度均高于59.74 mPa·s。综上所得,吞咽障碍胶基增稠剂具有良好的耐酸性和耐热性,且在蛋白热饮中也有良好的适用性。本文中的流变学性质研究虽然无法解释复杂吞咽过程中的所有现象,但对吞咽障碍增稠剂正确的临床使用具有很大的参考价值,为增稠剂在不同溶液环境中的安全应用提供理论数据支撑和应用指导,也为开发相关的特殊医学用途配方食品提供参考。
[1] WEI Y Y, GUO Y L, LI R Q, et al.Rheological characterization of polysaccharide thickeners oriented for dysphagia management:Carboxymethylated curdlan, konjac glucomannan and their mixtures compared to xanthan gum[J].Food Hydrocolloids, 2021, 110:106198.
[2] 陈建设, 王鑫淼.食品口腔加工研究的发展与展望[J].中国食品学报, 2018, 18(9):1-7.
CHEN J S, WANG X M.Deelopment and outlook of food oral processing research[J].Journal of Chinese Institute of Food Science and Technology, 2018, 18(9):1-7.
[3] ZARGARAAN A, RASTMANESH R, FADAI G, et al.Rheological aspects of dysphagia-oriented food products:A mini reiew[J].Food Science and Human Wellness, 2013, 2(3-4):173-178.
[4] TORRES O, YAMADA A, RIGBY N M, et al.Gellan gum:A new member in the dysphagia thickener family[J].Biotribology, 2019, 17:8-18.
[5] 陈伟, 陈建设.食品的质构及其性质[J].中国食品学报, 2021, 21(1):377-384.
CHEN W, CHEN J S.Food texture and properties[J].Journal of Chinese Institute of Food Science and Technology, 2021, 21(1):377-384.
[6] 吴君波, 王珂, 杨光, 等.改善吞咽功能食品增稠剂的研究[J].工业微生物, 2019, 49(3):38-45.
WU J B, WANG K, YANG G, et al.Food thickener for improing swallowing function[J].Industrial Microbiology, 2019, 49(3):38-45.
[7] LEONARD R J, WHITE C, MCKENZIE S, et al.Effects of bolus rheology on aspiration in patients with dysphagia[J].Journal of the Academy of Nutrition and Dietetics, 2014, 114(4):590-594.
[8] CLAÉ P, DE KRAA M, ARREOLA , et al.The effect of bolus iscosity on swallowing function in neurogenic dysphagia[J].Alimentary Pharmacology & Therapeutics, 2006, 24(9):1 385-1 394.
[9] GARCIA J M, CHAMBERS E 4th, MATTA Z, et al.iscosity measurements of nectar- and honey-thick liquids:Product, liquid, and time comparisons[J].Dysphagia, 2005, 20(4):325-335.
[10] IEIRA J M, OLIEIRA F D Jr, SALARO D B, et al.Rheology and soft tribology of thickened dispersions aiming the deelopment of oropharyngeal dysphagia-oriented products[J].Current Research in Food Science, 2020, 3:19-29.
[11] MART NEZ O, ICENTE M S, DE EGA M C, et al.Sensory perception and flow properties of dysphagia thickening formulas with different composition[J].Food Hydrocolloids, 2019, 90:508-514.
NEZ O, ICENTE M S, DE EGA M C, et al.Sensory perception and flow properties of dysphagia thickening formulas with different composition[J].Food Hydrocolloids, 2019, 90:508-514.
[12] JO W, BAK J H, YOO B.Rheological characterizations of concentrated binary gum mixtures with xanthan gum and galactomannans[J].International Journal of Biological Macromolecules, 2018, 114:263-269.
[13] AHMED J.Effect of pressure, concentration and temperature on the oscillatory rheology of guar gum dispersions:Response surface methodology approach[J].Food Hydrocolloids, 2021, 113:106554.
[14] 苏明松. 老年吞咽障碍患者特殊液体膳食质构等级评测与临床测试[D].杭州:浙江工商大学, 2018.
SU M S.Texture standarization and characterization of liquid foods for elderly dysphagia and clinical test[D].Hangzhou:Zhejiang Gongshang Uniersity, 2018.
[15] CHO H M, YOO B.Rheological characteristics of cold thickened beerages containing xanthan gum-based food thickeners used for dysphagia diets[J].Journal of the Academy of Nutrition and Dietetics, 2015, 115(1):106-111.
[16] NISHINARI K, TAKEMASA M, SU L, et al.Effect of shear thinning on aspiration - Toward making solutions for judging the risk of aspiration[J].Food Hydrocolloids, 2011, 25(7):1 737-1 743.
[17] NAKAUMA M, ISHIHARA S, FUNAMI T, et al.Swallowing profiles of food polysaccharide solutions with different flow behaiors[J].Food Hydrocolloids, 2011, 25(5):1 165-1 173.
[18] 曾瑞琪, 李苇舟, 赵欣, 等.魔芋胶-黄原胶复配体系流变学特性及其凝胶形成动力学分析[J].食品科学, 2018, 39(9):39-46.
ZENG R Q, LI W Z, ZHAO X, et al.Rheological properties and gelation kinetics of konjac gum-xanthan gum mixtures[J].Food Science, 2018, 39(9):39-46.
[19] RAZAI S M A, ALGHOONEH A.Understanding the physics of hydrocolloids interaction using rheological, thermodynamic and functional properties:A case study on xanthan gum-cress seed gum blend[J].International Journal of Biological Macromolecules, 2020, 151:1 139-1 153.
[20] 李慧, 关健, 盛桂华, 等.适用于吞咽困难的特定全营养医用食品的流变特性研究[J].现代食品科技, 2019, 35(3):106-110;94.
LI H, GUAN J, SHENG G H, et al.Rheological properties of specific complete nutrition medical foods for dysphagia[J].Modern Food Science and Technology, 2019, 35(3):106-110;94.
[21] GRISEL M, AGUNI Y, RENOU F, et al.Impact of fine structure of galactomannans on their interactions with xanthan:Two co-existing mechanisms to explain the synergy[J].Food Hydrocolloids, 2015, 51:449-458.
[22] LIN S Y, LIU X E, CAO Y, et al.Effects of xanthan and konjac gums on pasting, rheology, microstructure, crystallinity and in itro digestibility of mung bean resistant starch[J].Food Chemistry, 2021, 339:128001.
[23] ACHAYUTHAKAN P, SUPHANTHARIKA M.Pasting and rheological properties of waxy corn starch as affected by guar gum and xanthan gum[J].Carbohydrate Polymers, 2008, 71(1):9-17.
[24] HABIBI H, KHOSRAI-DARANI K.Effectie ariables on production and structure of xanthan gum and its food applications:A reiew[J].Biocatalysis and Agricultural Biotechnology, 2017, 10:130-140.
[25] ISLAMI F, BOFFETTA P, REN J S, et al.High-temperature beerages and foods and esophageal cancer risk:A systematic reiew[J].International Journal of Cancer, 2009, 125(3):491-524.
[26] NISHINARI K, TURCANU M, NAKAUMA M, et al.Role of fluid cohesieness in safe swallowing[J].Npj Science of Food, 2019, 3:5.
[27] CHUN M S, KIM C, LEE D E.Conformation and translational diffusion of a xanthan polyelectrolyte chain:Brownian dynamics simulation and single molecule tracking[J].Physical Reiew.E, Statistical, Nonlinear, and Soft Matter Physics, 2009, 79(5 Pt 1):051919.
[28] YOON S N, YOO B.Effect of pH on rheological properties of dysphagia-oriented thickened water[J].Preentie Nutrition and Food Science, 2016, 21(1):73-77.
[29] HADDE E K, NICHOLSON T M, CICHERO J A Y.Rheological characterisation of thickened fluids under different temperature, pH and fat contents[J].Nutrition & Food Science, 2015, 45(2):270-285.
[30] ZARIM N A, ZAINUL ABIDIN S, ARIFFIN F.Shelf life stability and quality study of texture-modified chicken rendang using xanthan gum as thickener for the consumption of the elderly with dysphagia[J].Food Bioscience, 2021, 42:101054.
[31] KHOURYIEH H A, HERALD T J, ARAMOUNI F, et al.Influence of mixing temperature on xanthan conformation and interaction of xanthan-guar gum in dilute aqueous solutions[J].Food Research International, 2006, 39(9):964-973.
[32] 王翠娜. 聚合乳清蛋白与多糖相互作用对其凝胶特性影响及应用[D].长春:吉林大学, 2015.
WANG C N.Interactions between polymerized whey protein and polysaccharides and its impact on the gelation properties and application[D].Changchun:Jilin Uniersity, 2015.
[33] 赵小敏. 可德胶多糖及其羧甲基衍生物的凝胶性能和流变学研究[D].上海:上海交通大学, 2017.
ZHAO X M.Rheological properties and gelation mechanism of curdlan and its carboxymethylated deriatie[D].Shanghai:Shanghai Jiao Tong Uniersity, 2017.