世界卫生组织建议在婴儿出生后的6个月进行纯母乳喂养[1],但母乳喂养受多重因素的影响,在某些情况下无法实现全母乳喂养或者不得不中断母乳喂养[2]。婴幼儿配方粉是替代母乳实施人工喂养婴幼儿的唯一营养来源,其营养品质和功能特性对婴幼儿的生长发育及健康体质十分重要。然而,为了保证食用安全性及长货架期,婴配粉往往经历比常规乳制品更强烈的热处理[3]。热处理虽能达到杀菌和制粉的目的,但也会对婴配粉的营养价值和食用安全性产生一定的不利影响[4]。
美拉德反应是乳制品热处理过程中重要的化学变化之一,它是以乳蛋白赖氨酸的糖基化为主要反应并交互作用形成复杂产物的特定羰氨褐变反应,也可以称之为非酶褐变。婴配粉中富含蛋白质和还原糖,因此极易发生美拉德反应。该反应主要有早、中、晚3个过程,糠氨酸是早期反应的主要指示物。糠醛化合物和α-二羰基化合物是中期反应的主要产物[5]。糖基化终末产物(advanced glycation end products, AGEs),是由BROWNLEE等[6]提出的概念,用于描述美拉德反应晚期的产物,N-ε-羧甲基-L-赖氨酸[N-ε(carboxymethyl)lysine,CML]和N-ε-羧乙基-L-赖氨酸[N-ε(carboxyethyl)lysine,CEL]是乳制品中常见的美拉德晚期糖基化产物。AGEs可能会对人体心血管、肾脏造成一定的影响[7],也有可能促进炎症的发生[8],在糖尿病和尿毒症中发挥重要的病理生理学作用[9]。
美拉德反应的影响因素有很多,比如贮藏温度、贮藏时间、pH等[10]。本研究主要通过测定市售婴配粉中不同阶段美拉德反应产物糠氨酸、5-羟甲基糠醛(5-hydroxymethylfurfural,5-HMF)、乙二醛、丙酮醛、2,3-丁二酮、CML以及CEL含量的变化,调研不同品牌婴配粉美拉德副产物含量及贮藏过程中美拉德副产物的变化规律,用于指导提高市售婴配粉的质量和安全性。
1 材料与方法
1.1 试剂与设备
糠氨酸盐酸盐标准品,上海安谱实验科技有限公司;乙二醛、丙酮醛、2,3-丁二酮标准品、CML标准品、羧乙基赖氨酸标品(CEL),美国Sigma公司;5-HMF标准品,上海摩贝试剂公司;甲醇(色谱纯)、乙腈(色谱级)、甲酸(色谱纯)、浓盐酸(密度 1.19 g/mL)、三氟乙酸(色谱纯)、乙酸铵,北京国药有限公司;Ⅰ段婴幼儿配方粉,北京各大超市。
YQ107-02超高效液相色谱仪,美国Waters公司;DHG-9123A电热恒温鼓风干燥箱,上海精宏实验设备有限公司;2300全自动凯氏定氮仪,安捷伦科技丹麦FOSS;3K15离心机,德国Sigma公司;Model 680 酶标仪,美国Bio-Rad公司。
1.2 样品制备
Ⅰ段婴幼儿配方粉包括6种国内品牌和8种国外品牌,婴配粉的信息包括蛋白质含量、生产日期以及生产原材料等。具体样品信息如表1所示。
表1 样品信息表
Table 1 Sample information sheet

编号品牌编号蛋白质含量/%乳糖含量/%脂肪含量/%生产日期原始材料1国产奶粉(D1)11.556.326.5201911生牛乳2国产奶粉(D2)11.554.027.0201911生牛乳3国产奶粉(D3)11.152.327.9201911全脂奶粉、脱脂奶粉4国产奶粉(D4)9.8657.627.7201911脱脂乳粉5国产奶粉(D5)10.654.926.4201910生牛乳6国产奶粉(D6)10.555.425.0201911高油乳清粉7进口奶粉(I1)10.654.027.0201910脱脂乳粉8进口奶粉(I2)10.1554.1727.27201911脱脂乳粉9进口奶粉(I3)11.553.527.0201911脱脂牛乳10进口奶粉(I4)10.450.426.5201910脱脂牛乳11进口奶粉(I6)11.654.025.5201910高油乳清粉、全脂奶粉12进口奶粉(I7)10.450.426.5201910脱脂牛乳13进口奶粉(I8)11.055.625.7201910脱脂牛乳14进口奶粉(I9)11.055.225.0201910脱脂牛乳
1.3 糠氨酸和赖氨酸的测定
参照NY/T 939—2016《巴氏杀菌乳和UHT灭菌乳中复原乳的测定》,改变部分条件进行测定。称取1.5 g样品于水解管中,加2 mL蒸馏水进行溶解,加入10.6 mol/L HCl溶液6 mL,混合均匀,在110 ℃下加热水解18~24 h。取出样品冷却后过滤,滤液待测。取2 mL样品水解液,按照GB 5009.5—2016《食品安全国家标准 食品中蛋白质的测定》中的凯氏定氮法测定样品溶液中的蛋白质含量。将1 mL水解液与5 mL质量浓度6 g/L的乙酸铵溶液混匀以后用0.22 μm水相滤膜过滤,经UHPLC测定,按照外标法进行定量检测。
色谱条件:色谱柱:HSST3(100 mm×4.6 mm,2.5 μm);柱温35 ℃;检测波长280 nm;流动相:0.1%三氟乙酸水溶液为流动相A,甲醇为流动相B;洗脱条件:流速0.5 mL/min;B相梯度洗脱程序:0~8 min,0%~13.2%;8~8.5 min,13.2%~100%;8.5~10 min,100%~0%;10~12 min,0%。
牛奶中发现的赖氨酸阻滞物为Amadori化合物形式,不能被消化,称为“封闭赖氨酸”,封闭的或糖基化的赖氨酸降低了赖氨酸在代谢过程中的生物利用度,这意味着牛乳营养价值的损失[11]。参考BOSCH等[12]的计算方法,利用全自动氨基酸分析仪测定样品中赖氨酸的含量,并计算封闭赖氨酸的含量,来指示赖氨酸的损失程度,计算如公式(1)所示:
封闭赖氨酸含量/%=

(1)
式中:M赖,赖氨酸的相对分子质量,146.19 Da;M糠,糠氨酸相对分子质量,254.28 Da;ω(糠), 糠氨酸含量;ω(赖),赖氨酸含量。
1.4 5-HMF的测定
按照NY/T 1332—2007《乳与乳制品中5-羟甲基糠醛含量的测定 高效液相色谱法》测定。分别称取2 g婴配粉样品于50 mL离心管中,加7.3 mL水溶解,向各样品离心管中加入5 mL草酸溶液混匀,80 ℃水浴加热30 min,冷却至室温,再加入10 mL甲醇混匀后加入3 mL亚铁氰化钾和3 mL乙酸锌混匀,振摇后静置15 min,然后将样液以6 000 r/min离心10 min,将上清液置于50 mL容量瓶中,沉淀中加入10 mL甲醇,6 000 r/min离心10 min,合并2次上清液,滤纸过滤后用甲醇定容至50 mL,用0.22 μm的有机滤膜过滤待测。
色谱条件:色谱柱:C18(250 mm×4.6 mm,5 μm);柱温30 ℃;检测波长284 nm;流动相:甲醇为流动相A,水为流动相B;洗脱条件:流速0.8 mL/min;洗脱程序:甲醇与水按照15%和85%等度洗脱。
1.5 α-二羰基化合物的测定
参照毕日秀等[13] 的方法进行测定。分别配制不同浓度的乙二醛、丙酮醛、2,3-丁二酮3种化合物的标准溶液,取1 mL进行衍生反应,加入10 mg/mL的邻苯二胺水溶液300 μL,在60 ℃水浴(50 r/min)条件下反应30 min,冰水冷却后经过0.22 μm有机滤膜过滤,上样测定,分别绘制目标物的线性标准曲线。称取1 g样品溶解,加2 mL蒸馏水于15 mL离心管中,加入8 mL甲醇,涡旋振荡1 min,离心15 min(10 000 r/min)使蛋白沉淀,上清液备用。取3 mL上清液于密封棕色瓶中,加入400 μL邻苯二胺水溶液(10 mg/mL),60 ℃水浴振荡30 min。后经0.22 μm有机滤膜过滤,进行UHPLC。
色谱条件:色谱柱:HSST3(100 mm×4.6 mm,2.5 μm);柱温35 ℃;检测波长320 nm;流动相:0.1%甲酸水溶液为流动相A,乙腈为流动相B;洗脱条件:流速0.3 mL/min;B相梯度洗脱程序,0~15 min,20%~30%;15~18 min,30%~50%;18~22 min,50%~80%;22~30 min,80%;30~32 min,80%~20%;32~35 min,20%。
1.6 CEL、CML测定
参照贾晓迪[14]的方法,稍作修改进行测定。称取0.4 g样品,加3 mL正己烷脱脂3次,晾干;加1 mL硼氢化钠溶液和1.5 mL硼酸盐缓冲溶液,4 ℃还原12 h,随后缓慢加入 0.5 mL 20%的三氯乙酸终止反应,再以10 000 r/min离心10 min使蛋白沉淀,除去上清液后将沉淀蛋白用4 mL 6 mol/L的盐酸溶解,氮吹 1 min后封管,置于110 ℃的烘箱中水解24 h备用。水解后的样品经N2吹干,用超纯水复溶后过固相萃取柱净化,收集样液并过0.22 μm水相滤膜上样测定。
色谱条件:色谱柱:HSST3(100 mm×4.6 mm,2.5 μm);检测波长320 nm;流动相:0.1%甲酸水溶液为流动相A,乙腈为流动相B;洗脱条件:流速0.3 mL/min;进样量5 μL;B相梯度洗脱程序,0~2 min,10%~90%;2~3 min,90%;3~4 min,90%~10%;4~5 min,10%。
质谱条件:在正电离模式下运行:源温度110 ℃,脱溶剂气温度400 ℃,碰撞气流0.15 mL/min,脱溶剂气体流量600 L/h,毛细管电压3 kV。色谱运行在5 min内完成。通过监控CML和CEL的母离子分别为205和219 m/z,子离子均为84 m/z进行采集。
1.7 荧光强度测定
用酶标仪测定荧光强度,反映美拉德反应程度。参照毕日秀等[13]的方法进行测定,取0.5 g样品放入10 mL离心管中,加入1 mL超纯水溶解后,再加入4 mL pH 4.6的乙酸盐缓冲溶液。摇匀后,以4 000×g离心10 min。用滤纸过滤后,向0.5 mL上清液中加入4.5 mL超纯水。当测量高级美拉德产品的荧光强度(fluorescence of advanced Maillard reaction products,FAMP)时,激发波长设置为360 nm,发射波长设置为440 nm。当测量色氨酸的荧光强度(fluorescence of tryptophan,FTrp)时,激发波长设定为290 nm,发射波长设定为340 nm。综合热损伤指数(fluorescence of advanced Maillard products and soluble tryptophan,FAST)反映了单位蛋白质中FAMP的相对含量,可以综合指示热处理后牛乳的损伤程度。根据公式(2)计算FAST指数:
(2)
式中:FAST,综合热损伤指数;FAMP,高级美拉德反应产物荧光强度;FTrp,色氨酸荧光强度。
1.8 数据分析
所有实验数据均采用SPSS 25和Microsoft Excel 2010软件进行统计处理与作图分析。各实验均平行重复3次,试验结果以平均值±标准差表示。
2 结果与分析
2.1 不同婴配粉美拉德早期反应程度
糠氨酸是人造氨基酸,由Amadori化合物用6 mol/L HCl溶液在110 ℃ 24 h水解形成的。早期美拉德产品没有明显的颜色,在280 nm没有紫外吸收峰,转变为糠氨酸在280 nm处有很强的紫外线吸收,可以通过高效液相色谱检测[15]。因此,美拉德反应早期的反应程度可以根据产物中糠氨酸的含量来反映,从而进一步判断婴配粉加工过程中蛋白质的热损伤程度。
如图1、2所示,不同品牌的婴配粉糠氨酸和封闭赖氨酸含量不同,糠氨酸含量在300.44~856.64 mg/100 g,封闭赖氨酸含量在6.06%~16.16%,其中D4品牌的糠氨酸及封闭赖氨酸含量显著高于其他品牌,其封闭赖氨酸含量高达16%,封闭赖氨酸比例高会影响婴幼儿对赖氨酸的摄入。CONTRERAS-CALDER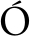 N等[16]研究了4种婴配粉的糠氨酸含量在55~1 937 mg/100 g,糠氨酸含量的差异性可能是由各市售品牌的婴配粉的加工工艺条件和其中的糖类成分含量、蛋白质种类以及金属离子的种类的差异性引起[17-18]。以生牛乳为原料的婴配粉和以奶粉为原料的婴配粉糠氨酸含量差异不显著(图1-b)。室温储存15个月与室温储存3个月相比,贮藏期间糠氨酸含量有增加的趋势,反映出美拉德反应在储存过程中仍在进行。
N等[16]研究了4种婴配粉的糠氨酸含量在55~1 937 mg/100 g,糠氨酸含量的差异性可能是由各市售品牌的婴配粉的加工工艺条件和其中的糖类成分含量、蛋白质种类以及金属离子的种类的差异性引起[17-18]。以生牛乳为原料的婴配粉和以奶粉为原料的婴配粉糠氨酸含量差异不显著(图1-b)。室温储存15个月与室温储存3个月相比,贮藏期间糠氨酸含量有增加的趋势,反映出美拉德反应在储存过程中仍在进行。
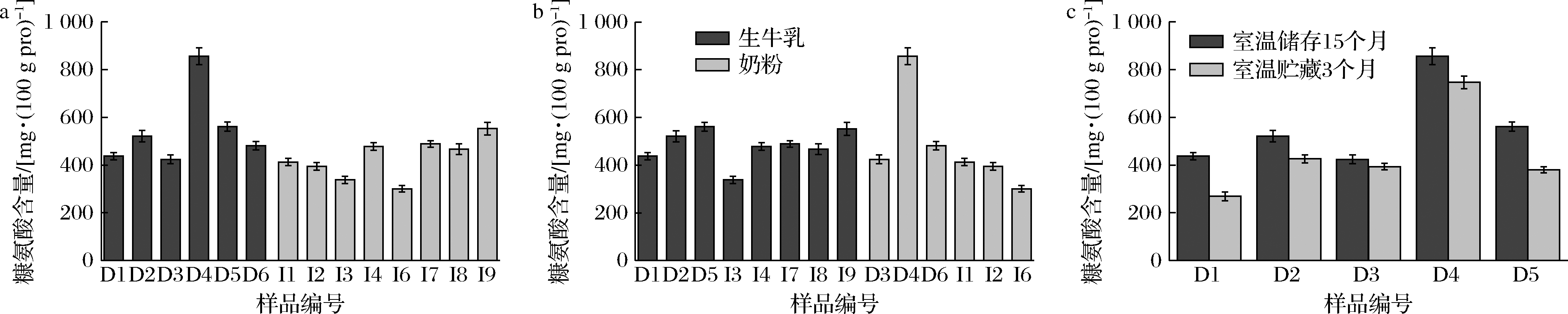
a-国内外品牌对比;b-原材料对比;c-生产日期对比
D-表示国产品牌;I-表示进口品牌(下同)
图1 不同品牌婴配粉糠氨酸含量
Fig.1 Furosine content in different brands of infant formula
2.2 不同婴配粉美拉德中期反应程度
2.2.1 5-HMF含量
美拉德反应的中间产物,如5-HMF和α-二羰基化合物,没有明显的颜色,在一定波长下有较强的紫外吸收峰。因此,可以通过测定中间代表产物的含量来判断美拉德反应程度。目前尚不清楚人类接触5-HMF是否会造成潜在的健康风险,但高浓度的5-HMF具有细胞毒性,可对眼睛、上呼吸道、皮肤和黏膜造成刺激,且5-HMF具有潜在的诱变和致癌作用[19-20]。如图3所示,不同品牌的婴配粉5-HMF含量在11.89~18.51 mg/kg。原料为生牛乳或乳粉不影响产品中5-HMF的含量。国内及国外品牌婴配粉中5-HMF差异不显著。在贮藏期间5-HMF整体含量变化较小,可能与其自身不稳定性及与其他中间产物相互作用有关[21]。JANZOWSKI等[19]制定了成人摄入5-HMF的每日容许摄入量(allowable daily intake,ADI)(30~60 mg/kg体重)。新生儿正常体重在2.5~4 kg,根据Ⅰ段奶粉的包装上对新生儿的推荐冲泡次数,新生儿每天摄入约63 g,如果按照20 mg/100 g计算(根据测得的5-HMF含量均小于20 mg/100 g),新生儿每日摄入5-HMF含量在3.15~5.04 mg/kg,远低于成人的ADI值,说明市场上的奶粉都是相对可靠的。
a-国内外品牌对比;b-原材料对比;c-生产日期对比
图2 不同品牌婴配粉封闭赖氨酸含量
Fig.2 blocked lysine content in different brands of infant formula

a-国内外品牌对比;b-原材料对比;c-生产日期对比
图3 不同品牌婴配粉的5-HMF含量
Fig.3 5-HMF content in different brands of infant formula
2.2.2 三种α-二羰基化合物含量的变化
α-二羰基化合物是美拉德反应的中间产物,也是AGEs的前体物质,该系列物质在体内累积的含量与糖尿病及其并发症相关[22]。如图4所示,不同品牌的婴配粉α-二羰基化合物含量不同,乙二醛含量在0.14~0.87 mg/kg,丙酮醛含量在0.15~2.7 mg/kg,2,3-丁二酮含量在3.16~9.31 mg/kg。D3品牌的丙酮醛含量显著高于其他品牌,可能与其加工工艺条件以及额外添加的酪蛋白相关,据报道,不同产地、不同配方会导致美拉德反应最终状态不同[23]。奶粉作为原料和生牛乳作为原料的产品之间二羰基化合物含量无显著差异。而且随着储存时间的延长,这3种二羰基化合物含量均上升,乙二醛含量最低增加90%,最高增加4.2倍,丙酮醛含量最低增加2.6倍,最高增加3.4倍,2,3-丁二酮含量最低增加1.2倍,最高增加1.8倍。乙二醛含量较低,基数比较小,所以含量变化明显。这3种美拉德反应的中间产物性质不稳定,易受外界因素影响,反应活性高。在胺类化合物的存在下,它们会进一步反应生成杂环芳香族化合物,并与高级糖基化化合物(如CML)发生反应,影响奶粉的质量和品质[24]。

a、d、g-国内外品牌乙二醛、丙酮醛、2,3-丁二酮对比;b、e、h-原材料乙二醛、丙酮醛、2,3-丁二酮对比;c、f、i-生产日期乙二醛、丙酮醛、2,3-丁二酮对比
图4 不同品牌婴配粉3种二羰基化合物含量
Fig.4 three dicarbonyl compounds content in different brands of infant formula
2.3 不同品牌婴配粉AGEs含量
如图5所示,不同品牌婴配粉AGEs含量不同,CEL含量在0.14~0.34 μg/mL,CML含量在5.99~32.76 μg/mL,随着贮藏时间的增加,特别是CML的含量增加显著,最低增加3.2倍,最高增加7.4倍,与LI等[21]结果相似。AGEs含量上升,这可能与热加工强度、储藏时间与加工次数间存在一定的叠加作用,能够导致乳制品中赖氨酸水平的快速降低和美拉德反应有害产物水平的迅速升高。AGEs的ADI值为32~252 μg/kg[14]。按新生儿婴配粉冲泡方式计算, CML、CEL含量之和都低于31 μg/mL,按照此值计算,新生儿每日摄入CML和CEL含量在38.8~62.0 μg/kg,与成人的ADI值相近。婴配粉中CML及CEL应引起注意。
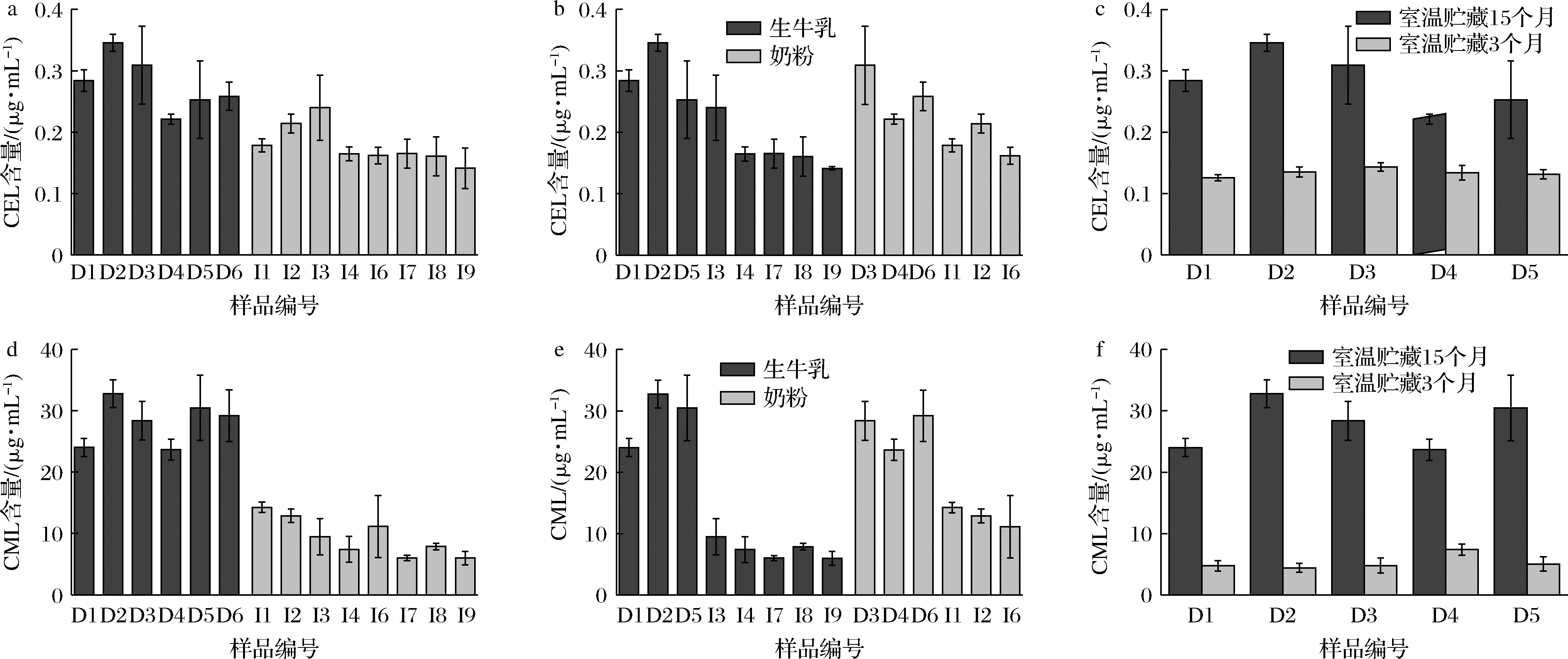
a-国内外品牌CEL含量对比;b-原材料CEL含量对比;c-生产日期CEL含量对比
d-国内外品牌CML含量对比;e-原材料CML含量对比;f-生产日期CML含量对比
图5 不同品牌婴配粉AGEs含量
Fig.5 Advanced glycation end products content in different brands of infant formula
2.4 不同品牌婴配粉综合热损伤指数的变化
牛奶在加热过程中,蛋白质被降解,色氨酸的荧光减弱,随着美拉德反应产物的积累,荧光增强。因此,结合色氨酸的荧光强度和美拉德反应后期产物的荧光强度,计算FAST值来评价婴幼儿配方奶粉的综合热损伤程度的变化[13]。如图6所示,不同品牌的婴配粉FAST不同,国内品牌和国外品牌没有明显的差异,原料对FAST的变化影响不大。随着储存时间的增加FAST变大,FAST越大表明婴配粉的美拉德反应程度越剧烈[25],印证了储藏过程中美拉德反应也在不断进行。

a-国内外品牌对比;b-原材料对比;c-生产日期对比
图6 不同品牌婴配粉FAST变化
Fig.6 Changes of FAST index in different brands of infant formula
3 结论与讨论
本研究分析了不同品牌的婴配粉中美拉德反应早期、中期以及晚期产物含量的情况,不同品牌的婴配粉美拉德产物含量不同,丙酮醛和CML的含量在贮藏期间有明显差异。这些婴配粉在储藏过程中美拉德反应仍然在进行,各种产物在反应过程中均有累积,其中美拉德反应中、末期产物增加速率高于初期产物。由于国外品牌进口需要一定时间的运输和海关的检验,所以国外品牌婴配粉的生产日期与食用期一般差距较大。各种品牌的婴配粉蛋白质含量、金属离子含量与种类、热处理强度以及贮藏时间差异[21,24]导致美拉德产物在储藏过程中增加的幅度有所不同,所以在控制美拉德反应程度和副产物产生方面,要注意加工工艺条件的选择。综合评价市售婴配粉在储藏期间的安全性,建议购买生产日期新鲜的奶粉,开封后在推荐日期内食用,同时也不建议大量购买囤积,以保证其质量和安全性。
[1] MARTIN C R, LING P R, BLACKBURN G L.Review of infant feeding:Key features of breast milk and infant formula[J].Nutrients, 2016, 8(5):279.
[2] 项云仙. 影响母乳喂养的因素及对策[J].中国农村卫生事业管理, 2018, 38(4):523-525.
XIANG Y X.Influencing factors and Countermeasures of breast feeding[J].Chinese Rural Health Service Administration, 2018, 38(4):523-525.
[3] 汪之顼, 丁叶, 邵莹莹.热处理工艺对婴幼儿配方粉中营养素消化吸收的影响[J].临床儿科杂志, 2016, 34(3):237-240.
WANG Z X, DING Y, SHAO Y Y.Effect of heat treatment process on digestion and absorption of nutrients in infant formula powder[J].Journal of Clinical Pediatrics, 2016, 34(3):237-240.
[4] 孙琦, 刘鹭, 蒋士龙, 等.不同热处理工艺对牛乳中热敏感成分的影响[J].食品与发酵工业, 2012, 38(11):47-53.
SUN Q, LIU L, JIANG S L, et al.Effects of heat treatment processing on the heat-sensitive components in milk[J].Food and Fermentation Industries, 2012, 38(11):47-53.
[5] LI Y, WU Y R, QUAN W, et al.Quantitation of furosine, furfurals, and advanced glycation end products in milk treated with pasteurization and sterilization methods applicable in China[J].Food Research International, 2021, 140:110088.
[6] BROWNLEE M, VLASSARA H, CERAMI A.Nonenzymatic glycosylation and the pathogenesis of diabetic complications[J].Annals of Internal Medicine, 1984, 101(4):527-537.
[7] BIRLOUEZ-ARAGON I, SAAVEDRA G, TESSIER F J, et al.A diet based on high-heat-treated foods promotes risk factors for diabetes mellitus and cardiovascular diseases[J].The American Journal of Clinical Nutrition, 2010, 91(5):1 220-1 226.
[8] POULSEN M W, HEDEGAARD R V, ANDERSEN J M, et al.Advanced glycation endproducts in food and their effects on health[J].Food & Chemical Toxicology, 2013, 60:10-37.
[9] SICILIANO R A, MAZZEO M F, ARENA S, et al.Mass spectrometry for the analysis of protein lactosylation in milk products[J].Food Research International, 2013, 54(1):988-1 000.
[10] AALAEI K, RAYNER M, SJÖHOLM I.Chemical methods and techniques to monitor early Maillard reaction in milk products:A review[J].Critical Reviews in Food Science and Nutrition, 2019, 59(12):1 829-1 839.
[11] MEHTA B M, DEETH H C.Blocked lysine in dairy products:Formation, occurrence, analysis, and nutritional implications[J].Comprehensive Reviews in Food Science and Food Safety, 2016, 15(1):206-218.
[12] BOSCH L, ALEGR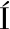 A A, FARRÉ R, et al.Effect of storage conditions on furosine formation in milk-cereal based baby foods[J].Food Chemistry, 2008, 107(4):1 681-1 686.
A A, FARRÉ R, et al.Effect of storage conditions on furosine formation in milk-cereal based baby foods[J].Food Chemistry, 2008, 107(4):1 681-1 686.
[13] 毕日秀, 芦晶, 张书文, 等.市售褐色酸奶在不同贮藏条件下美拉德反应副产物变化规律[J].食品与发酵工业, 2021, 47(1):116-124.
BI R X, LU J, ZHANG S W, et al.Changes of Maillard reaction by-products in brown yogurt under different storage conditions[J].Food and Fermentation Industries, 2021, 47(1):116-124.
[14] 贾晓迪. 全脂液态乳及乳粉中美拉德反应有害产物生成影响因素研究[D].无锡:江南大学, 2019.
JIA X D.Studies on the factors affecting the formation of Maillard reaction harmful products in whole milk and milk powder[D].Wuxi:Jiangnan University, 2019.
[15] ERBERSDOBLER H F, SOMOZA V.Forty years of furosine-Forty years of using Maillard reaction products as indicators of the nutritional quality of foods[J].Molecular Nutrition & Food Research, 2007, 51(4):423-430.
[16] CONTRERAS-CALDER N J, GUERRA-HERN
N J, GUERRA-HERN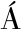 NDEZ E, GARC
NDEZ E, GARC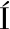 A-VILLANOVA B.Utility of some indicators related to the Maillard browning reaction during processing of infant formulas[J].Food Chemistry, 2009, 114(4):1 265-1 270.
A-VILLANOVA B.Utility of some indicators related to the Maillard browning reaction during processing of infant formulas[J].Food Chemistry, 2009, 114(4):1 265-1 270.
[17] OH N S, LEE H A, LEE J Y, et al.The dual effects of Maillard reaction and enzymatic hydrolysis on the antioxidant activity of milk proteins[J].Journal of Dairy Science, 2013, 96(8):4 899-4 911.
[18] JANSSON T, CLAUSEN M R, SUNDEKILDE U K, et al.Lactose-hydrolyzed milk is more prone to chemical changes during storage than conventional ultra-high-temperature (UHT) milk[J].Journal of Agricultural and Food Chemistry, 2014, 62(31):7 886-7 896.
[19] JANZOWSKI C, GLAAB V, SAMIMI E, et al.5-Hydroxymethylfurfural:Assessment of mutagenicity, DNA-damaging potential and reactivity towards cellular glutathione[J].Food and Chemical Toxicology, 2000, 38(9):801-809.
[20] BRUSTUGUN J, TØNNESEN H H, EDGE R, et al.Formation and reactivity of free radicals in 5-hydroxymethyl-2-furaldehyde-the effect on isoprenaline photostability[J].Journal of Photochemistry and Photobiology B:Biology, 2005, 79(2):109-119.
[21] LI Y, QUAN W, JIA X D, et al.Profiles of initial, intermediate, and advanced stages of harmful Maillard reaction products in whole-milk powders pre-treated with different heat loads during 18 months of storage[J].Food Chemistry, 2021, 351:129361.
[22] BROZ K, WALK R E, TANG S Y.Complications in the spine associated with type 2 diabetes:The role of advanced glycation end-products[J].Medicine in Novel Technology and Devices, 2021, 11:100065.
[23] MARTINS S I F S, JONGEN W M F, VAN BOEKEL M A J S.A review of Maillard reaction in food and implications to kinetic modelling[J].Trends in Food Science & Technology, 2000, 11(9-10):364-373.
[24] 贾宏信, 苏米亚, 陈文亮, 等.婴幼儿配方乳粉贮存过程中品质劣变的研究进展[J].食品工业科技, 2017, 38(23):330-334.
JIA H X, SU M Y, CHEN W L, et al.Research progress on quality deterioration of infant formula during storage[J].Science and Technology of Food Industry, 2017, 38(23):330-334.
[25] MASTROCOLA D, MUNARI M.Progress of the Maillard reaction and antioxidant action of Maillard reaction products in preheated model systems during storage[J].Journal of Agricultural and Food Chemistry, 2000, 48(8):3 555-3 559.