低温等离子保鲜技术是一种新型的非热杀菌保鲜技术,通过各种活性物质和独特的光电效应协同作用,具有良好的杀菌保鲜作用[1],在各种不同食品基质中,如即食火腿[2]、干腌牛肉[3]等都具有较好的微生物灭活效果。相对于传统的热加工体系,低温等离子保鲜技术对产品质地、风味、感官的改变较小,可以保持水产品的良好品质,同时其具有处理范围广、能耗低、环境友好、灭菌环境温度要求低等优势[4]。
我国是全球最大的水产品养殖与出口国,截止2019年底,全国水产品总产量共计6 480.36万t[5],然而水产品营养物质丰富、组织脆弱、极易滋生微生物[6],因而极易腐败变质,亟需一定方法来抑制水产品的腐败变质。如何提高水产品的保鲜效果,同时最大限度保留其营养价值和良好品质,进而延长产品货架期是生鲜食品保鲜研究所要克服的主要困难,而低温等离子体技术可以在温度较低的情况下灭活大量的微生物,进而保留水产品原有品质的同时抑制保鲜水产品的腐败变质,延长其货架期。
近几年来低温等离子体在水产品保鲜中的应用得到了广泛的研究,本文初步阐述了低温等离子体的保鲜原理以及在水产品中应用研究进展,并讨论了低温等离子体在应用中亟待解决的问题,为低温等离子体在水产品中的应用研究提供一定的指导作用。
1 低温等离子体概述
等离子体的形成是通过电场或强紫外辐射使物质外层电子击出,形成具有高位能、高动能的自由电子并与背景气体发生碰撞,从而引发一系列活性物质的产生。其本质上是由电子、正负离子、自由基、激发或非激发态气体分子和光子等组成的具有电中性的电离气体。
等离子的种类受相态、压力、温度、湿度等条件的影响,不同条件产生的等离子体的活性物质种类和数量、温度、电离程度、热力学平衡状态都不尽相同。如图1所示,根据电子、离子和气体分子的相对温度,可以将等离子体分为高温等离子体(106~108 K)和低温等离子体(300~103 K)。高温等离子体需要在足够高的能量条件(核聚变、太阳日冕等)下产生,是处于热力学平衡状态的高度电离气体,所有的粒子温度都相同。低温等离子体又称为热力学非平衡状态等离子体,可分为热等离子体(准平衡等离子体,≤2×104 K)和冷等离子体(非平衡等离子体,300~103 K)。相较而言,低温等离子体易控制、易制备且成本低,在食品、医药、污水处理等方面都具有广泛的应用潜力。

图1 等离子体的分类[7]
Fig.1 Classification of plasma
注:Te为电子;Ti为离子;Tg为气体分子;Tp为等离子体
1.1 等离子体发生方式
目前,应用于科学研究和生产实践的低温等离子发生器有很多种,常见的低温等离子体制备方法有介质阻挡放电法(dielectric barrier discharge,DBD)、大气压等离子体射流法(atmospheric pressure plasma jet, APJ)、接触辉光放电法、电晕放电法等。电晕放电均匀性差,电子密度和能量低,活性物质相对较少,效率偏低,无法大量制备。而接触辉光放电电极寿命短,能耗较高。因此这2种放电方法目前在食品杀菌领域应用较少。目前由于介质阻挡放电法和大气压等离子体射流法适用压力广、易于大量制备等优点,在食品领域中较为常用,主要应用于食品物料表面杀菌以及食品加工设备表面杀菌,尤其是果蔬、肉制品、水产品等需要较低杀菌温度和较高杀菌效率的生鲜食品。因此,本文主要针对这2种方法的工作原理进行了详细介绍。
1.1.1 介质阻挡放电
介质阻挡放电法在两电极中任意一侧或双侧放上绝缘介质,用于阻断2个电极之间的电流通道,通过高频、高功率放电在放电间隙中产生等离子体[8]。其等离子体发生装置如图2所示,主要由高压电极、绝缘介质层和地电极构成,其中绝缘介质层主要由塑料、玻璃、石英、云母、陶瓷等绝缘材料制成。
介质阻挡放电法电离强度高,适用的压力范围广,能够在大气压下生产大体积的低温等离子体,且具有设备简单,操作方便等优点。但是介质阻挡放电在大气压下表现为丝状流注放电模型,常常出现放电区域中放电细丝局部能量密度过高而灼伤物料的现象,研究者发现通过调节电源类型、电极结构、气流等参数可以使其表现出均匀、稳定、无放电细丝的放电形式[9]。

图2 介质阻挡放电等离子源示意图
Fig.2 Basic configuration of DBD
1.1.2 大气压等离子体射流
大气压等离子射流等离子体发生装置(图3)主要由高压电极、喷嘴、环形地电极构成,流动的工作气体在同轴的电极之间缝隙间通过,在高压作用下被电离产生等离子体,源源不断地从喷嘴中喷出,形成大气低温等离子体,如若作用于水气界面或水下则可生成等离子体活化水[10]。
大气压等离体射流法将放电区域和工作区域分开,气体在放电区域内持续流动,可以带走产生的热量,防止介质层过热;而流动气体可以减弱丝状放电现象,放电更加均匀和稳定[9]。大气压等离子体射流法在生物医药、材料表面改性、清洗杀菌等[11]方面都有广泛研究。

图3 等离子射流等离子源示意图
Fig.3 Basic configuration of APJ
1.2 等离子体的存在形式
除了放电形式影响等离子应用效果外,等离子体的存在形式也直接影响等离子体的应用范围及杀菌效果。目前应用于食品领域的低温等离子体主要以大气低温等离子体、等离子体活化水和等离子体活化冰的形式存在。
1.2.1 大气低温等离子体
大气低温等离子体产生机制是在大气压下向中性的气体施加电场或者强紫外辐射使得气体发生电离,来产生活性氧(reactive oxygen species,ROS)、活性氮(reactive nitrogen species,RNS)、高能粒子、紫外辐射、激发态分子等活性物质[12]。等离子源的功率强度、电源类型、处理时间、工作气体类型及其比例是等离子体性质的主要影响因素。科学家们最早研究大气低温等离子体时使用氩气、氦气等惰性气体作为工作气体,因为惰性气体具有高导热系数(散热)、具有较低的工作放电电压和丰富的紫外发射光谱[13],等离子体易于产生。然而,惰性气体产生的低温等离子体半衰期短,粒子种类较少,抗菌活性受限,在面对实际的工业应用时,惰性气体的来源、成本以及回收率都应纳入考虑,因此其广泛应用会受到极大的限制。如今,利用大气作为工作气体是低温等离子体的研究热点,相较惰性气体而言,大气低温等离子体含有丰富的ROS、RNS,对微生物的灭活作用更为有效。除此之外,可以调节工作气体的类型和比例对食品物料进行气调包装,如提高氧气含量、增加惰性气体等,对微生物灭活效果更为显著。
1.2.2 等离子体活化水
等离子体活化水是等离子体技术中一种更为新型的非热加工技术,是指通过在水中、水气界面或者水相上方施加电场,同时在气相和液相内产生活性物质。两相产生的各种化学物质会相互扩散,产生种类更为丰富的活性物质,同时会对水的pH 值、氧化还原电位、电导率等物理性质产生影响[14] ,同时上述物理性质也可以用于反映等离子体活化水的杀菌时效性,确定等离子体活化水中长效杀菌物质[15]等。相较于大气低温等离子体,等离子体活化水的液体性质可以克服食品物料形状不规则性,杀灭食品凹陷、狭小缝隙中的微生物[14] ,同时具有良好的流动性,便于物质的交换。
1.2.3 等离子体活化水
等离子体活化冰是在等离子体活化水的基础上制作的,等离子体活化后的水通过低温冻结成冰(一般为-20 ℃ ),兼具低温特性和杀菌特性,是一种新型的冰鲜杀菌技术。等离子体活化水中具有较长半衰期的活性物质,如H2O2 、O3和![]() 能够更稳定地存在于固态冰中,并且此类物质在微生物灭活机制中起主要作用[16] 。研究者发现等离子活化冰的氧化还原电位、电导率显著增大,pH值明显低于正常冰,表现出强氧化性和酸性,从而产生抑菌作用;同时各类活性物质在固态冰中具有缓释作用,可以在食品的贮藏期内持续发挥抑菌作用[17] ,因而等离子体活化冰可能会比等离子体活化水具有更好的时效性。
能够更稳定地存在于固态冰中,并且此类物质在微生物灭活机制中起主要作用[16] 。研究者发现等离子活化冰的氧化还原电位、电导率显著增大,pH值明显低于正常冰,表现出强氧化性和酸性,从而产生抑菌作用;同时各类活性物质在固态冰中具有缓释作用,可以在食品的贮藏期内持续发挥抑菌作用[17] ,因而等离子体活化冰可能会比等离子体活化水具有更好的时效性。
2 低温等离子体对微生物的灭活机理
低温等离子体主要的保鲜机制是低温等离子体对食品微生物的灭活。如今低温等离子体对微生物具体的灭活机制尚不明晰,但是低温等离子体中的各种活性成分、光子辐射、稳态的离子等对微生物繁殖代谢起到阻遏的作用被广泛认可,研究者认为低温等离子体可能主要通过对微生物细胞壁、细胞膜和核酸作用(图4),导致微生物活性降低甚至死亡。

图4 低温等离子体的灭活机理
Fig.4 Microbial inactive mechanisms of low temperature plasma in biological and physical aspects
2.1 低温等离子体对细胞壁的作用
肽聚糖是细菌细胞壁中特有成分,肽聚糖可以形成机械性很强的网状结构,对细菌细胞壁的机械强度有重要影响。低温等离子体中的ROS尤其O、O3和H2O2可以破坏肽聚糖中的C—O、C—C、C—N键,从而导致细菌细胞壁的损伤[18]。脂多糖是革兰氏阴性菌细胞壁的基本成分,经低温等离子体处理后同样发生了改性,BARTIS等[19]通过X射线光电子能谱对大肠埃希氏菌细胞壁脂多糖表面化学键进行了分析,发现脂多糖表面C—C键减少,O—C![]() O、O—C—O或N—C
O、O—C—O或N—C![]() O略有减少,这可能是等离子体灭活革兰氏阴性菌的主要原因。
O略有减少,这可能是等离子体灭活革兰氏阴性菌的主要原因。
陈玥等[20]研究了常压冷等离子体对食源性腐败菌失活作用机制,同时探究等离子体对金黄色葡萄球菌和大肠埃希氏菌形态影响,观察到低温等离子体处理后细菌细胞的形态发生改变,细胞出现褶皱、收缩(图5)。ZIUZINA等[21]也得到了相似的结果,发现经等离子体处理后大多数的大肠埃希氏菌表面粗糙、变形,甚至形成凹痕和孔洞,细胞出现缩小和脱水现象。低温等离子体中强氧化性物质破坏细胞的氧化还原状态,作用于细胞壁中的肽聚糖、磷脂和脂肪酸,引发细胞失稳死亡。

图5 常压冷等离子体对不同食源性腐败菌形态的影响[20]
Fig.5 Effect of atmospheric cold plasma on morphology of food-borne spoilage microorganisms
2.2 低温等离子体对细胞膜的作用
当细胞暴露在强电场中时,低温等离子体中的带电离子会聚集在细胞膜表面,影响细胞膜表面带电粒子的流动行为,会使细胞膜发生去极化[22] ,更容易受到低温等离子体活性物质的攻击。如图4 所示,由于带电粒子的不断积聚,细胞膜失稳,内部高电荷所产生的的静电张力超过细胞膜的抗拉强度时,细胞膜会发生电穿孔,从而形成结构性缺陷或者微孔,甚至发生破裂[23-24] ,导致内容物的泄露和活性物质在细胞内的扩散,进一步导致细胞的氧化损伤。由于革兰氏阳性菌的细胞外膜更厚,能抵抗更大的静电张力,因而革兰氏阳性菌对低温等离子体具有更高的耐受性[25] 。此外,等离子体中的RNS 也可以通过降低溶液pH 的方式影响膜表面电荷的性质和膜的通透性,导致微生物氧化失活。等离子体中丰富的自由基还会直接攻击细胞表面,破坏细胞膜上的化学键,造成细胞表面的损伤[26] 。除此之外,低温等离子体还可以有效地诱导病原菌生物膜的直接失活,并可能在减弱病原菌的毒力方面发挥重要作用[11] 。
膜脂是生物膜的骨架,常含不饱和脂肪酸。低温等离子中大量的活性物质和自由基如ROS、过氧亚硝酸盐(ONOOH)会引发脂质,尤其多不饱和脂肪酸的过氧化反应,形成脂质过氧化物,生成的丙二醛会使细胞膜的整体结构发生破坏,致使膜的流动性降低、通透性增强[27-28]。
膜蛋白是生物膜功能的主要承担者,控制着细胞的增殖分化、信号传导、物质运输等重要生理功能。低温等离子体中的活性物质可与蛋白质中的氨基酸残基发生反应,导致蛋白质结构功能的变化[29] 。
2.3 低温等离子体对核酸的作用
核酸是储存、复制和传递遗传信息的主要物质基础。如图4所示,低温等离子体中的活性物质,尤其是ROS活性氧成分可以刺激DNA双螺旋链结构的断裂从而导致氧化损伤[30];在脂质氧化过程中形成的丙二醛会参与DNA的解旋作用,造成严重的DNA损伤[31];同时由于细胞壁的失稳,细胞膜的通透性增加,导致细胞中DNA和RNA大量渗透,细胞外核酸物质增加,更有利于低温等离子体对核酸物质的氧化[32]。
紫外线辐射直接诱导的DNA损伤被认为是微生物失活的重要机制,尤其是波长在260 nm左右的紫外光,会导致同一条DNA链中的胸腺嘧啶和胞嘧啶反应形成二聚体,严重损害细菌的复制能力[27]。但也有研究认为紫外线的作用可以忽略不计,因为在大气压条件下近紫外辐射很容易被气体原子和分子吸收,而且大部分紫外辐射都会被细胞中生物大分子吸收,且产生的波长为220~280 nm有效杀菌紫外辐射通常达不到所需的杀菌剂量[27]。因而紫外辐射在低温等离子体中的灭活效果和机制有待更深入的研究。
综上所述,低温等离子体各类物质的复合效应会通过改变细菌细胞形态、造成细胞膜穿孔、攻击细胞内的核酸、蛋白质和脂质等大分子物质,影响细胞的繁殖代谢,引起细菌细胞渗漏和细胞功能的丧失,从而达到微生物灭活保鲜的作用。
3 低温等离子体在水产品杀菌保鲜中的应用
在我国,水产品主要还是以低温贮藏保鲜,依靠冷链鲜销为主,消费者越来越追求安全、营养、鲜美的品质。近年来,许多国内外学者利用低温等离子体技术对水产品进行保鲜。如表1所示,研究者们采用了不同的等离子体制备方式和处理参数,证明了低温等离子体具有保鲜有效性,也验证了在不同处理条件下对微生物的灭活效果不同。
表1 低温等离子体对水产品常见微生物的杀菌保鲜应用
Table 1 Application of cold plasma in sterization and preservation of common microorganisms in aquatic products

微生物种类等离子体产生方式等离子体作用形态处理参数试验结果参考文献大肠埃希氏菌等离子体射流气射频电压:1 ~5 kV;频率:1.5 MHz;工作气体:Ar;气体流量:4.9 L/min;处理时间:0~45 min;处理15 min 和45 min,分别有55%和88%大肠埃希氏菌处于不可培养状态[28]大肠埃希氏菌等离子体射流液功率:1.5 W;频率:9.4 kHz;无菌超纯水处理时间:10 min;作用时间分别为:0、5、10、15、20、30、40 min等离子体活化水(plasma-activated wa-ter,PAW)与大肠埃希氏菌作用时间越长,对大肠埃希氏菌的杀伤效果越好;作用时间为40 min 时,大肠埃希氏菌存活率为0[33]大肠埃希氏菌、酿酒酵母(樱桃汁)介质阻挡放电气处理电压:9 kV;频率:1 500 Hz;工作气体:Ar;气体流量:1.5 L/min;处理时间:1~5 min;进样量:1~5 mL进样量2 mL时大肠埃希氏菌和酿酒酵母可减少了2.27和1.23 lgCFU/mL[22]希瓦氏菌-液功率:0.9 kW;PAW处理时间:0、15、30、45、60 min;鱼块在PAW中浸泡时间:0、7.5、15、22.5、30 min使用处理了60 min的PAW浸泡染菌鱼块30 min时,鱼肉菌落总数最低降至(3.01±0.02)lgCFU/g;对希瓦氏菌生长的抑制效果明显,其中制备时间60 min组的抑菌率高达99.9%[34]金黄色葡萄球菌、单增李斯特菌(干腌牛肉)等离子体射气处理电压:25 kV;处理时间:3 min 和5 min;频率:42 kHz;O2、Ar、O2∶Ar (1∶3)、O2∶Ar (1∶1)气调包装金黄色葡萄球菌最大减少0.85 lgCFU/cm2,单增李斯特菌计数最大减少0.83 lg CFU/cm2[3]巴氏葡萄球菌介质阻挡放电液工作电流:5.6 A;功率:1 055 W;制备时间(水下):0、15、30、45、60 min处理60 min后PAW对巴氏葡萄球菌的抑制率(95.25±0.05)%[35]沙门氏菌等离子体射流液功率:750 W;工作气体:空气;等离子体射流装置对无菌去离子水的处理时间分别为0.5、1、1.5 minPAW作用6 min S.Typhimurium菌落总数分别降低0.63、1.78 和4.32 lgCFU/mL[36]单增李斯特菌介质阻挡放电固工作电压:100 kV;工作电流:0.48 mA;等离子体射流末端置于无菌水液面下20 mm;无菌水处理时间:30、60 min;处理体积:100、500 mL;后制备成固态冰100 mL 处理了30 min 的等离子体活化冰具有最高的灭菌效果;作用30 min,单增李斯特菌可降低2.9 lgCFU/mL[37]南美白对虾优势腐败菌介质阻挡放电气处理电压70 kV;处理时间0、0.5、1、1.5、2、2.5 min60 kV、2 min或70 kV、1.5 min可完全杀灭Enterobacter sp.;60 kV、2.5 min或70 kV、2 min可完全杀灭Shewanella sp.[38]
注:-表示无数据
低温等离子体作为非平衡状态的活性体,其作用效力会受到各种因素的影响,一般而言,处理电压越大、处理时间越长,产生的活性物质越多,保鲜效果越好,贮藏时间和作用方式都直接影响其对微生物灭活的效果。研究结果显示,低温等离子体普遍能将水产品的货架期延长到8~15 d左右。
目前低温等离子体在鱼类和甲壳类水产品都有应用(表2)。低温等离子体在生鲜鱼片的研究和应用较多,研究者利用了介质阻挡放电法和等离子体射流法产生不同形态的低温等离子体对生鲜鱼片的保鲜效果进行了研究。研究表明,介质阻挡放电法常常与改性气体包装技术进行联合协同保鲜,形成调节气体比例达到厌氧抑菌和活性等离子体灭活的协同保鲜机制;通过增大氧气浓度增强低温等离子体的灭活效力,同时添加稀有气体氩气来降低的工作放电电压,来达到较好的灭活保鲜效果,并降低设备对电力的要求。等离子体射流法则多用于PAW的制备,在液体或气液界面产生活性物质,利用液态介质直接作用于鱼体表面,适用于非包装食品的表面直接杀菌。
表2 低温等离子体在水产品杀菌中的应用
Table 2 Application of cold plasma in sterization of aquatic products

研究对象等离子体产生方式等离子体作用形态处理参数试验结果参考文献冷藏大西洋鲭鱼鱼片介质阻挡放电气处理电压70、80 kV;处理时间1、3、5 min;工作气体:空气80 kV 处理5 min 的鲭鱼鱼片总需氧嗜温菌数无明显下降;嗜冷菌、乳酸菌和假单胞菌数显著降低[39]冷藏亚洲鲈鱼鱼片介质阻挡放电气处理电压:80 kV;处理时间:5 min;CO2∶Ar∶O2(60∶30∶10)或Ar∶O2(10∶90)气调包装CO2∶Ar∶O2 (60∶30∶10)气体比例,总菌数、嗜冷菌、假单胞菌数显著降低,货架期可达15 d[40]冷藏亚洲鲈鱼鱼片介质阻挡放电气处理电压:16 kV;处理时间:5 min;处理极距:2 cm;Ar∶O2(90∶10)气调包装16 kV 处理5 min 的鲭鱼鱼片总菌数和嗜冷菌数至少降低了0.7 lgCFU/g;产硫化氢细菌、肠杆菌科细菌、假单胞菌和乳酸菌数量显著降低,货架期可达12 d[41][42]亚洲鲈鱼片介质阻挡放电气处理电压:80 Kv;处理时间:5 min;处理温度:(28±2) ℃ ;CO2∶Ar∶O2(60∶30∶10)气调包装未经处理的对照组以变形菌门为主,而经高压冷等离子体结合椰壳乙醇提取物脂质体处理的样品中以厚壁菌为主;革兰氏阳性菌具有更大的生长繁殖优势;假单胞菌属以及希瓦氏菌数量可降低10%左右[43]干制丝背细鳞鲀鱼片强紫外辐射电离气处理时间:0、3、5、10、20 min处理10 min 后可以使90%枝孢霉和桔孢霉失活[44]黄鱼鱼片等离子体射流液工作电压:19 kV;工作气体:空气;气体流速:22.5 L/min;鱼片在活化水中浸泡30 s;等离子体射流装置对去离子水处理时间1、2 和3 min等离子体射流装置处理3 min 的等离子活化水使得鱼片中沙门氏菌数降低1.12 lgCFU/g,杀菌率达92.41%[15]冷藏罗非鱼片介质阻挡放电气处理电压:70 kV;处理时间:1 min;CO2∶O2∶N2(60∶10∶30)气调包装总菌数降低了2.21 lgCFU/g;且贮藏期间细菌增长缓慢,货架期可达12 d 以上[45]南美白对虾介质阻挡放电气处理电压:20、40、60 kV;工作气体:空气;处理时间:3 min60 kV 处理3 min 后菌落总数降低0.45 lgCFU/g[46]刀额新对虾介质阻挡放电固输入功率:30 W;水经等离子体活化10 min 后在-20 ℃ 下冻结成固态冰;冰藏;处理量:100 mL显著延缓对虾体内微生物的生长,保质期可达8 d以上[16]太平洋白对虾介质阻挡放电气处理电压:16 kV;处理时间:10 min;Ar∶O2(80∶20)或Ar∶空气(80∶20)气调包装1% 茶木芒叶提取物处理后的虾在Ar∶空气(80∶20)混合气体中处理后,货架期可延长到15 d[47]即食酒渍泥螺介质阻挡放电气处理电压:40、50、60 kV;工作气体:空气;处理时间:3 min;频率:36 kHz60 kV 组的抑菌率达到了69. 52% ;货架期可延长到12 d[48]
气态低温等离子体是目前生鲜鱼片杀菌常用的形式,由于介质阻挡放电法处理电压较高,所需电压普遍在60~100 kW左右,常常出现放电区域中放电细丝局部能量密度过高而灼伤物料的现象,因而介质阻挡放电法结合气态介质时,处理时间普遍在5 min左右。液态的低温等离子体在灭菌时,需要将鱼片浸渍于液体介质中,会引起鱼肉溶胀和水溶性成分的损失,导致鱼肉食用品质降低。同时由于大多数生鲜食品不宜进行长时间浸泡,因而采用气态低温等离子体能更好维持产品品质。
低温等离子体在甲壳类水产品保鲜方面也有应用,目前研究者采用了不同形态(气体和固体)低温等离子体对南美白对虾、刀额新对虾、太平洋白对虾和即食酒渍泥螺的保鲜效果进行了研究。研究发现,施加低温等离子体后产品的菌群数量显著降低,有效延长货架期。SHIEKH等[47]研究了低温等离子体结合茶木芒叶提取物对太平洋白对虾的保鲜效果的影响,发现经处理后虾体内肠杆菌科细菌、产硫化氢细菌、假单胞菌、乳酸菌数量都显著降低,各类理化品质得到很好保持,有效将其保质期延长到15 d。LIN等[48]利用以空气为介质的气态低温等离子体对即食酒渍泥螺进行灭活杀菌,当施加电压为60 kV时,其抑菌率达到了69.52%,货架期延长到12 d,相对未处理组增加了6 d。与生鲜鱼片不同,甲壳类水产品在高电压下不易发生灼伤,因而可以通过提高电压、延长作用时间来提升微生物的灭活效果。
在水产品的贮藏条件中,致腐致病的主要菌群类型是嗜冷菌,而且多为革兰氏阴性菌,如大肠埃希氏菌、希瓦氏菌、沙门氏菌等会引起蛋白质降解,营养价值的降低,产生不良气味,食用被菌体污染的水产品会引起严重腹泻和败血症。低温等离子体对此类微生物的灭菌效果显著,灭菌率普遍达到了90%以上。
相启森等[36]利用PAW对沙门氏菌菌液处理6 min时,沙门氏菌降低了4.32 lgCFU/mL。DOLEZALOVA等[28]利用以氩气为介质制备的低温等离子体对大肠埃希氏菌处理45 min,88%大肠埃希氏菌处于不可培养状态,研究显示经等离子体处理后水中检测到了游离的丙二醛和DNA,说明大肠埃希氏菌的膜脂成分可能发生了氧化损伤,细胞膜形成了孔洞甚至发生破裂。同时生成的丙二醛可能与DNA反应发生交联形成核苷酸加合物,从而抑制细胞的生长繁殖。
在革兰氏阳性菌中,主要以单增李斯特菌、乳酸菌、葡萄球菌等为主,在食品冷藏冷冻中具有较大的致病风险,会引发食物中毒、败血症、炎症甚至死亡。低温等离子体对其具有良好的灭活作用,能使菌体数量显著降低。GÖK等[3]研究了大气低温等离子体对干腌牛肉中金黄色葡萄球菌和单增李斯特菌的灭活作用,研究发现金黄色葡萄球菌可以最大减少0.85 lgCFU/cm2,而单增李斯特菌计数最大减少0.83 lgCFU/cm2,因而能有效提高产品的安全性。金黄色葡萄球菌经等离子体处理后菌体表面所受到的表面张力增大,活性物质促使膜脂的氧化。但研究发现经处理后金黄色葡萄球菌并未发生细胞破裂,仅出现细胞表面粗糙、变形,形成凹痕和孔洞的现象。
据目前的研究表明,低温等离子对革兰氏阴性菌的灭菌效果更好,低温等离子体中含有的高活性的羟基自由基是灭活革兰性阴性菌的主要因素,可以引发细菌细胞壁肽聚糖分子关键化学键断裂,造成细菌内蛋白质或核酸损伤;相较于革兰性阴性菌,革兰氏阳性菌细胞壁具有多层交联紧密的肽聚糖网络,往往对低温等离子体的抗性更强[49]。
目前低温等离子体对真菌的灭活作用研究甚少,研究成果不多,对真菌的细胞结构分析,真菌细胞壁几丁质的交联程度更大,稳定性更强,可能对各类灭活因素敏感性都较低[23],并未表现较为明显的灭菌作用。在水产品的贮藏条件中,造成水产品腐败的主要菌群类型是嗜冷菌,而且多为革兰氏阴性菌,因而低温等离子体在水产品贮藏保鲜领域具有更广阔的应用空间。
4 展望
低温等离子体对微生物灭活保鲜作用已经被广泛证实,其在生鲜食品的保鲜加工有着巨大的应用潜力,因水产品本身品质的特殊性,对保鲜技术的要求也更为苛刻。作为一种新型的非热杀菌形式,虽然低温等离子体具有显著的微生物灭活效果、灭活环境温度低、处理范围广等的优势,但是低温等离子体作为活跃的反应体,对物质的各类作用并不具有选择性,不可避免也会对食品中的各类大分子物质造成损害,如低温等离子体中的活性氧攻击氨基酸分子中的自由氨基或亚氨基,造成蛋白质的氧化,使得蛋白质特定化学键的断裂或对侧链基团的化学改性[50]。低温等离子体中的活性物质ROS,尤其是是羟自由基、H2O2和超氧阴离子可以与食物脂质相互作用并启动自动氧化过程[51],造成食品营养价值降低。因此低温等离子体在食品中的应用还应该注意活性物质对营养物质的破坏,设定适宜的工作参数最大化杀灭微生物,最小化品质损害。
此外,有关低温等离子体具体的作用机制、影响因素及其调控手段还没有较为完善的理论作为支撑。等离子体源装置的精确调控、工作气体的最优比例、活性物质的生成机制、活性物质的长效保留都是低温等离子体制备阶段所面临的的主要问题。低温等离子体作为活跃的反应体,所含有的成分难以统一标准化,反应各级产物鉴定、最终产物的测定、残留问题、安全性评估都面临挑战。除此之外,其制备机理、作用机理、具体作用效果、效益性都有待完善的理论和实验数据支持。
因此,低温等离子体在保鲜领域的广泛应用要求对低温等离子体制备及应用理论化、标准化、规模化,则需要对低温等离子体进行更多的研究与探索。
[1] MISRA N N, JO C.Applications of cold plasma technology for microbiological safety in meat industry[J].Trends in Food Science & Technology, 2017, 64: 74-86.
[2] YADAV B, SPINELLI A C, GOVINDAN B N., et al. Cold plasma treatment of ready-to-eat ham: Influence of process conditions and storage on inactivation of Listeria innocua [J].Food Research International, 2019, 123: 276-285.
[3] GÖK V, AKTOP S, ÖZKAN M, et al. The effects of atmospheric cold plasma on inactivation of Listeria monocytogenes and Staphylococcus aureus and some quality characteristics of past rma-A dry-cured beef product[J].Innovative Food Science and Emerging Technologies, 2019, 56: 102188.
rma-A dry-cured beef product[J].Innovative Food Science and Emerging Technologies, 2019, 56: 102188.
[4] 徐文慧, 周锦云, 蔡静, 等. 基于低温等离子体技术的果蔬生鲜杀菌保鲜研究进展[J].浙江农业科学, 2020, 61(1): 121-124.
XU W H, ZHOU J Y, CAI J, et al.Rsesarch progress on sterilization and preservation of fresh fruits and vegetables by low temperature plasma technology[J].Journal of Zhejiang Agricultural Sciences, 2020, 61(1):121-124.
[5] 农业农村部渔业渔政管理局, 全国水产技术推广总站, 中国水产学会编制. 中国渔业统计年鉴-2020[M].北京:中国农业出版社. 2020.
Bureau of Fisheries, Ministry of Agriculture, PRC.China Fishery Statistical Yearbook[M]. Beijing: China Agriculture Press. 2020.
[6] GHALY. Fish spoilage mechanisms and preservation techniques:Review[J].American Journal of Applied Sciences, 2010, 7(7):859-877.
[7] 相启森, 张嵘, 范刘敏, 等. 大气压冷等离子体在鲜切果蔬保鲜中的应用研究进展[J].食品工业科技, 2021, 42(1): 368-372.
XIANG Q S, ZHANG R, FAN L M, et al.Research progress of atmospheric cold plasma in fresh-cut fruits and vegetables preservation[J].Science and Technology of Food Industry, 2021, 42(1):368-372.
[8] 郑哲, 李昌.低温等离子体在农产品加工保藏中应用的研究进展[J].食品工业科技, 2021, 42(11):390-396.
ZHENG Z, LI C. Research progress on the application of cold plasma in food sterilization and preservation[J]. Science and Technology of Food Industry, 2021, 42(11): 390-396.
[9] 邵涛, 严萍. 大气压气体放电及其等离子体应用[M]. 北京:科学出版社, 2015.
SHAO T, YAN P. Atmospheric Pressure Gas Discharge and Its Plasma Application[M]. Beijing: Science Press, 2015.
[10] 李嘉慧, 成军虎, 韩忠.低温等离子体活性水在食品领域的应用进展[J]. 保鲜与加工, 2020, 20(4): 207-214.
LI J H, CHENG J H, HAN Z.Applications of plasma-activated water in food field: A review[J]. Storage and Process, 2020, 20(4):207-214.
[11] DUARTE S, PANARIELLO B H D. Comprehensive biomedical applications of low temperature-plasmas[J].Archives of Biochemistry and Biophysics, 2020, 693: 108560.
[12] BOURKE P, ZIUZINA D, BOEHM D, et al. The potential of cold plasma for safe and sustainable food production[J]. Trends in Biotechnology, 2018, 36(6): 615-626.
[13] KONESKY G. Dwell time considerations for large area cold plasma decontamination[C]//SPIE Defense, Security, and Sensing. Florida: 2009, 7 304: 157-166.
[14] 康超娣, 相启森, 刘骁, 等.等离子体活化水在食品工业中应用研究进展[J]. 食品工业科技, 2018, 39(7): 348-352.
KANG C D, XIANG Q S, LIU X, et al.A review of application of plasma-activated water in food industry[J]. Science and Technology of Food Industry, 2018, 39(7): 348-352.
[15] 钱婧, 仲安琪, 王露丹, 等. 等离子体活性水对生鲜黄鱼杀菌效果及品质的影响[J]. 食品工业科技, 2020, 41(450): 277-283.
QIAN J, ZHONG A Q, WANG L D, et al. Effects of plasma-activated water on the microbial decontamination and quality of yellow croaker slices[J]. Science and Technology of Food Industry, 2020, 41(10): 277-283.
[16] LIAO X Y, SU Y, LIU D H, et al. Application of atmospheric cold plasma-activated water (PAW) ice for preservation of shrimps(Metapenaeus ensis)[J]. Food Control, 2018, 94: 307-314.
[17] 艾春梅, 谢小本, 廖新浴, 等. 等离子体活化冰对东方对虾保鲜及品质的影响[J].食品与机械, 2019, 35(3): 130-136.
AI C M, XIE X B, LIAO X Y, et al.Effect of plasma-activated water (PAW) ice on the quality of shrimps (Penaeus orientalis) during storage[J]. Food & Machinery, 2019, 35(3): 130-136.
[18] YUSUPOV M, BOGAERTS A, HUYGH S, et al. Plasma-in-duced destruction of bacterial cell wall components: A reactive mo-lecular dynamics simulation[J]. The Journal of Physical Chemis-try C, 2013, 117(11): 5 993-5 998.
[19] BARTIS E J, GRAVES D B, SEOG J, et al. Atmospheric pressure plasma treatment of lipopolysaccharide in a controlled environment[J]. Journal of Physics D: Applied Physics, 2013, 46(31):321002.
[20] 陈玥, 李书红, 孟琬星, 等. 常压冷等离子体对食源性腐败菌失活作用机制研究[J]. 食品研究与开发, 2021, 42(5): 71-76.
CHEN Y, LI S H, MENG W X, et al. Study on the inactivation mechanism of atmospheric cold plasma on food-borne spoilage bacteria[J].Food Research and Development, 2021, 42(5): 71-76.
[21] ZIUZINA D, PATIL S, CULLEN P J, et al. Atmospheric cold plasma inactivation of Escherichia coli in liquid media inside a sealed package[J]. Journal of Applied Microbiology, 2013, 114(3): 778-787.
[22] GAN Z L, FENG X R, HOU Y N, et al. Cold plasma jet with dielectric barrier configuration: Investigating its effect on the cell membrane of E.coli and S.cerevisiae and its impact on the quality of chokeberry juice[J]. LWT, 2021, 136: 110223.
[23] LIAO X Y, LIU D H, XIANG Q S, et al. Inactivation mechanisms of non-thermal plasma on microbes:A review[J].Food Control, 2017, 75: 83-91.
[24] MENDIS D A, ROSENBERG M, AZAM F. A note on the possible electrostatic disruption of bacteria[J]. IEEE Transactions on Plasma Science, 2000, 28(4): 1 304-1 306.
[25] KOSTOV K G, ROCHA V, KOGA-ITO C Y, et al. Bacterial sterilization by a dielectric barrier discharge (DBD) in air[J]. Surface and Coatings Technology, 2010, 204(18-19): 2 954-2 959.
[26] THIRUMDAS R, KADAM D, ANNAPURE U S. Cold plasma: An alternative technology for the starch modification[J]. Food Biophysics, 2017, 12(1): 129-139.
[27] LAROUSSI M, LEIPOLD F. Evaluation of the roles of reactive species, heat, and UV radiation in the inactivation of bacterial cells by air plasmas at atmospheric pressure[J]. International Journal of Mass Spectrometry, 2004, 233(1-3): 81-86.
[28] DOLEZALOVA E, LUKES P. Membrane damage and active but nonculturable state in liquid cultures of Escherichia coli treated with an atmospheric pressure plasma jet [J]. Bioelectrochemistry, 2015, 103: 7-14.
[29] PARK J H, KUMAR N, UHM H S, et al. Effect of nanosecond-pulsed plasma on the structural modification of biomolecules[J]. RSC Advances, 2015, 5(59): 47 300-47 308.
[30] KEYER K, GORT A S, IMLAY J A. Superoxide and the production of oxidative DNA damage[J]. Journal of Bacteriology, 1995,177(23): 6 782-6 790.
[31] THIRUMDAS R, SARANGAPANI C, ANNAPURE U S. Cold plasma: A novel non-thermal technology for food processing[J]. Food Biophysics, 2015, 10(1): 1-11.
[32] TIAN Y, MA R N, ZHANG Q, et al. Assessment of the physicochemical properties and biological effects of water activated by non-thermal plasma above and beneath the water surface[J]. Plasma Processes & Polymers, 2015, 12(5): 439-449.
[33] 刘玉亭. 大气压射流等离子体杀菌效果研究[D]. 大连: 大连理工大学, 2018.
LIU Y T. Study on atmospheric pressure jet plasma sterilization effect[D]. Dalian: Dalian University of Technology, 2018.
[34] 刘舒彦, 李海蓝, 李湃, 等. 等离子体活化水对希瓦氏菌及鲈鱼品质的影响[J]. 肉类研究, 2020, 34(9): 25-30.
LIU S Y, LI H L, LI P, et al. Effects of plasma-activated water on inhibiting Shewanella and improving the quality of Micropterus salmoides[J]. Meat Research, 2020, 34(9): 25-30.
[35] 鉏晓艳, 刘舒彦, 李海蓝, 等. 等离子体活化水对加州鲈巴氏葡萄球菌的抑制作用[J]. 食品科技, 2020, 45(11): 124-130.
ZU X Y, LIU S Y, LI H L, et al. Inhibition effect of plasma activated water on Staphylococcus pasteuri in Micropterus salmoides[J]. Food Science and Technology,2020,45(11): 124-130.
[36] 相启森, 张嵘, 杜桂红, 等. 等离子体活化水对沙门氏菌的灭活作用及机制研究[J]. 食品工业科技, 2021, 42(8):138-143.
XIANG Q S, ZHANG R, DU G H, et al. Inactivation effects and mechanisms of plasma-activated water against S. Typhimurium[J]. Science and Technology of Food Industry, 2021, 42(8):138.
[37] 焦浈, 朱育攀, 许航博, 等. 等离子体活化水冰对纯培养及三文鱼片表面单增李斯特菌杀菌效果研究[J]. 郑州大学学报(理学版), 2019, 51(3): 97-103.
JIAO Z, ZHU Y P, XU H B, et al. Plasma-activated water ice inactivation of Listeria monocytogenes in pure culture and salmon strips[J]. Journal of Zhengzhou University (Natural Science Edition), 2019, 51(3): 97-103.
[38] 陈俊羽. 低温等离子体对南美白对虾品质及优势腐败菌AHLs的影响研究[D]. 舟山: 浙江海洋大学, 2019.
CHEN J Y. Effects of atmospheric cold plasma on the quality of Penaeus vannamei and AHLs in specific spoilage organism[D]. Zhoushan: Zhejiang Ocean University, 2019.
[39] ALBERTOS I, MART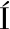 N-DIANA A. B, CULLEN P J, et al. Effects of dielectric barrier discharge (DBD) generated plasma on microbial reduction and quality parameters of fresh mackerel (Scomber scombrus) fillets[J]. Innovative Food Science & Emerging Technologies, 2017, 44: 117-122.
N-DIANA A. B, CULLEN P J, et al. Effects of dielectric barrier discharge (DBD) generated plasma on microbial reduction and quality parameters of fresh mackerel (Scomber scombrus) fillets[J]. Innovative Food Science & Emerging Technologies, 2017, 44: 117-122.
[40] OLATUNDE O O, BENJAKUL S, VONGKAMJAN K. Shelf-life of refrigerated Asian Sea bass slices treated with cold plasma as affected by gas composition in packaging[J]. International Journal of Food Microbiology, 2020, 324: 108612.
[41] OLATUNDE O O, BENJAKUL S, VONGKAMJAN K. Combined effects of high voltage cold atmospheric plasma and antioxidants on the qualities and shelf-life of Asian Sea bass slices[J]. Innovative Food Science & Emerging Technologies, 2019, 54: 113-122.
[42] SINGH A, BENJAKUL S. The combined effect of squid pen chitooligosaccharides and high voltage cold atmospheric plasma on the shelf-life extension of Asian Sea bass slices stored at 4 ℃[J]. Innovative Food Science & Emerging Technologies, 2020,64: 102339.
[43] OLATUNDE O O, BENJAKUL S, VONGKAMJAN K. Microbial diversity, shelf-life and sensory properties of Asian Sea bass slices with combined treatment of liposomal encapsulated ethanolic coconut husk extract and high voltage cold plasma [J]. LWT, 2020, 134: 110232.
[44] PARK S Y, HA S D. Application of cold oxygen plasma for the reduction of Cladosporium cladosporioides and Penicillium citrinum on the surface of dried filefish (Stephanolepis cirrhifer) fillets[J]. International Journal of Food Science & Technology, 2015, 50(4):966-973.
[45] 汪春玲, 周佳莹, 付仁豪, 等. 等离子体处理对气调罗非鱼片保鲜品质的影响[J]. 食品科技, 2019, 44(10): 147-152.
WANG C L, ZHOU J Y, FU R H, et al. Effect of plasma treatment on fresh-keeping quality of air-conditioned tilapia fillets[J]. Food Science and Technology, 2019, 44(10): 147-152.
[46] 徐慧倩, 严金红, 唐玲玲, 等. 低温等离子体对南美白对虾冷藏期间品质保持的效果[J]. 现代食品科技, 2021, 37(4):116-123;138.
XU H Q, YAN J H, TANG L L, et al. Effect of cold atmospheric plasma on quality maintenance of Penaeus vannamei during cold storage[J]. Modern Food Science and Technology, 2021, 37(4):116-123;138.
[47] SHIEKH K A, BENJAKUL S. Effect of high voltage cold atmospheric plasma processing on the quality and shelf-life of Pacific white shrimp treated with Chamuang leaf extract[J]. Innovative Food Science & Emerging Technologies, 2020, 64: 102435.
[48] LIN H M, ZHANG S, ZHENG R S, et al. Effect of atmospheric cold plasma treatment on ready-to-eat wine-pickled Bullacta exarata[J]. LWT, 2020, 120(8): 108953.
[49] YOUBI G K,HERRY J M,MEYLHEUC T,et al.Microbial inactivation using plasma-activated water obtained by gliding electric dischar-ges[J]. Letters in Applied Microbiology, 2010, 48(1):13-18.
[50] MISRA N N, PANKAJ S K, SEGAT A, et al. Cold plasma interac-tions with enzymes in foods and model systems[J]. Trends in Food Science & Technology, 2016, 55:39-47.
[51] ATTRI P, KIM Y H, PARK D H, et al.Generation mechanism of hydroxyl radical species and its lifetime prediction during the plasma-initiated ultraviolet(UV)photolysis[J].Scientific Reports,2015, 5(1):9 332.