葡萄酒发酵过程中,酵母承受乙醇毒性、营养缺乏、高糖、渗透压等多种环境胁迫的影响[1]。尤其值得注意的是,近年来气候变暖引起葡萄的含糖量逐年上升[2]。使葡萄酒发酵产生的乙醇含量升高,酵母生长受到抑制甚至死亡。因此筛选具有良好乙醇耐性的酿酒酵母能保证发酵完全,减少发酵停滞的风险[3]。此外,在复杂的葡萄酒发酵过程中,一些酵母合成的蛋白质或毒素有助于抑制其他不良微生物的生长[4]。筛选嗜杀酵母来防治腐败酵母,可以提高葡萄酒香气的纯净度,避免葡萄酒生产的经济损失[5]。在与葡萄酒香气有关的挥发性代谢产物中,含硫化合物的检测阈值非常低,会对葡萄酒的感官特性产生较大的影响。高挥发性的硫化氢浓度超过其感知阈值则具有强烈的还原味,给葡萄酒带来腐烂鸡蛋、大蒜、洋葱和白菜的粗劣香气。酿酒师可以选择低产硫化氢能力的菌株,来调节葡萄酒中硫化氢的产量。
发酵过程中酿酒酵母会产生多种香气活性物质[6],这些物质对于啤酒、葡萄酒和清酒等发酵饮料的复杂风味至关重要。酵母在酿造中和其他酵母的竞争、发酵、自溶等机制进一步决定葡萄酒的香气成分[7]。在葡萄酒中发现了几种类型的挥发性化合物,如醇类、脂肪族、苯衍生物、羰基、酯类、有机酸、含硫化合物、多元醇、甲氧基吡嗪、乙烯基和挥发性酚类等[8],源自发酵的挥发性化合物占葡萄酒总香气成分的百分比最大。其中乙基酯类物质赋予葡萄酒馥郁的水果香气[9],在葡萄酒中乙酯含量与葡萄酒评分呈正相关[10]。
葡萄酒酵母对葡萄酒质量有重要影响,筛选优良的酿酒酵母菌株也成为改善葡萄酒质量的重要方式之一。利用本土酿酒酵母资源,有助于适应产区环境、酿造具有香气独特性的葡萄酒[11]。在实验室前期工作基础上,获得13株不同来源的本土酿酒酵母菌株。本研究对其生理特性和发酵特性进行探究,进而对其产香能力进行分析,初步筛选得到具有良好香气特征的本土酿酒酵母。
1 材料与方法
1.1 材料与试剂
前期研究获得不同来源的本土酿酒酵母菌株13株,由西北农林科技大学葡萄酒学院刘延琳教授实验室保藏。试验菌株为酿酒酵母XM1、XM2、XM3、XM4、XM5、XM6、XM7、XM8、XM9、XM10、XM11、XM12、XM13和1株商业对照菌株SY-CK。敏感菌株 Saccharomyces cerevisiae 1296 由西北农林科技大学食品学院馈赠。
47种色谱纯标准品(φ=98%),Sigma-Aldrich,如1-己醇、(E)-3-己烯-1-醇、(Z)-3-己烯-1-醇、橙花醇、苯乙醇、乙酸乙酯、辛酸等用于定量。
YPD培养基(g/L):葡萄糖20、蛋白胨20、酵母粉10,固体培养基中添加琼脂20。
MS300培养基:配方参考BELY等[12]的方法,将其含糖调整为250 g/L,其中葡萄糖与果糖的质量比为1∶1。
1.2 仪器与设备
高速冷冻离心机,Thermofisher;恒温摇床,上海福马实验设备有限公司;SW-CJ-1FD超净工作台,苏净集团苏州安泰空气技术有限公司;ES-1000HA电子天平,长沙湘平科技发展有限公司;高压灭菌锅;ELX800酶标仪,美国BioTek公司;安捷伦GC7890B气相色谱仪、Agilent 5977B气质联用仪,安捷伦科技有限公司。
1.3 实验方法
1.3.1 酵母种子液的制备
将保存在-80 ℃的本土酿酒酵母菌株划线培养2~3 d。挑取单菌落分别接种于含有30 mL筛选培养基的锥形瓶,置于150 r/min,28 ℃摇床活化24 h。
1.3.2 本土酿酒酵母的酒精耐受性
在YPD中加入不同体积分数的酒精进行酵母培养,测定细胞悬浮液吸光度(OD600):以10%(体积分数)的乙醇起始,3%递增,最大为16%(体积分数)的乙醇。
1.3.3 本土酿酒酵母的嗜杀性
酵母嗜杀性的测定参照DE ULLIVARRI等[13]的方法。
1.3.4 本土酿酒酵母的产硫化氢特性
将22 g BIGGY 琼脂培养基溶于500 mL无菌水中,煮沸约45~60 s灭菌。将活化后的菌液点样于BIGGY培养基,将接种后的BIGGY培养皿置于28 ℃的培养箱中培养4 d,观察菌落颜色。
1.3.5 菌株生长曲线测定
将-20 ℃保存的菌株接种于YPD液体培养基中,28 ℃、150 r/min条件下,活化24 h。取活化好的菌液按1×106 cells/mL的接种量接种于50 mL YPD液体培养基中,28 ℃,150 r/min振荡培养,每隔2 h取样1 mL,使用酶标仪在600 nm处测定菌悬液的吸光度OD600,以无菌YPD为对照。以培养时间为横坐标,OD600为纵坐标,绘制生长曲线。
1.3.6 模拟发酵
取-20 ℃甘油保藏菌液划线于YPD固体培养基,于28 ℃培养2 d,挑取单菌落于装有50 mL模拟汁的锥形瓶中,28 ℃,150 r/min 振荡培养48 h。
模拟发酵:配制模拟葡萄汁,对模拟汁进行无菌处理。将酵母种子液以1×106 cells/mL的接种量接种于装有300 mL模拟汁的锥形瓶中,25 ℃静置培养。发酵过程中通过检测还原糖监控发酵过程,连续3 d糖含量不变视为发酵结束。每组重复3次。发酵结束后,参照GB/T 15038—2006《葡萄酒、果酒通用分析方法》测定残糖、总酸和挥发酸,用密度瓶法测定酒精度。
1.3.7 香气测定
固相微萃取(solid-phase microextraction,SPME)与GC-MS结合用于鉴定和定量主要挥发物,参照LAN等[14]的方法。通过自动化的顶空固相微萃取提取葡萄酒样品中的挥发性化合物,并使用气相色谱/质谱法进行分析。将5 mL葡萄酒样品和1 g NaCl放入20 mL样品瓶中。将样品瓶用PTFE-硅隔垫盖紧,在加热平台上以400 r/min的转速在40 ℃下平衡30 min。将50/30 μm DVB/CAR/PDMS在40 ℃,250 r/min转速下吸附30 min。随后将萃取头在GC进样器中解吸8 min,固相微萃取自动进样采用不分流模式。质谱接口温度为280 ℃,离子源温度为230 ℃,电离方式EI,离子能源70 eV,质量扫描范围为29~350 u,GC循环时间67 min。
1.3.8 数据分析
采用SPSS 20.0软件进行数据分析处理,方差分析采用Duncan检验法,每组实验3个重复。采用Graphpad Prism 7.0软件进行绘图,Origin 2021进行主成分分析。
2 结果与分析
2.1 酒精耐性
如图1所示,在14株酿酒酵母中,菌株XM1、XM10、XM5、XM12均在酒精体积分数为10%和13%时具有显著较高的OD600值,其中体积分数为13%时,XM10具有较高的酒精耐性,XM8具有较弱的酒精耐性(OD600值<0.5)。在体积分数为16%时酿酒酵母的OD600值均<0.25,酵母在培养基中微量生长或不生长[15],即14株酿酒酵母均无耐受16%体积分数酒度的能力。高浓度的酒精引起酵母细胞膜流动性的增加[16],减少酵母葡萄糖转运和抑制酵母生长[17]。在葡萄酒酿造中选择酒精耐性良好的酿酒酵母,有助于酵母对糖的完全利用和葡萄酒的发酵彻底。

图1 不同酒精度对酵母生长的影响
Fig.1 The influence of alcohol on yeast growth 注:不同小写字母表示差异显著(P<0.05)(下同)
2.2 嗜杀性
如图2所示,在添加次甲基蓝的培养基中观察本土酵母对敏感菌株1296的嗜杀能力,蓝色抑菌圈直径越大则菌株的嗜杀能力越强。在14株酿酒酵母中,7株菌株具有嗜杀性。其中菌株XM12、XM11、XM10、XM1、XM8、XM3和XM5对于敏感菌株1296的嗜杀性较强,菌株XM8和XM3的嗜杀性较弱。一些具有嗜杀能力的酵母能分泌细胞外蛋白或糖蛋白,抑制其他敏感酵母和真菌的活性[18]。在酿酒工业中使用嗜杀酵母,可以减少腐败微生物对葡萄酒的负面影响[19],保证葡萄酒发酵风味的纯净。

图2 不同酿酒酵母对敏感菌株1296的嗜杀能力
Fig.2 The killer activity of S.cerevisiae strains against a sensitive strain 1296
2.3 产H2S能力
BD BIGGY琼脂培养基可以测试酵母产H2S的能力,菌落颜色越深则H2S产量越高,菌落颜色为白色则不产H2S。如图3所示,SY-CK、XM12、XM2、XM13、XM5(浅棕色)是低产硫化氢菌株,XM4、XM8、XM7、XM6、XM9、XM3、XM11是高产硫化氢菌株(深棕色),XM10、XM1是不产硫化氢菌株(白色)。葡萄酒酿造过程中,酿酒酵母主要通过硫酸盐还原途径产生H2S,葡萄汁中元素硫的高水平残留、二氧化硫和有机硫化合物的存在都会影响H2S的产量[20]。葡萄酒中H2S含量的增加带来还原味和腐烂臭鸡蛋的味道,降低葡萄酒的感官质量[21]。

图3 不同酵母产H2S能力
Fig.3 Evaluation of H2S production in yeast isolates
2.4 生长曲线
测定酵母生长曲线可以掌握酵母生长繁殖的规律,为酵母的培养时间和发酵所需的接种数量提供依据。如图4所示,14株酿酒酵母在6 h进入指数生长期,在14 h进入生长稳定期。其中XM12在稳定期的OD600值高于其他菌株,SY-CK在稳定期的OD600值低于其他菌株。

图4 酿酒酵母生长曲线
Fig.4 Growth curve of S.cerevisiae strains
2.5 发酵速率
对模拟发酵过程中的酵母生长量进行测定,如图5所示,菌株在第1天~第5天为指数生长期,在第7天进入生长稳定期。其中XM3在发酵前3 d OD600值增长较慢,在3 d后OD600值逐渐上升到3.4左右。14株菌株进入生长稳定期后,XM11的OD600相对较高为3.5左右;XM5、SY-CK、XM12的OD600值进入稳定期后相对较低在3.0以下。14株酵母发酵液的含糖量均在前7 d的发酵中快速下降。前7 d的发酵中,XM11发酵液的含糖量相对降低较快,XM3发酵液的含糖量相对降低较慢。XM3与XM11菌株消耗的糖含量与发酵过程中的菌株生物量变化相关联,最终在发酵完全所需的时间相同。其中,XM4菌株对含糖量发酵完全所需的时间最长,表现为发酵缓慢。
发酵液的基本理化指标见表1,XM12发酵产生的酒度最高为12.59%(体积分数),其他菌株发酵产生的酒度在11%~12.4%(体积分数)。14株菌株中,XM3产生的总酸含量显著较高,XM2、XM6和XM9产生的总酸含量较低。葡萄酒的挥发酸含量反应葡萄酒的健康程度,14株酵母产生的挥发酸含量都在0.60 g/L以下,符合葡萄酒生产的卫生标准。

a-OD值;b-含糖量
图5 酵母发酵过程的OD值、含糖量变化
Fig.5 Changes of OD value and sugar content during fermentation
表1 基本理化指标分析
Table 1 Basic physiochemical parameters in wine samples

菌株酒度/%残糖/(g·L-1)总酸/(g·L-1)挥发酸/(g·L-1)XM112.39±0.20ab3.01±0.31b10.34±0.15abc0.24±0.04bcXM212.06±0.09b3.44±0.19ab10.04±0.07c0.21±0.06cdXM312.05±1.19b3.53±0.58ab10.16±0.24a0.27±0.06abcXM411.98±0.09b3.59±0.5ab9.89±0.10abc0.15±0.12dXM512.38±0.07b3.55±0.37ab10.02±0.28ab0.29±0.00abcXM612.09±0.14ab3.82±0.2ab9.94±0.15c0.23±0.01bcdXM712.21±0.12ab3.41±0.31ab10.32±0.01abc0.25±0.01bcXM812.20±0.33ab3.54±0.29ab10.10±0.34abc0.33±0.05abXM911.88±0.30b3.88±0.1a10.58±0.17c0.27±0.01abcXM1012.34±0.17ab3.54±0.29ab10.02±0.17abc0.35±0.04aXM1111.87±0.24b3.54±0.29ab10.13±0.16abc0.29±0.00abcXM1212.59±0.11a3.46±0.18ab10.44±0.03abc0.28±0.02abcXM1312.21±0.20ab3.75±0.22ab10.47±0.07bc0.25±0.00abcSY-CK11.90±0.42b3.13±0.56ab10.22±0.12bc0.31±0.01ab
注:不同字母显示显著差异(Duncan检验,P<0.05);挥发酸以醋酸计
2.6 香气测定
对挥发性物质进行SPME-GC-MS分析,检测出47种挥发性化合物。包括乙酸酯4种,乙酯类8种,其他酯类4种,脂肪酸5种,高级醇8种,C6醇4种,苯乙基2种等,这些挥发性化合物对葡萄酒香气具有主要贡献。主要是香气成分分析如图6所示。

a-乙酸酯;b-乙基酯;c-其他酯;d-C6醇;e-高级醇;f-脂肪酸
图6 主要香气成分分析
Fig.6 Analysis of main volatile compounds
乙酸酯由乙酸和醇基(乙醇或氨基酸代谢衍生的复合醇)组成,在发酵过程中由微生物产生的酯酶和脂肪酶催化而成[22],包括乙酸乙酯(菠萝)、乙酸异丁酯(溶剂)、乙酸异戊酯(香蕉)、乙酸己酯(柑橘)等。乙酸乙酯是葡萄酒中含量最丰富的酯,是影响葡萄酒香气的重要因素[23]。14株酵母产生的乙酸乙酯含量均低于80 mg/L,给模拟酒带来水果香气。XM1、XM12产生的乙酸酯含量最高,主要由于其产生的乙酸乙酯含量最高。在这些乙酸酯化合物中,14株酵母产生的乙酸异丁酯含量均小于感官阈值,不会带来负面的溶剂味道。乙酸异戊酯能明显提升白葡萄酒的香气质量[24],14株菌株乙酸异戊酯含量均超过阈值,给模拟酒带来香蕉香气。乙酸己酯是酵母发酵的产物,与红色浆果香气有关[25],酵母产生的乙酸己酯含量都没有超过感官阈值。SY-CK、XM13产生的乙酸酯含量相对较高,而XM8、XM4和XM6产生的乙酸酯含量最少。
乙基酯由醇基(乙醇)和酸基组成,包括己酸乙酯(水果)、辛酸乙酯(橙子)、癸酸乙酯(水果)和丁酸乙酯(水果)等。在葡萄酒中乙基酯与果香和花香有关[26],在评价体系中具有高酯的葡萄酒均获得高分[10]。尽管酯的含量很少,相对于高级醇而言,挥发性酯对葡萄酒香气的影响更大。XM1和XM4产生的乙基酯含量最高,XM1产生显著较高的丁酸乙酯、己酸乙酯、辛酸乙酯、壬酸乙酯和癸酸乙酯,XM4则主要由月桂酸乙酯、乳酸乙酯和癸酸乙酯引起较高的乙基酯含量。XM8、XM10产生的乙基酯含量最低,其他菌株产生的乙基酯含量相近。大多数酵母产生的己酸乙酯、辛酸乙酯、癸酸乙酯超过其香气阈值,贡献树木果实的香气[27]。
XM3产生的丁二酸二乙酯(具有花香、果香和薰衣草香气)含量高于其他菌株含量的5倍以上,使其他酯的含量显著升高;XM2和XM11产生的其他酯含量最低。C6醇具有植物、草本类的香气,包括正己醇(花香)、Z-3-己烯-1-醇(青草)、E-3-己烯-1-醇(青草)、E-2-已烯-1-醇(花香)等。XM4的C6醇含量最高,主要由于产生较高的E-2-已烯-1-醇含量,XM1、XM3、SY-CK、XM13的C6醇含量最低。14株菌株产生的E-2-已烯-1-醇均高于其感官阈值,给模拟酒带来花香香气。
高级醇包括脂肪醇和芳香醇,主要包括异丁醇、苯乙醇和异戊醇等。在白葡萄酒中高级醇的总质量浓度在0.2~1.2 g/L,在红葡萄酒中总质量浓度为0.4~1.4 g/L[28],低于0.3 g/L会增加葡萄酒的果香和花香,而高于0.4 g/L的高级醇则会给葡萄酒带来不良风味[29]。在14株酵母都能产生少于0.3 g/L的高级醇,给葡萄酒香气带来正面影响。XM3产生的高级醇含量最多,主要由比其他菌株高2倍以上的异丁醇含量和显著较高的丙醇含量产生,XM5、XM12、SY-CK、XM10产生的高级醇含量最少。少量的脂肪酸对香气有积极作用,过多的脂肪酸含量产生令人不愉快的脂肪、奶酪香气[30]。XM5产生的总脂肪酸含量最高,主要由于其异丁酸产量较高,XM8、XM9、XM10、XM11、XM13产生的脂肪酸含量最少。
挥发性化合物的香气活力值(odor activity value,OAV)是每种化合物的含量与其检测阈值浓度的比率,对47种物质中OAV值>1的挥发性化合物计算平均值并进行主成分分析。主成分分析解释了前2个主成分(principal components,PC)的总方差为69.3%,PC1的比例为52.6%,PC2的比例为16.7%。由图7可知,XM2位于第一象限,成分包括异戊醇、乙酸乙酯、E-2-已烯-1-醇、β-紫罗兰酮、苯乙醇、辛酸乙酯等,对葡萄酒香气质量有积极作用。XM3、XM6、XM7、XM13和SY-CK位于第二象限,与异丁醇有关。XM1、XM4、XM5和XM12位于第四象限,与己酸乙酯、异丁酸、己酸、辛酸有关。XM9和XM10在则在PC1负半轴得分较高。

a-菌株;b-香气成分
图7 香气成分主成分分析
Fig.7 Principal component analysis of main volatile compounds
3 结论与讨论
使用本土来源的酿酒酵母有助于获得良好的酿造学结果,以13株本土酿酒酵母为研究对象,进行酵母的生理特性和发酵特性探究。获得XM10在乙醇的体积分数为13%时具有显著性酒精耐受性,以及具有嗜杀性和不产H2S特性。可以筛选用于高酒度葡萄酒的酿造,促进葡萄酒生产中酵母对糖的完全利用,以应对全球气候变暖使葡萄含糖量升高带来的挑战。XM12具有良好的酒精耐受性、嗜杀性和低产H2S特性,有助于葡萄酒发酵完全和减少低劣风味。发酵过程中XM4发酵完全所需的时间最长,不利于葡萄酒生产。XM11在发酵前期含糖量降低最快,在发酵进入稳定期后OD值最高。XM3在发酵前期含糖量降低最慢,OD值相对较低,发酵后期含糖量降低变快并最终能在13 d发酵完全,可以根据其不同发酵阶段的酿造学表现选择合适的酿造工艺。
发酵液共检测出47种香气成分,其中XM1和XM4的乙基酯产量最高。XM4的乙基酯和C6醇含量相对较高,C6醇赋予葡萄酒草本香气。主成分分析表明XM1位于第四象限,与己酸乙酯、异丁酸、己酸、辛酸等化合物有关。乙酯类会增加葡萄酒的水果香气,脂肪酸的产量和酯类含量的互作有待进一步探究。XM3位于第二象限,与异丁醇有关。初步筛选XM1为酯类物质产量较高的产酯酵母,XM3产生的其他酯和高级醇含量较高,其分子机理有待进一步探究。XM12具有良好的生理特性和产酯能力,有助于促进葡萄酒的风味纯净和提高葡萄酒品质。
[1] TIAN T, WU D, NG C T, et al.Uncovering mechanisms of greengage wine fermentation against acidic stress via genomic, transcriptomic, and metabolic analyses of Saccharomyces cerevisiae[J].Applied Microbiology and Biotechnology, 2020, 104(17):7 619-7 629.
[2] BERBEGAL C, FRAGASSO M, RUSSO P, et al.Climate changes and food quality:The potential of microbial activities as mitigating strategies in the wine sector[J].Fermentation, 2019, 5(4):85.
[3] HENDERSON C M, BLOCK D E.Examining the role of membrane lipid composition in determining the ethanol tolerance of Saccharomyces cerevisiae[J].Applied and Environmental Microbiology, 2014, 80(10):2 966-2 972.
[4] FENG L, JIA H, WANG J M, et al.Selection of indigenous Saccharomyces cerevisiae strains for winemaking in northwest China[J].American Journal of Enology and Viticulture, 2019, 70(2):115-126.
[5] FERNáNDEZ DE ULLIVARRI M, MENDOZA L M, RAYA R R.Characterization of the killer toxin KTCf20 from Wickerhamomyces anomalus, a potential biocontrol agent against wine spoilage yeasts[J].Biological Control, 2018, 121:223-228.
[6] GONZ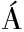 LEZ-BARREIRO C, RIAL-OTERO R, CANCHO-GRANDE B, et al.Wine aroma compounds in grapes:A critical review[J].Critical Reviews in Food Science and Nutrition, 2015, 55(2):202-218.
LEZ-BARREIRO C, RIAL-OTERO R, CANCHO-GRANDE B, et al.Wine aroma compounds in grapes:A critical review[J].Critical Reviews in Food Science and Nutrition, 2015, 55(2):202-218.
[7] STYGER G, PRIOR B, BAUER F F.Wine flavor and aroma[J].Journal of Industrial Microbiology and Biotechnology, 2011, 38(9):1 145-1 159.
[8] BISSON L F, KARPEL J E.Genetics of yeast impacting wine quality[J].Annual Review of Food Science and Technology, 2010, 1:139-162.
[9] YANG Y J, XIA Y J, WANG G Q, et al.Comparison of oenological property, volatile profile, and sensory characteristic of Chinese rice wine fermented by different starters during brewing[J].International Journal of Food Properties, 2017, 20.DOI:10.1080/10942912.2017.1325900.
[10] WANGY Q, YE D Q, LIU P T, et al.Synergistic effects of branched-chain amino acids and phenylalanine addition on major volatile compounds in wine during alcoholic fermentation[J].South African Journal of Enology and Viticulture, 2016, 37(2):169-175.
[11] LOPES C A, RODR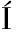 GUEZ M E, SANGORR
GUEZ M E, SANGORR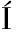 N M, et al.Patagonian wines:The selection of an indigenous yeast starter[J].Journal of Industrial Microbiology and Biotechnology, 2007, 34(8):539-546.
N M, et al.Patagonian wines:The selection of an indigenous yeast starter[J].Journal of Industrial Microbiology and Biotechnology, 2007, 34(8):539-546.
[12] BELY M, SABLAYROLLES J M, BARRE P.Automatic detection of assimilable nitrogen deficiencies during alcoholic fermentation in oenological conditions[J].Journal of Fermentation and Bioengineering, 1990, 70(4):246-252.
[13] DE ULLIVARRI M F, MENDOZA L M, RAYA R R, et al.Killer phenotype of indigenous yeasts isolated from Argentinian wine cellars and their potential starter cultures for winemaking[J].Biotechnology Letters, 2011, 33(11):2 177-2 183.
[14] LAN Y B, XIANG X F, QIAN X, et al.Characterization and differentiation of key odor-active compounds of ‘Beibinghong’ icewine and dry wine by gas chromatography-olfactometry and aroma reconstitution[J].Food Chemistry, 2019, 287:186-196.
[15] 冯莉, 陈雪, 李丽, 等.5株克鲁维毕赤酵母的酿造学特性[J].中国食品学报, 2018, 18(12):66-73.
FENG L, CHEN X, LI L, et al.The enology characteristics of five strains of Pichia kluyveri[J].Journal of Chinese Institute of Food Science and Technology, 2018, 18(12):66-73.
[16] ISHMAYANA S, KENNEDY U J, LEARMONTH R P.Further investigation of relationships between membrane fluidity and ethanol tolerance in Saccharomyces cerevisiae[J].World Journal of Microbiology and Biotechnology, 2017, 33(12):1-10.
[17] QIU Z L, JIANG R R.Improving Saccharomyces cerevisiae ethanol production and tolerance via RNA polymerase Ⅱ subunit Rpb7[J].Biotechnology for Biofuels, 2017, 10(1):125.
[18] LIU Z L, DU S, REN Y, et al.Biocontrol ability of killer yeasts (Saccharomyces cerevisiae) isolated from wine against Colletotrichum gloeosporioides on grape[J].Journal of Basic Microbiology, 2018, 58(1):60-67.
[19] BAJAJ B K, SINGH S.Yeast Diversity in Human Welfare[M].Singapore:Springer, 2017:163-190.
[20] HUANG C W, WALKER M E, FEDRIZZI B, et al.Hydrogen sulfide and its roles in Saccharomyces cerevisiae in a winemaking context[J].FEMS Yeast Research, 2017, 17(6).DOI:10.1093/femsyr/fox058.
[21] FRANCO-LUESMA E, S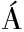 ENZ-NAVAJAS M P, VALENTIN D, et al.Study of the effect of H2S, MeSH and DMS on the sensory profile of wine model solutions by Rate-All-That-Apply (RATA)[J].Food Research International, 2016, 87:152-160.
ENZ-NAVAJAS M P, VALENTIN D, et al.Study of the effect of H2S, MeSH and DMS on the sensory profile of wine model solutions by Rate-All-That-Apply (RATA)[J].Food Research International, 2016, 87:152-160.
[22] PLATA C, MILL N C, MAURICIO J C, et al.Formation of ethyl acetate and isoamyl acetate by various species of wine yeasts[J].Food Microbiology, 2003, 20(2):217-224.
N C, MAURICIO J C, et al.Formation of ethyl acetate and isoamyl acetate by various species of wine yeasts[J].Food Microbiology, 2003, 20(2):217-224.
[23] NIU Y W, WANG P P, XIAO Z B, et al.Evaluation of the perceptual interaction among ester aroma compounds in cherry wines by GC-MS, GC-O, odor threshold and sensory analysis:An insight at the molecular level[J].Food Chemistry, 2019, 275:143-153.
[24] VAN DER MERWE C A, VAN WYK C J.The contribution of some fermentation products to the odor of dry white wines[J].American Journal of Enology and Viticulture, 1981, 32(1):41-46.
[25] DENNIS E G, KEYZERS R A, KALUA C M, et al.Grape contribution to wine aroma:Production of hexyl acetate, octyl acetate, and benzyl acetate during yeast fermentation is dependent upon precursors in the must[J].Journal of Agricultural and Food Chemistry, 2012, 60(10):2 638-2 646.
[26] PINEAU B, BARBE J C, VAN LEEUWEN C, et al.Examples of perceptive interactions involved in specific “red-” and “black-berry” aromas in red wines[J].Journal of Agricultural and Food Chemistry, 2009, 57(9):3 702-3 708.
[27] FERREIRA V, FERN NDEZ P, PE
NDEZ P, PE A C, et al.Investigation on the role played by fermentation esters in the aroma of young Spanish wines by multivariate analysis[J].Journal of the Science of Food and Agriculture, 1995, 67(3):381-392.
A C, et al.Investigation on the role played by fermentation esters in the aroma of young Spanish wines by multivariate analysis[J].Journal of the Science of Food and Agriculture, 1995, 67(3):381-392.
[28] CAMELEYRE M, LYTRA G, TEMPERE S, et al.Olfactory impact of higher alcohols on red wine fruity ester aroma expression in model solution[J].Journal of Agricultural and Food Chemistry, 2015, 63(44):9 777-9 788.
[29] ESCRIBANO-VIANA R, GONZ LEZ-ARENZANA L, PORTU J, et al.Wine aroma evolution throughout alcoholic fermentation sequentially inoculated with non-Saccharomyces/Saccharomyces yeasts[J].Food Research International, 2018, 112:17-24.
LEZ-ARENZANA L, PORTU J, et al.Wine aroma evolution throughout alcoholic fermentation sequentially inoculated with non-Saccharomyces/Saccharomyces yeasts[J].Food Research International, 2018, 112:17-24.
[30] LAMBRECHTS M G, PRETORIUS I S.Yeast and its importance to wine aroma-a review[J].South African Journal of Enology Viticulture, 2019, 21(1):97-129.