纳米银颗粒(silver nanoparticles,AgNPs),因其具备特殊的理化性能,主要作为保鲜和抗菌材料被广泛应用于食品贮藏保鲜、纺织制造、化妆品、信息材料和医疗抗菌等领域[1-4]。其中,纳米银作为涂膜或复合涂膜保鲜剂应用于果蔬保鲜,可延缓果蔬的衰老和改进果蔬的食用品质,使其货架期得到延长。近年来,纳米银涂膜技术由于具有广谱杀菌、快捷方便、保鲜效果明显和成本低等优点,在果蔬保鲜领域有巨大的应用潜力,引起了众多科研工作者的兴趣,使纳米银粒子的绿色制备成为当前纳米技术研究热点之一[5-6]。然而,纳米银的功能特性与其尺寸、形态和粒径分布密切相关[7]。因此,研究纳米银颗粒的制备以及其粒径的大小和形貌的控制对纳米银应用于果蔬贮藏保鲜方面具有重要意义。
现阶段,制备纳米银颗粒的方法主要有物理法、化学法和生物还原法。物理方法原理简单,制备的纳米银颗粒纯度高,但合成的纳米银颗粒粒径不均匀,易发生团聚,而且对仪器设备的要求很高、能源消耗大[8]。化学法对设备要求较为简单,但化学法通常会使用一些化学试剂,产生许多有害的副产品,对环境造成危害[9]。近年来,随着环保意识的增强,绿色合成法在纳米银的合成中逐渐受到研究人员的青睐。绿色合成法即生物还原法,其包括植物合成法和微生物合成法[10]。绿色合成法是指利用无毒、无污染、无害的原料来制备纳米银,该法较物理法具有能耗小、成本低且合成简单等优点,较化学法具有绿色环保、可再生性和反应条件温和等优点,该法合成纳米银对营造良好的生态环境有积极影响[11]。
目前,我国每年产生大量的芒果皮废弃物,但对芒果皮废弃物的高值化利用研究却较少,利用芒果皮浸提液制备纳米银的报道更少。芒果皮中含有丰富的黄酮化合物、维生素C、多酚化合物和芒果甙类等物质,其中的羟基和醛基起还原的作用,是天然的还原剂[10,12]。将芒果皮用作还原剂绿色合成纳米银颗粒,既提高了芒果的附加值和利用率,又避免资源浪费和环境污染[12-13]。同时,纳米银是否成功制备可从其颜色变化来直观判断,且其反应时间、反应温度、芒果皮浸提液浓度、硝酸银浓度和十二烷基硫酸钠(sodium dodecyl sulfate,SDS)添加量是影响形貌特征、尺寸大小和分布状况的重要因素[14]。因此,本研究以硝酸银为银源,芒果皮浸提液为还原剂,采用生物还原法,探索制备条件对AgNPs颜色、形貌和粒径的影响,为纳米银粒子的可控合成提供理论和实践依据。
1 材料与方法
1.1 材料与试剂
硝酸银(分析纯)、粉状SDS,成都市科龙化工试剂厂;芒果,四川攀枝花凯特农贸市场。
1.2 实验设备
MDSH i3x型酶标仪,美谷分子仪器有限公司;UV3 600型紫外-可见分光光度计,日本岛津公司;Nano ZS型马尔文激光粒度仪,上海思百吉仪器系统有限公司;Tecnai g20型透射电子显微镜,美国FEI公司;Thermo fisher Nicolet 6700型傅立叶变换红外(Fourier transform infrared,FTIR)光谱仪,美国Thermo Fisher Scientific公司。
1.3 实验方法
1.3.1 芒果皮浸提液的制备
用蒸馏水清洗新鲜芒果皮后,切成碎片,称量25 g芒果皮加入100 mL超纯水并榨成汁。将得到的混合液在85 ℃水浴中加热30 min,自然冷却抽滤后,在2 000 r/min下离心10 min,将上清液抽滤,用0.45 μm的微孔滤膜过滤后得到芒果皮浸提液。将芒果皮浸提液于4 ℃下储存备用。
1.3.2 硝酸银溶液的制备
准确称量0.425 g硝酸银,将其溶于超纯水并定容至50 mL,配制成50 mmol/L的硝酸银溶液,取其制备浓度为1.5 mmol/L的硝酸银溶液,并低温避光储存。
1.3.3 纳米银末粉的制备
称取0.06 g SDS于烧杯中,倒入25 mL硝酸银溶液和2 mL芒果皮浸提液,加热搅拌至溶液颜色变为棕黄色,表明已制备出纳米银溶胶。反应完成后,反应液在10 000 r/min条件下离心10 min,除去上清液,将沉淀用超纯水超声分散5 min后再次离心10 min,重复3次,将所得沉淀真空冷冻干燥,得到纳米Ag粉,储存于无水乙醇中备用[15-16]。
1.3.4 结构与性能表征
通过纳米银颜色、粒径、紫外可见吸收光谱(ultraviolet and visible spectrophotometry,UV-vis)分析反应时间、反应温度、浸提液添加量、硝酸银浓度、SDS添加量对制备纳米Ag的影响。
(1)纳米Ag的粒径测定
采用马尔文激光粒度仪(25 ℃下)对制备的纳米Ag溶胶的粒径进行表征。
(2)UV-vis的测定
使用酶标仪测定AgNPs的SPR峰,在300~500 nm内,带宽2 nm的条件下测定纳米Ag溶胶的吸光值,初步检测是否有纳米Ag合成并比较纳米Ag的粒径。
(3)纳米Ag透射电子显微镜(transmission electron microscope,TEM)表征
参考刘冲冲等[17]的方法对AgNPs的形貌及分散情况用透射电子显微镜进行表征。将均匀分散的5 μL纳米银溶液滴加在覆炭铜网上,室温干燥后并固定在仪器采样台。在点分辨率0.24 nm、线分辨率0.14 nm和加速电压200 kV的条件下测试。
(4)FTIR分析
采用FTIR对制备的纳米Ag颗粒表面吸附情况进行表征。将纳米Ag溶液充分干燥后,采用KBr压片法测定红外光谱。扫描次数32次,分辨率4 cm-1,检测波数范围为400~4 000 cm-1。
1.3.5 数据统计分析
采用SPSS 20.0和OriginPro 8.5.1软件进行数据分析处理与作图,并进行显著性分析,显著性水平P<0.05,试验重复3次,结果以![]() 表示。
表示。
2 结果与讨论
2.1 反应时间的影响
以不同反应时间(0.5、1.0、1.5、2.0、2.5和3.0 h)制备银纳米溶胶(其他反应条件不变),结果见图1。溶液颜色从淡黄色变为棕黄色(图1-a),不同反应时间的吸收峰均约在420 nm左右处(图1-b),表明有纳米Ag生成,可能是芒果皮浸提液与银离子的反应几率较大[18]。并且合成的纳米Ag溶胶浓度先增大后减小,表明在反应开始时,银离子未完全被还原,随着时间增加,纳米银颗粒团聚而沉淀。反应初期,AgNPs粒径缓慢增加,反应1 h后迅速增长(图1-c),这是因为AgNPs浓度增加到一定程度,晶粒产生奥斯特瓦尔熟化现象,粒子间的碰撞聚集几率增大[19]。因此,反应时间为1 h时,合成的纳米Ag产量高、粒径小。

a-颜色图;b-紫外吸收光谱;c-反应时间对粒径的影响
图1 反应时间对纳米Ag溶胶颜色、紫外-可见吸收光和粒径的影响
Fig.1 Effect of reaction time on color,UV-Vis absorption and particle size of AgNPs sol
2.2 反应温度的影响
以不同反应温度(65、70、75、80、85和90 ℃)制备银纳米溶胶(其他反应条件不变),结果见图2。反应体系的颜色随反应温度升高而加深(图2-a)。吸收峰强度呈现先增大后降低的趋势(图2-b),纳米Ag浓度随温度升高先增大后减小。温度为65和70 ℃时,呼吸峰弱,呼吸峰值不同,只产生极少的AgNPs。当温度≥75 ℃时,均在410 nm附近出现明显吸收峰,表明有大量AgNPs生成[7]。从图2-c可知,反应体系的粒径随温度升高先减小后增大,且在75 ℃时粒径最小。因此,适当高温有利于AgNPs快速形成。然而,在高温下反应速率太快,稳定剂无法包裹AgNPs颗粒,出现二次团聚,使生成AgNPs的粒径增大。综上,选取温度为75 ℃制备纳米Ag。
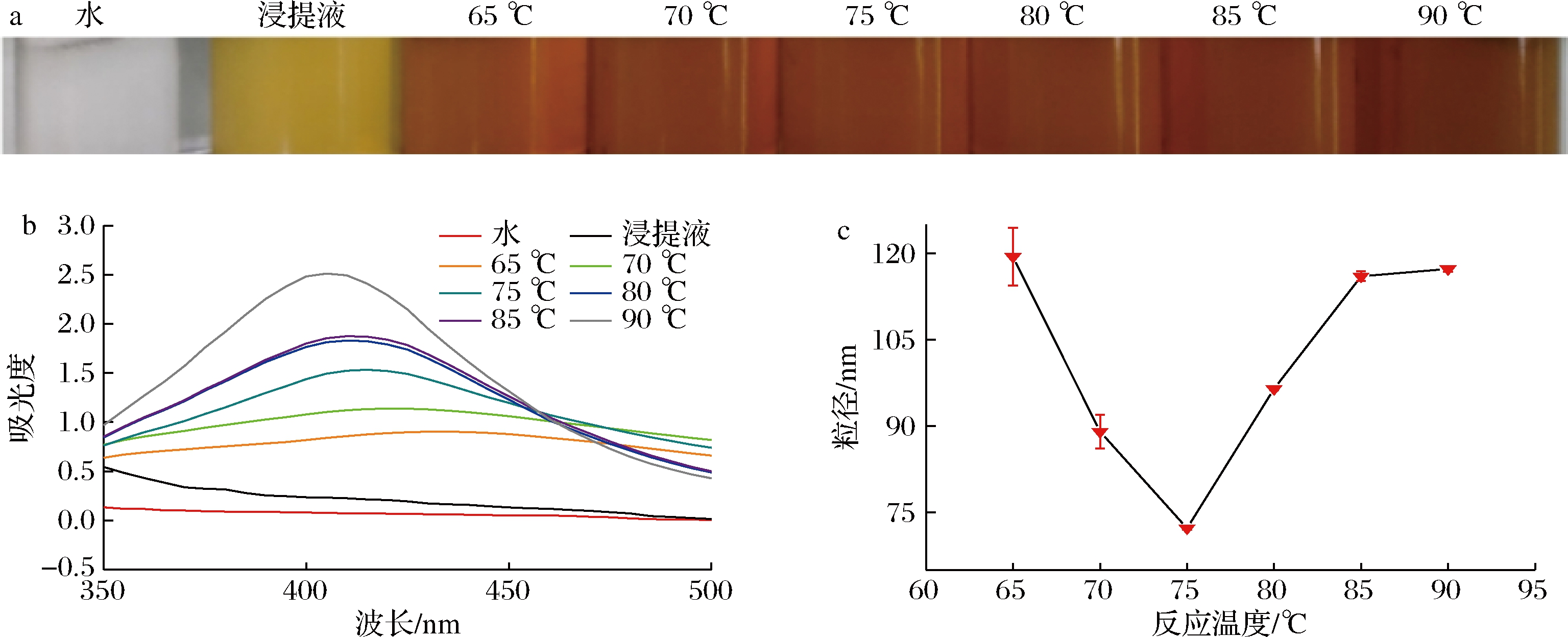
a-颜色图;b-紫外吸收光谱图;c-反应温度对粒径的影响
图2 反应温度对纳米Ag溶胶颜色、紫外-可见吸收光和粒径的影响
Fig.2 Effect of reaction temperature on color,UV-Vis absorption and particle size of AgNPs sol
2.3 芒果皮浸提液浓度的影响
以不同浸提液质量浓度(0.10、0.15、0.20、0.25、0.30和0.35 g/mL)制备银纳米溶胶(其他反应条件不变),结果如图3所示。反应体系的颜色随芒果皮浸提液浓度增大而加深(图3-a),且其吸收峰值逐渐增大(图3-b),吸收峰位置有红移现象,表明纳米Ag发生团聚[18]。芒果皮浸提液的质量浓度增大到0.2 g/mL时(图3-c),合成纳米Ag的粒径开始迅速增大,纳米Ag粒径与峰位置移动的变化趋势是一致的。SONG等[20]在研究木兰叶提取物合成纳米Ag时,也得到类似结论,可能是形成的原子核表面积累较多还原基团,增加了纳米Ag合成速率。另一方面,AgNPs增长速率由自由Ag+扩散速率决定,随着反应的进行,AgNPs晶核生成量增加,反应速率加快,使纳米银浓度上升过快而聚沉[7,19]。所以,选择质量浓度为0.20 g/mL的芒果皮浸提液来制备纳米Ag。

a-颜色图;b-紫外吸收光谱图;c-芒果皮浸提液浓度对粒径的影响
图3 芒果皮浸提液浓度对纳米Ag溶胶颜色、紫外-可见吸收光和粒径的影响
Fig.3 Effect of mango peel extract concentration on color,UV-Vis absorption and particle size of AgNPs sol
2.4 硝酸银浓度的影响
以不同硝酸银浓度(0.2、0.5、1.0、1.5、2.0和2.5 mmol/L)制备纳米银溶胶(其他反应条件不变),结果见图4。随着硝酸银浓度增加,反应体系颜色逐渐加深(图4-a)。当硝酸银浓度为0.2 mmol/L时,无明显的吸收峰(图4-b),表明无AgNPs生成。硝酸银浓度为1.0~2.5 mmol/L时,吸收峰位置变化微小,说明继续增加浓度对AgNPs合成量影响小。当硝酸银浓度<2.0 mmol/L时,纳米Ag粒径<80 nm,>2.0 mmol/L后纳米Ag的粒径迅速增大(图4-c)。这可能是当晶核浓度处于过饱和状态时,新合成的纳米银富集在晶核表面合成新的晶核,使AgNPs的粒径增大[12]。另一方面,AgNPs浓度过大引起部分AgNPs聚集沉降,导致AgNPs的UV-vis特征吸收峰强度减弱[21]。综上所述,在2.0 mmol/L硝酸银浓度下合成的纳米Ag浓度和密度均较高,且颗粒尺寸较小。

a-颜色图;b-紫外吸收光谱图;c-硝酸银浓度对粒径的影响
图4 硝酸银浓度对纳米Ag溶胶颜色、紫外-可见吸收光和粒径的影响
Fig.4 Effect of AgNO3 concentration on the color,UV-Vis absorption and particle size of AgNPs sol
2.5 SDS添加量的影响
以不同SDS添加量(0.03、0.06、0.09、0.12、0.15和0.18 g)制备银纳米溶胶(其他反应条件不变),结果见如图5。反应体系颜色随SDS添加量的增加先变浅后加深(图5-a),且在添加量≤0.15 g时,吸收峰强度随SDS添加量的增大而增大,其峰位置左移(图5-b)。增加添加量到0.18 g时,合成量反而减少。这表明增大SDS添加量有利于纳米Ag合成,但不是越大越好。由图5-c可知,纳米Ag粒径随SDS添加量的增大而减小。当添加SDS较低,合成AgNPs相应较少,但其粒径较大,使纳米Ag溶胶的颜色变深和吸收峰强度降低;随着添加量进一步增加,合成纳米Ag的粒径减小,合成数量却增加,使纳米Ag溶胶的颜色加深。而过量添加SDS会吸附纳米Ag粉体,阻碍纳米Ag的合成,从而减少被还原的纳米银粒子。因此,选择SDS添加量为0.15 g来合成纳米Ag。
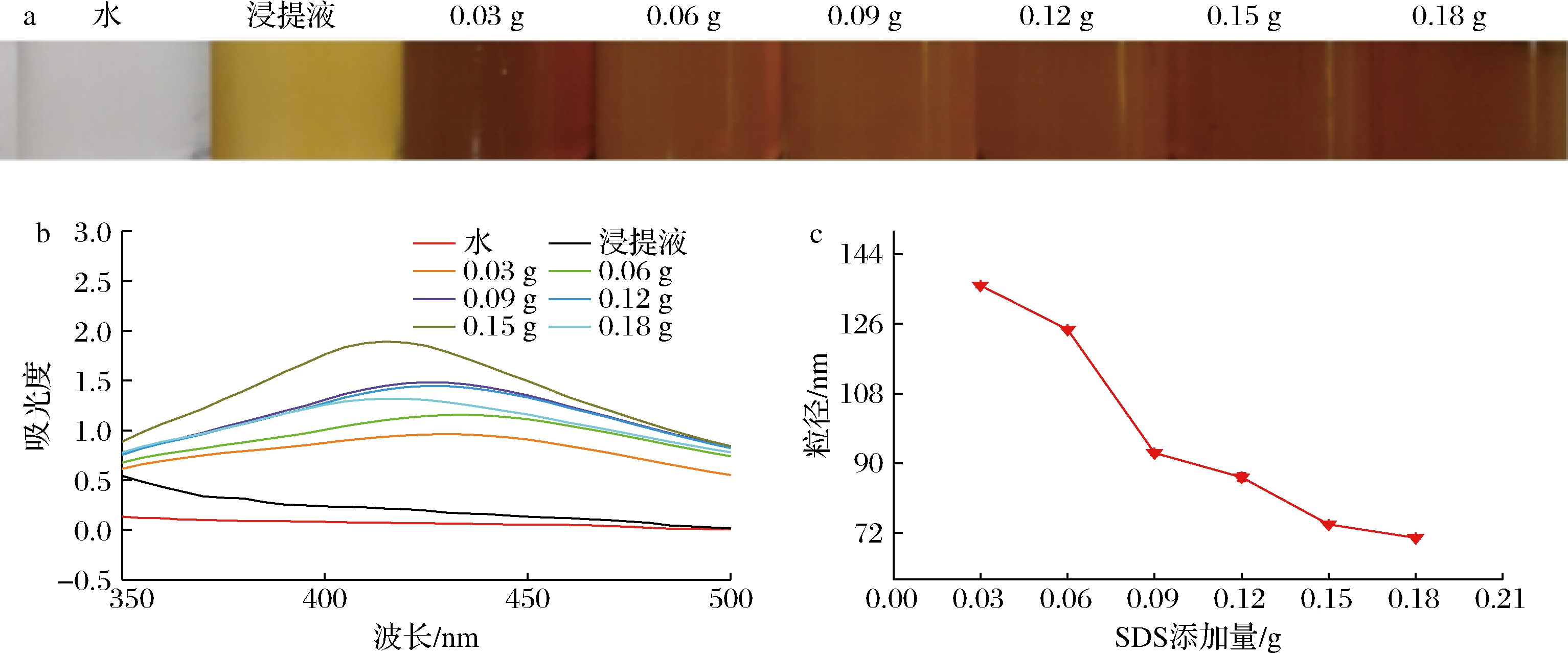
a-颜色图;b-紫外吸收光谱图;c-分散剂添加量对粒径的影响
图5 分散剂添加量对纳米Ag溶胶颜色、紫外-可见吸收光和粒径的影响
Fig.5 Effect of dispersant addition on color,UV-Vis absorption and particle size of AgNPs sol
2.6 TEM和FTIR对纳米银表征分析
2.6.1 不同浓度芒果皮浸提液制备的纳米银的粒径及形貌
如图6所示,AgNPs的粒径随浸提液浓度增大而增大,且不同浓度浸提液可制备出不同形状的纳米Ag颗粒。当质量浓度为0.15和0.25 g/mL时,合成的纳米Ag为球形;当浸提液质量浓度为0.35 g/mL时,纳米Ag从球形变为棒状。这可能和晶核生长速度有关。当芒果皮浸提液浓度低时,纳米Ag成核速率缓慢,各个晶面的生长速率差异微弱,使最终产物形成类球体。进一步增加芒果皮浸提液浓度,体系反应速率加快,使其晶核朝着某一方向生长,形成棒状的纳米银粒子[22]。所得到的纳米Ag粒径范围为25~70 nm,小于激光粒度仪测定的纳米银的粒径。

a-0.15 g/mL;b-0.25 g/mL;c-0.35 g/mL
图6 不同浓度芒果皮浸提液制备纳米Ag的透射电镜图
Fig.6 Transmission electron microscope of AgNPs prepared by
mango peel extract with different concentrations
2.6.2 纳米银红外吸收光谱
利用FTIR鉴定提取液中起还原作用的官能团,其红外光谱图见图7。在1 083.2,1 218.7,1 467.4,1 642.4,2 850.1,2 918.1,3 452.5 cm-1处有峰,均为含—OH的物质所产生的。芒果皮浸提液中本身含有—OH、—COH等基团,其作为封端剂使纳米Ag更稳定,并且包覆在纳米Ag表面,可能是电镜观察到的纳米Ag粒径比激光粒度仪测得粒径要小。另外,芒果皮浸提液中的氨基、羟基、羧基起还原作用,与纳米Ag形成稳定的—N—H···Pd、—C—O···Pd和—CO—O···Pd等键合作用,不仅增加产物稳定性,而且改变纳米Ag晶核生长的方向[22]。
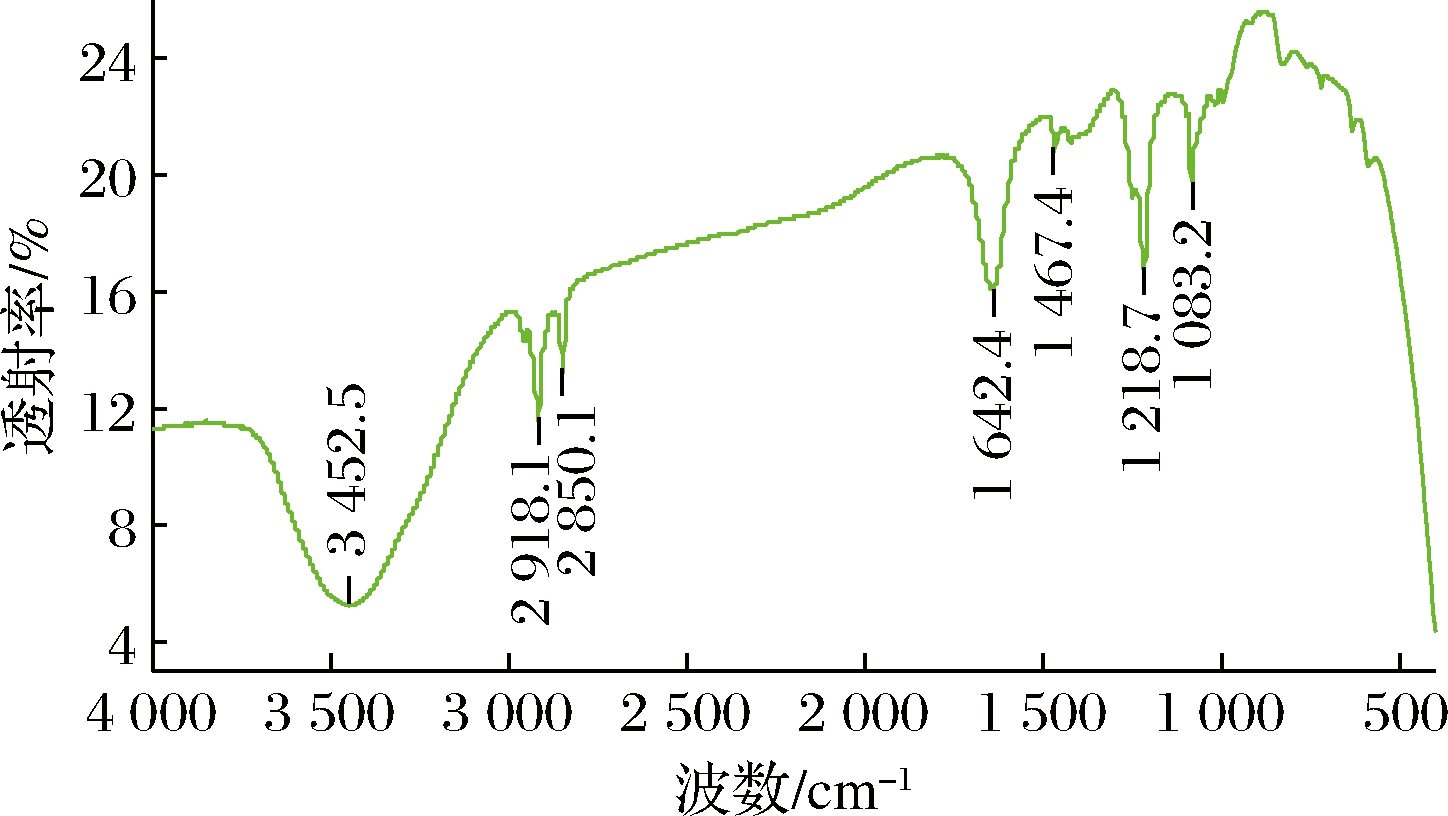
图7 纳米Ag粒子的红外光谱图
Fig.7 Infrared spectrum of silver nanoparticles
3 结论
通过改变不同制备条件,对纳米银粒径和形貌有较大的影响。可得出以下结论:(1)纳米银的颜色随时间、温度、芒果皮和硝酸银浸提液浓度增加均呈加深趋势,但随分散剂增加先变浅后加深。(2)纳米银的浓度随各条件参数增加而增加,但过量使其聚沉而浓度降低。(3)制得的纳米银分布均匀,且粒径均在25~70 nm。(4)各因素的最佳制备条件为反应时间1 h,反应温度75 ℃,芒果皮浸提液质量浓度0.20 g/mL,硝酸银浓度2.0 mmol/L,SDS添加量0.15 g。利用芒果皮浸提液合成纳米银,使芒果副产物得到高值化利用,且绿色环保。然而,芒果皮浸提液合成纳米银的反应机理尚不明确,还需进一步深入研究。本研究为纳米银应用于果蔬保鲜提供理论依据,对解析芒果皮合成AgNPs机制有重要的指导作用。
[1] 王馨,胡文忠,陈晨,等.纳米材料在果蔬保鲜中的应用[J].食品与发酵工业,2017,43(1):281-286.
WANG X,HU W Z,CHEN C,et al.Application of nanomaterials in storage of fruits and vegetables[J].Food and Fermentation Industries,2017,43(1):281-286.
[2] 刘小莉,图尔荪阿依,图尔贡,等.纳米银对革兰氏阴性水产品腐败菌的抑制作用[J].中国食品学报,2019,19(11):186-190.
LIU X L,TURS A Y,TUR G,et al.Inhibitory activity of silver nanoparticles against gram-negative bacteria in spoiled fishes[J].Journal of Chinese Institute of Food Science and Technology,2019,19(11):186-190.
[3] 高雪.纳米银的制备及其对羊毛织物的整理[D].天津:天津工业大学,2020.
GAO X.Preparation of nano silver and its finishing of wool fabric[D].Tianjin:Tianjin Polytechnic University,2020.
[4] ALKHULAIFI M M,ALSHEHRI J H,ALWEHAIBI M A,et al.Green synthesis of silver nanoparticles using Citrus limon peels and evaluation of their antibacterial and cytotoxic properties[J].Saudi Journal of Biological Sciences,2020,27(12):3 434-3 441.
[5] 杨斌,曹银娟,余群力,等.纳米银酯化淀粉膜对牛肉保鲜的影响[J].食品科学,2019,40(23):199-205.
YANG B,CAO Y J,YU Q L,et al.Application of nanosilver esterified starch film in beef preservation[J].Food Science,2019,40(23):199-205.
[6] 龙娅,胡文忠,萨仁高娃,等.鲜切果蔬精准保鲜包装技术的研究进展[J].食品与发酵工业,2019,45(12):249-256.
LONG Y,HU W Z,SAREN G W,et al.Precise fresh-keeping packaging for fresh-cut fruits and vegetables[J].Food and Fermentation Industries,2019,45(12):249-256.
[7] 吴宗山,李莉.天然产物绿色合成小尺寸纳米银及抗菌性[J].精细化工,2014,31(8):964-968;973.
WU Z S,LI L.Green synthesis of small size silver nanoparticles by nature product and their antimicrobial properties[J].Fine Chemicals,2014,31(8):964-968;973.
[8] 陶晶,付争伟,董春法,等.芦荟叶提取物绿色制备单分散纳米金及其性能(英文)[J].稀有金属材料与工程,2019,48(11):3 470-3 475.
TAO J,FU Z W,DONG C F,et al.Green synthesis and characterization of monodisperse gold nanoparticles using aloe vera leaf extract[J].Rare Metal Materials and Engineering,2019,48(11):3 470-3 475.
[9] NILUXSSHUN M C D,MASILAMANI K,MATHIVENTHAN U,et al.Green synthesis of silver nanoparticles from the extracts of fruit peel of Citrus tangerina,Citrus sinensis,and Citrus limon for antibacterial activities[J].Bioinorganic Chemistry and Applications,2021.DOI:10.1155/2021/6695734.
[10] 彭红,刘洋,袁林,等.银纳米粒子材料制备研究进展[J].现代化工,2017,37(7):23-28.
PENG H,LIU Y,YUAN L,et al.Progress in preparation of silver nanoparticle materials[J].Modern Chemical Industry,2017,37(7):23-28.
[11] 朱雨婕,代安然,李佳铭,等.金针菇无细胞滤液合成纳米银颗粒[J].食品与发酵工业,2021,47(5):71-78.
ZHU Y J,DAI A R,LI J M,et al.Synthesis of silver nanoparticles using cell-free filtrate of Flammulina velutipes[J].Food and Fermentation Industries,2021,47(5):71-78.
[12] 杨宁,郝林,杨鹏.芒果皮提取物合成纳米银及抑菌性研究[J].山西农业大学学报(自然科学版),2013,33(1):59-65.
YANG N,HAO L,YANG P.Mango peel extract mediated novel route for synthesis of silver nanoparticles and antibacterial application of silver nanoparticles[J].Journal of Shanxi Agricultural University(Natural Science Edition),2013,33(1):59-65.
[13] 付锐平,董春法,郭小燕,等.桔子皮提取液绿色可控制备单分散纳米银的研究[J].电子元件与材料,2021,40(1):30-35.
FU R P,DONG C F,GUO X Y,et al.Green and controllable synthesis of monodisperse silver nanoparticles by using orange peel extract[J].Electronic Components and Materials,2021,40(1):30-35.
[14] 张青山,岳秀萍.纳米银粒子的生物制备及应用研究进展[J].材料导报,2014,28(1):53-58.
ZHANG Q S,YUE X P.Research progress of biological preparation and application of silver nanoparticles[J].Materials Review,2014,28(1):53-58.
[15] 曹雪玲,陆书来,张东杰,等.纳米银作为抗菌剂的抗菌性能研究[J].吉林化工学院学报,2017,34(11):30-34.
CAO X L,LU S L,ZHANG D J,et al.Study on antimicrobial activity of nano silver as antimicrobial agents[J].Journal of Jilin Institute of Chemical Technology,2017,34(11):30-34.
[16] 姚平,邢铁玲,陈国强.杜仲纳米银的制备及其对直接橙26的催化还原降解[J].纺织学报,2018,39(1):104-110.
YAO P,XING T L,CHEN G Q.Biosynthesis of Eucommia ulmoides silver nanoparticles and application thereof in reductive catalytic degradation of Direct Orange 26[J].Journal of Textile Research,2018,39(1):104-110.
[17] 刘冲冲,王磊,徐慧,等.姜提取物生物合成纳米银抑菌活性的研究[J].食品与生物技术学报,2017,36(6):590-597.
LIU C C,WANG L,XU H,et al.Antibacterial study of silver nanoparticles biosynthesized with ginger extract[J].Journal of Food Science and Biotechnology,2017,36(6):590-597.
[18] 薛海燕,张颖,张宝艳,等.安石榴苷还原壳聚糖/纳米银溶胶制备表征及其抑菌性能[J].农业工程学报,2018,34(4):306-314.
XUE H Y,ZHANG Y,ZHANG B Y,et al.Preparation characterization and bacteriostatic properties of punicalagin reducing chitosan/nano silver Sol[J].Transactions of the Chinese Society of Agricultural Engineering,2018,34(4):306-314.
[19] 吴宗山.纳米银的可控制备及其抗菌性研究[D].北京:北京林业大学,2015.
WU Z S.Controllable preparation of silver nanoparticles and its antibacterial property[D].Beijing:Beijing Forestry University,2015.
[20] SONG J Y,KIM B S.Rapid biological synthesis of silver nanoparticles using plant leaf extracts[J].Bioprocess and Biosystems Engineering,2009,32(1):79-84.
[21] 司友琳,张胜义,闵宏林.Ag/TiO2纳米复合物的模板法制备及其性质研究[J].硅酸盐通报,2010,29(1):72-76.
SI Y L,ZHANG S Y,MIN H L.Preparation and characterization of silver deposited nano-TiO2 through the chitosan template method[J].Bulletin of the Chinese Ceramic Society,2010,29(1):72-76.
[22] 秦聪丽,傅吉全.桑叶提取物还原制备钯纳米颗粒[J].贵金属,2016,37(3):29-32.
QIN C L,FU J Q.Preparation of palladium nanoparticles using mulberry leaf extract[J].Precious Metals,2016,37(3):29-32.