鮰鱼(Leiocassis longirostris)俗称肥王鱼、淮王鱼等,是我国重要的淡水养殖水产品之一,2020年的产量为30.85万t[1]。鮰鱼肉嫩且味美,富含蛋白质和脂肪,被誉为淡水鱼中的食用上品。鮰鱼最美味之处在于软边的腹部,常被加工成冻鱼片,但会产生约40%~55%的副产物,如鱼骨、鱼皮、鱼鳞等[2]。其中,鮰鱼骨含有丰富的蛋白质、不饱和脂肪酸、矿物质元素等营养成分,钙磷比接近2∶1,易被人体吸收,是一种优良的补钙食物资源[3]。但鮰鱼骨质构坚硬,不便利用,目前主要被加工成动物饲料,造成资源浪费。
钙是人体中必需的矿物质营养素,对维持人体正常的新陈代谢和酸碱平衡起着重要的作用。约99%的钙以羟基磷灰石的形式存在于骨骼、牙齿中。缺钙则易导致骨质疏松、佝偻病等疾病,且多发生在中老年和儿童群体中[4]。根据《中国居民膳食营养素参考摄入量(2013版)》显示,中国成年居民每日的钙推荐摄入量在800~1 000 mg,而人们实际每日摄入钙量低于400 mg[5],因此,补钙至关重要。目前,市场上常见的补钙制剂有无机钙、有机酸钙、有机钙等,但部分产品存在吸收率低、补钙效果差等问题,无法满足当代群体对补钙的需求[6-7]。研究表明,肽-钙螯合物具有溶解性好、易吸收、生物利用率高且无毒副作用等优点,逐渐成为人们一种理想选择的补钙剂[8]。如ZHANG等[9]研究证明,肽-钙螯合物可提高肠道的钙生物利用率,从而改善大鼠的骨质疏松问题。因此,基于低值鮰鱼骨制备蛋白水解物,开发新型钙制剂,不仅可以丰富钙制剂的种类,还能提高鱼骨资源利用率,降低环境污染,促进渔业产品的经济效益。
本文以鮰鱼骨为原料,以钙结合能力为指标,采用单因素试验优化制备胶原多肽的酶解工艺,采用Sephadex G-25进行分离纯化,筛选出与钙结合活性较好的胶原多肽组分。制备胶原多肽-钙螯合物,通过傅里叶红外光谱、扫描电镜、能谱分析技术探究鮰鱼骨胶原多肽螯合前后的形态结构变化,最后对胶原多肽-钙螯合物的热稳定性、酸碱稳定性、体外模拟消化稳定性进行评价,为其生物利用率提供理论依据。
1 材料与方法
1.1 材料与仪器
1.1.1 材料与试剂
冷冻鮰鱼脊骨,由安徽富煌三珍公司提供。
S1063S钙含量显色检测试剂盒,上海碧云天生物技术有限公司;碱性蛋白酶(200 000 U/g)、胃蛋白酶(250 U/mg)、胰蛋白酶(250 U/mg),北京索莱宝科技有限公司;细胞色素C(12 384 Da),阿拉丁试剂(上海)有限公司;抑肽酶(6 511.51 Da)、L-氧化型谷胱甘肽(612.63 Da)、羟脯氨酸(131.13 Da),上海源叶生物科技有限公司;CaCl2,西陇科学股份有限公司;三氟乙酸(trifluoroacetic acid,TFA)、乙腈(acetonitrile,ACN),赛默飞世尔科技有限公司。
1.1.2 仪器与设备
S—3400 N扫描电子显微镜,日本Hitachi公司;Spectrum One傅立叶变换红外光谱仪,美国Perkin Elmer公司;EASY-nLC 1000型超高效液相,赛默飞世尔科技(中国)有限公司;Synergy H1酶标仪,美国Bio Tek公司;HH-6型数显恒温水浴锅,国华电器有限公司;5430R型冷冻离心机,德国Eppendorf公司;FiveEasy Plus台式pH计,梅特勒-托利多仪器(上海)有限公司;SR-AON-50型冷冻干燥机,上海舍岩仪器有限公司。
1.2 实验方法
1.2.1 鮰鱼骨的预处理
将冷冻鮰鱼骨沸水蒸煮5 min,去除鱼骨表面残留的鱼肉和膜性组织。按照1∶6(g∶mL)的料液比向鱼骨中加入0.3 mol/L NaOH溶液脱脂,1 h后换液摇匀,静置浸泡1 h后用蒸馏水反复冲洗鱼骨至中性,沥干水分,于60 ℃烘箱中烘干,粉碎备用。
1.2.2 鮰鱼骨的酶解提取工艺
碱性蛋白酶由多种不同的蛋白酶组成,对胶原蛋白的水解程度较高,一定程度上有助于产生更多的生物活性肽和活性位点[10],因此本文采用碱性蛋白酶水解鮰鱼骨粉制备鮰鱼骨胶原多肽。以钙结合能力为评价指标进行单因素试验设计,通过固定其他因素,依次研究料液比(1∶20、1∶13、1∶10、1∶8、1∶6,g∶mL)、酶添加量(1%、2%、3%、4%、5%,质量分数)、pH(8.0、8.5、9、9.5、10)、酶解时间(1、2、3、4、5 h)、酶解温度(30、40、50、60、70 ℃)对水解物钙结合能力的影响。
1.2.3 鮰鱼骨胶多肽的分子质量分布
采用高效体积排阻色谱法测定最优条件下酶解的鮰鱼骨胶原多肽的分子质量分布[11-12]。2 mg/mL的鮰鱼骨胶原多肽溶液过0.22 μm水系滤膜后进行上样分析。测定条件:色谱柱,Waters XBridge Protein BEH 125Å SEC(3.5 μm,7.8 mm×300 mm);流动相:V(ACN)∶V(0.1%TFA溶液)=40∶60;紫外检测220 nm;流速0.4 mL/min;柱温30 ℃;进样量10 μL。以细胞色素C(12 384 Da)、抑肽酶(6 511.51 Da)、L-氧化型谷胱甘肽(612.63 Da)和羟脯氨酸(131.13 Da)为标准品绘制相对分子质量校正曲线,利用校正曲线方程计算酶解液的分子质量分布情况。
1.2.4 Sephadex G-25分离纯化
参照李军等[13]的方法略作修改。将溶胀好的Sephadex G-25填料装入玻璃层析柱(1.6 cm×80 cm)中,超纯水平衡2~3个柱体积,胶原多肽溶液过0.22 μm水系滤膜后上样分析。洗脱条件:洗脱液为超纯水,流速0.4 mL/min,检测波长220 nm,每5 min收集1管。多次制备后合并相同组分,冻干。
1.2.5 胶原多肽钙结合能力分析
称取0.5 g鮰鱼骨胶原多肽及其最优组分和0.25 g CaCl2溶于20 mL蒸馏水中,40 ℃水浴1 h。冷却至室温后用8倍体积的无水乙醇沉淀4 h,离心取沉淀冻干得到肽-钙螯合物。最后采用钙含量显色检测试剂盒测定鮰鱼骨胶原多肽-钙螯合物的钙含量,钙含量可直接反应胶原多肽的钙结合能力[14]。
1.2.6 鮰鱼骨胶原多肽-钙螯合物的结构表征
1.2.6.1 傅里叶红外光谱测定
将1.2.5小节中确定的钙螯合能力最强肽组分及其钙螯合物与干燥的KBr于玛瑙研钵中混合,充分研磨后压片,采用傅里叶变换红外光谱仪在500~4 000 cm-1扫描[15]。
1.2.6.2 扫描电镜及能谱分析
参照张玲[16]的方法将1.2.5小节中确定的钙螯合能力最强肽组分及其钙螯合物分别固定在导电胶带上,喷金镀膜,放入扫描电镜施加电压获取微观结构图像,并对其进行能谱分析。
1.2.7 鮰鱼骨胶原多肽-钙螯合物的稳定性评价
1.2.7.1 热稳定性分析
配制5 mg/mL的鮰鱼骨胶原多肽-钙螯合物溶液,分别放置于25(控制组)、50、60、70、80 ℃条件下恒温水浴1 h,冷却至室温后用无水乙醇沉淀,离心冻干,测定其钙结合能力。以控制组的钙保留率为100%,计算不同温度下鮰鱼骨胶原多肽-钙螯合物的钙保留率。
1.2.7.2 酸碱稳定性分析
配制5 mg/mL的鮰鱼骨胶原多肽-钙螯合物溶液,以原液为控制组,其余组分别调pH为2、4、6、8、9,37 ℃水浴2 h,冷却至室温后用无水乙醇沉淀,离心冻干,评价样品的钙结合能力。以控制组的钙保留率为100%,计算不同pH条件下鮰鱼骨胶原多肽-钙螯合物的钙保留率。
1.2.7.3 体外模拟消化稳定性
用0.01 mol/L HCl溶液(pH 2.0)配制质量浓度为5 mg/mL的鮰鱼骨胶原多肽-钙螯合物,按照1∶50的酶底物质量比添加胃蛋白酶模拟胃消化环境,37 ℃水浴酶解1 h后,用1 mol/L NaOH溶液调节pH至7.5,再按照1∶25的酶底物质量比加入胰蛋白酶模拟肠消化环境,37 ℃水浴酶解2 h后,沸水浴加热灭酶10 min终止酶解。最后冷却至室温,并用无水乙醇沉淀,离心冻干,测定其钙结合能力。以未消化的鮰鱼骨胶原多肽-钙螯合物(控制组)的钙保留率为100%,计算模拟消化过程中鮰鱼骨胶原多肽-钙螯合物的钙保留率。
1.3 数据处理
所有试验重复3次,实验结果以平均值±标准偏差表示,采用Origin 8.6软件作图,用SPSS 22.0软件中的单因素方差分析(ANOVA)评价数据间的显著性差异,P<0.05认定具有显著性差异。
2 结果与分析
2.1 鮰鱼骨胶原蛋白多肽酶解单因素试验
碱性蛋白酶酶解鮰鱼骨制备胶原多肽的单因素试验结果如图1所示。由图1-a中可知,钙结合能力随料液比的增加整体呈先上升后下降的趋势,这是因为底物浓度会影响酶解液的分子扩散性,其底物浓度太低,酶与底物不易接近,在料液比为1∶13(g∶mL)时,钙结合能力最高,达到22.95 mmol/L(P<0.05)。由图1-b可知,碱性蛋白酶的添加量在1%~4%,钙结合能力基本呈上升的趋势,最大值达到28.47 mmol/L(P<0.05)。继续增加酶添加量时,钙结合能力反而下降。这是因为碱性蛋白酶的酶添加量增加,其水解能力增强,当继续增加酶量,此时的钙结合能力几乎没有发生改变,说明酶与底物达到饱和,因此确定最佳酶添加量为4%。由图1-c可知,钙结合能力随着pH的增加整体上呈下降的趋势,当pH为8.0时,钙结合能力最高达到27.68 mmol/L(P<0.05),这是因为当pH较低时,H+与Ca2+竞争供电基团,并促进肽-钙螯合物中Ca2+的解离,而pH过高时,溶液中的OH-会与Ca2+形成Ca(OH)2沉淀物,导致肽钙结合能力下降[17-18]。同时,当酶解pH值为8.0时,正好为碱性蛋白酶的最适pH,此时的酶解活性最高[13]。
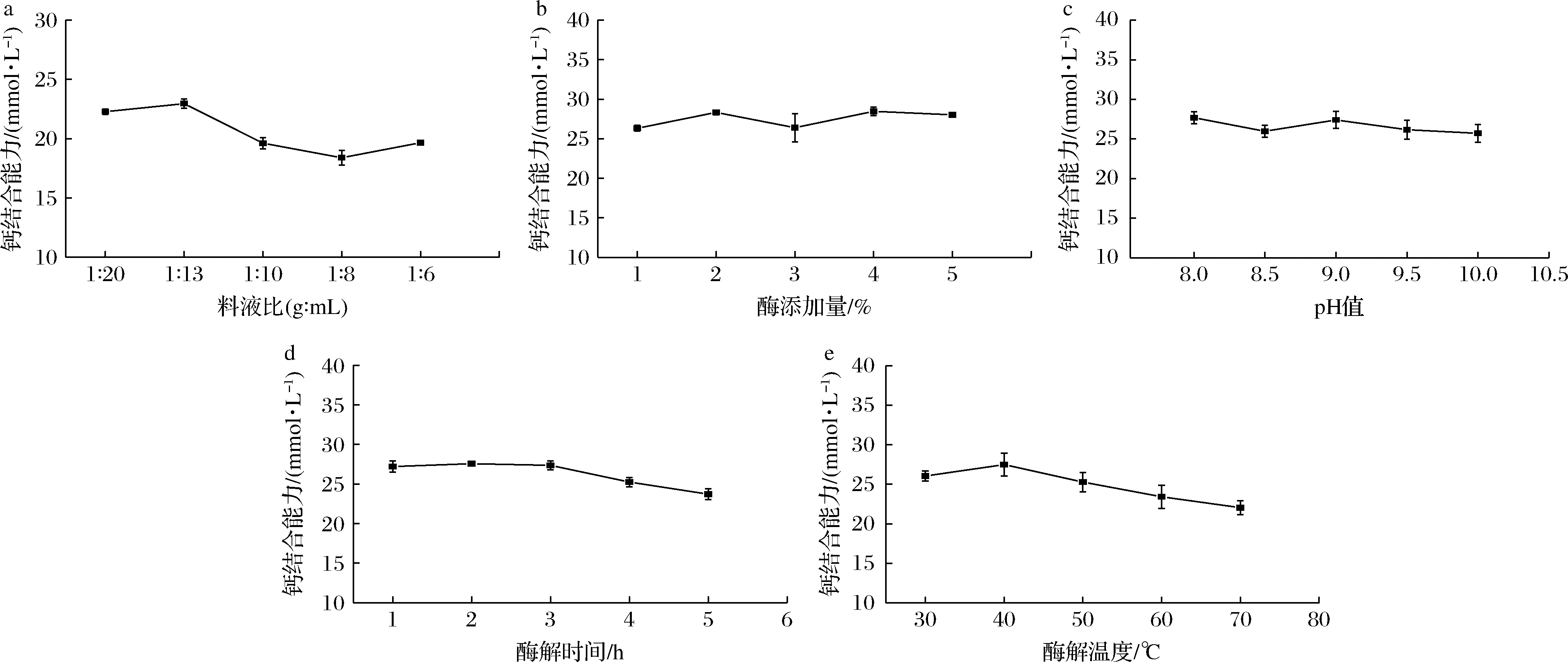
a-料液比;b-酶添加量;c-pH值;d-酶解时间;e-酶解温度
图1 酶解条件对钙结合能力的影响
Fig.1 Effects of enzymatic hydrolysis conditions on calcium binding capacity
由图1-d可知,随着酶解时间的延长,钙结合能力呈现先上升后下降的趋势,当酶解时间为2 h时,钙结合活性达到最大值27.56 mmol/L(P<0.05)。这是因为当酶解反应开始时,碱性蛋白酶与鱼骨底物激烈反应,胶原多肽含量增加,其钙结合能力也随之增加,但随着酶解时间的延长,胶原多肽也会被过度水解成氨基酸,使与钙结合的胶原多肽含量降低。由图1-e可知,钙结合能力随着酶解温度增加呈先上升后下降的趋势,在酶解温度为40 ℃时,其钙结合能力达到最大值27.48 mmol/L(P<0.05)。其原因在于随着温度的逐渐增加,碱性蛋白酶活性增强,但过高的温度会导致碱性蛋白酶酶活力下降甚至失活,影响胶原多肽与钙的结合能力。综上所述,由单因素试验可确定碱性蛋白酶制备鮰鱼胶原多肽的最佳酶解工艺:料液比1∶13(g∶mL),酶添加量4%,pH 8.0,酶解时间2 h,酶解温度40 ℃,此时制备的鮰鱼胶原多肽与钙结合能力为29.37 mmol/L。
2.2 鮰鱼骨胶原蛋白肽的分子质量分布分析
鮰鱼骨胶原多肽分子质量分布情况如图2-a所示,混合标准品分离效果良好。依据标准品与保留时间的关系,以相对分子质量的对数(lgMw)对保留时间(t)作线性回归得到相对分子质量校正曲线,如图2-b所示,其相对分子质量校正曲线方程:lg(Mw)=-0.188 1 t+6.642 1,R2=0.996 6,表明相对分子质量的对数与保留时间(t)具有良好的线性关系,可根据相对分子质量校正曲线方程和鮰鱼骨胶原多肽的出峰时间,计算出鮰鱼骨胶原多肽粉末各组分的分子质量分布情况。

a-标准品的体积排阻色谱图;b-相对分子质量校正曲线;c-鮰鱼骨胶原多肽分子质量范围
图2 标准品的体积排阻色谱图、相对分子质量校正曲线和鮰鱼骨胶原多肽分子质量分布
Fig.2 Size exclusion chromatogram, relative molecular mass calibration curve and molecular mass distribution of catfish bone collagen polypeptide
注:相对含量的数据来源于高效液相色谱分析结果
鮰鱼骨胶原多肽的高效体积排阻色谱图如图2-c所示,图中主要出现4个峰,表明鮰鱼骨胶原多肽由4种不同分子质量胶原多肽所组成。通过相对分子质量校正曲线方程和鮰鱼骨胶原多肽的出峰时间计算,分子质量分布如2-c所示,鮰鱼骨胶原多肽的分布范围广,大小不一,且分子质量范围为195~1 967 Da的胶原多肽相对含量最高,约占鮰鱼骨胶原多肽整体的77.73%。因此,采用Sephadex G-25分子层析将其进行分离纯化,并分析各个组分对钙结合活性的影响。
2.3 鮰鱼骨胶原多肽Sephadex G-25分离纯化分析
凝胶过滤层析可根据样品的分子质量大小对样品进行分离,分子质量大的样品不能进入凝胶颗粒,先被洗脱下来,分子质量小的样品后被洗脱出来[19]。鮰鱼骨胶原多肽经Sephadex G-25分离纯化的图谱如图3-a所示,鮰鱼骨胶原多肽按照分子质量大小被分离成3个不同组分,依次命名为F1、F2、F3。3个组分的钙结合能力如图3-b所示,F1、F2、F3组分与钙的结合能力分别为1.78、5.43、6.69 mmol/L,其中F3组分显示出最高的钙结合能力,这与低分子质量的多肽更容易与金属离子结合相符合[20]。

a-Sephadex G-25凝胶过滤层析色谱图;b-肽-钙结合能力
图3 鮰鱼骨胶原多肽的Sephadex G-25凝胶过滤层析色谱图和各个组分的钙结合能力
Fig.3 Sephadex G-25 gel filtration chromatography of catfish bone collagen polypeptide-calcium chelate and calcium binding capacity of different components
注:不同小写字母表示显著性差异(P<0.05)(下同)
2.4 鮰鱼骨胶原多肽-钙螯合物结构表征分析
2.4.1 傅里叶红外光谱
当金属离子和胶原多肽的有机基团结合时,傅里叶红外光谱的特征吸收峰会发生改变,可有效区分胶原多肽及其金属螯合物的光谱差异[21]。F3组分及其肽-钙螯合物的红外光谱图如图4所示。F3组分与Ca2+螯合后,其多肽的氨基特征吸收峰发生改变,—NH2的伸缩振动带由3 525.24 cm-1移动到3 421.10 cm-1;在酰胺Ⅰ带,C![]() O键伸缩振动引起的特征峰波数从1 652.70 cm-1移动到1 646.91 cm-1;而—COOH的特征吸收峰从1 402.00 cm-1移动到1 398.14 cm-1,波数发生明显降低。表明多肽上的氨基、羧基和酰胺键主要是Ca2+与多肽的结合位点,该结果与WANG等[22]的研究相一致。
O键伸缩振动引起的特征峰波数从1 652.70 cm-1移动到1 646.91 cm-1;而—COOH的特征吸收峰从1 402.00 cm-1移动到1 398.14 cm-1,波数发生明显降低。表明多肽上的氨基、羧基和酰胺键主要是Ca2+与多肽的结合位点,该结果与WANG等[22]的研究相一致。
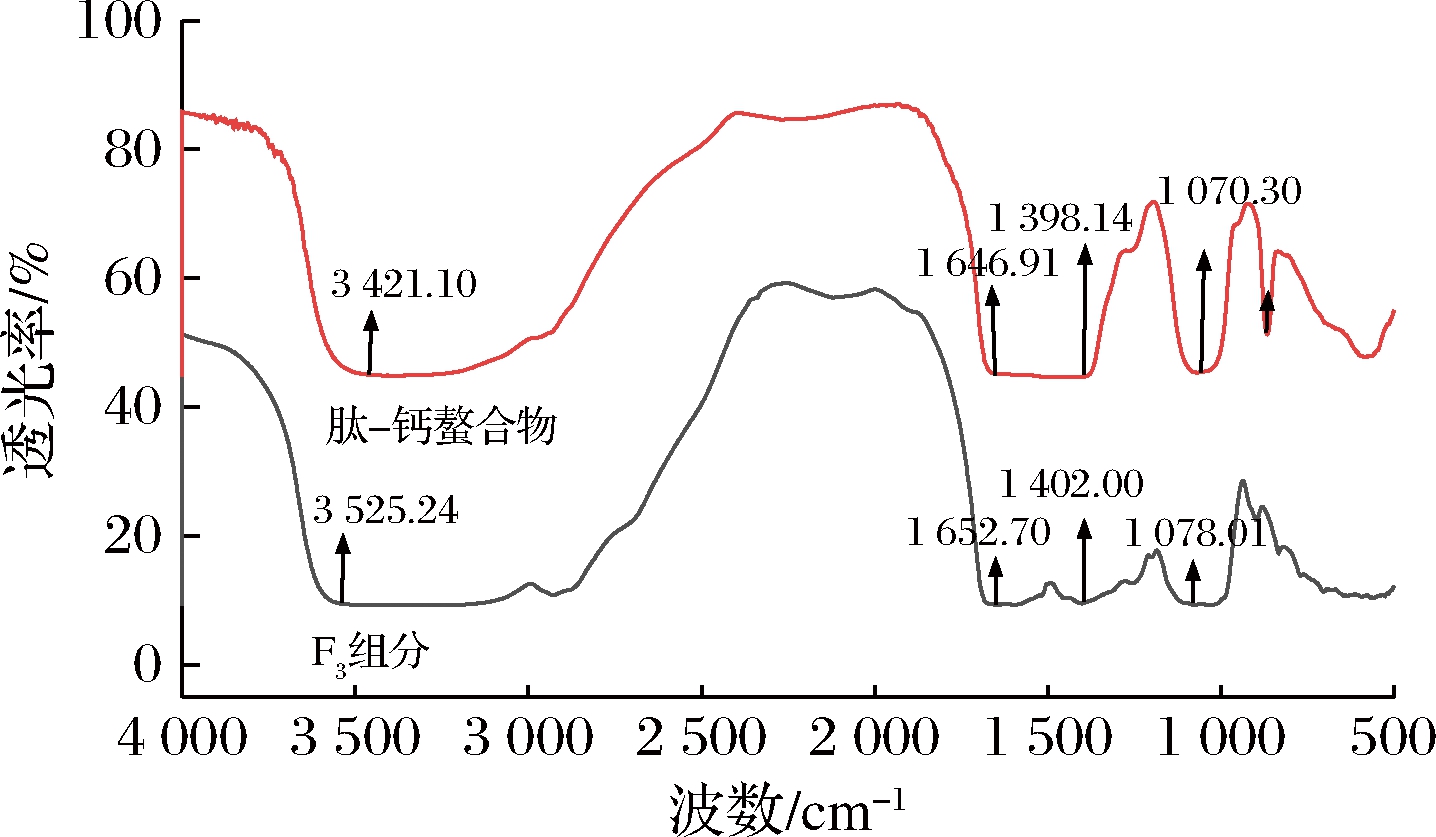
图4 F3和肽-钙螯合物的红外光谱图
Fig.4 Infrared spectra of F3 and peptide-calcium chelate
2.4.2 扫描电镜及能谱分析
F3组分及其肽-钙螯合物的扫描电镜如图5-a和图5-b所示,F3组分表面呈现光滑的平面,其表面还存在由于快速冷冻干燥而形成的裂纹。与Ca2+螯合后,其表面变为粗糙、疏松、多孔的形状,且多个球状连接一起,这是由于胶原多肽和Ca2+发生配位结合,Ca2+的嵌入和胶原多肽对Ca2+的截留共同作用的结果。为了更详细了解F3组分及其肽-钙螯合物中内部元素分布情况,采用能谱进行分析,结果如图5-c和图5-d所示。F3组分及其肽-钙螯合物都能检测到钙元素,同时还共同含有N、C、O、Na、Cl等元素。但肽-钙螯合物中钙元素的信号强度要明显强于F3组分,说明肽-钙螯合物中的钙含量要明显高于F3组分。通过扫描电镜和能图分析可知,F3组分与Ca2+发生了螯合作用,形成了新的物质。

a-F3扫描电镜图;b-肽-钙螯合物扫描电镜图;c-F3能谱图;d-肽-钙螯合物能谱图
图5 F3及肽-钙螯合物的扫描电镜及能谱分析
Fig.5 Scanning electron microscopy and energy spectrum analysis of F3 and its peptide-calcium chelate
2.5 鮰鱼骨胶原多肽钙螯合物稳定性评价
2.5.1 热稳定性
热处理是食品加工的常用手段,因此本研究以钙保留率为评价指标,考察了不同热处理温度对鮰鱼骨胶原多肽-钙螯合物稳定性的影响。如图6-a所示,随着热处理温度的升高(50~80 ℃),鮰鱼骨胶原多肽-钙螯合物的钙保留率先保持稳定,后缓慢降低,但钙保留率仍在95.91%以上,且无显著性差异(P>0.05),说明鮰鱼骨胶原多肽-钙螯合物具有一定的热稳定性。这可能是因为Ca2+与鮰鱼骨胶原多肽通过配位键相互作用将形成有序、紧密的结构,使其空间结构更加稳定[23]。

a-温度与钙保留率关系;b-pH与钙保留率关系;c-消化稳定性
图6 鮰鱼骨胶原多肽-钙螯合物温度、pH和消化稳定性关系分析
Fig.6 Calcium retention rate of catfish bone collagen polypeptide-calcium chelate at different temperatures, different acid-base environment, different digestion methods
2.5.2 酸碱稳定性
鮰鱼骨胶原多肽-钙螯合物的酸碱稳定性如图6-b所示,随着pH值(2.0~9.0)的增加,鮰鱼骨胶原多肽-钙螯合物的钙保留率呈现出先增加后下降的趋势,但钙保留率均在77.52%以上。与控制组相比,鮰鱼骨胶原多肽-钙螯合物在强酸性环境下的钙保留率下降较快,这是由于高H+浓度可与Ca2+竞争活性基团,导致鮰鱼骨胶原多肽-钙螯合物的钙结合能力下降[18]。而在碱性环境下,鮰鱼骨胶原多肽-钙螯合物的钙保留率略有下降,这是因为碱性环境下的OH-与Ca2+结合发生少量的沉淀所致,但有研究表明金属肽钙复合物一旦形成稳定结构,其解离需要克服较大的活化能[24],所以在弱碱性条件下(pH 8.0)的钙保留率下降趋势不明显。
2.5.3 体外消化稳定性
膳食营养素的吸收利用需要经过胃肠道的消化吸收,其吸收利用率会受到pH及各种消化酶的影响。因此,需要评价鮰鱼骨胶原多肽-钙螯合物在胃肠道模拟消化过程中的稳定性,其结果如图6-c所示。经过胃蛋白酶消化后,鮰鱼骨胶原多肽-钙螯合物的钙保留率下降到82.25%,这是因为模拟胃消化环境的pH为2.0,其高浓度的H+与Ca2+发生竞争,与图6-b的强酸环境下导致钙保留率下降的结果相一致。加入胰蛋白酶再次消化后,鮰鱼骨胶原多肽-钙螯合物的钙保留率再次下降,其值为73.84%,这可能是胃消化阶段的强酸环境和胰蛋白酶可能对鮰鱼骨胶原多肽存在一定的降解作用,导致其钙螯合能力降低[25]。但总体来说,其钙保留率均在70%以上,表明鮰鱼骨胶原多肽-钙螯合物对胃蛋白酶、胰蛋白酶消化和胃肠道pH环境不敏感,能较好地保持结构不被破坏,促进人体对钙的吸收。
3 结论
本文以鮰鱼骨为原料,经碱性蛋白酶水解后与CaCl2螯合制备鮰鱼骨胶原多肽-钙螯合物。采用钙结合能力为评价指标,通过单因素试验得到鮰鱼骨胶原多肽的最佳酶解工艺为:料液比1∶13(g∶mL),酶添加量4%,pH 8.0,酶解时间2 h,酶解温度40 ℃,此时制备的鮰鱼骨胶原多肽与钙结合能力达到29.37 mmol/L。HPLC分析发现,鮰鱼骨胶原多肽的分子质量主要集中在195~1 967 Da,其相对含量约占鮰鱼骨胶原多肽整体的77.73%。利用Sephadex G-25分离纯化得到3个组分,其中F3组分的钙结合活性最佳。红外光谱、扫描电镜和能谱结果显示,鮰鱼骨胶原多肽的氨基、羧基和酰胺键是Ca2+的结合位点,与Ca2+螯合之后,其光滑的平面变为粗糙、疏松、多孔的形状,钙含量明显增加,都表明有新物质的产生。热稳定性和酸碱稳定性分析表明,鮰鱼骨胶原多肽-钙螯合物具有一定的耐热性、耐弱碱性,但在强酸环境下不稳定。消化稳定性分析发现,鮰鱼骨胶原多肽-钙螯合物可在胃肠道的环境中保持稳定,其钙保留率在70%以上,具有促进人体钙吸收的潜力。
[1] 农业部渔业渔政管理局. 中国渔业统计年鉴[Z].北京:中国农业出版社, 2019.
Fisheries and Fisheries Administration of the Ministry of Agriculture.China fishery statistical yearbook[Z].Beijing:China Agriculture Press, 2019.
[2] 陈紫红, 林志杰, 薛雅茹, 等.斑点叉尾鮰鱼下脚料的多肽制备工艺[J].食品工业, 2021, 42(4):162-165.
CHEN Z H, LIN Z J, XUE Y R, et al.Preparation technique of polypeptide from leftovers of channel catfish[J].The Food Industry, 2021, 42(4):162-165.
[3] 沙小梅, 郝君晖, 涂宗财, 等.基于亚临界水技术的鱼骨软化及其在鱼糜中的应用[J].食品与发酵工业, 2018, 44(2):154-159.
SHA X M, HAO J H, TU Z C, et al.Fish bone softened by subcritical water and its application in fish surimi[J].Food and Fermentation Industries, 2018, 44(2):154-159.
[4] 李军. 鲢鱼骨胶原多肽的制备及其抗氧化、钙螯合活性的研究[D].南昌:江西师范大学, 2020.
LI J.Study on the preparation and antioxidant, calcium chelating activities of collagen polypeptides from silver carp bone[D].Nanchang:Jiangxi Normal University, 2020.
[5] BALK E M, ADAM G P, LANGBERG V N, et al.Global dietary calcium intake among adults:A systematic review[J].Osteoporosis International, 2017, 28(12):3 315-3 324.
[6] SUN N, WU H T, DU M, et al.Food protein-derived calcium chelating peptides:A review[J].Trends in Food Science & Technology, 2016, 58:140-148.
[7] VAVRUSOVA M, SKIBSTED L H.Calcium nutrition.bioavailability and fortification[J].LWT - Food Science and Technology, 2014, 59(2):1 198-1 204.
[8] CUI P B, LIN S Y, JIN Z Q, et al.In vitro digestion profile and calcium absorption studies of a sea cucumber Ovum derived heptapeptide-calcium complex[J].Food & Function, 2018, 9(9):4 582-4 592.
[9] ZHANG K, LI B F, CHEN Q R, et al.Functional calcium binding peptides from Pacific cod (Gadus macrocephalus) bone:Calcium bioavailability enhancing activity and anti-osteoporosis effects in the ovariectomy-induced osteoporosis rat model[J].Nutrients, 2018, 10(9):1325.
[10] 柯枭, 胡晓, 杨贤庆, 等.罗非鱼皮胶原蛋白肽-锌螯合物的制备及结构表征与体外消化分析[J].食品与发酵工业, 2021, 47(14):38-44.
KE X, HU X, YANG X Q, et al.Preparation, structure characterization and in vitro gastrointestinal digestion of tilapia skin collagen peptide-zinc chelate[J].Food and Fermentation Industries, 2021, 47(14):38-44.
[11] 张耀, 张露, 刘俊, 等.青鱼肉活性肽的制备及其抗肿瘤活性研究[J].食品与发酵工业, 2021, 47(5):35-42.
ZHANG Y, ZHANG L, LIU J, et al.Preparation and antitumor activity of peptides from Mylopharyngodon piceus muscle[J].Food and Fermentation Industries, 2021, 47(5):35-42.
[12] 朱敏方. 草鱼鱼肉抗氧化肽的制备、分离鉴定及其活性研究[D].南昌:江西师范大学, 2020.
ZHU M F.Preparation, isolation, identification and activity of antioxidant peptides from grass carp(Ctenopharyngodon idella) muscle[D].Nanchang:Jiangxi Normal University, 2020.
[13] 李军, 罗娟, 涂宗财, 等.鲢鱼骨胶原多肽的制备及其抗氧化活性研究[J].食品与发酵工业, 2020, 46(2):222-230.
LI J, LUO J, TU Z C, et al.Study on the preparation and antioxidant activity of collagen polypeptide from silver carp bone[J].Food and Fermentation Industries, 2020, 46(2):222-230.
[14] WU J H, CAI X X, TANG M R, et al.Novel calcium-chelating peptides from Octopus scraps and their corresponding calcium bioavailability[J].Journal of the Science of Food and Agriculture, 2019, 99(2):536-545.
[15] ZHANG K, LI J W, HOU H, et al.Purification and characterization of a novel calcium-biding decapeptide from Pacific cod (Gadus macrocephalus) bone:Molecular properties and calcium chelating modes[J].Journal of Functional Foods, 2019, 52:670-679.
[16] 张玲. 罗非鱼皮胶原降解反应行为及肽钙螯合物制备研究[D].广州:华南理工大学, 2020.
ZHANG L.Studies on tilapia skin collagen degradation behavior and preparation of peptide calcium chelate[D].Guangzhou:South China University of Technology, 2020.
[17] 刘玉玉, 胡筱波, 蔡晓雯, 等.白鲢鱼皮胶原蛋白肽钙螯合物的制备及其对Caco-2细胞钙转运的影响[J].食品科技, 2020, 45(8):138-145.
LIU Y Y, HU X B, CAI X W, et al.Preparation and effect on calcium transport in caco-2 cells of silver carp skin collagen peptide-calcium chelate[J].Food Science and Technology, 2020, 45(8):138-145.
[18] WU W M, HE L C, LIANG Y H, et al.Preparation process optimization of pig bone collagen peptide-calcium chelate using response surface methodology and its structural characterization and stability analysis[J].Food Chemistry, 2019, 284:80-89.
[19] LIU X Y, WANG Z X, ZHANG J, et al.Isolation and identification of zinc-chelating peptides from sea cucumber (Stichopus japonicus) protein hydrolysate[J].Journal of the Science of Food and Agriculture, 2019, 99(14):6 400-6 407.
[20] CHEN M, JI H W, ZHANG Z W, et al.A novel calcium-chelating peptide purified from Auxis thazard protien hydrolysate and its binding properties with calcium[J].Journal of Functional Foods, 2019, 60:103447.
[21] HUANG W, LAN Y Q, LIAO W W, et al.Preparation, characterization and biological activities of egg white peptides-calcium chelate[J].LWT, 2021, 149:112035.
[22] WANG L, DING Y Y, ZHANG X X, et al.Isolation of a novel calcium-binding peptide from wheat germ protein hydrolysates and the prediction for its mechanism of combination[J].Food Chemistry, 2018, 239:416-426.
[23] WANG X Q, ZHANG Z, XU H Y, et al.Preparation of sheep bone collagen peptide-calcium chelate using enzymolysis-fermentation methodology and its structural characterization and stability analysis[J].RSC Advances, 2020, 10(20):11 624-11 633.
[24] 毕景硕. 鹿骨多肽螯合钙的制备方法与吸收的特性研究[D].长春:吉林大学, 2018.
BI J S.Study on the preparation of deer bone peptide-chelated calcium and its effect on promoting calcium absorption[D].Changchun:Jilin University, 2018.
[25] YANG X, YU X J, YAGOUB A G, et al.Structure and stability of low molecular weight collagen peptide (prepared from white carp skin)-calcium complex[J].LWT, 2021, 136:110335.