茴香,又称小茴香(Foeniculum vulgare Mill.),伞形科茴香属,味辛性温,具有散寒止痛,理气健胃等功效[1]。茴香精油是小茴香主要成分之一,由茴香脑、单萜类、苯丙烷等有机化合物组成。大量实验证明,茴香精油中的反式茴香脑、多酚类及黄酮类等物质可以促使机体代谢生成的自由基解离,抗氧化能力更强[2-3]。但茴香精油的水溶性差和稳定性低等特性,很大程度上限制了其应用。目前,微胶囊技术是提高茴香精油稳定性的主要手段,但由于微胶囊的制备工艺繁琐、成本较高、制备工艺复杂等因素[4],限制了茴香精油在食品中的应用。因此,需要一种合适的手段改善茴香精油的溶解性,提高茴香精油的稳定性和生物活性。
微乳液是一种由水相、油相、表面活性剂及助表面活性剂,在适合的比例下自发形成的一种油水混合物体系,具有热力学稳定性、各向同性、低黏度等特点。微乳粒径<100 nm,按照构型可分为油包水型(O/W型)、水包油型(W/O型)及双连续型(B.C型)[5]。微乳具有稳定性高、操作简单及提高生物活性和载油量等优点,在食品、医药、工业等领域应用广泛[6]。无限稀释型微乳液是指随着水相不断增加,微乳体系依然稳定,这种体系对脂溶性物质有很好的增容效果,能显著提升脂溶性物质的生物利用度[7-8]。
本研究通过探究茴香精油微乳的最优配方及影响因素,分析茴香精油微乳的结构及性能,旨在提高茴香精油的稳定性、溶解度及生物利用率,为茴香精油微乳在食品和医药领域的应用提供参考。
1 材料与方法
1.1 材料与试剂
茴香,铜川市恒润食品有限公司;吐温-80、吐温-60、吐温-40,国药集团化学试剂有限公司;司盘-80,无锡市亚泰联合化工有限公司;聚乙二醇400、丙二醇、丙三醇,天津市致远化学试剂有限公司;DPPH,美国Sigma公司;邻苯三酚、水杨酸,天津市大茂化学试剂厂。其他化学药品和试剂均为分析纯。
1.2 仪器与设备
ALC-2100.2分析天平,赛多利斯科学仪器有限公司;79-1磁力搅拌器,天津市赛得利实验仪器制造厂;Nano-ZS-9激光粒度分析仪,英国马尔文仪器有限公司;DDS-11A电导率仪,上海仪电科学仪器股份有限公司;HT7800透射电子显微镜,日本株式会社日立高新技术;TG16-WS高速离心机,上海浦东物理光学仪器厂;HH-511恒温水浴锅,上海跃进医疗器械厂;α-1506紫外可见分光光度计,上海光谱有限公司。
2 实验方法
2.1 茴香精油微乳三元相图的绘制
参考文献[9]的方法并稍作修改。准确称取Km(表面活性剂与助表面活性剂的比值)分别为4∶1、3∶1、2∶1、1∶1和1∶2的表面活性剂和助表面活性剂,充分混匀作为混合乳化剂备用。再将混合乳化剂与茴香精油按照9∶1、8∶2、7∶3、6∶4、5∶5、4∶6、3∶7、2∶8和1∶9质量比混合,逐滴加入去离子水并均匀振荡,直至体系由澄清变浑浊或由浑浊变澄清,记录离子水的添加量,根据各组分临界点时的质量分数,确定微乳区域和最小可稀释比(DR:三相图中可稀释线对应的表面活性剂与茴香精油质量比值)S∶O表示在最小可稀释比下,表面活性剂与茴香精油的质量比。
2.2 茴香精油微乳的最优配方
2.2.1 表面活性剂种类对微乳的影响
室温下,将吐温-80与司盘-80按一定比例复配成不同亲水亲油平衡(hydrophilic-lipophilic balance,HLB)值的表面活性剂,助表面活性剂为丙三醇,Km=2,按2.1制备茴香精油微乳并绘制三元相图,计算微乳区面积和DR。HLB值计算如公式(1)所示:
HLBMAX=HLBA×wA+HLBB×wB
(1)
式中:HLBA和 HLBB为吐温-80和司盘-80的HLB值;wA和wB为吐温-80和司盘-80质量分数。
2.2.2 表面活性剂复配对微乳的影响
室温下,选择不同配比的表面活性剂,与助表面活性剂丙三醇混匀,Km=2,按2.1制备茴香精油微乳并绘制三元相图,计算微乳区面积和DR。
2.2.3 助表面活性剂种类对微乳的影响
室温下,以吐温-80+吐温-40(质量比1∶1)为表面活性剂,丙三醇、丙三醇、聚乙二醇400和无水乙醇为助表面活性剂,Km=2,按2.1制备茴香精油微乳并绘制三元相图,计算微乳区面积和DR。
2.2.4 Km值对微乳的影响
室温下,表面活性剂为吐温-80+吐温-40(质量比1∶1),丙三醇为助表面活性剂,将表面活性剂与助表面活性剂按Km=4、3、2、1和0.5混匀,按2.1制备茴香精油微乳并绘制三元相图,计算微乳区面积和DR。
2.3 茴香精油微乳构型分析
采用陶紫等[10]的电导率法分析茴香精油微乳液的构型。
2.4 茴香精油微乳粒径分析
采用马尔文激光粒度仪在659 nm、25 ℃、散射角90°条件下[11-12]测定茴香精油微乳粒径。
2.5 茴香精油微乳的形貌观察
将铜网置于蜡板上,滴加2 μL微乳,自然风干,把质量分数2%磷钨酸(pH=7.4)滴在蜡板上,将晾干的铜网倒置于染液上,负染15 min,用蒸馏水冲洗,吸干,采用透射电镜研究茴香精油微乳的形态。
2.6 茴香精油微乳稳定性的研究
离心稳定性按SONG等[13]的方法稍作改动,按吐温-80+吐温-40∶丙三醇∶茴香精油=4∶2∶1.5的质量比例,配制含水量为90%茴香精油微乳,在3 000、4 000、5 000、6 000、7 000 r/min离心30 min,测定离心前后在550 nm下的吸光度,透光率计算如公式(2)所示:
(2)
式中:T,透光率;A0,离心后的微乳吸光度;A1,离心前的微乳吸光度。
将茴香精油微乳分别在30、40、50、60、70、80、90 ℃加热30 min,观察微乳外观,有无浑浊、沉淀现象。并测定透光率、粒径和多分散性指数(polydispersity index,PDI)值,表征热稳定性。
将茴香精油微乳分别于4和25 ℃贮藏,测定第0、15、30、45、60、75、90天的茴香精油微乳粒径和PDI值,表征贮藏稳定性。
2.7 茴香精油微乳液抗氧化能力测定
DPPH自由基清除能力测定采用WANG等[14]和KIM等[15]的方法稍作改动,量取不同浓度的茴香精油乙醇溶液及其微乳乙醇溶液与2.5 mL DPPH乙醇溶液置于暗处反应20 min,测定其在517 nm下的吸光值,另外,在试管中分别加入乙醇溶液和DPPH乙醇溶液各2.5 mL混匀,测定吸光度A2。取不同浓度的茴香精油及微乳乙醇溶液于试管中,分别加入2.5 mL乙醇溶液,测定吸光值。DPPH自由基清除率计算如公式(3)所示:
DPPH自由基清除率![]()
(3)
式中:A0,空白组吸光值;A1,待测液吸光值;A2,乙醇代替DPPH溶液的吸光值。
对·OH清除能力参考文献[16]的方法稍作改动,分别取不同浓度的茴香精油乙醇溶液及其微乳乙醇溶液2 mL,依次加入FeSO4溶液、水杨酸乙醇溶液和H2O2溶液,静置平衡3 min后,移至50 ℃恒温水浴锅,反应30 min后,测定其在510 nm处的吸光值。·OH清除能力计算如公式(4)所示:
·OH清除率![]()
(4)
式中:A1,加样品时吸光值;A2,不加样品的吸光值;A3,不加H2O2溶液的吸光值。
·O2-清除能力按CHOI等[17]的方法测定,计算如公式(5)所示:
·O2-清除率![]()
(5)
式中:A0,空白组吸光值;Al,实验组吸光值;A2,不加邻苯三酚样品的吸光值。
分别取不同浓度的茴香精油乙醇溶液及其微乳乙醇溶液2 mL,分别加入PBS和铁氰化钾,移至50 ℃恒温水浴锅,反应2 min后添加2 mL三氯乙酸,3 000 r/min离心10 min,取上清液,加入蒸馏水和FeCl3溶液,50 ℃水浴10 min测定吸光值[18]测定总还原力。
2.8 数据处理
采用Excel 2010、AutoCAD 2020、Orgin 2018和SPSS 17.0进行数据统计分析,平行试验3次。
3 结果与讨论
3.1 茴香精油微乳最优配方
3.1.1 表面活性剂种类对微乳的影响
HLB值是指表面活性剂中亲水基和亲油基达到平衡时的量,当亲水基与亲油基的大小和力量达到平衡时,微乳的形成能力最强。据食品添加剂使用标准可知:吐温亲水性强,HLB值高;司盘类亲油性强,HLB值低。两者复配可得HLB值范围较广的混合表面活性剂[19]。通过拟三元相图探究茴香精油微乳最适的HLB值,绘制的三元相图见图1,图中相关信息见表1。
表1 HLB值对茴香精油微乳的影响
Table 1 Effect of HLB value on microemulsion of fennel essential oil
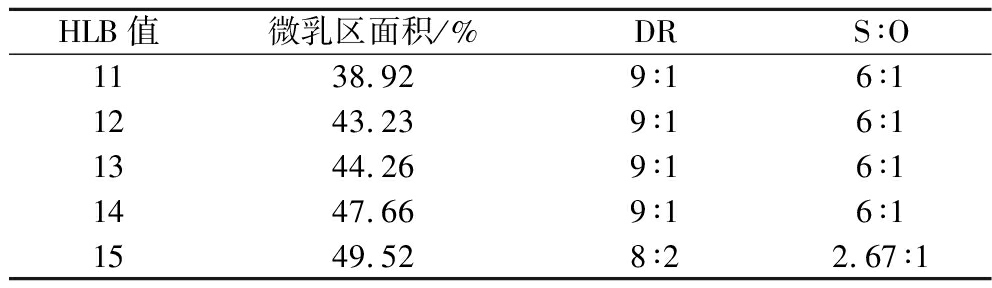
HLB值微乳区面积/%DRS∶O1138.929∶16∶11243.239∶16∶11344.269∶16∶11447.669∶16∶11549.528∶22.67∶1

图1 不同HLB值的茴香精油微乳相图
Fig.1 Phase diagram of microemulsion of fennel essential oil with different HLB values
拟三相图中阴影区域为微乳区,面积的大小与微乳的稳定性成正比。当HLB值到15时,微乳区最大,达49.52%,DR为8∶2,表面活性剂与茴香精油比仅为2.67∶1,远小于其他HLB值下的S/O值,这说明当茴香精油微乳变为可无限稀释体系时,茴香精油含量不变,表面活性剂含量降低[20]。因此,HLB值=15的表面活性剂最适合制备茴香精油微乳。
3.1.2 表面活性剂复配对微乳的影响
由图2和表2可得,上述表面活性剂乳化效果由高到低依次为:吐温-80+吐温-40>吐温-80>吐温-60>吐温-60+吐温-40>吐温-40>吐温-60+吐温-80,其中吐温-40、吐温-60和吐温-80疏水链长分别为16.18和18,这说明微乳形成能力与表面活性剂疏水链长度正相关,这与张昭[21]的研究结果一致。当吐温-80和吐温-40配伍性较好时,可以降低体系内的空间位阻,增加油水相界面的流动性,提高微乳对水的增溶效果[22]。因此,选择吐温-80与吐温-40按1∶1复配,作为茴香精油微乳的表面活性剂。
表2 表面活性剂对微乳相图的影响
Table 2 Influence of surfactant on phase diagram of microemulsion

表面活性剂HLB面积比/%DRS∶O吐温-4015.5048.719∶16∶1吐温-6014.9049.288∶22.67∶1吐温-8015.0049.398∶22.67∶1吐温-80+吐温-6014.9547.629∶16∶1吐温-60+吐温-4015.0048.869∶16∶1吐温-80+吐温-4015.3051.108∶22.67∶1

图2 不同表面活性剂的茴香精油微乳相图
Fig.2 Phase diagram of microemulsion of fennel essential oil with different surfactants
3.1.3 助表面活性剂对微乳的影响
助表面活性剂不仅能降低体系内部张力,提升微乳体系的稳定性和流动性,还可用做助溶剂,对外来物质有增溶作用[23]。
由图3和表3可知,当助表面活性剂为丙三醇时,微乳区面积最高占比51.10%,稳定性最好,这是因为丙三醇能降低表面活性剂分子间的相互作用力和界面弯曲能,使茴香精油微乳体系整体的流动性和稳定性最佳。无水乙醇和聚乙二醇400制备的茴香精油微乳形成能力小、微乳稳定性欠佳;丙二醇作为助表面活性剂不能制备出可无限稀释型微乳。
表3 助表面活性剂对微乳相图的影响
Table 3 Effect of cosurfactants on the phase diagram of microemulsion

助表面活性剂微乳区面积/%DRS∶O微乳外观丙三醇51.108∶22.67∶1澄清透明,流动性好,久置不分层乙醇45.699∶16∶1澄清透明,流动性好,久置分层聚乙二醇40039.679∶16∶1澄清透明,流动性较差,久置分层丙二醇39.30有絮状物,无法滴出可无限稀释微乳

图3 不同助表面活性剂的茴香精油微乳相图
Fig.3 Phase diagram of microemulsion of fennel essential oil with different cosurfactants
3.1.4 Km值对微乳的影响
Km值是指表面活性剂与助表面活性剂的比值,在二者种类相同时,合适的Km值可以显著提升微乳的稳定性[24]。
由图4和表4可知,随着Km的上升,微乳的稳定性先上升再下降,当Km=2时,微乳区面积达最高值51.11%,微乳稳定性最好。这是因为过量的助表面活性剂和表面活性剂,会使微乳体系难以维持油水界面的平衡,导致形成微乳能力变弱[25]。因此,制备茴香精油微乳的最佳Km值为2。
表4 Km值对茴香精油微乳的影响
Table 4 Influence of Km values on fennel essential oil microemulsion
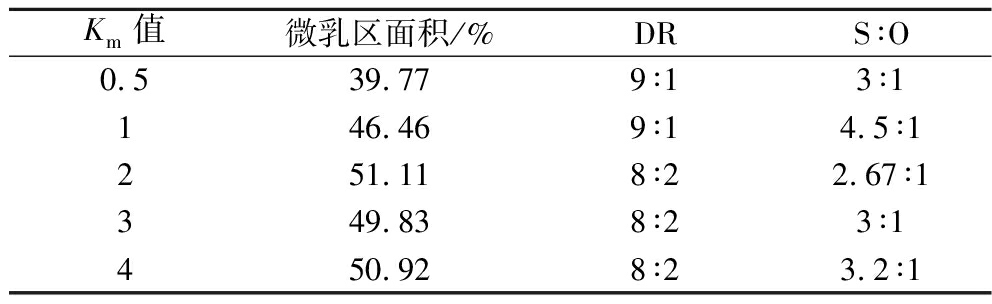
Km值微乳区面积/%DRS∶O0.539.779∶13∶1146.469∶14.5∶1251.118∶22.67∶1349.838∶23∶1450.928∶23.2∶1
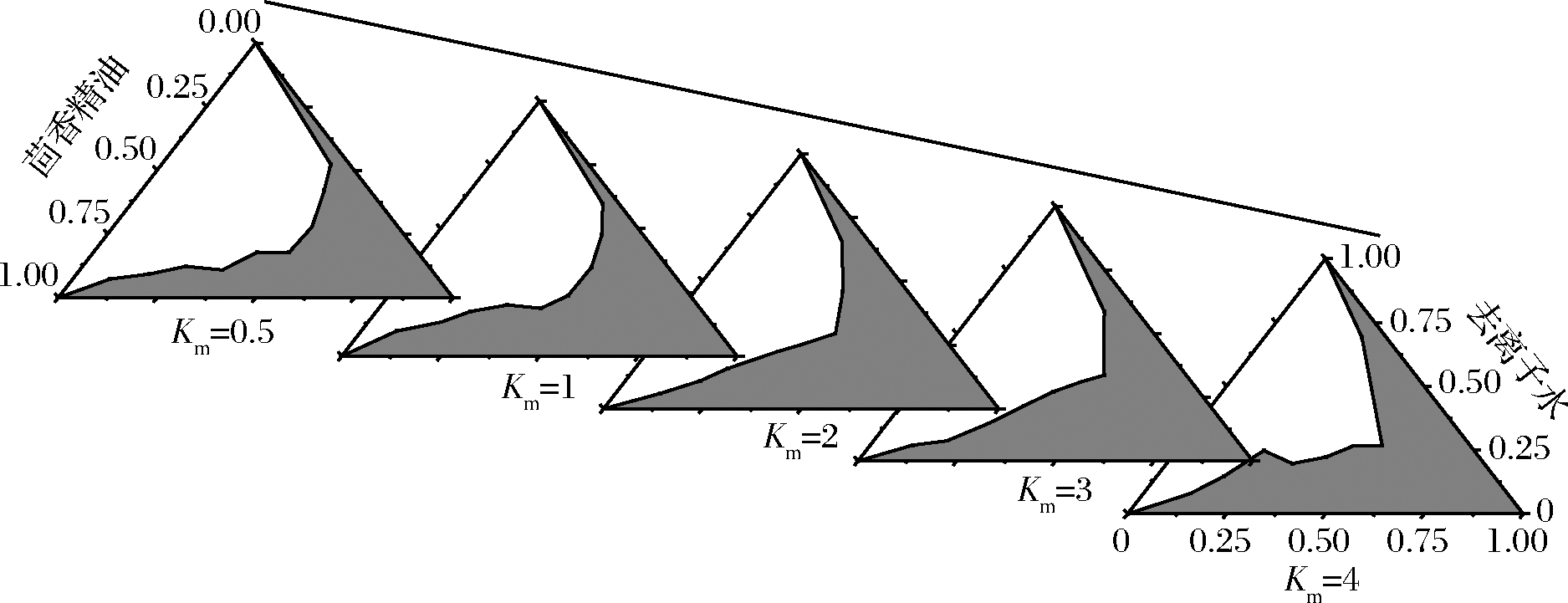
图4 不同Km值的茴香精油微乳相图
Fig.4 Phase diagram of microemulsion of fennel essential oil with different Km values
3.2 茴香精油微乳的构型分析
由图5所示,电导率值随着水分含量的上升呈先上升后平缓再下降的趋势。这是因为,当水分含量较少时,体系内的连续相为油相,在电场的作用下,水离子会不断地相互碰撞,产生导电链,随着水分不断增加,离子之间的碰撞加剧电导率急速上升,此时微乳为W/O型。当水分含量为48%~62%,体系内呈现水相与油相的网络通道,离子间碰撞缓慢,导电率变化缓慢,此时微乳构型为B.C型[26-27]。水分继续增加,体系内连续相为水相,此时稀释导电离子的油滴浓度和电导率下降,微乳构型为O/W型[28-29]。
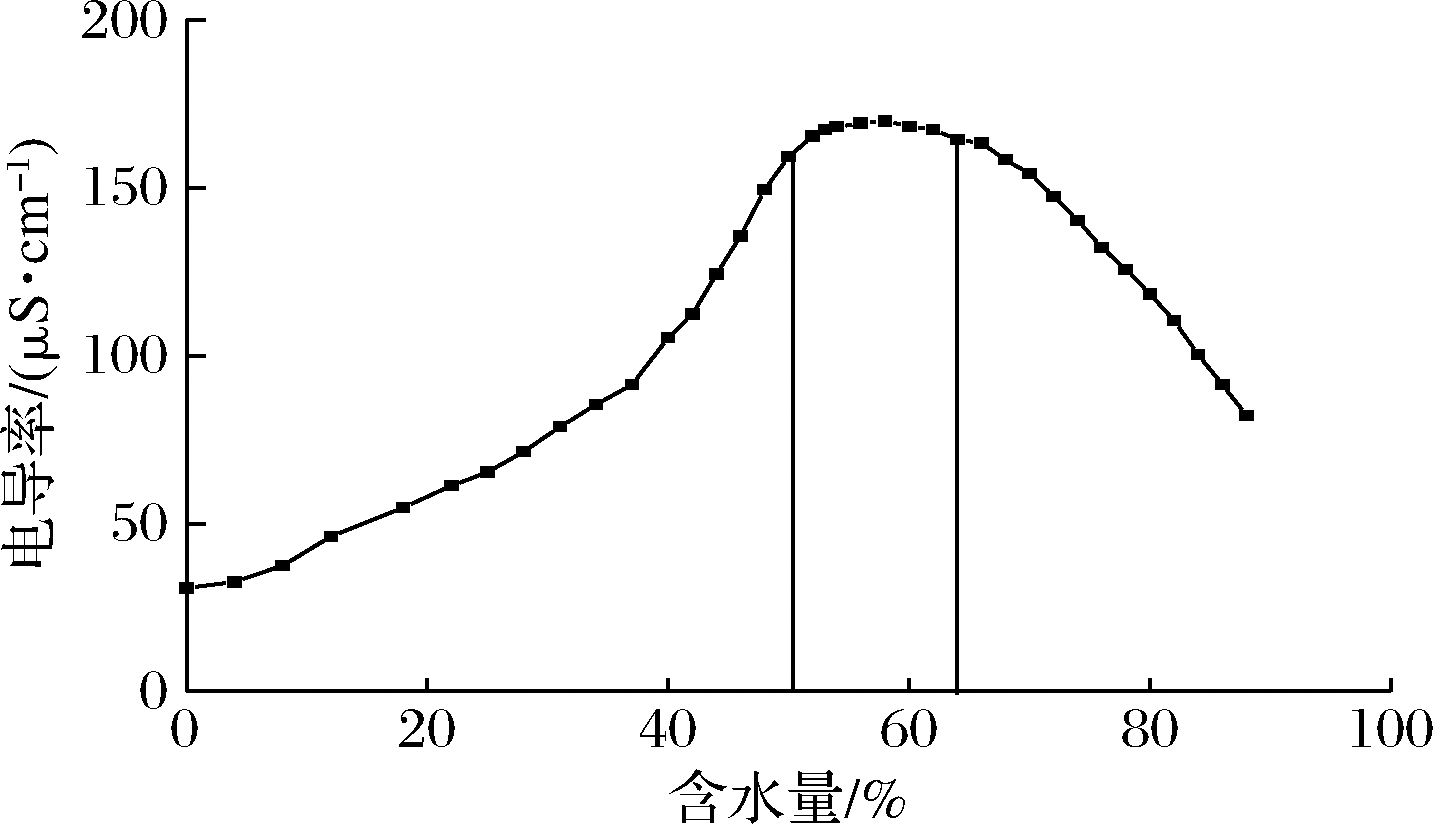
图5 茴香精油微乳电导率
Fig.5 Conductivity of fennel essential oil microemulsion
3.3 茴香精油微乳粒径及多分散指数分析
由以上茴香精油微乳优化结果可知,2种可无限稀释型茴香精油微乳配方分别为吐温-80+吐温-40∶丙三醇∶茴香精油=4∶2∶1.5(A)和6∶3∶1(B)。配方A、B粒径与PDI值如图6与表5所示。
表5 茴香精油微乳粒径相关信息
Table 5 Fennel essential oil microemulsion particle size related information
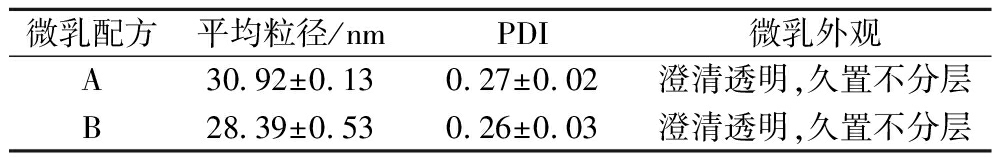
微乳配方平均粒径/nmPDI微乳外观A30.92±0.130.27±0.02澄清透明,久置不分层B28.39±0.530.26±0.03澄清透明,久置不分层
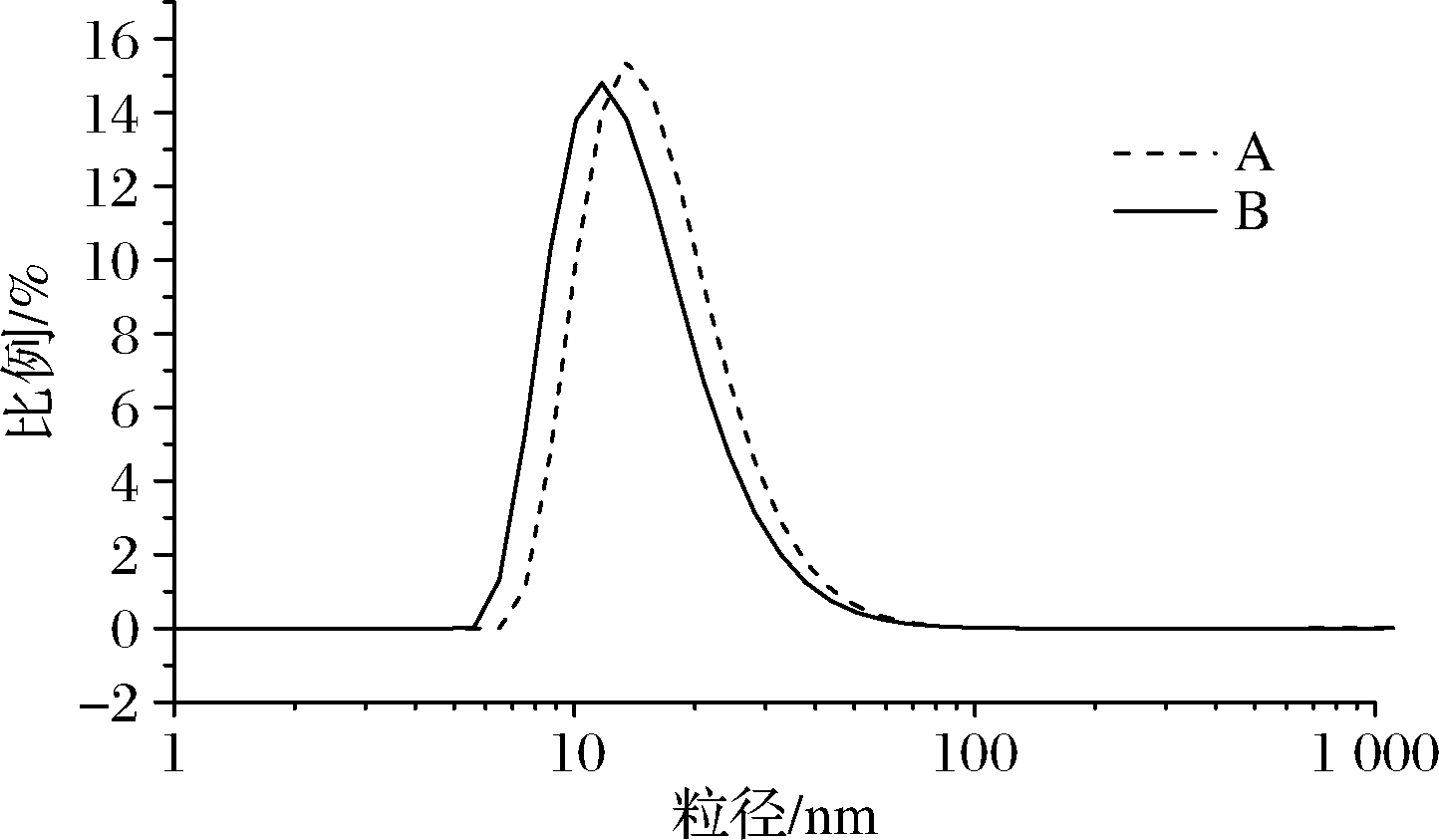
图6 茴香精油微乳粒径分布图
Fig.6 Particle size distribution of fennel essential oil microemulsion
微乳液的粒径范围值为10~100 nm,且PDI值越小,粒径分布越符合正态分布,体系越稳定。2种配方的平均粒径与PDI值相近,外观均呈现澄清透明的状态,因此,2种配方所得微乳差别不大。
3.4 茴香精油微乳液形貌分析
如图7所示,微乳颗粒表面呈球状或类球状分布,其中水相被磷钨酸染成黑色,不能被光线穿透,茴香精油可以被光线透过,符合可无限稀释型微乳特点,微乳体系粒子分散均匀、不聚集。

a-5 000×;b-6 000×
图7 茴香精油微乳的透射电镜图
Fig.7 Transmission electron microscope image of fennel essential oil microemulsion
3.5 茴香精油微乳液的性质
利用离心法判断该微乳在久置情况下的稳定性,由表6可知,茴香精油微乳在不同转速下,离心前后均澄清透明,久置不分层,透光率在90%以上,说明此微乳体系稳定性良好。
表6 离心速率对微乳稳定性的影响
Table 6 Effect of centrifugal speed on microemulsion stability

离心速率/(r·min-1)透光率/%微乳外观3 00097.49±2.39澄清透明,久置不分层4 00096.04±1.17澄清透明,久置不分层5 00095.04±1.76澄清透明,久置不分层6 00094.08±1.82澄清透明,久置不分层7 00096.15±2.75澄清透明,久置不分层
由图8可知,当温度>80 ℃时,茴香精油微乳的透光率快速下降,这可能由于随着温度的升高,分子热运动加剧,连接水相与表面活性剂的氢键断裂,导致表面活性剂吸附粒子速率下降,小油滴不断聚集,进而导致微乳液粒径突增,透光率骤降,微乳出现浑浊。因此,茴香精油微乳应在80 ℃以下进行保存。

a-微乳粒径、PDI;b-透光率
图8 不同温度下茴香精油微乳粒径、PDI变化及透光率变化
Fig.8 Changes of particle size, PDI and light transmittance of fennel essential oil microemulsion at different temperatures
微乳的稳定性与粒径和PDI值密切相关,PDI值越小微乳粒径越符合正态分布,体系越稳定。由图9可知,茴香精油在25 ℃贮藏90 d,其粒径大小和PDI值无显著差异,而茴香精油微乳在4 ℃贮藏过程中,微乳粒径和PDI值均出现显著上升趋势,这可能由于低温会破坏微乳体系的液界膜,使微乳出现分层浑浊现象。

a-25 ℃;b-4 ℃
图9 在25 ℃和4 ℃下微乳粒径随贮藏时间的变化
Fig.9 Changes in particle size of microemulsion with storage time at 25 ℃ and 4 ℃
3.6 茴香精油抗氧化能力
茴香精油中含有多种抗氧化的活性成分,为判断微乳体系对茴香精油自身生物活性的影响,因此,进行DPPH自由基、·OH、·O2-清除能力及总还原力实验。
由图10可知,相同质量浓度的茴香精油微乳与茴香精油的抗氧化性存在显著差异,乳化后的茴香精油抗氧化性得到显著提高,这是因为微乳体系作为载体能够有效保护茴香精油中的活性物质不被破坏,使其均匀分布在微乳体系内,增加活性成分的作用效果。且茴香精油所占比例分数越大,反应体系中茴香脑和萜类内酯等成分越多,茴香精油微乳中的油水液界膜能保护茴香脑和萜类内酯等抗氧化成分,进而终止自由基的自氧化链式反应,虽无法与一些天然抗氧化剂相比,但仍存在较好的抗氧化活性,且从以上4个指标得出,茴香精油微乳的抗氧化活性高度依赖剂量。

a-DPPH自由基清除能力;b-·OH清除能力;c-·O2-清除能力;d-总还原力测定
图10 茴香精油及微乳液抗氧化活性
Fig.10 Antioxidant activity of fennel essential oil and microemulsion
4 结论
本研究提供了一种可有效提高茴香精油稳定性及作用效果的微乳制备方法。以茴香精油生物活性为基础,选用吐温-80+吐温-40、丙三醇及茴香精油乳化形成外观澄清透明流动性强的茴香精油微乳,该微乳具体配比如下:吐温-80+吐温-40∶丙三醇∶茴香精油=4∶2∶1.5和6∶3∶1。通过电导法,可知该微乳水分含量>62%时为O/W型,水分含量<48%时为W/O型,水分含量在48%~62%时为B.C型。对其粒径检测后,发现该微乳粒径较小,聚合程度较高且较稳定。经过透射电镜观察可知茴香精油微乳为规则的圆球状或类球状,说明乳液分散均匀,不聚集,微乳整体稳定性高。对该微乳离心稳定性、热稳定性及贮藏稳定性研究可知,茴香精油微乳稳定性较好,常温下更利于茴香精油微乳的贮藏,可在25 ℃下贮藏90 d。茴香精油具有较好的体外抗氧化活性,故此茴香精油微乳可以有效提高茴香精油活性成分利用率及稳定性。该研究改善了茴香精油活性成分利用度和稳定性,为食品行业提供了一种新的食品保鲜剂方案。
[1] ABDELLAOUI M, BOUHLALI E D T, DEROUICH M, et al.Essential oil and chemical composition of wild and cultivated fennel (Foeniculum vulgare Mill.):A comparative study[J].South African Journal of Botany, 2020, 135:93-100.
[2] SHAHAT A A, IBRAHIM A Y, HENDAWY S F, et al.Chemical composition, antimicrobial and antioxidant activities of essential oils from organically cultivated fennel cultivars[J].Molecules (Basel, Switzerland), 2011, 16(2):1 366-1 377.
[3] RATHER M A, DAR B A, SOFI S N, et al.Foeniculum vulgare:A comprehensive review of its traditional use, phytochemistry, pharmacology, and safety[J].Arabian Journal of Chemistry, 2016, 9:S1574-S1583.
[4] 彭茜, 戴志远, 宋恭帅, 等.壳聚糖微胶囊对鱼油品质的影响[J].中国食品学报, 2020, 20(5):222-230.
PENG X, DAI Z Y, SONG G S, et al.Effect of chitosan microcapsules on the quality of fish oil[J].Journal of Chinese Institute of Food Science and Technology, 2020, 20(5):222-230.
[5] 吕奇晏, 林诗叶, 米亚妮, 等.聚乙二醇1000维生素E琥珀酸酯-皂皮皂素微乳液的制备、表征及活性[J].食品科学, 2021, 42(24):9-15.
LYU Q Y, LIN S Y, MI Y N, et al.Preparation, characterization and activity of D-α-tocopheryl polyethylene glycol 1000 succinate-saponin microemulsion[J].Food Science, 2021, 42(24):9-15.
[6] 易醒, 罗俊溢, 骆叶晴, 等.紫苏子油O/W型纳米微乳的制备及其氧化稳定性[J].中国食品学报, 2021, 21(4):185-192.
YI X, LUO J Y, LUO Y Q, et al.Preparation and oxidation stability of perilla seed oil O/W nano-emulsion[J].Journal of Chinese Institute of Food Science and Technology, 2021, 21(4):185-192.
[7] 朱加进, 叶璐, 常成, 等.南极磷虾油W/O型微乳液制备及稳定性研究[J].中国食品学报, 2017, 17(10):80-87.
ZHU J J, YE L, CHANG C, et al.Preparation and stability study of krill oil microemulsion[J].Journal of Chinese Institute of Food Science and Technology, 2017, 17(10):80-87.
[8] MONTEIRO C, FERREIRA L L, DE PAULA L G F, et al.Thymol and eugenol microemulsion for Rhiphicephalus sanguineus sensu lato control:Formulation development, field efficacy, and safety on dogs[J].Veterinary Parasitology, 2021, 296:109501.
[9] VON CORSWANT C, THORÉN P E G.Solubilization of sparingly soluble active compounds in lecithin-based microemulsions: Influence on phase behavior and microstructure[J].Langmuir, 1999, 15(11):3 710-3 717.
[10] 陶紫, 赵振刚.香茅草精油微乳液的构建及其抗氧化活性分析[J].现代食品科技, 2018, 34(10):156-164.
TAO Z, ZHAO Z G.Preparation of microemulsion of Cymbopogon citratus(DC) stapf essential oil and analysis of antioxidant activity[J].Modern Food Science and Technology, 2018, 34(10):156-164.
[11] REGEV O, EZRAHI S, ASERIN A, et al.A study of the microstructure of a four-component nonionic microemulsion by cryo-TEM, NMR, SAXS, and SANS[J].Langmuir, 1996, 12(3):668-674.
[12] 闫梦茹, 张文博, 罗国平, 等.复方丁香油自微乳化给药系统的制备及体外评价[J].化学工程师, 2019, 33(3):6-9.
YAN M R, ZHANG W B, LUO G P, et al.Preparation of self-microemulsifying drug delivery system of Compound Clove Oil[J].Chemical Engineer, 2019, 33(3):6-9.
[13] SONG X Q, WANG L P, LI S T, et al.Evaluation of phase behavior, microstructure transition and antiradical activity of lavender essential oil-based microemulsions[J].Journal of Dispersion Science and Technology, 2019, 40(9):1 360-1 367.
[14] WANG L, WU H L, YIN X L, et al.Simultaneous determination of umbelliferone and scopoletin in Tibetan medicine Saussurea laniceps and traditional Chinese medicine Radix angelicae pubescentis using excitation-emission matrix fluorescence coupled with second-order calibration method[J].Spectrochimica Acta Part A:Molecular and Biomolecular Spectroscopy, 2017, 170:104-110.
[15] KIM S, NG W K, SHEN S C, et al.Phase behavior, microstructure transition, and antiradical activity of sucrose laurate/propylene glycol/the essential oil of Melaleuca alternifolia/water microemulsions[J].Colloids and Surfaces A:Physicochemical and Engineering Aspects, 2009, 348(1-3):289-297.
[16] 吾哈丽妮萨·麦麦提托合提, 帕尔哈提·柔孜, 杨晓君, 等.响应面优化马骨髓蛋白的提取工艺及其抗氧化活性研究[J].食品工业科技, 2021, 42(12):151-159.
WUGULNISA M, PARHAT R, YANG X J, et al.Optimization of extraction technology of horse bone marrow protein by response surface methodology and its antioxidant activity[J].Science and Technology of Food Industry, 2021, 42(12):151-159.
[17] CHOI O, CHO S K, KIM J, et al.In vitro antibacterial activity and major bioactive components of Cinnamomum verum essential oils against cariogenic bacteria, Streptococcus mutans and Streptococcus sobrinus[J].Asian Pacific Journal of Tropical Biomedicine, 2016, 6(4):308-314.
[18] 郭刚军, 胡小静, 彭志东, 等.不同压榨方式澳洲坚果油品质及抗氧化活性比较[J].食品科学, 2018, 39(13):125-132.
GUO G J, HU X J, PENG Z D, et al.Comparison of quality and antioxidant activity of press-processed macadamia(Macadamia ternifolia F.muell.) oils[J].Food Science, 2018, 39(13):125-132.
[19] 中华人民共和国国家卫生和计划生育委员会. GB 2760—2014食品安全国家标准 食品添加剂使用标准[S].北京:中国标准出版社, 2014.
National Health Commission of the People’s Republic of China.GB 2760—2014 National food safety standard for use of food additives[S].Beijing:China Standards Press, 2014.
[20] 崔绮嫦, 吴克刚, 莫镕弛, 等.溶剂和微乳化的稀释效应对食用植物精油抗菌活性的影响[J].中国食品学报, 2020, 20(3):195-203.
CUI Q C, WU K G, MO R C, et al.Dilution effect of solvent and micro emulsification on the antibacterial activity of plant essential oils[J].Journal of Chinese Institute of Food Science and Technology, 2020, 20(3):195-203.
[21] 张昭. 基于百里香精油微乳液层层自组装微胶囊的淀粉基薄膜的抗菌保鲜应用[D].武汉:华中农业大学, 2019.
ZHANG Z.Application on antiseptic preservation of starch films with thyme essential oil microemulsion and layer-by-layer self-assembly microcapsule[D].Wuhan:Huazhong Agricultural University, 2019.
[22] JIN J F, WANG H Y, JING Y N, et al.An efficient and environmental-friendly dispersant based on the synergy of amphiphilic surfactants for oil spill remediation[J].Chemosphere, 2019, 215:241-247.
[23] PENG C, SVIRSKIS D, LEE S J, et al.Design of microemulsion system suitable for the oral delivery of poorly aqueous soluble beta-carotene[J].Pharmaceutical Development and Technology, 2018, 23(7):682-688.
[24] 郭静, 蒋建国, 韦林洪, 等.橄榄油微乳体系的相行为及影响因素研究[J].食品工业科技, 2019, 40(7):35-40.
GUO J, JIANG J G, WEI L H, et al.Study on phase behavior and influence factors of olive oil microemulsion[J].Science and Technology of Food Industry, 2019, 40(7):35-40.
[25] WARISNOICHAROEN W, LANSLEY A B, LAWRENCE M J.Nonionic oil-in-water microemulsions:The effect of oil type on phase behaviour[J].International Journal of Pharmaceutics, 2000, 198(1):7-27.
[26] ABBASI S, RADI M.Food grade microemulsion systems:Canola oil/lecithin:n-propanol/water[J].Food Chemistry, 2016, 194:972-979.
[27] 陈宗淇, 郝策, 赵泽荣, 等.pH和盐类对非离子型表面活性剂所组成微乳液的异常流变性影响[J].化学学报, 1995, 53(7):625-631.
CHEN Z Q, HAO C, ZHAO Z R, et al.The effects of salts and pH value on bizarre rheological properties of microemulsions with nonionic surfactant[J].Acta Chimica Sinica, 1995, 53(7):625-631.
[28] CHEN B R, HOU M N, ZHANG B, et al.Enhancement of the solubility and antioxidant capacity of α-linolenic acid using an oil in water microemulsion[J].Food &Function, 2017, 8(8):2 792-2 802.
[29] XU Z B, JIN J, ZHENG M Y, et al.Co-surfactant free microemulsions:Preparation, characterization and stability evaluation for food application[J].Food Chemistry, 2016, 204:194-200.