鲍鱼又称“腹鱼”、“海耳”,是一种原始的海洋贝类,是海味八珍之一,因其肉质细嫩,味泽鲜美,被称为海味之冠。主要分布在我国福建、山东、广东海域[1],养殖产量逐年上升,传统的简单加工已不能满足当前社会的需求。鲍鱼营养价值极高,富含丰富的氨基酸、矿物质[2],且种类齐全,是典型的高蛋白低脂肪海洋食品[3],同时也具有药用价值,《本草纲目》中记载,鲍鱼性平,味甘、咸,可明目补虚、清热滋阴、养血益胃、补肝肾[4]。现代食品药品领域研究发现,鲍鱼是开发海洋生物活性物质的重要生物来源,具有抗炎[4]、抗氧化[5]、抗菌[6]、抗肿瘤[7]、降血脂[8]、抗动脉粥样硬化[8]、免疫调节[9]等多种活性,其活性成分主要为多糖和多肽,本课题组前期研究中,以多种海洋贝类为原料进行酶解工艺优化[10],其中任鼎鼎等[9]以斑马鱼为动物模型验证了鲍鱼肌肉酶解产物的抗氧化和免疫活性。
衰老也称为老化,是一种随着年龄增长的自然退行性变化。随着科学的发展,人类寿命上升的同时也伴随着老龄化社会问题的加剧。因此抗衰老产品的开发已大势所趋。目前常见的抗衰老产品开发的原料多来源于食品及药食用源植物食材,如苹果、蓝莓、铁皮石斛、枸杞、党参等[11]。海洋生物由于其特殊的生存环境,常具有高活性、低毒性的特点,受到大量关注,成为抗衰老研究与开发的重要资源,如牡蛎、海参等[12-13]。目前虽未见鲍鱼抗衰老的相关研究报道,但其传统的保健功效及很多生物活性均与抗衰老密切相关,如抗氧化和免疫调节等功效。因此,深入系统地研究鲍鱼的抗衰老作用为新型海洋抗衰老产品的研发提供依据。
本研究在前期研究基础上,以秀丽隐杆线虫为动物模型,对鲍鱼肌肉酶解产物影响线虫应激损伤和寿命等进行研究,并确定其抗衰老的作用浓度,对鲍鱼的精深加工和新型产品的开发具有重要意义。
1 材料与方法
1.1 材料、试剂与仪器
材料:生鲜皱纹盘鲍,购于湛江市场;N2型秀丽隐杆线虫和OP50大肠杆菌,购于福建上源生物科学技术有限公司;
试剂:动物蛋白酶、风味蛋白酶(食品级),广西南宁庞博生物工程有限公司;次氯酸钠,上海易恩化学技术有限公司;NGM培养基,山东拓普生物工程有限公司;LB肉汤,青岛海博生物技术有限公司;LB琼脂,广东环凯微生物科技有限公司;盐酸左旋咪唑,上海麦克林生化科技有限公司;琼脂糖,翌圣生物科技有限公司。
仪器与设备:Thermo Lynx 6000高速落地离心机,美国Thermo Fisher Scientific公司;HH-8CJ 恒温磁力搅拌水浴锅,常州市金坛友联仪器研究所;EYELA旋转蒸发仪,日本EYELA公司;SRL-7045体式显微镜,北京天诺翔科学仪器有限公司;B60F生物正置显微镜,广州道一科学技术有限公司。
1.2 实验方法
1.2.1 鲍鱼肌肉酶解产物(Abalone muscle water extract residue enzymatic product,ARE)制备
将新鲜鲍鱼去壳去内脏,去除表面黑渍,洗净后沥干水分分装,-80 ℃贮存备用。酶解方法根据参考文献稍作修改[9],主要步骤如下:鲍鱼解冻后吸干表面水分,切粒,加入超纯水(1∶4,g∶mL)打浆,100 ℃蒸煮1 h,200目纱布过滤后取滤渣,各加入0.3%(质量分数)的动物蛋白酶和风味蛋白酶,于53 ℃恒温水浴锅中酶解4 h,100 ℃灭酶10 min,迅速冷却后,4 ℃离心(8 000 r/min)20 min,取上清液,过滤收集上清液,45 ℃真空旋转蒸发浓缩,冷冻干燥得鲍鱼肌肉酶解提取物,即ARE,-80 ℃贮存。
1.2.2 一般营养成分分析
对ARE进行一般营养成分分析,蛋白质测定参考GB 5009.5—2016采用凯氏定氮法;总糖测定参考GB/T 9695.31—2008采用硫酸-苯酚法;脂肪测定参考GB 5009.6—2016采用索氏抽提法;灰分测定参考GB 5009.4—2016采用高温灼烧法;水分测定参考GB 5009.3—2016采用直接干燥法。
1.2.3 线虫的培养和同期化
参考试剂说明,配制NGM培养基,高温高压灭菌后,倒入60 mm培养皿,得到新鲜培养板,于培养板上涂布有200 μL的OP50菌液,晾干过夜培养。次日,将线虫转移至新鲜食物板,于20 ℃恒温培养箱中培养[14]。同期化采用高氯酸钠裂解法[15]。用M9缓冲液冲洗线虫培养基,将大量处于产卵期的秀丽隐杆线虫收集至EP管中,静置,待线虫沉淀完全后,去上清液,再加入1 mL现配裂解液[V(H2O)∶V(NaOH)∶V(NaClO)=8∶1∶1],振荡3 min,离心,弃上清液,加入M9缓冲液清洗3次,将洗涤后的虫卵转移至含有OP50的NGM培养基上,于20 ℃培养 48 h,即完成同期化。
1.2.4 ARE对线虫寿命的影响
将同期化培养至L4时期的线虫随机挑入涂布有3种不同质量浓度的ARE(与OP50菌液以体积比1∶1混合,终质量浓度分别为2.50、1.25、0.25 mg/mL)培养基中,以LB肉汤组作为空白对照。期间若缺少食物或者生长环境不佳,及时更换至新鲜NGM培养基板,每个浓度设置3个平行,每个平板不少于30只线虫,置于20 ℃恒温培养箱中培养,每隔24 h记录线虫的存活数,死亡数,消失数,直至线虫全部死亡,绘制生存曲线。
1.2.5 ARE对线虫运动能力的影响
收集同期化培养至L4时期的线虫,实验分组及处理同方法1.2.4。在第5、10、15天观察线虫的运动能力,按分类标准记录每组线虫的运动情况,实验重复3次。线虫的运动能力被分为3个等级标准,分别为A,线虫自发而平稳地运动;B,线虫在受到刺激时可运动;C,线虫在受到刺激时仅头部和尾部摆动。
1.2.6 ARE对线虫的体长及脂褐素的影响
收集同期化培养至L4时期的线虫,按照方法1.2.4处理72 h后,将各组线虫分别转移至准备好的琼脂糖垫片上,滴加左旋盐酸咪唑碱溶液进行麻醉处理,每组线虫不少于15只,荧光显微镜观察并采集线虫图片,通过Image J软件分析线虫体内脂褐素相对含量和体长。
1.2.7 ARE对线虫繁殖力的影响
将同期化培养至L4时期的线虫随机挑入涂有不同浓度ARE食物的培养板中,每个板放置1只线虫,每组数量不少于10个,置于20 ℃恒温培养。每隔24 h将线虫转移至新鲜培养板,同时统计旧板上的产卵数及幼虫数量,直至线虫产卵期结束,统计产卵量总和。
1.2.8 ARE对线虫热应激损伤的影响
将同方法1.2.4处理72 h的线虫转移至不含任何食物的新鲜培养板中,每个板30只,每组3个平行,于35 ℃培养箱中培养8 h,再将线虫转移至20 ℃培养箱中恢复12 h后,统计每组存活数,并计算存活率。
1.2.9 ARE对百草枯氧化应激损伤线虫的影响
收集同期化至L4时期的线虫,将线虫随机挑入涂有不同浓度ARE和5 mmol/L百草枯的培养板中进行培养,以不含ARE的培养板作为空白对照,每隔24 h记录线虫的存活数,死亡数,消失数,直至线虫全部死亡,绘制生存曲线。
1.2.10 ARE对线虫体内抗氧化酶活力的影响
收集同期化培养至L4时期的线虫,按照方法1.2.4处理72 h后,收集各处理组与对照组的线虫于EP管中,用M9缓冲液洗涤数次,加入提取液冰浴超声破碎,4 ℃离心(3 000 r/min)10 min,取上清液,按照试剂盒所述方法测定超氧化物歧化酶(superoxide dismutase,SOD)、谷胱甘肽(glutathione,GSH)活力和丙二醛(malondialdehyde,MDA)含量。
1.2.11 数据分析
试验均独立重复3次,结果以平均数±标准差(Mean±SD)表示,采用JMP Pro 16 软件通过单因素方差分析法进行显著性分析(P<0.05)。采用Graphpad prism 9.2.0对实验结果进行绘图。
2 结果与分析
2.1 ARE基本成分分析结果
成分分析结果显示,ARE中蛋白含量最高,达86.94%,总糖含量为8%,脂肪含量最低,约占0.05%(均为质量分数)(表1),表明ARE的主要成分为蛋白质。鲍鱼肌肉中的大部分碳水化合物水溶性较强[2],且与课题组前期研究相比[9],该处理方法获得的鲍鱼肌肉酶解产物蛋白含量提高,总糖含量降低,表明ARE是一种高蛋白,低脂肪的优质海洋食品来源。
表1 ARE基本成分分析 单位:%
Table 1 Analysis of the basic components of ARE
蛋白质碳水化合物脂肪灰分水分86.94±1.938.00±0.700.05±0.012.7±0.054.61±0.30
注:数据以干基计(质量分数)
2.2 ARE对线虫寿命的影响
秀丽隐杆线虫的寿命实验是评价ARE抗衰老效果最为直观的一个指标。本研究参考文献[16]并通过预实验设置多个浓度进行寿命实验,最终筛选出0.25、1.25、2.50 mg/mL 3个浓度进行后续实验。如表2所示,与空白对照相比,低中高浓度的ARE均能够显著延长秀丽隐杆线虫的寿命(P<0.05),分别延长了10.36%、14.13%和17.36%,其寿命曲线均明显右移,并呈现浓度梯度依赖式的增长(图1)。王力等[17]在牡蛎多肽组分的抗衰老作用研究结果中表明高剂量浓度处理组线虫平均寿命(19.67 d)与空白组(14.53 d)相比显著延长,其趋势与本研究结果较为接近。
表2 ARE对线虫寿命的影响(n=3)
Table 2 Effect of ARE on the lifespan of C.elegans

质量浓度/(mg·mL-1)数量平均寿命/d百分比/%最长寿命/d2.5010317.78±0.38a117.36221.259417.29±0.05ab114.13210.2510216.73±0.32c110.3620对照组9615.15±0.08d100.0019
注:同一列不同字母表示各组间存在显著性差异(P<0.05)(下同)
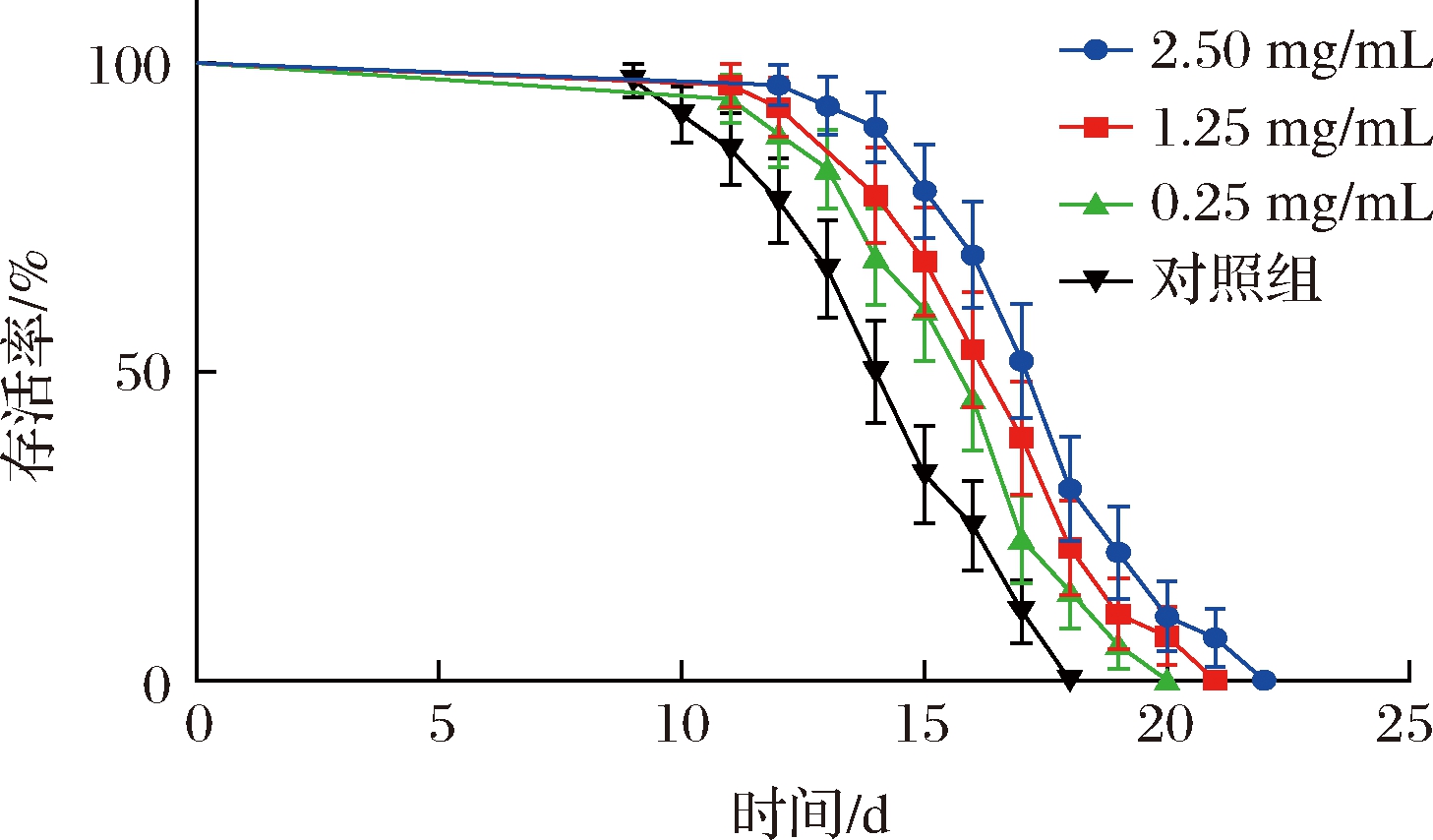
图1 ARE对线虫寿命的影响
Fig.1 Effect of ARE on the lifespan of C.elegans
2.3 ARE对线虫运动能力的影响
与人类一样,线虫的衰老往往伴随着运动能力的退化,线虫运动能力直观反映了其生长的健康状态,是评价抗衰老的重要指标之一[18]。由图2可知,与对照组相比,ARE处理组明显改善了线虫的运动能力,在生命中后期尤为显著。第5天,ARE处理组及对照组的线虫无须刺激便可自发运动,均处于A级运动;第10天,处于BC级运动的线虫占比均增加,其中2.50 mg/mL处理组仍有85%的线虫处于A级运动,与对照组相比处于A级运动的占比明显升高。第15天,对照组中处于A级运动的线虫约占33.33%,ARE 3个质量浓度(2.50、1.25、0.25 mg/mL)处理组中处于A级运动的线虫分别占56.66%、50.00%、40.00%。表明ARE显著提高了线虫的运动能力,且呈明显的剂量效应。

A级-线虫可自主运动;B级-线虫受到刺激可运动; C级-线虫受到刺激仅头尾运动
图2 ARE对线虫运动能力的影响
Fig.2 Effect of ARE on the motility of C.elegans
2.4 ARE对线虫体内脂褐素积累以及体长的影响
脂褐素是线虫肠道内自带荧光的一种老年色素,是由细胞内溶酶体消化产物和脂肪残积组成,不可通过胞吐作用排除,也无法降解,因此会随着年龄的增长在体内不断积累[19]。如图3-A和图4所示,与对照组相比,随着ARE浓度的增加,高中低浓度处理组线虫的荧光强度显著减弱,呈剂量依赖性,分别下降了21.93%、16.17%、8.18%(P<0.05),说明ARE能够有效降低线虫体内的脂褐素积累,但线虫体长没有显著变化(图3-B)。
2.5 ARE对线虫繁殖能力的影响
秀丽隐杆线虫繁殖能力极强,根据能量守恒原则,线虫寿命的增加将会伴随着繁殖力升高而下降[20]。如PARK等[21]在研究中发现在膳食中补充磷脂酰乙醇胺延长了秀丽隐杆线虫的寿命同时降低了线虫的繁殖能力。本研究中,与对照组相比,ARE显著增加了产卵量,最高增加了40%以上,说明ARE在延长线虫寿命的同时未损害其繁殖能力(图5),这与ZHANG等[22]的研究结果类似,他们的结果表明苦参种子多糖可延长线虫的寿命同时提高其繁殖能力。
2.6 ARE对线虫热应激损伤的保护作用
研究表明,秀丽隐杆线虫寿命延长与其对外界压迫的耐受能力及适应能力密切相关。秀丽隐杆线虫在高温环境下的抗逆能力是考察其抗衰老能力的一个重要指标,抗衰老能力与其抗热应激能力成正比[23]。由图6可知,经热激处理后,与对照组(51.72%)相比,经ARE处理组的线虫存活率随着浓度的增加而升高,不同质量浓度ARE(2.50、1.25、0.25 mg/mL)处理组的线虫存活率分别提高了35.85%、21.36%、12.96%,说明ARE对线虫热应激损伤具有保护作用,能增强线虫抵抗外界高温环境的应激能力。熊磊[24]在研究中发现,枸杞多糖不仅显著提高线虫的平均寿命,且大大提高了线虫在热应激情况下的存活率。

A-脂褐素水平;B-体长
图3 ARE对秀丽隐杆线虫体长及体内脂褐素含量的影响
Fig.3 Effect of ARE on lipofuscin and body size content in C.elegans 注:不同小写字母表示差异显著(P<0.05)(下同)
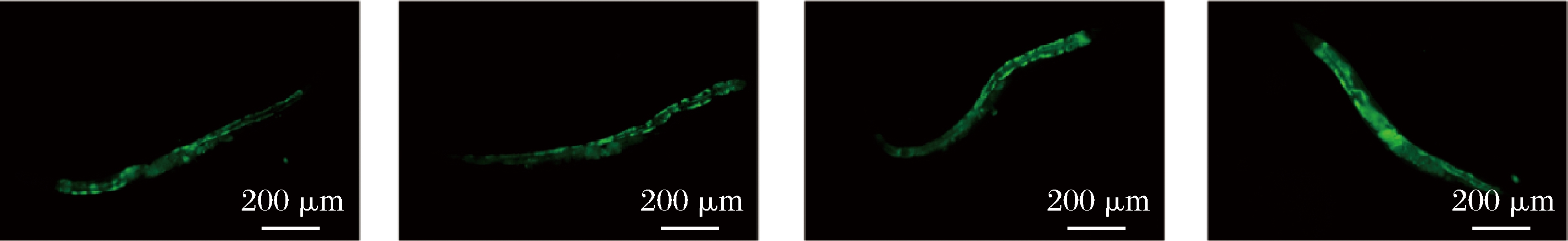
A-2.5 mg/mL ARE组;B-1.25 mg/mL ARE组;C-0.25 mg/mL ARE组;D-对照组
图4 ARE不同浓度处理组线虫荧光显微图片
Fig.4 Fluorescent micrographs of nematodes treated with different concentrations of ARE

图5 ARE对秀丽隐杆线虫繁殖力的影响
Fig.5 Effect of ARE on the fecundity of C.elegans
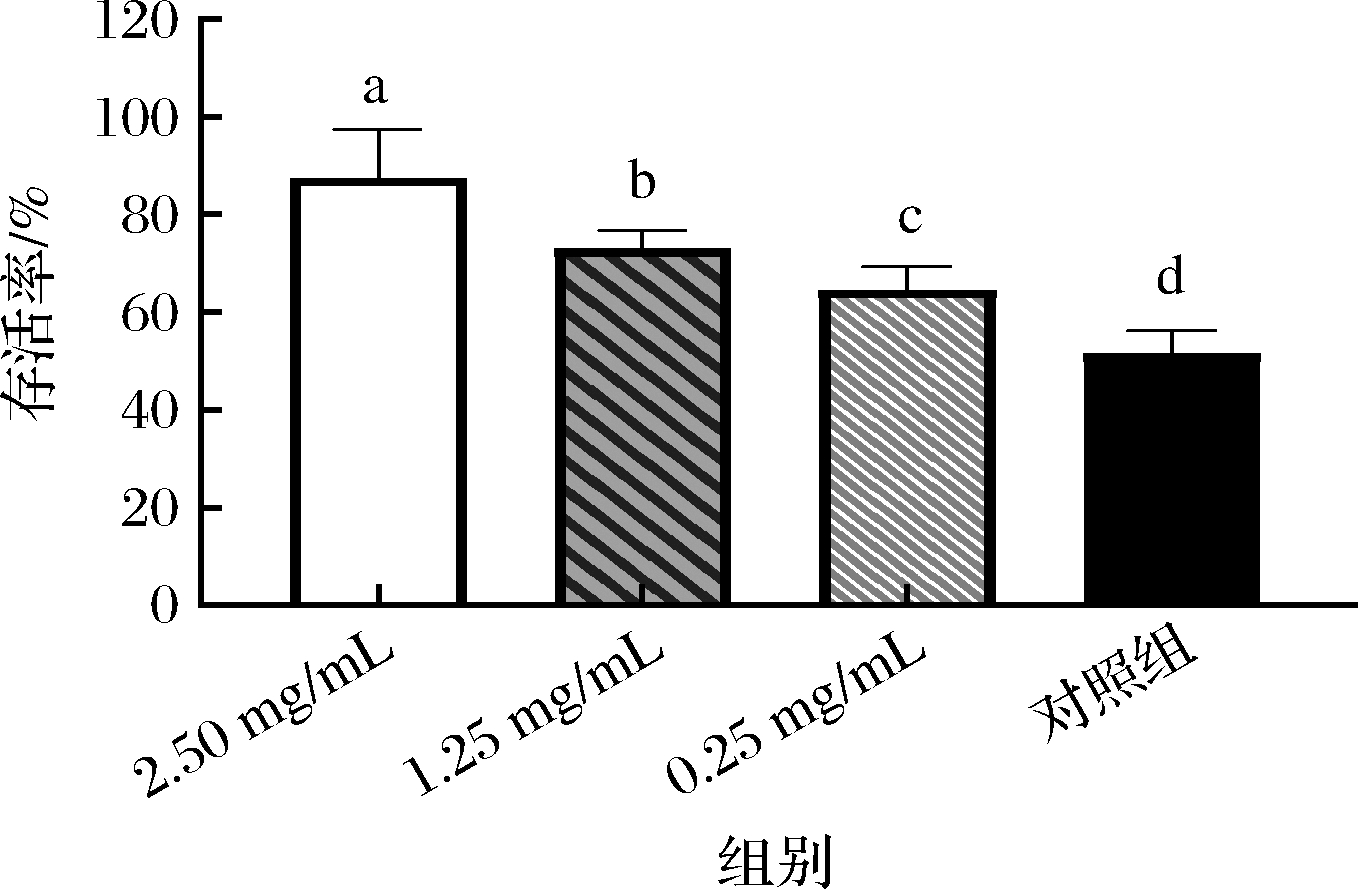
图6 ARE对线虫热应激损伤的影响
Fig.6 Effect of ARE on heat stress damage in C.elegans
2.7 ARE对线虫氧化应激损伤的影响
过量诱导的氧化应激会导致生物体细胞结构及分子功能损伤,具有抗氧化性物质可缓解氧化应激。百草枯作为氧化应激胁迫实验模型建立的诱导物质,是众所周知的线粒体毒物,而线粒体参与生物体的发育、寿命和繁殖[25]。由表3可知,在百草枯氧化应激处理下,空白组线虫平均寿命(9.25±0.69) d。与对照组相比,ARE处理线虫寿命显著延长,在0~2.50 mg/mL,从(9.25±0.69) d延长到(11.63±0.53) d。与空白对照组相比分别延长了9.51%、15.78%、25.73%,如图7所示,ARE处理组寿命曲线明显右移,呈现一定的剂量依赖性。说明,ARE对线虫百草枯氧化应激损伤具有明显的保护作用(表3)。林春秀等[26]以秀丽隐杆线虫为模型,分析了苦瓜青钱复合茶在不同氧化应激模型中的存活率,结果表明在百草枯胁迫下,复合茶对线虫有明显的保护作用,其平均寿命显著延长。
表3 ARE对百草枯氧化应激损伤线虫寿命的影响(n>3)
Table 3 Effect of ARE on life span damaged by paraquat in C.elegans
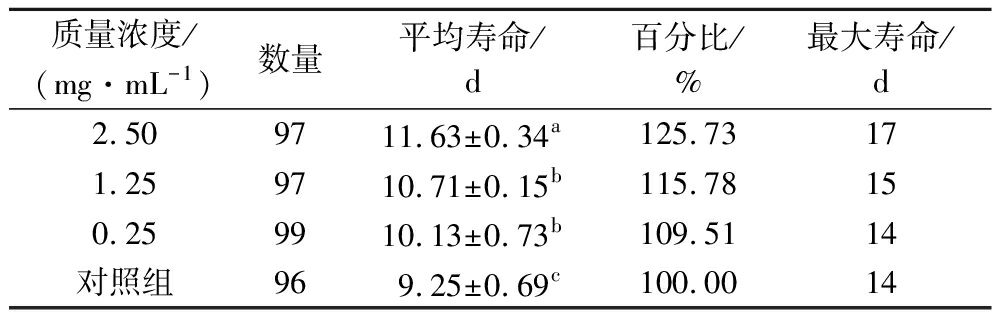
质量浓度/(mg·mL-1)数量平均寿命/d百分比/%最大寿命/d2.509711.63±0.34a125.73171.259710.71±0.15b115.78150.259910.13±0.73b109.5114对照组969.25±0.69c100.0014

图7 ARE对百草枯氧化应激损伤线虫寿命的影响
Fig.7 Effect of ARE on life span damaged by paraquat in C.elegans
2.8 ARE对线虫体内抗氧化酶活力的影响
随着年龄的增加,线虫体内抗氧化酶活力会随之降低,且在前期的研究中发现ARE能够减少年龄色素的积累,这表明ARE具有抑制体内氧化副产物产生的潜力。SOD、GSH是线虫体内主要的抗氧化酶,是抗氧化防御系统研究的重要指标。而MDA含量是细胞中多不饱和脂肪酸过氧化的重要产物之一,通常被认为是脂质过氧化和氧化应激最常用的指标[27]。如图8-A所示,与对照组相比,ARE高中低处理组中,SOD活性分别提高了33.33%、18.73%、11.06%;如图8-B所示,GSH活性分别提高了135.18%、40.16%、1.31%。MDA含量显著降低,与对照组相比,ARE高中低处理组MDA含量分别降低了73.39%、54.59%、51.83%(图9)。综上所述,ARE可有效提高线虫体内抗氧化酶活性,降低MDA含量,增强线虫体内氧化应激能力,进而延缓衰老。
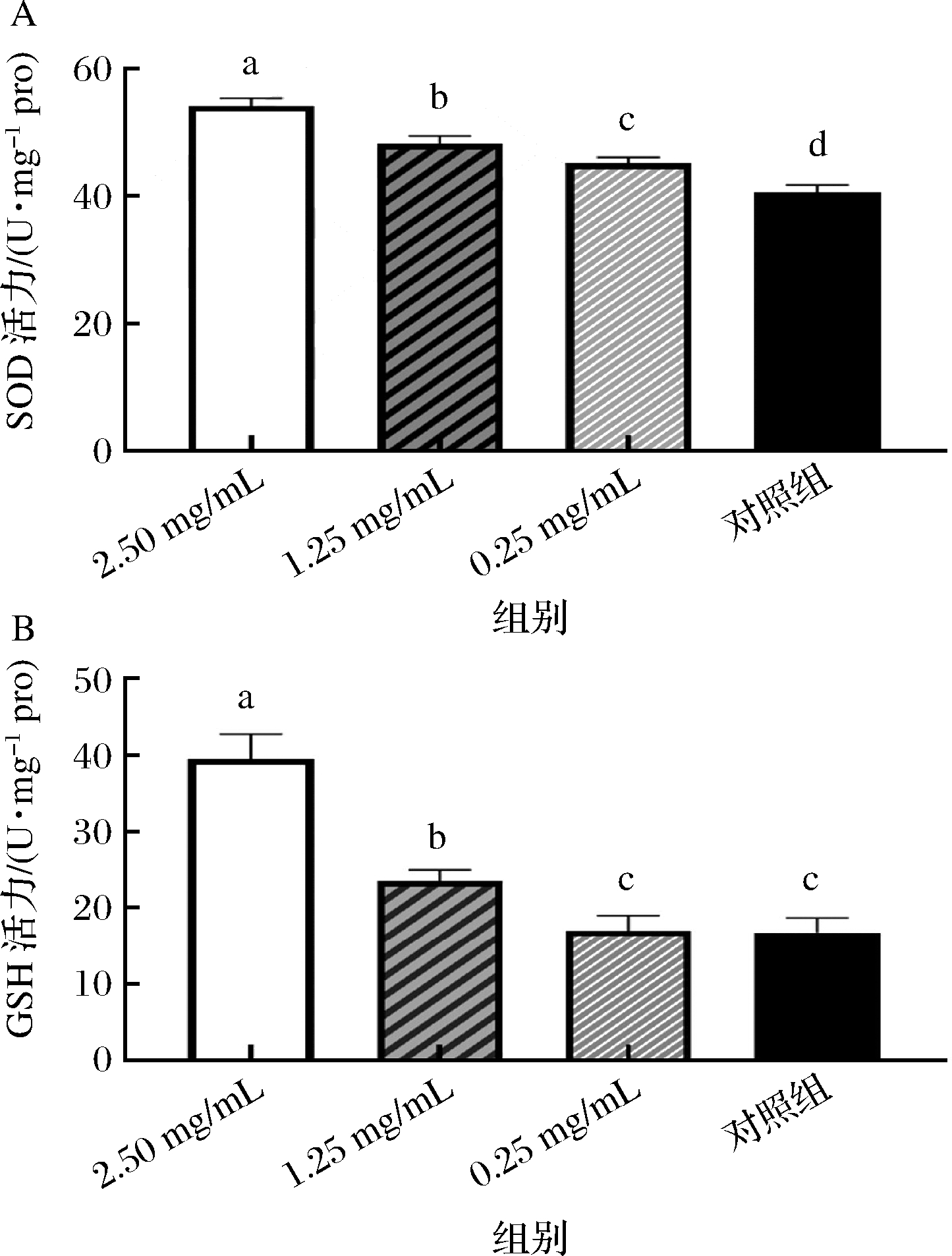
A-SOD;B-GSH
图8 ARE对线虫体内SOD、GSH活力的影响
Fig.8 Effect of ARE on SOD and GSH activities in C.elegans

图9 ARE对线虫体内MDA含量的影响
Fig.9 Effect of ARE on MDA content in C.elegans
3 结论
本实验以秀丽隐杆线虫作为动物实验模型,研究了ARE对秀丽隐杆线虫抗衰老作用的影响。结果发现,ARE可显著提高线虫的寿命,并且优化其生命健康体征,提高了线虫的运动能力,降低了线虫体内脂褐素水平,且不影响线虫的生殖能力,同时提高了线虫在急性应激损伤下的耐受力,提高了线虫体内抗氧化酶SOD和GSH的活力并降低线虫体内MDA含量,表明ARE具有延缓衰老的功效,为之后以鲍鱼为原料开发功能性食品奠定了基础。
[1] 王丹,吴反修.中国渔业统计年鉴[M].北京:中国农业出版社,2022.
WANG D, WU F X.China Fishery Statistical Yearbook[M].Beijing:China Agriculture Press, 2022.
[2] SHI L F, HAO G X, CHEN J, et al.Nutritional evaluation of Japanese abalone (Haliotis discus hannai Ino) muscle:Mineral content, amino acid profile and protein digestibility[J].Food Research International, 2020,129:108876.
[3] 刘先进, 陈胜军, 李来好, 等.四种鲍鱼肌肉营养成分分析与品质评价[J].食品与发酵工业, 2018,44(5):227-231.
LIU X J, CHEN S J, LI L H, et al.Nutritional analysis and quality evaluation of four kinds of abalone muscle[J].Food and Fermentation Industries, 2018,44(5):227-231.
[4] 王敏, 卢赛, 张曾亮, 等.鲍鱼水解肽的抗氧化、抗炎及免疫调节作用[J].食品工业科技, 2021,42(5):282-288.
WANG M, LU S, ZHANG Z L, et al.Antioxidant, anti-inflammatory and immunomodulatory effects of abalone hydrolytic peptide[J].Science and Technology of Food Industry, 2021,42(5):282-288.
[5] ZHENG P S, HAO G X, WENG W Y, et al.Antioxidant activities of hydrolysates from abalone viscera using subcritical water-assisted enzymatic hydrolysis[J].Food and Bioprocess Technology, 2019,12(6):910-918.
[6] 张瑞娟, 柯莉娜, 郑静, 等.鲍鱼内脏多糖的提取、纯化及其抗氧化和抑菌活性[J].厦门大学学报(自然科学版), 2018,57(1):58-64.
ZHANG R J, KE L N, ZHENG J, et al.Extraction,purification and antioxidant and antibacterial activity analysis of polysaccharides from abalone viscera[J].Journal of Xiamen University(Natural Science), 2018,57(1):58-64.
[7] GONG F, CHEN M F, CHEN J L, et al.Boiled abalone byproduct peptide exhibits anti-tumor activity in HT1080 cells and HUVECs by suppressing the metastasis and angiogenesis in vitro[J].Journal of Agricultural and Food Chemistry, 2019,67(32):8 855-8 867.
[8] LIU B X, JIA Z, LI C C, et al.Hypolipidemic and anti-atherogenic activities of crude polysaccharides from abalone viscera[J].Food Science &Nutrition, 2020,8(5):2 524-2 534.
[9] 任鼎鼎, 黄梦怡, 郑惠娜, 等.皱纹盘鲍(Haliotis discus hannai Ino)肌肉酶解产物制备及其免疫活性研究[J].食品与发酵工业, 2020,46(23):21-28.
REN D D, HUANG M Y, ZHENG H N, et al.Preparation and immunoactivity of enzymatically hydrolyzed products of abalone (Haliotis discus hannai Ino) muscle[J].Food and Fermentation Industries, 2020,46(23):21-28.
[10] 张雪妍, 秦小明, 高加龙, 等.牡蛎酶解工艺优化及其酶解产物对小鼠睾酮分泌的影响[J].广东海洋大学学报, 2019,39(3):96-102.
ZHANG X Y,QIN X M,GAO J L, et al.Optimization of enzymatic hydrolysis from crassostrea gigas and effects of its enzymatic hydrolysate on TM3 leydig cells[J].Journal of Guangdong Ocean University, 2019,39(3):96-102.
[11] 李敏,王德民,李峰,等.药食同源中药抗衰老研究进展[J].食品与药品,2019,21(5):414-418.
LI M, WANG D M, LI F, et al.Progress in anti-aging function of traditional Chinese medicine with characteristics of medicine and food[J].Food and Drug, 2019,21(5):414-418.
[12] 李鹏程. 海洋生物资源高值利用研究进展[J].海洋与湖沼, 2020,51(4):750-758.
LI P C.Research progress in high-value utilization of marine biological resources[J].Oceanologia et Limnologia Sinica, 2020,51(4):750-758.
[13] 王力, 肖嵋方, 刘斌, 等.海洋生物活性物质抗衰老作用研究进展[J].食品工业科技, 2021,42(22):433-441.
WANG L, XIAO M F, LIU B, et al.Research progress on the anti-aging effect of marine bioactive substances[J].Science and Technology of Food Industry, 2021,42(22):433-441.
[14] MUDD N, LICEAGA A M.Caenorhabditis elegans as an in vivo model for food bioactives:A review[J].Current Research in Food Science,2022,5:845-846.
[15] 迟东泽, 何源, 刘芳芳, 等.鹿鞭醇提物对秀丽隐杆线虫衰老的影响[J].食品工业科技, 2021,42(10):327-335.
CHI D Z, HE Y,LIU F F, et al.Effect of ethanol extracts of penis cervi on anti-aging in caenorhabditis elegans[J].Science and Technology of Food Industry, 2021,42(10):327-335.
[16] 王雪. 鹿茸醇提物对秀丽隐杆线虫抗衰老机制的研究[D].长春:吉林农业大学, 2020.
WANG X Anti-aging mechanism of velvet antler extract on Caenorhabditis elegans[D].Changchun:Jilin Agricultural University,2020.
[17] 王力, 肖嵋方, 陈弘培, 等.牡蛎多肽组分OE-I抗氧化活性及其对秀丽隐杆线虫抗衰老作用[J].食品科学, 2022,43(3):152-160.
WANG L, XIAO M F, CHEN H P, et al.Antioxidant activity of oyster peptide fraction OE-I and its anti-aging effect on caenorhabditis elegans[J].Food Science, 2022,43(3):152-160.
[18] YANG X Y, WANG H, LI T, et al.Nobiletin delays aging and enhances stress resistance of Caenorhabditis elegans[J].International Journal of Molecular Sciences, 2020,21(1):341.
[19] ZHANG M H, YANG X, XU W, et al.Evaluation of the effects of three sulfa sweeteners on the lifespan and intestinal fat deposition in C.elegans[J].Food Research International, 2019,122:66-76.
[20] 宋兵兵. 蓝莓和苹果皮提取物联合抗衰老活性及作用机制研究[D].广州:华南理工大学, 2020.
SONG B B.Antiaging activity of combination of blueberry and apple peel extracts:Mechanisms of action[D].Guangzhou:South China University of Technology, 2020.
[21] PARK S, KIM B, PARK S K.Supplementation with phosphatidylethanolamine confers anti-oxidant and anti-aging effects via hormesis and reduced insulin/IGF-1-like signaling in C.elegans[J].Mechanisms of Ageing and Development, 2021,197:111498.
[22] ZHANG Y, MI D Y, WANG J, et al.Constituent and effects of polysaccharides isolated from Sophora moorcroftiana seeds on lifespan, reproduction, stress resistance, and antimicrobial capacity in Caenorhabditis elegans[J].Chinese Journal of Natural Medicines, 2018,16(4):252-260.
[23] HUI H, XIN A Y, CUI H Y, et al.Anti-aging effects on Caenorhabditis elegans of a polysaccharide, O-acetyl glucomannan, from roots of Lilium davidii var.unicolor Cotton[J].International Journal of Biological Macromolecules, 2020,155:846-852.
[24] 熊磊. 枸杞多酚提取物抗衰老活性及其作用机制研究[D].广州:华南理工大学, 2021.
XIONG L. Study on anti-aging activity and mechanism of Lycium barbarum polyphenol extract.Guangzhou: South China University of Technology, 2021.
[25] BORA S,VARDHAN G S H,DEKA N,et al.Paraquat exposure over generation affects lifespan and reproduction through mitochondrial disruption in C.elegans[J].Toxicology,2021,447:152632.
[26] 林春秀, 林伊梓, 沈少丹, 等.苦瓜青钱柳复合茶对秀丽线虫的抗氧化作用[J].食品与发酵工业, 2020,46(23):178-183.
LIN C X, LIN Y Z, SHEN S D, et al. Antioxidant effect of a compound Momordica charantia and Cyclocarya paliurus tea on Caenorhabditis elegans. Food and Fermentation Industries, 2020, 46(23):178-183.
[27] LIN C X, CHEN Y, LIN Y Z, et al.Antistress and anti-aging activities of Caenorhabditis elegans were enhanced by Momordica saponin extract[J].European Journal of Nutrition, 2021,60(4):1 819-1 832.