柑橘在世界范围内不仅种植广泛,其在国际贸易农产品中也占有重要地位,我国是世界上主要的柑橘生产和贸易大国[1-2]。长期以来,柑橘的病虫害是引起柑橘果实生长发育不良的重要因素之一,不仅会引起柑橘品质的下降,也会造成严重的经济损失[3],甚至严重的地区可能会造成柑橘的绝收。近年国内外学者对水果挥发性成分进行了大量的研究[4-9],发现水果在感染病虫害前后,其所含挥发性成分的种类、含量均会有所变化,不同挥发性物质在空气系统中的扩散速度也不相同。然而,对于柑橘内部病虫害的检测,一直没有很好的方法,因此研究柑橘病虫害侵染前后几种含量发生显著变化的挥发性物质的运动轨迹及扩散能力具有重要意义,可为进一步快速检测柑橘内部病虫害提供一定的参考价值。
柑橘中的挥发性物质主要包括挥发性萜类物质、有机酸类、脂类、酮类、醇类、醛类和环氧化物等[10],在以桔小实蝇作为害虫侵染砂糖桔时,测定不同侵染时期柑橘的挥发性物质,其中β-榄香烯和正己醇为虫害侵染后新合成的,而α-松油醇的相对含量在虫害侵染达到一定时间后为零[11]。本研究采用分子动力学方法对β-榄香烯、正己醇和α-松油醇(以下简称不同挥发性物质)在空气中的运动扩散情况进行跟踪分析,并对其中机理进行阐述。
本研究从微观角度出发,构建了不同挥发性物质的层模型和气体混合模型。利用分子模拟对构建的层模型和气体混合模型分别通过结构优化,在NPT(isothermal-isobaric ensemble)、NVT(canonical ensemble)状态下进行动力学模拟,并且从质心运动、均方位移等参数,对不同挥发性物质的扩散能力以及运动状况进行分析,从相互作用能的角度对其机理进行解释。
1 分子动力学模拟
伴随科技的进步和计算机算力的快速发展,分子模拟技术也运用到各个领域之中,具有多学科交叉研究的特点。Material Studio(MS)是材料学科领域内的分子模拟软件,本文利用其构建分子的三维结构模型,通过对构建好的模型进行运算分析可以准确预测物质的相关性质及分子或原子间的互作关系,在近年来普遍被用于食品行业的研究,ZHOU等[12]利用MS对含水量的β-环糊精进行分子动力学模拟以预测其Tg,为扩大β-环糊精在提高食品基质的水溶性、稳定性和生物利用度等方面的应用提供参考;邱福生等[13]借助MS的分子动力学技术预测了壳聚糖的Tg,对壳聚糖在食品领域的应用有重要意义,同时借助实验验证了模拟结果的准确性,证明基于MS的分子动力学技术可用于预测高聚物Tg;LIU等[14]基于MS的分子动力学技术,解释了壳聚糖与姜黄素分子之间的微观相互作用对其形成的共混膜宏观性能的影响,并通过红外光谱进一步确定了模拟结果的正确性,认为该共混膜在食品包装和农产品贮藏方面具有潜在应用价值。在计算材料科学领域经常采用的数字模拟方法有分子动力学、第一性原理计算和有限元法,由于单一分子模拟方法可能无法满足科研需求,故采用以上3种常用方法,本研究涉及的所有计算均基于密度泛函理论(density functional theory,DFT)[15-16]。
1.1 模型的建立
1.1.1 层模型构建
本文研究建立的模型是层模型结构,首先把氮气、氧气、二氧化碳和稀有气体结构构建并组成空气系统,然后构建α-松油醇、β-榄香烯和正己醇结构,第一层为空气,第二层为挥发物。以α-松油醇构建的层模型为例,其层模型结构如图1所示。

图1 α-松油醇与空气系统层模型结构
Fig.1 Structure of the α-terpineol and air system layer model
1.1.2 混合模型构建
首先把氮气、氧气、二氧化碳和稀有气体结构构建组成空气系统,然后构建β-榄香烯、正己醇和α-松油醇结构,分别将以上3种挥发物质按比例混合到空气系统中,组成空气-挥发物混合模型。图2~图4分别是β-榄香烯、正己醇和α-松油醇的混合模型。

图2 β-榄香烯与空气系统混合模型结构
Fig.2 Structure of the β-elemene and air system mixing model

图3 正己醇与空气系统混合模型结构
Fig.3 Structure of the hexanol and air system mixing model

图4 α-松油醇与空气系统混合模型结构
Fig.4 Structure of the α-terpineol and air system mixing model
1.2 模拟细节
分子动力学主要是根据经典力学理论,通过分子力学力场、原子之间的相互作用势以及分子体系在空间和时间上运动的计算机模拟技术,通过微观体系反映物质宏观性质的技术[17]。
本研究使用Universal力场[18-19],在模拟分子运动时,为了使模型趋向稳定状态,一定要先进行充分放松,使得各个模型能量达到最小,然后优化每个模型的结构,在NVT集成下进行300~900 K的动态循环仿真,并在每次仿真后进行能量最小化。经上述过程,模型的能量处于较低状态,模型的结构也趋向稳定状态,与现实中材料的能量相近。这样分子动力学模拟得出的结果可以更好地反映实际材料在稳态下的性能变化。在上述完全松弛的条件下对NVT系综和NPT系综下的各个模型进行500 ps动力学模拟[20]。整个模拟的过程使用周期性边界条件。积分步骤为1 fs,且每500 fs收集1次系统中每个原子的动力学信息。
2 模拟结果与分析
2.1 质心运动轨迹
本研究分析了系统中不同挥发物质心运动的位移轨迹,清晰地展示了不同挥发物在空气中的扩散路径。分子扩散的位移计算如公式(1)所示:
(1)
式中:R(t)表示分子在t时刻相对于初始坐标的位移;![]() 代表初始时刻分子的空间位移矢量;
代表初始时刻分子的空间位移矢量;![]() 代表t时刻分子的空间位移矢量。
代表t时刻分子的空间位移矢量。
不同挥发性物质整体质心的运动轨迹如图5所示。在进行分子动力学模拟之前,首先将不同挥发性物质的质心位于空气中,即将挥发性物质整体的运动起点都设置于空气中,观察分子动力学模拟过程中不同挥发性物质质心在X、Y及Z轴方向的移动距离可知,正己醇在对应轴的最大移动位置分别是136.3、109、105.6 Å;α-松油醇在对应轴的最大移动位置分别是52.3、83.5、116 Å;β-榄香烯对应轴的最大移动位置分别是81.7、49.9、78.5 Å。通过对比不同挥发性物质的质心在空气中的极限位置可知,正己醇的质心在X、Y轴方向上移动的距离均是三者之中最大的,在Z轴方向虽然略小于α-松油醇质心移动距离,但并不影响其整体质心移动距离大于α-松油醇的质心移动距离。同理可知,由于α-松油醇的质心在Y、Z轴方向上移动的距离远大于β-榄香烯的质心移动距离,使得即使β-榄香烯的质心在X轴方向上移动距离比α-松油醇的质心移动距离大29.4 Å,但是α-松油醇整体质心移动距离大于β-榄香烯的质心移动距离。
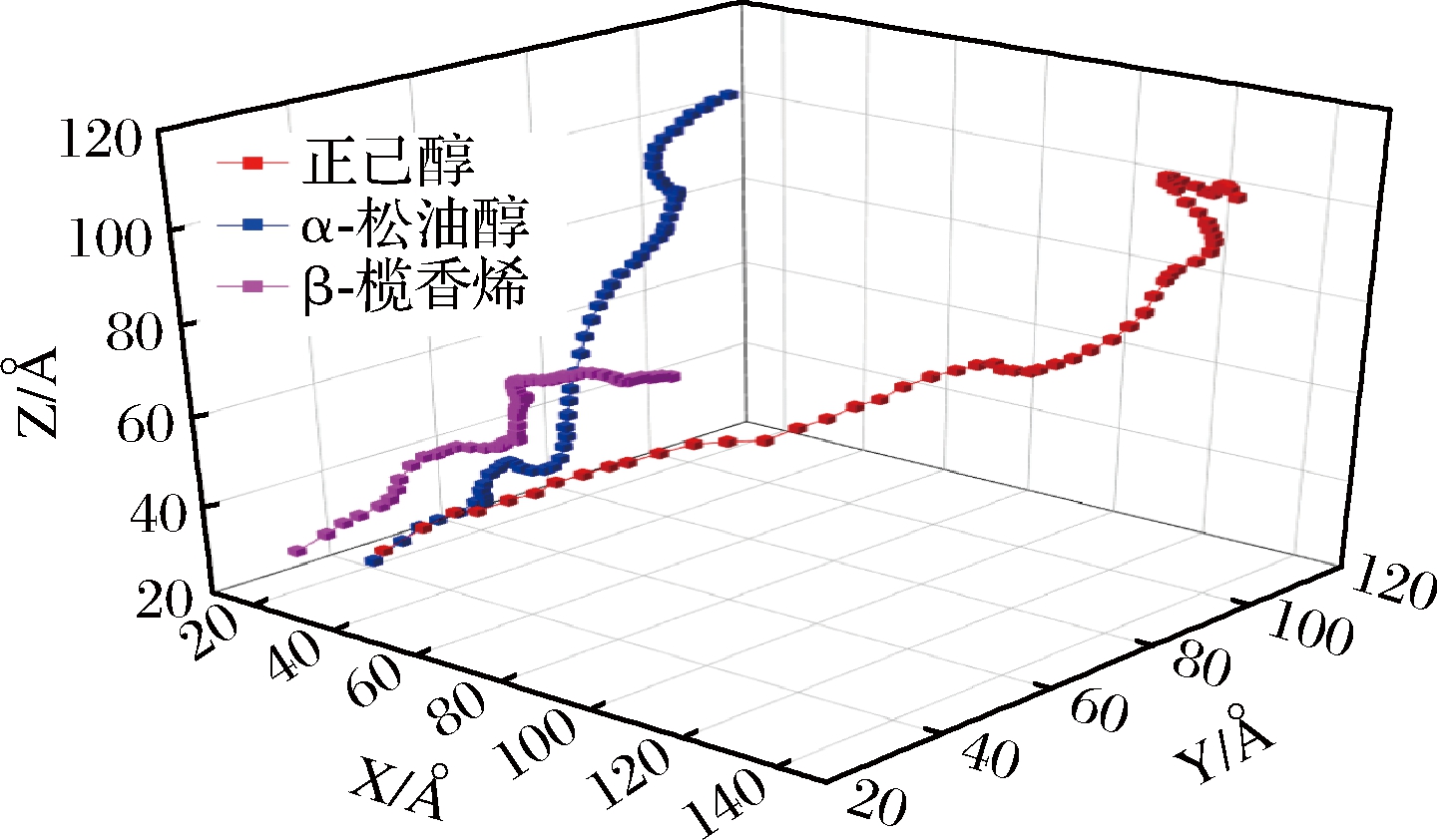
图5 不同挥发性物质质心运动轨迹
Fig.5 Barycenter’s trajectories of different volatile substances
综上所述可知,因为不同挥发性物质对于空气的亲和度存在差异,因此不同挥发性物质在空气中的运动情况也不相同,随着挥发性物质扩散时间的叠加,3种挥发性物质在空气中的质心扩散位移在X、Y和Z轴方向上的分量均出现不同差异,因此3种挥发性物质的质心移动距离也不相同,且它们之间的大小关系为:正己醇>α-松油醇>β-榄香烯。
2.2 不同挥发物与空气间的相互作用
2种物质之间的相互作用能计算如公式(2)所示:
Einter=Etotal-(EA+EB)
(2)
式中:Etotal为模型的总势能;Einter为模型中2种物质之间的相互作用能;EA和EB分别代表物质A与物质B的势能。相互作用能的正值与负值分别代表物质之间的相互排斥和吸附作用,其吸附作用效果随着负值的增大而增强。
图6反映的是不同挥发性物质与空气的相互作用能随着模拟时间变化的关系。由图6可知,不同挥发性物质与空气的相互作用能不同,β-榄香烯对应的相互作用能值均为负值且大小接近于0 kca/mol,其整体波动趋势十分平稳并无明显突变情况;α-松油醇对应的相互作用能值虽然在-40 kca/mol左右波动,但是波动幅度较小,整体处于相对平稳状态,且明显大于β-榄香烯,因此α-松油醇与空气的吸附作用强于β-榄香烯;正己醇对应的相互作用能值在-200 kca/mol上下波动,虽然波动幅度较大,但其大小明显大于α-松油醇的相互作用能值,且从整个时间线上观察可知,正己醇的相互作用能值波动趋势在一定范围内趋向平稳状态,并没有长时间随时间的延长出现相互作用能值持续增长或降低的趋势,因此正己醇与空气的吸附作用强于α-松油醇。综上可得,三者之间相互作用能的大小关系为:正己醇>α-松油醇>β-榄香烯。单一挥发性物质的作用能虽然有所波动,但整体波动趋势在一定范围内趋向平稳状态。三者相互作用能的大小存在明显差异,其中空气对正己醇的吸附能力最强,α-松油醇次之,β-榄香烯最弱。
2.3 分子扩散运动
为了进一步研究不同挥发性物质在空气中的扩散情况,本研究构建了3种挥发性物质-空气复合模型。对体系中粒子的运动轨迹进行分析,得到其热稳定性和动力学特性参数,分子链运动能表征不同挥发性物质在热运动下的微观情况。均方位移(mean square displacement,MSD)是反映分子链在一段时间内的质心位移情况,是描述分子链的重要参数之一。MSD计算如公式(3)所示:
MSD=s(t)=![]()
(3)
式中:l(0)为分子的初始位置,l(t)为t时刻分子的坐标。MSD值的大小代表扩散能力的强弱,二者之间成正比。

图6 不同挥发物质与空气的相互作用能
Fig.6 Interaction energy between different volatile substances
图7反映的是不同挥发性物质在空气复合模型中的MSD随着模拟时间的变化关系。由图7可知,在模拟初始阶段3种挥发性物质的MSD十分接近,并无明显差距。随着模拟时间的延长,虽然3种挥发性物质的MSD均呈现增长趋势,但是α-松油醇的MSD在模拟过程中随着时间的延长其模拟值均大于β-榄香烯,且两者之间的差距在模拟后期更加明显,所以α-松油醇在空气中的扩散能力强于β-榄香烯。正己醇的MSD在整个模拟过程中随着时间的延长明显大于α-松油醇,因此正己醇在空气中的扩散能力强于α-松油醇。综上可知,不同挥发性物质在空气中的扩散能力大小顺序为:正己醇>α-松油醇>β-榄香烯,而不同挥发性物质与空气的结合能大小排序为:正己醇>α-松油醇>β-榄香烯,由此可见挥发性物质与空气的相互作用能越大,其在空气中的扩散能力就越强,二者之间存在正相关性。

图7 不同挥发性物质在空气中的MSD
Fig.7 MSD of different volatile substances in air
3 结论
本文基于分子动力学模拟,通过对柑橘中正己醇、α-松油醇和β-榄香烯3种挥发性物质的运动轨迹和扩散能力的研究。分析了不同挥发性物质在空气系统中的分布,并从相互作用能的角度对其机理进行解释,得出以下结论:
(1)不同挥发性物质与空气的相互作用能不同,导致其在空气系统中的分布不同。经过对不同挥发性物质的运动轨迹进行跟踪,发现不同挥发性物质质心移动距离的大小与其相互作用能的大小之间成正相关性,正己醇质心移动距离最大。
(2)不同挥发性物质在空气中的扩散能力与相互作用能成正相关性。通过分析正己醇、α-松油醇、β-榄香烯在空气中的MSD发现,三者扩散能力的大小顺序为:正己醇>α-松油醇>β-榄香烯。
(3)对不同挥发性物质在空气中的扩散情况,分别从质心运动、相互作用能和扩散能力3个角度分析,得到的结果均显示正己醇在空气中扩散性能是三者中最适合检测的挥发性物质。因此在以挥发性物质对于柑橘内部病虫害进行检测时,选用正己醇用来检测较为合适。
[1] 温晗秋子, 郑永强, 刘杨.柑橘大数据研究与应用[J].农业大数据学报, 2021(1):33-44.
WEN H, ZHENG Y Q, LIU Y. Construction and application of a big data platform for intelligent apiculture. Journal of Agricultural Big Data, 2021(1): 33-44.
[2] 奎国秀, 祁春节.我国柑橘产业生产贸易的变化及机遇与挑战[J].中国果树, 2021(6):93-97.
KUI G X, QI C J.Changes, opportunities and challenges of citrus production and trade in China[J].China Fruits, 2021(6):93-97.
[3] 霍斐尔. 黄龙病菌对寄主植物淀粉代谢相关酶的影响及检测技术研究. 广州: 华南农业大学, 2016.
HUO F E. Effect of Huanglong pathogen on enzymes related to starch metabolism in host plants and its detection technology. Guangzhou: South China Agricultural University, 2016.
[4] 胡梓妍, 刘伟, 何双, 等.基于HS-SPME-GC-MS法分析3种金橘的香气挥发性成分[J].食品科学, 2021, 42(16):176-184.
HU Z Y, LIU W, HE S, et al.Analysis of volatile components in three varieties of kumquat by headspace solid phase microextraction-gas chromatography-mass spectrometry[J].Food Science, 2021, 42(16):176-184.
[5] 李莹. 基于电子鼻的苹果品质无损检测研究[D].杨凌:西北农林科技大学, 2014.
LI Y.Non-destructive testing of apple quality based on electronic nose[D].Yangling:Northwest Agriculture &Forestry University, 2014.
[6] 赵江丽, 何近刚, 岳盈肖, 等.1-甲基环丙烯对‘香水’梨果实品质和挥发性成分及相关基因表达的影响[J].食品科学, 2022,43(15):209-217.
ZHAO J L, HE J G, YUE Y X, et al.Effect of 1-MCP on quality and volatile organic components and related gene expression in ‘Xiangshui’ pear[J].Food Science, 2022,43(15):209-217.
[7] CECCARELLI A, FARNETI B, FRISINA C, et al.Harvest maturity stage and cold storage length influence on flavour development in peach fruit[J].Agronomy, 2018, 9(1):10.
[8] HIJAZ F, GMITTER JR F G, BAI J H, et al.Effect of fruit maturity on volatiles and sensory descriptors of four mandarin hybrids[J].Journal of Food Science, 2020, 85(5):1 548-1 564.
[9] 肖作兵, 蒋新一, 牛云蔚.水果香气物质分析研究进展[J].食品科学技术学报, 2021, 39(2):14-22.
XIAO Z B, JIANG X Y, NIU Y W.Research progress on analysis of aroma compounds in fruits[J].Journal of Food Science and Technology, 2021, 39(2):14-22.
[10] 张海朋, 刘翠华, 刘园, 等.柑橘中挥发性萜类物质代谢研究进展[J].园艺学报, 2020, 47(8):1 610-1 624.
ZHANG H P, LIU C H, LIU Y, et al.Research advances of volatile terpenoids metabolism in citrus[J].Acta Horticulturae Sinica, 2020, 47(8):1 610-1 624.
[11] 郑立章. 吹扫式仿生嗅觉检测分析平台的设计及试验研究. 长沙: 中南林业科技大学, 2018.
ZHENG L Z. Design and experimental study of purging bionic olfactory detection and analysis platform. Changsha: Central South University of Forestry &Technology, 2018.
[12] ZHOU G H, ZHAO T H, WAN J, et al. Predict the glass transition temperature and plasticization of β-cyclodextrin/water binary system by molecular dynamics simulation. Carbohydrate Research, 2015, 401: 89-95.
[13] 邱福生, 任力, 王家鸣, 等. 分子动力学模拟预测壳聚糖的玻璃化转变温度. 化工学报, 2012, 63(7): 2 285-2 289.
QIU F S, REN L, WANG J M, et al. Prediction of glass transition temperature of chitosan through molecular dynamics simulation. CIESC Journal, 2012 (7): 2 285-2 289.
[14] LIU Y J, CAI Y X, JIANG X Y, et al. Molecular interactions, characterization and antimicrobial activity of curcumin-chitosan blend films. Food Hydrocolloids, 2016, 52: 564-572.
[15] SHANKARA S, HYUNGTAK S. An experimental and density functional theory studies of Nb-doped BiVO4 photoanodes for enhanced solar water splitting. Journal of Catalysis, 2022, 410:144-155.
[16] 林艳, 刘芸, 魏晓楠, 等.基于密度泛函理论的叶绿素A性质的研究[J].原子与分子物理学报, 2017, 34(4):581-586.
LIN Y, LIU Y, WEI X N, et al.Study on the nature of chlorophyll A based on density functional theory[J].Journal of Atomic and Molecular Physics, 2017, 34(4):581-586.
[17] 张宝花, 徐顺.GROMACS软件并行计算性能分析[J].计算机系统应用, 2016, 25(12):16-23.
ZHANG B H, XU S.Parallel computing performance analysis on GROMACS software[J].Computer Systems &Applications, 2016, 25(12):16-23.
[18] 王晴, 康升荣, 吴丽梅, 等.地聚合物凝胶结构建模及分子动力学模拟[J].材料导报, 2020, 34(4):4 056-4 061.
WANG Q, KANG S R, WU L M, et al.Structural modeling and molecular dynamics simulation of geopolymers gel[J].Materials Review, 2020, 34(4):56-61.
[19] 黄世强, 朱申敏, 程时远.聚合物分子模拟中的力场[J].高分子材料科学与工程, 1999, 15(4):18-22.
HUANG S Q, ZHU S M, CHENG S Y.Force field for molecular simulations of macromolecules[J].Polymer Materials Science &Engineering, 1999, 15(4):18-22.
[20] DU D Y, TANG C, ZHANG J W, et al.Effects of hydrogen sulfide on the mechanical and thermal properties of cellulose insulation paper:A molecular dynamics simulation[J].Materials Chemistry and Physics, 2020, 240:122153.