草莓富含维生素C、叶酸和酚类成分[1],与其他水果相比,草莓以其独特的风味和营养价值而备受推崇。但由于其质地光滑、软化率高和易受真菌侵袭的性质,草莓在贮存过程中极易腐烂[2]。因此,寻求合适的方法来延长其保质期尤为重要。冷冻是一种有效保存草莓的方式,由于液态水转化为冰,大大降低了微生物和酶的活性[3]。DELGADO等[4]通过比较不同冷冻速度对新鲜草莓组织的影响,证实了快速冷冻可以最大限度地减少冰晶生长带来的不利影响。保持草莓果实硬度的一个关键因素是钙离子在邻近聚脲酸酯链羧基之间作为交联的螯合作用,在多数情况下,CaCl2冷冻处理能稳定草莓组织的结构[5]。GALETTO等[6]研究了草莓在CaCl2溶液中的浸渍冻结(immersion freezing, IF),分析了汁液损失、果胶含量、果胶酯化程度、钙含量、结合钙与总钙的比例等参数,与慢速冷冻(slow freezing, SF)相比,草莓品质显著提升。另一种将浸渍冻结和流态化速冻结合在一起的方法是冷冻液流态化速冻(hydrofluidization quick-freezing, HF),该方法由Fikiin在1992年提出并获得专利[7]。它是基于将一组小颗粒食品浸入一个充满适当液体的容器,通过位于底部的一系列孔泵入,由于液体介质的密集流动,食品在室内呈现流化现象。因此,流体下方冲击射流的产生确保了极高的传热系数[8]。
HF系统的一些操作变量对制冷剂和食物样品之间的传热传质现象是近几十年来许多专家学者研究的主题[9-12]。PERALTA等[13]使用计算流体力学(computational fluid dynamics, CFD)对HF系统进行了数值分析并提出了一个经过实验验证的数学模型,用于模拟具有规则形状的食品样品在速冻过程的传热传质现象。PALACZ等[9]在装有透明HF室的实验台上进行了研究,采用粒子图像测速仪对冷却介质的速度场进行了测量,为HF的流动过程选择了合适的湍流模型。PALACZ等[14]研究了以乙醇水溶液为介质的HF系统,对几种不同大小的食品样品在HF过程的流动传热进行分析,以评估速冻所需要的时间。STEBEL等[11]研究了球形马铃薯样品在乙醇、甘油、葡萄糖多种组合方式的水溶液中的冷冻过程,利用数值模拟对速冻过程的传热传质进行了分析,并量化了传热系数、溶液温度和浓度对该过程的影响。
然而,与HF系统几何布置相关的一些重要参数对传热传质现象的影响研究较少,如产生射流的孔径和食物样品高度。本研究通过CFD Fluent对CaCl2溶液中草莓流态化速冻过程进行数值模拟,分析几何布置对冻结过程传热传质的影响。此外,建立了HF过程的实验装置,通过实验与数值模拟结果进行比较,对数值方法的准确性进行了验证。
1 材料与方法
1.1 材料属性
以质量浓度300 g/L浓度的CaCl2溶液(CaCl2 solution, CCS)作为冷冻介质,温度为-20 ℃,热物性参数如表1所示。
表1 CaCl2溶液物性参数
Table 1 physical parameters of CaCl2 solution

临界温度/℃密度/[kg·(m3)-1]比热容/[J·(kg·K)-1]导热系数/[W·(m·K)-1]动力黏度/(Pa·s)-551 2862 6800.5021.44×10-2
草莓鲜果选自中国东北地区生产的丹东草莓,草莓由多种成分构成[15],各成分质量分数如表2所示,其中,水分是草莓最主要的组成成分。通过实验得到了草莓冻结前后的热物性参数,如表3所示。密度由质量和体积测量评估,草莓质量由梅特勒托利多电子天平XPR404S/AC测得,比热容由Q1000热流型差式量热扫描仪测得,热导率由Hot Disk热常数分析仪获取。
表2草莓鲜果的化学成分
Table 2 Chemical constituents of fresh strawberry fruit
成分水固体基质蛋白质碳水化合物矿物质含量(质量分数)/%91.368.640.747.000.24
表3 草莓冻结前后的热物性参数
Table 3 Thermophysical parameters of strawberries before and after freezing

状态密度/[kg·(m3)-1]比热容/[J·(kg·K)-1]导热系数/[W·(m·K)-1]冻结前1 0793 5400.52冻结后8911 9261.64
由图1所示,CaCl2溶液中草莓流态化速冻过程中有着复杂的热量传递与溶质传递现象。HF过程中,热量通过直接接触从草莓传递到周围的低温液体中。在HF装置中通过液体介质对小型食品进行速冻时,除了对流,影响食品热量传递的第二机制是食品内部的热传导,这两种机制的结合决定了球状食品样品中心附近的温度变化[12]。由于冷冻过程产生的浓度梯度,草莓中的水分由内向外迁移,同时,草莓和溶液之间也在进行着溶质的传递,这种转移通过扩散过程发生。在数值分析过程,草莓中的固体部分可看作为隔离溶液的多孔介质,溶液看作为水和溶质的二元系统,其中,水的相变控制着草莓热物性参数的变化[16]。

图1 HF过程
Fig.1 HF process
在草莓的冻结过程中,总含水量包含可冻结水、不可冻结水和冰[17],如公式(1)所示:
xβ=xfβ+xuβ+xσ
(1)
其中,不可冻结水由公式(2)计算:
xuβ=0.25xα=0.25×(1-xβ)=0.25×(1-90.7%)=0.023
(2)
水的潜热(ΔH0)随温度变化表达如公式(3)所示:
ΔH0=334.2+2.12T+0.004 2T2
(3)
式中:xα为固体基质含量,xβ为总含水量,xfβ为可冻结水含量,xuβ为不可冻结水含量,xσ为冰含量。
依据CORNEJO等[18]对食品在冷冻范围内热物性特性的分析,草莓的表观比热容(CPeff)可以用公式(4)估算:
(4)
草莓的导热系数(keff)计算如公式(5)所示:
(5)
式中:CPf和kf分别为草莓完全冻结后的比热容和导热系数,ku为常温下草莓的导热系数,efβ为可冻结水的初始质量分数(%),T0是纯水的冰点(K),Tf为草莓的冰点(K)。
流态化速冻过程在液体环境中进行,水分流失对草莓质量影响较小。由于液态水是草莓的主要成分,因此,依据菲克扩散定律,在数值模型中制定了液态水的运输方程。液态水的质量守恒方程如公式(6)所示:
(6)
同理,用公式(7)来确定溶质的扩散:
(7)
式中:ρl为草莓中的液相密度(kg/m3),xwat 为液态水的质量分数(%),t为时间(s),Deff为有效质量扩散系数,xice(T)为冰的质量分数(%),与温度相关,xCCS是溶液中CaCl2的质量分数(%)。
为保持数值计算的稳定性,使用准焓法求解传热过程,基于傅里叶定律,能量守恒方程如公式(8)所示:
(8)
式中:ρ是草莓的密度(kg/m3),h是草莓的比焓(J/kg)。
1.2 物理模型
HF室依据传统风冷式流态化速冻间设计,主体部分为一个圆柱形的储液罐,如图2所示,由不锈钢材料制成,顶部开口,罐体高150 mm,直径130 mm。草莓的速冻过程在HF室内进行,草莓样品通过可伸缩的细棒安装在固定位置。低温CaCl2溶液通过位于罐底的有孔板流入罐内,该板由不锈钢制成,可拆卸,以进行不同流入配置的测试。孔板下方放置一个导流板,以稳定由流入管流体冲击而产生的压力和整个板下的液体流量。
HF系统的计算域由孔板截面至顶部开口处构成。草莓样品放置距孔板不同高度H处,孔板设有不同孔径d,图3显示了计算域结构参数。为简化计算模型,以孔板孔口为入口,HF室顶部为出口,采用模型的1/4作为计算域进行数值模拟。
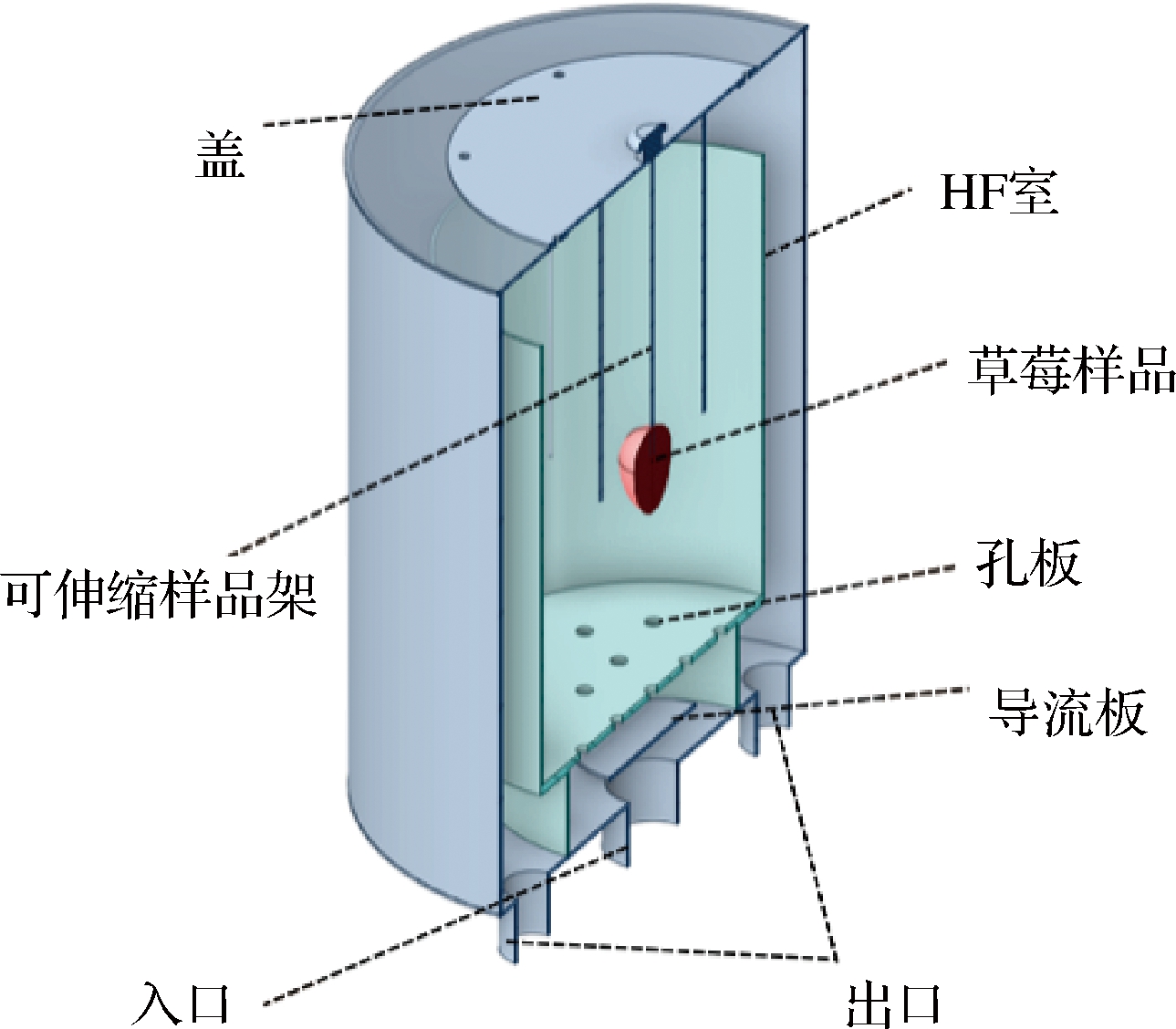
图2 HF室剖面示意图
Fig.2 Schematic diagram of HF chamber section

图3 HF系统计算域
Fig.3 HF system computing domain
采用ANSYS Fluent对所有研究条件下的几何模型进行了相同标准的网格划分,如图4所示,为了在相同的计算要求下提高模拟精度,网格密度在靠近孔口和草莓表面的区域较高,而在其他区域较低。全局网格生成采用非结构化网格,在固液交界面添加了边界层。在网格划分过程中,对所有模型分别划分了多组不同数量的网格单元,经网格无关性检验,网格单元总数在150万左右可满足计算精度要求。

图4 计算域网格划分
Fig.4 Computational domain gridding
1.3 边界和初始条件
针对HF过程,对计算模型进行多种边界条件设定,根据对称边界、壁面边界及进出口边界条件来模拟CaCl2溶液在HF室内的流动过程。边界条件的详细描述如下:
(1)入口设置为速度入口,出口为压力出口,根据环境压力,将出口赋予105 Pa的静压值。
(2)采用两个对称平面将计算域简化为四分之一,该区域为流体的自由表面,定义为绝热滑移壁面。
(3)草莓表面定义为无滑移壁面,按第三类边界条件定义,利用系统耦合来模拟流动传热过程。
(4)其他所有壁面定义为绝热无滑移壁面。
在本研究中,CaCl2溶液入口温度设置为-20 ℃,入口速度为0.5 m/s,草莓的初始温度为20 ℃。设置不同的草莓高度H、孔板孔径d,详细研究条件(Case)如表4所示。
表4数值模拟研究条件
Table 4 Research conditions of numerical simulation
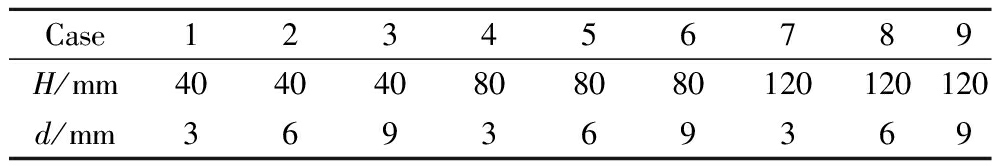
Case123456789H/mm404040808080120120120d/mm369369369
1.4 计算模型
采用ANSYS Fluent软件对草莓的速冻过程进行数值求解。利用瞬态下的不可压缩流动来描述CaCl2溶液在HF速冻间内的流动过程,应用标准k-ω湍流模型对流动过程进行建模,该模型比其他精度更高,在模拟流态化系统的流动特性方面效果最佳[19];利用基于焓的能量方程求解草莓内部的传热过程[20];草莓设置为多孔介质模型,应用凝固与融化模型来描述草莓中液态水的结晶过程[11]。
数值求解器基于解的隐式格式,为保证计算精度,采用二阶迎风格式对所有方程进行时间与空间的离散。瞬态冻结过程由入口开始进行标准初始化,每次模拟的时间步长均设为0.01 s。
2 结果与分析
2.1 实验验证
对CaCl2溶液中草莓的流态化速冻过程进行了实验测试,实验流程如5所示。实验台由两个主要部分组成,即低温恒温槽和HF室。CaCl2溶液在低温恒温槽内保持-20 ℃的恒温状态,由内部泵将溶液送入HF室。通过t型热电偶测量管路内部及草莓的温度,另外管路中还接有质量流量计和压力传感器。
以Case1为例,速冻过程草莓中心温度分布实验与模拟对比如图6所示。在达到初始冰点之前的第一阶段过程中,草莓中心温度的模拟值略高于实验值,在该过程的后续阶段中,随机出现了微小的差异,造成误差的原因可能与样品形状和热电偶的定位精度有关。由实验数据可以看到,草莓中心温度下降到初始冰点以下后,结冰相变瞬间发生,表现为温度的快速增长。由于数值模型的局限性,该过程在模拟条件下难以实现。考虑到实验的相关误差和模型设置使用的假设,实验与模拟之间的差异并不显著。从工业HF方法应用的实际角度来看,该数学模型具有较高的预测水平。

图5 HF实验测试
Fig.5 HF experimental test
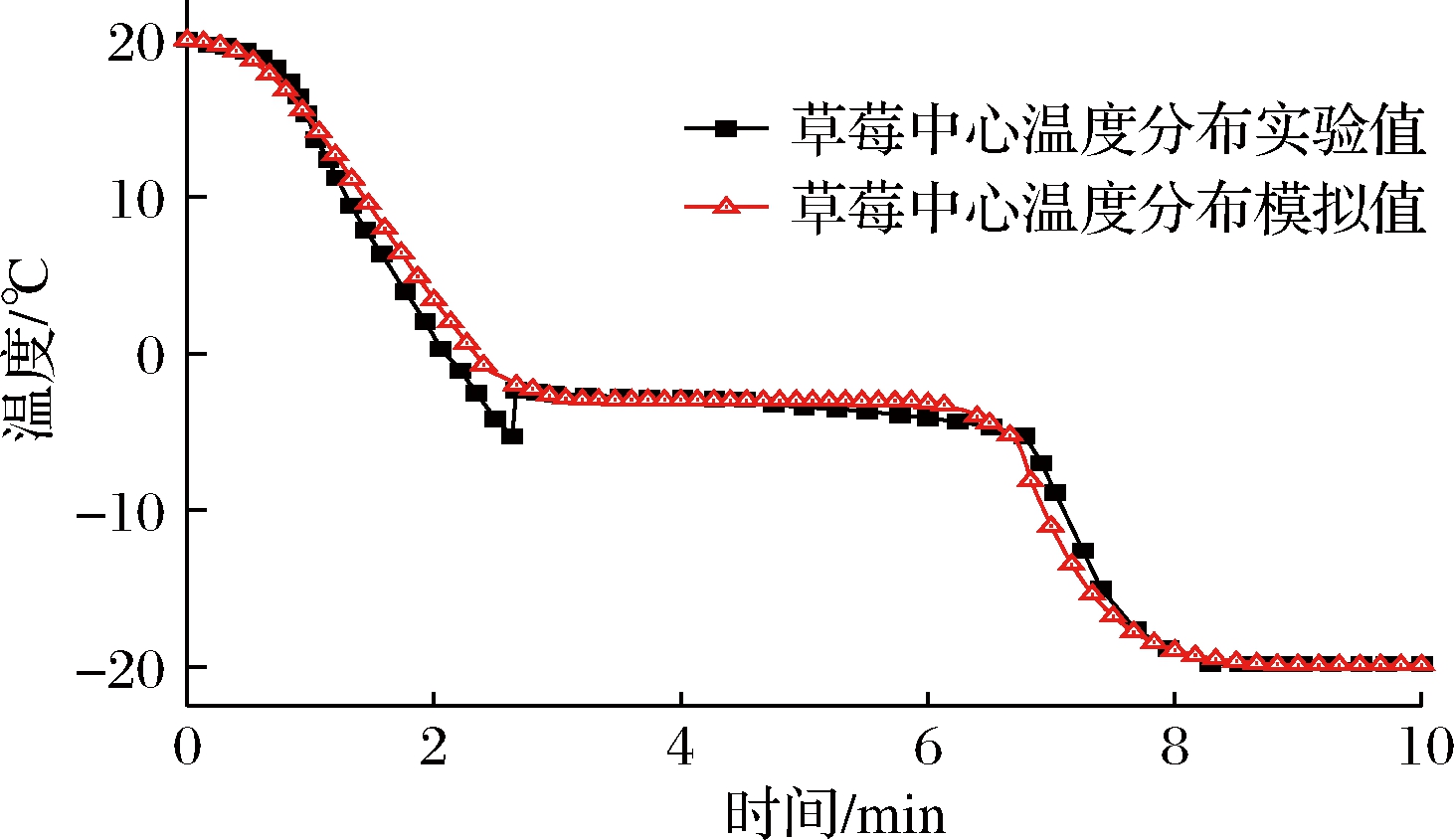
图6 草莓中心温度分布
Fig.6 Temperature distribution in the center of strawberry
2.2 HF过程传热传质分析
在HF过程中,热质传递机制影响着温度变化、溶质吸收以及草莓中水分的结晶。图7以Case1为例,比较了HF过程中草莓样品的温度分布与溶质吸收。如图7所示,在草莓的HF过程中,共经历3个阶段。1~2为HF过程开始到草莓中心温度达到结晶临界区的冷却阶段;2~3为草莓冰晶形成临界区,此时,草莓中心温度接近等温,大部分传热与潜热散失有关;3~4为从离开冰晶形成临界区到草莓中心温度接近溶液温度的冷冻阶段。
草莓HF过程的第一阶段开始时,热量从草莓传递到低温溶液,导致草莓表层迅速冻结,形成一层冰晶。由图7中溶质传递曲线可以看出,冰晶层的形成抑制了溶质的传递。在HF的初始阶段,溶质的吸收最强烈,随着速冻过程的发展,溶质的吸收逐渐减缓。根据STEBEL等[11]的描述,在HF过程中,只有靠近食品表面的区域即表面的30%才能吸收溶质,浓度接近溶液浓度。随着速冻过程进行,冰晶向食品中心传播,最终的含冰量大约为70%。草莓中心温度在2~3阶段变化最慢,几乎保持不变的过程接近3 min,持续在水结晶的临界区约4 min。因此,在HF过程中,缩短草莓度过冰晶形成临界区所需要的时间是强化速冻的关键。
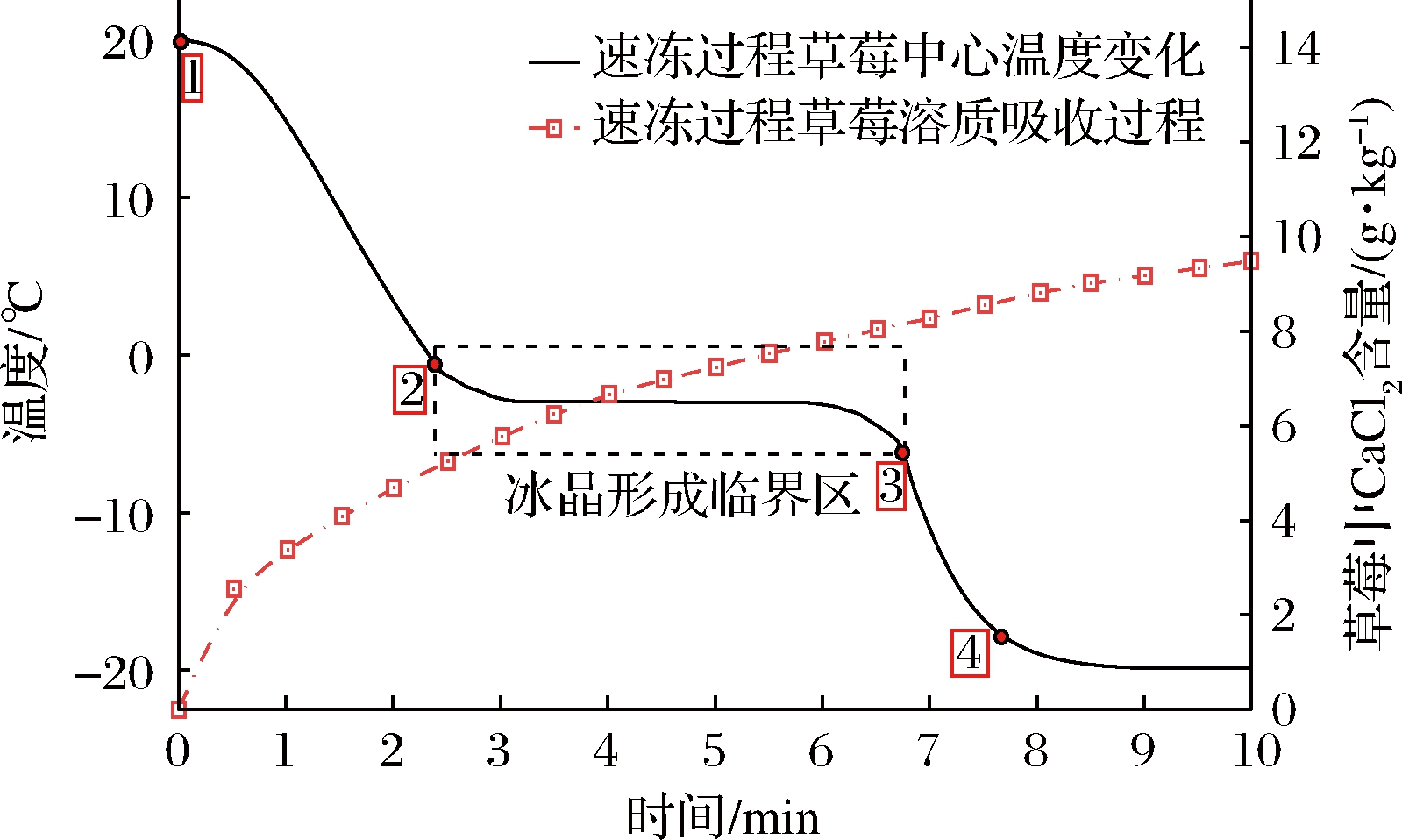
图7 HF过程中草莓样品的温度分布与溶质吸收
Fig.7 Temperature distribution and solute absorption of strawberry sample during HF
2.3 草莓高度H与孔板孔径d对HF过程的影响
草莓HF过程中所有研究条件下的速度云图与流线如图8所示。从速度云图中可以看出,孔径的增大会导致草莓周围局部流量的增加,在射流形成的区域和草莓底部区域最为明显。从流线能够看出,更大的孔径能够产生更剧烈扰动。由于孔径增大导致流速衰减减缓,在草莓周围形成较高的局部速度。在HF室中,流体流速自下而上逐渐衰减,射流充分发展,在出口附近形成更均匀流场。当草莓高度逐渐增加时,射流冲击对HF室内流体扰动的影响逐渐减弱,草莓周围速度梯度明显减小。

图8 所选工况的流线和速度云图
Fig.8 Streamlines and velocity contours for the selected conditions
依据所建立的传热传质模型,从冻结时间和冻结过程中溶质吸收两个方面进行了研究。在草莓样品的冷却和冻结过程中,最高温度位于几何中心。因此,草莓中心温度是确定冷冻过程时间的参考值。在研究中,以草莓中心温度降至-18 ℃作为速冻完成的标准。在传质分析中,以草莓中溶质相对于新鲜草莓的平均质量浓度为参考标准,所有数值分析结果如表5所示。数据表明,草莓高度H越小,孔板孔径d越大,HF过程传热效果越好,草莓溶质吸收越少。
表5 数值分析结果
Table 5 Results of numerical analysis

Case123456789速冻完成时间/min7.756.846.758.757.627.338.898.087.49含量/(g·kg-1)8.617.387.1610.138.958.029.819.528.89
比较了不同孔径d及不同高度H对HF过程传热传质的影响,在研究范围内,Case 1、5、9具有相同大小的H/d(13.33),其余研究条件按照H/d由小到大的顺序排列为Case 3、2、6、8、4、7(4.44、6.66、8.88、20、26.66、40)。图9、图10显示了H/d对草莓速冻过程中心温度变化与溶质吸收的影响,可以看出,H/d对草莓中心温度的影响主要集中在冰晶生成临界区,而在冷却阶段和冷冻阶段影响并不显著。由图9可以看出,当H/d相同时,草莓速冻过程中的降温速率基本保持一致,这是由于在相同的H/d下,尽管射流速度梯度发生变化,但草莓样品周围形成的湍流强度差异并不明显。图10的结果表明,当H/d逐渐增大时,草莓周围产生的搅拌射流逐渐减弱,导致传热效果弱化,这种趋势在H/d较高或较低时并不明显。对比Case 2、Case 3以及Case 4、Case 7可以看出,不同H/d的条件下,草莓中心降温速率基本相同。结果表明,当H/d小于8.88的某些高度,草莓样品位于最低处时,样品周围可产生最大限度的射流冲击,此时,质量流量的增加并没有显著影响样品周围流体的速度,样品附近的流场差异相对较小,孔径的增加并未提升传热效果。当H/d大于26.66的某些高度,射流得到了充分发展,草莓位置的改变没有影响传热的变化。
图9、图10中与溶质吸收有关的结果表明,几何参数的改变对HF过程中溶质吸收的影响并不明显。这些变化与总速冻时间的变化呈正相关,而与溶质吸收条件的关系并不显著,这是因为在所有研究条件下,草莓样品表面的冷冻速度均很快。由图10的结果可以看出,随着H/d的减小,草莓中溶质的吸收也有所减少,但每条曲线的斜率基本相同,原因主要来自于草莓接触溶液的时间缩短,草莓中溶质的浓度随温度的降低而降低。总而言之,草莓降温速率的提高可以有效减少HF过程中不必要的溶质吸收。

图9 H/d相同时草莓样品的温度分布与溶质吸收
Fig.9 Temperature distribution and solute absorption of strawberry samples with the same H/d
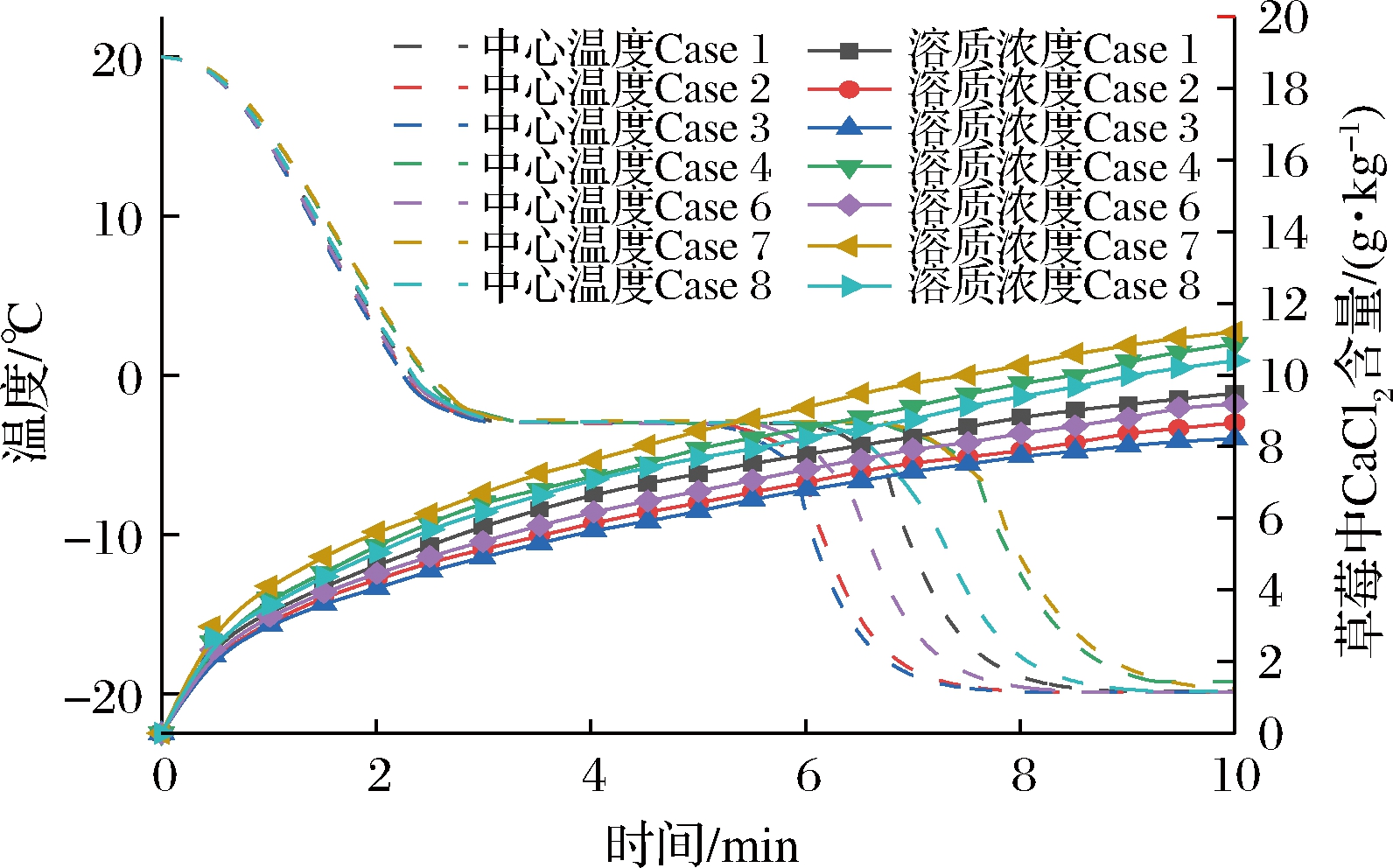
图10 H/d不同时草莓样品的温度分布与溶质吸收
Fig.10 Temperature distribution and solute absorption of strawberry samples with the different H/d
3 结论
依据HF方法对草莓在CaCl2溶液中流态化速冻过程进行了数值研究,基于傅里叶定律和菲克定律建立了表征草莓内部传热与溶质扩散的数值模型,并对模型进行实验验证。针对草莓几何中心温度、冻结时间和草莓中平均CaCl2浓度分布,研究了草莓几何中心距孔板的高度H和圆形阵列中孔口直径d之比(H/d)对静态草莓HF速冻过程的影响,结论如下:
(1)总体而言,H/d越小,草莓的冻结速率越快。当H/d小于8.88或大于26.66时,改变几何参数对HF过程的影响并不明显。因此,应根据HF室的尺寸合理设置几何参数来实现传热效果的最大化。
(2)几何参数的改变对草莓溶质吸收的影响并不显著,草莓溶质吸收的快慢主要取决于降温速率,冻结时间越短,草莓中CaCl2浓度越低。
(3)对于工业化的HF系统,加工产品会在HF室内移动,H/d会不断发生变化。一方面,靠近HF室顶部的产品流体速度值明显低于靠近孔口的产品。另一方面,增大孔径来获取更高的载冷剂流量会降低HF效率。因此,应对更多的操作条件进行研究,高效的基于CFD的HF过程数值模拟非常必要。
[1] GIAMPIERI F, TULIPANI S, ALVAREZ-SUAREZ J M, et al. The strawberry: Composition, nutritional quality, and impact on human health[J]. Nutrition, 2012, 28(1):9-19.
[2] 宁静红, 赵延峰, 孙朝阳, 等. 干冰喷射进出口位置对草莓速冻过程的影响[J]. 食品与发酵工业, 2021, 47(24):187-192.
NING J H, ZHAO Y F, SUN Z Y, et al. Influence of inlet and outlet position of dry ice spray on strawberry quick-freezing process[J]. Food and Fermentation Industries, 2021, 47(24):187-192.
[3] 胡中海, 孙谦, 龙勇, 等. 水果速冻保鲜技术研究进展[J]. 食品与发酵工业, 2015, 41(2):242-247.
HU Z H, SUN Q, LONG Y, et al. Advances in research on technology of quick-freezing fruits[J]. Food and Fermentation Industries, 2015, 41(2):242-247.
[4] DELGADO A E, RUBIOLO A C. Microstructural changes in strawberry after freezing and thawing processes[J]. LWT-Food Science and Technology, 2005, 38(2):135-142.
[5] SUUTARINEN J, HEISKA K, MOSS P, et al. The effects of calcium chloride and sucrose prefreezing treatments on the structure of strawberry tissues[J]. LWT-Food Science and Technology, 2000, 33(2):89-102.
[6] GALETTO C D, VERDINI R A, ZORRILLA S E, et al. Freezing of strawberries by immersion in CaCl2 solutions[J]. Food Chemistry, 2010, 123(2):243-248.
[7] FIKIIN A G. New method and fluidized water system for intensive chilling and freezing of fish[J]. Food Control, 1992, 3(3):153-160.
[8] FIKIIN K. Frozen Food Science and Technology[M]. Oxford: Blackwell Publishing Ltd., 2009:101-123.
[9] PALACZ M, ADAMCZYK W, PIECHNIK E, et al. Experimental investigation of the fluid flow inside a hydrofluidisation freezing chamber[J]. International Journal of Refrigeration, 2019, 107:52-62.
[10] STEBEL M, SMOLKA J, PALACZ M, et al. Numerical investigation of the fluid flow distribution for the hydrofluidisation food freezing method[J]. International Journal of Thermal Sciences, 2020, 151:106284.
[11] STEBEL M, SMOLKA J, PALACZ M, et al. Numerical modelling of conjugate heat and mass transfer during hydrofluidisation food freezing in different water solutions[J]. Innovative Food Science &Emerging Technologies, 2022, 75:102898.
[12] STEBEL M, SMOLKA J, PALACZ M, et al. Numerical modelling of the food freezing process in a quasi-hydrofluidisation system[J]. Innovative Food Science &Emerging Technologies, 2021, 74:102834.
[13] PERALTA J M, RUBIOLO A C, ZORRILLA S E. Mathematical modeling of the heat and mass transfer in a stationary potato sphere impinged by a single round liquid jet in a hydrofluidization system[J]. Journal of Food Engineering, 2012, 109(3):501-512.
[14] PALACZ M, PIECHNIK E, HALSKI M, et al. Experimental analysis of freezing process of stationary food samples inside a hydrofluidisation freezing chamber[J]. International Journal of Refrigeration, 2021, 131:68-77.
[15] SCHEERLINCK N, JANCS K P, VERBOVEN P, et al. Influence of shape on the fast freezing of small fruits by means of hydrofluidisation. Budapest: Proceedings of AgEng,2002.
K P, VERBOVEN P, et al. Influence of shape on the fast freezing of small fruits by means of hydrofluidisation. Budapest: Proceedings of AgEng,2002.
[16] 杨燕, 袁训锋, 乔希民, 等. 食品速冻保鲜过程冰晶生长的相场模拟[J]. 食品与机械, 2018, 34(12):108-114.
YANG Y, YUAN X F, QIAO X M, et al. Phase-field simulation of ice crystal growth on food quick-freezing preservation process[J]. Food &Machinery, 2018, 34(12):108-114.
[17] 邵双全,高玉平,田绅,等.枸杞鲜果速冻过程的数值研究[C].第七届中国冷冻冷藏新技术新设备研讨会论文集,2015.
SHAO S Q,GAO Y P,TIAN S, et al.Numerical investigantion on quick-freezing process of wolfberry fresh fruit[C].China Academic Journal Electronic Publishing House,2015.
[18] CORNEJO I, CORNEJO G, RAM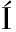 REZ C, et al. Inverse method for the simultaneous estimation of the thermophysical properties of foods at freezing temperatures[J]. Journal of Food Engineering, 2016, 191:37-47.
REZ C, et al. Inverse method for the simultaneous estimation of the thermophysical properties of foods at freezing temperatures[J]. Journal of Food Engineering, 2016, 191:37-47.
[19] BELIS E E, ZORRILLA S E, PERALTA J M. Effect of the number of orifices and operative variables on the heat and mass transfer in a hydrofluidization system with static spheres[J]. Journal of Food Engineering, 2015, 153:96-107.
[20] 唐君言, 邵双全, 徐洪波, 等. 食品速冻方法与模拟技术研究进展[J]. 制冷学报, 2018, 39(6):1-9.
TANG J Y, SHAO S Q, XU H B, et al. Progress in research on the food quick-freezing method and simulation technology[J]. Journal of Refrigeration, 2018, 39(6):1-9.