草酸是一种广泛分布于植物、动物及真菌中的二元羧酸[1-2],参与生物体内的代谢过程和能量贮存,具有重要的生理作用[3]。但过高的草酸,会破坏人体的酸碱度,甚至导致人体结石症,在原发性高草酸尿症的诊断和治疗监测中需要对草酸根进行检测[4-8];另外蔬菜、水果、饮料中的草酸含量过高也会降低其营养品质[9-10];因此快速识别检测水溶液中草酸根离子的含量在食品化学和临床分析等各个方面都有着至关重要的作用。
目前,有关![]() 的测定方法主要有高效液相色谱法、离子色谱法[11-14]、荧光法[15-17]、滴定法[18]等。
的测定方法主要有高效液相色谱法、离子色谱法[11-14]、荧光法[15-17]、滴定法[18]等。
这些方法虽然可实现水相中![]() 的测定,但不能实现多离子共存时对
的测定,但不能实现多离子共存时对![]() 的选择性识别,而目前有关阴离子识别与传感的报道却多在有机非质子溶液中进行[19-21],这就极大地限制了该研究的应用范围。因而,设计一个可在水相中进行,且能同时达到对
的选择性识别,而目前有关阴离子识别与传感的报道却多在有机非质子溶液中进行[19-21],这就极大地限制了该研究的应用范围。因而,设计一个可在水相中进行,且能同时达到对![]() 离子选择性裸眼识别及准确测定的新体系,将在临床医学、环境监测及食品化学方面有很好的应用价值。因此,本研究在前期工作的基础上[22-25],利用配位转换原理,以Fe3+与铬菁R为显色体系,通过条件优化,建立了一种选择性更好,效果更佳的识别检测水溶液中
离子选择性裸眼识别及准确测定的新体系,将在临床医学、环境监测及食品化学方面有很好的应用价值。因此,本研究在前期工作的基础上[22-25],利用配位转换原理,以Fe3+与铬菁R为显色体系,通过条件优化,建立了一种选择性更好,效果更佳的识别检测水溶液中![]() 离子的新方法,该体系可作为检测
离子的新方法,该体系可作为检测![]() 的化学敏感器。
的化学敏感器。
配制好5×10-4 mol/L Fe3+标准液、5×10-4 mol/L铬菁R标准液、0.15 mol/L表面活性剂十二烷基三甲基溴化铵溶液, 0.25 mol/L HAc, 0.25 mol/L NaAc溶液,0.02 mol/L各阴离子钠盐溶液,实验所用硫酸铁铵、铬菁R及各阴离子钠盐均为分析纯;溶剂用水均为高纯水。
材料:菠菜和韭菜均来自于蔬菜超市。
日本岛津UV-2600/2700型紫外-可见吸收光谱仪、1 cm石英比色皿、上海雷磁仪器厂;PHS-25型酸度计,赛多丽斯科学仪器(北京)有限公司;BSA124S型电子分析天平,德国赛多利斯公司。
分别在2支比色管中依次加入一定量的5×10-4 mol/L的Fe3+、铬菁R标准液、0.15 mol/L表面活性剂十二烷基三甲基溴化铵溶液、pH为4.5的HAc-NaAc缓冲溶液,其中1支再加入适量的![]() 另1支不加,最后定容,以蒸馏水为参比,在647 nm处测吸光度,加C2O42-的吸光度记为A,不加
另1支不加,最后定容,以蒸馏水为参比,在647 nm处测吸光度,加C2O42-的吸光度记为A,不加![]() 的吸光度记为A0,计算吸光度降低值:ΔA= A0-A, 测定系列浓度
的吸光度记为A0,计算吸光度降低值:ΔA= A0-A, 测定系列浓度![]() 的ΔA,并以ΔA对
的ΔA,并以ΔA对![]() 的浓度作图,通过得到的标准曲线确定样品中
的浓度作图,通过得到的标准曲线确定样品中![]() 含量。
含量。
将新鲜的菠菜样品洗干净并且晾干无水分时,称取剪碎混匀的样品100 g,加入水75 mL,放入榨汁机中成匀浆状,用水25 mL冲洗,将冲洗液加入匀浆液中混匀备用。称取匀浆液2.00 g(换算为1.00 g新鲜蔬菜样品)于小烧杯中,加水至30 mL左右,沸水浴提取20 min,冷却,定容于50 mL容量瓶中,以10 000 r/min转速离心10 min,过滤,用滤液进行实验测定。韭菜按相同的方法进行预处理[26]。
于一系列已编号的10 mL比色管中按1.3实验方法各加入1.00 mL 5×10-4 mol/L的Fe3+标准液、1.00 mL 5×10-4 mol/L的铬菁R标准液、1.00 mL 0.15 mol/L的表面活性剂十二烷基三甲基溴化铵溶液、3.00 mL pH为4.5的HAc-NaAc缓冲溶液,再分别加入1.00 mL浓度均为0.02 mol/L的![]() 水溶液,定容,摇匀,静置2 h,可以明显看到显色体系在不同阴离子存在时的颜色变化,如图1所示。
水溶液,定容,摇匀,静置2 h,可以明显看到显色体系在不同阴离子存在时的颜色变化,如图1所示。
按上述同样方法配制一系列显色体系及其与不同阴离子作用的水溶液,室温下静置2 h,以蒸馏水为参比,在400~750 nm内扫描显色体系与不同阴离子作用时吸收光谱的变化,结果见图2。

a-显色液;b-CH3COONa;c-NaNO2;d-NaCl;e-NaNO3;f-Na2CO3;g-NaHCO3;h-Na2C2O4;i-Na2SO3;j-K2SO4;k-KI;l-KBr; m-KClO3;n-KHSO4
图1 显色体系与不同阴离子的显色效果
Fig.1 Color changes for the chromogenic system in water upon the addition various anions
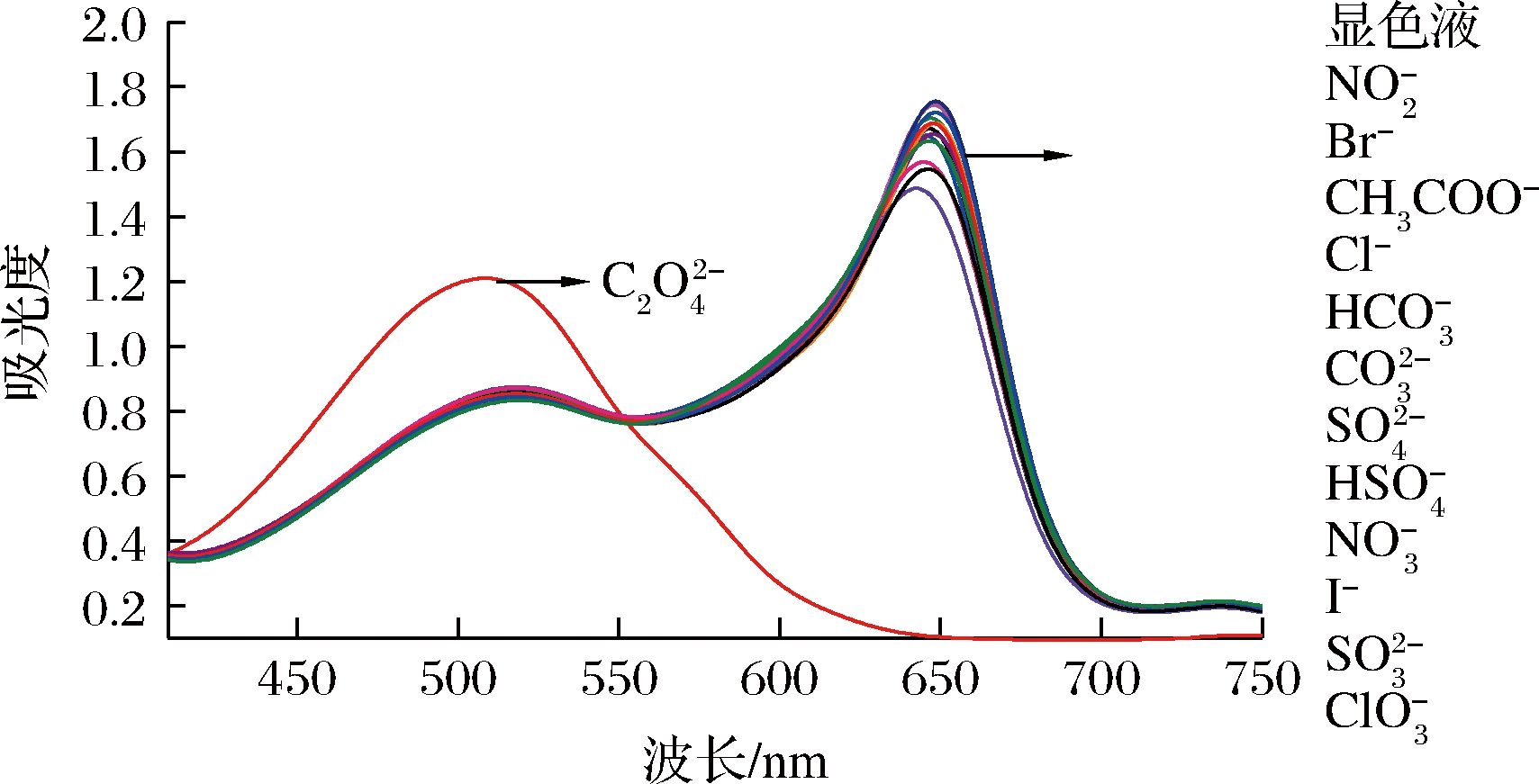
图2 显色体系与不同阴离子反应的吸收光谱图
Fig.2 UV-Vis absorption of the chromogenic system in the presence of various anions
从图1可以清楚地看到,当pH=4.5,且有表面活性剂存在的条件下,![]() 可夺取Fe(Ⅲ)-铬菁R络合物中的Fe3+形成稳定的配离子[Fe(C2O4)3]3-,溶液颜色由蓝色变为红色,使得Fe(Ⅲ)-铬菁R显色体系对
可夺取Fe(Ⅲ)-铬菁R络合物中的Fe3+形成稳定的配离子[Fe(C2O4)3]3-,溶液颜色由蓝色变为红色,使得Fe(Ⅲ)-铬菁R显色体系对![]() 表现出明显的选择性识别,而等量其他常见阴离子的加入并未引起显色液颜色变化。从图2显色体系与不同阴离子反应的吸收光谱图也可以看出,当向显色体系中加入
表现出明显的选择性识别,而等量其他常见阴离子的加入并未引起显色液颜色变化。从图2显色体系与不同阴离子反应的吸收光谱图也可以看出,当向显色体系中加入![]() 时,因为发生配位转换,
时,因为发生配位转换,![]() 与Fe3+形成更稳定配合物而释放出铬菁R,使得原配合物在647 nm处的最大吸收峰显著降低,在508 nm处铬菁R自身产生的吸收则明显加强,而等量的其他阴离子则没有使显色体系产生明显的光谱变化,所以说Fe(Ⅲ)-铬菁R显色体系可在水溶液中对
与Fe3+形成更稳定配合物而释放出铬菁R,使得原配合物在647 nm处的最大吸收峰显著降低,在508 nm处铬菁R自身产生的吸收则明显加强,而等量的其他阴离子则没有使显色体系产生明显的光谱变化,所以说Fe(Ⅲ)-铬菁R显色体系可在水溶液中对![]() 实现选择性裸眼识别。
实现选择性裸眼识别。
2.2.1 酸度对显色效果的影响
在系列已编号的25 mL比色管中按1.3中的实验方法保持其他条件不变,利用0.1 mol/L的HCl溶液、0.1 mol/L的NaOH溶液及HAc-NaAc缓冲溶液依次调节体系的pH分别为3.5、4.0、4.5、5.0、5.5、5.8,在647 nm处测吸光度,计算不同pH下的吸光度降低值ΔA,测试酸度对显色效果的影响,结果见图3。在溶液pH为4.5时,吸光度差值ΔA最大,反应最灵敏,所以实验选取pH为4.5的HAc-NaAc缓冲溶液。
2.2.2 缓冲溶液用量对显色效果的影响
保证其他条件及pH为上述所确定的最佳值4.5不变,改变缓冲溶液用量分别为1.00、1.50、2.00、2.50、3.00、3.50、4.00 mL,按1.3实验方法测定试液吸光度降低值,测试缓冲溶液用量对显色效果的影响,结果见图4,当pH=4.5的HAc-NaAc缓冲溶液用量为3.00 mL时,ΔA最大,所以实验选取缓冲溶液的最佳用量为3.00 mL。

图3 酸度对显色效果的影响
Fig.3 The effects of acidity on the chromogenic reaction
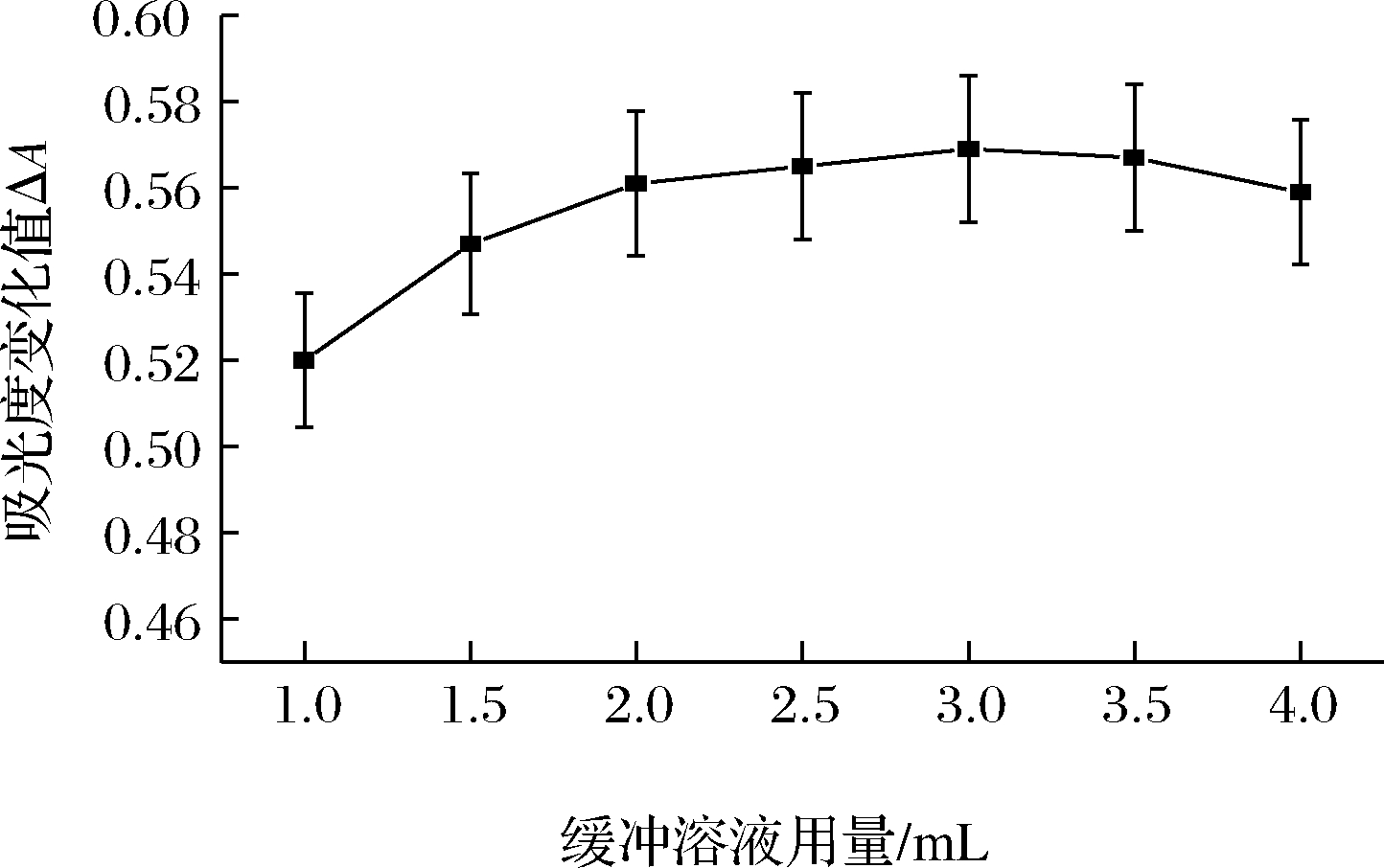
图4 缓冲溶液用量对显色效果的影响
Fig.4 The effects of the buffer solution addition on the chromogenic reaction
2.2.3 十二烷基三甲基溴化铵表面活性剂用量对显色效果的影响
由于离子缔合物具有疏水性,为使其稳定地存在于水溶液中,通常加入表面活性剂,固定其他条件为上述讨论的最佳量不变,改变0.15 mol/L的表面活性剂加入量分别为0、0.50、1.00、1.50、2.00、2.50、3.00 mL,测试十二烷基三甲基溴化铵的用量对显色效果的影响,结果见图5。当0.15 mol/L十二烷基三甲基溴化铵表面活性剂加入量为1.00 mL时,显色液和空白液之间的吸光度差值ΔA最大,反应最为灵敏,所以表面活性剂的最佳用量确定为1.00 mL。
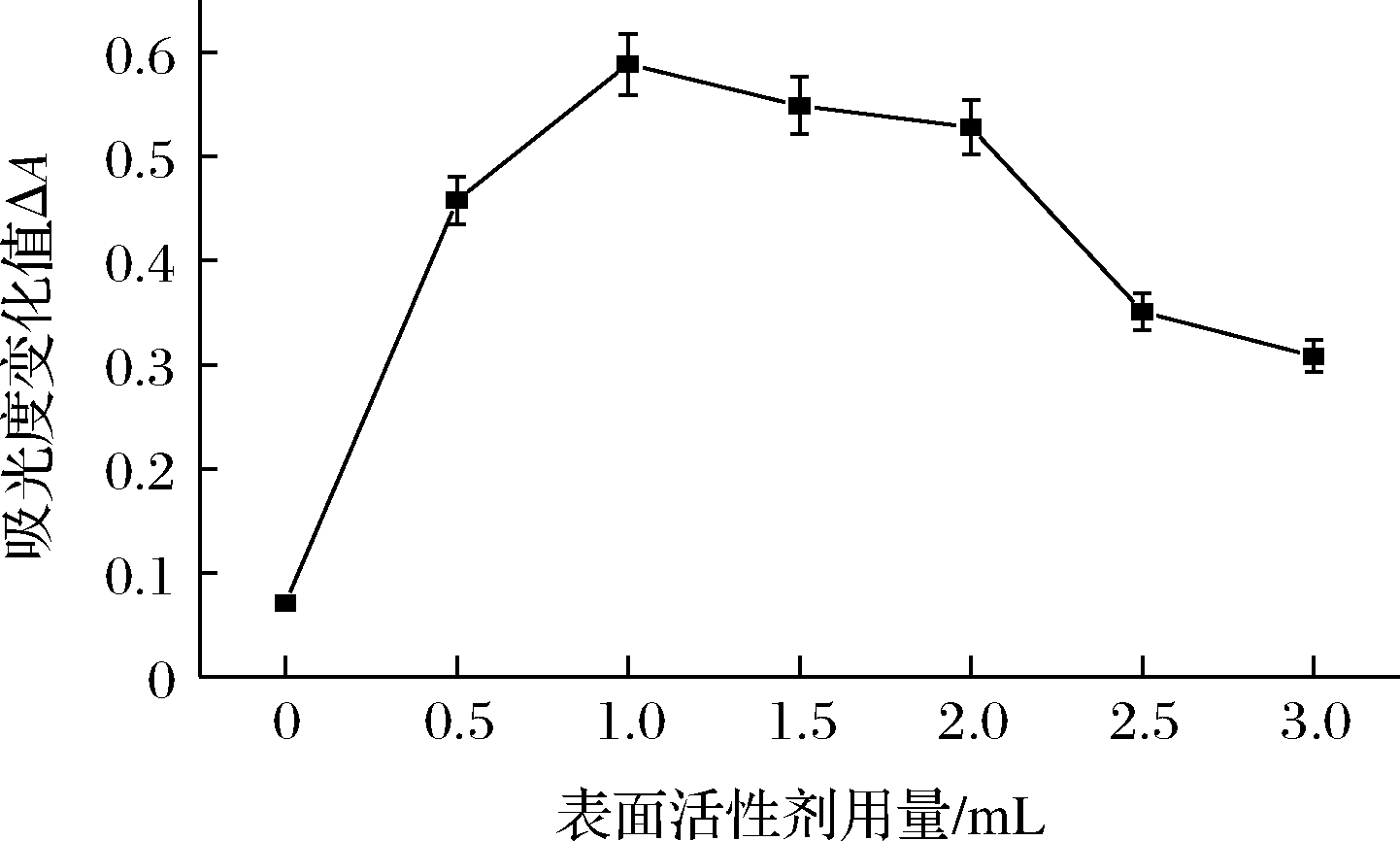
图5 表面活性剂用量对显色效果的影响
Fig.5 The effects of the surfactantaddition on the chromogenic reaction
2.2.4 时间对显色效果的影响
在上述讨论的最佳条件下,按照1.3实验方法,分别测定显色液及空白液在0.5、1、2、4、6、8 h时在647 nm处的吸光度,计算ΔA, 测试时间对显色效果的影响,结果见图6。当显色时间小于2 h时,反应不完全,显色液和空白液之间的吸光度差值ΔA随时间呈增大趋势,到2 h时达最大,之后虽略有降低,但不明显,因此确定最佳测量时间为显色后2~6 h内完成,时间过长则会引起较大误差。
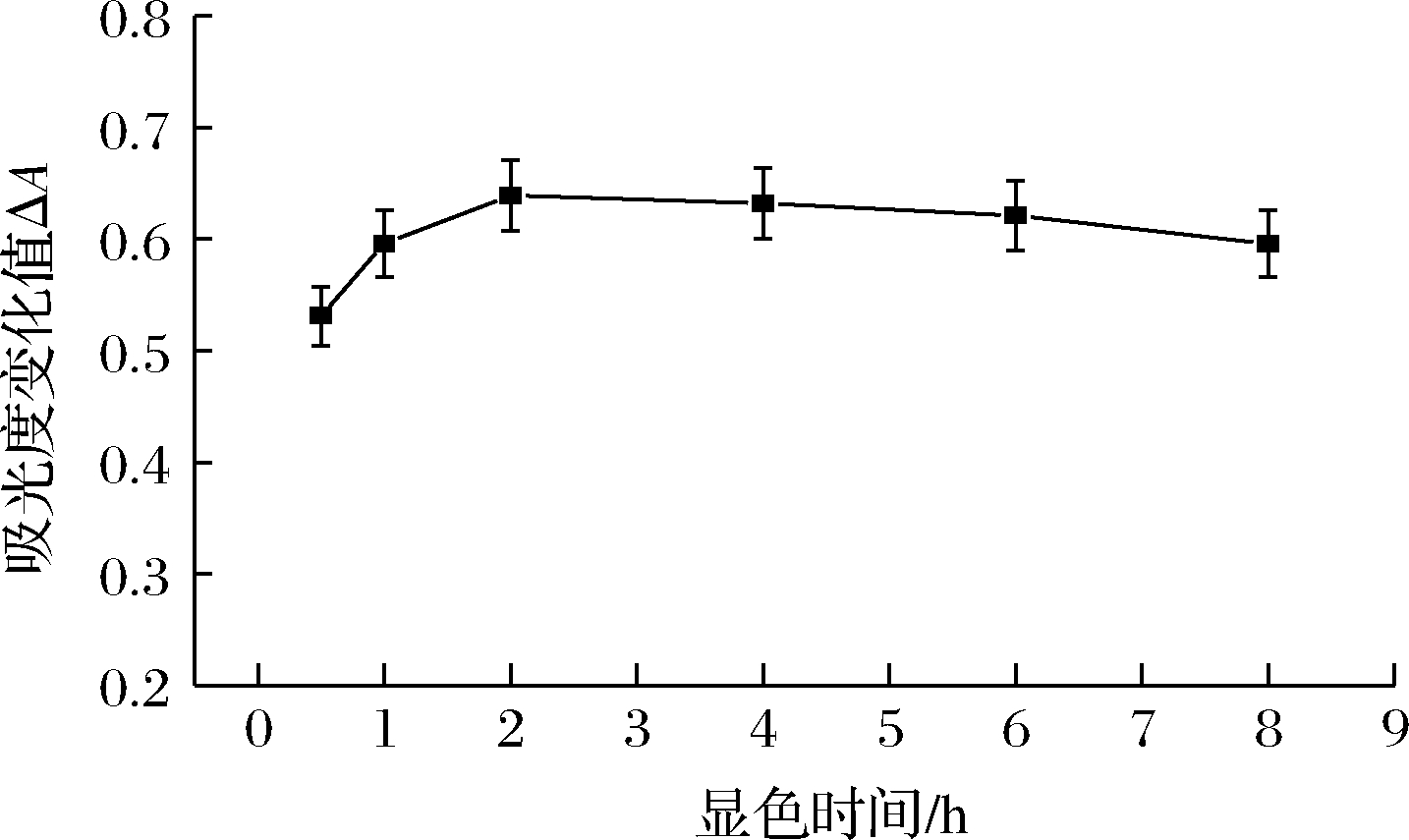
图6 时间对显色效果的影响
Fig.6 The effects of chromogenic time on the chromogenic reactio
综上实验,Fe(Ⅲ)-铬菁R显色体系对C2O42-的最佳检测条件为:pH=4.5的HAc-NaAc缓冲溶液用量3.00 mL, 0.15 mol/L十二烷基三甲基溴化铵表面活性剂用量为1.00 mL, 最佳测定时间为显色后2~6 h。常见的阳离子如K+、Na+、Ca2+、NH4+等均不会对测定产生干扰,但高浓度的Al3+、Zn2+、Ni2+因为会与C2O42-发生配位而产生一定影响,当测定对象中含有较多这几种离子时,可在酸性溶液中通过阳子交换树脂分离除去,或在强碱性溶液中使其生成沉淀并过滤来达到掩蔽目的。
按实验确定的最佳条件在25 mL比色管中分别加入1.00 mL 5×10-4mol/L的Fe3+、1.00 mL 5×10-4 mol/L的铬菁R、3.00 mL pH=4.5的缓冲溶液和1.00 mL 0.15 mol/L表面活性剂,再依次加入相应体积的1.0×10-3 mol/L的![]() 标准溶液,定容后使各比色管中的
标准溶液,定容后使各比色管中的![]() 浓度分别为2.0×10-5~1.6×10-4 mol/L,室温显色2 h,以蒸馏水做参比在647 nm处测吸光度,计算ΔA,绘制工作曲线如图7,草酸根离子浓度为2.0×10-5~1.4×10-4 mol/L范围内呈线性关系,回归方程:y=0.037 82x-0.020 86, 相关系数r=0.998 1,方法的检出限为1.5×10-5 mol/L。同时,对加入4.0×10-5 mol/L
浓度分别为2.0×10-5~1.6×10-4 mol/L,室温显色2 h,以蒸馏水做参比在647 nm处测吸光度,计算ΔA,绘制工作曲线如图7,草酸根离子浓度为2.0×10-5~1.4×10-4 mol/L范围内呈线性关系,回归方程:y=0.037 82x-0.020 86, 相关系数r=0.998 1,方法的检出限为1.5×10-5 mol/L。同时,对加入4.0×10-5 mol/L ![]() 标准溶液的试液进行11次平行测定,其相对标准偏差为2.7%。
标准溶液的试液进行11次平行测定,其相对标准偏差为2.7%。
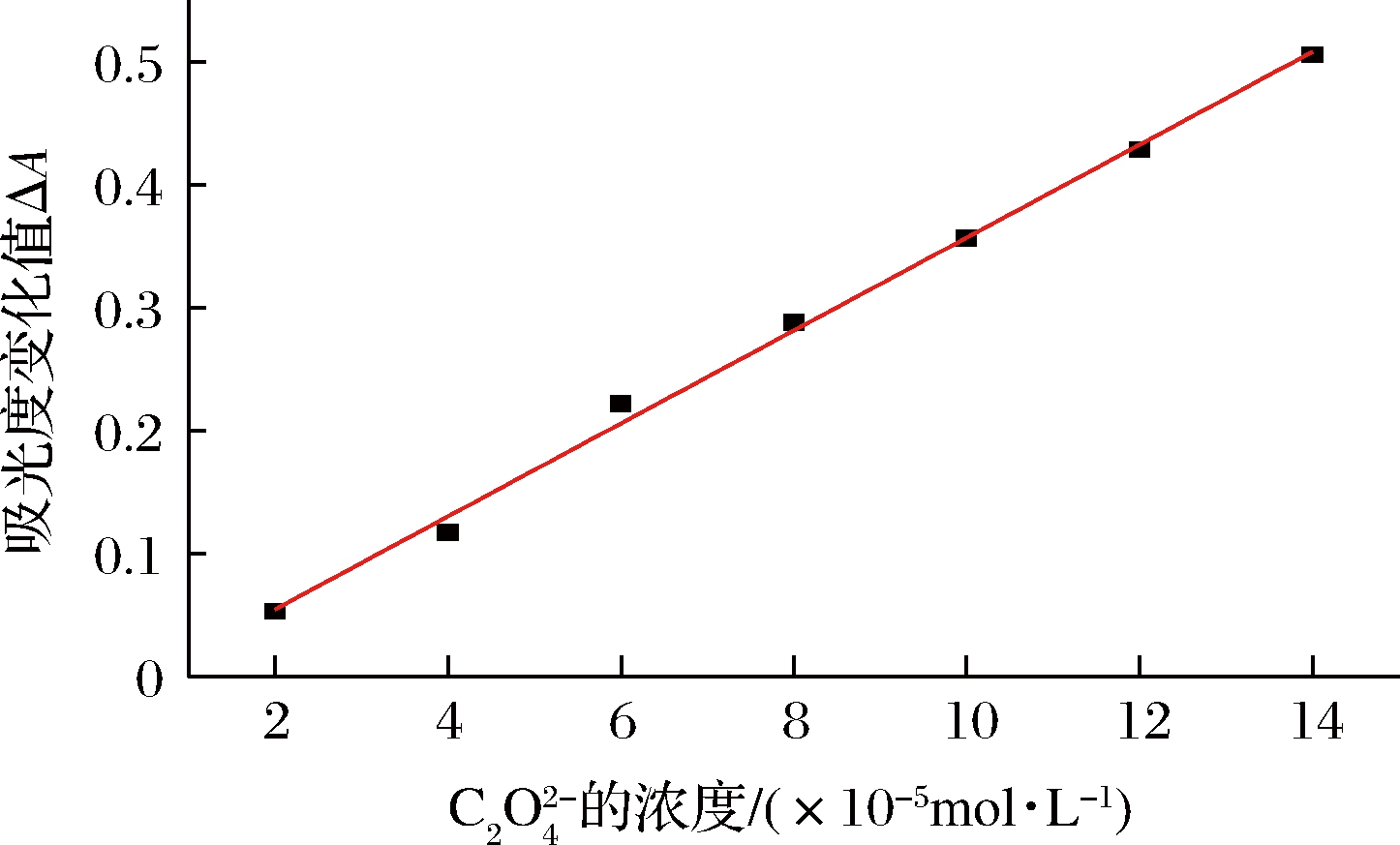
图7 标准曲线
Fig.7 Standard curve for the detection of ![]()
按照1.4样品处理的方法对蔬菜进行处理,分别移取2.00 mL的菠菜处理液及5.00 mL的韭菜处理液于25 mL比色管中,在最佳实验条件下按1.2实验方法进行测定,为了检验该方法的准确度,同时也采用容量法进行对比测定,并做加标回收率试验,结果如表1所示,测定值与容量法检测结果基本一致,所测回收率为93.3%~104.3%。
表1样品及回收率数据
Table 1 The recovery data

样品测定值/(mg·g-1)本方法容量法测定浓度1/(mol·L-1)加标量/(mol·L-1)测定浓度2/(mol·L-1)回收率/%菠菜3.063.355.46×10-54.0×10-59.19×10-593.3%韭菜0.700.593.11×10-54.0×10-57.28×10-5104.3%
有强配位性的![]() 能使Fe3+和铬菁R形成的蓝色络合物发生配位转换,从而引起溶液颜色和吸收光谱的显著变化,而等量其他常见阴离子的加入则不会引起Fe3+-铬菁R显色体系发生类似响应,因此可以实现对
能使Fe3+和铬菁R形成的蓝色络合物发生配位转换,从而引起溶液颜色和吸收光谱的显著变化,而等量其他常见阴离子的加入则不会引起Fe3+-铬菁R显色体系发生类似响应,因此可以实现对![]() 离子的裸眼识别。且体系在647 nm处的吸光度降低值ΔA与加入的
离子的裸眼识别。且体系在647 nm处的吸光度降低值ΔA与加入的![]() 浓度成正比,由此建立了一种简单、灵敏、准确的识别检测水溶液中草酸根的新方法。
浓度成正比,由此建立了一种简单、灵敏、准确的识别检测水溶液中草酸根的新方法。
该方法的优点为:(1)实现了在水相中对![]() 的目视比色识别,使之应用不受溶剂影响,同时可进行定量检测;对水溶液中比之前文献报道的显色效果更明显,选择性更突出;(2)相对于其他显色体系,Fe3+-铬菁R显色体系对
的目视比色识别,使之应用不受溶剂影响,同时可进行定量检测;对水溶液中比之前文献报道的显色效果更明显,选择性更突出;(2)相对于其他显色体系,Fe3+-铬菁R显色体系对![]() 的选择性更高,12种常见阴离子对其均不产生影响;(3)该新方法廉价易得,简单易操作,且体系稳定性好。
的选择性更高,12种常见阴离子对其均不产生影响;(3)该新方法廉价易得,简单易操作,且体系稳定性好。
[1] 李宝盛, 彭新湘, 李明启.植物中草酸积累与光呼吸乙醇酸代谢的关系[J].植物生理与分子生物学, 2000, 26(2):148-152.
LI B S, PENG X X, LI M Q.Relationship between oxalate accumulation and photorespiratory glycolate metabolism in plants[J].Acta Phytophysiologica Sinica, 2000, 26(2):148-152.
[2] 俞乐, 彭新湘, 杨崇, 等.反相高效液相色谱法测定植物组织及根分泌酸物中草酸[J].分析化学研究简报, 2002, 30(9):1 119-1 122.
YU L, PENG X X, YANG C, et al.Determination of oxalic acid in plant tissue and root exudate by reversed phase high performance liquid chromatography[J].Chinese Journal of Analytical Chemistry, 2002, 30(9):1 119-1 122.
[3] 张英鹏, 杨运娟, 杨力, 等.草酸在植物体内的累积代谢及生理作用研究进展[J].山东农业科学, 2007, 30(6):61-67.
ZHANG Y P, YANG Y J, YANG L, et al.Research progress of oxalate accumulation and metabolism in plant and its physiological function[J].Shandong Agricultural Sciences, 2007, 30(6):61-67.
[4] 彭婕, 葛卫红, 谈恒山, 等.高效液相色谱法同时测定健康人尿液中草酸和枸橼酸的含量[J].中国现代应用药学杂志, 2007, 24(1):72-74.
PENG J, GE W H, TAN H S, et al.Simultaneous determination of the contents of oxalate and citrate in human urine by RP-HPLC[J].Chinese Journal of Modern Applied Pharmacy, 2007, 24(1):72-74.
[5] BSC C N.Oxalate content of foods and its effect on humans[J].Asia Pacific Journal of Clinical Nutrition,1999, 8(1):64-74.
[6] 杭义萍, 卢祝靓子, 杨春英.抗坏血酸存在下离子色谱法直接测定尿液中草酸含量的研究[J].分析测试学报, 2014, 33(11):1 307-1 311.
HANG Y P, LU Z L Z, YANG C Y.Study on determination of oxalate in urine by ion chromatography in the presence of ascorbic acid[J].Journal of Instrumental Analysis, 2014, 33(11):1 307-1 311.
[7] WEIR T L, BAIS H P, STULL V J, et al.Oxalate contributes to the resistance of Gaillardia grandiflora and Lupinus sericeus to a phytotoxin produced by Centaurea maculosa[J].Planta, 2006, 223:785-795.
[8] 李文峰, 张士青, 顾欣.微量尿草酸测量的3种比色法比较[J].中国实验诊断学, 2006, 10(8):909-911.
LI W F, ZHANG S Q, GU X.Comparison with three colorimetries for determining urinary oxalate[J].Chinese Journal of Laboratory Diagnosis, 2006, 10(8):909-911.
[9] MAZEN A M A.Calcium oxalate deposits in leaves of Corchorus olitorius as related to accumulation of toxic metals[J].Russian Journal of Plant Physiology, 2004, 51(2):281-285.
[10] KIM D S, KIM H K, KIM M K.Analysis of oxalic acid of various vegetables consumed in Korea[J].Food Science and Biotechnology, 2007, 16:650-654.
[11] 施超欧, 栾绍嵘, 王洁姮.离子色谱法测定甘草提取物中草酸的含量[J].化学分析计量, 2005, 14(3):38-39.
SHI C O, LUAN S R, WANG J H.Determination of oxalic acid in liquorice extract by ion chromatography[J].Chemical Analysis and Meterage, 2005, 14(3):38-39.
[12] 卓静, 葛雪松, 孙桐, 等.离子色谱法测定维生素C注射液中草酸的含量[J].中国药师, 2022, 25(3):555-557.
ZHUO J, GE X S, SUN T, et al.Determination of oxalic acid in vitamin C injections by ion chromatography[J].China Pharmacist, 2022, 25(3):555-557.
[13] 汤立军, 王楠楠, 郭娇娇, 等.基于光化学传感器的二元羧酸阴离子识别研究进展[J].化学通报, 2012, 75(10):868-878.
TANG L J, WANG N N, GUO J J, et al.Progress in recognition of dicarboxylate anions based on optical chemosensors[J].Chemistry, 2012, 75(10):868-878.
[14] 张文龙, 赵青峰.离子色谱法测定地表水中丙酸、丙烯酸、丁酸和草酸的残留[J].化学工程师, 2021, 35(9):29-31.
ZHANG W L, ZHAO Q F.Determination of propionic acid, acrylic acid, butyric acid and oxalic acid residues in surface water by ion chromatography[J].Chemical Engineer, 2021, 35(9):29-31.
[15] 汤立军, 王楠楠, 郭娇娇, 等.一种光化学传感体系的构筑及其在水溶液中对草酸根的荧光识别[J].渤海大学学报(自然科学版), 2012, 33(3):225-229;272.
TANG L J, WANG N N, GUO J J, et al.Construction of a chemosensing ensemble and its fluorescent recognition for oxalate in water[J].Journal of Bohai University(Natural Science Edition), 2012, 33(3):225-229;272.
[16] 宋少飞, 张庆, 周福林.抑制动力学荧光法测定食品中草酸的含量[J].平顶山学院学报, 2022, 37(2):32-35;60.
SONG S F, ZHANG Q, ZHOU F L.Determination of oxalic acid in food by inhibitory kinetic spectrofluorimetry[J].Journal of Pingdingshan University, 2022, 37(2):32-35;60.
[17] 朱玉莲, 黄韬, 张岐, 等.对苯二甲醛缩二氨基硫脲-钆配合物的合成及阴离子识别研究[J].无机化学学报, 2011, 27(8):1 471-1 476.
ZHU Y L, HUANG T, ZHANG Q, et al.Synthesis of gadolinium complex based on terephthalic aldehyde bis-thiosemicarbazide and its anion recognition properties[J].Chinese Journal of Inorganic Chemistry, 2011, 27(8):1 471-1 476.
[18] 丁亚平, 吴庆生.示波电位滴定法测定僵蚕中草酸铵[J].分析试验室, 1997, (5):14-16.
DING Y P, WU Q S.Determination of ammonium oxalate in muscardine silkworm by oscillographic potentiometric titration[J].Chinese Journal of Analysis Laboratory, 1997, (5):14-16.
[19] 张成路, 李益政, 李金池, 等.两个新型1,3-硒唑酰腙的合成及其对醋酸根离子的特性荧光识别[J].应用化学, 2018, 35(2):197-205.
ZHANG C L, LI Y Z, LI J C, et al.Synthesis of two novel 1,3-selenazole carbonyl hydrazones and their specific fluorescent recognition toward acetate ions[J].Chinese Journal of Applied Chemistry, 2018, 35(2):197-205.
[20] 谭赞, 杜欢, 吕新阳, 等.含氨基蒽醌信号单元的咔唑磺胺类阴离子受体的合成及识别性能研究[J].有机化学, 2016, 36(6):1 389-1 394.
TAN Z, DU H, LYU X Y, et al.Synthesis and recognition properties of carbazole sulfonamide based anion receptor containing the aminoanthraquinone signalling units[J].Chinese Journal of Organic Chemistry, 2016, 36(6):1 389-1 394.
[21] 李勇军, 刘辉彪, 李玉良.基于氢键的阴离子识别主体分子的研究进展[J].无机化学学报, 2015, 31(9):1 687-1 704.
LI Y J, LIU H B, LI Y L. Recent development of anion receptors based on hydrogen bonding[J]. Chinese Journal of Inorganic Chemistry, 2015, 31(9): 1 687-1 704.
[22] LI Y J, LIU H B, LI Y L.Recent development of anion receptors based on hydrogen bonding[J].Chinese Journal of Inorganic Chemistry, 2015, 31(9):1 687-1 704.
[23] 刘鑫, 何少华, 闵瑞, 等.基于铝与铬菁R显色体系对水溶液中![]() 的识别与检测[J].化学试剂, 2016, 38(11):1 089-1 091.
的识别与检测[J].化学试剂, 2016, 38(11):1 089-1 091.
LIU X, HE S H, MIN R, et al.Recognition and detection of oxalate in aqueous solution by the chromogenic system of Al3+ and eriochrom cyanine R[J].Chemical Reagents, 2016, 38(11):1 089-1 091.
[24] 庞海霞. 基于Fe3+和磺基水杨酸定性定量检测水溶液中无机磷酸根总量[J].分子科学学报, 2014, 30(1):81-84.
PANG H X.Qualitative and quantitative determination of inorganic phosphate in aqueous solution by Fe(Ⅲ)ion and sulfosalicylic acid[J].Journal of Molecular Science, 2014, 30(1):81-84.
[25] 庞海霞, 强瑾, 姜敏, 等.KI-罗丹明6G荧光猝灭法测定火腿中的亚硝酸盐[J].食品与发酵工业, 2021, 47(16):253-257.
PANG H X, QIANG J, JIANG M, et al.Determination of nitrite in ham sausage by KI-rhodamine 6G fluorescence quenching method[J].Food and Fermentation Industries, 2021, 47(16):253-257.
[26] 曾芳, 刘忠珍, 许桂芝, 等.蔬菜中不同形态草酸的提取测定[J].食品科学, 2009, 30(16):216-219.
ZENG F, LIU Z Z, XU G Z, et al.Extraction and determination of different forms of oxalate in vegetables[J].Food Science, 2009, 30(16):216-219.