燕麦(Avena sativa L.),也被称为雀麦和野生小麦,主要有裸燕麦和有壳燕麦[1]。燕麦富含蛋白质、脂质和β-葡聚糖等,且必需氨基酸含量均衡[2-3],营养丰富。燕麦有许多健康益处,包括预防癌症,预防高血脂,减缓葡萄糖摄取等[3-4]。因此,燕麦现被广泛用于许多食品中,如面条、面包、饼干和饮品中。燕麦乳也成为一种非常受欢迎的植物乳。然而,燕麦乳储藏过程中淀粉回生会造成口感变差、沉淀分层问题,使燕麦乳品质变差[5]。在燕麦乳制作过程中加入淀粉酶水解淀粉,可以减轻淀粉老化造成的不良影响[6]。汪丽萍等[7]优化了α-淀粉酶和糖化酶酶解燕麦乳的工艺,提高了燕麦乳的稳定性。曹盼等[8]用α-淀粉酶水解淀粉制备的燕麦乳色泽、稳定性较好。然而,传统的酶解反应条件要求苛刻,需要适宜的pH条件以及高水分且较长的酶解时间[9]。
双螺杆挤压是一种高温、短时间、连续的多功能热技术,它集物料混合、搅拌、剪切、加热、成型等多种操作于一体,以达到持续的高生产率,被广泛应用于食品领域[10]。加酶挤压是在挤压过程中引入外源酶,由于螺杆的混合、剪切等作用,酶与底物接触表面积增加,表现出高效酶活性[11]。ZHAO等[12]用加酶挤压技术改性大麦粉以用于啤酒发酵,明显提高了酒精含量。焦爱权等[13]将加酶挤压作为土圞儿块茎的预处理方法,并生产了一种高度糊化、低黏度的挤出物,可用于黄酒发酵。加酶挤压技术因其降解效率高、废水排放少、可连续生产等优点而在糖化、酿造、重组配方食品等多个领域得到广泛应用。但将其应用于燕麦乳等谷物饮料的研究报道还比较少。
本试验系统研究了加酶挤压对燕麦淀粉表观结构特性、水合特性、糊化特性、流变特性等的影响,并探究了加酶挤压预处理燕麦粉制备的燕麦乳的稳定性以及感官评价。以期为燕麦乳的生产提供一种高效节能省时的新思路。
1 材料与方法
1.1 材料与试剂
燕麦(总淀粉64.07%,蛋白质12.48%,脂肪6.06%,水分10.88%),河北康希燕麦食品有限公司;NaOH、3,5-二硝基水杨酸、盐酸、醋酸钠、葡萄糖(均为分析纯),TaKa淀粉酶(1.2~1.8 U/mg),国药集团化学试剂有限公司;中温α-淀粉酶(最适pH 5~6,最适温度55~60 ℃,酶活力480 KNU/g),诺维信公司。
1.2 仪器与设备
ZE-16双螺杆挤压机,江苏ATS公司;SQP分析天平,赛多利斯科学仪器有限公司;HHS-21-4恒温水浴锅,上海百典仪器设备有限公司;TGL-18M台式高速离心机,上海卢湘仪离心机仪器有限公司;RVA 4500快速黏度分析仪,波通澳大利亚公司;SHA-AB恒温培养振荡器,常州市旭日实验仪器厂;SU8100冷场发射扫描电子显微镜,日本株式会社日立高新技术;DHG-9123A电热恒温鼓风干燥箱,上海柏欣仪器设备厂;PowerWaveX52酶标仪,美国PowerWave公司;Waters 1525EF 高效液相色谱仪,美国沃特世公司;DHR-3旋转流变仪,美国TA公司;HX-P01破壁机,佛山顺德汉熙电器有限公司;JHG-54-P100均质机,上海普丽盛融合机械设备有限公司。
1.3 实验方法
1.3.1 样品的挤压处理
挤压前,将燕麦粉与0、0.02%、0.06%、0.1%和0.2%的中温α-淀粉酶(燕麦粉干基,质量分数)进行预混合。然后将混合物在4 ℃下平衡水分12 h。经预实验,挤压机参数设置如下:6个筒区温度分别为30、45、60、65、85和100 ℃,进料速度为0.3 kg/h,螺杆转速为150 r/min,物料含水率50%。部分挤出物在0.2 mol/L醋酸钠缓冲液中(pH 3.5)灭酶后在40 ℃下干燥,研磨后备用,部分直接用于燕麦乳的制备。
1.3.2 燕麦淀粉的提取
将原燕麦粉及1.3.1节中挤压烘干后的燕麦粉与NaOH溶液(2.0 g/L)按1∶8的体积比均匀混合,在室温下搅拌4 h。结束后,6 000×g离心10 min,沉淀溶于去离子水,6 000×g离心10 min进行洗涤,重复清洗4次。将得到的淀粉样品在40 ℃下烘干,磨成粉末待用。
1.3.3 燕麦淀粉分子质量分布的测定
参照BIAN等[14]的方法。将淀粉样品配置成0.5 g/100 mL的溶液,在沸水浴中煮沸并搅拌1 h,样品经过0.45 μm滤膜过滤,然后通过高效液相色谱仪进行测试。
1.3.4 淀粉微观结构的观察
采用扫描电镜(scanning electron microscope,SEM)对样品的微观结构进行观察。将样品均匀地分散在导电胶上,真空条件下喷金,放大1 500倍后观察并拍照。
1.3.5 水溶性指数和吸水性指数的测定
水溶性指数(water solubility index,WSI)和吸水性指数(water absorption index,WAI)的测定参照HAGENIMANA等[15]的方法,并稍作修改。将1.0 g样品(m1)溶于12 mL去离子水中,随后在恒温振荡水浴中(30 ℃,160 r/min)孵育30 min,最后6 500×g离心15 min。上清液在105 ℃烘干至恒重,称量上清液(M1)和沉淀(M2)的质量并记录。WSI和WAI按公式(1)和公式(2)计算:
(1)
(2)
1.3.6 可溶性还原糖含量的测定
参照赵淑娜[16]的方法测定可溶性还原糖含量。
1.3.7 糊化度的测定
参照YANG等[17]的方法。称量0.5 g样品于装有20 mL去离子水的50 mL锥形瓶中,沸水浴20 min,使淀粉完全糊化。另取0.5 g样品按上述步骤处理,但不煮沸作为对照组。2组样品在37 ℃平衡30 min后,加入5 mL 30 g/L的TaKa淀粉酶,在恒温振荡水浴中孵育2 h (37 ℃,160 r/min),然后加入1 mL HCl (1 mol/L)灭酶,再加入1 mL NaOH(1 mol/L)中和pH,过滤,按照1.3.6节中的方法测定上清液中还原糖含量。糊化度表示为对照组与糊化组还原糖含量的比值。
1.3.8 淀粉糊化特性的测定
参照FU等[18]的方法。糊化特性用快速黏度分析仪(rapid visco analyzer,RVA)测定。将3.0 g样品加入装有25 g去离子水的铝罐中,初始温度50 ℃,在3.8 min内升至95 ℃,并保持2 min,然后在相同时间内降低到50 ℃,继续保持2 min。在最初的10 s内,样品以960 r/min的速度混合,随后将搅拌速率降低到160 r/min,直到分析结束。
1.3.9 淀粉流变特性的测定
使用流变仪测定样品的流变性能。燕麦淀粉样品(1.0 g,干基)与9.0 g去离子水混合,沸水浴15 min。样品冷却至室温后转移到40 mm平板上。设置应变为1%,频率扫描0.1~100 rad/s,以获得储存模量(G′),损耗模量(G″)和tanδ。同时测定淀粉剪切应力及黏度随剪切速率从0 s-1升至100 s-1,再从100 s-1降到0 s-1过程中的变化。
1.3.10 燕麦乳的制备
将原燕麦粉及挤出的燕麦粉与纯净水以1∶15(g∶mL)的比例混合,然后使用破壁机进行打浆,沸水浴20 min灭酶。将得到的燕麦浆过75 μm筛,加入1%菜籽油和2%食盐(燕麦浆,质量分数)。样品在室温、均质压力为40 MPa条件下均质2次。最后,85 ℃杀菌20 min后得到燕麦乳。同时,将燕麦米清洗后在纯净水中浸润2 h,在120 ℃烘烤30 min,随后在纯净水中浸泡12 h,沥水后打浆,添加0.2%的中温α-淀粉酶(干基燕麦粉,质量分数),60 ℃、pH 6.0酶解2 h后灭酶过75 μm筛,后续处理步骤同上,获得传统酶解方法生产的燕麦乳。
1.3.11 燕麦乳贮藏稳定性
测定燕麦乳在4 ℃贮藏条件下0、1、3、5、7、14、21 d的分离指数、感官评分以评估加酶挤压对燕麦乳感官评分、稳定性的影响。分离指数及感官评定测定方法如下:
1.3.11.1 燕麦乳分离指数的评定
分离指数(separation index,SI)的测定参照GUIMAR ES等[19]的方法。将杀菌罐装后的燕麦乳在冷藏条件下(4 ℃)储存以评估相分离,根据公式(3)计算分离指数:
ES等[19]的方法。将杀菌罐装后的燕麦乳在冷藏条件下(4 ℃)储存以评估相分离,根据公式(3)计算分离指数:
(3)
式中:hT,饮料的总高度,mm;hS,上相的高度,mm。
1.3.11.2 燕麦乳感官评定
燕麦乳的感官评定参考GB/T 31326—2014《植物饮料》并作适当修改。选择5名男生和5名女生经过为期2周的培训后对燕麦乳样品进行感官评定。感官评分标准见表1。
表1 燕麦乳的感官评分标准
Table 1 Sensory evaluation criteria of oat milk
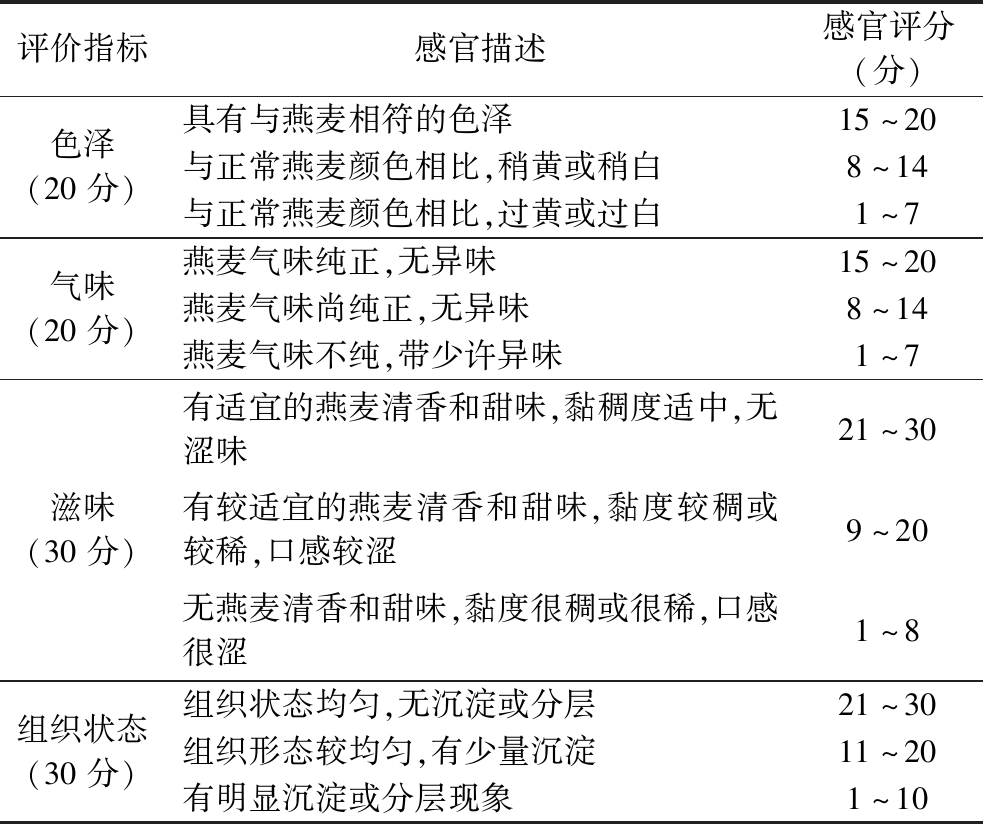
评价指标感官描述感官评分(分)色泽(20分)具有与燕麦相符的色泽15~20与正常燕麦颜色相比,稍黄或稍白8~14与正常燕麦颜色相比,过黄或过白1~7气味(20分)燕麦气味纯正,无异味15~20燕麦气味尚纯正,无异味8~14燕麦气味不纯,带少许异味1~7滋味(30分)有适宜的燕麦清香和甜味,黏稠度适中,无涩味21~30有较适宜的燕麦清香和甜味,黏度较稠或较稀,口感较涩9~20无燕麦清香和甜味,黏度很稠或很稀,口感很涩1~8组织状态(30分)组织状态均匀,无沉淀或分层21~30组织形态较均匀,有少量沉淀11~20有明显沉淀或分层现象1~10
1.4 统计分析
所有实验均重复3次,结果以平均数±标准差表示。采用 SPSS 26.0软件对数据进行单因素方差分析以及Duncan检验。
2 结果与分析
2.1 加酶挤压对燕麦淀粉分子质量的影响
分子质量越大,出峰时间越早。如图1所示,原淀粉的出峰时间最早,重均分子质量(Mw)为178.38×104 g/mol,0%样品出峰时间后移,Mw降为162.84×104 g/mol,说明双螺杆挤压的剪切作用对燕麦淀粉有一定的降解作用,但降解作用很小。随着α-淀粉酶浓度的增加,色谱峰的出峰时间逐渐后移,Mw值逐渐减小,当加酶量为0.2%时,Mw为41.42×104 g/mol和0.53×104 g/mol,淀粉降解显著。分子质量结果表明加酶挤压过程中由于挤压机的剪切以及淀粉酶酶解的协同作用可以导致淀粉的显著降解。淀粉降解为低聚糖后可以改善淀粉回生的问题,从而改善淀粉沉降引起的燕麦乳不稳定的问题。
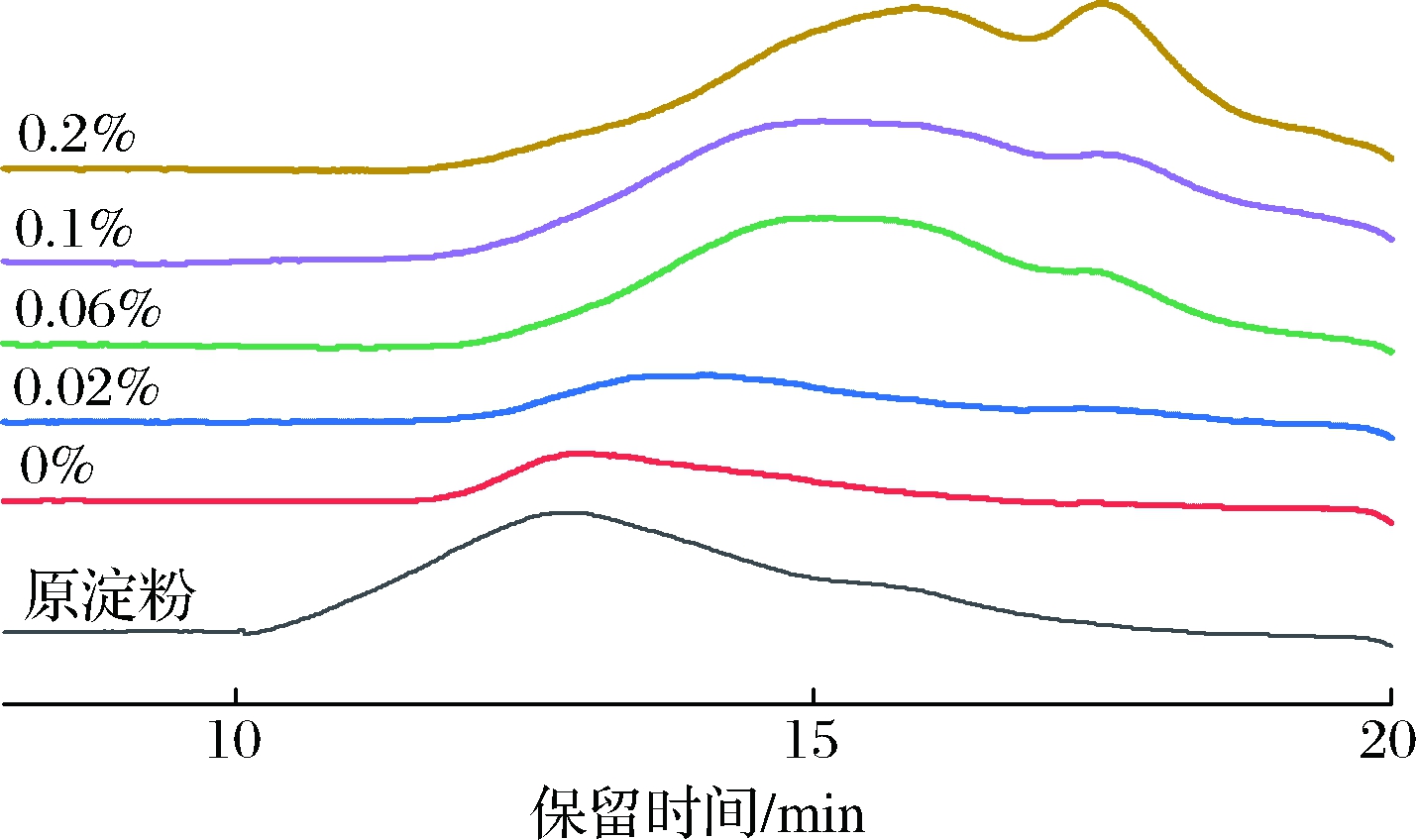
图1 不同燕麦淀粉的分子质量分布
Fig.1 Molecular weight distribution of different oat starch
2.2 加酶挤压对燕麦淀粉微观形貌的影响
样品的微观结构变化如图2所示,在原淀粉中可以观察到表面光滑的椭球状淀粉颗粒以及部分提取时形成的破碎颗粒。在0%样品中,淀粉失去了光滑的球形状态,淀粉颗粒被破坏,形成不规则的大颗粒淀粉块。
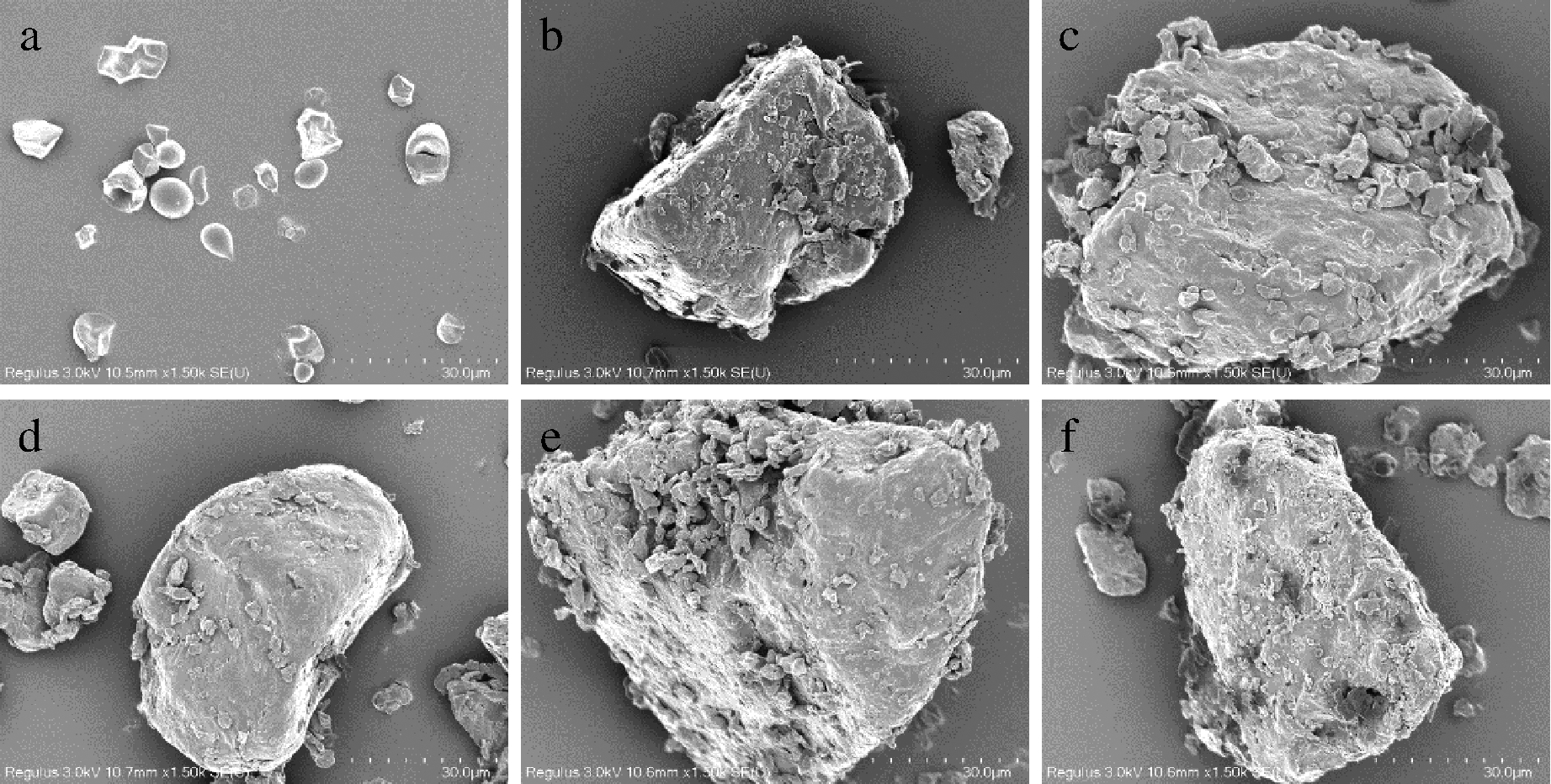
a-原淀粉;b-0%;c-0.02%;d-0.06%;e-0.1%;f-0.2%
图2 不同燕麦淀粉的扫描电镜图(×1 500)
Fig.2 Scanning electron microscope of different oat starch (×1 500)
随着酶的加入,淀粉颗粒的表面呈无定形结构,表面附着着许多小颗粒物质,且淀粉颗粒出现大量孔洞,其原因可能是α-淀粉酶水解淀粉时,小分子物质溶出。随着α-淀粉酶浓度的增加,完整颗粒逐渐被破坏,且由于挤压机的混合、剪切作用,从而形成不规则的大块颗粒。
2.3 加酶挤压对燕麦淀粉吸水性、水溶性、可溶性还原糖含量和糊化度的影响
吸水性反映了淀粉吸水膨胀的能力,而水溶性反映了原料加工过程中产生的可溶性组分的含量[20]。如表2所示,与原燕麦淀粉相比,0%样品的吸水性显著提高(从1.89 g/g提高到3.62 g/g),这可能是因为淀粉的糊化导致更多亲水基团的暴露[21]。但当淀粉降解程度大于糊化程度时,会导致吸水性降低[22]。随着α-淀粉酶添加量的增加,燕麦淀粉的吸水性值从3.62 g/g下降到2.61 g/g,这可能是淀粉酶促进淀粉降解,释放大量可溶性物质的结果。0%样品的水溶性从由原燕麦淀粉的0.41%提高到20.24%,表明在加酶量为0%时,挤压产生了一定数量的低分子量碳水化合物。此外,随着α-淀粉酶浓度的增加,水溶性从20.24%增加到44.39%(0.2%样品),说明加酶挤压能显著降解淀粉,从而释放出大量可溶性小分子。
表2 不同燕麦淀粉的吸水性指数、水溶性指数、还原糖含量、糊化度及黏度
Table 2 Water absorption index,water solubility index,reducing sugar content,gelatinization degree,and viscosity of different oat starch
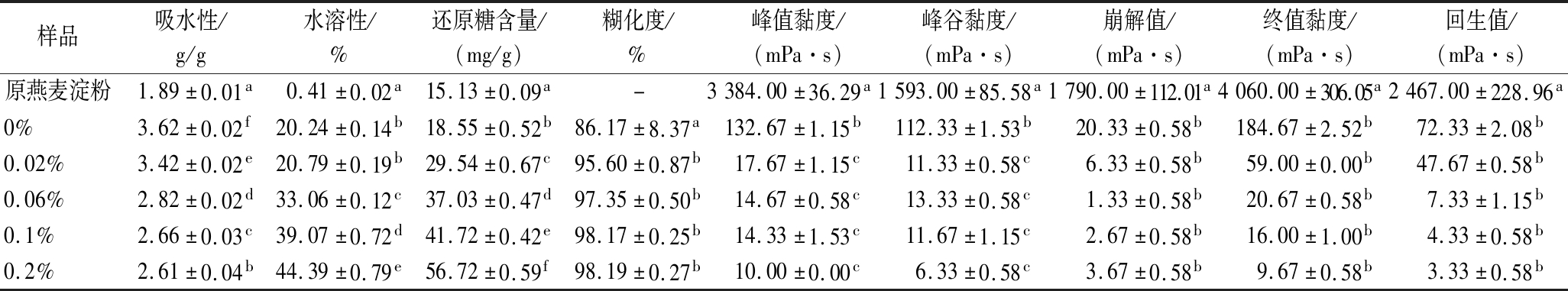
样品吸水性/g/g水溶性/%还原糖含量/(mg/g)糊化度/%峰值黏度/(mPa·s)峰谷黏度/(mPa·s)崩解值/(mPa·s)终值黏度/(mPa·s)回生值/(mPa·s)原燕麦淀粉1.89±0.01a0.41±0.02a15.13±0.09a-3384.00±36.29a1593.00±85.58a1790.00±112.01a4060.00±306.05a2467.00±228.96a0%3.62±0.02f20.24±0.14b18.55±0.52b86.17±8.37a132.67±1.15b112.33±1.53b20.33±0.58b184.67±2.52b72.33±2.08b0.02%3.42±0.02e20.79±0.19b29.54±0.67c95.60±0.87b17.67±1.15c11.33±0.58c6.33±0.58b59.00±0.00b47.67±0.58b0.06%2.82±0.02d33.06±0.12c37.03±0.47d97.35±0.50b14.67±0.58c13.33±0.58c1.33±0.58b20.67±0.58b7.33±1.15b0.1%2.66±0.03c39.07±0.72d41.72±0.42e98.17±0.25b14.33±1.53c11.67±1.15c2.67±0.58b16.00±1.00b4.33±0.58b0.2%2.61±0.04b44.39±0.79e56.72±0.59f98.19±0.27b10.00±0.00c6.33±0.58c3.67±0.58b9.67±0.58b3.33±0.58b
注:同一列中数字不同的上标字母表示差异性显著(P<0.05)。
与对水溶性的结果类似,0%样品的还原糖含量由原淀粉的15.13 mg/g提高到18.55 mg/g,对淀粉形成了一定的降解作用。加酶挤压后,还原糖含量显著增加,在0.2%淀粉酶质量分数下达到56.72 mg/g。糊化度也有同样的结果,添加0.2% α-淀粉酶淀粉几乎完全糊化(98.19%),这主要是淀粉降解和糊化的协同作用所致。
2.4 加酶挤压对燕麦淀粉糊化特性的影响
样品的糊化特征值如表2所示。原燕麦淀粉的峰值黏度、终值黏度最高,即使不添加α-淀粉酶的挤压,也会导致黏度下降。一般来说,糊化程度和淀粉颗粒的破坏程度对黏度起决定性作用[23]。在糊化过程中,原淀粉会因吸水而迅速膨胀,颗粒之间的摩擦增大,导致黏度迅速增加。因此,在RVA测量的加热过程中,糊化度较低的样品会发生二次糊化,导致黏度较高。RVA结果和糊化程度结果可以相互验证。崩解值体现了淀粉颗粒的热稳定性和剪切稳定性,崩解值越小二者越稳定。挤压处理后崩解值显著降低,可能是由于淀粉颗粒已被破坏,黏度低,故崩解值很小。回生值是指淀粉糊冷却时,直链淀粉分子之间的聚合引起的黏度增加。加酶挤压样品的回生值很小,可能是由于淀粉的降解、直链淀粉的浸出减少或加酶挤压过程中淀粉-脂复合物的形成抑制了淀粉的回生[24]。
2.5 加酶挤压对燕麦淀粉流变特性的影响
G′、G″和tanδ值与角频率的关系如图3所示。与原燕麦淀粉相比,加酶挤压样品的G′和G″值更低,表明加酶挤压处理后,样品的弹性和黏性都降低了。这可能是由于淀粉通过加酶挤压降解成小分子量的糊精,形成强网络凝胶结构能力减弱。所有样品的G′和G″都随着角频率的增加而增大。原燕麦淀粉的tanδ随频率变化不大,且tanδ<1,表现出弹性占主导的特征。加酶挤压处理后样品的tanδ值大于原燕麦淀粉的tanδ值,说明体系中黏性特征占比增大,更倾向于流体特征。
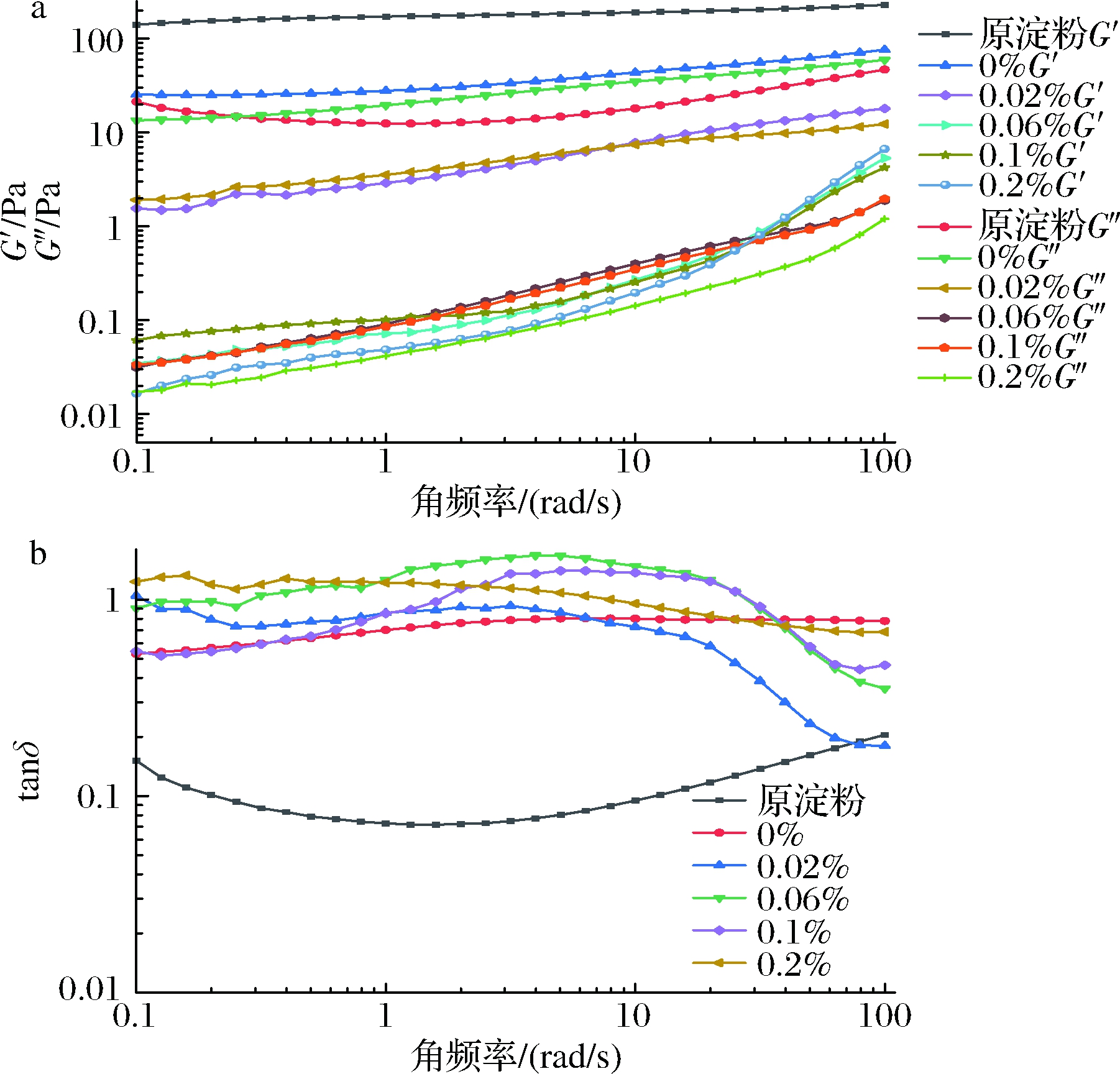
图3 不同燕麦淀粉的G′、G″(a)和tanδ(b)随角频率的变化曲线
Fig.3 Variation curves of G′,G″(a) and tanδ(b) with angular frequency of different oat starch
如图4所示,加酶挤压后,淀粉的剪切应力相比原淀粉显著降低,说明体系内部分子间的相互作用力很弱,没有较强的凝胶网络结构。样品黏度均随剪切速率的增大而减小,随后趋于平稳。样品的黏性行为是悬浮在液体介质中的粒子相互作用的结果。黏度的降低可能是由于外力作用下聚集体的分散或颗粒的破碎。进入平台期后,随着剪切速率的增加,物质的分散和颗粒破碎性不再显著[25]。在剪切速率相同的情况下,原燕麦淀粉的黏度最大,随加酶量的增大,体系的黏度减小。造成这一结果的原因可能是加酶挤压对淀粉的降解作用,小分子之间的相互作用较弱。样品随剪切速率的变化均形成了触变环,一般来说,触变环越大,淀粉凝胶结构的形成与恢复能力越差[26]。但相比于原淀粉,由于加酶挤压样品的黏度很小,故触变环也较小,但由于体系中低聚糖含量较多,故凝胶结构的形成与恢复能力更差。幂次定律拟合结果见表3。K值越大,增稠能力越强。原燕麦淀粉的K值最大,增稠能力最强,加酶挤压显著降低了样品的增稠能力。n为流动性特征指数,原淀粉样品和0%样品的n值较小,为假塑性流体,加酶挤压样品的n值趋向于1,倾向于牛顿流体特征,说明体系中化合物分子量较小,原因可能是淀粉降解为小分子化合物。
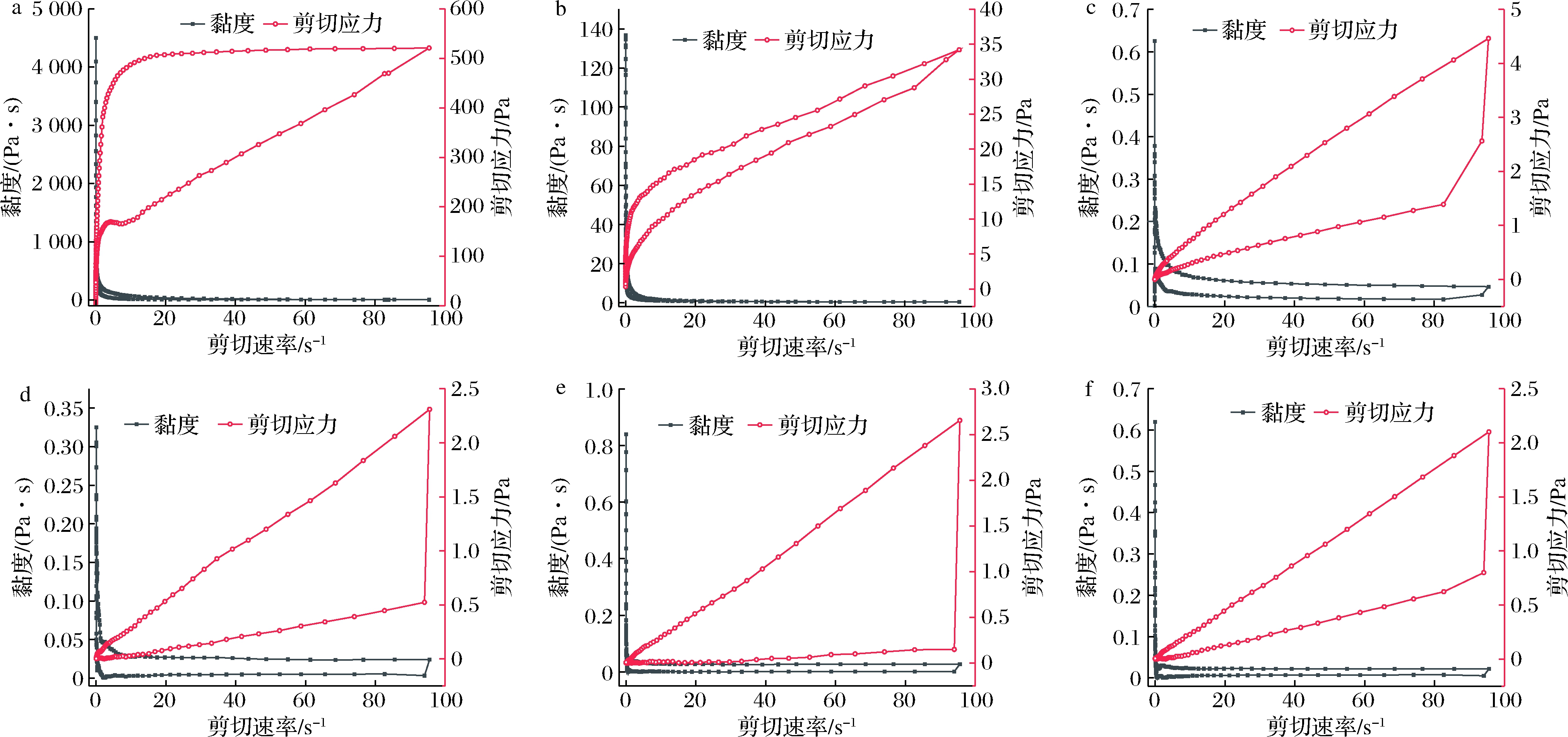
a-原淀粉;b-0%;c-0.02%;d-0.06%;e-0.1%;F-0.2%
图4 不同燕麦淀粉的静态流变曲线
Fig.4 Static rheological curves of different oat starch
表3 不同燕麦淀粉的流变方程拟合参数
Table 3 Rheological equation fitting parameters of different oat starch
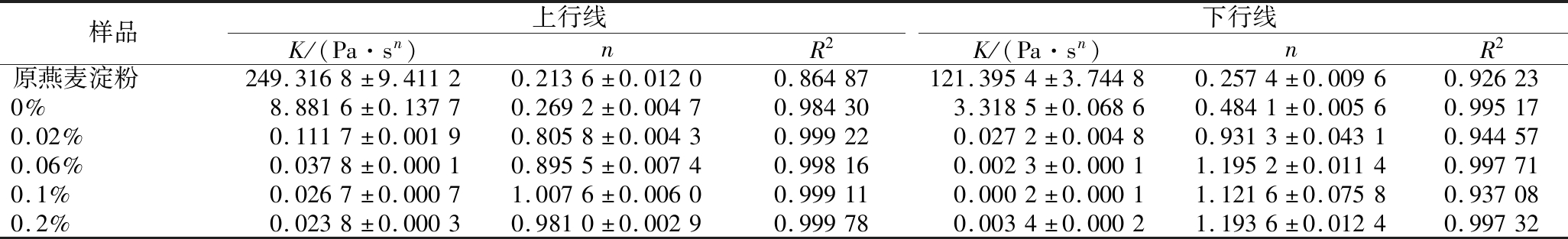
样品上行线下行线K/(Pa·sn)nR2K/(Pa·sn)nR2原燕麦淀粉249.3168±9.41120.2136±0.01200.86487121.3954±3.74480.2574±0.00960.926230%8.8816±0.13770.2692±0.00470.984303.3185±0.06860.4841±0.00560.995170.02%0.1117±0.00190.8058±0.00430.999220.0272±0.00480.9313±0.04310.944570.06%0.0378±0.00010.8955±0.00740.998160.0023±0.00011.1952±0.01140.997710.1%0.0267±0.00071.0076±0.00600.999110.0002±0.00011.1216±0.07580.937080.2%0.0238±0.00030.9810±0.00290.999780.0034±0.00021.1936±0.01240.99732
2.6 燕麦乳的贮藏稳定性及感官评价
燕麦乳在贮藏期内的分离指数如图5所示,通过相分离来评价燕麦乳的动力学稳定性。分离指数越高,上相高度越低,分子沉降越少,稳定性越好。原燕麦粉制备的燕麦乳在贮藏1 d后迅速沉降,分离指数为21.27%。加酶挤压后,燕麦乳稳定性得到显著改善,分离指数达到90%以上。与传统酶解相比,相同加酶量条件下,加酶挤压预处理生产的燕麦乳稳定性更好,可能是由于挤压的剪切作用协同酶解对淀粉的降解作用效果更好。贮藏21 d后,加酶挤压预处理后制备的燕麦乳分离指数减小但仍在90%左右,稳定性较好,表明加酶挤压处理燕麦粉可以显著提高燕麦乳的贮藏稳定性。
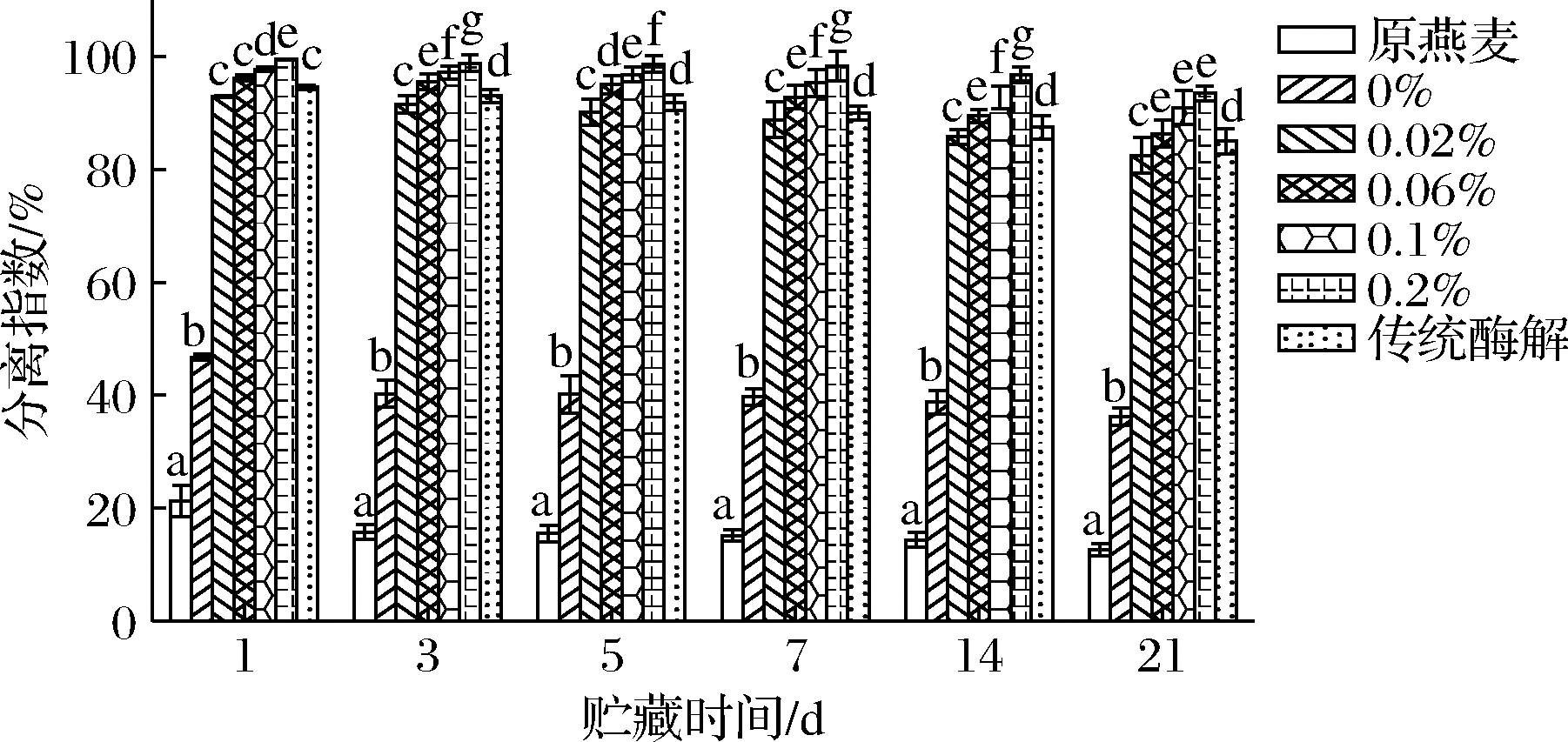
图5 不同燕麦乳在贮藏期内的分离指数
Fig.5 Separation index of different oat milk during storage period
燕麦乳在贮藏期内的感官评分如图6所示,加酶挤压处理后,淀粉降解为小分子还原糖,燕麦乳制备过程中发生的美拉德反应等可以使燕麦乳的气味和滋味更加醇厚。同时,加酶挤压可以使燕麦乳的组织状态更加均一稳定,故感官评分相比于原燕麦粉制备的燕麦乳更高。随着加酶量的增加,感官评分呈现上升趋势。随着贮藏时间的延长,燕麦乳品质下降,感官评分均呈现下降趋势。且在相同加酶量条件下,加酶挤压处理的燕麦乳的感官评分优于传统酶解方法生产的燕麦乳。
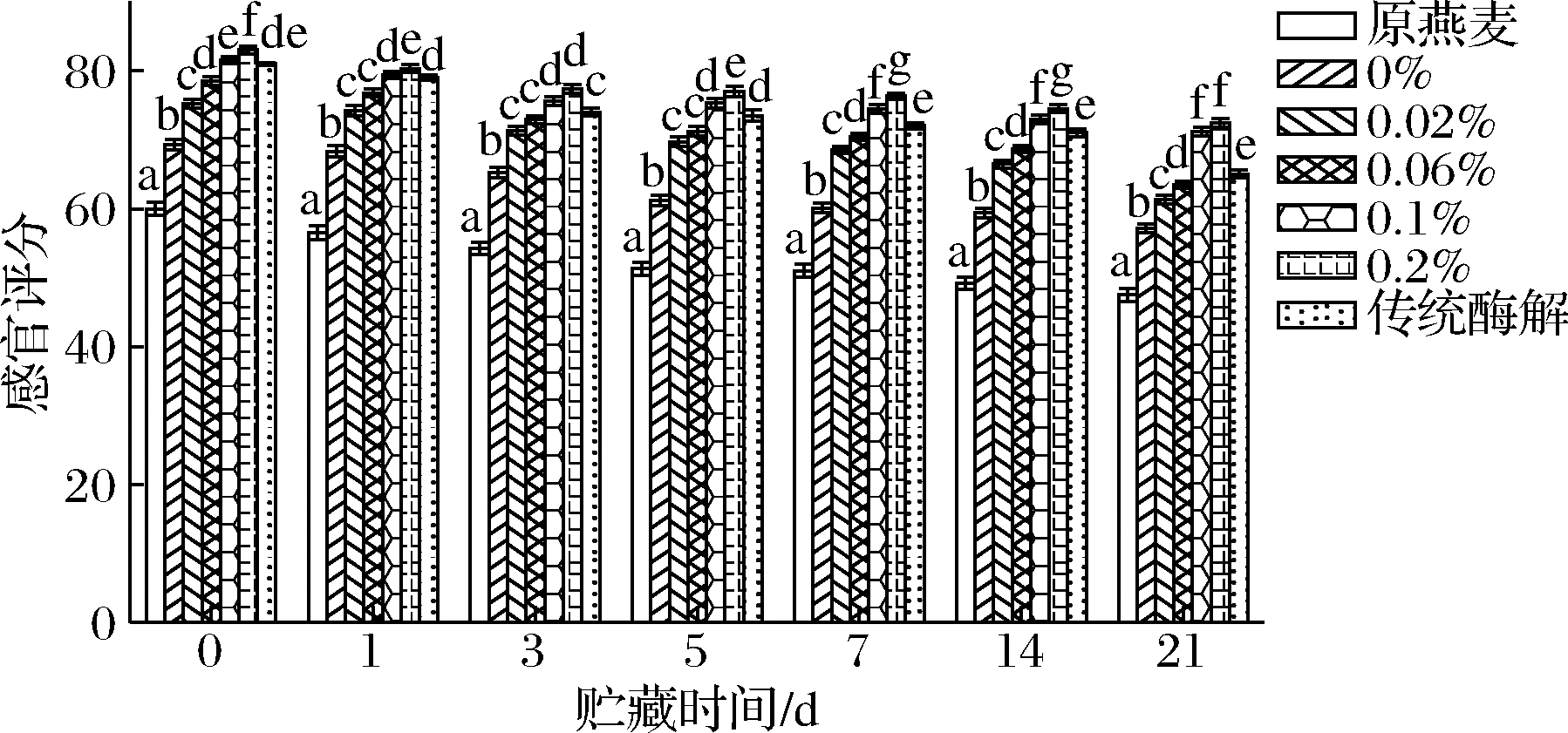
图6 不同燕麦乳在贮藏期内的感官评分
Fig.6 Sensory evaluation of different oat milk during storage period
3 结论
本文探究了加酶挤压对燕麦淀粉表观结构及理化性质的影响,根据处理后燕麦淀粉的性质以及相应的燕麦乳的贮藏稳定性以及感官评分等,确定了其在燕麦乳制备中的可行性。结果表明,加酶挤压处理后,淀粉降解为小分子糊精和低聚糖等,水溶性指数和还原糖含量显著增加,淀粉分子几乎完全糊化,黏度显著减小,表现出更显著的流体特征。本研究可以显著改善由淀粉老化引起的燕麦乳沉淀问题,提高燕麦乳贮藏稳定性,同时提高消费者的感官评价。然而由于酶的作用效果对底物浓度、温度、pH值、作用时间等环境条件依赖性较大,故对加酶挤压条件(挤压机温度、水分含量、螺杆转速、酶添加量等)的优化,将在我们之后的工作中进一步研究,以达到更好的酶解效果,进而提高燕麦乳的品质。
[1] BIEL W,JACYNO E,KAW![]() CKA M.Chemical composition of hulled,dehulled and naked oat grains[J].South African Journal of Animal Science,2014,44(2):189.
CKA M.Chemical composition of hulled,dehulled and naked oat grains[J].South African Journal of Animal Science,2014,44(2):189.
[2] MOHAMED A,BIRESAW G,XU J Y,et al.Oats protein isolate:Thermal,rheological,surface and functional properties[J].Food Research International,2009,42(1):107-114.
[3] RAMZAN S.Oat:A novel therapeutic ingredient for food applications[J].Journal of Microbiology,Biotechnology and Food Sciences,2020,9(4):756-760.
[4] KENDALL C W C,ESFAHANI A,JENKINS D J A.The link between dietary fibre and human health[J].Food Hydrocolloids,2010,24(1):42-48.
[5] 孟凡欢.燕麦品种及成分对燕麦乳稳定性的影响[D].天津:天津科技大学,2017.
MENG F H.Effects of oat varieties and components on the stability of oat milk[D].Tianjin:Tianjin University of Science and Technology,2017.
[6] 侯占群,文剑,吴逸民,等.谷物饮料关键制备技术及其稳定性研究进展[J].食品与发酵工业,2012,38(10):146-150.
HOU Z Q,WEN J,WU Y M,et al.Recent advances in key technologies of cereal beverage[J].Food and Fermentation Industries,2012,38(10):146-150.
[7] 汪丽萍,朱亚婧,冯叙桥,等.酶解工艺对燕麦浆稳定性和糖组分的影响[J].中国粮油学报,2015,30(3):12-18.
WANG L P,ZHU Y J,FENG X Q,et al.Influence of enzymatic hydrolysis processing on the stability and saccharide distribution of oats milk[J].Journal of the Chinese Cereals and Oils Association,2015,30(3):12-18.
[8] 曹盼,朱科学,彭伟,等.酶法制备燕麦浆工艺研究[J].食品工业科技,2012,33(8):309-313.
CAO P,ZHU K X,PENG W,et al.Optimization of enzymatic processing technology of oat milk[J].Science and Technology of Food Industry,2012,33(8):309-313.
[9] QU M,LIU Y J,ZHANG G,et al.Identification and characterization of soybean dreg soluble dietary fibre by combination of extrusion pre-treatment and enzymatic modification[J].Food Quality and Safety,2017,1(2):153-160.
[10] LI Y,JIAO A Q,LI J P,et al.Effect of extrusion pretreatment on the physical and chemical properties of broad bean and its relationship to koji preparation[J].Food Chemistry,2019,286:38-42.
[11] XU E B,CAMPANELLA O H,YE X Q,et al.Advances in conversion of natural biopolymers:A reactive extrusion (REX)-enzyme-combined strategy for starch/protein-based food processing[J].Trends in Food Science &Technology,2020,99:167-180.
[12] ZHAO S N,JIAO A Q,YANG Y Y,et al.Modification of physicochemical properties and degradation of barley flour upon enzymatic extrusion[J].Food Bioscience,2022,45:101243.
[13] 焦爱权,边士超,金征宇.加酶挤压预处理酿造土圞儿黄酒及其品质分析[J].食品与发酵工业,2022.DOI:10.13995/j.cnki.11-1802/ts.032892.
JIAO A Q,BIAN S C,JIN Z Y.Analysis on the quality of Tulou® Rice wine produced by enzymatic extrusion pretreatment[J].Food and Fermentation Industry,2022.DOI:10.13995/j.cnki.11-1802/ts.032892.
[14] BIAN S C,ZHANG R X,LIU Q,et al.Effects of the addition of thermostable α-amylase on the physicochemical and antioxidant properties of extrusion-pretreated Apios fortunei used for yellow wine fermentation[J].LWT,2022,154:112845.
[15] HAGENIMANA A,DING X L,FANG T.Evaluation of rice flour modified by extrusion cooking[J].Journal of Cereal Science,2006,43(1):38-46.
[16] 赵淑娜.加酶挤压对大麦粉理化性质的影响及其在大麦啤酒酿造中的应用[D].无锡:江南大学,2021.
ZHAO S N.Effect of enzymatic extrusion on physicochemical properties of barley and its application in barley beer brewing[D].Wuxi:Jiangnan University,2021.
[17] YANG Y Y,JIAO A Q,LIU Q,et al.Functional and physical properties of naked barley-based unexpanded extrudates:Effects of low temperature[J].International Journal of Food Properties,2020,23(1):1886-1898.
[18] FU X,LIU Q,XU E B,et al.The effect of Vaccinium bracteatum Thunb.leaves addition on antioxidant capacity,physicochemical properties,and in vitro digestibility of rice extrudates[J].Journal of Food Science,2021,86(10):4730-4740.
[19] GUIMAR ES J T,SILVA E K,COSTA A L R,et al.Manufacturing a prebiotic whey beverage exploring the influence of degree of inulin polymerization[J].Food Hydrocolloids,2018,77:787-795.
ES J T,SILVA E K,COSTA A L R,et al.Manufacturing a prebiotic whey beverage exploring the influence of degree of inulin polymerization[J].Food Hydrocolloids,2018,77:787-795.
[20] LAZOU A,KROKIDA M.Functional properties of corn and corn-lentil extrudates[J].Food Research International,2010,43(2):609-616.
[21] XU E B,WU Z Z,LONG J,et al.Effect of thermostable α-amylase addition on the physicochemical properties,free/bound phenolics and antioxidant capacities of extruded hulled and whole rice[J].Food and Bioprocess Technology,2015,8(9):1958-1973.
[22] SARAWONG C,SCHOENLECHNER R,SEKIGUCHI K,et al.Effect of extrusion cooking on the physicochemical properties,resistant starch,phenolic content and antioxidant capacities of green banana flour[J].Food Chemistry,2014,143:33-39.
[23] BRYANT R J,KADAN R S,CHAMPAGNE E T,et al.Functional and digestive characteristics of extruded rice flour[J].Cereal Chemistry,2001,78(2):131-137.
[24] QIAN X J,SUN B H,ZHU C K,et al.Effect of stir-frying on oat milling and pasting properties and rheological properties of oat flour[J].Journal of Cereal Science,2020,92:102908.
[25] HE C X,ZHENG J,LIU F J,et al.Fabrication and characterization of oat flour processed by different methods[J].Journal of Cereal Science,2020,96:103123.
[26] 张晶,张美莉.超高压处理对燕麦淀粉颗粒特性、热特性及流变学特性的影响[J].食品科学,2020,41(23):114-121.
ZHANG J,ZHANG M L.Effect of high hydrostatic pressure treatment on morphological,thermal and rheological properties of oat starch[J].Food Science,2020,41(23):114-121.
 10
10