香橙(Citrus junos Sieb.Ex Tanaka),原产于中国长江流域,具有耐寒性强、易种植、易剥皮等特点,单果重约100~130 g,果肉酸苦涩,不宜鲜食,其类黄酮等功能性成分含量较高、香气独特,可用于加工成高附加值产品。在日本、韩国有商业化种植[1],近年来我国湖南、浙江等地香橙种植量也逐年增多,并引进日本香橙品种[2]。香橙属于药食同源的柑橘品种,据我国《神农本草世界》、《新修本草》以及日本《医心方》中记载,香橙具有很好的药用价值,可以预防感染症、高血压、动脉硬化等疾病,并有改善血液循环、缓解疲劳的功效[3]。此外,香橙的果皮和果肉都具有独特的风味,常被加工成香橙精油、香橙皮粉和果茶等产品,广泛应用于食品、日用化工等领域[4]。
类黄酮是柑橘果实重要的组成部分,部分类黄酮物质(如柚皮苷、新橙皮苷等)除具有苦味等滋味特性外,其抗氧化、抗炎、抗肿瘤等生物活性已被众多研究者所明确[5-6]。为满足食品、日化品和医药行业的需求,不同柑橘类黄酮的种类和含量受到越来越多研究者的关注。柑橘类黄酮种类和含量主要与柑橘的品种和部位有关[7]。张芳芳等[7]在红美人柑橘果皮中检测到橙皮苷、芸香柚皮苷、香蜂草苷、圣草次苷、野漆树苷、枸橘苷、柚皮素、橙皮素8种类黄酮物质,在果肉中检测到橙皮苷、芸香柚皮苷、香蜂草苷3种类黄酮物质,并且果皮中含量(7 580.46 mg/kg)高于果肉含量(1 222.44 mg/kg)。岳超等[8]采用高效液相色谱-紫外检测器对13个柑橘果实类黄酮物质种类和含量进行检测,其中橙皮苷、芸香柚皮苷、川陈皮素、橘皮素在样品中分布含量差别较大。
香气是衡量柑橘果实品质的重要指标之一,不同种类的香橙中含有的不同挥发性物质形成了各自独特的香气,深受消费者的喜爱。TOMIYAMA等[9]采用溶剂辅助蒸馏提取结合GC-MS方法,对香橙、Sudachi酸橘和Kabosu酸橘果皮和果肉中挥发性物质进行检测分析,发现柠檬烯是含量最高的单萜类化合物,其次是香橙和Sudachi酸橘的γ-萜品烯和β-水芹烯,及Kabosu酸橘中的月桂烯。SONG等[10]发现34种萜烯类、37种醇类和16种醛类是冷榨香橙精油中主要的挥发性物质,其中甲基三硫醚(香橙味、涩味、甜味)、莰醇(香橙味、香料味)、辛醇(香橙味、甜味)、(+)-p-薄荷-1-烯-9-醇(香橙味、甜味)、丁子香酚(香橙味)、香芹酚(香橙味、香菜味)、反-2-十一烯醛(香橙味、树脂味)是香橙精油的特征风味物质。此外,(+)-香橙烯是香橙果实中具有代表性特征香味物质,在果肉中含量为0.31 μg/g,在果皮中含量为136.35 μg/g[4]。
目前,香橙中不同部位(果皮和果肉)中类黄酮物质和挥发性风味物质还未进行全面和深入的探究。为了明确香橙中柚皮苷、芸香柚皮苷、橙皮苷、新橙皮苷类、柚皮素、橙皮素6种黄酮物质和挥发性风味物质在果皮和果肉中的分布,本研究拟以日本香橙为研究对象,利用高效液相色谱-二极管阵列(high-performance liquid chromatography-diode array detector,HPLC-DAD)对香橙果皮和果肉中6种黄酮物质进行检测;采用固相微萃取(solid phase micro extraction,SPME)结合GC-MS/脉冲火焰检测器(pulsed flame photometric detector,PFPD)对香橙果皮和果肉中挥发性组分进行定性和定量分析,旨在为我国香橙加工产业发展提供理论依据。
1 材料与方法
1.1 材料与试剂
1.1.1 实验材料
香橙果实样品取自上海崇明日本香橙果园。将香橙样品皮和果肉分离,液氮冷冻后放入粉碎机粉碎成粉末,置于-80 ℃保存备用。
1.1.2 实验试剂
甲醇、乙腈,均为色谱纯,美国Honeywell公司;柚皮苷、芸香柚皮苷、柚皮素、橙皮苷、橙皮素、新橙皮苷,纯度均为98%,上海源叶有限公司;环己酮(纯度99%)、异丙基二硫醚(纯度96%),上海阿拉丁公司。
1.2 仪器与设备
Agilent 1260高效液相色谱系统,G1311B配有四元泵、G1329B自动进样器、G1316A柱温箱、G1315D并串联DAD、Poroshell 120 EC-C18保护柱(4.6 mm×5 mm,2.7 μm粒径填料),Eclipse Plus C18柱(4.6 mm×150 mm,5 μm 粒径填料),Agilent 7890B GC-5977A GC-MS气质联用仪、DB-5色谱柱(30 m×0.25 mm id×0.25 μm),美国安捷伦科技有限公司;0.22 μm有机相微孔滤头,上海安谱科学仪器有限公司;5380 PFPD脉冲火焰光度检测仪,美国OI公司;Milli-Q超纯水系统,德国Merck-Millpore公司;50/30 μm二乙烯基苯/碳分子筛/聚二甲基硅氧烷(divinylbenzene/carboxen/polydimethylsiloxane,DVB/CAR/PDMS)萃取头,美国Supelco公司;DF-101S集热式恒温加热磁力搅拌器,上海力辰科技有限公司。
1.3 实验方法
1.3.1 类黄酮物质的测定
分别取果肉冷冻粉末(1 g)和果皮冷冻粉末(0.5 g),加入纯甲醇,经振荡、超声波处理15 min、4 ℃ 10 000 r/min离心10 min,取上清液,以上提取操作重复3次,将上清液混合,经0.22 μm滤膜过滤,待测。
色谱条件:流动相包括A相0.05%乙酸水溶液、B相甲醇、C相乙腈;采用梯度洗脱(如表1所示);DAD检测器扫描范围为210~450 nm,检测波长为285 nm;其他设置参数包括柱温30 ℃、流速1 mL/min、进样量10 μL。采用HPLC-DAD对香橙果肉和果皮粉末中柚皮苷、芸香柚皮苷、橙皮苷、新橙皮苷类、柚皮素、橙皮素进行检测。
表1 流动相洗脱程序
Table 1 Gradient elution program

时间/minA相/%B相/%C相/%08551057510151568171525454015305801535580154085510
1.3.2 挥发性物质的测定
参考文献[11]的方法,略有修改:将2 g果肉粉末、0.05 g果皮粉末分别置于含有磁子的20 mL顶空瓶中,加入饱和NaCl溶液5 mL,2.5 μL(9.423 mg/mL)的内标环己酮和1.5 μL(0.943 mg/mL)的异丙基二硫醚,混匀后采用聚四氟乙烯材质的隔垫密封。将顶空瓶置于40 ℃水浴中平衡20 min,固相微萃取头插入顶空瓶中,萃取挥发性物质30 min。
GC-MS/PFPD测定条件:将备好的萃取头置于GC进样口200 ℃解析5 min,挥发性组分在色谱柱上进行分离后进入MS和PFPD检测器进行测定。柱温设置程序:初始温度35 ℃,保持6 min,7 ℃/min升至203 ℃,保持10 min。载气为氦气,流速1.5 mL/min。EI离子源的电子能量70 eV,传输线温度280 ℃。m/z扫描范围为33~500 amu。PFPD检测器温度250 ℃,PMT电压498 V,载气和燃气分别为氦气、空气和氢气。每个样品重复3次。
1.3.3 类黄酮物质的定性和定量分析
采用匹配目标峰与标品峰的紫外吸收光谱、色谱峰保留时间进行定性分析。
精确称取柚皮苷、芸香柚皮苷、橙皮苷、新橙皮苷类、柚皮素、橙皮素标准物质各10 mg,分别采用甲醇溶液溶解,定容至10 mL,配制成1.0 mg/mL的标准品母液备用。随后采用逐级稀释方法建立外标曲线,计算线性回归方程和相关系数(R2)。精确配制混合标准样品试样,通过计算测定浓度与配制浓度的相对误差表示精密度。采用加标回收的方法计算目标类黄酮物质的回收率。
1.3.4 挥发性物质的定性和定量分析
参考文献[11]和[12]中的方法。
定性分析:通过正构烷烃C5-C20进行挥发性组分的线性保留指数(linear retention index,LRI),并与已发表文献中的LRI进行匹配,柚汁中的挥发性非硫组分的定性也可通过匹配NIST11、W10N14库中MS总离子流,挥发性硫组分也通过硫检测器(PFPD)进行定性。
定量分析:挥发性非硫组分的定量主要通过内标环己酮进行,而挥发性硫组分的定量主要通过内标甲基乙基硫醚进行。计算如公式(1)所示:
c待![]()
(1)
式中:c待,待测的挥发性组分的质量浓度,μg/mL;A待,待测的挥发性组分的峰面积;c,内标质量浓度,μg/mL;A内标,内标组分在MS或PFPD上的峰面积。
1.3.5 气味活性值(odor activity value,OAV)计算
OAV是挥发性物质的浓度与感官阈值的比值,通常当OAV≥1时,表明该挥发性物质对整体风味呈现具有贡献。
1.3.6 数据处理
采用SPSS 25.0对数据进行方差分析(analysis of variance,ANOVA)和Duncan多重检验;采用化学工作站F.01.01.2317对挥发性组分进行定性分析;采用Origin 7.5绘图。
2 结果与分析
2.1 香橙中类黄酮物质的色谱特征和定性定量分析
如图1所示,芸香柚皮苷的紫外最大吸收波长为283 nm,柚皮苷、橙皮苷、新橙皮苷的紫外最大吸收波长为284 nm,柚皮素和橙皮素的紫外最大吸收波长分别为290和288 nm。因此,在本研究中,选取285 nm作为测定波长。

图1 类黄酮标准物质紫外吸收光谱
Fig.1 UV absorption spectra of flavonoid standards
HPLC-DAD对香橙中6种类黄酮物质进行检测,结果如图2所示。目标类黄酮物质在香橙不同部位分布相同,其中芸香柚皮苷、柚皮苷、橙皮苷、新橙皮苷4种物质在果肉和果皮中可以检测到,柚皮素和橙皮素并未被检测到。通过外标曲线对香橙果肉和果皮中检测到的4种类黄酮物质进行定量分析,外标曲线线性方程的相关系数R2范围在0.999 4~0.999 9,且测定浓度与配制浓度之间的相对误差范围在-1.4%~0.9%,4种类黄酮的回收率范围在96.2%~100.4%,满足实验精密度和回收率要求。如表2所示,果肉和果皮中目标类黄酮物质含量分别为(794.6±1.76)、(3 085.42±87.84) μg/g,其中果皮中4种目标类黄酮物质含量约为果肉中1.95~7.19倍。
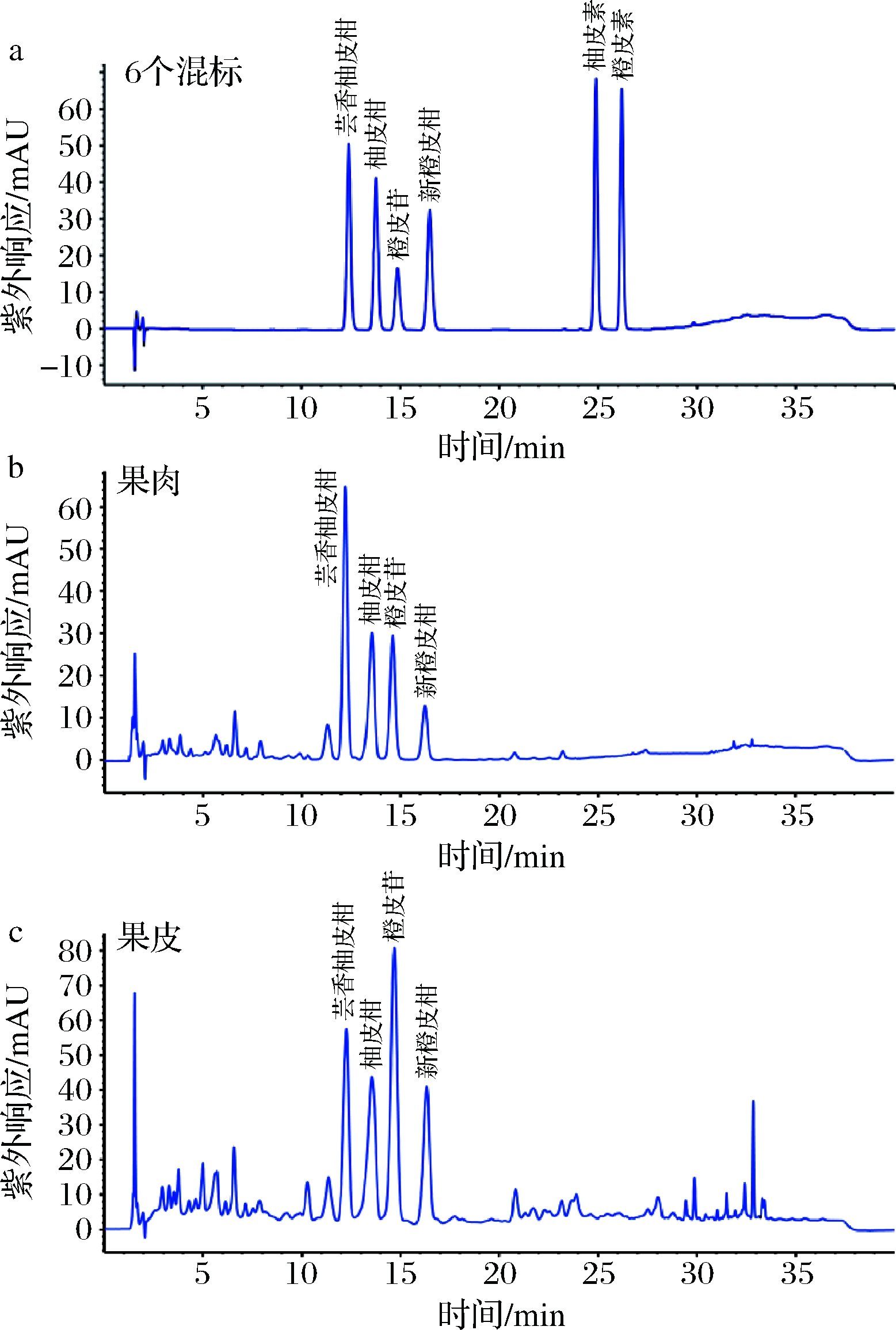
a-混标;b-果肉;c-果皮
图2 日本香橙果肉和果皮中6种黄酮类物质测定
Fig.2 Concentration of six flavonoids in pulp and peel of yuzu
表2 日本香橙果肉和果皮中4种类黄酮类物质含量
Table 2 Concentration of four flavonoids in pulp and peel of yuzu
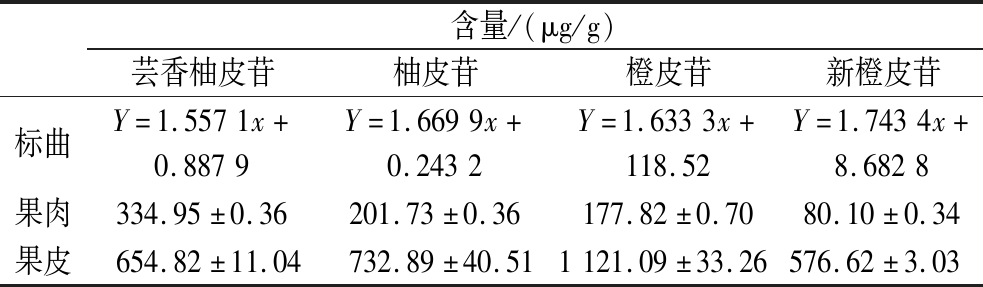
含量/(μg/g)芸香柚皮苷柚皮苷橙皮苷新橙皮苷标曲Y=1.5571x+0.8879Y=1.6699x+0.2432Y=1.6333x+118.52Y=1.7434x+8.6828果肉334.95±0.36201.73±0.36177.82±0.7080.10±0.34果皮654.82±11.04732.89±40.511121.09±33.26576.62±3.03
2.2 香橙中挥发性风味物质的定性和定量分析
2.2.1 香橙中挥发性风味物质的定性分析
采用SPME结合GC-MS/PFPD方法对香橙果肉和果皮中的挥发性化合物进行萃取、浓缩和检测,其中MS是主要检测器,对大多数挥发性化合物都可以进行检测(图3);PFPD是硫检测器,对香橙果实中挥发性硫化合物(volatile sulfur compounds,VSCs)进行检测(图4)。
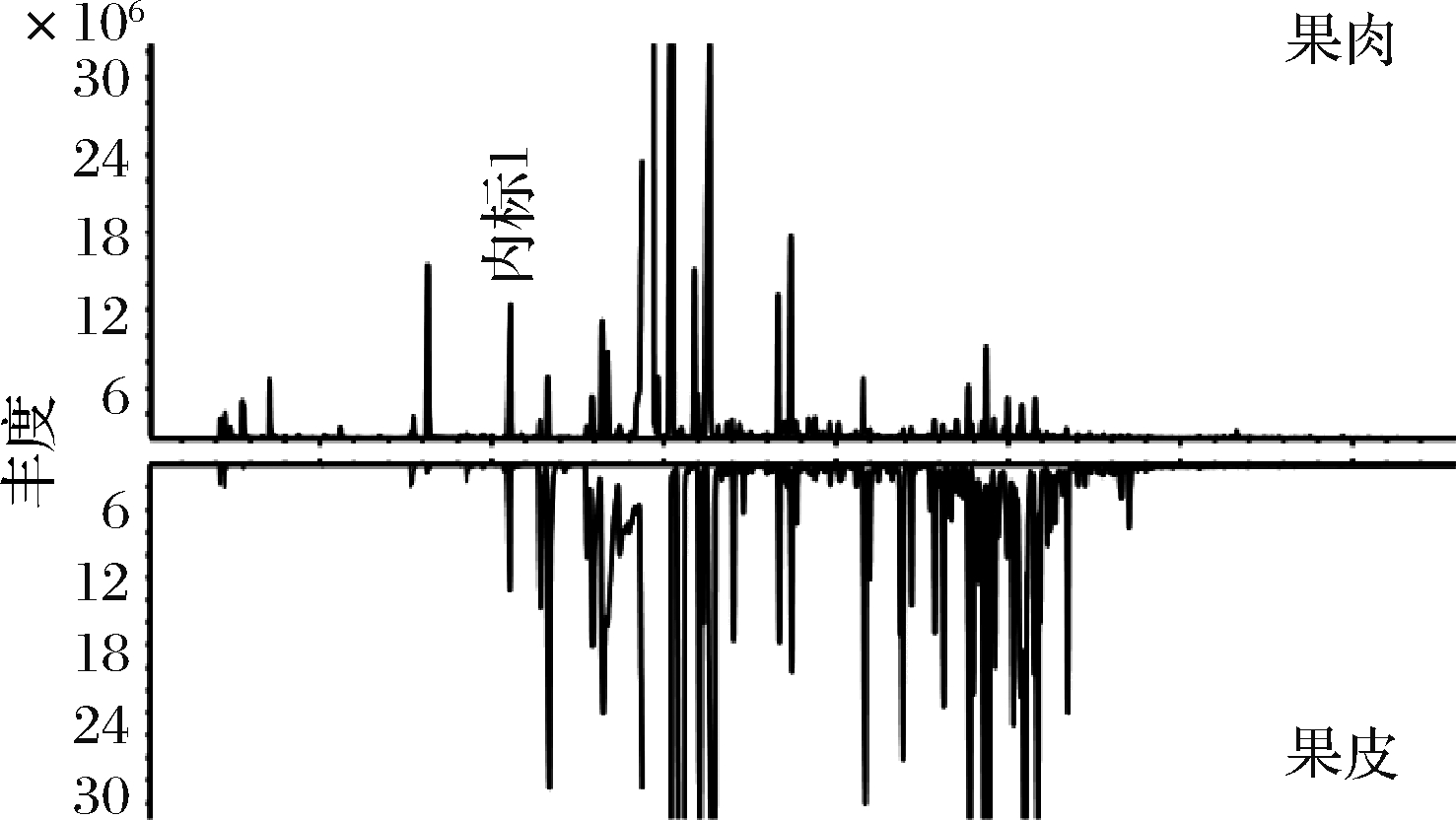
图3 采用 GC-MS对日本香橙果肉和果皮中挥发性物质检测色谱图
Fig.3 Chromatography of volatile compounds in pulp and peel of yuzu by GC-MS
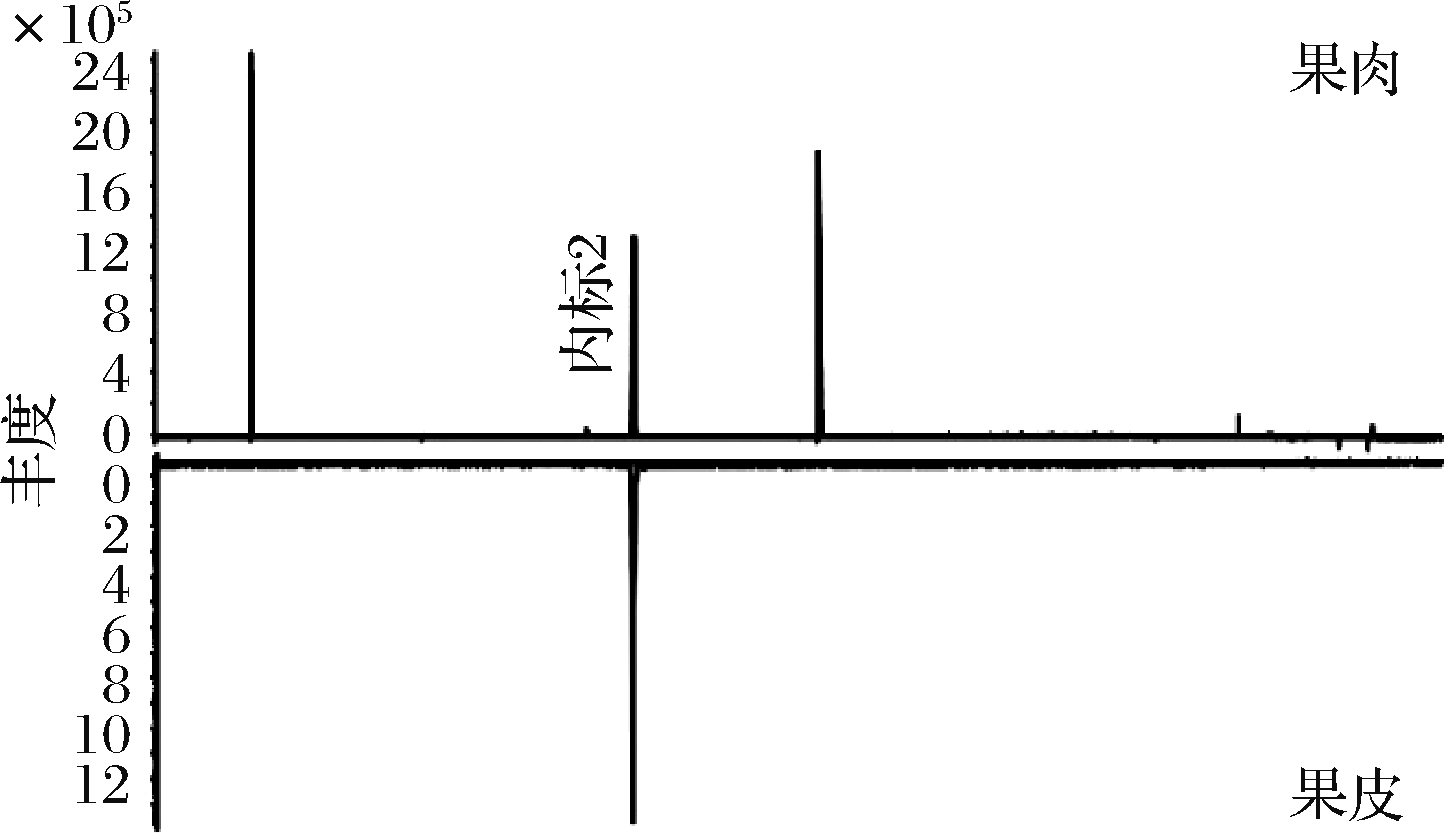
图4 采用GC-PFPD对日本香橙果肉和果皮中挥发性物质检测色谱图
Fig.4 Chromatography of volatile compounds in pulp and peel of yuzu by GC-PFPD
如表3所示,香橙果实中共鉴定出69种挥发性化合物,萜烯类(35种)是种类最多的挥发性物质,其次是酯类(10种)、醇类(7种)、醛类(7种)、酮类(3种)、其他类(3种)、酚类(2种)和VSCs(2种),其中仅挥发性硫化物在PFPD检测器上检测到,其他挥发性非硫化合物均在MS检测器检测到。香橙不同部位(果肉和果皮),挥发性化合物种类不同,分别检测到60种和57种挥发性物质,其中6种萜烯类物质[α-古芸烯、β-橄榄烯、香树烯、γ-衣兰油烯、大牛儿烯D、3,7(11)-蛇床而烯]、2种醛类物质[(Z)-癸-2-烯醛、十二醛]、1种酯类(辛酸甲酯)仅在香橙果皮中检测到;6种萜烯类物质[罗勒烯、(-)-异丁香烯、双环大牛儿烯、(+)-喇叭烯、α-依兰烯、菖蒲烯]、3种酯类(乙酸异戊酯、乙酸异戊二烯酯、巴豆酸丁酯)、2种挥发性硫化物(二硫化碳、苯并噻唑)、1种醇类(1-丁醇)仅在香橙果肉中检测到,其中,具有特殊气味属性和低感官阈值的二硫化碳(试剂味,介质为空气的感官阈值0.21 mg/L)[13]和苯并噻唑(汽油味,介质为水的感官阈值0.08 mg/L)[14]首次在香橙中检测到。
表3 日本香橙果肉和果皮中挥发性组分的定性和定量分析
Table 3 Identification and quantitative analysis of volatile compounds in pulp and peel of yuzu
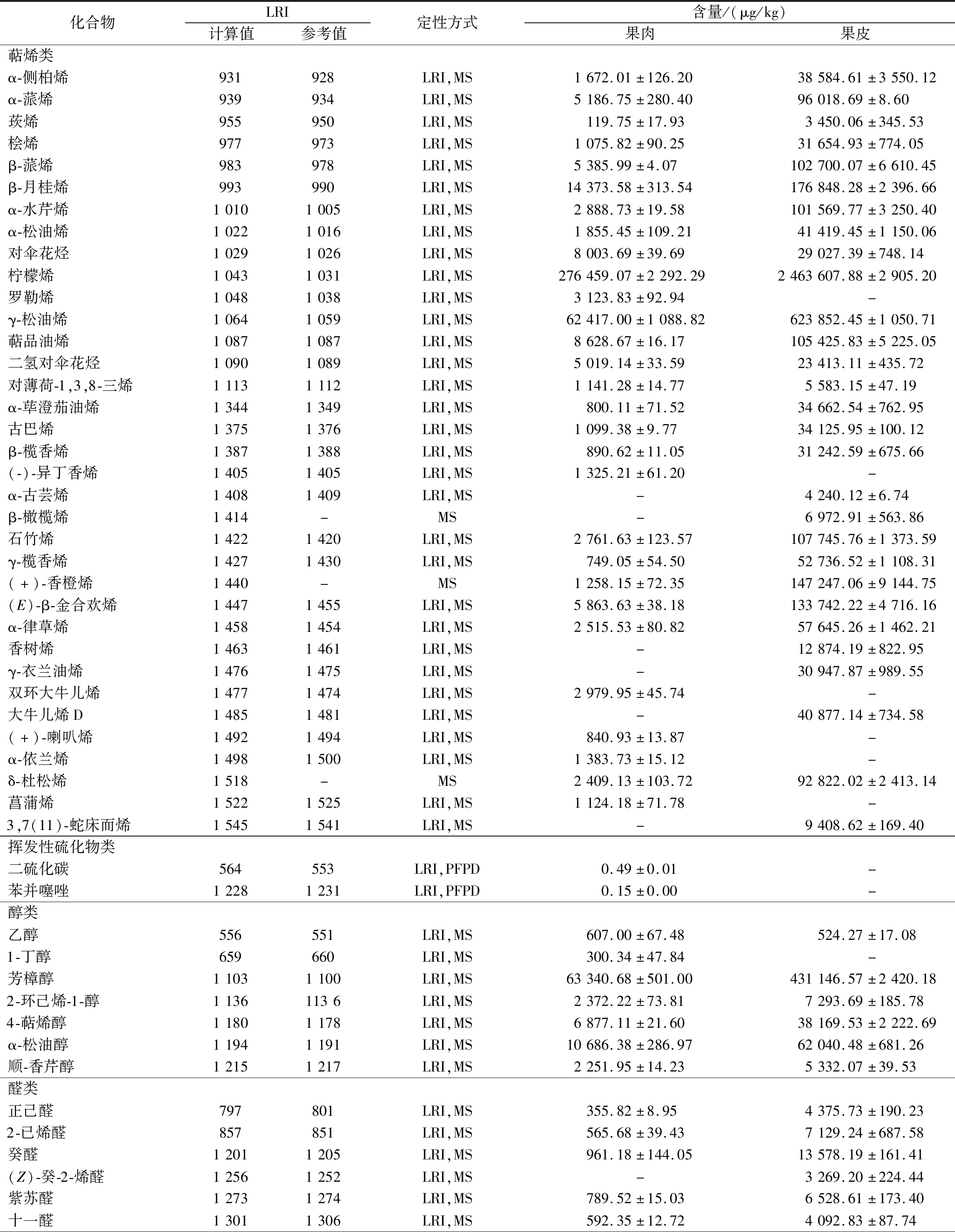
化合物LRI计算值参考值定性方式含量/(μg/kg)果肉果皮萜烯类α-侧柏烯931928LRI,MS1672.01±126.2038584.61±3550.12α-蒎烯939934LRI,MS5186.75±280.4096018.69±8.60莰烯955950LRI,MS119.75±17.933450.06±345.53桧烯977973LRI,MS1075.82±90.2531654.93±774.05β-蒎烯983978LRI,MS5385.99±4.07102700.07±6610.45β-月桂烯993990LRI,MS14373.58±313.54176848.28±2396.66α-水芹烯10101005LRI,MS2888.73±19.58101569.77±3250.40α-松油烯10221016LRI,MS1855.45±109.2141419.45±1150.06对伞花烃10291026LRI,MS8003.69±39.6929027.39±748.14柠檬烯10431031LRI,MS276459.07±2292.292463607.88±2905.20罗勒烯10481038LRI,MS3123.83±92.94-γ-松油烯10641059LRI,MS62417.00±1088.82623852.45±1050.71萜品油烯10871087LRI,MS8628.67±16.17105425.83±5225.05二氢对伞花烃10901089LRI,MS5019.14±33.5923413.11±435.72对薄荷-1,3,8-三烯11131112LRI,MS1141.28±14.775583.15±47.19α-荜澄茄油烯13441349LRI,MS800.11±71.5234662.54±762.95古巴烯13751376LRI,MS1099.38±9.7734125.95±100.12β-榄香烯13871388LRI,MS890.62±11.0531242.59±675.66(-)-异丁香烯14051405LRI,MS1325.21±61.20-α-古芸烯14081409LRI,MS-4240.12±6.74β-橄榄烯1414-MS-6972.91±563.86石竹烯14221420LRI,MS2761.63±123.57107745.76±1373.59γ-榄香烯14271430LRI,MS749.05±54.5052736.52±1108.31(+)-香橙烯1440-MS1258.15±72.35147247.06±9144.75(E)-β-金合欢烯14471455LRI,MS5863.63±38.18133742.22±4716.16α-律草烯14581454LRI,MS2515.53±80.8257645.26±1462.21香树烯14631461LRI,MS-12874.19±822.95γ-衣兰油烯14761475LRI,MS-30947.87±989.55双环大牛儿烯14771474LRI,MS2979.95±45.74-大牛儿烯D14851481LRI,MS-40877.14±734.58(+)-喇叭烯14921494LRI,MS840.93±13.87-α-依兰烯14981500LRI,MS1383.73±15.12-δ-杜松烯1518-MS2409.13±103.7292822.02±2413.14菖蒲烯15221525LRI,MS1124.18±71.78-3,7(11)-蛇床而烯15451541LRI,MS-9408.62±169.40挥发性硫化物类二硫化碳564553LRI,PFPD0.49±0.01-苯并噻唑12281231LRI,PFPD0.15±0.00-醇类乙醇556551LRI,MS607.00±67.48524.27±17.081-丁醇659660LRI,MS300.34±47.84-芳樟醇11031100LRI,MS63340.68±501.00431146.57±2420.182-环己烯-1-醇11361136LRI,MS2372.22±73.817293.69±185.784-萜烯醇11801178LRI,MS6877.11±21.6038169.53±2222.69α-松油醇11941191LRI,MS10686.38±286.9762040.48±681.26顺-香芹醇12151217LRI,MS2251.95±14.235332.07±39.53醛类正己醛797801LRI,MS355.82±8.954375.73±190.232-已烯醛857851LRI,MS565.68±39.437129.24±687.58癸醛12011205LRI,MS961.18±144.0513578.19±161.41(Z)-癸-2-烯醛12561252LRI,MS-3269.20±224.44紫苏醛12731274LRI,MS789.52±15.036528.61±173.40十一醛13011306LRI,MS592.35±12.724092.83±87.74
续表3
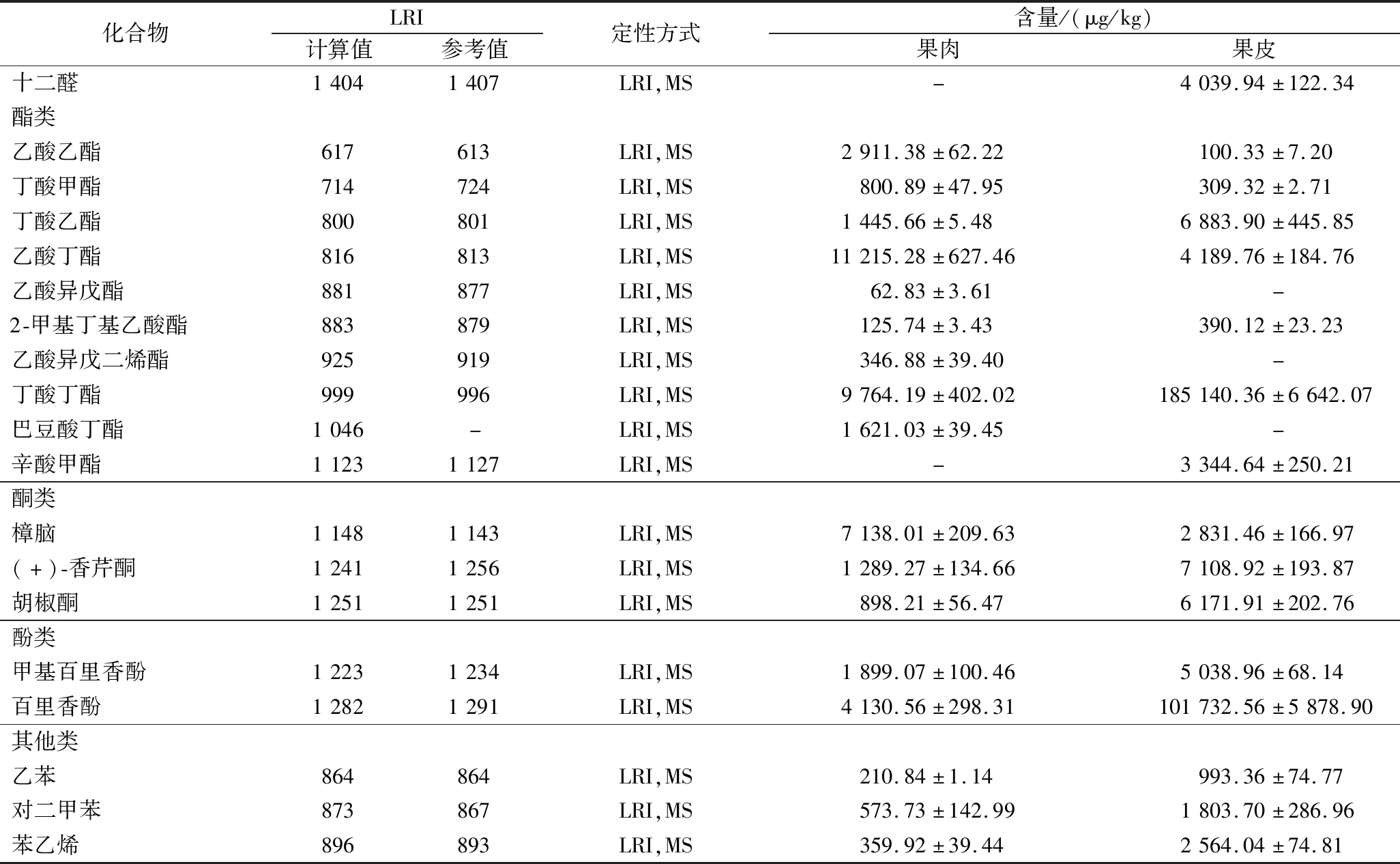
化合物LRI计算值参考值定性方式含量/(μg/kg)果肉果皮十二醛14041407LRI,MS-4039.94±122.34酯类乙酸乙酯617613LRI,MS2911.38±62.22100.33±7.20丁酸甲酯714724LRI,MS800.89±47.95309.32±2.71丁酸乙酯800801LRI,MS1445.66±5.486883.90±445.85乙酸丁酯816813LRI,MS11215.28±627.464189.76±184.76乙酸异戊酯881877LRI,MS62.83±3.61-2-甲基丁基乙酸酯883879LRI,MS125.74±3.43390.12±23.23乙酸异戊二烯酯925919LRI,MS346.88±39.40-丁酸丁酯999996LRI,MS9764.19±402.02185140.36±6642.07巴豆酸丁酯1046-LRI,MS1621.03±39.45-辛酸甲酯11231127LRI,MS-3344.64±250.21酮类樟脑11481143LRI,MS7138.01±209.632831.46±166.97(+)-香芹酮12411256LRI,MS1289.27±134.667108.92±193.87胡椒酮12511251LRI,MS898.21±56.476171.91±202.76酚类甲基百里香酚12231234LRI,MS1899.07±100.465038.96±68.14百里香酚12821291LRI,MS4130.56±298.31101732.56±5878.90其他类乙苯864864LRI,MS210.84±1.14993.36±74.77对二甲苯873867LRI,MS573.73±142.991803.70±286.96苯乙烯896893LRI,MS359.92±39.442564.04±74.81
注:图表中“-”表示未被检测出。
2.2.2 香橙中挥发性风味物质的定量分析
如表3和图5所示,香橙果肉和果皮中挥发性物质含量呈现显著不同(P<0.05),其中果肉中挥发性组分含量为(557 846.35±8 759.88) μg/kg,是由75.89%的萜烯类、15.49%的醇类、5.07%的酯类、1.67%酮类、1.08%酚类、0.59%醛类、0.21%其他类和0.000 11%的VSCs共同组成;果皮中挥发性物质总含量为(5 556 570.13±75 258.72) μg/kg,是由83.51%的萜烯类、9.80%的醇类、3.61%的酯类、1.92%酚类、0.77%醛类、0.29%酮类和0.10%其他类共同组成。此外,柠檬烯(44.34%)、γ-松油烯(11.23%)、芳樟醇(7.76%)、丁酸丁酯(3.33%)、β-月桂烯(3.18%)、(+)-香橙烯(2.65%)、(E)-β-金合欢烯(2.41%)、石竹烯(1.94%)、萜品油烯(1.90%)、β-蒎烯(1.85%)和百里香酚(1.83%)11种挥发性物质含量占果皮挥发性物质含量的82.42%,是果皮中主要的挥发性物质。柠檬烯(49.56%)、芳樟醇(11.35%)、γ-松油烯(11.19%)、β-月桂烯(2.58%)、乙酸丁酯(2.01%)、α-松油醇(1.92%)、丁酸丁酯(1.75%)和萜品油烯(1.55%)8种挥发性物质含量占果肉挥发性物质含量的81.91%,是果肉中主要的挥发性物质;其中,柠檬烯是香橙果实中含量最高的挥发性物质,这与前期研究结果一致[9,15]。除了香橙果汁中主要的挥发性化合物外,低浓度VSCs对柑橘果实风味的呈现具有重要影响。VSCs具有感官阈值低、化学性质活泼的特点,在柑橘果实中常以极低的浓度存在,常采用PFPD检测器进行检测。虽然前期文献报道,在香橙精油中检测到二甲基三硫醚、1-对孟烯-8-硫醇、4-巯基-4-甲基-2-戊酮、薄荷硫化物[15],而在本研究中,仅在香橙果肉中检测出二硫化碳和苯并噻唑两种VSCs,含量分别为(0.49±0.01)、(0.15±0.00) μg/kg。
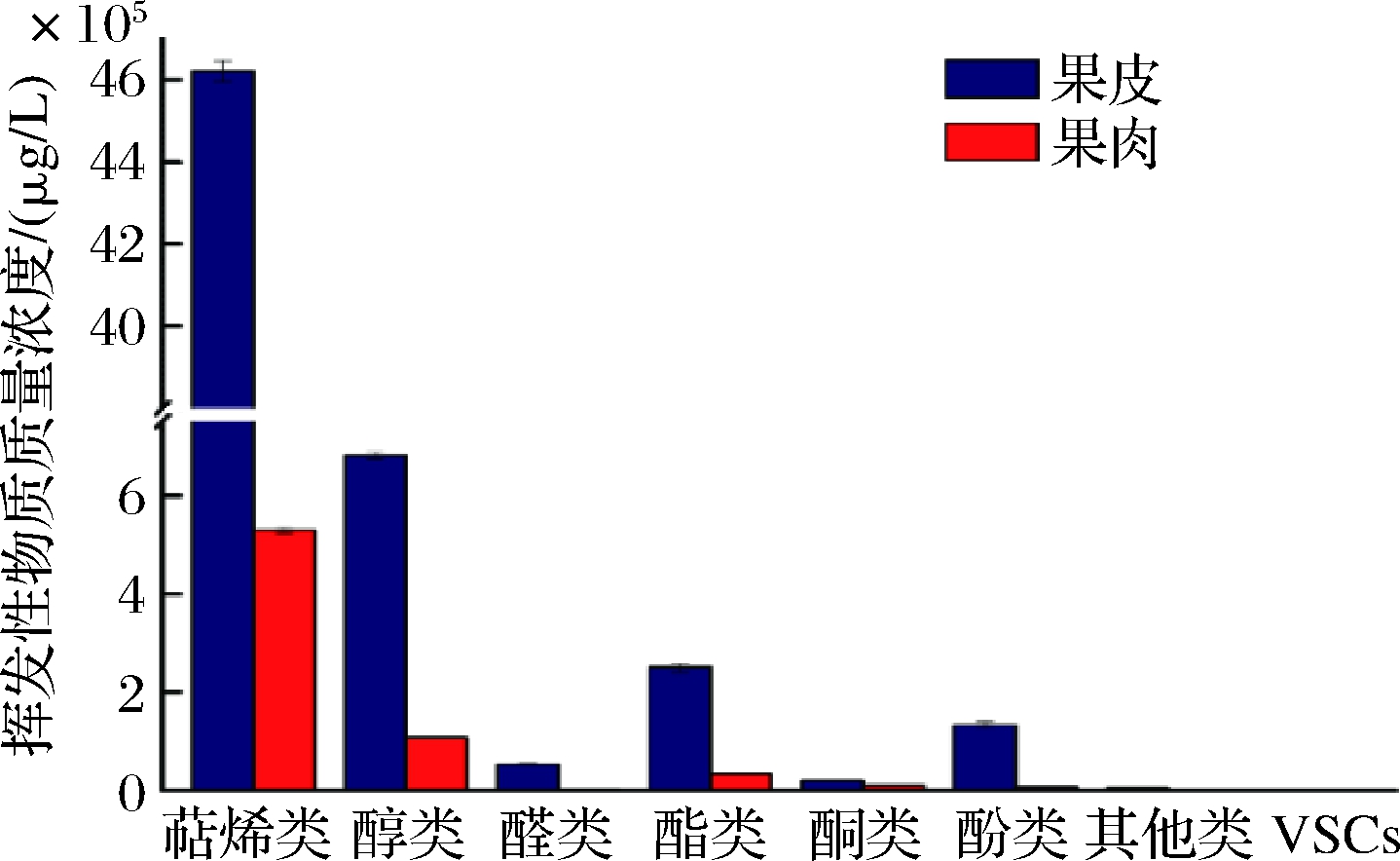
图5 日本香橙果肉和果皮中各类挥发性组分浓度
Fig.5 Concentration of volatile compounds in pulp and peel of yuzu
2.2.3 香橙中果肉和果皮中风味活性成分分析
通过计算各个挥发性物质的OAV,明确香橙果肉和果皮中的特征风味物质对香橙风味呈现的贡献度,结果如表4所示。
表4 香橙果肉和果皮中挥发性物质的OAV
Table 4 The OAV of volatile compounds in pulp and peel of yuzu
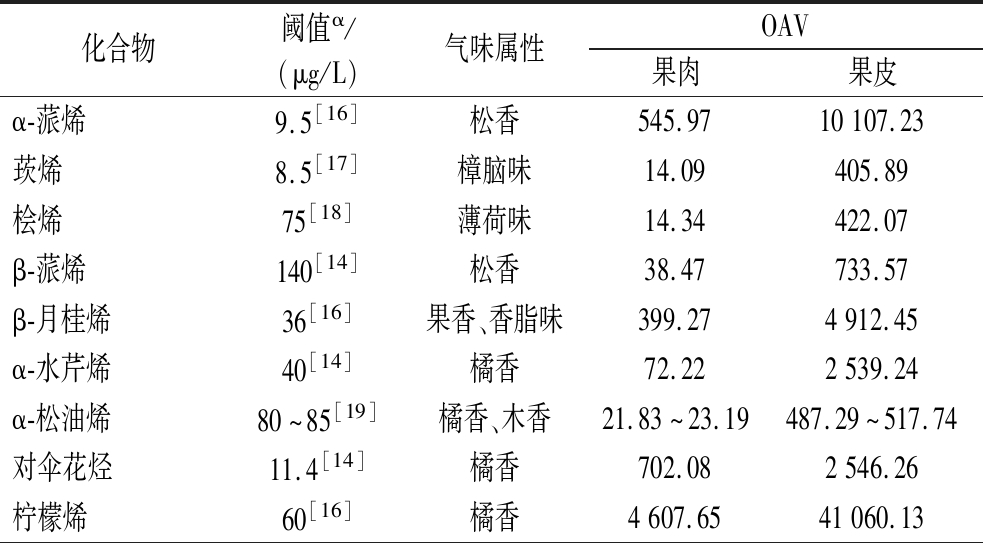
化合物阈值α/(μg/L)气味属性OAV果肉果皮α-蒎烯9.5[16]松香545.9710107.23莰烯8.5[17]樟脑味14.09405.89桧烯75[18]薄荷味14.34422.07β-蒎烯140[14]松香38.47733.57β-月桂烯36[16]果香、香脂味399.274912.45α-水芹烯40[14]橘香72.222539.24α-松油烯80~85[19]橘香、木香21.83~23.19487.29~517.74对伞花烃11.4[14]橘香702.082546.26柠檬烯60[16]橘香4607.6541060.13
续表4
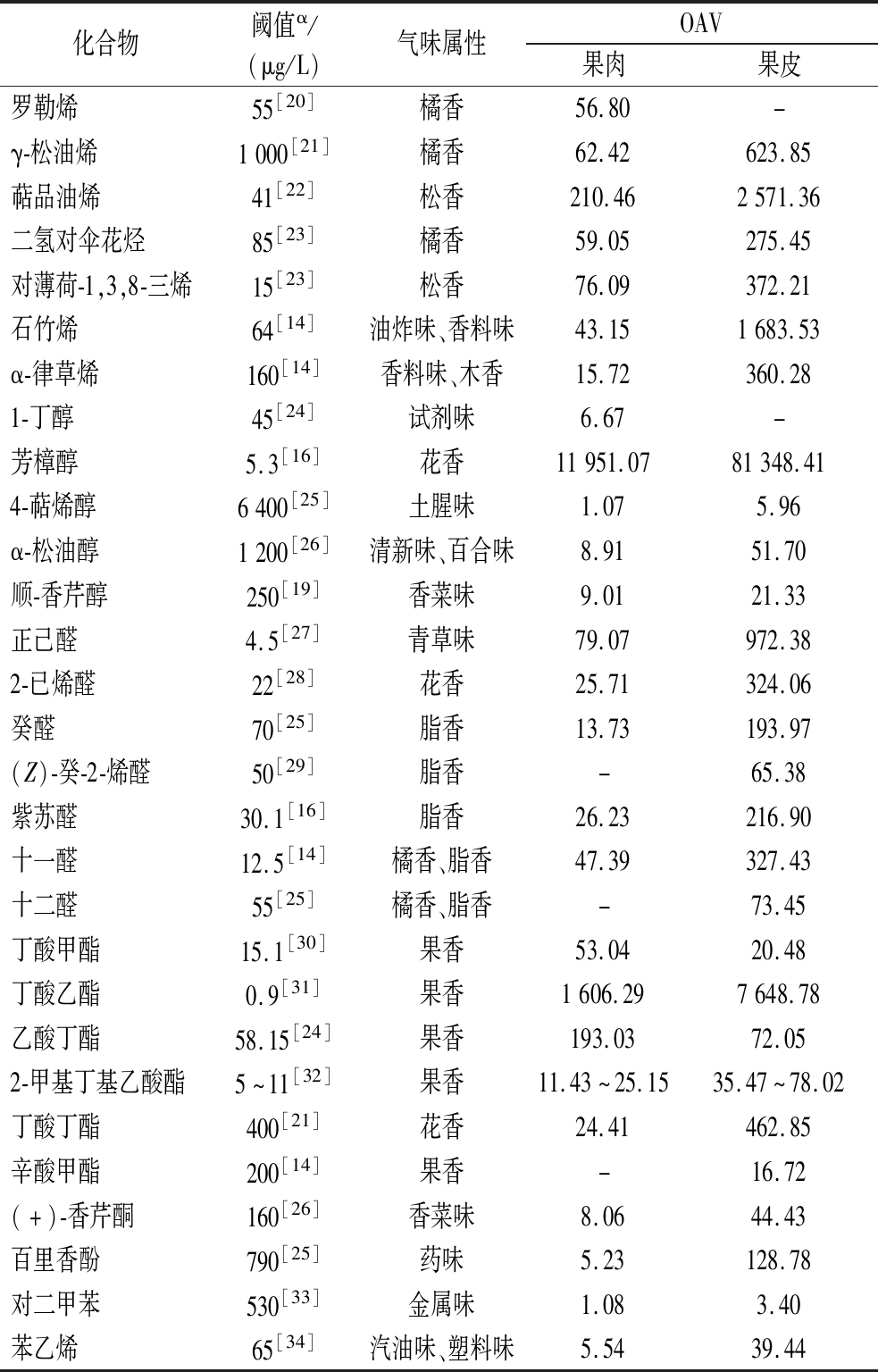
化合物阈值α/(μg/L)气味属性OAV果肉果皮罗勒烯55[20]橘香56.80-γ-松油烯1000[21]橘香62.42623.85萜品油烯41[22]松香210.462571.36二氢对伞花烃85[23]橘香59.05275.45对薄荷-1,3,8-三烯15[23]松香76.09372.21石竹烯64[14]油炸味、香料味43.151683.53α-律草烯160[14]香料味、木香15.72360.281-丁醇45[24]试剂味6.67-芳樟醇5.3[16]花香11951.0781348.414-萜烯醇6400[25]土腥味1.075.96α-松油醇1200[26]清新味、百合味8.9151.70顺-香芹醇250[19]香菜味9.0121.33正己醛4.5[27]青草味79.07972.382-已烯醛22[28]花香25.71324.06癸醛70[25]脂香13.73193.97(Z)-癸-2-烯醛50[29]脂香-65.38紫苏醛30.1[16]脂香26.23216.90十一醛12.5[14]橘香、脂香47.39327.43十二醛55[25]橘香、脂香-73.45丁酸甲酯15.1[30]果香53.0420.48丁酸乙酯0.9[31]果香1606.297648.78乙酸丁酯58.15[24]果香193.0372.052-甲基丁基乙酸酯5~11[32]果香11.43~25.1535.47~78.02丁酸丁酯400[21]花香24.41462.85辛酸甲酯200[14]果香-16.72(+)-香芹酮160[26]香菜味8.0644.43百里香酚790[25]药味5.23128.78对二甲苯530[33]金属味1.083.40苯乙烯65[34]汽油味、塑料味5.5439.44
注:-代表化合物并未被检测到;α气味感官阈值介质是水。
在果肉和果皮中分别检测到35种和36种气味活性物质。具有花香的芳樟醇(OAV=11 951.07)、橘香的柠檬烯(OAV=4 607.65)、果香的丁酸乙酯(OAV=1 606.29)、橘香的对伞花烃(OAV=702.08)、松香的α-蒎烯(OAV=545.97)、果香和香脂味的β-月桂烯(OAV=399.27)、松香的萜品油烯(OAV=210.46)和果香的乙酸丁酯(OAV=193.03)是果肉中OAV>100的重要特征风味组分。具有花香的芳樟醇(OAV=81 348.41)、橘香的柠檬烯(OAV=41 060.13)、松香的α-蒎烯(OAV=10 107.23)、果香和香脂味的β-月桂烯(OAV=4 912.45)、萜品油烯(OAV=2 571.36)、橘香的对伞花烃(OAV=2 546.26)、橘香的α-水芹烯(OAV=2 539.24)、油炸味、香料味的石竹烯(OAV=1 683.53)、果香的丁酸乙酯(OAV=7 648.78)是果皮中OAV>1 000的重要特征风味组分。其中,OAV最大的芳樟醇是香橙中最具风味活性的物质。
3 结论
采用HPLC-DAD和GC-MS/PFPD分别对香橙果肉和果皮中的6种类黄酮物质(芸香柚皮苷、柚皮苷、橙皮苷、新橙皮苷、柚皮素、橙皮素)和挥发性化合物进行测定。香橙果肉和果皮中检测出芸香柚皮苷、柚皮苷、橙皮苷和新橙皮苷4种类黄酮物质,总类黄酮物质含量分别为(794.6±1.76)、(3 085.42±87.84) μg/g,且果皮中4种类黄酮物质含量均高于果肉中含量。在香橙果实中共检测到69种挥发性化合物,其中二硫化碳和苯并噻唑是首次在香橙果实中检测到。香橙果肉和果皮中的挥发性化合物含量不同,分别为(557 846.35±8 759.88)、(5 556 570.13±75 258.72) μg/kg,其中柠檬烯、γ-松油烯、芳樟醇、丁酸丁酯、β-月桂烯、(+)-香橙烯、(E)-β-金合欢烯、石竹烯、萜品油烯、β-蒎烯和百里香酚是香橙果皮中的主要挥发性物质;柠檬烯、芳樟醇、γ-松油烯、β-月桂烯、乙酸丁酯、α-松油烯、丁酸丁酯和萜品油烯是香橙果肉中的主要挥发性物质。芳樟醇(花香)、柠檬烯(橘香)、丁酸乙酯(果香)、对伞花烃(橘香)、α-蒎烯(松香)、β-月桂烯(果香和香脂味)、萜品油烯(松香)和乙酸丁酯(果香)是果肉中OAV>100的重要特征风味组分;芳樟醇(花香)、柠檬烯(橘香)、α-蒎烯(松香)、β-月桂烯(果香和香脂味)、对伞花烃(橘香)、α-水芹烯(橘香)、石竹烯(油炸味、香料味)、丁酸乙酯(果香)是果皮中OAV>1 000的重要特征风味组分;芳樟醇是香橙中最具有风味活性的物质。此外,通过HPLC-DAD和GC-MS/PFPD结合使用,对香橙中6种重要类黄酮物质和挥发性物质进行全面检测,为香橙加工生产提供了重要的理论指导意义。
[1] 樊明耀,刘伟伟,赵四清.常山县香橙芳香产业发展初探[J].浙江柑橘,2020,37(3):2-4.
FAN M Y,LIU W W,ZHAO S Q.Preliminary study on the development of yuzu aroma industry in Changshan[J].Zhejiang Ganju,2020,37(3):2-4.
[2] 杨波,刘春荣,毕旭灿,等.常山县培育香橙产业的前景及对策分析[J].中国果业信息,2021,38(2):26-28;54.
YANG B,LIU C R,BI X C,et al.Prospect and countermeasure analysis of cultivating yuzu industry in Changshan[J].China Fruit News,2021,38(2):26-28;54.
[3] 程绍南.香橙的特征香气、营养成分及其保健功能[J].中国果业信息,2014,31(12):70-73.
CHENG S N.Characteristic aroma,nutrient composition and health care function of yuzu[J].China Fruit News,2014,31(12):70-73.
[4] 赵四清,段文宜,刘意隆,等.香橙果实挥发性物质检测及分析[J].中国南方果树,2021,50(2):48-52.
ZHAO S Q,DUAN W Y,LIU Y L,et al.Detection and analysis of volatile compounds in yuzu fruit[J].South China Fruits,2021,50(2):48-52.
[5] 姚周麟,吴韶辉,平新亮,等.常山胡柚中类黄酮等功能性成分的功效和开发进展[J].浙江柑橘,2021,38(4):2-6.
YAO Z L,WU S H,PING X L,et al.Efficacy and development progress of functional components such as flavonoids in Citrus changshanensis[J].Zhejiang Ganju,2021,38(4):2-6.
[6] 朱泰霖.不同品种柑橘果实的类黄酮分离纯化及相关活性研究[D].杭州:浙江大学,2021.
ZHU T L.Separation and purification of flavonoids from citrus fruits of different varieties and related activities[D].Hangzhou:Zhejiang University,2021.
[7] 张芳芳,张今君,夏慧丽,等.高效液相色谱法同时测定红美人柑橘不同组织中12种类黄酮化合物[J].食品安全质量检测学报,2022,13(7):2267-2273.
ZHANG F F,ZHANG J J,XIA H L,et al.Simultaneous determination of 12 kinds of flavonoids in different parts of ‘Hongmeiren’ citrus by high performance liquid chromatography[J].Journal of Food Safety &Quality,2022,13(7):2267-2273.
[8] 岳超,赵维良,郭增喜,等.高效液相色谱法同时测定不同来源柑橘幼果中10种类黄酮化合物和香豆素类化合物[J].理化检验-化学分册,2021,57(1):52-56.
YUE C,ZHAO W L,GUO Z X,et al.Simultaneous determination of 10 flavonoids and coumarins in green aurantii fructus from different origins by HPLC[J].Physical Testing and Chemical Analysis (Part B (Chemical Analysis)),2021,57(1):52-56.
[9] TOMIYAMA K,AOKI H,OIKAWA T,et al.Characteristic volatile components of Japanese sour citrus fruits:Yuzu,Sudachi and Kabosu[J].Flavour and Fragrance Journal,2012,27(5):341-355.
[10] SONG H S,SAWAMURA M,ITO T,et al.Quantitative determination and characteristic flavour of Citrus junos (yuzu) peel oil[J].Flavour and Fragrance Journal,2000,15(4):245-250.
[11] 程玉娇.宽皮柑橘果汁中挥发性硫化物和风味活性组分研究[D].重庆:西南大学,2020.
CHENG Y J.Study on volatile sulfur compounds and arom active volatiles in Mandarin juice[D].Chongqing:Southwest University,2020.
[12] DU X F,WHITAKER V,ROUSEFF R.Changes in strawberry volatile sulfur compounds due to genotype,fruit maturity and sample preparation[J].Flavour and Fragrance Journal,2012,27(6):398-404.
[13] YOSHIO N.Measurement of odor threshold by triangle odor bag method[J].Odor Measure Revience,2004:118-127.
[14] PINO J A,MESA J.Contribution of volatile compounds to mango (Mangifera indica L.) aroma[J].Flavour and Fragrance Journal,2006,21(2):207-213.
[15] UEHARA A,BALDOVINI N.Volatile constituents of yuzu (Citrus junos Sieb.ex Tanaka) peel oil:A review[J].Flavour and Fragrance Journal,2021,36(2):292-318.
[16] AHMED E M,DENNISON R A,DOUGHERTY R H,et al.Flavor and odor thresholds in water of selected orange juice components[J].Journal of Agricultural and Food Chemistry,1978,26(1):187-191.
[17] CHOI H S,SAWAMURA M,KONDO Y.Characterization of the key aroma compounds of Citrus flaviculpus Hort.ex Tanaka by aroma extraction dilution analysis[J].Journal of Food Science,2002,67(5):1713-1718.
[18] BUTTERY R G,SEIFERT R M,GUADAGNI D G,et al.Characterization of some volatile constituents of bell peppers[J].Journal of Agricultural and Food Chemistry,1969,17(6):1322-1327.
[19] BOONBUMRUNG S,TAMURA H,MOOKDASANIT J,et al.Characteristic aroma components of the volatile oil of yellow keaw mango fruits determined by limited odor unit method[J].Food Science and Technology Research,2001,7(3):200-206.
[20] TAKEOKA G R,GÜNTERT M,ENGEL K H.Volatile constituents of Asafoetida[J].Abstracts of Papers of the American Chemical Society,2001,794:33-44.
[21] TAKEOKA G R,TERANISHI R,WILLIAMS P J,et al.Biotechnology for Improved Foods and Flavors[M].Washington D.C.:American Chemical Society,1996
[22] TAMURA H,BOONBUMRUNG S,YOSHIZAWA T,et al.The volatile constituents in the peel and pulp of a green Thai mango,khieo sawoei cultivar(Mangifera indica L.)[J].Food Science and Technology Research,2001,7(1):72-77.
[23] MASANETZ C,GROSCH W.Key odorants of parsley leaves (Petroselinum crispum[Mill.]Nym.ssp.crispum) by Odour-activity values[J].Flavour and Fragrance Journal,1998,13(2):115-124.
[24] FLATH R A,BLACK D R,GUADAGNI D G,et al.Identification and organoleptic evaluation of compounds in Delicious apple essence[J].Journal of Agricultural and Food Chemistry,1967,15(1):29-35.
[25] TAMURA H,YANG R H,SUGISAWA H.Aroma profiles of peel oils of acid citrus[J].ACS Symposium Series,1993,525:121-136.
[26] AVERBECK M,SCHIEBERLE P.Influence of different storage conditions on changes in the key aroma compounds of orange juice reconstituted from concentrate[J].European Food Research and Technology,2011,232(1):129-142.
[27] BUTTERY R G,SEIFERT R M,GUADAGNI D G,et al.Characterization of additional volatile components of tomato[J].Journal of Agricultural and Food Chemistry,1971,19(3):524-529.
[28] CZERNY M,CHRISTLBAUER M,CHRISTLBAUER M,et al.Re-investigation on odour thresholds of key food aroma compounds and development of an aroma language based on odour qualities of defined aqueous odorant solutions[J].European Food Research and Technology,2008,228(2):265-273.
[29] BURDACK-FREITAG A,SCHIEBERLE P.Characterization of the key odorants in raw Italian hazelnuts (Corylus avellana L.var.Tonda Romana) and roasted hazelnut paste by means of molecular sensory science[J].Journal of Agricultural and Food Chemistry,2012,60(20):5057-5064.
[30] PINO J,TORRICELLA R,ORSI F.Correlation between sensory and gas-chromatographic measurements on grapefruit juice volatiles[J].Nahrung-Food,1986,30(8):783-790.
[31] GIRI A,OSAKO K,OHSHIMA T.Identification and characterisation of headspace volatiles of fish miso,a Japanese fish meat based fermented paste,with special emphasis on effect of fish species and meat washing[J].Food Chemistry,2010,120(2):621-631.
[32] TERANISHI R,FLATH R A,GUADAGNI D G,et al.Gas chromatographic,infrared proton magnetic resonance,mass spectral,and threshold analyses of all pentyl acetates[J].Journal of Agricultural and Food Chemistry,1966,14(3):253-262.
[33] ROSEN A A,PETER J B,MIDDLETON F M.Odor thresholds of mixed organic chemicals[J].Water Pollution Control Federation,1962,34(1):7-14.
[34] YOUNG W F,HORTH H,CRANE R,et al.Taste and odour threshold concentrations of potential potable water contaminants[J].Water Research,1996,30(2):331-340.