睡眠是维持机体平衡的最基本条件,睡眠障碍不仅损害身体健康,还会降低生活及工作质量[1-2]。存在睡眠障碍问题的人群相当庞大,据国外流行病学数据显示,15%~35%的成年人存在睡眠质量问题[3]。中国睡眠研究会发布的《2021运动与睡眠白皮书》亦显示,我国超3亿人存在睡眠障碍,约38%成年人有失眠困扰。然而,医学上并不建议轻易使用安定等镇静催眠类药物,因为存在成瘾性、停药反跳等风险。含有特定功能因子的保健食品可有效地避免这些安全性问题,为失眠人群的健康难题提供新的应对方案。因此,面对免疫力低下或者睡眠障碍等亚健康问题的困扰,人们对于传统中医药的药食产品或者天然产品的需求愈加强烈。
灵芝药用历史悠久,具有滋补强壮、扶正固本的功效,是用于治未病的“上品”,在民间为药膳食疗之佳品,安全无副作用。现代药理研究表明,灵芝多糖是其关键功效成分,具有改善睡眠[4-5]、抗肿瘤、调节免疫、护肝、抗辐射等作用[6-8]。国内外对灵芝的研究已深入到免疫系统、中枢神经系统,但相关成果在产品开发上的应用却十分有限,市场上除了灵芝饮片这类初加工产品,大多是由多种原料组成的大复方产品,灵芝特有的应用价值并未得到充分发挥。γ-氨基丁酸(γ-aminobutyric acid,GABA)是一种天然存在的功能性氨基酸,是哺乳动物中枢神经系统中重要的抑制性神经递质,具备改善睡眠[9-11]、降血压、抗焦虑、改善记忆力、抗癫痫、抗衰老等多种生理功能[12]。GABA在日本等国家作为一种功能食品因子已广泛应用于饮料、果酱以及其他功能食品中[13-14],在我国也是一种安全的新食品原料,可用于开发普通食品和保健食品,目前仍具有较大的应用前景。
结合现代营养学开发传统中药材是保健食品研发的新路径。本研究旨在开发功能因子明确、质量稳定可控的灵芝新产品,充分发挥灵芝多糖在改善睡眠方面的优势。通过将γ-氨基丁酸与富含灵芝多糖的灵芝提取物进行合理科学配伍,并制成易于服用、依从性好的片剂,使得二者产生出整体综合效应,为睡眠保健市场提供安全可靠的优质选择,也为药食同源精深加工产品的开发提供发展模式借鉴。
1 材料与方法
1.1 材料与试剂
灵芝提取物,公司自制;γ-氨基丁酸,上海统园食品技术有限公司;麦芽糊精、玉米淀粉,中粮生化能源有限公司;微晶纤维素、硬脂酸镁,湖州菱湖新望化学有限公司;交联羧甲基纤维钠、羧甲基淀粉钠,曲阜市天利药用辅料有限公司;乙醇,中山市华士达生物科技有限公司;以上物料均为食品级。聚维酮K30(药品级),博爱新开源医疗科技集团股份有限公司。
灵芝多糖γ-氨基丁酸片,0.41 g/片(包衣),由实验室自制,推荐服用量为每日1次,每次2片,以成人体重60 kg计,推荐量为0.013 7 g/kg。
SPF级KM雌性小白鼠,体重为18~22 g,由广东省医学实验动物中心提供,生产许可证号 SCXK(粤)2018-0002。在温度为(22±2) ℃、相对湿度为(55±15)%的屏障环境中饲养。
1.2 仪器与设备
DFY-500C万能高速粉碎机,温岭市林大机械有限公司;BSA224S-CW电子分析天平,北京赛多利斯天平有限公司;BS210S型电子天平,德国赛多利斯;101C-3B型电热鼓风干燥箱,上海实验仪器厂有限公司;ZP-7旋转式压片机,上海天峰制药设备有限公司;YD-20智能片剂硬度仪、ZB-1E智能崩解仪,天大天发科技有限公司;筛网。
1.3 实验方法
1.3.1 片剂工艺研究
1.3.1.1 制备工艺流程
本品设计为片剂,根据前期的初步研究结果,灵芝提取物黏度较大,辅料使用量需达到60%~65%时才能较好成型。综合考虑片剂大小、服用次数、服用量等影响依从性的因素,本品规格设定为0.4 g/片(素片),每日服用2片。工艺路线设计为:
主料与辅料混合→制软材→制粒(20目筛)→干燥(烘干至水分为3%~5%)→整粒(20目筛)→总混→压片→包衣→包装等。
1.3.1.2 质量评价标准
本试验选定制粒情况、压片情况、片剂硬度和崩解时限作为评价指标,筛选辅料的种类及用量,以制备得到良好的片剂。
1.3.1.3 填充剂的筛选
本试验选择片剂常用的填充剂玉米淀粉、麦芽糊精和微晶纤维素进行筛选,通过加入不同种类及用量的填充剂进行试验,以制备1 000片为1次试验,试验方案见表1,其他因素不变,根据制粒过程中颗粒的性状和所得片剂的性能指标来选择适宜的填充剂用量。
表1 填充剂的种类和用量优化设计 单位:g
Table 1 Optimization of the type and dosage of fillers
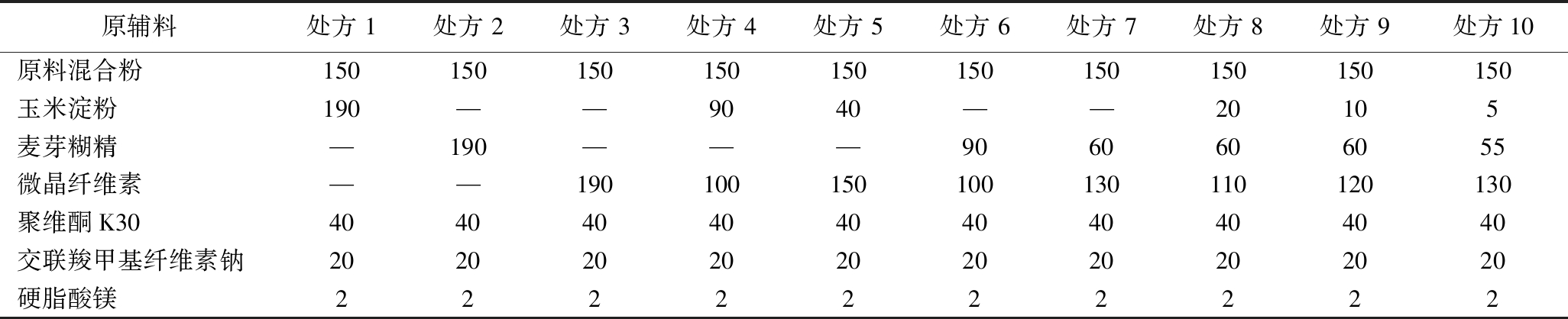
注:—表示无(下同)。
原辅料处方 1处方 2处方 3处方 4处方 5处方 6处方 7处方 8处方 9处方10原料混合粉150150150150150150150150150150玉米淀粉190——9040——20105麦芽糊精—190———9060606055微晶纤维素——190100150100130110120130聚维酮K3040404040404040404040交联羧甲基纤维素钠20202020202020202020硬脂酸镁2222222222
1.3.1.4 黏合剂的筛选
根据预试验结果,分别对100 g/L淀粉浆、400 g/L羟丙甲基纤维素水溶液、400 g/L羧甲基纤维素钠水溶液和650 g/L聚维酮K30乙醇溶液进行筛选,添加量为处方量的10%,其他因素不变,以制粒过程中颗粒的性状和所得片剂的性能指标为依据来选择适宜的黏合剂。
1.3.1.5 崩解剂的筛选
根据预试验分别对干淀粉、羧甲基淀粉钠和交联羧甲基纤维素钠进行筛选,添加量为处方量的5%(质量分数,下同),其他因素不变,以所得片剂的性能指标为依据来选择适宜的崩解剂。
1.3.1.6 润滑剂的筛选
根据预试验分别对滑石粉、微粉硅胶和硬脂酸镁进行筛选,添加量为处方量的0.5%,其他因素不变,以所得片剂的性能指标为依据来选择适宜的润滑剂。
1.3.1.7 片剂制备工艺验证
根据以上考察结果,优选最佳工艺,进行五批制剂工艺验证试验,每批压制1 000片。使用60 g/L透明薄膜包衣预混液进行包衣,控制增重2%~2.5%,包衣温度40~45 ℃,雾化压力约0.4 MPa。记录制粒情况,检查片剂的外观、硬度和崩解时限,并进行标志性成分含量测定。
1.3.2 改善睡眠功能学实验
本研究中的动物实验均依据《保健食品检验与评价技术规范》(2003年版)进行,实施方案通过了伦理委员会审核和批准(实验动物研究伦理审查申请书:W96-027C)。将SPF小鼠在实验室条件下喂养适应3 d,以下每个实验均随机将48只小鼠分为4组,每组12只,每日灌胃给予受试物,给药量根据每周体重增减调整,实验时间为4周。
1.3.2.1 样品配制及给药途径
实验时称取样品0.35、0.7、2.05 g,分别用纯净水制成50 mL的药液,形成低(0.07 g/kg BW)、中(0.14 g/kg BW)、高(0.41 g/kg BW)3个剂量组,相当于人推荐日服量的5、10、30倍。每日按0.1 mL/10 g BW经口灌胃受试物,阴性对照组给予同等体积的纯净水。
1.3.2.2 直接睡眠实验
观察受试组动物给予3个剂量的受试样品、阴性对照组给予同等体积溶媒后,是否出现睡眠现象。当小鼠置于背卧位时,能立即翻正身位,如超过30~60 s不能翻正者,即认为翻正反射消失,进入睡眠。翻正反射恢复即为动物觉醒,翻正反射消失至恢复这段时间为动物睡眠时间,记录阴性对照组与受试样品组入睡动物数及睡眠时间。
1.3.2.3 延长戊巴比妥钠睡眠时间实验
动物末次给予溶剂及不同浓度受试样品后15 min,给各组动物腹腔注射戊巴比妥钠55 mg/kg BW,注射量为0.1 mL/10 g BW,以翻正反射消失为指标,观察受试样品是否延长戊巴比妥钠诱导睡眠时间。
1.3.2.4 戊巴比妥钠阈下剂量催眠实验
动物末次给予溶剂及不同浓度受试样品后15 min,给各组动物腹腔注射戊巴比妥钠30 mg/kg BW,记录30 min内入睡动物数。
1.3.2.5 巴比妥钠睡眠潜伏期实验
动物末次给予溶剂及不同浓度受试样品后15 min,给各组动物腹腔注射巴比妥钠300 mg/kg BW,注射量为0.1 mL/10 g BW,以翻正反射消失为指标,观察受试样品对巴比妥钠诱导睡眠潜伏期的影响。
1.4 数据处理
用SPSS软件包对各实验结果进行统计分析。其中,入睡动物数为计数资料,用X2检验,若四格表总例数<40,或总例数≥40但理论数≤1时,改用确切概率法。动物体重和睡眠时间为计量资料,采用方差分析,对非正态或方差不齐的数据进行变量转换后再统计;若变量转换后仍未满足正态或方差齐性,则改用秩和检验。统计结果中的动物体重和睡眠时间是各实验组的平均值,用平均值±标准误表示。
2 结果与分析
2.1 片剂工艺研究
2.1.1 填充剂种类的筛选结果
填充剂考察试验结果见表2,从处方1~处方3的结果来看,单用一种填充剂,制粒情况和片剂的指标均不理想,但是对比之下,单用微晶纤维素较单用玉米淀粉或麦芽糊精的效果要好。2种填充剂组合使用效果逊于3种填充剂组合使用效果。根据各指标的结果综合评判,处方10的填充剂种类及用量制得的颗粒均匀适宜,所压的片剂片面光洁,硬度和崩解时限符合片剂质量要求。
表2 填充剂考察试验结果
Table 2 Results of the optimization of fillers
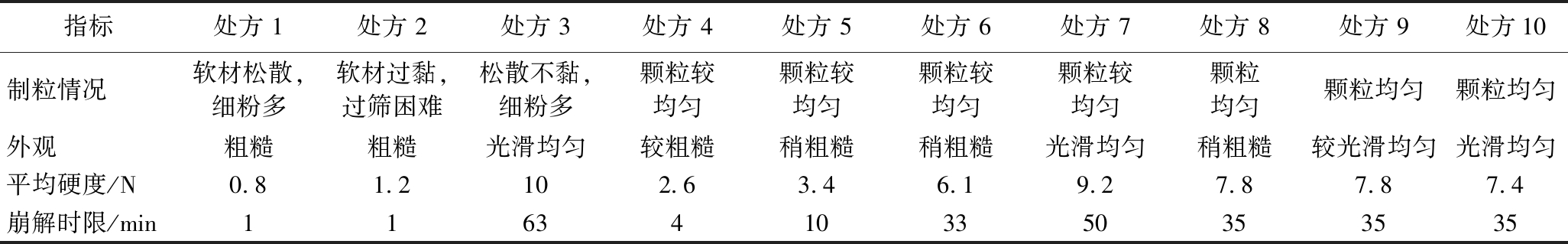
指标处方 1处方 2处方 3处方 4处方 5处方 6处方 7处方 8处方 9处方10制粒情况软材松散,细粉多软材过黏,过筛困难松散不黏,细粉多颗粒较均匀颗粒较均匀颗粒较均匀颗粒较均匀颗粒均匀颗粒均匀颗粒均匀外观粗糙粗糙光滑均匀较粗糙稍粗糙稍粗糙光滑均匀稍粗糙较光滑均匀光滑均匀平均硬度/N0.81.2102.63.46.19.27.87.87.4崩解时限/min11634103350353535
2.1.2 黏合剂种类的筛选结果
黏合剂考察试验结果见表3,用100 g/L淀粉浆、400 g/L羟丙甲基纤维素水溶液、400 g/L羧甲基纤维素钠水溶液作为黏合剂时,制粒过程困难,软材黏性大,过筛粘筛网,且可能由于黏度过大造成片剂崩解时限延长。而使用650 g/L聚维酮K30乙醇溶液作为黏合剂时,黏合效果最好,容易制粒,压制后片面光洁,片剂硬度和崩解时限均符合片剂质量要求。因此,应选用650 g/L聚维酮K30乙醇溶液作为制备灵芝多糖γ-氨基丁酸片剂的黏合剂。
表3 黏合剂考察试验结果
Table 3 Results of the optimization of adhesives

黏合剂制粒情况压片情况外观平均硬度/N崩解时限/min100 g/L淀粉浆制粒较难,颗粒较粗,易粘筛网 光滑均匀10.455400 g/L羟丙甲基纤维素水溶液制粒较难,颗粒较粗,易粘筛网 光滑均匀10.650400 g/L羧甲基纤维素钠水溶液制粒较难,颗粒较粗,易粘筛网 光滑均匀10.152650 g/L聚维酮K30乙醇溶液制粒方便,颗粒紧密,几乎无团块光滑均匀8.935
2.1.3 崩解剂种类的筛选结果
崩解剂考察试验结果见表4,用干淀粉、羧甲基淀粉钠作为崩解剂时,制备所得的片剂外观不够光洁,且崩解时限过长。而使用交联羧甲基纤维素钠作为崩解剂时,制得的片剂外观和崩解性能均较好。因此,应选用交联羧甲基纤维素钠作为制备灵芝多糖γ-氨基丁酸片剂的崩解剂。
表4 崩解剂考察试验结果
Table 4 Results of the optimization of disintegrants

崩解剂压片情况外观平均硬度/N崩解时限/min干淀粉稍粗糙 7.245羧甲基淀粉钠较光洁 8.145交联羧甲基纤维素钠光洁均匀8.835
2.1.4 润滑剂种类的筛选结果
润滑剂考察试验结果见表5,用滑石粉、微粉硅胶和硬脂酸镁作为润滑剂时,制备所得的片剂硬度和崩解时限区别不大,主要区别在于片剂的片面光洁程度,滑石粉和微粉硅胶润滑效果一般,片剂外观表现为较光洁,而使用硬脂酸镁润滑剂制得的片剂外观完整光洁,说明硬脂酸镁可有效减小颗粒间及颗粒与模具间摩擦力,能显示出良好的润滑效果。因此,应选用硬脂酸镁作为制备灵芝多糖γ-氨基丁酸片剂的润滑剂。
表5 润滑剂考察试验结果
Table 5 Results of the optimization of lubricants
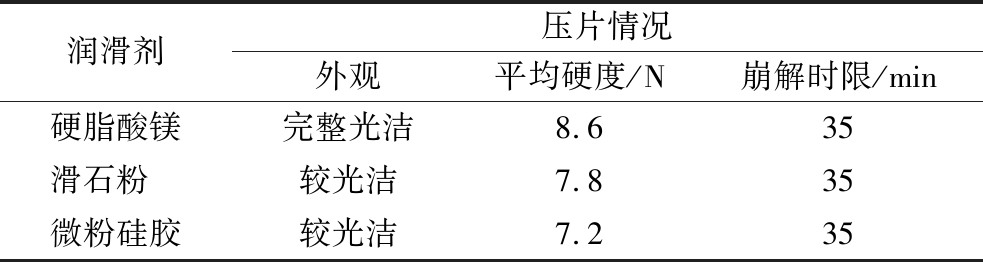
润滑剂压片情况外观平均硬度/N崩解时限/min硬脂酸镁完整光洁8.635滑石粉 较光洁7.835微粉硅胶较光洁7.235
2.1.5 片剂制备工艺验证结果与分析
采用最佳工艺条件制备5批灵芝多糖γ-氨基丁酸片,结果见表6。制粒方便,颗粒均匀,过筛容易,所压片剂片面光洁,包衣后片面均匀光滑,片芯呈棕褐色。各项指标良好,且符合质量标准规定,表明此制备工艺稳定可靠。
表6 五批片剂工艺验证结果
Table 6 Results of the process validation of five batches of tablets
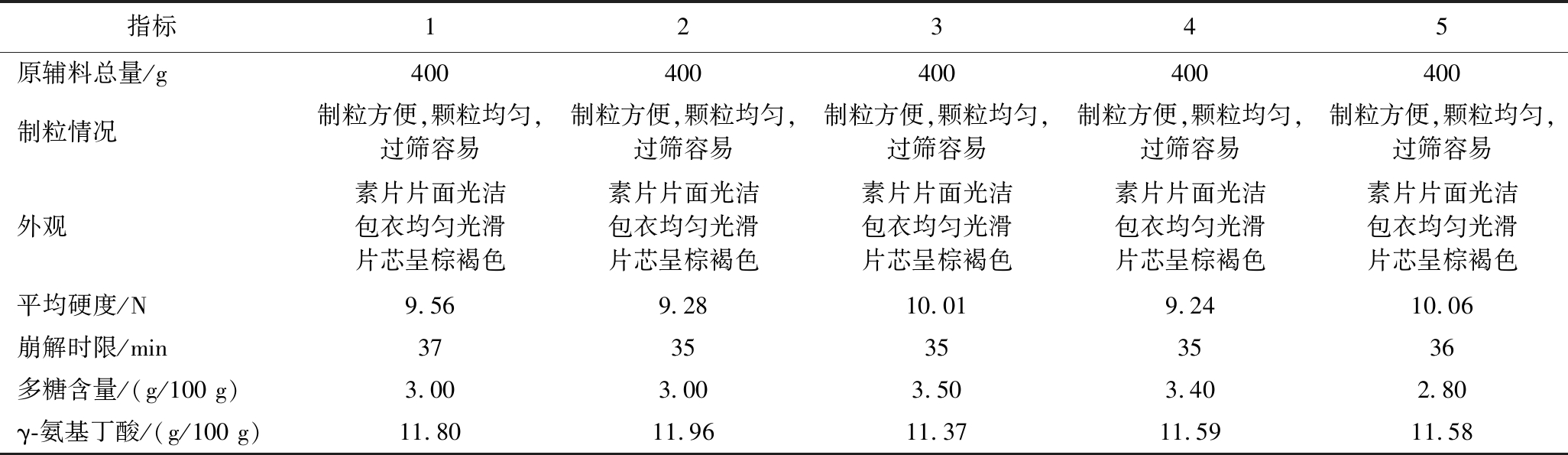
指标12345原辅料总量/g400400400400400制粒情况制粒方便,颗粒均匀,过筛容易制粒方便,颗粒均匀,过筛容易制粒方便,颗粒均匀,过筛容易制粒方便,颗粒均匀,过筛容易制粒方便,颗粒均匀,过筛容易外观素片片面光洁包衣均匀光滑片芯呈棕褐色素片片面光洁包衣均匀光滑片芯呈棕褐色素片片面光洁包衣均匀光滑片芯呈棕褐色素片片面光洁包衣均匀光滑片芯呈棕褐色素片片面光洁包衣均匀光滑片芯呈棕褐色平均硬度/N9.569.2810.019.2410.06崩解时限/min3735353536多糖含量/(g/100 g)3.003.003.503.402.80γ-氨基丁酸/(g/100 g)11.8011.9611.3711.5911.58
2.2 灵芝多糖γ-氨基丁酸片改善睡眠功能学实验
2.2.1 灵芝多糖γ-氨基丁酸片对小鼠体重的影响
记录各实验中小鼠的不同时期的体重,进行增重分析,统计结果如表7所示。各剂量组增重与阴性对照组比较,差异均无统计学意义,表明灵芝多糖γ-氨基丁酸片对小鼠体重无明显影响。
表7 灵芝多糖γ-氨基丁酸片对小鼠体重的影响![]()
Table 7 Effect of the tablets composed of Ganoderma lucidum polysaccharide and γ-aminobutyric acid on body weight of mice (n=12, ![]()
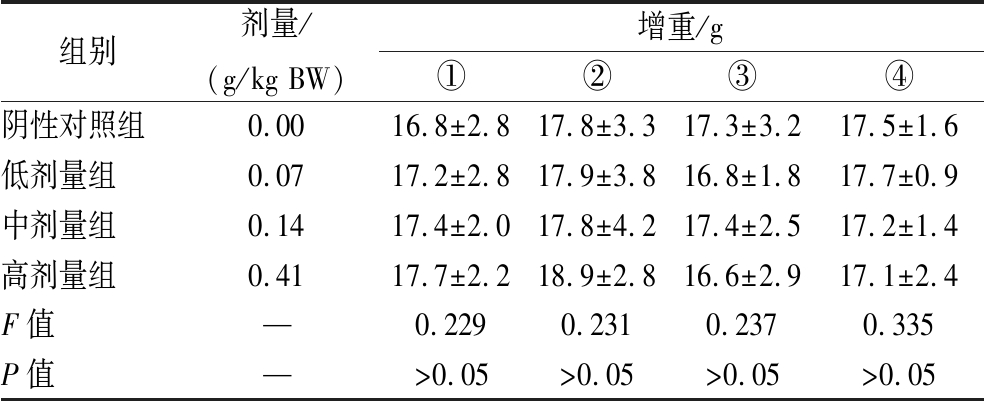
注:直接睡眠实验组(“1.3.2.2”节,①),延长戊巴比妥钠睡眠时间实验组(“1.3.2.3节”,②),戊巴比妥钠阈下剂量催眠实验组(“1.3.2.4”节,③),巴比妥钠睡眠潜伏期实验组(“1.3.2.5”节,④)。
组别剂量/(g/kg BW)增重/g①②③④阴性对照组0.0016.8±2.817.8±3.317.3±3.217.5±1.6低剂量组0.0717.2±2.817.9±3.816.8±1.817.7±0.9中剂量组0.1417.4±2.017.8±4.217.4±2.517.2±1.4高剂量组0.4117.7±2.218.9±2.816.6±2.917.1±2.4F值—0.2290.2310.2370.335P值—>0.05>0.05>0.05>0.05
2.2.2 灵芝多糖γ-氨基丁酸片对小鼠直接睡眠作用的影响
实验中观察发现,各剂量组入睡动物数均为0,与阴性对照组比较差异均无统计学意义(表8),说明灵芝多糖γ-氨基丁酸片对小鼠无明显的直接睡眠作用。
表8 灵芝多糖γ-氨基丁酸片对小鼠直接睡眠作用观察结果![]()
Table 8 Effect of the tablets composed of Ganoderma lucidum polysaccharide and γ-aminobutyric acid on mice to direct sleep (n=12, ![]()
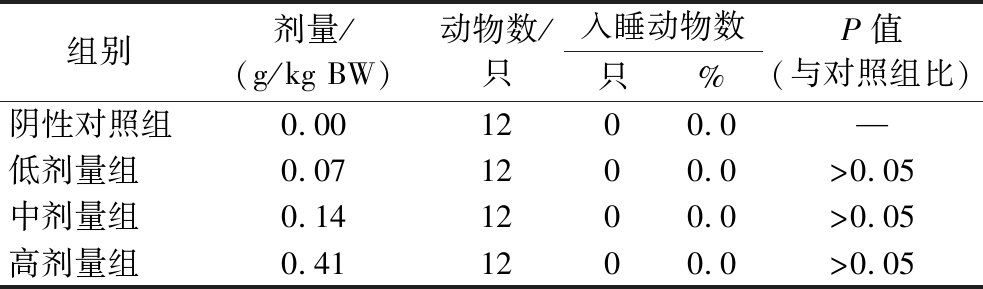
组别剂量/(g/kg BW)动物数/只入睡动物数只%P值(与对照组比)阴性对照组0.001200.0—低剂量组0.071200.0>0.05中剂量组0.141200.0>0.05高剂量组0.411200.0>0.05
2.2.3 灵芝多糖γ-氨基丁酸片对戊巴比妥钠诱导小鼠睡眠时间的影响
中、高剂量组动物入睡时间缩短、睡眠时间延长,与阴性对照组比较差异有统计学意义(表9),表明灵芝多糖γ-氨基丁酸片延长戊巴比妥钠睡眠时间实验结果为阳性。
表9 灵芝多糖γ-氨基丁酸片对戊巴比妥钠诱导小鼠睡眠时间的影响![]()
Table 9 Effect of the tablets composed of Ganoderma lucidum polysaccharide and γ-aminobutyric acid on the sleep time of mice induced by pentobarbital sodium (n=12, ![]()

组别剂量/(g/kg BW)动物数/只入睡时间/minP值(与阴性对照组比)睡眠时间/minP值(与阴性对照组比)阴性对照组0.00128.3±0.5—27.3±3.5—低剂量组 0.07127.4±1.3>0.0530.0±8.1>0.05中剂量组 0.14126.5±0.6<0.0142.1±10.2<0.01高剂量组 0.41126.2±1.2<0.0143.6±10.1<0.01F值 ——11.909(P<0.01)—11.562(P<0.01)—
2.2.4 灵芝多糖γ-氨基丁酸片对戊巴比妥钠阈下剂量催眠作用的影响
各剂量组入睡动物数与阴性对照组比较,差异无统计学意义(表10),表明灵芝多糖γ-氨基丁酸片的戊巴比妥钠阈下剂量催眠实验结果为阴性。
表10 灵芝多糖γ-氨基丁酸片对戊巴比妥钠阈下剂量催眠作用的影响![]()
Table 10 Effect of the tablets composed of Ganoderma lucidum polysaccharide and γ-aminobutyric acid on the hypnotic effect of subthreshold dose of pentobarbital ![]()
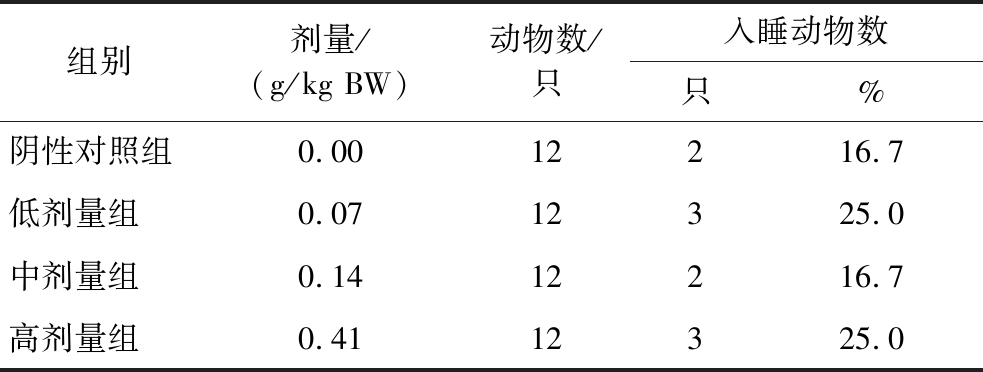
组别剂量/(g/kg BW)动物数/只入睡动物数只%阴性对照组0.0012216.7低剂量组0.0712325.0中剂量组0.1412216.7高剂量组0.4112325.0
2.2.5 灵芝多糖γ-氨基丁酸片对巴比妥钠诱导小鼠睡眠潜伏期的影响
高剂量组动物睡眠潜伏期缩短,与阴性对照组比较差异有统计学意义(表11),表明灵芝多糖γ-氨基丁酸片的巴比妥钠睡眠潜伏期实验结果为阳性。
表11 灵芝多糖γ-氨基丁酸片对巴比妥钠诱导小鼠睡眠潜伏期的影响![]()
Table 11 Effect of the tablets composed of Ganoderma lucidum polysaccharide and γ-aminobutyric acid on the sleep latency of mice induced by barbital sodium![]()
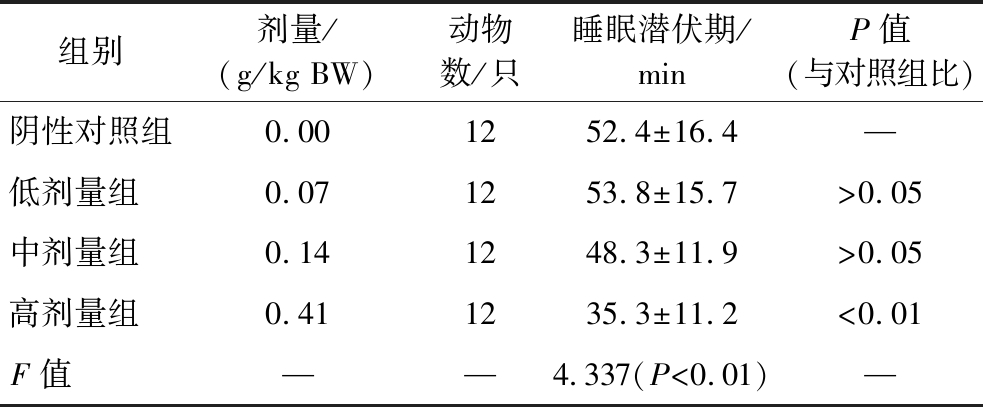
组别剂量/(g/kg BW)动物数/只睡眠潜伏期/minP值(与对照组比)阴性对照组0.001252.4±16.4—低剂量组 0.071253.8±15.7>0.05中剂量组 0.141248.3±11.9>0.05高剂量组 0.411235.3±11.2<0.01F值 ——4.337(P<0.01)—
综合上述实验结果,根据《保健食品检验与评价技术规范》中的改善睡眠功能评价标准判断,灵芝多糖γ-氨基丁酸片具有改善睡眠功能作用。
3 讨论
片剂是保健食品的常用剂型,不仅服用方便,且适宜于工业化大生产,但在实际开发时,原料本身的特性对于片剂成型性与稳定性具有较大影响。灵芝提取物黏性大,可能影响制剂时的物料均匀性、硬度、崩解时限等。本研究利用多种辅料进行制粒、压片,获得功效成分均一的灵芝多糖γ-氨基丁酸片,加上包衣工序则有利于片剂的稳定保存。
将此灵芝多糖γ-氨基丁酸片作为样品,进行功能学实验,结果表明其具有改善睡眠的作用。灵芝多糖和GABA是处方中的2种主要功能因子,灵芝多糖可通过调节神经系统影响松果体对褪黑素的分泌,γ-氨基丁酸在非快动眼期引导入睡,并延长深睡眠时间,二者可协同增效,发挥改善睡眠的保健功能。引起睡眠障碍的因素较多,在压力等不良情绪刺激时,人体下丘脑-垂体-肾上腺(hypothalamic-pituitary-adrenal,HPA)轴异常兴奋,容易诱发失眠症状。灵芝多糖和GABA在抑制HPA轴时起到的协同作用可能与抑制氯离子通路和清除自由基有关,具体分子机制有待进一步研究。
灵芝是传统的补益类药材,安全有效,适宜于开发成满足现代人需求的健康产品。结合现代营养学研究成果,与新食品原料γ-氨基丁酸复配并制成服用方便的剂型,得到一款帮助亚健康人群改善睡眠障碍的新兴产品,可充分发挥二者的健康价值,实现从初级农产品到保健食品的转变,引发灵芝下游经济新的增长点,有利于促进灵芝产业链的延伸发展,并促进产业转型升级。
[1] 温艳琼. 睡眠障碍简析[J].大家健康(学术版), 2015, 9(9):272-273.
WEN Y Q.A brief analysis of sleep disorder[J].For All Health, 2015, 9(9):272-273.
[2] 卢启冉, 王利凯, 邓蕊.睡眠障碍的发生机制及其治疗研究进展[J].山西中医药大学学报, 2021, 22(4):291-297.
LU Q R, WANG L K, DENG R.Research progress on the mechanism and treatment of sleep disorders[J].Journal of Shanxi University of Chinese Medicine, 2021, 22(4):291-297.
[3] CRUZ M M E, KRYGER M H, MORIN C M, et al.Comorbid insomnia and sleep apnea:Mechanisms and implications of an underrecognized and misinterpreted sleep disorder[J].Sleep Medicine, 2021, 84:283-288.
[4] CUI X Y, CUI S Y, ZHANG J, et al.Extract of Ganoderma lucidum prolongs sleep time in rats[J].Journal of Ethnopharmacology, 2012, 139(3):796-800.
[5] CHU Q P, WANG L E, CUI X Y, et al.Extract of Ganoderma lucidum potentiates pentobarbital-induced sleep via a GABAergic mechanism[J].Pharmacology Biochemistry and Behavior, 2007, 86(4):693-698.
[6] 陈文华, 程显好, 谭会颖, 等.灵芝多糖的药理作用及其机制研究进展[J].中国药房,2018,29(24):3446-3450.
CHEN W H, CHENG X H, TAN H Y, et al.Research progress on pharmacological action and mechanism of Ganoderma lucidum polysaccharide[J].China Pharmacy, 2018, 29(24):3446-3450.
[7] 陈伟, 马飞, 张琳, 等.灵芝有效成分提取及药理活性研究进展[J].安徽农业科学, 2016, 44(8):147-149;202.
CHEN W, MA F, ZHANG L, et al.Progress on the studies of extraction and pharmacological activities of bioactive compounds from Ganoderma lucidum[J].Journal of Anhui Agricultural Sciences, 2016, 44(8):147-149;202.
[8] 谢怡琼, 王琪瑞, 孙思雅, 等.灵芝的药理作用和临床应用研究进展[J].临床医学研究与实践, 2020, 5(10):191-193.
XIE Y Q, WANG Q R, SUN S Y, et al.Research progress on the pharmacological effects and clinical applications of Ganoderma lucidum[J].Clinical Research and Practice, 2020, 5(10):191-193.
[9] 李科, 俞兰秀, 刘小雨, 等.γ-氨基丁酸改善睡眠作用机制的研究进展[J].食品工业科技, 2019, 40(14):353-358.
LI K, YU L X, LIU X Y, et al.Research progress on improving sleep mechanism of γ-aminobutyric acid[J].Science and Technology of Food Industry, 2019, 40(14):353-358.
[10] YAMATSU A, YAMASHITA Y, PANDHARIPANDE T, et al.Effect of oral γ-aminobutyric acid (GABA) administration on sleep and its absorption in humans[J].Food Science and Biotechnology, 2016, 25(2):547-551.
[11] HONG K B, PARK Y, SUH H J.Sleep-promoting effects of the GABA/5-HTP mixture in vertebrate models[J].Behavioural Brain Research An International Journal, 2016(310):36-41.
[12] 于荣贤, 刘兵, 余玉芳, 等.γ-氨基丁酸的保健功能研究进展[J].现代养生, 2016,16(4):59-60.
YU R X, LIU B, YU Y F, et al.Research progress on health function of γ-aminobutyric acid[J].Health Protection and Promotion, 2016,16(4):59-60.
[13] 梁恒宇, 邓立康, 林海龙, 等.新资源食品:γ-氨基丁酸(GABA)的研究进展[J].食品研究与开发, 2013, 34(15):119-123.
LIANG H Y, DENG L K, LIN H L, et al.Research progress of new resource food:γ-aminobutanoic acid (GABA)[J].Food Research and Development, 2013, 34(15):119-123.
[14] 林杨, 唐琦勇, 楚敏, 等.γ-氨基丁酸的功能、生产及食品应用研究进展[J].中国调味品, 2021, 46(6):173- 179.
LIN Y, TANG Q Y, CHU M, et al.Research progress on function, production and food application of γ-aminobutyric acid[J].China Condiment, 2021, 46(6):173-179.