大球盖菇(Stropharia rugoso-annulata),又被称为赤松茸、皱环球盖菇、酒红球盖菇,富含蛋白质、多糖、维生素等营养物质,具有降血糖、抗肿瘤、抗氧化和抑制破骨细胞形成等多种生物活性功能,是联合国粮农组织向发展中国家推荐栽培的优良食用菌[1-2],其菌柄粗壮,质地鲜美,易于加工。近几年我国大球盖菇栽培面积迅速扩大,成为国内快速发展的食用菌之一[3]。然而,大球盖菇在我国一般用于鲜食或制成干菇,其产品形式单一且风味寡淡,影响消费者的选择,在一定程度上阻碍了大球盖菇产业的发展,因此有必要改善其风味以满足消费者对多元化食品的需求。
风味是食品的一个关键特征,主要由挥发性成分和非挥发性成分共同组成,赋予食品独特的感官特性,并明显影响着人们的喜好[4]。挂糊油炸是改善食品风味的一种重要加工方式,其主要采用挂糊工艺,即在食品表面裹上一层面糊,然后通过油炸而成[5]。基于此,王泽华[6]研究了挂糊油炸金针菇脚加工前后非挥发性风味物质的变化,发现油炸后等鲜浓度值呈现不同幅度的增加趋势,并提高了产品的甜味和鲜味水平,降低了酸味和涩味水平。在油炸过程中,食品会发生复杂的变化,比如淀粉糊化、美拉德反应、焦糖化作用以及形成酥脆和色泽金黄的外壳,赋予产品独特的口感和令人愉悦的风味[7]。在改善大球盖菇的风味方面,包陈力根等[8]研究发现140 ℃烘烤5 min的大球盖菇挥发性风味更突出,增加了麦芽香、可可香、坚果香。此外,HU等[9]研究表明,真空冷冻干燥可有效保留大球盖菇的非挥发性风味成分,热风干燥的大球盖菇等鲜浓度值最高,但是采用挂糊油炸工艺处理大球盖菇的研究目前尚未有报道。
本研究通过顶空固相微萃取结合气相色谱-质谱(headspace solid-phase microextraction gas chromatography-mass spectrometry, HS-SPME-GC-MS)以及电子鼻技术,分析挂糊油炸大球盖菇菌柄在加工过程中挥发性风味物质的组成及相对含量,通过计算相对气味活度值(relative odor activity value, ROAV)确定不同加工阶段的关键风味物质和具有重要修饰作用的风味物质,并运用主成分分析法(principal component analysis, PCA)对挥发性风味物质的ROAV值进行对比分析,确定不同加工过程中的主体风味物质,以此阐明挂糊油炸大球盖菇菌柄的风味特征,为大球盖菇的风味研究和拓展大球盖菇的产品形式提供理论参考。
1 材料与方法
1.1 材料与试剂
新鲜大球盖菇购于重庆市大足区,选择大小一致的样品经除杂、清洗、沥干后剥离菌柄备用;实验所需油炸粉、食盐、金龙鱼黄金比例食用植物调和油、鸡蛋、膨松剂等购于重庆永辉超市。
1.2 仪器与设备
GCMS-QP201010200型气相色谱-质谱联用仪,日本岛津公司;CAR/PDMS型75 μm萃取纤维头、57330-U型SPME手动进样手柄,美国Supelco公司;RJ-81型电炸炉,广州佛洛丽斯厨具设备有限公司;HH-4型数显恒温水浴锅,常州普天仪器制造有限公司;cNose型电子鼻,上海保圣实业发展有限公司。
1.3 实验方法
1.3.1 样品制备
1.3.1.1 工艺流程
挂糊油炸大球盖菇菌柄工艺流程如下:
鲜菌柄→切分→挂糊→预炸→复炸→成品
1.3.1.2 调糊工艺
称取100 g油炸粉(由玉米淀粉、红薯淀粉、木薯淀粉、小麦面粉组成)置于不锈钢盆中,添加87.5 g水和25 g全蛋液,添加3.20 g食盐和1.87 g的复合膨松剂,用筷子充分搅拌均匀即可得到挂糊糊料。
1.3.1.3 样品处理
挑选大小一致的菌柄切分成0.8 cm×0.8 cm×2 cm块状,完全浸没于糊料中约10 s后取出,待菌柄上的糊料不成股滴下时置于160 ℃油温中预炸120 s,随后捞出置于滤网中,待另一锅油温度升高并稳定至180 ℃后复炸60 s即得到成品。
1.3.2 样品编号及描述
为便于表述,将所测的6组样品进行编号,如表1所示。
表1 样品编号及描述
Table 1 Sample number and description

编号名称描述A鲜菌柄原材料,即新鲜的大球盖菇菌柄B挂糊工艺流程中挂糊阶段的样品,即面糊+鲜菌柄C预炸菌柄经预炸处理后,剥离面糊外壳后所得到的内部菌柄D预炸工艺流程中预炸阶段的样品,即面糊+预炸菌柄E复炸菌柄经复炸处理后,剥离面糊外壳后所得到的内部菌柄F复炸工艺流程中复炸阶段的样品,即面糊+复炸菌柄
1.3.3 顶空固相微萃取-气相色谱-质谱检测条件
顶空固相微萃取:将样品绞碎,称取5.00 g于20 mL顶空萃取瓶中,在60 ℃水浴中平衡10 min,插入活化好的SPME萃取头,在60 ℃水浴条件下萃取30 min,萃取完成后立即插入GC进样口。
气相条件:参考廖林等[10]的方法并略有修改。GC分析毛细管柱为DB-5MS(30 m×0.2 mm, 0.25 μm),压力为100.0 kPa;总流量为50.0 mL/min;柱流量为1.78 mL/min;进样温度为250 ℃;载气为氦气,不分流进样。升温程序为:起始温度40 ℃,保持2 min;再以2 ℃/min的速度升温至90 ℃,保持5 min;最后以10 ℃/min的速度升温至250 ℃并保持1 min。
质谱条件:电子电离源,电子能量为70 eV;接口温度为250 ℃;离子源温度为250 ℃;检测器电压为350 V;质量扫描范围为30~500 m/z,溶剂延迟为2 min。
结果分析:根据化合物保留时间,将质谱数据与计算机中MS定性谱库(NIST17-1.lib)进行检索并匹配,选择相似度大于80的化合物进行定性,按峰面积计算相对含量。
1.3.4 关键风味物质评价
关键风味物质采用刘登勇等[11]ROAV的评定方法,首先定义对样品风味贡献最大的组分为ROAVstan=100,然后其他挥发性风味物质的计算如公式(1)所示:
(1)
式中:CA和Cstan分别为该挥发性风味物质的相对含量和对整体风味贡献最大的挥发性风味物质的相对含量,%;TA和Tstan分别为该挥发性风味物质的阈值和对整体风味贡献最大的挥发性风味物质的阈值,μg/kg。
1.3.5 电子鼻检测
称取绞碎的样品2.00 g置于25 mL顶空瓶中,50 ℃水浴30 min,室温平衡10 min后测定。主要实验参数:清洗时间80 s,测试时间80 s,气体流速1 L/min。
电子鼻设备由10个传感器组成,其传感器对多种气味有强烈的响应值,具体见表2。
表2 电子鼻传感器名称及其响应物质
Table 2 Names of electronic nose sensors and their response substances
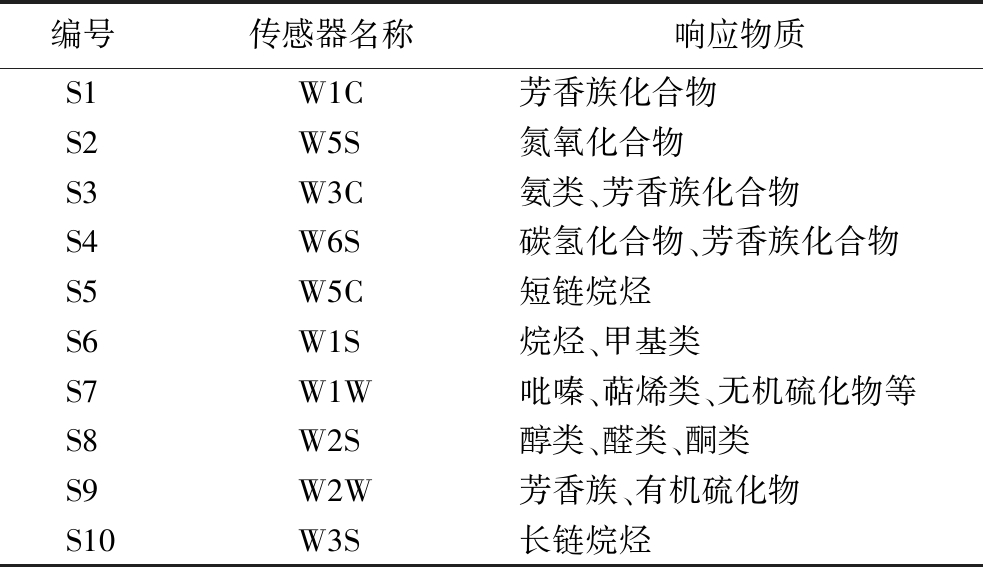
编号传感器名称响应物质S1W1C芳香族化合物S2W5S氮氧化合物S3W3C氨类、芳香族化合物S4W6S碳氢化合物、芳香族化合物S5W5C短链烷烃S6W1S烷烃、甲基类S7W1W吡嗪、萜烯类、无机硫化物等S8W2S醇类、醛类、酮类S9W2W芳香族、有机硫化物S10W3S长链烷烃
1.4 数据处理
采用Microsoft Excel 2019对数据进行统计,利用Origin 2018绘制柱形图、折线图和PCA进行分析,使用SPSS Statistics 18软件进行显著性分析。
2 结果与分析
2.1 挥发性风味物质整体分析
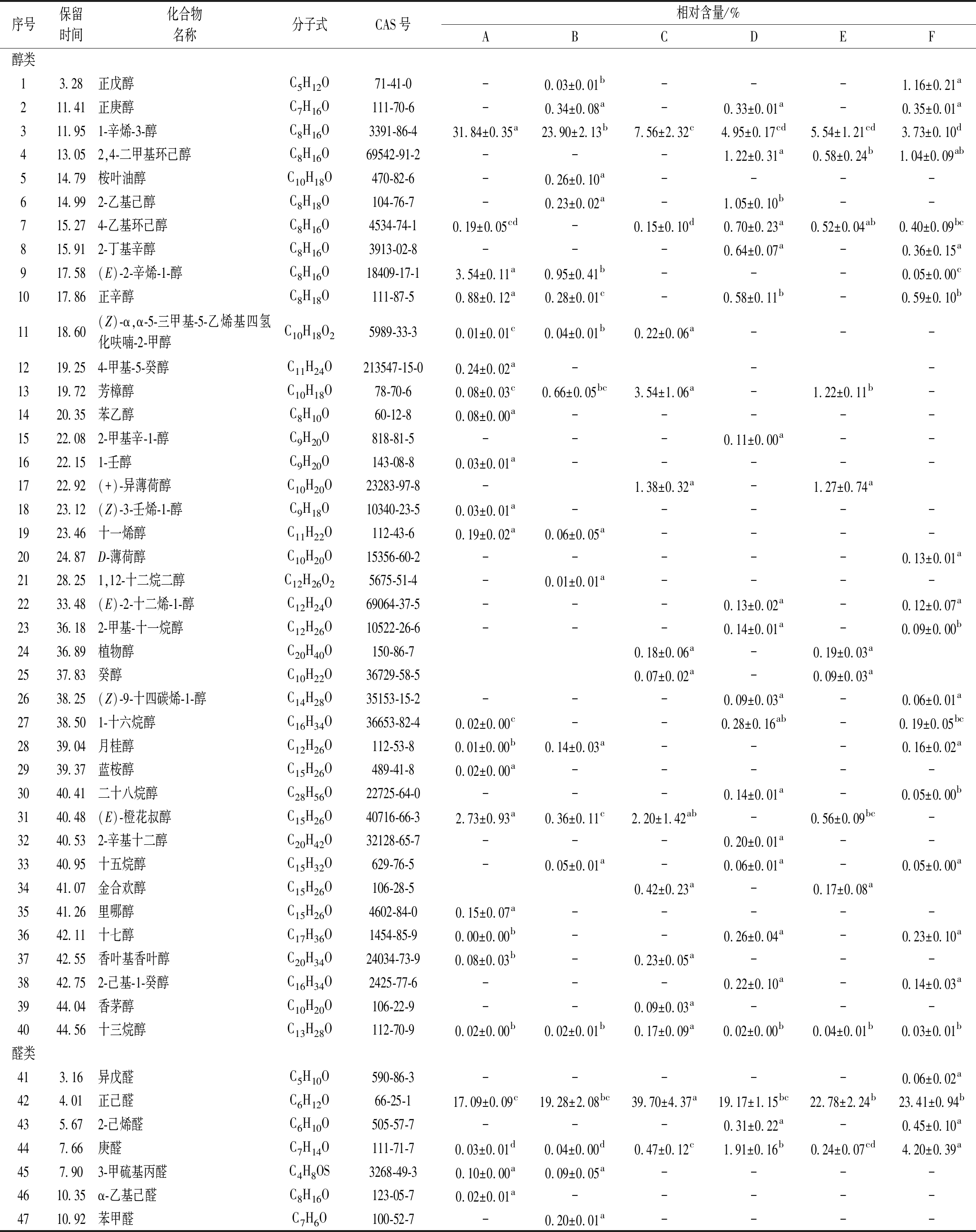
由图1和附表1(https://doi.org/10.13995/j.cnki.11-1802/ts.031882)可知,挂糊油炸大球盖菇菌柄在加工过程中共检出166种挥发性风味物质,其中醇类40种、醛类35种、酮类14种、酸类3种、酯类19种、烷烃22种、烯烃16种以及其他类17种;在6组样品中分别检出72种、64种、61种、79种、52种和89种挥发性风味物质。由预炸菌柄(C组)和预炸(D组)对比、复炸菌柄(E组)和复炸(F组)对比可知,预炸和复炸样品分别增加了28种和37种挥发性风味物质,并且总物质数含量高于未油炸的样品,说明油炸提高了样品的风味丰富度,并且其贡献主要来源于面糊外壳。鲜菌柄(A组)中的挥发性物质主要是醇类、醛类和酯类,分别占相对百分含量的40.14%、19.29%和37.84%。相比于鲜菌柄,在挂糊阶段(B组)所检测到的挥发性风味物质数有所减少,可能是具有一定黏度的糊料黏附于组织表面,阻碍了物质的挥发。在C、D、E和F这4组样品中,醇类、酯类物质的相对含量迅速减少,醛类、烯烃、其他类化合物的含量显著增加,且主要挥发性风味物质都是醛类,占比分别为61.58%、54.65%、60.81%和62.30%。

a-挥发性风味物质数;b-相对百分含量
图1 挂糊油炸大球盖菇菌柄不同加工过程挥发性风味物质数和相对百分含量
Fig.1 Number and relative percentage of volatile flavor substances in the stalk of the deep-fried and battered S.rugoso-annulata at different processing processes
2.2 醇类风味物质分析
醇类风味物质相对百分含量在加工过程中迅速降低,由鲜菌柄的40.14%降至复炸阶段的8.92%,其中1-辛烯-3-醇的变化主导了这个趋势。1-辛烯-3-醇,也被称为蘑菇醇,在1938年首次被鉴定为一种类似蘑菇的化合物,具有独特的青香、蘑菇香和泥土香,在许多食用菌中被确认是重要的挥发性风味物质[4,12],其在6组样品中的相对百分含量依次为31.84%、23.90%、7.56%、4.95%、5.54%和3.73%,并且油炸前后差异显著。值得注意的是,1-辛烯-3-醇和6组样品中被检测到的多种醇类物质均为8个碳原子,这些C8挥发物主要由脂肪酸经脂肪氧合酶水解产生,然后成为食用菌中重要的风味贡献者[13]。C8醇具有热敏性,在热处理时容易降解或分解[14],这可能是1-辛烯-3-醇等醇类物质相对含量显著下降的主要原因。
2.3 醛类风味物质分析
醛类是食用菌中一类重要的风味物质,主要由多不饱和脂肪酸的双键氧化产生,其阈值普遍较低,大多数检测到的醛主要表现出青香、果香、脂香和白葡萄酒风味[15]。未油炸前的2组样品检测到了3-甲硫基丙醛,这是一种具有肉香味的化合物,并且阈值较低,其可能来源于蛋氨酸的酶分解[16]。与醇类的变化不同,醛类物质经油炸处理后,所检出的物质数有所增加,相对百分含量明显提高,成为油炸后样品占比最大的风味化合物,并且醛类物质数均最多,其中正己醛和(E)-2-壬烯醛的相对含量均较高,可赋予样品脂香、青香;正辛醛、(E,E)-2,4-庚二烯醛和2-十三烯醛为仅在油炸后检测到并且含量占比相对较高的物质,可赋予果香、鸡肉香;经过预炸或复炸,庚醛、(E)-2-辛烯醛、壬醛、2,4-癸二烯醛、癸醛、2-十一烯醛和十三醛等醛类相对百分含量显著增加,这些化合物对于油炸后的产品风味具有较大影响。
2.4 酮类风味物质分析
酮类主要由多不饱和脂肪酸氧化、美拉德反应、氨基酸降解或微生物氧化产生,其阈值一般高于醛类,对食用菌的风味特征有重要影响[15,17]。在6组样品中,酮类相对含量均较低,且6组样品均无法检测到同一种酮类化合物。1-辛烯-3-酮在鲜菌柄和挂糊阶段的相对百分含量分别为0.46%、0.17%,其要呈现蘑菇香和泥土香,阈值仅为0.005,对样品整体的风味贡献较大。1-辛烯-3-酮对生食用菌的风味有较大影响,如ZHANG等[16]的研究表明,1-辛烯-3-酮是生牛肝菌贡献最大的香气活性化合物,气味活性值(odor activity value, OAV)最高,对生样品的风味贡献度大于1-辛烯-3-醇。
2.5 酸类、酯类风味物质分析
在6组样品中,酸类物质检测到的物质数分别为0、1、0、2、0和1种,并且相对含量较低。酯类物质主要呈现果香和脂香,在鲜菌柄和挂糊阶段的样品中相对含量占比较大,其中甲酸正己酯在这2组样品中分别占比37.34%和48.10%。酯类物质经油炸后含量显著降低,6组样品的含量依次为37.84%、48.49%、4.87%、3.09%、1.29%和1.40%。
2.6 烃类风味物质分析
烷烃类风味物质在6组样品中能检测到的物质数量较多但相对含量较低,经油炸后相对含量有一定程度的增加。烯烃在油炸后含量显著增加,6组样品烯烃的相对含量分别为0.82%、0.57%、7.47%、13.76%、1.74%和14.26%。一般而言,烃类物质的阈值往往较高,对样品的风味贡献较小,但多种烷烃和烯烃的协同作用可能对食品的风味有一定贡献[18]。
2.7 其他类风味物质分析
其他类风味物质主要包括吡嗪、呋喃、吡啶、醚、芳香化合物等,油炸后无论是种类和含量都有较大幅度增加,并且180 ℃复炸后对其他类物质的影响更大。2-甲基吡嗪、2,5-二甲基吡嗪、2-戊基呋喃等都是经过油炸后才被检测到,这些物质可能是高温条件下美拉德反应的典型产物[19]。此外,其他类物质在D组和F组中的丰富度更明显,说明其主要来源于面糊油炸后所形成的外壳,这些杂环化合物一般呈现脂香、肉香、巧克力香和烤坚果香,对样品的整体风味具有良好的修饰作用。
2.8 关键风味物质鉴定
挂糊油炸大球盖菇菌柄加工过程的整体风味是由各挥发性物质的阈值与其在风味体系中的浓度共同决定的,为进一步明确关键风味物质,引入ROAV这一评价指标,ROAV值越大的组分表明对样品总体风味的贡献越大,通常ROAV≥1的组分为所分析样品的关键风味化合物,0.1≤ROAV<1的组分对样品的总体风味具有重要修饰作用[11]。在未油炸阶段(A组、B组),1-辛烯-3-酮对样品挥发性风味物质的贡献最大,因此定义1-辛烯-3-酮为ROAVstan1=100;(E)-2-壬烯醛具有柑橘香、甜瓜香,阈值仅为0.065,在油炸后(C、D、E、F组)为贡献最大的挥发性风味物质,因此将其定义为ROAVstan2=100。通过参考相关文献,本研究选取能明确查到阈值的共计55种风味化合物进行相对气味活度值分析,具体见图2和表3。
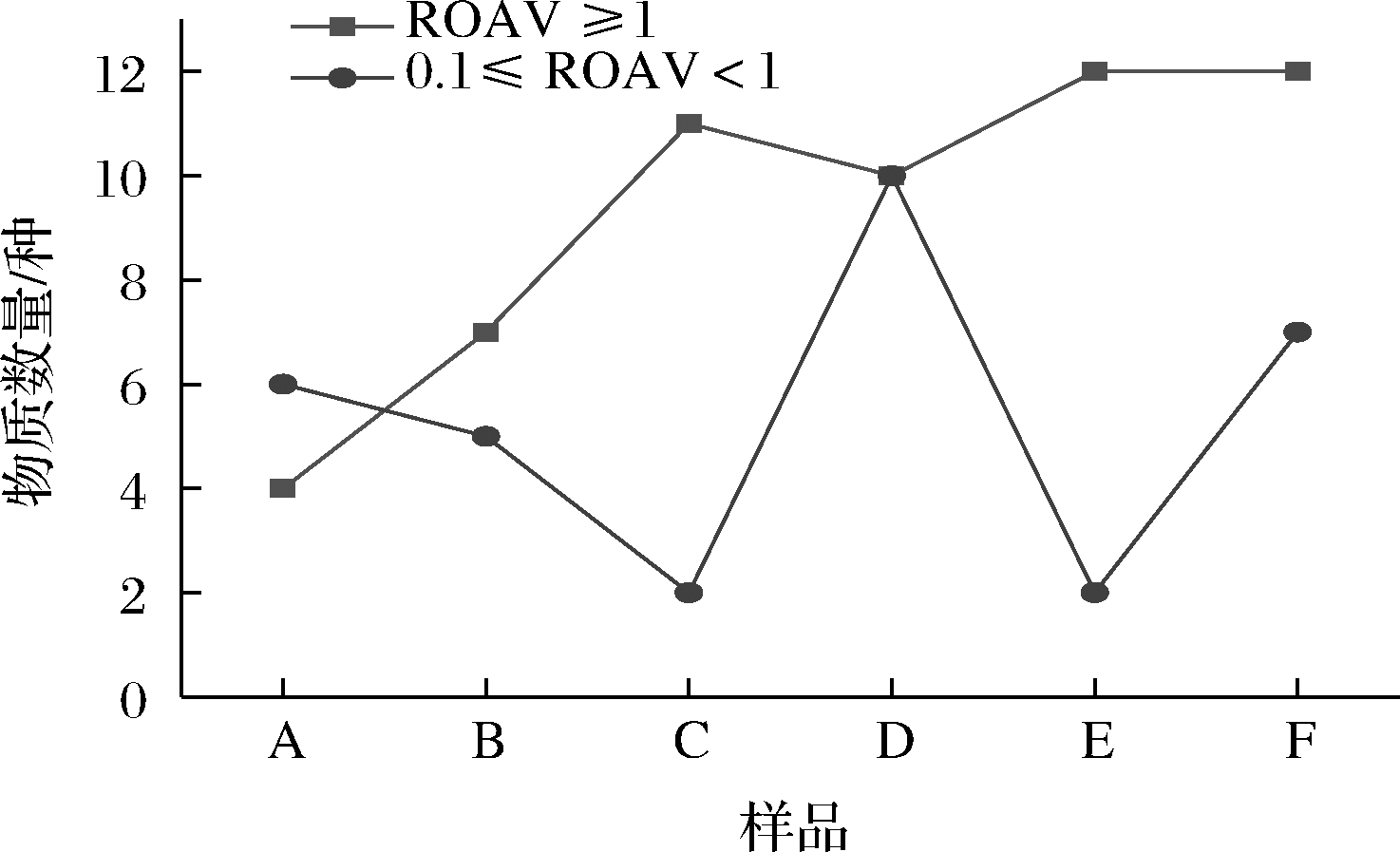
图2 挂糊油炸大球盖菇菌柄不同加工过程ROAV≥1以及0.1≤ROAV<1的挥发性风味物质数量
Fig.2 Number of volatile flavor substances with ROAV≥1 and 0.1≤ROAV<1 at different processing stages in the stalk of the deep-fried and battered S.rugoso-annulata
表3 挂糊油炸大球盖菇菌柄不同加工过程挥发性风味物质的ROAV值
Table 3 ROAV of volatile flavor substances in the stalk of the deep-fried and battered S.rugoso-annulata at different processing processes

注:表中“-”表示未检测到此化合物。
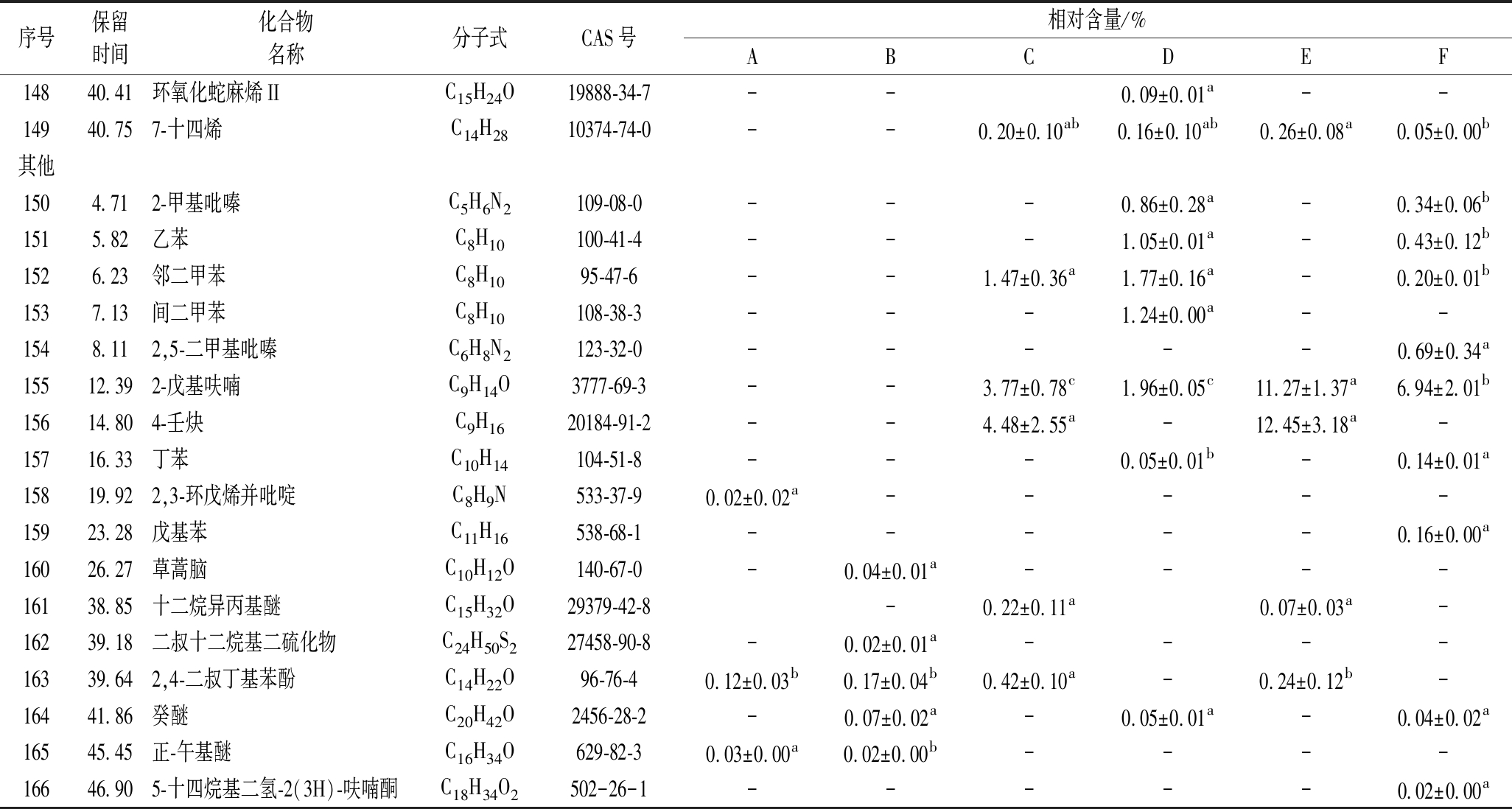
序号化合物名称气味描述[21-22]阈值/(μg/kg)[21,23]ROAVABCDEF1正戊醇脂香、甜香、酒香4 000-<0.01 ---<0.01 2正庚醇脂香、酒香3 -0.34 -0.56 -0.45 31-辛烯-3-醇蘑菇香、青香134.88 72.34 64.8724.63 43.4914.62 4桉叶油醇樟脑香、薰衣草香0.26-3.04 ----52-乙基己醇花香、柑橘香740-<0.01 -0.01 --6正辛醇脂香、柑橘香、玫瑰香230.04 0.04 -0.13 -0.10 7芳樟醇花香、柑橘香60.01 0.33 5.07-1.60-8苯乙醇花香、木香21<0.01 -----91-壬醇脂香、玫瑰香、橙子香20.01 -----10(+)-异薄荷醇薄荷香7--1.70-1.4311D-薄荷醇薄荷香300-----<0.01 12月桂醇脂香、柑橘香66<0.010.01 ---0.01 13(E)-橙花叔醇青香、花香、果香3000.01 <0.01 0.06-0.0114香茅醇花香、柑橘香40--0.02--15异戊醛坚果香、可可香0.2-----1.19 16正己醛脂香、青香、苹果香4.54.16 12.97 75.7221.19 39.7320.40 172-己烯醛青香3.1---0.49 -0.57 18庚醛青香、果香30.01 0.04 1.343.17 0.635.49 193-甲硫基丙醛肉香、果香0.20.55 1.35 ----20α-乙基己醛青香、花香1 000<0.01 -----21苯甲醛杏仁香、果香3-0.20 ----22正辛醛果香0.7---22.88 29.0121.35 23(E,E)-2,4-庚二烯醛青香、鸡肉香30---0.42 -0.29 24苯乙醛甜香、风信子香40.07 0.21 2.630.86 3.110.70 25(E)-2-辛烯醛青香、脂香30.24 0.50 2.645.54 3.745.05 26(E)-4-壬烯醛果香40<0.01 ----0.01 27壬醛脂香、柑橘香、玫瑰香10.36 1.83 74.9047.95 92.3736.74 28(E)-2-壬烯醛柑橘香、甜瓜香0.0654.78 -100.00100.00 100.00100.00 29(E)-4-癸醛柑橘香、青香10---0.18 -0.12 30癸醛脂香、柑橘香0.10.39 1.15 35.9516.15 83.6715.64 31(E,E)-2,4-壬二烯醛酯香、花香0.060.67 --26.41 -14.63 32(E)-2-十一烯醛玫瑰香、柑橘香3---0.17 3.250.08 33椰子醛脂香、椰子香65<0.01 <0.01 -0.01 -<0.01 34紫苏醛木香、辛香、柑橘香25.3---0.14 --35十二醛皂香、柑橘香、紫罗兰香20.02 0.10 0.520.26 0.720.18 362,4-十一碳二烯醛坚果香、柑橘香、甜瓜香250---<0.01 -<0.01 37十三醛脂香、蜡香、柑橘香10 000---<0.01 -<0.01 38十四烷醛脂香、果香60-<0.01 0.04<0.01 0.02<0.01 392-辛酮霉香、酮香、蘑菇香50-----0.09 401-辛烯-3-酮蘑菇香、泥土香0.005100.00 100.00 ----413-辛酮蘑菇香、霉香28 0.02 -----425-癸酮蘑菇香、霉香1 000-----<0.01 432-十三烷酮脂香、蘑菇香500<0.01 <0.01 0.02---44香叶基丙酮青香、花香、果香60<0.01 <0.01 0.09-0.03-45己酸乙酯果香、花香、酒香10.06 -----46乙酸己酯果香、脂香0.040.97 -----47丁酸丁酯果香、脂香100-----<0.01 48(+)-柠檬烯柑橘香、甜香200<0.01 -----49β-石竹烯辛香64-0.03--<0.01 50α-蒎烯松脂香60.390.05512-甲基吡嗪肉香、烤坚果香60---0.07 -0.02 52乙苯芳香29---0.18 -0.06532,5-二甲基吡嗪脂香、巧克力香1.8-----1.50 542-戊基呋喃果香、青香、泥土香6--5.391.62 14.744.54 55草蒿脑果香、薰衣草香7.5-0.01 ----
由图2可知,ROAV≥1的关键风味物质数量在加工过程呈现上升趋势,6组样品中依次为4种、7种、11种、10种、12种和12种;具有重要的修饰作用(0.1≤ROAV<1)的风味物质分别有6种、5种、2种、10种、2种和7种。并且由C组和D组对比、E组和F组对比可知,具有重要修饰作用的物质主要来源于油炸后的面糊外壳。结果表明油炸处理能提高风味物质的丰富度,对于挂糊油炸大球盖菇菌柄风味的形成具有良好地促进作用。
由表3可知,鲜菌柄的关键风味物质主要是1-辛烯-3-酮、1-辛烯-3-醇、(E)-2-壬烯醛和正己醛,风味特征主要集中在蘑菇香、泥土味、青香、脂香和果香;挂糊阶段新增了关键风味物质桉叶油醇,并且3-甲硫基丙醛、壬醛、癸醛从具有重要修饰作用的物质变成了关键风味物质,1-辛烯-3-醇和正己醛的ROAV值有较大幅度提高。油炸后样品的关键风味物质有一定相似,主要集中在正己醛、正辛醛、壬醛以及(E)-2-壬烯醛,其ROAV值均大于20,对产品的风味占据主导作用,同时与其他物质共同发挥效果,出现鸡肉香、烤坚果香、巧克力香等新的香型,共同组成更复杂的风味体系。油脂内的脂肪酸在高温下易热裂解和热氧化产生醇类、醛类、酮类等物质,其中的饱和醛、烯醛和二烯醛等是典型的醛类产物[20],因此推断油炸样品的风味贡献主要来源于油脂。此外,油脂的温度越高,生成醛的种类越多[20],这与180 ℃复炸后的样品检测到的醛类物质最多的结果一致。
2.9 挥发性风味物质主成分分析
PCA是一种多元统计分析技术,通过确定几个主成分因子来代表原始样本中许多复杂且难以找到的变量,然后根据主成分因子在不同样本中的贡献率来评价样本之间的规律性和差异性[24]。采用Origin 2018软件的Principal Component Analysis功能,通过线性变换减少数据维度,并保留样本的主要信息,对挂糊油炸大球盖菇菌柄加工过程的19种关键风味物质(ROAV≥1)进行主成分分析,结果如图3所示,其中PC1和PC2的方差贡献率分别为52.23%和30.26%,累计方差贡献率为82.49%,符合主成分分析的要求。
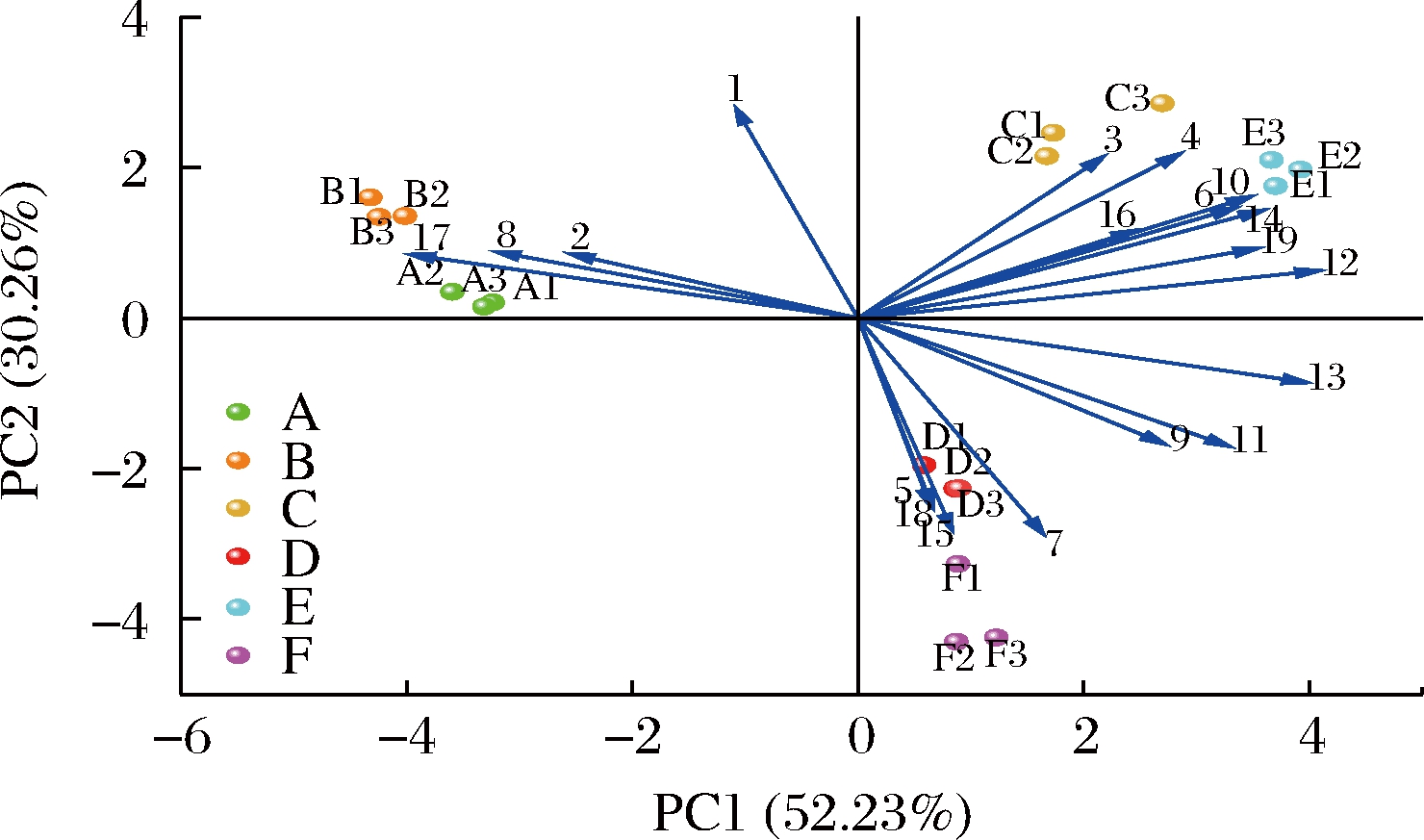
1-1-辛烯-3-醇;2-桉叶油醇;3-芳樟醇;4-(+)-异薄荷醇;5-异戊醛;6-正己醛;7-庚醛;8-3-甲硫基丙醛;9-正辛醛;10-苯乙醛;11-(E)-2-辛烯醛;12-壬醛;13-(E)-2-壬烯醛;14-癸醛;15-(E,E)-2,4-壬二烯醛;16-(E)-2-十一烯醛;17-1-辛烯-3-酮;18-2,5-二甲基吡嗪;19-2-戊基呋喃
图3 不同加工过程样品的主成分分析图
Fig.3 Principal component analysis of samples with different processing processes
注:图中A1、A2、A3表示A组的3个平行,B、C、D、E和F组同理。
在主成分分析图中,同一样品的数据点聚集程度越好,表明同一样品的重复性和稳定性越高[8];不同组样品之间的距离越远,表明其风味差异越明显,并且样品的分布区域和某种挥发性风味物质的分布越接近,说明该物质对其风味贡献越大[25]。由结果可知,油炸前后的样品分布区域明显不同,未油炸的A组(鲜菌柄)和B组(挂糊)均位于第二象限,且分布位置较为接近,说明两者的挥发性风味较为相似,其主要挥发性风味物质为1-辛烯-3-醇、桉叶油醇、3-甲硫基丙醛和1-辛烯-3-酮。C组(预炸菌柄)和E组(复炸菌柄)均位于第一象限,说明风味相似,正己醛、苯乙醛、癸醛等物质分布于这两组附近,对其风味贡献较大。D组(预炸)和F组(复炸)的样品均位于第四象限,典型挥发性风味物质如(E)-2-壬烯醛、(E,E)-2,4-壬二烯醛、庚醛等对这2组的风味具有明显影响。整体来看,油炸前后样品的挥发性风味差异明显,PCA可对不同样品的风味进行较可靠的区分。
2.10 电子鼻分析
电子鼻可灵敏地识别样品中的挥发性风味物质并反映其综合信息。由图4可知,A组和B组的各传感器响应值相近,D组和F组的各响应值相似,C组和E组响应值相似但有一定区别。W3C和W2S这2个传感器在6组样品中均表现较高的响应值,说明芳香族化合物、醇类、醛类和酮类是各组中的重要挥发性风味物质。此外,6组样品在W5S传感器的响应值均较低,证明氮氧化合物含量均较少,但C组和E组的响应值相对较高。包陈力根等[8]在研究中发现,大球盖菇在180 ℃条件下烘烤后氮氧化合物的响应值出现较大幅度提高,与本研究结果一致。相对于A组和B组,W1W和W2W的响应值在D组和F组显著升高,表明油炸后吡嗪、萜烯类和芳香族化合物显著增加。值得注意的是,油炸后的样品(C组和F组)在W5C和W1S的响应值显著高于鲜菌柄(A组),说明油炸后烃类物质增加明显。研究表明,油脂在高温条件下会产生大量自由基,导致其中的三酰基甘油水解产生游离脂肪酸,并进一步裂解成烃类化合物[20],因此推测油炸样品中增加的烃类物质主要来源于油脂裂解。综上所述,电子鼻可准确区分油炸前和油炸后的样品,并且挥发性风味物质的丰度表现与HS-SPME-GC-MS的检测结果较一致。

图4 不同加工过程样品的电子鼻传感器响应值雷达图
Fig.4 Radar chart of electronic nose sensor response values for different process samples
3 结论
以挂糊油炸大球盖菇菌柄为研究对象,采用HS-SPME-GC-MS技术在挂糊油炸大球盖菇菌柄加工过程中共检出166种挥发性风味物质,未油炸阶段的样品以醇类和酯类为主,其中1-辛烯-3-酮是贡献最大的风味化合物;油炸后的样品以醛类挥发性风味物质为主,对整体风味贡献最大的化合物是(E)-2-壬烯醛。PCA分析结果进一步表明,不同加工过程的挥发性风味物质存在较大差异。电子鼻可有效区分油炸前和油炸后样品的挥发性风味物质,其传感器响应值表现与HS-SPME-GC-MS的检测结果较一致。整体而言,油炸后风味物质的丰富度明显提高,其主要来源于大球盖菇特有的食用菌风味、油脂高温条件下所产生的脂香类物质以及面糊外壳经高温炸制所产生的杂环类物质三方面,其综合效果使样品的风味体系更为复杂,形成良好的风味特征。本文探究了挂糊油炸大球盖菇菌柄加工过程中的风味变化规律,为大球盖菇的风味研究以及拓宽大球盖菇的产品形式提供了理论参考。
[1] 金明枝. 大球盖菇多糖的结构表征、化学修饰及生物活性研究[D].合肥:合肥工业大学, 2021.
JIN M Z.Structure characterization, chemical modification and biological activity of polysaccharides from Stropharia rugosoannulata[D].Hefei:Hefei University of Technology, 2021.
[2] 高欢, 包怡红.大球盖菇保健功能与保鲜加工研究进展[J].食品与发酵工业, 2017, 43(12):277-282.
GAO H, BAO Y H.A review of health functions of Stropharia rugoso-annulata and its fresh keep processing technology[J].Food and Fermentation Industries, 2017, 43(12):277-282.
[3] 叶建强, 蓝桃菊, 黄卓忠, 等.大球盖菇鲜品各等级菇在栽培过程中的分布规律及经济效益分析[J].中国食用菌, 2021, 40(11):25-31.
YE J Q, LAN T J, HUANG Z Z, et al.Analysis of distributing rules and economic income of the different fresh mushroom grades of Stropharia rugosoannulata during cultivation[J].Edible Fungi of China, 2021, 40(11):25-31.
[4] SUN L B, ZHANG Z Y, XIN G, et al.Advances in umami taste and aroma of edible mushrooms[J].Trends in Food Science &Technology, 2020, 96:176-187.
[5] 樊浩然. 酥肉类菜肴开发中糊料组成与菜肴品质的相关性研究[D].哈尔滨:哈尔滨商业大学, 2020.
FAN H R.Correlation between paste composition and dish quality in the development of crispy meat dishes[D].Harbin:Harbin University of Commerce, 2020.
[6] 王泽华. 油炸金针菇脚工艺优化及其产品品质研究[D].沈阳:沈阳农业大学, 2020.
WANG Z H.Processing optimization and quality of fried Flammulina velutipes’s feet[D].Shenyang:Shenyang Agricultural University, 2020.
[7] ZHANG X T, ZHANG M, ADHIKARI B.Recent developments in frying technologies applied to fresh foods[J].Trends in Food Science &Technology, 2020, 98:68-81.
[8] 包陈力根, 关淳博, 辛明航, 等.HS-SPME-GC-MS结合电子鼻分析烘烤对大球盖菇挥发性风味物质的影响[J].食品科学, 2022,43(14):226-233.
BAO C L G, GUAN C B, XIN M H, et al.To analyze the effects of roasting on volatile flavor compounds of Stropharia rugoso-annulate using HS-SPME-GC-MS and electronic nose[J].Food Science, 2022,43(14):226-233.
[9] HU S, FENG X, HUANG W, et al.Effects of drying methods on non-volatile taste components of Stropharia rugoso-annulata mushrooms[J].LWT, 2020, 127:109428.
[10] 廖林, 贺稚非, 刘悦, 等.基于HS-SPME-GC-MS的卤烤兔肉丁加工过程中挥发性风味物质变化分析[J].食品与发酵工业, 2022, 48(14): 235-243.
LIAO L, HE Z F, LIU Y, et al.Analysis of volatile flavor substances during processing of halogen roast rabbit meat based on HS-SPME-GC-MS[J].Food and Fermentation Industries, 2022, 48(14): 235-243.
[11] 刘登勇, 周光宏, 徐幸莲.确定食品关键风味化合物的一种新方法:“ROAV”法[J].食品科学, 2008, 29(7):370-374.
LIU D Y, ZHOU G H, XU X L.“ROAV” method:A new method for determining key odor compounds of Rugao ham[J].Food Science, 2008, 29(7):370-374.
[12] LI G J, WANG Y, ZHANG Z Q, et al.Mushroom alcohol controls gray mold caused by Botrytis cinerea in harvested fruit via activating the genes involved in jasmonic acid signaling pathway[J].Postharvest Biology and Technology, 2022, 186:111843.
[13] AISALA H, SOLA J, HOPIA A, et al.Odor-contributing volatile compounds of wild edible Nordic mushrooms analyzed with HS-SPME-GC-MS and HS-SPME-GC-O/FID[J].Food Chemistry, 2019, 283:566-578.
[14] HOU H, LIU C, LU X S, et al.Characterization of flavor frame in shiitake mushrooms (Lentinula edodes) detected by HS-GC-IMS coupled with electronic tongue and sensory analysis:Influence of drying techniques[J].LWT, 2021, 146:111402.
[15] XUN W, WANG G Y, ZHANG Y J, et al.Analysis of flavor-related compounds in four edible wild mushroom soups[J].Microchemical Journal, 2020, 159:105548.
[16] ZHANG H Y, PU D D, SUN B G, et al.Characterization and comparison of key aroma compounds in raw and dry porcini mushroom (Boletus edulis) by aroma extract dilution analysis, quantitation and aroma recombination experiments[J].Food Chemistry, 2018, 258:260-268.
[17] GUO Q Y, ADELINA N M, HU J T, et al.Comparative analysis of volatile profiles in four pine-mushrooms using HS-SPME/GC-MS and E-nose[J].Food Control, 2022, 134:108711.
[18] 朱文政, 严顺阳, 徐艳, 等.顶空固相微萃取-气质联用分析不同烹制时间红烧肉挥发性风味成分[J].食品与发酵工业, 2021, 47(2):247-253.
ZHU W Z, YAN S Y, XU Y, et al.Analysis of volatile flavor components of braised pork with different cooking time by SPME-GC-MS[J].Food and Fermentation Industries, 2021, 47(2):247-253.
[19] DU X F, SISSONS J, SHANKS M, et al.Aroma and flavor profile of raw and roasted Agaricus bisporus mushrooms using a panel trained with aroma chemicals[J].LWT, 2021, 138:110596.
[20] 李文娟, 吴彦, 李从虎, 等.油脂热加工产生醛类的机理及影响因素研究进展[J].中国粮油学报, 2019, 34(8):139-146.
LI W J, WU Y, LI C H, et al.Research progress on the mechanism and influencing factors of aldehydes production in oil hot work[J].Journal of the Chinese Cereals and Oils Association, 2019, 34(8):139-146.
[21] 孙宝国. 食用调香术[M].北京:化学工业出版社, 2010.
SUN B G.Food Flavoring[M].Beijing:Chemical Industry Press, 2010.
[22] ACHEMS, AACC, ACS, et al.TGSC Information System[EB/OL].2022.http://thegoodscentscompany.com/.
[23] 刘强, 冒德寿, 汤峨, 等.化合物香味阈值汇编[M].第二版.北京:科学出版社, 2015.
LIU Q, MAO D S, TANG E, et al.Compilations of Flavour Threshold Values in Water and Other Media[M].2nd ed.Beijing:Science Press, 2015.
[24] LI M Q, YANG R W, ZHANG H, et al.Development of a flavor fingerprint by HS-GC-IMS with PCA for volatile compounds of Tricholoma matsutake Singer[J].Food Chemistry, 2019, 290:32-39.
[25] 李芳. 硬脂鱼油的品质特征及在火锅底料中的应用研究[D].重庆:西南大学, 2021.
LI F.Study on the quality characteristics of fish oil stearin and its application in hotpot seasoning[D].Chongqing:Southwest University, 2021.