淀粉作为自然界存量丰富的天然多糖高分子,是一种有前景的低成本、可再生、丰富的生物可降解胶凝剂。1995年,GLENN等[1]首次利用淀粉成功制备出气凝胶材料,并将其称作“微孔泡沫”,该气凝胶具有较低的密度(0.10~0.24 g/cm3),导热系数低至0.024~0.043 W/(m·K),是优良的环保型保温材料,其奠定了淀粉在气凝胶研制领域中的基础。与纤维素[2-5]、海藻酸钠[6-7]、壳聚糖[8-11]等多糖高分子相比,淀粉制备气凝胶的工艺流程更加清洁环保,其溶解过程只需水浴加热不需要用到浓度较高的碱性溶液作为溶剂,因此不会有污染环境的废液产生,且在没有交联剂的情况下自身就可形成完整的三维网络结构,制备过程简单且成本较低,适合实际生产操作情况。此外,淀粉分子具有许多反应活性较高的羟基,可以作为多种改性反应的结合位点,这使得淀粉气凝胶容易进行表面改性,有助于拓展淀粉气凝胶的应用范围。
淀粉基气凝胶已用作吸附材料[12-14]以及合成新型功能材料的基材[15],并被广泛应用于生物活性化合物的包封和控制释放、生物医学用途和组织工程等领域[16-17]。淀粉基气凝胶优异的孔隙结构使其具有作为一种新型可生物降解的隔热保温[18]以及活性包装材料的巨大应用潜力,FRANCO等[19]用超临界二氧化碳吸附法,将具有良好抗氧化和抗菌性能的黄酮类化合物槲皮素吸附在玉米淀粉气凝胶上,通过体外溶出试验,证明该复合体系可用于食品保鲜的活性包装。而其良好的隔热性能使其可以成为目前广泛用于保持冷藏或热包装食品和饮料所需温度的发泡聚苯乙烯的一种有益替代品。
虽然目前关于淀粉气凝胶的研究较多[20-21],但多集中于某一特定种类淀粉制备气凝胶,对不同来源淀粉制备气凝胶的差异性缺乏详实论证。淀粉颗粒由支链淀粉组成的结晶区和直链淀粉组成的非结晶区交替排列而构成,淀粉糊化时结晶区被破坏,直链淀粉溶出,凝胶时直链淀粉沉积缠绕构成凝胶网络的骨架结构,同时支链淀粉重新与直链淀粉进行连接从而丰富凝胶网络结构。不同来源的淀粉由于其直链淀粉和支链淀粉含量有很大差异,凝胶网络结构也有很大区别,这对气凝胶的性能有很大影响。研究不同来源淀粉制备气凝胶的性能差异可为未来选择合适的淀粉制备性能优异的气凝胶提供参考。此外,由于淀粉的亲水性较大,使天然淀粉气凝胶对水有高度的敏感性,在环境湿度改变时其性能会发生变化,导致其应用受到限制,因此必须对其进行疏水改性以改善其水敏性,提高其实际应用能力。目前针对多糖气凝胶疏水改性的研究多采用两步法进行表面改性,即先制备气凝胶后对其进行表面接枝疏水基团进行改性,而在溶胶-凝胶阶段内添加疏水试剂通过一步法制备疏水气凝胶的研究较少。
本研究的主要目的是探索淀粉类型对气凝胶性能的影响,并对气凝胶进行疏水改性,使其更具有功能性。主要从以下几个方面展开研究:a)研究淀粉种类和直链/支链比例对气凝胶的形态和性质的影响,通过溶解-回生-冷冻干燥的途径制备气凝胶,探究不同种类的淀粉制备得到的气凝胶之间的差异。b)通过对气凝胶的密度、体积収缩、孔隙率、热导率等性质进行测定并详细分析,经过比较选出最适宜做气凝胶保温材料的淀粉类型。c)利用交联剂制备交联改性淀粉气凝胶来达到降低淀粉气凝胶吸水性的目的。d)利用纳米SiO2和其他硅烷助剂制备疏水改性剂,采用内添法对淀粉气凝胶做进一步疏水改性,提升淀粉气凝胶的疏水性能。
1 材料与方法
1.1 材料与试剂
普通玉米淀粉(normal corn starch,NCS),食品级,海宁枫园食品有限公司;豌豆淀粉(pea starch,PES)、马铃薯淀粉(potato starch,NPS)、小麦淀粉(wheat starch,NWS),食品级,昆山臻乐门食品有限公司;木薯淀粉(tapioca starch,NTS),食品级,泰国粉业有限公司;蜡质玉米淀粉(waxy corn starch,WCS),食品级,美国康生物制品公司;柠檬酸(citric acid,CA),食品级,潍坊英轩实业有限公司;次亚磷酸钠(sodium hypophosphite,SHP),分析纯,天津市科密欧化学试剂有限公司;气相疏水型纳米SiO2,分析纯,河北博诚冶金科研中心;无水乙醇,分析纯,江苏强盛功能化学股份有限公司;甲基三甲氧基硅烷(methyltrimethoxysilane,MTMS)、十六烷基三甲氧基硅烷(hexadecyltrimethoxysilan,HDTMS),分析纯,罗恩试剂。
1.2 仪器与设备
L5S型紫外可见分光光度计,上海仪电分析仪器有限公司;Quanta FEG场发射环境扫描电子显微镜,美国Perkin/Elmer有限公司;DRE-Ⅲ型多功能快速导热系数测试仪(瞬态平面热源法、HotDisk法),湖南湘潭湘仪仪器有限公司;Data Physics OCA2接触角测量仪,德国Dataphysics公司;AL104型电子天平(精确度0.000 1 g),梅特勒-托利多仪器(上海)有限公司;DF-101T-5型集热式磁力搅拌器,深圳鼎鑫宜实验仪器设备有限公司;AF-200Q型搅拌器,昆山市千灯镇宇曦五金机电经营部;Scientz-系列N型冷冻干燥机,宁波新芝生物科技有限公司;BCD-160TMPQ冰箱,青岛海尔股份有限公司。
1.3 实验过程
淀粉气凝胶的生产步骤如图1所示。通过糊化将淀粉溶液转化为水凝胶,通过低温冷冻将凝胶中的水凝固成固态,最后通过真空冷冻干燥将冷冻凝胶转化为气凝胶。

图1 淀粉气凝胶的制备流程图
Fig.1 Flow chart of starch aerogel preparation
1.3.1 不同种类淀粉气凝胶的制备
称取一定量的NCS、PES、NPS、NWS、NTS、WCS 6种类型的淀粉,加水配制成80 g/L的淀粉乳液。随后将其置于95 ℃水浴条件下糊化40 min,糊化过程以600 r/min的速度搅拌使淀粉颗粒充分溶解。待糊化完成后立即将糊液倒入40 mm×20 mm×9 mm的硅胶模具中并用保鲜膜覆盖防止其水分蒸发,待模具中淀粉糊液冷却到室温后将其转移至4 ℃的冰箱中老化成型24 h,获得淀粉水凝胶。回生完成后将该水凝胶移至低温冰箱预冻7 h。最后将冷冻凝胶脱模放入冷阱温度-65 ℃、真空度为1 Pa的冷冻干燥机中干燥40 h,得到以不同种类淀粉为原料的淀粉气凝胶。记作NCA(普通玉米淀粉气凝胶)、WCA(蜡质玉米淀粉气凝胶)、PEA(豌豆淀粉气凝胶)、NPA(马铃薯淀粉气凝胶)、NWA(小麦淀粉气凝胶)、NTA(木薯淀粉气凝胶。)
1.3.2 改性淀粉气凝胶的制备
1.3.2.1 交联改性淀粉气凝胶
在1.3.1节糊化步骤前,加入3%(质量分数)交联剂[m(CA):m(SHP)=2:1],搅拌使其均匀分散,其余处理步骤相同,干燥后即可得到交联改性的淀粉气凝胶,记作CA/NTA。
1.3.2.2 硅烷疏水改性淀粉气凝胶
取一定量疏水纳米SiO2粉末、MTMS和HDTMS添加到烧杯中,加入无水乙醇溶液作为溶剂至100 mL,将所得混合溶液用搅拌器搅拌1 h使溶液均匀分散,得到混合疏水溶液(MTMS-HDTMS-SiO2,简称M-H-SiO2)。在1.3.2.1节的基础上在糊化前加入15 mL混合疏水溶液,其余步骤相同即可得到硅烷疏水改性的淀粉气凝胶,记作M-H-SiO2/CA/NTA。
1.4 测试与表征
1.4.1 不同类型淀粉糊的透明度
利用分光光度法对淀粉糊的透明度进行测试,用蒸馏水作为空白对照,设定波长为400~700 nm全波长扫描。由于淀粉水凝胶的成分较为单一,几种淀粉糊对吸收波长均无特异性,但淀粉糊的透光率随波长的增加而增加,因此选择700 nm处为测定波长,测定淀粉糊的透光率,以透光率的值表示淀粉糊的透明度。
1.4.2 淀粉气凝胶的形貌特征
取一块制备好的淀粉气凝胶,放置于直尺旁边,使用手机相机进行拍摄,得到气凝胶的宏观形貌特征照片。
取一块制备好的淀粉气凝胶并淬断成合适大小的薄片,使用扫描电子显微镜(scanning electron microscopy,SEM)观察其内部断面。将一小片气凝胶粘贴在载物台上,使用导电胶将薄片上表面与载物台相连,之后喷金300 s。将样品及载物台放入电子显微镜,抽真空后进行观察。
1.4.3 淀粉气凝胶的体积收缩
在冷冻干燥过程中,生物气凝胶的前体会收缩。收缩程度主要取决于多糖的类型及其浓度(浓度越高,收缩期越短)。由于本次实验使用的浓度相同,故气凝胶的收缩程度主要受多糖类型影响。收缩率(ΔV)的计算如公式(1)所示:
(1)
式中:V0表示凝固前淀粉凝胶的体积;V1表示干燥后的体积。
1.4.4 淀粉气凝胶的密度
由于制备的气凝胶表面存在不均匀的凹凸,故采用排阻法测量体积。在量筒中用直径0.8 mm的玻璃珠垫底,之后放入气凝胶,再倒入适量玻璃珠覆盖整块气凝胶,轻轻抖动振荡使玻璃珠填满缝隙,记录体积。之后取出气凝胶,测量玻璃珠的体积,气凝胶的质量使用分析天平称重得到。密度的计算如公式(2)所示:
(2)
式中:M为气凝胶的质量;V1为玻璃珠和气凝胶的体积;V2为玻璃珠的体积。
1.4.5 淀粉气凝胶的孔隙率
孔隙率是淀粉气凝胶的一个重要参数,根据王唯等[15]估算气凝胶的孔隙率。首先称量干燥状态的气凝胶样品,之后将其完全浸入装有乙醇的容器中,然后将容器放入真空干燥箱中并抽真空,直到样品中没有气泡溢出,取出容器并称重。从容器中取出样品后,称量含有残余乙醇的容器。具体流程见图2,样品的孔隙率按公式(3)计算:

图2 孔隙率测量流程图
Fig.2 Flow chart of porosity measurement
孔隙率![]()
(3)
式中:m0为干燥的气凝胶的质量;m1为容器加气凝胶和乙醇的质量;m2取出气凝胶后为残余乙醇的质量。
1.4.6 淀粉气凝胶的隔热性能
气凝胶的隔热性能利用导热系数来表征,试样尺寸为40 mm×20 mm×9 mm,测试温度为室温,采样时间为160 s,将探头放置在2个需要测量热性能的样本平面之间,把探头和样本牢牢地装配或固定在实验台上,多次测量取平均值。
1.4.7 淀粉气凝胶的疏水性能
气凝胶的疏水性能利用水滴滴在样品表面的接触角来表征,每次滴到样品表面的液滴体积约5 μL,为减小测量误差选取样品表面5个不同点进行测量,最终结果为5次接触角测量的平均值。
2 结果与分析
2.1 不同种类淀粉糊的透明度
淀粉糊液透明度高低对淀粉气凝胶的用途有一定的影响,若采用淀粉基气凝胶作为功能填料制备涂料,填料的透明度将会直接影响涂层的颜色。表1和图3的结果表明在同一生产条件下NPS糊液的透明度最高,达到了58.33%,NTS和WCS糊液透明度次之,分别为32.67%和28.48%,且明显优于PES、NCS和NWS,NWS糊液透明度最差。这主要是因为NPS颗粒的直径最大,淀粉加热糊化后水分子更容易进入淀粉颗粒内部,使淀粉颗粒溶解更充分,从而透明度得以提高。
表1 不同种类淀粉糊的吸光度和透光率
Table 1 Absorbance and transmittance of starch paste from different sources
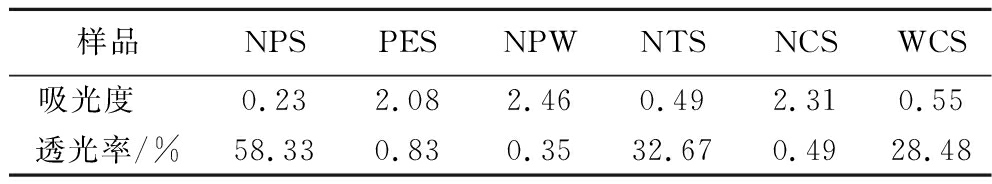
样品NPSPESNPWNTSNCSWCS吸光度 0.232.082.460.492.310.55透光率/%58.330.830.3532.670.4928.48
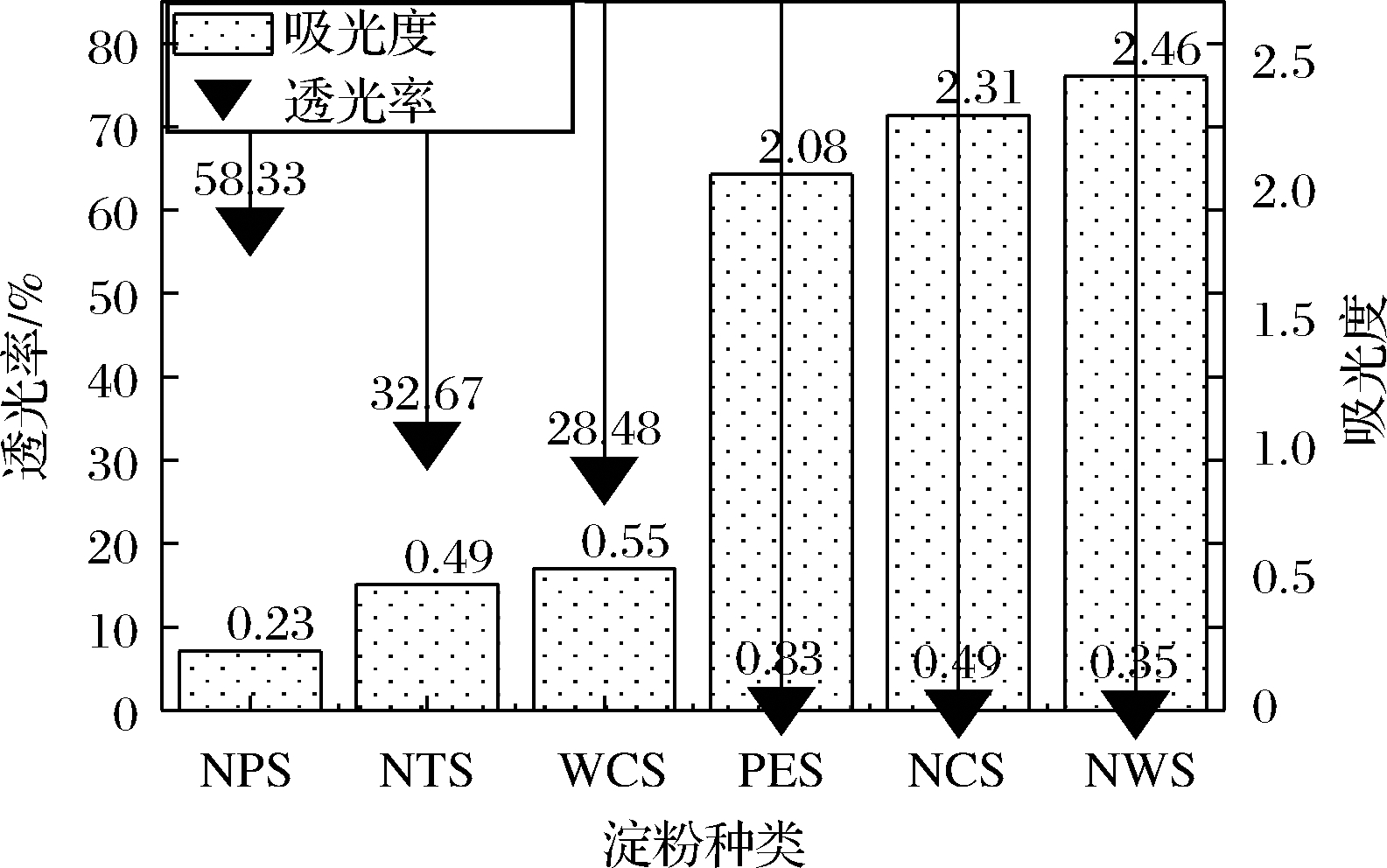
图3 不同类型淀粉糊的吸光度和透光率
Fig.3 Absorbance and transmittance of different types of starch pastes
2.2 淀粉气凝胶的形貌特征
淀粉气凝胶是多个微观淀粉颗粒经历糊化、重组、干燥后形成的均一整体,不同种类淀粉由于其自身颜色以及直链/支链比例有所差异,制备出的气凝胶材料在宏观表现上就已经表现出了极大的差异以及特殊性。
图4是不同种类淀粉气凝胶的宏观照片,6种类型的气凝胶均呈现规整的四方体结构。WCA与NCA差异较大,NCA整体颜色偏黄,且表面出现部分裂痕,WCA整体透光性较好,这与其淀粉糊本身透明度较高有关,仔细观察可以发现其结构呈现为多层较薄透光的片层状结构,与其他气凝胶的无规则多孔结构有着较大的差异。NWA表面有肉眼可见的严重裂痕,这可能是由于小麦淀粉颗粒较小,糊化阶段水分子难以进入颗粒内部,部分水分子仍留在外面,冷冻阶段冰晶快速生长破坏了材料内部结构,导致材料表面有明显裂纹。

a-NPA;b-NTA;c-PEA;d-WCA;e-NCA;f-NWA
图4 不同种类淀粉气凝胶的宏观照片
Fig.4 Macroscopic photographs of starch aerogels from different sources
对比标尺可知,本次实验条件下PEA长边变化量ΔL为0.6,尺寸有较大程度的收缩,这与其凝胶阶段水分大量析出有关,与其他气凝胶细密的孔洞有所不同,PEA表面可以看到明显粗大且分布不均的孔洞及部分裂痕。NPA和NTA均保持了较好的形态,基本没有回缩且孔洞细密,肉眼很难分辨,不同的是NTA表面也有部分片层状结构,这与图5中展示的SEM结果一致。

a-NPA;b-NTA;c-CA/NTA;d-M-H-SiO2/CA/NTA
图5 马铃薯淀粉气凝胶及改性前后木薯淀粉气凝胶的SEM图
Fig.5 SEM images of NPA and NTA before and after modification
图5为改性前后气凝胶的SEM图,可以明显看出,未添加交联剂的NTA(图5-b)呈现出较大且不均匀的孔洞,孔壁较厚,并且具有部分片层结构。添加交联剂后气凝胶的形貌结构呈现出变化,一方面,气凝胶的片层结构消失,气凝胶单个孔洞的平均直径减小,孔洞密度增加,其SEM图像直观地展现出细密的孔洞。另一方面,孔洞呈现出更多不规则的形状,不仅具有较大的开孔结构,同时也出现很多细密的闭孔结构,整体结构变得更加复杂。这些变化都与交联剂的添加有关。交联剂本身可以为淀粉分子之间提供更多的连接位点,使得淀粉分子之间在凝胶老化阶段能够更快更多地结合在一起,因此呈现出了较为密集的孔洞结构(图5-c)。在添加交联剂的基础上加入M-H-SiO2溶液,所得改性气凝胶的形态发生变化,孔壁由图5-c的锯齿状变得更加光滑,粗糙度得到改善,且孔洞变得更加细密(图5-d),这可能是由于将M-H-SiO2溶液加入淀粉糊液后,在凝胶形成过程中,随着水的蒸发,M-H-SiO2纳米复合颗粒与淀粉颗粒逐渐靠近并排列紧密,使得HDTMS聚结,SiO2纳米复合颗粒与长链十六烷基及淀粉颗粒相互扩散和缠绕,形成孔洞更加致密的M-H-SiO2改性淀粉气凝胶。
2.3 不同类型淀粉气凝胶的体积收缩特性
直链淀粉含量对淀粉的性质影响极大,使用不同直链淀粉含量的淀粉制备气凝胶也会有极大的差异。本次实验直链淀粉含量测定方法参照GB/T 15683—2008《大米 直链淀粉含量测定》,将淀粉完全糊化使得直链淀粉溶出,直链淀粉与碘成比例形成复合物,利用分光光度法测得直链淀粉含量。由图6可知直链/支链比例不同的6种类型淀粉气凝胶的体积变化,其中WCA的收缩率最低,为15.99%,PEA的收缩率最大,达到了34.33%,这主要是由于PES中直链含量高达38.27%,较其他类型的淀粉高,直链淀粉的抗老化性能差,在凝胶形成过程中,直链淀粉逐渐沉积导致水分析出,使得PEA在凝胶阶段就产生较大的体积变化,随着干燥过程水分的减少其收缩更加明显。随着支链淀粉含量的升高,淀粉与水结合能力逐渐提高,且支链淀粉的超长分叉结构能够在老化过程中提供分子间更多的结合位点,因此,支链淀粉含量较高气凝胶的网络结构更加坚固和密实,收缩率较低。
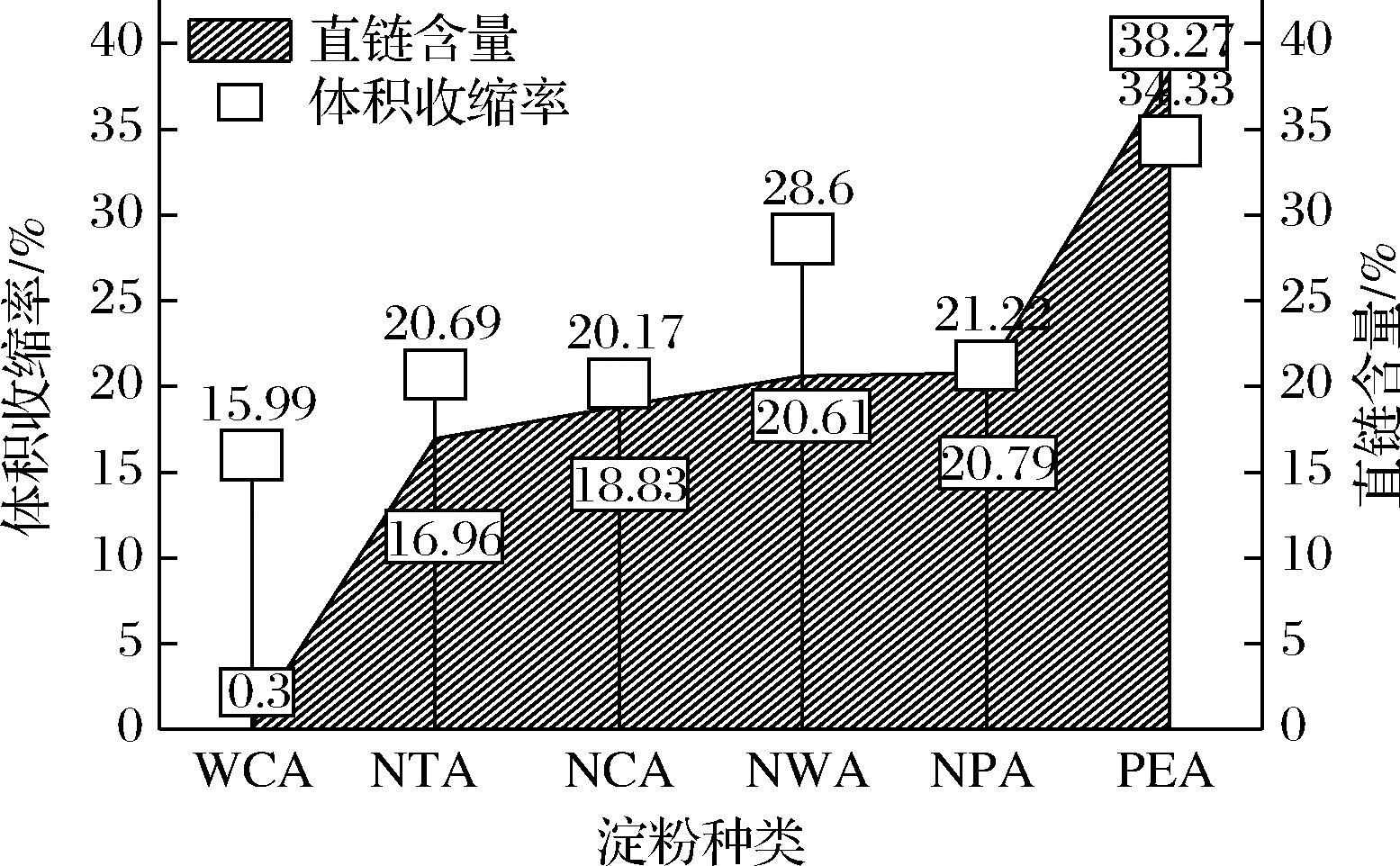
图6 不同种类淀粉中直链含量及对应气凝胶的体积収缩率
Fig.6 Straight chain content in starch from different sources and the corresponding volume shrinkage of aerogel
2.4 淀粉气凝胶的密度
图7所示为6种不同种类淀粉气凝胶的密度,由柱状图可知PEA的密度最大。主要是由于PES中直链淀粉含量较其他类型的淀粉高,老化回生阶段凝胶形成过程中水分析出导致的体积减小,符合图4中观测的气凝胶宏观形貌特征。WCA的密度略小于NCA,这是由于支链淀粉对水分有着更强的亲和力,形成的凝胶中更易存水,在凝胶形成过程中未有明显析水现象,气凝胶形成时体积收缩相较NCA小,因此密度略低。NPA表现出最低的密度,这可能是由于NPS颗粒较大(直径5~100 nm),加热糊化时水分子更易进入淀粉颗粒内部,使得淀粉颗粒充分分散。总之,不发生明显析水的气凝胶密度基本没有变化,PEA的密度升高主要是由于凝胶步骤中的严重析水导致体积收缩的影响。
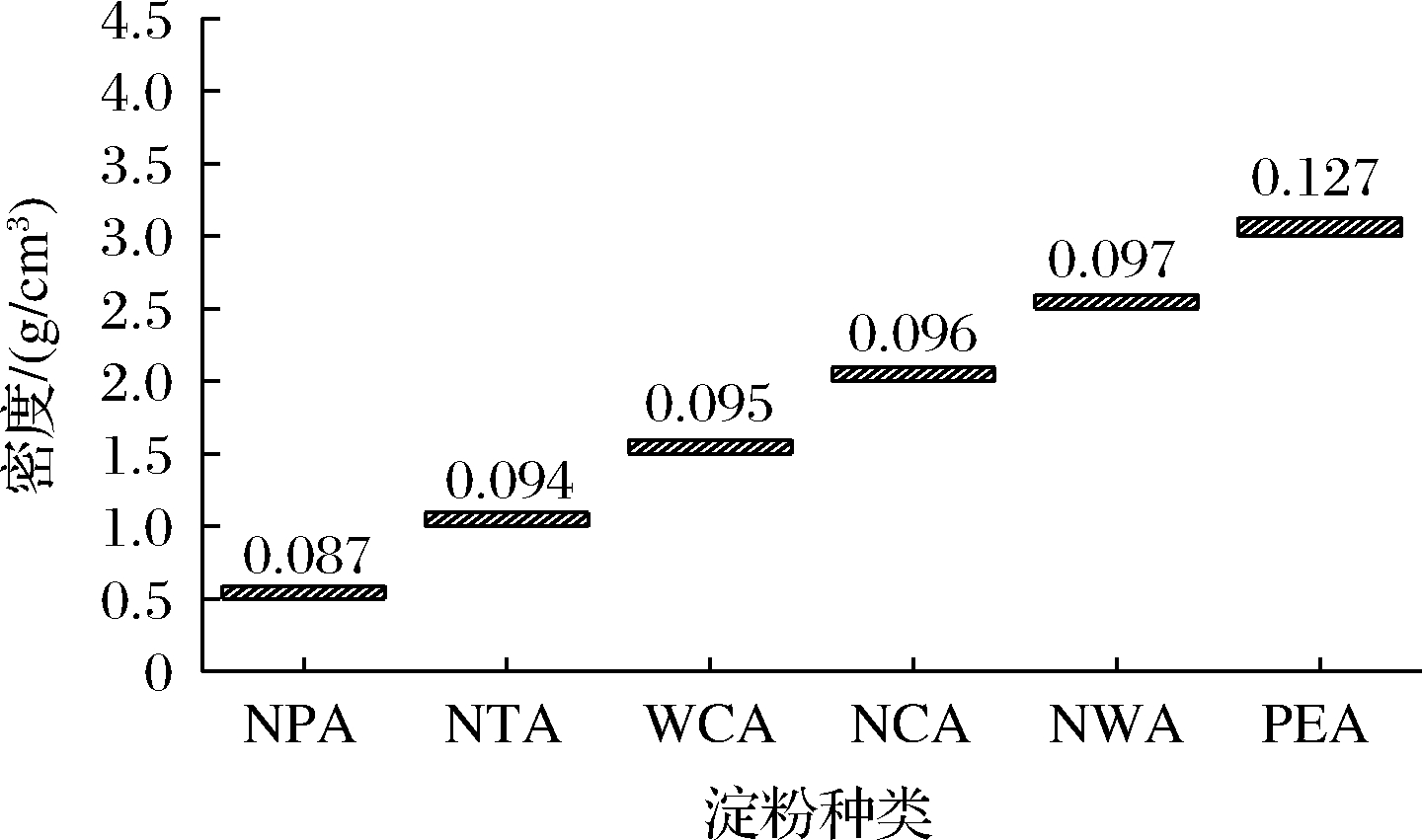
图7 不同种类淀粉气凝胶的密度
Fig.7 Density of starch aerogel from different sources
表2展示了改性前后木薯淀粉气凝胶的密度变化,结果表明,交联以及硅烷化疏水改性会略微提高气凝胶的密度,但交联和疏水试剂复合改性与只加交联剂对气凝胶密度的影响并无显著性差异,说明加入自制疏水试剂不仅不会显著影响气凝胶的密度反而会使其疏水性更优异。改性气凝胶有更加坚实的网络结构和更加密集的孔洞,片层结构消失,孔壁增加,故而密度略微上升。
表2 交联及疏水改性对木薯淀粉气凝胶密度的影响
Table 2 Effect of cross-linking and hydrophobic modification on the density of NTS starch aerogel
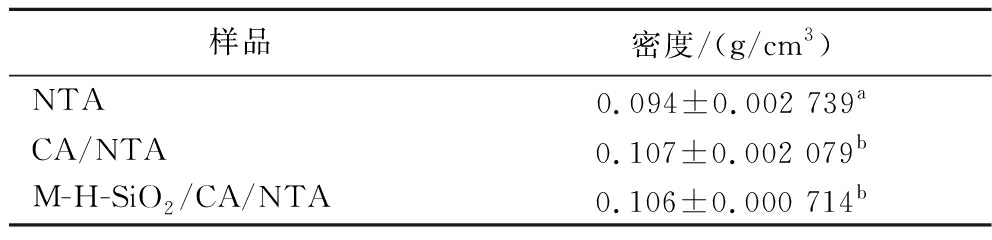
样品密度/(g/cm3)NTA0.094±0.002 739aCA/NTA0.107±0.002 079bM-H-SiO2/CA/NTA0.106±0.000 714b
注:同列不同小写字母代表显著性差异(P≤0.05)。
2.5 不同种类淀粉气凝胶的孔隙率
图8显示了6种类型淀粉气凝胶的孔隙率高低,由图可知NCA和WCA的孔隙率无明显差异,这也与图7中两者密度研究结果一致,PEA的孔隙率略低,这可能是由于PES本身直链含量较其他类型淀粉高,在凝胶形成阶段直链淀粉沉积缠绕阻碍了支链淀粉的伸展,同时直链淀粉沉积引起了PES凝胶的体积收缩,导致部分孔隙塌陷。NPA孔隙率最低,仅为74.8%,这可能是由于凝胶阶段部分区域未形成网络,此结果与SEM显示结果相同(图5-a)。
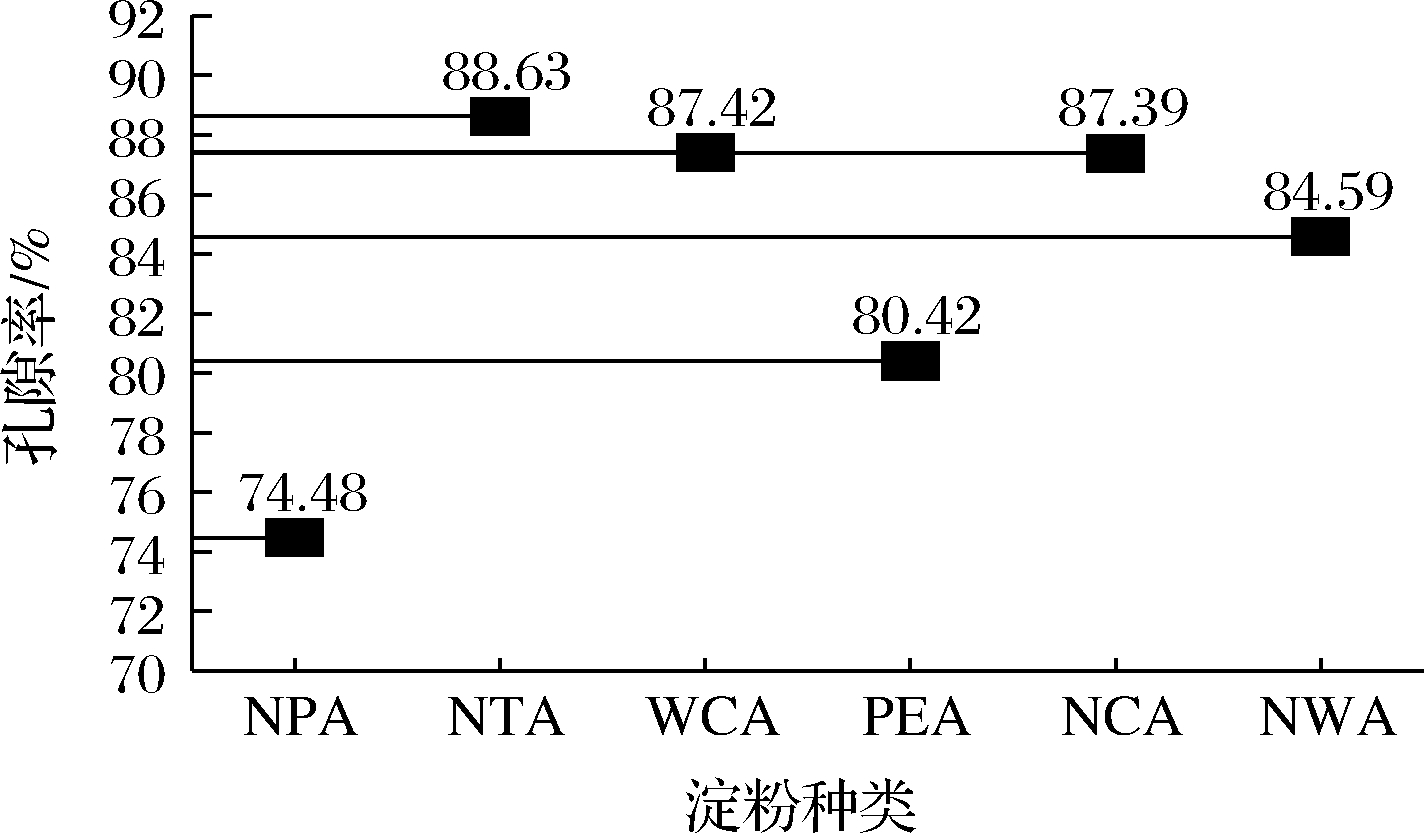
图8 不同类型淀粉气凝胶的孔隙率
Fig.8 Porosity of different types of starch aerogels
2.6 淀粉气凝胶的导热系数
淀粉气凝胶的导热率测试结果如图9所示。GB/T 4272—2008《设备及管道绝热技术通则》中指出,在平均温度为298 K(25 ℃)时,导热系数≤0.08 W/(m·K)的材料称为保温材料,而导热系数≤0.05 W/(m·K)高效保温材料。由图9可知,6种类型的淀粉气凝胶均符合保温材料的要求,其中NTA、NPA以及WCA均符合高效保温材料的要求。
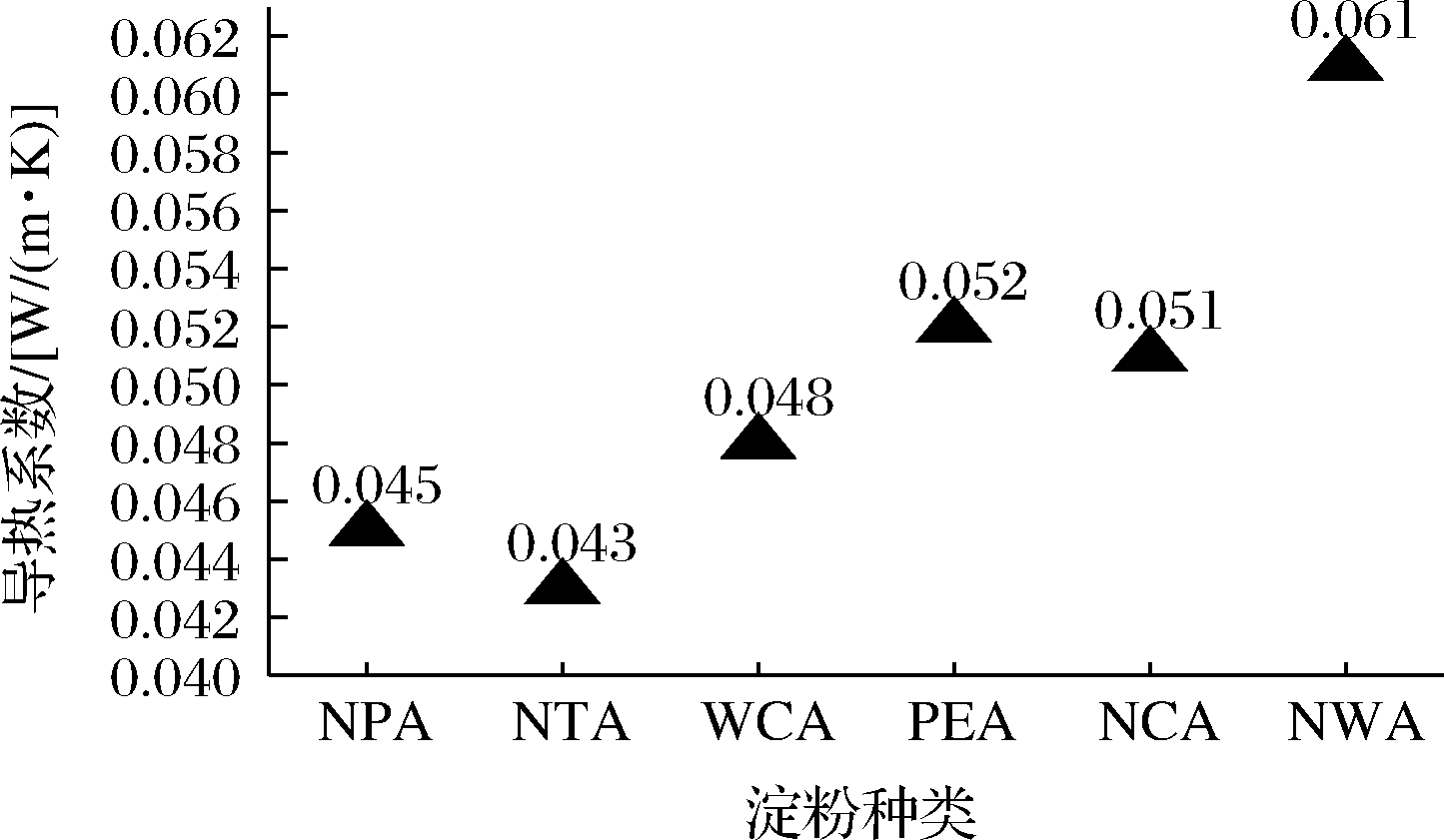
图9 不同种类淀粉气凝胶的导热系数
Fig.9 Thermal conductivity of starch aerogels from different sources
表3利用均值比较中的单因素ANOVA分析法对于6种类型淀粉气凝胶导热系数的差异性给出了直观的展示。由表3可知,6种类型的淀粉气凝胶的导热系数有显著性差异,这除了与其物质组成(直链/支链比例)有关还和其密度以及内部孔隙结构有关。由表4中相关系数r值的大小可知,密度对于导热系数的影响最大,r密>r直>r孔>0,而密度与淀粉中直链淀粉所占比例有着高度相关性,r=0.71>0.6。直链淀粉含量和密度则与孔隙率呈现负相关性,孔隙率可以直接反映材料的空间占有体积比,表明材料的密实程度,孔隙率越高,材料密实程度越小,内部空气成分占比越高,而空气是良好的热绝缘体,可以有效隔绝热量。NTA的导热系数最低,为0.043 W/(m·K),此结果与密度和孔隙率分析结果一致,NTA具有较低的密度和较高的孔隙率。直链含量最高的PEA的导热系数相对较高,这与其在凝胶网络形成阶段直链淀粉沉积带来体积收缩,造成密度偏大孔隙率降低有关。虽然直链淀粉可以增强淀粉气凝胶的强度,有助于构建凝胶网络,但直链含量过高也会导致孔隙塌陷,因此适当的直链含量可以提高淀粉气凝胶的性能。NWA的导热系数偏大,这是由于NWA在表面及内部有严重裂痕。
表3 不同类型淀粉气凝胶的密度、孔隙率及导热系数
Table 3 Density, porosity, and thermal conductivity of different types of starch aerogels
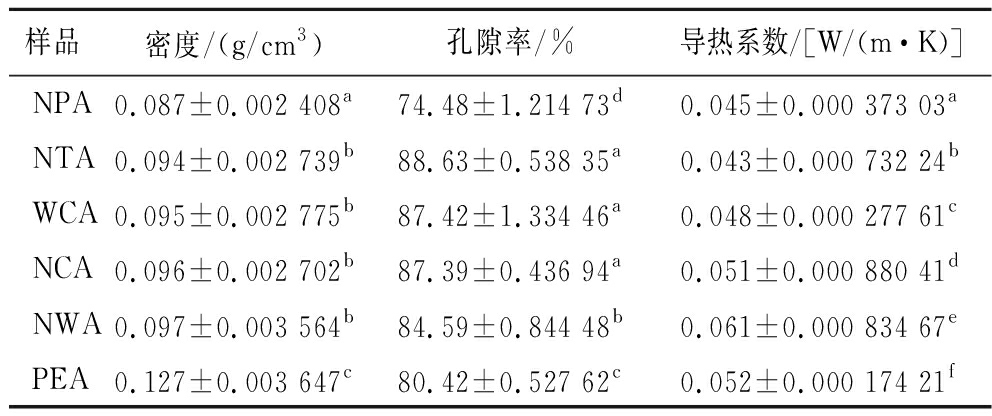
样品密度/(g/cm3)孔隙率/%导热系数/[W/(m·K)]NPA0.087±0.002 408a74.48±1.214 73d0.045±0.000 373 03aNTA0.094±0.002 739b88.63±0.538 35a0.043±0.000 732 24bWCA0.095±0.002 775b87.42±1.334 46a0.048±0.000 277 61cNCA0.096±0.002 702b87.39±0.436 94a0.051±0.000 880 41dNWA0.097±0.003 564b84.59±0.844 48b0.061±0.000 834 67ePEA0.127±0.003 647c80.42±0.527 62c0.052±0.000 174 21f
注:同列不同小写字母代表显著性差异(P≤0.05)。
表4 各个因素之间的相关性
Table 4 Correlation between the factors

相关系数(r)密度孔隙率导热系数直链淀粉含量0.71-0.4640.238密度/-0.0720.318孔隙率//0.07
注:相关系数(r)中数值的大小代表相关程度,r越大相关程度越高;数值的正负表示2个变量的相关方向,r>0正相关,r<0负相关;/表示无。
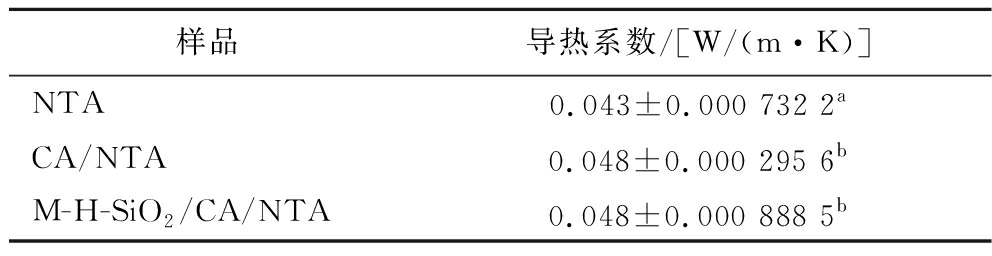
表5显示出疏水改性前后NTA导热性能的差异性,CA交联及M-H-SiO2改性后气凝胶的导热系数均为0.048 W/(m·K),相比于原NTA略微提高,2种改性气凝胶之间未有明显差异,说明M-H-SiO2的加入并不会导致气凝胶整体隔热性能下降,但却可以进一步提高气凝胶疏水性。此处导热系数提高也和表2中展示的2种改性气凝胶的密度略微提高有关。密度增大导致固相传导多于气相传导,因而导热系数略微提高。
表5 交联及疏水改性对木薯淀粉气凝胶导热系数的影响
Table 5 Effect of cross-linking and hydrophobic modification on the thermal insulation properties of NTS starch aerogel
样品导热系数/[W/(m·K)]NTA0.043±0.000 732 2aCA/NTA0.048±0.000 295 6bM-H-SiO2/CA/NTA0.048±0.000 888 5b
注:同列不同小写字母代表显著性差异(P≤0.05)。
2.7 改性淀粉气凝胶的疏水性能
图10为NTA、CA/NTA、M-H-SiO2/CA/NTA的接触角测试图。水珠滴在NTA表面会迅速没入,结构坍塌形成明显凹陷;CA交联木薯淀粉气凝胶则有一定疏水效果,CA是三元酸,分子上含3个羧基,在SHP催化和加热的条件下一分子CA与淀粉分子发生酯化反应形成交联结构。交联反应消耗了淀粉分子的部分羟基使得淀粉亲水性下降,交联改性的木薯淀粉气凝胶水滴滴入立即测量接触角高达133.3°,5 min后再次测量,接触角降至56.7°,这主要是因为气凝胶本身就是多孔结构加之毛细渗透作用使得水分会逐渐渗入气凝胶,交联作用可以降低淀粉气凝胶的亲水性。

a-NTA (0 min);b-CA/NTA (0 min);c-M-H-SiO2/CA/NTA (0 min);d-CA/NTA (5 min);e-M-H-SiO2/CA/NTA (5 min)
图10 淀粉气凝胶的水接触角测试图
Fig.10 Water contact angle test chart of starch aerogel
在CA交联作用的基础上添加M-H-SiO2疏水改性,改性后的M-H-SiO2/CA/NTA水滴滴入立即测量接触角达139.5°,5 min后测量接触角仍有129.5°,且水滴处未出现明显塌陷。一方面,HDTMS、MTMS等疏水硅烷所包裹的SiO2纳米粒子对淀粉颗粒产生了保护层,隐藏了淀粉分子上的部分羟基从而降低了淀粉分子上羟基的利用率,提高了气凝胶的疏水性[22]。另一方面,HDTMS的长链十六烷基具有较低的表面能,可以有效地降低M-H-SiO2-CA/NTA的表面能[22]。此外,包覆作用极大地改善了SiO2纳米颗粒在淀粉基质间的分布,分散和稳定了淀粉糊液,不仅抑制了纳米颗粒在淀粉糊液中团聚也提高了凝胶的稳定性,制备的M-H-SiO2/CA/NTA孔洞致密且均匀,减少了水分的渗透及扩散,从而增强了改性气凝胶的疏水性。
3 结论与讨论
本文研究了淀粉种类及其直链/支链比例对淀粉气凝胶各种性能的影响,依此优选出木薯淀粉是最适合制备淀粉气凝胶的类型。随后用木薯淀粉制备气凝胶,并加入CA对其做交联改性达到增强网络结构,减少水分吸收的目的,并以HDTMS、MTMS包覆疏水纳米SiO2制备疏水溶液,采用一步法将交联剂以及疏水溶液加入淀粉溶液中,制备可生物降解的保温疏水气凝胶,并对其性能进行测试。相关结论如下:
a)淀粉气凝胶的体积收缩率测试:PES直链淀粉含量为38.27%时,收缩率高达34.33%,NWA收缩率次之,为28.6%,这两者表面均有裂痕,而直链淀粉含量为16.96%的NTS的收缩率较小仅为20.69%,因此NTS是最适宜制备气凝胶的原材料。
b)密度、孔隙率测试:通过对6种淀粉气凝胶密度和孔隙率的测试分析可知NTA具有较低的密度(0.094 g/cm3)且孔隙率高达88.63%,适宜用作隔热保温材料。
c)导热系数测试:NTA导热系数低至0.043 W/(m·K);CA/NTA导热系数略微提高,为0.048 W/(m·K);添加自制疏水试剂对气凝胶热导率几乎无影响,M-H-SiO2/CA/NTA 导热系数为0.048 W/(m·K),3种淀粉气凝胶均为高效保温材料。
d)SEM测试:交联和内添M-H-SiO2溶液改性可以增强NTA的网络结构使其具有更加坚实且细密的孔洞。
e)接触胶测试:水滴滴到纯NTA表面会产生明显凹陷;水滴在CA交联气凝胶表面不会立即浸入气凝胶内部,此时接触角高达133.3°,停留5 min后再次测量,接触角降至56.7°,水分全部浸入需要20 min,说明交联可以延缓水分浸入,起到一定的阻水作用;水滴在M-H-SiO2/CA/NTA表面立即测量接触角达139.5°,5 min后测量接触角仍有129.5°。
综上所述,木薯淀粉制备气凝胶的性能最优,且经CA交联和内添M-H-SiO2制备疏水改性木薯淀粉气凝胶的方法是可行并且有效的,制备的M-H-SiO2/CA/NTA是一种良好的疏水保温功能材料,可应用于食品保温领域。
[1] GLENN G M, IRVING D.Starch-based microcellular foams.1995;72:155-161.
[2] 陈苏琴, 邓稳, 左克曼, 等.交联型超双疏细菌纤维素复合气凝胶[J].纤维素科学与技术, 2020, 28(1):1-7.
CHEN S Q, DENG W, ZUO K M, et al.Cross-linked superamphiphobic bacterial cellulose composite aerogel[J].Journal of Cellulose Science and Technology, 2020, 28(1):1-7.
[3] 段一凡, 张光磊, 史新月, 等.纤维素气凝胶的制备与应用研究进展[J].陶瓷学报, 2021, 42(1):36-43.
DUAN Y F, ZHANG G L, SHI X Y, et al.Research progress in preparation and application of cellulose aerogels[J].Journal of Ceramics, 2021, 42(1):36-43.
[4] LI Z D, ZHONG L, ZHANG T, et al.Sustainable, flexible, and superhydrophobic functionalized cellulose aerogel for selective and versatile oil/water separation[J].ACS Sustainable Chemistry &Engineering, 2019, 7(11):9984-9994.
[5] 陈名扬, 沈勇.植物纤维素基水凝胶的制备以及对亚甲基蓝染料吸附的应用进展[J].化工新型材料, 2021, 49(7):47-51.
CHEN M Y, SHEN Y.Preparation of plant cellulose-based hydrogel and removal of methylene blue dye from aqueous solution[J].New Chemical Materials, 2021, 49(7):47-51.
[6] CUADROS T R, ERICES A A, AGUILERA J M.Porous matrix of calcium alginate/gelatin with enhanced properties as scaffold for cell culture[J].Journal of the Mechanical Behavior of Biomedical Materials, 2015, 46:331-342.
[7] 唐茂文. 功能性海藻酸钠基气凝胶的制备及性能研究[D].青岛:青岛大学, 2019.
TANG M W.Preparation and properties of functional sodium alginate-based aerogels[D].Qingdao:Qingdao University, 2019.
[8] TAKESHITA S, KONISHI A, TAKEBAYASHI Y, et al.Aldehyde approach to hydrophobic modification of chitosan aerogels[J].Biomacromolecules, 2017, 18(7):2172-2178.
[9] 王岩. 壳聚糖/阳离子瓜尔胶复合凝胶的制备与应用研究[D].西安:陕西科技大学, 2021.
WANG Y.Preparation and application of chitosan/cationic guar gum composite gel[D].Xi′an:Shaanxi University of Science and Technology, 2021.
[10] 赵进. 壳聚糖气凝胶的结构设计与性能调控[D].成都:四川师范大学, 2021.
ZHAO J.Structure design and performance regulation of chitosan aerogels[D].Chengdu:Sichuan Normal University, 2021.
[11] 朱忠杰. 壳聚糖基复合材料的制备及其油水分离性能研究[D].南京:南京林业大学, 2021.
ZHU Z J.Preparation of chitosan-based composite materials and study on their oil-water separation performance[D].Nanjing:Nanjing Forestry University, 2021.
[12] 高靖阳. 淀粉基气凝胶的制备及其性质测定[D].广州:华南理工大学, 2020.
GAO J Y.Preparation and characterization of starch-based aerogel[D].Guangzhou:South China University of Technology, 2020.
[13] 黄婷, 符珍, 林莹.交联改性对木薯淀粉气凝胶吸附性能的影响[J].宁夏大学学报(自然科学版), 2021, 42(2):167-172.
HUANG T, FU Z, LIN Y.Effect of cross-linking on the adsorption properties of cassava starch aerogel[J].Journal of Ningxia University (Natural Science Edition), 2021, 42(2):167-172.
[14] 谢静, 黄靓澳, 曹雅琪, 等.淀粉微球气凝胶的制备及吸附性能与形态研究[J/OL].中国粮油学报, 2022, 37(12):113-119.
XIE J, HUANG L A, CAO Y Q, et al.Preparation, adsorption properties and morphology of starch microsphere aerogels[J/OL]. Journal of the Chinese Cereals and Oils Association, 2022, 37(12):113-119.
[15] 王唯, 王浩, 匡映, 等.魔芋葡甘聚糖-明胶-淀粉气凝胶过滤材料的结构与性能研究[J].食品工业科技, 2021, 42:48-55.
WANG W, WANG H, KUANG Y, et al.Study on structure and properties of konjac glucomannan-gelatin-starch aerogels as filtration materials[J].Science and Technology of Food Industry, 2021, 42(15):48-55.
[16] MOHAMMADI A, MOGHADDAS J.Mesoporous tablet-shaped potato starch aerogels for loading and release of the poorly water-soluble drug celecoxib[J].Chinese Journal of Chemical Engineering, 2020, 28(7):1778-1787.
[17] MOHAMMADI A, MOGHADDAS J.Mesoporous starch aerogels production as drug delivery matrices:Synthesis optimization, ibuprofen loading, and release property[J].Turkish Journal of Chemistry, 2020, 44(3):614-633.
[18] DRUEL L, BARDL R, VORWERG W, et al.Starch aerogels:A member of the family of thermal superinsulating materials[J].Biomacromolecules, 2017, 18(12):4232-4239.
[19] FRANCO P, ALIAKBARIAN B, PEREGO P, et al.Supercritical adsorption of quercetin on aerogels for active packaging applications[J].Industrial &Engineering Chemistry Research, 2018, 57(44):15105-15113.
[20] BAUDRON V, GURIKOV P, SMIRNOVA I, et al.Porous starch materials via supercritical- and freeze-drying[J].Gels, 2019, 5(1):12.
[21] UBEYITOGULLARI A, BRAHMA S, ROSE D J, et al.In vitro digestibility of nanoporous wheat starch aerogels[J].Journal of Agricultural and Food Chemistry, 2018, 66(36):9490-9497.
[22] 李春颖. 木薯淀粉膜的疏水改性及性能研究[D].南宁:广西大学, 2019.
LI C Y.Hydrophobic modification and properties of cassava tapioca film[D].Nanning:Guangxi University, 2019.