罐头食品为常温预制菜肴的重要品类,由于其种类多样,加工工艺不一,因此对其金属包装提出了苛刻的要求。目前,覆膜铁容器因其优异的耐腐蚀性能已广泛应用于如罐头食品、饮料、啤酒、乳制品等各类食品包装。覆膜铁材料是采用镀铬薄钢板(tin free steel,TFS)作基板,在钢板表面热覆上一层或多层塑料薄膜而制成的复合材料,因此覆膜铁兼具金属板材和塑料薄膜的双重特性[1-4]。覆膜铁用镀铬薄钢板替代了传统的镀锡薄钢板,解决了锡资源短缺的问题;与涂料铁相比,覆膜铁不含双酚A、甲醛等毒性物质,而且其生产过程绿色环保、成本低[5-6],无需使用黏合剂,无挥发性有机物(volatile organic compounds,VOCs)的排放,因此其更能满足当今社会食品安全与绿色环保的要求,是未来金属包装领域的发展方向[7-8]。
覆膜铁的表面聚酯薄膜材料主要有聚对苯二甲酸乙二醇酯(polyethylene terephthalate,PET)、聚对苯二甲酸丁二醇酯(polybutylene terephthalate,PBT)、聚丙烯(polypropylene,PP)等,其中以PET最为常见、综合性能最优、应用最为广泛[9-14]。这些聚酯材料在由单体发生缩聚反应合成聚合物的生产过程中,由于聚合的不完全或发生热降解或水解等作用均可能产生低聚物[15-16]。这些低聚物的种类众多、分子质量大小不一,主要分为线性和环状结构,且具有不同的毒理学特征[17]。目前国内外均无PET和PBT环状低聚物毒理学的研究报道,GB 2762—2022 《食品安全国家标准 食品中污染物限量》中也无环状聚酯低聚物的限量要求,但根据毒理学关注阈值(threshold of toxicological concern,TTC)决策树方法可将其归为Cramer Ⅲ类结构[18],大量摄入也可能存在健康风险。
尽管国内外对低聚物的迁移及相关问题进行了大量研究[19-22],但是还未有覆膜铁实罐中低聚物含量检测的相关报道。食品中的低聚物的检测较为复杂,不同的食品基质对低聚物检测的影响未知,因此迫切需要探索一种简单易行的样品前处理方法并确定基质效应的影响,以对覆膜铁实罐中的低聚物进行检测分析。本研究采用UPLC-QTOF-MS技术对国内外市场上的31种覆膜铁罐装食品中的PET及PBT环状低聚物进行检测,并对其建立了样品前处理方法,以便评估目前市面上覆膜铁罐装食品的安全性。
1 材料与方法
1.1 试剂与仪器
试剂:PET环状二聚体标准品、PET环状三聚体标准品、PET环状四聚体标准品、PET环状五聚体标准品,北京汇科同创科学仪器有限公司;PBT环状二聚体标准品、PBT环状三聚体标准品,北京百灵威科技有限公司;乙腈、甲醇,均为质谱纯,上海霍尼韦尔贸易有限公司;六氟异丙醇(色谱纯),上海安谱实验科技股份有限公司;二氯甲烷、正己烷、无水乙醇,均为色谱纯,德国Meck公司;甲酸、甲酸铵,质谱纯,上海霍尼韦尔贸易有限公司;2,2,2-三氟乙醇(色谱纯),西格玛奥德里奇贸易有限公司;无水MgSO4、NaCl,均为色谱纯,中国医药上海化学试剂公司;PSA、Al2O3,均为色谱纯,上海安谱公司。
仪器:Agilent 1290 UPLC-Agilent 6546 UHD QTOF,美国安捷伦仪器公司;KQ-500DE超声波清洗仪,江苏昆山超声波仪器有限公司;TG18K高速离心机,上海舜制仪器制造有限公司;VORTEX05涡旋混匀器,上海达姆实业有限公司;AB204-N分析天平,梅特勒-托利多仪器有限公司;UGC-45C圆形水浴氮吹仪,北京优晟联合科技有限公司;QSE-12D固相萃取仪,上海比朗仪器制造有限公司。
1.2 实验样品
共收集了31种覆膜铁罐装食品,包括水果罐头、肉类罐头、饮料和啤酒4种食品类型。其中水果罐头8种,包括黄桃罐头4种、橘子罐头3种、山楂罐头1种,国内相关生产企业;肉类罐头8种,包括畜禽肉罐头和水产类罐头,国内相关企业;饮料样品共8种,包括国内3种水果汁饮料(桃汁、芒果汁、桔子汁),国内相关生产企业;国外5种水果汁饮料(菠萝汁、苹果汁、百香果汁、猕猴桃汁、椰果汁),国内海关;啤酒7种(其中国内啤酒4种,国内啤酒企业提供的精酿啤酒;国外精酿啤酒3种,日本)。
1.3 标准溶液的制备
分别准确称取各低聚物标准品10 mg至10 mL容量瓶中,用六氟异丙醇(hexafluoroisopropanol,HFIP)溶解并定容至刻度线,得到1 000 mg/L的6种低聚物标准储备液。分别从6种低聚物标准储备液中吸取0.1 mL至10 mL容量瓶中,然后用乙腈定容至刻度线,得到10 mg/L的6种低聚物混合标准中间溶液。
标准储备液配制完成后在20 ℃下储存,最长可以稳定存放4个月。标准工作液配制完成后在4 ℃下储存,每隔2周制备1份新的标准工作溶液。由于低聚物性质不太稳定,标准储备溶液和标准工作溶液均贮存在棕色玻璃瓶中,以防止光诱导降解或异构体转化。
1.4 样品前处理方法
将样品内容物全部均质,然后称取均质样品2.0 g,置于50 mL离心管中,加入适量混合标准溶液。加入8 mL乙腈(肉类罐头加入10 mL乙腈和10 mL正己烷),将混合物涡旋振荡5 min,然后超声处理20 min,后于4 000×g离心10 min,离心结束后,将离心管取出静置10 min,吸取上清液(肉类罐头吸取下层溶液)在常温下氮吹至干,再用1 mL乙腈复溶,然后过PTFE滤膜,使用UPLC-QTOF-MS检测分析。
1.5 仪器条件与参数设置
色谱条件:采用了UPLC系统与四极杆飞行时间(time of flight,TOF)质谱仪耦合。分析柱为ZORBAX RRHD Eclipse Plus C18 2.1 mm×50 mm,1.8 μm,温度控制在40 ℃。流动相(A)为含体积分数0.1%甲酸的水,(B)为含体积分数0.1%甲酸和5 mmol/L甲酸铵的乙腈,流速为300 μL/min,梯度程序设置如下:0 min(20% B)、3 min(50% B)、15 min(100% B)。设置3 min的平衡时间使流动相达到初始条件。进样量设置为5 μL。
质谱条件:质谱选用正电离模式,离子源为带有安捷伦喷射流技术的Jet Stream ESI源。毛细管电压3 500 V,离子源温度325 ℃,鞘气温度350 ℃,流速11 L/min,雾化器压力35 psi,干燥气流速6 L/min,喷嘴电压500 V,分裂压力120 V,锥口压力65 V,Oct 1 RF Vpp为750 V。TOF-MS的采集模式为全扫描MS,在100~1 700 Da的m/z范围内采集数据。
1.6 数据处理
采用Excel 2019处理试验数据,采用Origin 2019进行图表处理与制作。
2 结果与分析
2.1 前处理方法的选择与优化
2.1.1 提取溶剂的优化
本实验分别考察了乙腈、甲醇和二氯甲烷对样品中PET和PBT环状低聚物的提取效果,同类样品平行测定3次,结果如图1所示,使用甲醇和二氯甲烷作为提取溶剂时,6种低聚物的回收率均较低,尤其是PET环状二聚体和PBT环状二聚体的回收率低于80%,当使用乙腈作为提取溶剂时,6种目标物的回收率较好,均在80%~120%,因此,本实验采用乙腈作为PET和PBT环状低聚物的提取溶剂。

图1 乙腈、甲醇和二氯甲烷三种提取溶剂对目标物回收率的影响
Fig.1 Effect of three extraction solvents of acetonitrile, methanol and dichloromethane on the recovery rate of the target product
2.1.2 其他条件的优化
在实验过程中,发现将样品仅仅经过涡旋处理后,并不能达到很好的提取效果,因此尝试了在涡旋步骤后对样品再进行超声处理,结果发现将样品超声处理20 min后可以取得相对更好的提取效果。对于氮吹步骤后所使用的复溶试剂也进行了考察,分别使用了乙腈、甲醇和含体积分数0.1%甲酸铵的乙腈溶液3种试剂进行了实验比较,结果发现当使用乙腈作为复溶试剂时,所得的溶解效果最好,因此本实验选择乙腈作为氮吹处理后的复溶剂。另外,对于肉类食品,由于其内容物基质比较复杂,含有油脂,因此需要选择合适的有机试剂对肉类样品进行脱脂处理,经过实验比对以及对样品和目标物的综合考虑,实验最终决定使用正己烷作为脱脂试剂。
2.2 仪器条件的优化
2.2.1 流动相的选择与优化
将甲醇和乙腈分别作为流动相和有机相,对相应条件下低聚物的色谱行为进行比较,如图2所示。结果发现,当以甲醇作为有机相时,部分目标物的响应值较低(图2-a),而使用乙腈为有机相时,6种目标物的相应值均较好,分离效果也很好(图2-b)。根据文献[23],在流动相中添加甲酸-甲酸铵缓冲溶液可以提高PET及PBT环状低聚物的质谱响应,因此本研究分别考察加入不同浓度甲酸和甲酸铵对目标物峰面积的影响,结果表明,随着甲酸和甲酸铵浓度的增加,PET及PBT环状低聚物的峰面积先是显著增加然后又开始下降,原因可能是随着加入甲酸浓度的增加,流动相的pH值降低,当流动相的pH值过低时,PET及PBT环状低聚物在溶液中倾向于以分子型的状态存在,不利于[M-H]ˉ的形成,因此目标物的峰面积在甲酸浓度过高时表现出下降趋势。另外,PET及PBT环状低聚物的峰面积随着添加甲酸铵浓度的增加表现出先上升后下降的趋势,可能是因为向流动相中加入铵盐可以提供NH4+,这有利于PET及PBT环状低聚物生成[M+NH4]+离子,但是,如果甲酸铵浓度过大时,分子间会产生竞争从而抑制电离,降低目标物的离子化效率。因此,综合考虑,本实验最终选择向流动相中加入体积分数0.10%甲酸和5 mmol/L甲酸铵进行目标物的检测分析。
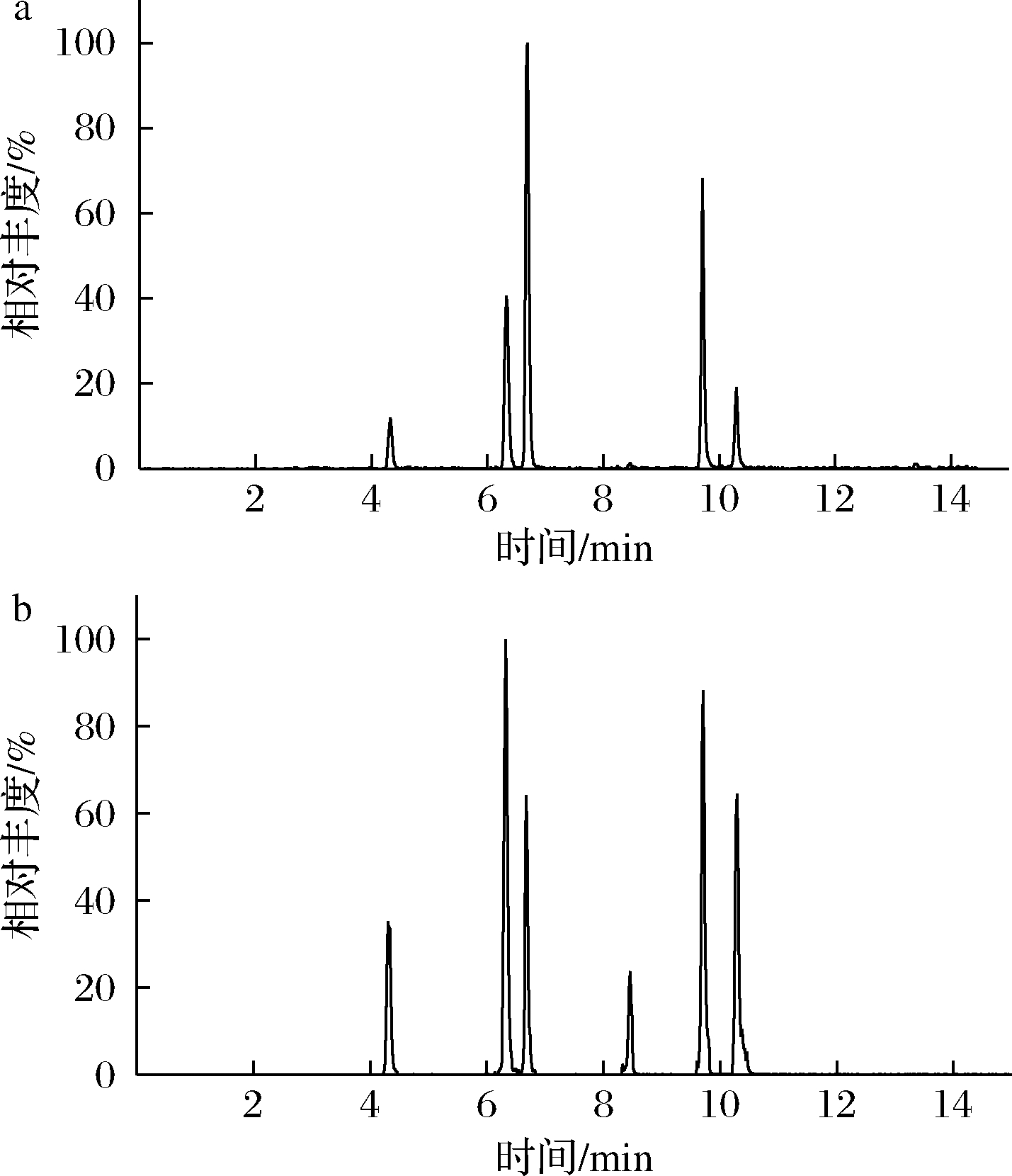
a-水-甲醇;b-水-乙腈
图2 不同流动相对6种PET及PBT环状低聚物分离的影响(TIC谱)
Fig.2 Effect of different flow phases on the separation of 6 kinds of PET and PBT cyclic oligomers
2.2.2 其他色谱条件的优化
由于较高的进样量会显著影响色谱峰的形状,因此将进样量设置为5 μL。实验发现,目标物在有机相达到50%以上时将开始被洗脱,因此,设置有机相在3 min内上升到50%,然后在10 min内,目标物逐步被洗脱,为了能够得到更加稳定的效果,将洗脱时间设置为15 min。并且为了达到样品的高通量检测要求,设置3 min的平衡时间使流动相达到初始条件。
2.3 基质效应
在样品中除被分析物以外的组分称为基质,基质会干扰目标物的分析过程,导致分析结果缺乏准确性,这就称为基质效应。本研究采用标准曲线法来评估基质效应,通过比较标准溶液标准曲线的斜率和样品基质标准曲线的斜率来计算基质效应,计算如公式(1)所示。当-50%<C(%)<50%时,表明该化合物的基质效应不明显,可以忽略;当C(%)<-50%或C(%)>50%时,表明该化合物的基质效应明显,不可被忽略。
C/%=(1-Sm/Ss)×100
(1)
式中:Ss,用有机溶剂配成含有系列浓度目标物的标准曲线的斜率;Sm,用食品样品在提取前加入与Ss相同系列浓度目标物,再经提取步骤后所制得的标准曲线。
从实验结果(图3)可以看出,4种罐装食品中仅肉类罐头中低聚物的基质效应会在50%以上,说明6种环状低聚物在水果罐头、罐装饮料及罐装啤酒中的基质效应可以忽略。而在肉类罐头中,仅PET五聚体的基质效应在50%以下,其余低聚物的基质效应均比较明显,因此,为了得到更为准确的测试结果,本实验统一采用基质加标标准曲线对肉类罐头食品样品进行定量分析。即采用国内同一厂家生产的非覆膜铁包装的、同一批次的同一类型肉类罐头食品作为空白基质制作标准曲线。
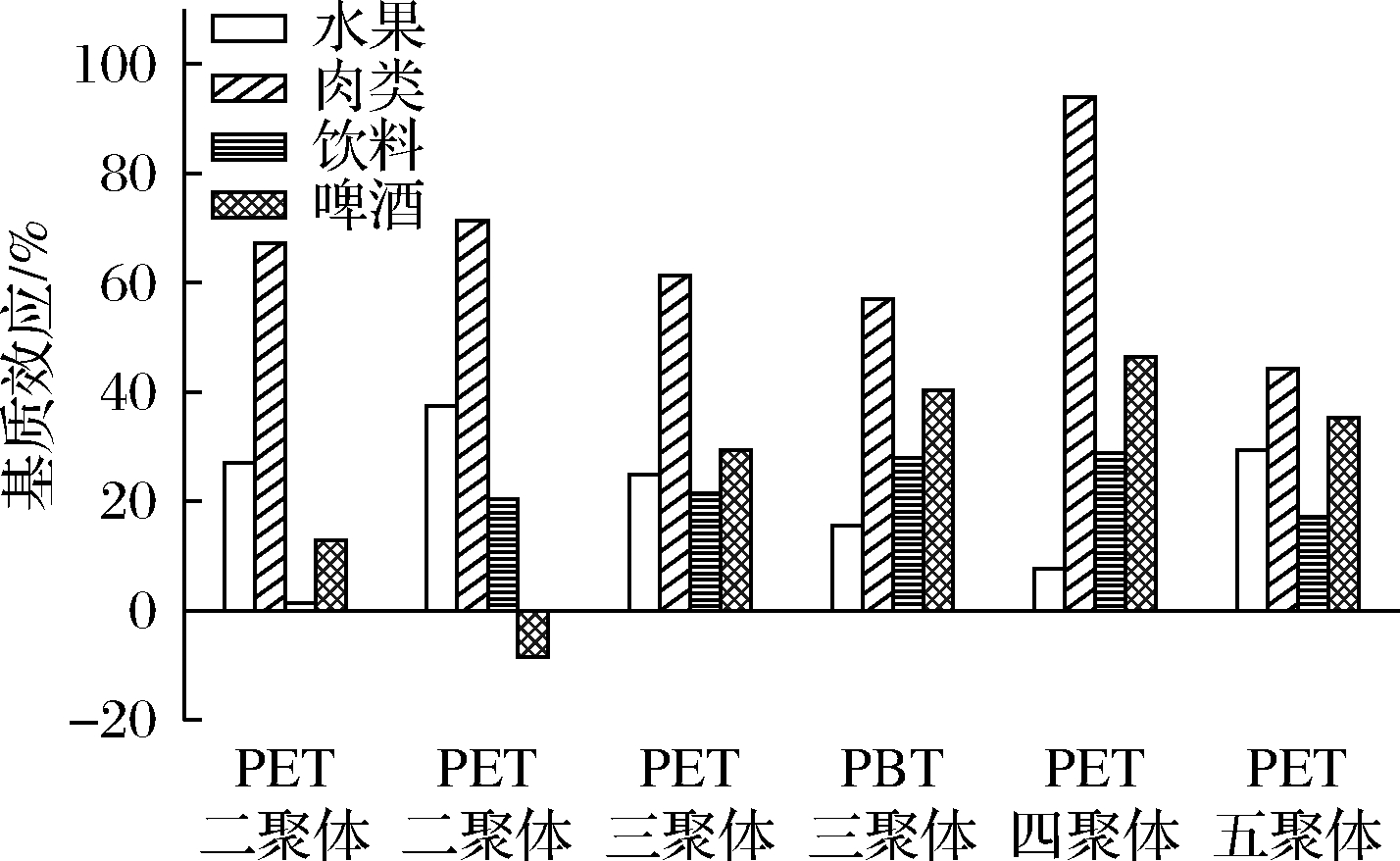
图3 四种食品类型中被测分析物的基质效应
Fig.3 The matrix effect of the tested analytes in the four food types
2.4 线性关系及检出限、定量限
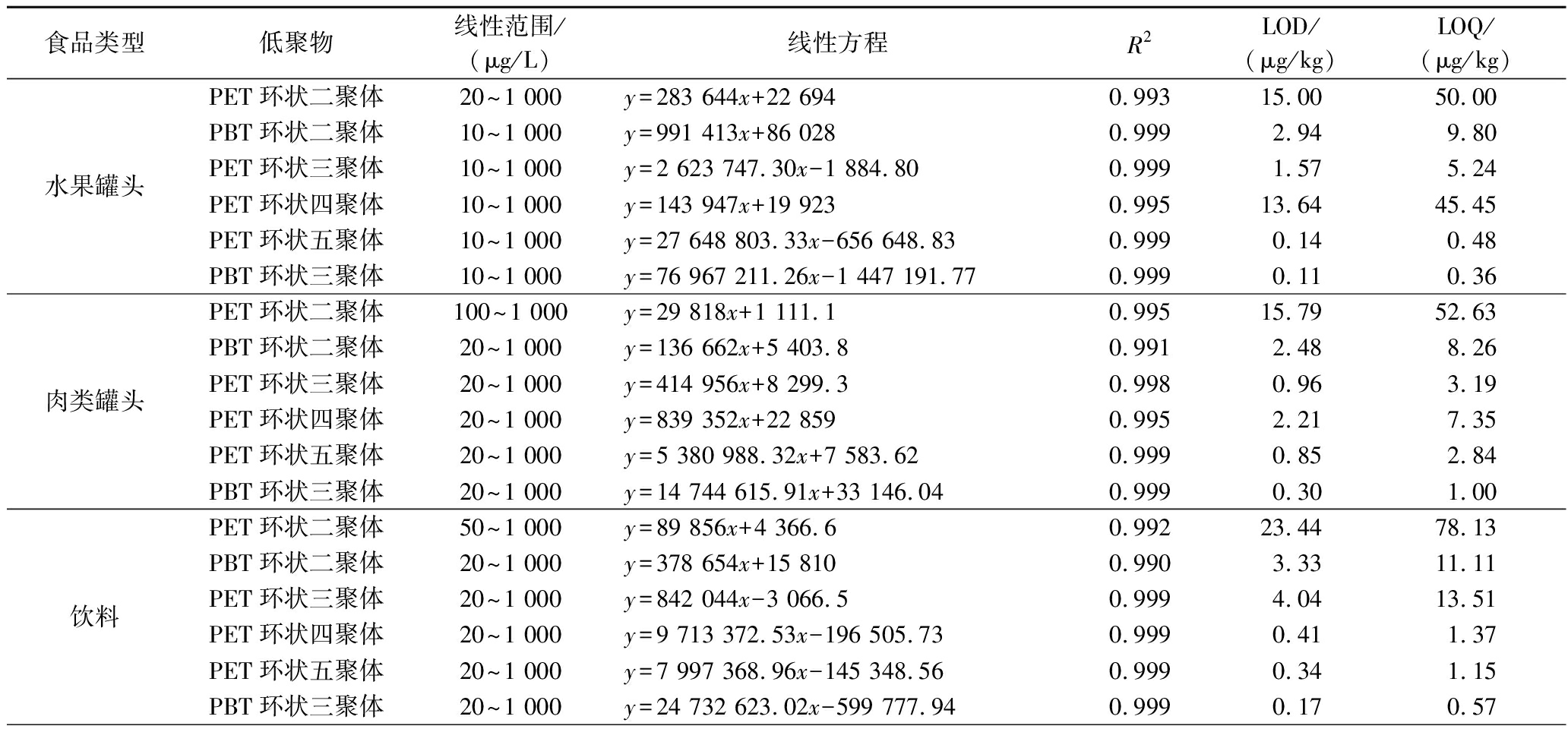
向食品样品基质中分别加入20、50、100、200、500、1 000 μg/L 6种不同质量浓度的低聚物标准工作溶液,按照2.1节的前处理方法进行处理后使用UPLC-QTOF-MS分析,每个浓度平行试验3次。然后以目标物的峰面积(y)为纵坐标,相应的质量浓度(x,μg/L)为横坐标绘制标准曲线。如果样品浓度高出线性范围,则将溶液稀释适当倍数后再进行测定。结果表明,6种低聚物在20~1 000 μg/L线性关系良好,相关系数均大于0.99。检出限(limit of detection,LOD)和定量限(limit of quantitation,LOQ)的估计基于信噪比(signal to noise ratio,SNR),LOD=3×SNR,LOQ=10×SNR,得出目标物检出限为0.11~44.12 μg/L,定量限为0.36~147.06 μg/L,结果详见表1,表明该方法具有较好的灵敏度。
表1 六种PET及PBT低聚物的线性范围、标准曲线、相关系数(R2)、检测限和定量限
Table 1 Linear range, standard curve, correlation coefficient (R2), detection limit and quantification limit of six PET and PBT oligomers
食品类型低聚物线性范围/(μg/L)线性方程R2LOD/(μg/kg)LOQ/(μg/kg)水果罐头PET环状二聚体20~1 000y=283 644x+22 6940.99315.0050.00PBT环状二聚体10~1 000y=991 413x+86 0280.9992.949.80PET环状三聚体10~1 000y=2 623 747.30x-1 884.800.9991.575.24PET环状四聚体10~1 000y=143 947x+19 9230.99513.6445.45PET环状五聚体10~1 000y=27 648 803.33x-656 648.830.9990.140.48PBT环状三聚体10~1 000y=76 967 211.26x-1 447 191.770.9990.110.36肉类罐头PET环状二聚体100~1 000y=29 818x+1 111.10.99515.7952.63PBT环状二聚体20~1 000y=136 662x+5 403.80.9912.488.26PET环状三聚体20~1 000y=414 956x+8 299.30.9980.963.19PET环状四聚体20~1 000y=839 352x+22 8590.9952.217.35PET环状五聚体20~1 000y=5 380 988.32x+7 583.620.9990.852.84PBT环状三聚体20~1 000y=14 744 615.91x+33 146.040.9990.301.00饮料PET环状二聚体50~1 000y=89 856x+4 366.60.99223.4478.13PBT环状二聚体20~1 000y=378 654x+15 8100.9903.3311.11PET环状三聚体20~1 000y=842 044x-3 066.50.9994.0413.51PET环状四聚体20~1 000y=9 713 372.53x-196 505.730.9990.411.37PET环状五聚体20~1 000y=7 997 368.96x-145 348.560.9990.341.15PBT环状三聚体20~1 000y=24 732 623.02x-599 777.940.9990.170.57
续表1

食品类型低聚物线性范围/(μg/L)线性方程R2LOD/(μg/kg)LOQ/(μg/kg)啤酒PET环状二聚体20~1 000y=79 416x+79.0930.99844.12147.06PBT环状二聚体10~1 000y=516 120x+4 420.30.9977.1423.81PET环状三聚体10~1 000y=758 172x-9 830.40.9951.494.95PET环状四聚体10~1 000y=7 312 744x-52 013.890.9990.311.02PET环状五聚体10~1 000y=6 250 663.4x-52 845.40.9990.270.91PBT环状三聚体10~1 000y=20 493 879.66x-319 883.870.9900.130.44
2.5 加标回收率和精密度
采用空白样品加标方法进行加标回收和精密度试验。分别对水果、饮料、啤酒和肉类进行3个水平(50、100、200 μg/L)加标,每个浓度平行测定6次,计算方法平均回收率和相对标准偏差(relative standard deviation,RSD),所得实验结果见表2。从结果可以看出,各类食品中低聚物的加标回收率在80.80%~102.71%,RSD在0.37%~9.26%,表明该实验的回收率和稳定性良好。
表2 水果、肉类、饮料和啤酒四种食品类型中目标物的平均加标回收率和精密度
Table 2 The average recovery rate and precision of target substances in the four food types of fruits, meat, beverages, and beer

食品类型低聚物加标质量浓度(50 μg/L)加标质量浓度(100 μg/L)加标质量浓度(200 μg/L)回收率/%RSD/%回收率/%RSD/%回收率/%RSD/%水果罐头PET环状二聚体90.52±2.667.17±0.5185.64±1.566.40±0.7681.62±1.791.41±0.35PET环状三聚体91.09±2.783.85±0.36100.97±6.782.54±0.3586.40±1.902.61±0.44PET环状四聚体80.66±1.663.87±0.2586.83±1.977.14±0.6692.79±3.015.67±0.76PET环状五聚体81.32±1.711.93±0.3182.72±2.541.48±0.1483.23±2.152.69±0.37PBT环状二聚体97.98±1.901.32±0.1893.97±2.902.13±0.2783.05±1.971.91±0.33PBT环状三聚体92.39±2.183.84±0.29102.71±5.914.57±0.3896.54±4.513.69±0.29肉类罐头PET环状二聚体99.03±2.333.73±0.76117.36±2.043.35±0.71102.81±2.117.47±1.22PET环状三聚体113.75±3.091.23±0.29110.86±3.111.61±0.12111.49±3.072.72±0.47PET环状四聚体92.22±1.255.80±0.59101.96±2.363.89±0.39116.01±2.953.42±0.77PET环状五聚体93.64±3.113.05±0.35100.54±1.941.14±0.0899.83±1.990.68±0.09PBT环状二聚体91.90±1.090.77±0.09119.11±1.204.92±1.01116.93±2.032.79±0.57PBT环状三聚体95.58±4.104.61±0.69101.00±2.431.13±0.2899.92±2.112.03±0.19饮料PET环状二聚体109.79±3.51 2.55±0.47107.38±3.330.50±0.08112.23±2.202.81±0.37PET环状三聚体95.12±2.695.48±0.8996.61±2.100.64±0.1395.04±1.632.26±0.19PET环状四聚体115.17±3.661.81±0.2196.72±3.071.06±0.3685.51±1.090.43±0.05PET环状五聚体115.79±2.972.07±0.4697.54±1.290.81±0.4086.85±1.722.48±0.27PBT环状二聚体108.29±1.712.66±0.19116.83±2.058.58±1.24119.09±0.972.88±0.30PBT环状三聚体80.59±1.090.92±0.2783.57±3.120.66±0.2087.37±3.580.53±0.07啤酒PET环状二聚体119.07±1.11 9.26±0.5593.66±4.558.07±0.39111.96±3.337.84±0.49PET环状三聚体86.42±3.655.47±0.4385.51±2.794.92±0.4185.81±2.902.65±0.33PET环状四聚体86.19±4.112.13±0.3784.35±1.600.93±0.0587.85±1.490.41±0.02PET环状五聚体99.30±2.090.49±0.0791.25±3.010.37±0.0189.54±2.011.41±0.29PBT环状二聚体103.19±4.101.12±0.0284.97±2.945.02±0.93104.90±3.447.38±0.82PBT环状三聚体80.80±1.013.70±0.2981.89±1.051.08±0.3786.29±3.090.72±0.04
2.6 真实样品检测
从国内外市场上共收集了31种覆膜铁罐装食品,包括水果罐头、肉类罐头、饮料和啤酒4种食品类型,其中水果罐头8种、饮料8种、啤酒7种、肉类罐头8种,采用优化后的前处理方法对这31种食品样品分别进行检测,检测结果见表3。在4种食品类型中,PET环状三聚体的含量均是最多的,PET环状三聚体的平均含量从水果罐头中17.14 μg/L到肉类罐头中1 155.22 μg/L,远远高于其他种类的低聚物。
表3 四种食品类型中6种低聚物的含量 单位:μg/L
Table 3 The content of six oligomers in different types of food

低聚物水果肉类饮料啤酒PET二聚体均值ndnd6.58±0.16ndP50ndnd3.12ndP90ndnd24.78nd范围ndndnd~32.09ndPBT二聚体均值2.10±0.19314.91±4.9472.00±1.25ndP501.85249.7766.34ndP907.92597.31150.92nd范围nd~10.88135.26~641.88nd~224.96ndPET三聚体均值17.14±1.121 155.22±12.74151.84±1.3914.46±1.36P5020.57951.27101.7710.99P9085.421 440.79398.2425.61范围nd~113.77402.15~1 826.89nd~439.10nd~30.93PBT三聚体均值nd3.68±0.5024.82±0.660.22±0.02P50nd2.3720.980.31P90nd6.8478.200.85范围ndnd~7.89nd~135.50nd~1.23PET四聚体均值7.63±0.2920.16±0.834.91±0.37ndP5010.5621.333.71ndP9061.2067.9015.67nd范围nd~83.98nd~80.65nd~20.40ndPET五聚体均值4.34±0.2527.36±1.422.42±0.35ndP505.1020.112.96ndP9036.2776.496.30nd均值nd~47.755.61~80.07nd~7.95nd
注:nd为未检出。
本课题组此前已采用不同食品模拟物对覆膜铁空罐中的PET及PBT环状低聚物进行了检测[22],详见表4。采用食品模拟物对覆膜铁空罐进行迁移实验时,PET环状三聚体的迁移量也是最多的,和本文覆膜铁罐装食品中的检测结果一致。
表4 覆膜铁样品中的环状PET和PBT低聚物的定量结果 单位:μg/L
Table 4 Quantitative results of cyclic PET and PBT oligomers in laminated steel samples

低聚物10%乙醇50%乙醇异辛烷PET环状二聚体ndnd 1.22±0.03PET环状三聚体1.87±0.17118.74±8.97866.27±7.21PET环状四聚体nd35.77±2.43171.30±5.47PET环状五聚体0.19±0.011.66±0.072.44±0.13PBT环状二聚体nd5.23±1.212.76±0.30PBT环状三聚体nd2.45±0.782.24±0.19
在实验所测试的4种食品类型中,低聚物的含量大小顺序为:肉类>饮料>水果>啤酒。分析原因可能是肉类罐头在加工过程中,杀菌温度约为121 ℃,温度较高,高温促使聚合物发生降解,从而使得食品中的PET和PBT环状低聚物含量增加。水果罐头和饮料的杀菌温度相对于肉类罐头较低,而啤酒一般为巴氏杀菌,杀菌温度约为65 ℃,因此,啤酒中的低聚物含量最低。另外,啤酒的pH值相较于其他3种食品类型也较高,这使得其对内壁覆膜的腐蚀相对较轻,低聚物的迁出量即随之减少。
3 结论与讨论
本研究通过优化提取溶剂及液相条件,建立了液液萃取-超高效液相色谱-四极杆飞行时间-质谱法对四类覆膜铁罐装食品中6种PET及PBT环状低聚物的测定方法,并对该方法的准确度、精密度及提取效果进行充分验证及评价,又将该方法成功应用于4种覆膜铁罐装食品类型的实际样品测定过程。该方法成本较低、操作简单、加标回收率高、重复性良好,能够为覆膜铁罐装食品中PET及PBT低聚物的检测提供可靠的技术支持。
[1] 宋伟伟, 王洁琼, 柏建国, 等.覆膜铁与涂料铁在金属包装应用中的性能研究[J].中国包装工业, 2015(21):73-75.
SONG W W, WANG J Q, BAI J G, et al.Study on properties of coated iron and coated iron in metal packaging application[J].China Packaging Industry, 2015(21):73-75.
[2] 张清, 郭文渊, 丁树民, 等.我国覆膜铁新材料的研究与应用[J].上海包装, 2017(8):58-61.
ZHANG Q, GUO W Y, DING S M, et al.Research and application of new coated iron materials in China[J].Shanghai Packaging, 2017(8):58-61.
[3] 洪梦寒, 陈晋阳, 顾婕.浅析我国食品包装材料的问题与发展趋势[J].上海包装, 2019(4):22-25.
HONG M H, CHEN J Y, GU J.Analysis on the problems and development trend of food packaging materials in China[J].Shanghai Packaging, 2019(4):22-25.
[4] LIU T, LIU Y H.Research on life cycle assessment of film-laminated steel packaging[J].Baosteel Technical Research, 2020, 14(2):42-48.
[5] 刘志浩, 曾科, 赵宇晖.覆膜铁:金属食品包装的“绿色革命”[J].包装学报, 2012, 4(4):9-15.
LIU Z H, ZENG K, ZHAO Y H.Polymer-coated steel:A green revolution in metal packaging for food and beverage[J].Packaging Journal, 2012, 4(4):9-15.
[6] 高康. 覆膜铁在金属包装上的应用[J].上海包装, 2016(10):59-61.
GAO K.Application of coated iron in metal packaging[J].Shanghai Packaging, 2016(10):59-61.
[7] 夏利勇, 邓潮玉, 齐永杰.覆膜铁技术在我国的发展前景预测[J].中国包装工业, 2013(4):12;14.
XIA L Y, DENG C Y, QI Y J.Prediction of development prospect of coated iron technology in China[J].China Packaging Industry, 2013(4):12;14.
[8] 李乐, 侯存霞, 付亚波, 等.金属包装覆膜技术的研究与应用进展[J].包装工程, 2021, 42(7):99-107.
LI L, HOU C X, FU Y B, et al.Research and application progress of polymer-coated metal packaging[J].Packaging Engineering, 2021, 42(7):99-107.
[9]  WIEK-LUDWICKA K.Polyethylene terephthalate (PET):health aspects and food packaging application[J].Roczniki Państwowego Zakadu Higieny, 2003, 54(2):175-182.
WIEK-LUDWICKA K.Polyethylene terephthalate (PET):health aspects and food packaging application[J].Roczniki Państwowego Zakadu Higieny, 2003, 54(2):175-182.
[10] KAI M, TAYA S, TOMARU H.Influence of film adhesion on PET-hair of laminated steel in the forming process of DI can[J].Tetsu-to-Hagane, 2013, 99(8):503-508.
[11] YAMANAKA Y, JUNICHI K, NAKAMARU H.Surface properties of PET film laminated steel sheets coated with polyester resin containing fatty acid amides[J].Journal of the Surface Finishing Society of Japan, 2014, 65(11):531-538.
[12] YAMANAKA Y, KITAGAWA J, KOJIMA K, et al.Effect of crystal structural changes of PET in can-making process on properties of film laminated steel for containers[J].ISIJ International, 2018, 58(12):2330-2337.
[13] YAMANAKA Y, KITAGAWA J, NAKAMARU H.Effect of surface free energy of film laminated steel sheets on content release properties[J].Packaging Technology and Science, 2015, 28(9):811-821.
[14] YAMANAKA Y, KITAGAWA J, KOJIMA K, et al.Precipitation phenomenon of cyclic oligomers on the surface of PET film laminated steel sheets during wet-heat treatment[J].Journal of the Surface Finishing Society of Japan, 2018, 69(7):302-307.
[15] 赵梦肖. PET环状低聚物的制备及高黏体系下开环聚合的研究[D].杭州:浙江理工大学, 2021.
ZHAO M X.Study on preparation of cyclic oligomer of PET and ring-opening polymerization in high viscosity system[D].Hangzhou:Zhejiang Sci-Tech University, 2021.
[16] GELBKE H P, BANTON M, BLOCK C, et al.Risk assessment for migration of styrene oligomers into food from polystyrene food containers[J].Food and Chemical Toxicology, 2019, 124:151-167.
[17] SCHAEFER A, OHM V A, SIMAT T J.Migration from can coatings:Part 2.identification and quantification of migrating cyclic oligoesters below 1000 Da[J].Food Additives &Contaminants, 2004, 21(4):377-389.
[18] 李倩云, 吴刚, 王亚, 等.覆膜金属罐中PBT/PET环状低聚物在食品中的迁移测试及基于膳食暴露量的风险评估[J].分析测试学报, 2022, 41(10):1494-1500.
LI Q Y, WU G, WANG Y, et al.Migration test of PBT/PET cyclic oligomer in coated metal cans in food and risk assessment based on dietary exposure[J].Journal of Instrumental Analysis, 2022, 41(10):1494-1500.
[19] NASSER A L M, LOPES L M X, EBERLIN M N, et al.Identification of oligomers in polyethyleneterephthalate bottles for mineral water and fruit juice[J].Journal of Chromatography A, 2005, 1097(1-2):130-137.
[20] KHANEGHAH A M, LIMBO S, SHOEIBI S, et al.HPLC study of migration of terephthalic acid and isophthalic acid from PET bottles into edible oils[J].Journal of the Science of Food and Agriculture, 2014, 94(11):2205-2209.
[21] GENUALDI S, NYMAN P, BEGLEY T.Updated evaluation of the migration of styrene monomer and oligomers from polystyrene food contact materials to foods and food simulants[J].Food Additives &Contaminants:Part A, 2014, 31(4):723-733.
[22] XU T T, QIU K, GAO H B, et al.Simultaneous determination of cyclic PET and PBT oligomers migrated from laminated steel cans for food[J].Food Control, 2021, 130:108396.
[23] TSOCHATZIS E D, ALBERTO LOPES J, KAPPENSTEIN O, et al.Quantification of PET cyclic and linear oligomers in teabags by a validated LC-MS method—In silico toxicity assessment and consumer’s exposure[J].Food Chemistry, 2020, 317:126427.