单核细胞增生李斯特氏菌(Listeria monocytogenes,LM),简称单增李斯特菌,是一种兼性厌氧的革兰氏阳性杆菌,摄入被单增李斯特菌污染的食物可引起李斯特菌病,致死率高达20%~30%[1]。全球化食品生产的改变和消费者习惯的变化,倾向于最低限度加工、即食、冷藏或冷冻食品,增加了李斯特菌病的发病率[2]。在2018—2021年间,我国北京丰台区确诊了多例单增李斯特菌病患者,但食品和环境溯源调查成功率较低[3]。2018年,欧洲报道了2 549例侵袭性李斯特菌病确诊病例,其中死亡病例229例[4]。对李斯特菌病暴发的流行病调查显示,大多数病例的暴发可归因于食品,且与食品加工环境(如食品接触面、包装线)的持续污染有关[5]。
单增李斯特菌能在环境中长期存在的能力与其生物被膜形成能力、消毒剂耐受性等多种抗逆表型相关[6]。单增李斯特菌可在不锈钢等食品接触表面形成坚固的生物被膜,增强其对理化因子、杀菌剂、抗生素等的抗性,从而使常规的清洗杀菌措施无法完全清除细菌[6-7]。其次,在消毒剂、高温、低pH等环境的选择压力下,微生物可通过遗传调节或者生理适应性进化成耐受菌株,在环境中长期存活,最终发展成为持久性菌株[8]。目前,从食品加工环境中分离出的持久性单增李斯特菌的数量逐年增加,虽已有部分研究者围绕其表型特征进行了一些探索,但都不够全面,单增李斯特菌在食品加工环境中持久存在的原因仍不明晰,由其污染导致的李斯特菌病暴发事件不断发生,因此非常有必要结合现有的研究结论,对促进其持久性的相关表型和相关功能基因进行系统的总结。
综上所述,本文对持久性的概念和由单增李斯特菌污染引发的暴发事件进行整理介绍,重点分析单增李斯特菌持久性与生物被膜形成能力、消毒剂耐受性、耐热性和耐酸性等表型的联系,并对相关的功能基因进行总结,为单增李斯特菌持久性菌株的预防和控制提供理论参考。
1 持久性菌株及相关安全事件
1.1 持久性和持久性菌株的定义及判定
“持久性(persistence)”一词可以具有多种含义,可以描述病原体在人类宿主中的长期存活;也用于描述病原体在肉制品、奶酪、水产品和蔬菜等食品中的长期存活;同样可用于描述病原体在土壤、不锈钢表面或复杂的加工厂环境中的长期存活[9]。
目前对于“单增李斯特菌持久性菌株”的定义还没有一个完全统一的标准,不同研究中对持久性菌株分离时间、分离环境以及亚型的确定方法等细节上存在些许差异,如表1所示。总的来说,持久性菌株可被定义为从同一环境不同日期重复分离出的具有相同亚型的菌株[10],而不满足这一定义的其他菌株则被称为散发性菌株(sporadic strains)[11]或者非持久性菌株(nonpersistent strains)[12]。
表1 有关单增李斯特菌持久性菌株的判定方法及内容
Table 1 Determination method and content of persistent L.monocytogenes strains

分型方法分离时间分离来源持久性判定参考文献PFGE每月采样,为期27个月猪肉加工厂及产品相同亚型在环境中反复发现3次或更多[13]PFGE不定期采样,为期2年肉类加工厂菌株在6个月或更长时间重复分离,并属于相同亚型[14]MVLST不定时采样,为期6个月零售鸡肉菌株在6个月内从零售鸡中反复分离,并由MVLST确定为相同基因型[15]PFGE、MLST和cgMLST不定时采样,为期2年食品工厂环境及各个环节的产品相同亚型在2年内重复分离[16]Ribotyping不定时采样,为期1年鸡肉加工厂环境菌株被分离2次,间隔至少6个月,核糖分型无法区分[11]WGS每月取样,为期14个月熟食零售肉类通过单核苷酸多态性(SNP)差异度量[17]
注:脉冲场凝胶电泳(pulsed-field gel electrophoresis,PFGE), 多毒力位点序列分型(multi-virulence-locus sequence typing,MVLST),多位点序列分型(multi-locus sequence typing,MLST),核心基因组多位点序列分型(core genome multilocus sequence typing,cgMLST),核糖分型(ribotyping),全基因组测序(whole genome sequencing,WGS)。
1.2 李斯特菌病暴发事件及其溯源技术
单增李斯特菌持久性菌株已被确定为食品加工后的主要污染物,对公共健康和经济造成了极大影响[11]。目前,PFGE、MLST和cgMLST等分型技术已被用作分子流行病学调查和溯源分析中的常规工具[18]。这些分型方法的发展,很大程度上为识别和控制持久性菌株提供了技术支持。
近年来,由单增李斯特菌持久性菌株引起人类李斯特病的暴发或散发事件频频发生,如表2所示。其中,多个国家的李斯特菌病暴发事件与ST5型菌株污染食品环境有关,分子流行病学研究显示其临床分离亚型与工厂中存在的持久性亚型同属于一个克隆。该亚型的菌株在奶制品[19-20]、水果以及蔬菜类[21-23]等不同的即食加工环境都能持续存在,这显示了ST5菌株在各个环境中的污染致病能力,需要我们进一步加强关注。另外,南非香肠[24]和德国血肠[25]污染导致了多人死亡,这两起暴发事件是都由ST6型克隆菌株引发的,据调查显示,该亚型菌株在不同大陆的食品生产设施中实现了交叉污染,且持续传播的时间长达3年。此外,还有一些ST型(例如ST1、ST382、ST4等)也形成了“环境—食品—临床”的传播链[19, 23, 26],对人类健康安全和社会经济都造成一定的影响。由此可见,单增李斯特菌持续存在于食品加工环境是食品安全和人类健康面临的一大挑战,探究其在食品加工环境长期存在的原因对于如何预防和控制致病菌将具有重要意义。
表2 近年来由单增李斯特菌持久性菌株引发的部分暴发性事件
Table 2 Selected outbreaks caused by persistent L.monocytogenes in recent years

年份国家工厂类型分离物来源ST型参考文献2019—2020中国即食肉加工场所、中间产品、上市产品5、121[16]2018—2019德国肉肠设备、血肠、临床6[25]2017—2018南非即食肉生产设施环境、香肠产品、临床6[24]2015—2018瑞士肉食加工生产环境、产品9、204、121[27]2015—2016美国绿叶沙拉沙拉产品382[22]2014—2015美国水果农场焦糖苹果种植产地、包装线和环境分离物、上市产品、临床1、382[28]2014美国核果工厂加工环境、产品、临床5、382[23]2013—2014瑞士肉食加工沙拉原料,成品,临床4[26]2011美国水果工厂加工环境、哈密瓜、临床5、7、561[21]
注:在表格中,序列型(sequence type, ST)。
2 单增李斯特菌持久性菌株的表型特征研究
随着单增李斯特菌在环境中不断被检出,与单增李斯特菌持久性相关的表型的研究逐步开展,通常认为持久性菌株具有某些特定的表型特征,例如:菌株的生物被膜形成能力、对消毒剂的耐受性以及对酸、热、渗透压或干燥等不同环境下的抗逆性,以下分述之。
2.1 生物被膜形成能力
生物被膜是由细菌和自身分泌的胞外聚合物质(extracellular polymeric substances,EPS)组成,可黏附在生物及非生物表面具有三维立体空间结构的细胞群体[29]。已有研究表明,单增李斯特菌可在常见的不锈钢、聚苯乙烯等食物接触表面上形成生物被膜[1,30]。生物被膜有助于微生物在不利环境中的持久性,因为它们提供了表型的多样性和生态优势。例如,生物被膜的胞外基质可充当物理屏障,并提供保护性生态位,以阻碍抗菌剂渗透到深层生物被膜中[31]。另外,生物被膜内养分转移或代谢通量的随机变化,使得生物被膜内细胞显示出的生理状态有利于细胞的持久存活[32]。而由水平基因转移引起的整个种群在压力条件下的适应性则是持久性形成的另一原因[33]。微生物在环境中形成难以清除的生物被膜给食品工业带来了严重危害,因为它们构成了致病微生物和腐败微生物的储存库,增加了加工厂中食品污染的风险。
生物被膜的形成会提高菌株在不利环境中的存活率,不少研究者对持久性菌株和散发性菌株的生物被膜形成能力进行了比较分析,如表3所示。结晶紫染色和活细胞计数通常被用来测量生物被膜的形成量,也有少数研究采用了荧光显微镜和扫描电子显微镜从微观角度对生物被膜的结构进行观察。另外,研究选择聚苯乙烯或不锈钢片作为生物被膜的接触介质,这在很大程度上是对工厂常见生产设备表面的模拟,提高了研究结果的实际参考价值。从表3中的结果可知,所有的单增李斯特菌菌株都具有生物被膜的形成能力,一些研究者的实验结果支持持久性菌株具备更强的生物膜形成能力这一猜想[11,34-37]。然而,另一些研究小组发现,持久性菌株和散发菌株的生物膜形成能力没有显著差异[38-39]。这些结果的差异可能与实验样本量的选择及生物被膜的培养时间等实验条件的不同有关。总体而言,单增李斯特菌形成生物被膜的能力与食品加工厂环境中分离的菌株的持久性之间的相关性仍不明晰,还需要更多的研究加以说明。
表3 单增李斯特菌持久性和散发性菌株:生物被膜形成能力的比较研究
Table 3 Persistent and sporadic L.monocytogenes:A comparative study of biofilm formation capacity

PS/株SS/株接触面测量方法结果参考文献3524不锈钢片25 ℃,24 h,黏附细胞计数PS>SS[34]314不锈钢片25 ℃,1,2,72 h,吖啶橙染色黏附细胞并用荧光显微镜计数1 h和2 h,PS>SS;72 h,PS与SS无显著差异[35]1115聚苯乙烯30 ℃,40 h,结晶紫染色,扫描电镜观测结构PS>SS[36]55聚苯乙烯37 ℃,24 h,结晶紫染色PS>SS[11]88聚苯乙烯30 ℃,48 h,结晶紫染色,活细胞计数PS>SS[37]7625聚苯乙烯30 ℃,48 h,结晶紫染色PS与SS无显著差异[38]108聚苯乙烯37 ℃,48 h,结晶紫染色PS与SS无显著差异[39]
注:PS,持久性菌株(persistent strains);SS,散发性菌株(sporadic strains)。
2.2 消毒剂耐受性
消毒剂针对细菌细胞的不同部位具有不同的作用机制,包括细胞成分(如核酸、蛋白质或酶)、细胞膜(蛋白质和转运泵)或巯基(酶和辅酶)[40]。长时间进行高浓度的消毒操作使得消毒剂残留于环境中,细菌反复暴露于亚致死浓度下,并且在这种选择性压力下进化出对消毒剂的耐受性[41],这可能有助于细菌在环境中持久存活。CASEY等[42]则发现许多生物过程,如肽聚糖生物合成、细菌趋化性和运动性以及碳水化合物摄取,都参与了持久性单增李斯特菌对消毒剂的耐受反应。表4将部分针对持久性菌株和散发性菌株对消毒剂耐受能力的研究进行了整理,以了解单增李斯特菌持久性菌株与消毒剂耐受性的潜在关系。
表4 单增李斯特菌持久性和散发性菌株:消毒剂耐受性的比较研究
Table 4 Persistent and sporadic L.monocytogenes:A comparative study of disinfectant tolerance

PS/株SS/株菌株状态处理条件结果参考文献55生物被膜10%SHY、BAC下处理5 minBAC下,PS
注:BAC,苯扎氯氨(benzalkonium chloride);SHY,次氯酸钠(sodium hypochlorite)。
如表4所示,大多数研究选用了工厂中最常见的消毒剂(季铵盐类消毒剂和含氯类消毒剂)对菌株的耐受能力进行评估比较,部分研究还对不同状态下的菌株(浮游态、生物被膜)进行了消毒剂耐受能力测试。虽然之前有研究者提出消毒剂耐受性作为一种重要的环境适应能力,有助于单增李斯特菌在食品加工环境中长时间存活[43-44],但仅有部分研究证明了对消毒剂的抗性与病原体在不同食品加工环境中的持久性之间存在关联[13,43-45],在其他一些研究中没有记录到持久性和增加的消毒剂耐性之间的明确联系[12,46-48]。另外,大多数对消毒剂耐受性的研究仅简单比较了消毒剂处理后,微生物的失活数量,却忽略了微生物对消毒剂的适应及生长恢复能力。
ORGAZ等[49]对食品加工厂分离出来的6株持久性菌株和6株非持久性菌株进行壳聚糖或过氧乙酸消毒处理,并在24 h内比较了它们的活细胞数的恢复情况,结果表明持久性菌株在壳聚糖处理后显示出更好的恢复能力。因此,未来对持久性菌株与散发菌株对消毒剂耐受性的比较研究,不仅要考虑微生物的失活水平,也要关注微生物接触抗菌化合物后的亚致死细胞的恢复能力。
2.3 耐酸性、耐热性及其他抗逆表型研究
研究表明,细菌在酸、热、渗透压或干燥等其他环境的抗逆性也与菌株的持久性有关。单增李斯特菌在这些不利的环境条件下可直接或间接诱发突变,进一步分化成具有独特遗传特征的菌株集群[50]。基于不同应激反应系统对生存的可能重要性,研究人员评估了持久性和非持久性菌株对各种应激的耐受性。LUNDEN等[51]发现从肉类加工厂分离得到持久性菌株对酸性条件的耐受性显著高于散发性菌株,这表明耐酸性可能帮助这些菌株在卫生程序中存活,从而促成单增李斯特菌在环境中的持久性。NOWAK等[37]对8株单增李斯特菌持久性菌株和8株散发性菌株的耐热性、运动性和在干燥表面的存活能力进行了比较,结果发现持久性与运动性无关,而耐热性可能有助于持久性,并且在干燥条件下,持久性菌株往往比散发菌株存活得更好。VOGEL等[52]的研究也表明,单增李斯特菌在干燥条件下存活数月的能力与其持久性的形成有关。鉴于每个细胞的生理异质性和复杂性,持久性细菌的出现是不同的耐受性相关机制的结果。最近对细菌持久性机制的研究发现,细菌SOS反应的激活,一种上调DNA修复功能的信号通路,可能与细菌持久性有关[53]。
值得注意的是,以上大多数研究仅将持久性分别与某一具体表型特性联系起来讨论,而忽略了整体环境的复杂性。例如,生物被膜的形成会增强单增李斯特菌对消毒剂的耐受性[6],而菌株对盐、消毒剂等环境因子的适应也能反向影响生物被膜的形成[54-55],这些特性共同作用促进了菌株在环境中的持久性。所以对持久性菌株的研究,不因局限于某一因素,还应结合实际环境情况。
3 单增李斯特菌持久性菌株的抗逆基因研究
表型差异不是由单一突变、前噬菌体或其他遗传差异引起的,而可能是不同的单增李斯特菌谱系所独有的,或者是环境刺激和遗传背景的多因素组合。因此,深入了解与单增李斯特菌持久性相关的基因或遗传特征,对于如何更好地识别、预防和控制工厂生态位中的单增李斯特菌持久性菌株,避免食品安全事件的发生具有重要意义。
3.1 与生物被膜形成相关的基因
研究发现,单增李斯特菌生物被膜的形成与鞭毛、群体感应、EPS、毒力等各种功能基因调控有关,如表5所示。
表5 单增李斯特菌生物被膜相关的基因表达研究
Table 5 Gene expression studies related to biofilm of
L.monocytogenes

功能类型基因/蛋白作用参考文献鞭毛基因flaA、motB、FlhB、FliM、FliY促进鞭毛合成,从而促进生物被膜的形成[56-57]群体感应agr、luxS群体感应系统可以直接正调控生物被膜的形成[58]EPSDegU、BapL在最初聚集到介质表面的过程起重要作用,直接影响生物被膜的形成[60, 11]毒力基因actA、prfA、inlL在生物被膜中表达增加,对生物被膜形成能力具有积极影响[62]
单增李斯特菌鞭毛的合成受flaA、motB、FlhB、FliM、FliY等基因/蛋白的调控。其中,flaA 基因编码鞭毛蛋白作为鞭毛的结构亚基,motB基因可调控鞭毛的运动能力,FlhB、FliM和FliY等蛋白不仅介导单增李斯特菌的运动,还参与调节鞭毛的合成[56]。cheA/Y是一种双组分趋化系统,细菌通过CheA蛋白感知外部信号,并通过趋化蛋白CheY调节鞭毛转子参与细菌运动,促进生物被膜的形成[57]。细菌群体感应(quorum sensing,QS)在食物腐败、生物被膜形成和与食物相关的发病机制中起着重要作用。在单增李斯特菌中有2个群体感应体系,即寡肽介导的Agr群体感应系统和自诱导2(AI-2)LuxS群体感应系统[58]。其中Agr群体感应系统可以直接正调控生物被膜的形成,也可以调控毒力因子、耐药因子并间接调控生物被膜的形成,是一种整体水平的调控网络体系[59]。表面黏附蛋白BapL在单增李斯特菌聚集到介质表面的过程也起重要作用[60]。由基因lmo2515编码的DegU是鞭毛蛋白基因flaA的转录激活剂,与鞭毛糖蛋白的形成密切相关,直接影响生物被膜的形成[61]。此外,由prfA编码的 PrfA蛋白是一种关键的转录激活剂,调节大多数单增李斯特菌毒力基因的表达,也被证明能促进单增李斯特菌生物被膜的形成[59]。其中,单增李斯特菌主要的毒力决定因子actA,作为一种PrfA调节的基因产物,能够使肌动蛋白聚合,从而促进其细胞内运动和细胞间扩散,对细菌聚集和生物被膜形成至关重要[52]。
3.2 与消毒剂耐受性相关的基因
目前在单增李斯特菌中发现的与消毒剂耐受性相关的基因包括但不仅限于lde、mdrL、bcrABC、qacH和ermC等。其中,编码外排泵转运蛋白的lde、mdrL基因多次在单增李斯特菌中被检出,对苯扎氯铵的耐受性起重要作用[63]。bcrABC在1998—1999年美国李斯特菌病爆发涉及的H7550菌株的质粒(pLM80)上被首次发现[64],能介导高水平的苯扎氯铵耐受率。qacH被指出与食品加工环境中持续存在的单增李斯特菌紧密相关。MØRETRØ等[44]在来自9家挪威肉类和鲑鱼加工厂的101个分离菌株中发现了qacH和bcrABC的存在,并通过实验确定了携带qacH和bcrABC抗性基因的单增李斯特菌在亚致死浓度的季铵盐类消毒剂下更具有生长优势。KROPAC等[65]发现,多药外排泵蛋白EmrC与单增李斯特菌ST6菌株引起的苯扎氯铵耐受性增强有关,在苯扎氯铵的作用下,与EmrC和TetR转录调控因子基因相关的mRNAs表达增加。HURLEY等[66]对从食品加工环境中分离的单增李斯特菌持久性菌株进行全基因组测序,发现72%的菌株中存在苯扎氯铵耐受性编码基因,其中最相关的基因是emrC,其次是bcrABC、qacH-Tn6188和qacC。
3.3 与耐酸性、耐热性及其他表型相关的基因
单增李斯特菌与耐酸性、耐热性等其他表型相关的基因有argR、arcA、sigB、clpL、clpB,以及应激生存岛1(stress survival islet 1,SSI-1)和应激生存岛2(stress survival islet 2,SSI-2)等。
许多研究发现sigB的表达是单增李斯特菌在酸性胁迫下存活的关键[67]。argR基因可编码一种功能性ArgR,属于ArgR/AhrC精氨酸抑制家族的转录调控因子,arcA和sigB的转录和表达受到ArgR的显著抑制。CHENG等[68]证明了argR的缺失导致arcA和sigB的表达激活,提高了单增李斯特菌在pH 3.5的BHI培养基中的存活率。PÖNTINEN等[69]将clpL基因导入1株天然的热敏单增李斯特菌,显著提高了受体菌株在55 ℃时的耐热性,说明ClpL可以作为耐热性升高的潜在预测因子。CHENG等[70]发现DegU可自动调节并上调hrcA-grpE-dnaK-dnaJ操纵子,导致热休克蛋白的产生增加,从而增强单增李斯特菌的耐热性。RINGUS等[71]通过定量逆转录聚合酶链反应发现SigB调节基因inlA和gadD3以及CtsR调节基因lmo1138和clpB在盐胁迫条件下,转录水平显著增强,这说明这4个基因与菌株耐高渗能力有一定关系。
据报道,从食品加工场所分离的单增李斯特菌的毒力和持久性特征与SSI-1和SSI-2的存在有关[8]。SSI-1包含lmo0444、lmo0445、lmo0446 (pva)、lmo0447 (gadD1) 和 lmo0448 (gadT1)5个基因,在不同的李斯特氏菌中高度保守,其缺失突变体在低pH值和高盐浓度下显示出生长受损[72]。另外,PIERCEY等[73]发现表现出脱水抗性的菌株也含有SSI-1,这说明SSI-1与菌株的抗干燥性也有一定联系。SSI-2由lin0464和lin0465基因构成,目前仅存在于单增李斯特菌CC121相关菌株分离物中[74]。HARTER等[75]发现在氧化应激条件下,lin0464和lin0465两个基因的表达显著增加,且不受SigB的影响。另外,该研究构建了Δlin0464缺失突变体,发现lin0464的缺失降低了菌株在碱性和氧化应激下的存活率,这表明SSI-2的存在有利于菌株在碱性和氧化应激下存活。
随着相关基因研究的深入,现已有一些研究者通过药物干扰群体感应途径、破坏细胞外DNA、蛋白质、胞外多糖和参与各种信号通路的次级信使来抑制或降低生物被膜的形成。SHUKLA等[76]通过鉴定Bap的功能和保守区域,靶向开发了抗生物被膜策略(一种合成肽,STVTVTF)干扰Bap介导的生物被膜积累,成功抑制并分散了细菌生物被膜,预防了单增李斯特菌在环境中进一步的传播。此外,孙奇凡[77]利用比较基因组学挖掘出了一些持久性菌株的特异性分子检测靶标,并建立了基于特异性分子检测靶标的单增李斯特持留型CC87和CC88菌株的多重PCR检测体系。因此,未来还应继续探索更多的功能基因,并借助基因层面的研究来更好地识别监测和防控单增李斯特菌持久性菌株。
4 结语与展望
食品加工环境中持续存在的单增李斯特菌大大增加了食品(再)污染的风险,对食品安全和人类健康构成了巨大挑战。尽管我们对持久性菌株已经有了初步的了解,但还有很多问题没有解决,如文中所述,当前对于定义持久性菌株的分型方法和重复分离次数等的界定比较宽泛,一定程度上造成了信息无法及时有效地整合;其次,大多数关于单增李斯特菌持久性菌株的研究都只围绕一个或两个表型,如生物被膜的形成或对消毒剂的耐受性,且这些表型与食品加工厂环境中分离的菌株的持久性之间的相关性仍不明晰,还需要更多的研究加以说明。另外,单增李斯特菌对于其他工厂环境因素(如温度、渗透压、pH值和干燥条件等)的表型反应的数据较少,缺乏对其表型特征的系统研究;最后,现有的关于持久性菌株的研究主要集中在表型,只有相对较少的研究关注了持久性相关的基因和遗传特征,目前对于相关功能基因的探索还相对有限,持久性现象背后的分子机制还有待探索。因此未来的工作可从以下3方面开展:
其一,目前确定持久性菌株采用的分型方法较多,导致许多研究结论无法统一。未来可以将单增李斯特菌持久性菌株按不同的亚型进行分类整理,总结不同单增李斯特菌亚型的流行规律;其二,未来研究应充分考虑食品工厂环境的复杂性,在多种环境因素下对持久性菌株的表型进行全面的探索,并且在这些实验中,研究者需尽可能保持实验样本量及相关实验条件的一致,这有助于揭示各表型与持久性的关系;其三,持久性的形成可受到多种遗传机制的调控,未来可利用基因组学、转录组学等多种技术,从分子水平继续探究持久性菌株的功能基因和遗传学特征,并借助基因层面的研究来更好地识别监测和防控单增李斯特菌持久性菌株,进一步为未来开发靶向治疗方案提供基础研究数据。
[1] WANG Y, SUN L J, HU L L, et al.Adhesion and kinetics of biofilm formation and related gene expression of Listeria monocytogenes in response to nutritional stress[J].Food Research International, 2022, 156:111143.
[2] CAROLINA I,VIRGINIA G M,LENZ ROMINA M, et al.Response of sensitive and resistant Listeria monocytogenes strains against bacteriocins produced by different Enterococcus spp.strains[J].International Journal of Food Microbiology, 2022, 382:109928.
[3] 肖贵勇, 马晓曼, 王佳佳, 等.一例孕产妇单核细胞增生李斯特菌感染的溯源调查及发病机制探讨[J].中国食品卫生杂志, 2022, 34(2):287-291.
XIAO G Y, MA X M, WANG J J, et al.Tracing investigation and pathogenesis of a maternal Listeria monocytogenes infection[J].Chinese Journal of Food Hygiene, 2022, 34(2):287-291.
[4] The European Union One Health 2018 Zoonoses Report[J].EFSA Journal, 2019, 17(12):e05926.
[5] KURPAS M, OSEK J, MOURA A, et al.Genomic characterization of Listeria monocytogenes isolated from ready-to-eat meat and meat processing environments in Poland[J].Frontiers in Microbiology, 2020, 11:1412.
[6] CIOFU O, MOSER C, JENSEN P Ø, et al.Tolerance and resistance of microbial biofilms[J].Nature Reviews Microbiology, 2022, 20(10):621-635.
[7] SKOWRON K, WA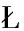 ECKA-ZACHARSKA E, GRUDLEWSKA K, et al.Disinfectant susceptibility of biofilm formed by Listeria monocytogenes under selected environmental conditions[J].Microorganisms, 2019, 7(9):280.
ECKA-ZACHARSKA E, GRUDLEWSKA K, et al.Disinfectant susceptibility of biofilm formed by Listeria monocytogenes under selected environmental conditions[J].Microorganisms, 2019, 7(9):280.
[8] BFATRIZ M,BEATRIZ M,BEATRI X S,et al.Characterization of virulence and persistence abilities of Listeria monocytogenes strains isolated from food processing premises[J].Journal of Food Protection, 2019, 82(11):1922-1930.
[9] FERREIRA V, WIEDMANN M, TEIXEIRA P, et al.Listeria monocytogenes persistence in food-associated environments:Epidemiology, strain characteristics, and implications for public health[J].Journal of Food Protection, 2014, 77(1):150-170.
[10] FAGERLUND A, LANGSRUD S, SCHIRMER B C T, et al.Genome analysis of Listeria monocytogenes sequence type 8 strains persisting in salmon and poultry processing environments and comparison with related strains[J].PLoS One, 2016, 11(3):e0151117.
[11] RODR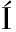 GUEZ-CAMPOS D, RODR
GUEZ-CAMPOS D, RODR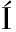 GUEZ-MELC
GUEZ-MELC N C, ALONSO-CALLEJA C, et al.Persistent Listeria monocytogenes isolates from a poultry-processing facility form more biofilm but do not have a greater resistance to disinfectants than sporadic strains[J].Pathogens, 2019, 8(4):250.
N C, ALONSO-CALLEJA C, et al.Persistent Listeria monocytogenes isolates from a poultry-processing facility form more biofilm but do not have a greater resistance to disinfectants than sporadic strains[J].Pathogens, 2019, 8(4):250.
[12] COSTA A, BERTOLOTTI L, BRITO L, et al.Biofilm formation and disinfectant susceptibility of persistent and nonpersistent Listeria monocytogenes isolates from Gorgonzola cheese processing plants[J].Foodborne Pathogens and Disease, 2016, 13(11):602-609.
[13] ORTIZ S, L PEZ-ALONSO V, RODR
PEZ-ALONSO V, RODR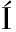 GUEZ P, et al.The connection between persistent, disinfectant-resistant Listeria monocytogenes strains from two geographically separate Iberian pork processing plants:Evidence from comparative genome analysis[J].Applied and Environmental Microbiology, 2016, 82(1):308-317.
GUEZ P, et al.The connection between persistent, disinfectant-resistant Listeria monocytogenes strains from two geographically separate Iberian pork processing plants:Evidence from comparative genome analysis[J].Applied and Environmental Microbiology, 2016, 82(1):308-317.
[14] PALAIODIMOU L, FANNING S, FOX E M.Genomic insights into persistence of Listeria species in the food processing environment[J].Journal of Applied Microbiology, 2021, 131(5):2082-2094.
[15] OCHIAI Y, YOSHIKAWA Y, MOCHIZUKI M, et al.Unique response characteristics in persistent strains of Listeria monocytogenes exposed to low pH[J].Food Microbiology, 2020, 86:103312.
[16] ZHANG H Z, WANG J, CHANG Z Y, et al.Listeria monocytogenes contamination characteristics in two ready-to-eat meat plants from 2019 to 2020 in Shanghai[J].Frontiers in Microbiology, 2021, 12:729114.
[17] STASIEWICZ M J, OLIVER H F, WIEDMANN M, et al.Whole-genome sequencing allows for improved identification of persistent Listeria monocytogenes in food-associated environments[J].Applied and Environmental Microbiology, 2015, 81(17):6024-6037.
[18] 刘耀, 魏元苗, 李玲, 等.食源性致病菌溯源分型技术研究进展[J].食品工业科技, 2022, 43(12):427-437.
LIU Y, WEI Y M, LI L, et al.Advances in traceability typing and identification of foodborne pathogens[J].Science and Technology of Food Industry, 2022, 43(12):427-437.
[19] MUHTEREM-UYAR M, CIOLACU L, WAGNER K H, et al.New aspects on Listeria monocytogenes ST5-ECVI predominance in a heavily contaminated cheese processing environment[J].Frontiers in Microbiology, 2018, 9:64.
[20] RÜCKERL I, MUHTEREM-UYAR M, MURI-KLINGER S, et al.L.monocytogenes in a cheese processing facility:Learning from contamination scenarios over three years of sampling[J].International Journal of Food Microbiology, 2014, 189:98-105.
[21] MCCOLLUM J T, CRONQUIST A B, SILK B J, et al.Multistate outbreak of listeriosis associated with cantaloupe[J].New England Journal of Medicine, 2013, 369(10):944-953.
[22] CHEN Y, GONZALEZ-ESCALONA N, HAMMACK T S, et al.Core genome multilocus sequence typing for identification of globally distributed clonal groups and differentiation of outbreak strains of Listeria monocytogenes[J].Applied and Environmental Microbiology, 2016, 82(20):6258-6272.
[23] CHEN Y, BURALL L S, LUO Y, et al.Listeria monocytogenes in stone fruits linked to a multistate outbreak:Enumeration of cells and whole-genome sequencing[J].Applied and Environmental Microbiology, 2016, 82(24):7030-7040.
[24] SMITH A M, TAU N P, SMOUSE S L, et al.Outbreak of Listeria monocytogenesin South Africa, 2017-2018:Laboratory activities and experiences associated with whole-genome sequencing analysis of isolates[J].Foodborne Pathogens and Disease, 2019, 16(7):524-530.
[25] HALBEDEL S, WILKING H, HOLZER A, et al.Large nationwide outbreak of invasive listeriosis associated with blood sausage, Germany, 2018-2019[J].Emerging Infectious Diseases, 2020, 26(7):1456-1464.
[26] STEPHAN R, ALTHAUS D, KIEFER S, et al.Foodborne transmission of Listeria monocytogenes via ready-to-eat salad:A nationwide outbreak in Switzerland, 2013-2014[J].Food Control, 2015, 57:14-17.
[27] STOLLER A, STEVENS M, STEPHAN R, et al.Characteristics of Listeria monocytogenes strains persisting in a meat processing facility over a 4-year period[J].Pathogens, 2019, 8(1):32.
[28] ANGELO K M, CONRAD A R, SAUPE A, et al.Multistate outbreak of Listeria monocytogenes infections linked to whole apples used in commercially produced, prepackaged caramel apples:United States, 2014-2015[J].Epidemiology and Infection, 2017, 145(5):848-856.
[29] 胡丽丽, 董庆利, 夏阳, 等.单增李斯特菌生物膜形成及其调控机制研究进展[J].食品与发酵工业, 2021, 47(8):276-282.
HU L L, DONG Q L, XIA Y, et al.Advances on the formation and regulation mechanism of Listeria monocytogenes biofilm[J].Food and Fermentation Industries, 2021, 47(8):276-282.
[30] LIU X, CHEN W J, FANG Z X, et al.Persistence of Listeria monocytogenes ST5 in ready-to-eat food processing environment[J].Foods, 2022, 11(17):2561.
[31] FLEMMING H C, WINGENDER J.The biofilm matrix[J].Nature Reviews Microbiology, 2010, 8(9):623-633.
[32] SADIQ F A, FLINT S, LI Y J, et al.Phenotypic and genetic heterogeneity within biofilms with particular emphasis on persistence and antimicrobial tolerance[J].Future Microbiology, 2017, 12(12):1087-1107.
[33] GIAOURIS E, SIM ES M, DUBOIS-BRISSONNET F.The role of biofilms in the development and dissemination of microbial resistance within the food industry[J].Foods, 2020, 9(6):816.
ES M, DUBOIS-BRISSONNET F.The role of biofilms in the development and dissemination of microbial resistance within the food industry[J].Foods, 2020, 9(6):816.
[34] NORWOOD D E, GILMOUR A.Adherence of Listeria monocytogenes strains to stainless steel coupons[J].Journal of Applied Microbiology, 1999, 86(4):576-582.
[35] LUNDÉN J M, MIETTINEN M K, AUTIO T J, et al.Persistent Listeria monocytogenes strains show enhanced adherence to food contact surface after short contact times[J].Journal of Food Protection, 2000, 63(9):1204-1207.
[36] BORUCKI M K, PEPPIN J D, WHITE D, et al.Variation in biofilm formation among strains of Listeria monocytogenes[J].Applied and Environmental Microbiology, 2003, 69(12):7336-7342.
[37] NOWAK J, CRUZ C D, TEMPELAARS M, et al.Persistent Listeria monocytogenes strains isolated from mussel production facilities form more biofilm but are not linked to specific genetic markers[J].International Journal of Food Microbiology, 2017, 256:45-53.
[38] CRUZ C D, FLETCHER G C.Prevalence and biofilm-forming ability of Listeria monocytogenes in New Zealand mussel (Perna canaliculus) processing plants[J].Food Microbiology, 2011, 28(7):1387-1393.
[39] JENSEN A, LARSEN M H, INGMER H, et al.Sodium chloride enhances adherence and aggregation and strain variation influences invasiveness of Listeria monocytogenes strains[J].Journal of Food Protection, 2007, 70(3):592-599.
[40] YUAN L, SADIQ F A, WANG N, et al.Recent advances in understanding the control of disinfectant-resistant biofilms by hurdle technology in the food industry[J].Critical Reviews in Food Science and Nutrition, 2021, 61(22):3876-3891.
[41] BONNEVILLE L, ORTIZ S, MAIA V, et al.Strain and growth conditions may regulate resistance of Listeria monocytogenes biofilms to benzalkonium chloride[J].Applied Sciences, 2020, 10(3):988.
[42] CASEY A, FOX E M, SCHMITZ-ESSER S, et al.Transcriptome analysis of Listeria monocytogenes exposed to biocide stress reveals a multi-system response involving cell wall synthesis, sugar uptake, and motility[J].Frontiers in Microbiology, 2014, 5:68.
[43] MART NEZ-SU
NEZ-SU REZ J V, ORTIZ S, L
REZ J V, ORTIZ S, L PEZ-ALONSO V.Potential impact of the resistance to quaternary ammonium disinfectants on the persistence of Listeria monocytogenes in food processing environments[J].Frontiers in Microbiology, 2016, 7:638.
PEZ-ALONSO V.Potential impact of the resistance to quaternary ammonium disinfectants on the persistence of Listeria monocytogenes in food processing environments[J].Frontiers in Microbiology, 2016, 7:638.
[44] MØRETRØ T, SCHIRMER B C T, HEIR E, et al.Tolerance to quaternary ammonium compound disinfectants may enhance growth of Listeria monocytogenes in the food industry[J].International Journal of Food Microbiology, 2017, 241:215-224.
[45] FOX E M, LEONARD N, JORDAN K.Physiological and transcriptional characterization of persistent and nonpersistent Listeria monocytogenes isolates[J].Applied and Environmental Microbiology, 2011, 77(18):6559-6569.
[46] WANG J J, RAY A J, HAMMONS S R, et al.Persistent and transient Listeria monocytogenes strains from retail deli environments vary in their ability to adhere and form biofilms and rarely have inlA premature stop codons[J].Foodborne Pathogens and Disease, 2015, 12(2):151-158.
[47] HOLAH J T, TAYLOR J H, DAWSON D J, et al.Biocide use in the food industry and the disinfectant resistance of persistent strains of Listeria monocytogenes and Escherichia coli[J].Journal of Applied Microbiology, 2002, 92:111S-120S.
[48] KASTBJERG V G, GRAM L.Model systems allowing quantification of sensitivity to disinfectants and comparison of disinfectant susceptibility of persistent and presumed nonpersistent Listeria monocytogenes[J].Journal of Applied Microbiology, 2009, 106(5):1667-1681.
[49] ORGAZ B, PUGA C H, MART NEZ-SU
NEZ-SU REZ J V, et al.Biofilm recovery from chitosan action:A possible clue to understand Listeria monocytogenes persistence in food plants[J].Food Control, 2013, 32(2):484-489.
REZ J V, et al.Biofilm recovery from chitosan action:A possible clue to understand Listeria monocytogenes persistence in food plants[J].Food Control, 2013, 32(2):484-489.
[50] NILSSON R E, LATHAM R, MELLEFONT L, et al.MudPIT analysis of alkaline tolerance by Listeria monocytogenes strains recovered as persistent food factory contaminants[J].Food Microbiology, 2012, 30(1):187-196.
[51] LUNDÉN J, TOLVANEN R, KORKEALA H.Acid and heat tolerance of persistent and nonpersistent Listeria monocytogenes food plant strains[J].Letters in Applied Microbiology, 2007, 46(2):276-280.
[52] VOGEL B F, HANSEN L T, MORDHORST H, et al.The survival of Listeria monocytogenes during long term desiccation is facilitated by sodium chloride and organic material[J].International Journal of Food Microbiology, 2010, 140(2-3):192-200.
[53] MAISONNEUVE E, GERDES K.Molecular mechanisms underlying bacterial persisters[J].Cell, 2014, 157(3):539-548.
[54] SILVA D A L, TAVARES R M, NERO L A.Interference of sanitizers, NaCl and curing salts on Listeria monocytogenes adhesion and subsequent biofilm formation[J].Letters in Applied Microbiology, 2020, 71(5):438-443.
[55] RODR GUEZ-MELC
GUEZ-MELC N C, CAPITA R, RODR
N C, CAPITA R, RODR GUEZ-JEREZ J J, et al.Effect of low doses of disinfectants on the biofilm-forming ability of Listeria monocytogenes[J].Foodborne Pathogens and Disease, 2019, 16(4):262-268.
GUEZ-JEREZ J J, et al.Effect of low doses of disinfectants on the biofilm-forming ability of Listeria monocytogenes[J].Foodborne Pathogens and Disease, 2019, 16(4):262-268.
[56] CHENG C Y, WANG H, MA T T, et al.Flagellar basal body structural proteins FlhB, FliM, and FliY are required for flagellar-associated protein expression in Listeria monocytogenes[J].Frontiers in Microbiology, 2018, 9:208.
[57] FAN Y, QIAO J J, LU Z X, et al.Influence of different factors on biofilm formation of Listeria monocytogenes and the regulation of cheY gene[J].Food Research International, 2020, 137:109405.
[58] YU T, MA M Y, SUN Y X, et al.The effect of sublethal concentrations of benzalkonium chloride on the LuxS/AI-2 quorum sensing system, biofilm formation and motility of Escherichia coli[J].International Journal of Food Microbiology, 2021, 353:109313.
[59] JIANG X B, JIANG C Y, YU T, et al.Benzalkonium chloride adaptation increases expression of the agr system, biofilm formation, and virulence in Listeria monocytogenes[J].Frontiers in Microbiology, 2022, 13:856274.
[60] JORDAN S J, PERNI S, GLENN S, et al.Listeria monocytogenes biofilm-associated protein (BapL) may contribute to surface attachment of L.monocytogenes but is absent from many field isolates[J].Applied and Environmental Microbiology, 2008, 74(17):5451-5456.
[61] GUERIRI I, CYNCYNATUS C, DUBRAC S, et al.The DegU orphan response regulator of Listeria monocytogenes autorepresses its own synthesis and is required for bacterial motility, virulence and biofilm formation[J].Microbiology (Reading, England), 2008, 154(Pt 8):2251-2264.
[62] TRAVIER L, GUADAGNINI S, GOUIN E, et al.ActA promotes Listeria monocytogenes aggregation, intestinal colonization and carriage[J].PLoS Pathogens, 2013, 9(1):e1003131.
[63] POPOWSKA M, KRAWCZYK-BALSKA A, OSTROWSKI R, et al.InlL from Listeria monocytogenes is involved in biofilm formation and adhesion to mucin[J].Frontiers in Microbiology, 2017, 8:660.
[64] ELHANAFI D, DUTTA V, KATHARIOU S.Genetic characterization of plasmid-associated benzalkonium chloride resistance determinants in a Listeria monocytogenes strain from the 1998—1999 outbreak[J].Applied and Environmental Microbiology, 2010, 76(24):8231-8238.
[65] KROPAC A C, ESHWAR A K, STEPHAN R, et al.New insights on the role of the pLMST6 plasmid in Listeria monocytogenes biocide tolerance and virulence[J].Frontiers in Microbiology, 2019, 10:1538.
[66] HURLEY D, LUQUE-SASTRE L, PARKER C T, et al.Whole-genome sequencing-based characterization of 100 Listeria monocytogenes isolates collected from food processing environments over a four-year period[J].mSphere, 2019, 4(4):e00252-19.
[67] HE K, XIN Y P, SHAN Y, et al.Phosphorylation residue T175 in RsbR protein is required for efficient induction of sigma B factor and survival of Listeria monocytogenes under acidic stress[J].Journal of Zhejiang University-SCIENCE B, 2019, 20:660-669.
[68] CHENG C Y, YANG Y C, DONG Z M, et al.Listeria monocytogenes varies among strains to maintain intracellular pH homeostasis under stresses by different acids as analyzed by a high-throughput microplate-based fluorometry[J].Frontiers in Microbiology, 2015, 6:15.
[69] PÖNTINEN A, AALTO-ARANEDA M, LINDSTRÖM M, et al.Heat resistance mediated by pLM58 plasmid-borne ClpL in Listeria monocytogenes[J].mSphere, 2017, 2(6):e00364-e00317.
[70] CHENG C Y, LIU F, JIN H B, et al.The DegU orphan response regulator contributes to heat stress resistance in Listeria monocytogenes [J].Frontiers in Cellular and Infection Microbiology, 2021;11:761335.
[71] RINGUS D L, IVY R A, WIEDMANN M, et al.Salt stress-induced transcription of σB-and CtsR-regulated genes in persistent and non-persistent Listeria monocytogenes strains from food processing plants[J].Foodborne Pathogens and Disease, 2012, 9(3):198-206.
[72] HEIN I, KLINGER S, DOOMS M, et al.Stress survival islet 1 (SSI-1) survey in Listeria monocytogenes reveals an insert common to Listeria innocua in sequence type 121 L.monocytogenes strains[J].Applied and Environmental Microbiology, 2011, 77(6):2169-2173.
[73] PIERCEY M J, ELLS T C, MACINTOSH A J, et al.Variations in biofilm formation, desiccation resistance and Benzalkonium chloride susceptibility among Listeria monocytogenes strains isolated in Canada[J].International Journal of Food Microbiology, 2017, 257:254-261.
[74] CHEN Y, CHEN Y H, POUILLOT R, et al.Genetic diversity and profiles of genes associated with virulence and stress resistance among isolates from the 2010—2013 interagency Listeria monocytogenes market basket survey[J].Plos One, 2020, 15(4):e0231393.
[75] HARTER E, WAGNER E M, ZAISER A, et al.Stress survival islet 2, predominantly present in Listeria monocytogenes strains of sequence type 121, is involved in the alkaline and oxidative stress responses[J].Applied and Environmental Microbiology, 2017, 83(16):e00827-e00817.
[76] SHUKLA S K, RAO T S.Targeting hydrophobicity in biofilm-associated protein (Bap) as a novel antibiofilm strategy against Staphylococcus aureus biofilm[J].Biophysical Chemistry, 2022, 289:106860.
[77] 孙奇凡. 食用菌工厂中单增李斯特菌污染溯源与快速检测技术研究[D].广州:广东工业大学, 2021.
SUN Q F.Study on traceability and rapid detection technology of Listeria monocytogenes pollution in edible fungi factory[D].Guangzhou:Guangdong University of Technology, 2021.