随着社会经济快速发展,人们生活品质提高,食品安全与品质得到越来越多的关注。在食品流通过程中,温度和时间是影响产品质量的重要因素,但是难以直观判断,因此传统标注保质期的方式并不能准确代表其实际品质[1]。此外,人们健康意识的增强使得更多的消费者青睐于无添加、短保质期食品,而这类产品往往只提供简易包装甚至无包装,并且很容易因贮存、运输不当发生微生物污染、过氧化值超标等食品安全问题。因其保质期较短,在食品安全抽检中短保食品常出现检验报告发出时样品已超过保质期的情况[2],报告结果效力存在疑问,并且不便于消费者对食品品质的实时判断。时间-温度传感器(time-temperature indicator, TTI)可监测、记录和传达食品经历的时间-温度历史[3],尤其对高温暴露响应灵敏,可以通过颜色变化等易感知的方式让消费者掌握产品质量、剩余货架期等信息。
已有报道的TTI类型包括酶型[4]、美拉德反应型[5]、扩散型[6]、聚合反应型[7]等,主要应用于冷冻和冷藏产品。MENG等[8]基于葡萄糖淀粉酶微胶囊开发了一种固态酶促时间温度指示剂,在4 ℃条件下指示冷冻新鲜猪肉的时间-温度历史。酶型TTI在长期贮藏过程中,温度变化导致酶不稳定和不可逆失活,会造成巨大成本[9]。扩散型TTI由温感部分与显示部分组成,通过有色扩散边界移动来指示产品品质。其一端固定熔融物质需要硬壳保护体积较大,且温敏性低,因此纯粹基于物理扩散的TTI正逐渐被淘汰[10]。二乙炔类时间-温度指示器颜色变化明显,通过复配其他物质或改性等方式调控其温度敏感性,可操作性强[11],可根据实际需求设计定制TTI。此外,相比于温度感知与显示器两部分分离的扩散型TTI,二乙炔类指示剂同时进行温度感知与显示,可制成油墨喷涂于外包装或不干胶标签等形式[12-13],应用于对食品品质的监测,使用方便有利于商业化。聚二乙炔(polydiacetylenes, PDAs)是被研究的温度敏感变色材料最多的化合物之一[11],目前已有聚二乙炔在时间温度指示剂方面的相关研究。GOU等[14]在聚二乙炔的悬浮液中加入两亲性聚合物,认为聚二乙炔/两亲性聚合物体系可以在10~50 ℃应用于时温色敏传感器,但是外加物质的体系变色速度过快,适用范围有限。邱灵敏[15]构建了一种由聚二乙炔脂质体的凝胶微球和吐温20溶液组成的TTI,可以较准确地指示三文鱼的货架寿命,但是所添加的吐温20溶液易泄露导致对TTI包装要求高。
对PDAs变色机理的研究表明,可通过化学修饰改变侧链基团调控聚二乙炔的变色性能[16-20],以达到良好的指示性能。作为富含电子的芳香族杂环化合物, 咪唑类受体因能形成较强的(C-H)+…X-离子氢键而受到广泛研究[21]。基于咪唑鎓基聚二乙炔开发的各类传感器已有报道[21-23],但应用于时温传感器的研究却很少。因此,本文构建了咪唑鎓基聚二乙炔复合体,研究时间-温度对其变色影响。本文所提出的咪唑鎓基聚二乙炔复合体具有适用时间-温度范围广、响应灵敏、无损监测等优势,在实现连续记录食品、药品等产品经历的时间-温度历史对于品质的影响方面具有巨大的应用潜力。
1 材料与方法
1.1 材料与试剂
10,12-二十五二炔酸(10,12-pentacosadiynoic acid, PCDA)、1-(3-氨基丙基)咪唑、二氯甲烷、无水甲醇、乙腈、硅胶(200~300目),国药集团化学试剂有限公司;N,N’-二环己基碳二亚胺(N,N’-dicyclohexylcarbodiimide, DCC),北京伊诺凯科技有限公司,N-羟基琥珀酰亚胺(N-hydroxysuccinimide, NHS)、碘甲烷(CH3I),上海泰坦科技股份有限公司。
1.2 仪器与设备
三用紫外分析仪,邦西仪器科技(上海)有限公司;RE-52A型旋转蒸发仪,上海亚荣仪器有限公司;BCD-226SK型冰箱,青岛海尔股份有限公司;UV-2450型紫外可见分光光度计,日本岛津公司;Avance Ⅲ 400 MHz型全数字化核磁共振波谱仪,德国布鲁克公司;NEXUS型傅里叶变换红外光谱仪,美国尼高力仪器公司。
1.3 实验方法
1.3.1 咪唑鎓基聚二乙炔复合体{3-methyl-1-[3-(pentacosa-10,12-diynamido)propyl]-1H-imidazol-3-ium, PCDA-IUM}的合成
根据文献[21],在含有0.75 g(2.01 mmol)PCDA的二氯甲烷(20 mL)溶液中,加入300 mg(2.61 mmol)NHS和600 mg(2.91 mmol)DCC。将此溶液在室温下N2保护搅拌过夜。滤除白色沉淀物后的滤液经旋蒸浓缩,以二氯甲烷为洗脱剂经硅胶柱层析纯化,旋转蒸发除去溶剂后得到PCDA-NHS。将PCDA-NHS加入含有500 mg(4.0 mmol)1-(3-氨基丙基)咪唑的二氯甲烷(10 mL)溶液中,室温下搅拌反应24 h,反应后的混合物经旋蒸浓缩后,通过硅胶柱层析[V(甲烷)∶V(甲醇)=97∶3]纯化得到PCDA-IM中间产物。在含有0.25 g (0.52 mmo1)PCDA-IM的乙腈(20 mL)溶液中,加入400 mg(2.81 mmol)CH3I,将溶液在85 ℃下回流过夜。旋转蒸发除去溶剂后,得到高纯度单体PCDA-IUM。
1.3.2 聚二乙炔的制备
根据文献[22]方法,修改如下:称取4.96 mg PCDA-IUM和3.75 mg PCDA,加入20 mL去离子水,将此溶液在80 ℃水浴超声30 min,超声完成后冷却至室温,过滤后的溶液在冰箱中于4 ℃自组装至少12 h。自组装后的溶液置于254 nm紫外光下照射3 min,聚合得到蓝色的聚PCDA/PCDA-IUM(物质的量之比为1∶1)溶液,贮存于4 ℃冰箱备用。聚PCDA、聚PCDA-IUM及其他比例的复合体依比例称取相应量,按照上述方法制备。
1.3.3 红外光谱表征
聚PCDA、聚PCDA/PCDA-IUM(1∶1)、聚PCDA-IUM溶液经冻干处理,得到固体样品。使用NEXUS型傅里叶变换红外光谱仪直接对固体样品进行光谱扫描。波长范围为650~4 000 cm-1,以空气为背景,扫描次数为32。
1.3.4 不同比例聚PCDA/PCDA-IUM的变色温度试验设计
各取0.15 mL不同比例的聚二乙炔溶液加入装有1.35 mL去离子水的试管中,置于不同温度(25~80 ℃)水浴中孵育10 min,在日光条件下拍照记录不同温度溶液的颜色变化。通过紫外可见分光光度计测定其紫外-可见吸收光谱,狭缝宽度为2.0 nm,波长范围为400~700 nm。使用比色响应(colorimetric response, CR)表示聚二乙炔由蓝向红的颜色转变程度,CR越大表明颜色转变程度越大,其计算如公式(1)和公式(2)所示[24]:
(1)
(2)
式中:CR,溶液的比色响应,%;Ablue,溶液在蓝相特征峰对应的吸光度值;Ared,溶液在红相特征峰对应的吸光度值;PB0,溶液在初始温度下的蓝相百分比,%;PB1,溶液在不同温度不同时间的蓝相百分比,%。
1.3.5 不同浓度聚PCDA/PCDA-IUM的变色寿命试验设计
将聚PCDA/PCDA-IUM(1∶1)用去离子水配制成0.01、0.05、0.1、0.2、0.3 mmol/L浓度体系。将不同浓度体系分别置于30、35、40 ℃水浴中,使用紫外可见分光光度计测量不同时间温度的体系在640、545 nm的吸光度值,并计算CR。
2 结果与分析
2.1 聚PCDA/PCDA-IUM的结构表征
本文合成的PCDA-IUM通过1H NMR和13C NMR进行表征,结果与先前报道基本一致[21]。1H NMR (CDCl3,600 MHz) δ (ppm):9.84 (d, J=1.7 Hz, 1H), 7.77 (t, J=1.8 Hz, 1H), 7.37 (t, J=1.9 Hz, 1H), 4.40 (t, J=6.5 Hz, 2H), 4.04 (s, 3H), 3.26 (q, J=6.0 Hz, 2H), 2.28~2.19 (m, 8H), 1.59~1.22 (m, 32H), 0.84 (t, J=7.0 Hz, 3H)。13C NMR (CDCl3,151 MHz) δ(ppm):173.870、136.105、122.219、122.170、64.246, 46.573、35.995、30.904、29.309、28.616、28.471、28.331、28.278、28.091、27.961、27.828、27.366、24.835、21.675、18.198、13.120。
为了分析复合体的结构,对聚PCDA、聚PCDA/PCDA-IUM(1∶1)和聚PCDA-IUM进行了红外光谱检测。如图1所示,2 919 cm-1和2 847 cm-1处分别为—CH2的对称和不对称伸缩振动峰[25],作为共性特征出现于3个不同的聚合物中。聚PCDA-IUM在3 290 cm-1处出现酰胺中N—H伸缩振动峰[26],聚PCDA在1 690 cm-1处出现氢键作用的—COOH中C![]() O的吸收振动峰,二者在聚PCDA/PCDA-IUM(1∶1)中皆出现,但强度大幅减弱,这证实了复合体制备成功,且PCDA与PCDA-IUM分子是交替排列的。
O的吸收振动峰,二者在聚PCDA/PCDA-IUM(1∶1)中皆出现,但强度大幅减弱,这证实了复合体制备成功,且PCDA与PCDA-IUM分子是交替排列的。

图1 聚PCDA、聚PCDA-IUM与聚PCDA/PCDA-IUM(1∶1)的 红外光谱
Fig.1 FT-IR spectra of poly PCDA, poly PCDA-IUM, and poly PCDA/PCDA-IUM(1∶1)
2.2 比例对聚PCDA/PCDA-IUM变色温度的影响
如图2所示,分别是不同物质的量之比(10∶0、6∶4、5∶5、4∶6、0∶10)的聚PCDA/PCDA-IUM经历不同加热温度后的颜色变化。PCDA含量不同,聚PCDA/PCDA-IUM变色温度不同,因此调整复合体比例可以得到适用于不同温度范围的指示剂。纯聚PCDA(10∶0)加热至60 ℃变成橘红色,这是由于温度升高促进聚PCDA中尾部的烷基、头部羧基和共轭主链的热运动,分子链的链段重排,从而引发颜色转变[24]。相比于聚PCDA与聚PCDA-IUM,复合体的变色温度降低10~35 ℃。其中,聚PCDA/PCDA-IUM(1∶1)于25 ℃变成蓝紫色,30 ℃变成粉红色,该变色温度范围适用于多数常温贮存、运输食品的流通环境温度。并且撤去加热条件后,颜色并未恢复,说明该体系变色不可逆。
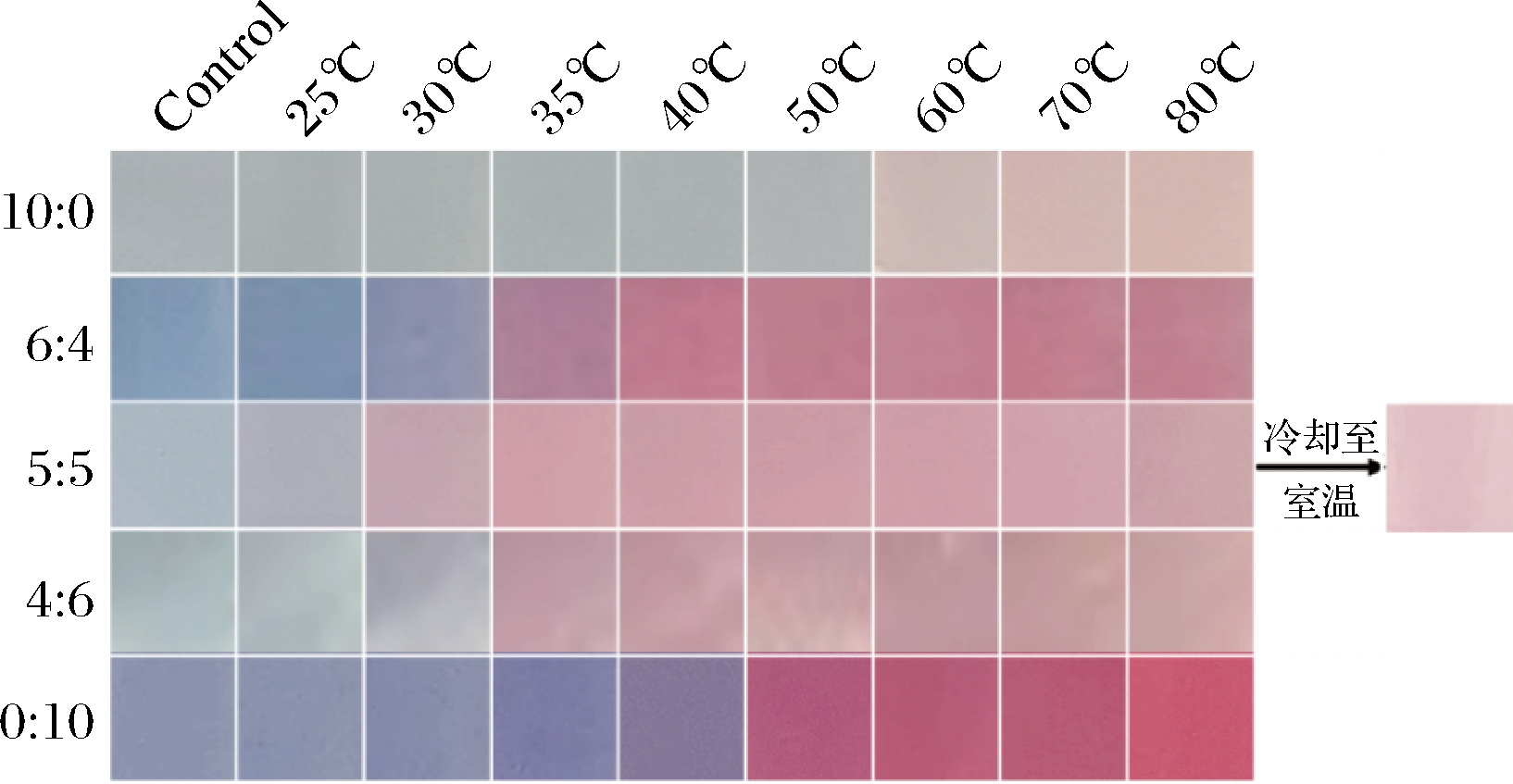
图2 不同比例的聚PCDA/PCDA-IUM在不同温度下的照片
Fig.2 Photographs of different ratios of poly PCDA/PCDA-IUM at different temperatures
聚二乙炔的颜色转变通常伴随可见光光谱从低能带到高能带的显著转变[8]。如图3所示,分别是不同比例聚PCDA/PCDA-IUM在不同温度的紫外可见光谱图。随着温度升高,聚二乙炔的最大吸收峰波长发生蓝移。聚PCDA、聚PCDA/PCDA-IUM(5∶5)和聚PCDA-IUM的吸收峰分别从655、640、626 nm(蓝相特征峰)蓝移至545 nm(红相特征峰)左右,符合聚二乙炔由蓝向红色转变的特征峰。在这5种比例体系中,相较于未升温的初始对照,聚PCDA/PCDA-IUM(5∶5)的蓝相特征峰在温度升至30 ℃时即显著下降(图3-c),伴随红相特征峰大幅上升,对应于图2中在30 ℃时明显的肉眼可见变色。

a-10∶0;b-6∶4;c-5∶5;d-4∶6;e-0∶10
图3 不同比例聚PCDA/PCDA-IUM在不同温度的紫外光谱
Fig.3 UV-Vis spectra of poly PCDA/PCDA-IUM with different molar ratios at different temperatures
为了量化5种聚二乙炔的变色结果,采用CR定量计算其颜色转变程度。CR越大,材料的颜色转变程度越大[24]。如图4所示,不同比例聚二乙炔的CR在升温的过程中逐渐增大,对应于图2中由蓝向红色转变程度的增加。其中,聚PCDA、聚PCDA-IUM和聚PCDA/PCDA-IUM(5∶5)分别在60、45、30 ℃左右骤增;在70、50、35 ℃到达肉眼可见变色终点,对应值分别为23.9%、90.9%、96.2%。聚PCDA/PCDA-IUM的CR高于其他比例体系,尤其在30 ℃时,说明其变色程度更高,这与图2拍摄记录的变色情况一致。结果进一步验证了聚PCDA/PCDA-IUM(1∶1)体系对热刺激响应更灵敏,因此选择物质的量之比为1∶1的体系进行后续研究。
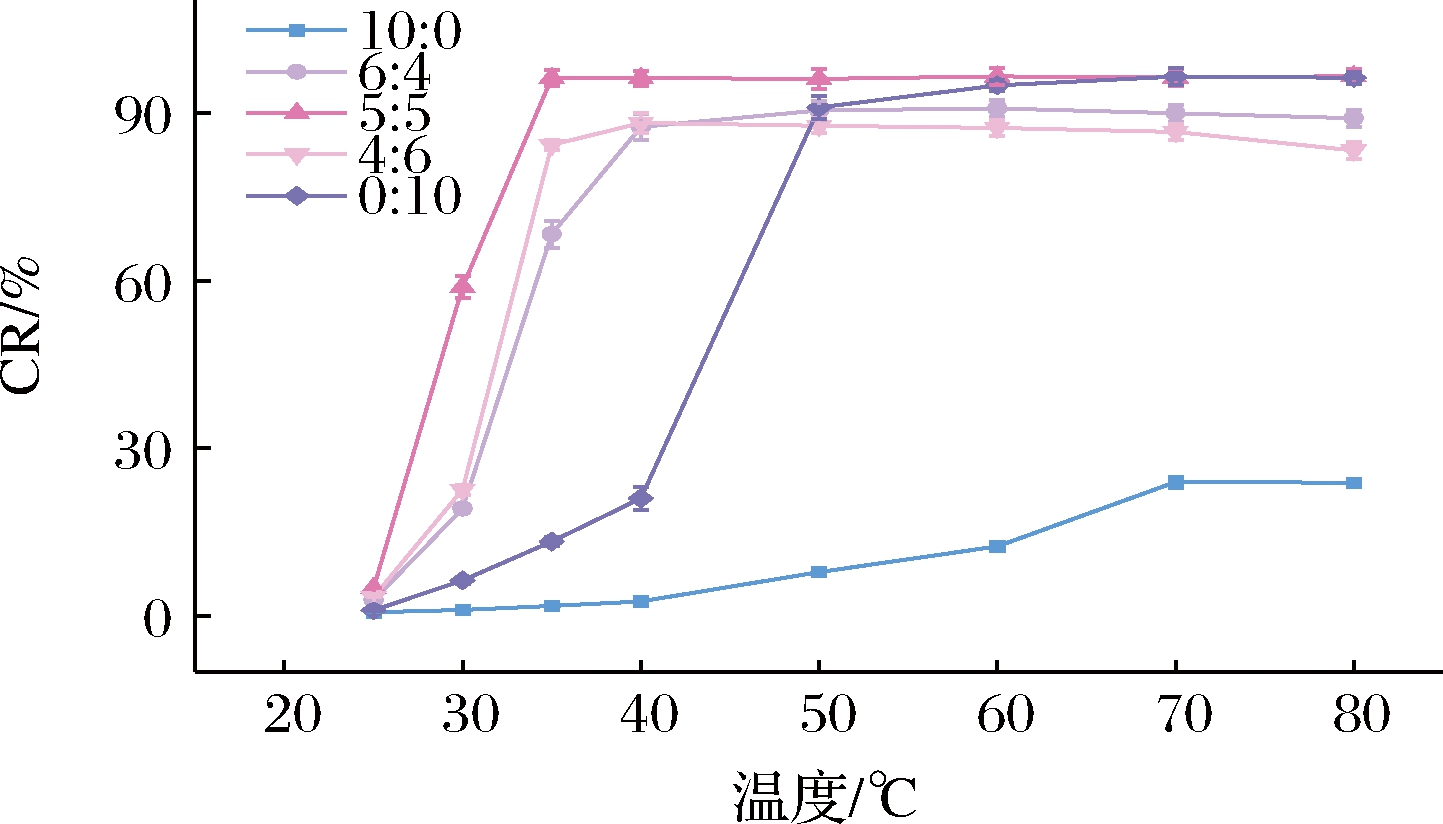
图4 不同比例聚PCDA/PCDA-IUM在不同温度的CR
Fig.4 The CR of poly PCDA/PCDA-IUM with different molar ratios at different temperatures
2.3 浓度对聚PCDA/PCDA-IUM变色寿命的影响
如图5所示,聚PCDA/PCDA-IUM(5∶5)在30~40 ℃发生明显肉眼可见颜色转变,不同浓度、温度条件下,颜色转变情况不同。但随着加热时间延长,颜色都不再发生明显变化。这表明了聚PCDA/PCDA-IUM热致变色具有时间累积效应,存在变色寿命。以0.3 mmol/L为例,在40 ℃时加热1 min即从蓝色转变为橙红色,并且随着时间延长,颜色不再发生明显变化,可认为已到达变色终点;35 ℃时加热1 min体系仍呈现紫色,直至72 h才转变为橙红色;而在30 ℃时转变为橙红色需要168 h。这是因为温度越高,聚二乙炔变色速率越快[13]。如图5-a所示,在30 ℃条件下,聚PCDA/PCDA-IUM(1∶1)体系浓度从0.01 mmol/L提高至0.3 mmol/L,到达变色终点的时间从3 min延长至168 h左右,推测在此基础上提高体系浓度,可进一步延长变色寿命。
为了定量聚PCDA/PCDA-IUM(1∶1)的变色程度与时间的关系,建立了CR与时间的关系曲线,如图6所示。对于物质的量之比为1∶1的复合体体系,40 ℃温度较高,以致不同浓度体系的CR在1 min左右快速升至最大值并趋于稳定;在30 ℃条件下,随着浓度的提高,CR达到最大值的时间显著延长,CR变化的趋势与图5记录的颜色变化一致。进一步证明了聚PCDA/PCDA-IUM(1∶1)所在环境温度越高,变色寿命越短。恒温条件下,通过简单调整聚PCDA/PCDA-IUM(1∶1)体系浓度,可以得到不同热致变色寿命的复合体。

a-30 ℃;b-35 ℃;c-40 ℃
图5 不同浓度聚PCDA/PCDA-IUM(1∶1)在不同温度时间的颜色变化
Fig.5 Color change of poly PCDA/PCDA-IUM (1∶1) with different concentrations under different temperatures and time
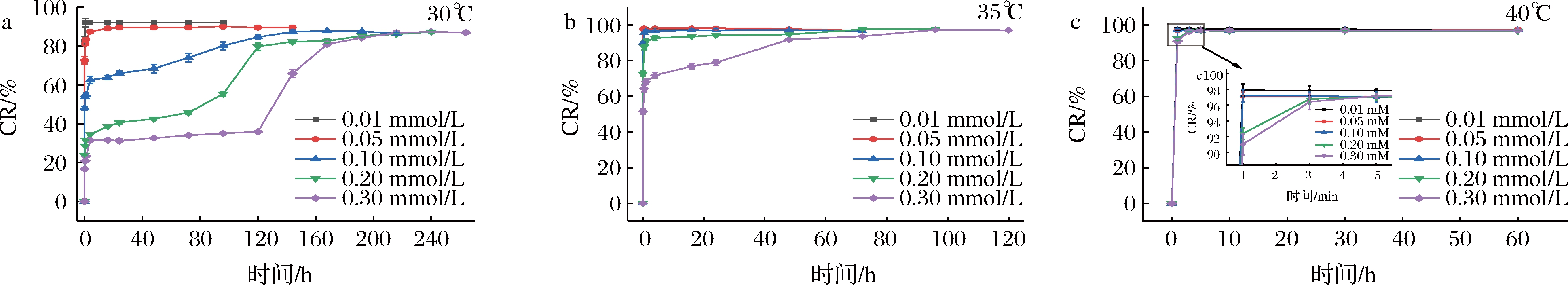
a-30 ℃;b-35 ℃;c-40 ℃
图6 不同浓度聚PCDA/PCDA-IUM(1∶1)在不同温度的CR与时间的关系
Fig.6 Relationship between the CR values and time of poly PCDA/PCDA-IUM (1∶1) with different concentrations at different temperatures
3 结论
本文将咪唑鎓基修饰的二乙炔单体与PCDA单体复配,得到的聚二乙炔复合体显著降低了聚PCDA的变色温度。其中,PCDA/PCDA-IUM(1∶1)在25 ℃即可发生肉眼可见的颜色转变,且可以通过改变比例调整变色温度,扩大应用温度范围。聚PCDA/PCDA-IUM在不同温度下的颜色变化具有时间累积效应,随着时间的延长变色程度逐渐提高,到达变色终点后趋于稳定,提高聚PCDA/PCDA-IUM(1∶1)浓度显著延长其变色寿命。因此,其在指示长保质期产品的货架期和监测短保质期食品的品质变化方面都有广泛的应用前景。
[1] 成欢, 朱光明, 宋蕊.时间温度指示剂研究进展[J].化工进展, 2013, 32(4):885-890.
CHENG H, ZHU G M, SONG R.Progress of time-temperature indicators[J].Chemical Industry and Engineering Progress, 2013, 32(4):885-890.
[2] 朱云. 短保食品抽检问题分析及风险防控[J].食品安全导刊, 2021(3):57;59.
ZHU Y.Analysis of sampling inspection of short-term food and risk prevention and control[J].China Food Safety Magazine, 2021(3):57;59.
[3] TAOUKIS P S, LABUZA T P.Applicability of time-temperature indicators as shelf life monitors of food products[J].Journal of Food Science, 1989, 54(4):783-788.
[4] 李慧杰, 贾玲, 彭雅茜子, 等.一种酶型时间温度指示器的研究[J].绿色包装, 2016(7):30-35.
LI H J, JIA L, PENG Y, et al.Research on time temperature indicator based on lipase[J].Green Packaging, 2016(7):30-35.
[5] TEODOROWICZ M, VAN NEERVEN J, SAVELKOUL H.Food processing:The influence of the Maillard reaction on immunogenicity and allergenicity of food proteins[J].Nutrients, 2017, 9(8):835-835.
[6] 杨加敏, 胥义.扩散型时间-温度指示器在预测奇异果品质中的应用[J].食品与发酵工业, 2019, 45(9):176-182.
YANG J M, XU Y.Application of a new diffuse type time-temperature indicator in characterizing the quality of kiwifruits during storage[J].Food and Fermentation Industries, 2019, 45(9):176-182.
[7] WESTON M, KUCHEL R P, CIFTCI M, et al.A polydiacetylene-based colorimetric sensor as an active use-by date indicator for milk[J].Journal of Colloid and Interface Science, 2020, 572:31-38.
[8] MENG J J, QIAN J, TANG Y Y.A solid-state time-temperature indicator used in chilled fresh pork monitoring[J].Packaging Technology and Science, 2018, 31(5):353-360.
[9] 刘冬青, 陈朴, 臧鹏, 等.时间-温度指示器在食品保质期预测中的应用[J].食品工业科技, 2021, 42(22):1-10.
LIU D Q, CHEN P, ZANG P, et al.Application of time-temperature indicator in food shelf life prediction[J].Science and Technology of Food Industry, 2021, 42(22):1-10.
[10] 蔡梦琪, 李琳, 俞朱敏, 等.时间-温度指示器在冷链运输中的应用进展[J].包装工程, 2022, 43(19):1-10.
CAI M Q, LI L, YU Z M, et al.Application process of time-temperature indicator in cold chain transportation[J].Packaging Engineering, 2022, 43(19):1-10.
[11] 钱艳峰, 王娅, 张明玥, 等.用于监测食品新鲜度的时间-温度指示器研究现状[J].食品工业科技, 2022, 43(7):10-20.
QIAN Y F, WANG Y, ZHANG M Y, et al.Research status of time-temperature indicator for monitoring food freshness[J].Science and Technology of Food Industry, 2022, 43(7):10-20.
[12] 王少东. 时间温度指示器在易腐败食品包装中的研究应用现状[J].中国包装工业, 2014(14):7-8.
WANG S D.Research and application status of time and temperature indicator in perishable food packaging[J].China Packaging Industry, 2014(14):7-8.
[13] 成欢, 朱光明, 宋蕊.二乙炔类时间温度指示剂[J].化学进展, 2013, 25(12):2112-2118.
CHENG H, ZHU G M, SONG R.Diacetylenic time-temperature indicators[J].Progress in Chemistry, 2013, 25(12):2112-2118.
[14] GOU M L, GUO G, ZHANG J, et al.Time-temperature chromatic sensor based on polydiacetylene (PDA) vesicle and amphiphilic copolymer[J].Sensors and Actuators B:Chemical, 2010, 150(1):406-411.
[15] 邱灵敏. 基于聚二乙炔的时间温度指示器的制备及其应用[D].无锡:江南大学, 2021.
QIU L M.Preparation and application of time and temperature indicator based on polydiacetylene[D].Wuxi:Jiangnan University, 2021.
[16] POTISATITYUENYONG A, ROJANATHANES R, TUMCHARERN G, et al.Electronic absorption spectroscopy probed side-chain movement in chromic transitions of polydiacetylene vesicles[J].Langmuir, 2008, 24(9):4461-4463.
[17] CHAROENTHAI N, PATTANATORNCHAI T, WACHARASINDHU S, et al.Roles of head group architecture and side chain length on colorimetric response of polydiacetylene vesicles to temperature, ethanol and pH[J].Journal of Colloid and Interface Science, 2011, 360(2):565-573.
[18] PHONCHAI N, KHANANTONG C, KIELAR F, et al.Enhancing thermal and chemical sensitivity of polydiacetylene colorimetric sensors:The opposite effect of zinc oxide nanoparticles[J].Colloids and Surfaces A:Physicochemical and Engineering Aspects, 2020, 589:124459.
[19] KHANANTONG C, CHAROENTHAI N, KIELAR F, et al.Influences of bulky aromatic head group on morphology, structure and color-transition behaviors of polydiacetylene assemblies upon exposure to thermal and chemical stimuli[J].Colloids and Surfaces A:Physicochemical and Engineering Aspects, 2019, 561:226-235.
[20] KIM J M, LEE J S, CHOI H, et al.Rational design and in-situ FTIR analyses of colorimetrically reversibe polydiacetylene supramolecules[J].Macromolecules, 2005, 38(22):9366-9376.
[21] CHEN X Q, KANG S, KIM M, et al.Thin-film formation of imidazolium-based conjugated polydiacetylenes and their application for sensing anionic surfactants[J].Angewandte Chemie International Edition, 2010, 49(8):1422-1425.
[22] ZHANG Z J, LI J, WANG F, et al.A polydiacetylenes-based sensor for the efficient detection of phospholipase D activity[J].Sensors and Actuators B:Chemical, 2019, 282:636-643.
[23] LEE W, LEE D, KIM J Y, et al.Imidazole and triazole head group-containing polydiacetylenes for colorimetric monitoring of pH and detecting HCl gas[J].Materials Chemistry Frontiers, 2018, 2(2):291-295.
[24] 张亚娜. 聚二乙炔基复合材料的制备及其热致可逆变色性能研究[D].兰州:西北师范大学, 2019.
ZHANG Y N.Preparation and thermochromic properties of polydiacetylene-based composites[D].Lanzhou:Northwest Normal University, 2019.
[25] SAGONG H Y, SON M H, MIN S H, et al.Controllable color change of polydiacetylene vesicles under thermal-photo stimuli[J].Polymer, 2021, 233:124211.
[26] XU Y Y, FU S Y, LIU F Y, et al.Multi-stimuli-responsiveness of a novel polydiacetylene-based supramolecular gel[J].Soft Matter, 2018, 14(39):8044-8050.