赭曲霉毒素A(ochratoxin A,OTA)是低分子质量真菌次级代谢产物,在谷物、葡萄、可可、咖啡豆及其加工产品中均被检测发现[1]。OTA具有多种毒性作用,包括肾毒性、肝毒性、神经毒性和免疫毒性,被国际癌症研究机构划分为能够导致人类和动物患癌的ⅡB类致癌物[2]。作为一种弱有机酸,OTA结构中的羧基与羟基会发生解离,在碱性、中性及弱酸性条件下OTA多带有负电(OTA-,OTA2-)[3]。虽然OTA物理化学性质稳定,很难通过高温加热等传统的食品加工与生产途径将其消除[4]。但是利用OTA的电负性,采用带正电吸附剂以静电相互作用脱除OTA,为解决真菌毒素的消除困难提供了新的思路和方法。
葡萄在采前与采后均易受到青霉属与曲霉属真菌侵染,并在生长过程中产生并积累OTA毒素。葡萄浆果的污染直接导致葡萄汁中的OTA曝露,但是不同葡萄果汁中OTA的污染存在差异,红葡萄果汁中较为严重,而白葡萄汁检出率则相对较低。德国分析发现89%的红葡萄汁中OTA含量超过10 ng/L,而白葡萄汁的比例为81%(OTA>10 ng/L)[5]。有研究检测发现中国葡萄汁阳性率高达100%,伊朗检测样本中OTA污染水平达到了55.7%[6-7]。此外,评估计算发现全球葡萄汁中OTA流行率为36%,因此葡萄汁中OTA的消除成为了该产业亟待解决的问题[8]。
无机陶瓷基膜具有价格低廉、耐高温、耐酸碱、机械强度高、易再生、安全等优点,广泛应用于饮用水净化、医药、牛奶除菌等领域[8]。当荷电材料覆盖在无机陶瓷膜的表面与孔径内时,可获得与基膜带有不同荷电性质的无机陶瓷膜[9]。荷电无机陶瓷膜因带有电荷,除了能够以物理截留的方式分离组分外,还可以利用静电吸附作用来分离细菌、病毒、小分子染料等粒径较小且带有相反电荷的微粒,如四环素、有机染料等[10]。截至目前,荷电无机陶瓷膜在污水处理领域被广泛研究,而利用该材料消除食品中真菌毒素尚未见报道。传统的真菌毒素物理脱除材料单一,主要包括活性炭、膨润土和壳聚糖等,这些材料一般通过较大的比表面积和较小的孔径来物理截留真菌毒素[1]。而真菌毒素大多为小分子化合物,很难利用物理筛分进行去除。此外,物理吸附剂的截留作用在去除毒素的同时,会对食品中大分子营养物质造成损失。相较传统的物理吸附材料,荷电无机陶瓷膜可利用静电作用选择性吸附食品中真菌毒素,且陶瓷膜较大的孔径能有效避免吸附剂对食品营养品质及风味的影响,可作为新型、高效的真菌毒素的脱除剂来使用。
本文首次提出了一种利用纳米-氧化镁(nano-MgO)荷正电无机陶瓷膜与带负电OTA间的静电吸附作用来去除葡萄汁中OTA的新方法。采用荷正电纳米材料对无机陶瓷膜进行改性,利用聚乙二醇作为分散剂来提高无机陶瓷膜表面纳米材料的覆盖度。以荷正电无机陶瓷膜作为OTA脱除部件,通过改变蠕动泵的流速、溶液的pH、溶液的温度等来确定MgO荷正电膜脱除OTA的最佳条件,应用于葡萄汁中OTA的脱除,并对葡萄汁的品质和香气变化进行分析。nano-MgO荷正电无机陶瓷膜能够静电脱除食品中带负电的真菌毒素,提供了一种真菌毒素物理脱除的新材料与新方法。荷电无机陶瓷膜价格低廉、使用简单、安全可靠,将无机陶瓷膜修饰不同的荷电材料,还可延伸至其他真菌毒素的脱除。
1 材料与方法
1.1 材料与试剂
无机陶瓷基膜,广州净易高科技股份有限公司;尿素,烟台市双双化工有限公司;硝酸,天津市标准科技有限公司;MgCl2·6H2O,天津市凯通化学主要试剂有限公司;聚乙二醇6000(polyethylene glycol,PEG),天津市大茂化学主要试剂厂;OTA,青岛普瑞邦生物工程有限公司;以上试剂均为分析纯;甲醇、乙腈,均为色谱纯,成都市科隆化学品有限公司。
1.2 仪器与设备
TECNAIG2透射电子显微镜,FEI公司;KSL-1400X马弗炉,合肥科晶材料技术有限公司;ZEN3600纳米粒度仪,马尔文公司;265079气相色谱-质谱联用仪,美国Thermo Fisher Scientific公司;JEOL-5600LV扫描电子显微镜,日本电子株式会社;DS-2510超声波清洗仪,上海奥谱勒仪器有限公司;LC-20A高效液相色谱仪串联RF-20A荧光检测器,日本岛津;MFC229多功能固相净化柱,青岛普瑞邦生物工程有限公司。
1.3 实验方法
1.3.1 nano-MgO荷正电无机陶瓷的制备
无机陶瓷打磨加工为直径2 cm、厚3 mm、2.0 g的基膜,然后在2 mol/L HNO3 溶液中浸泡8 h,去离子水超声清洗30 min后,100 ℃下烘干处理,重复上述步骤3次[11]。
MgCl2·6H2O和尿素(摩尔质量之比为4∶1)分别溶于100 mL去离子水。将质量为MgCl2·6H2O 1.5%的PEG倒入圆底烧瓶,加入尿素溶液,并逐滴滴加MgCl2·6H2O溶液,于90 ℃反应5 h后获得涂膜液。涂膜液加去离子水超声清洗,静置8 h后保留下层白色乳浊液备用。涂膜时先用去离子水超声清洗涂膜液1 h,放入洁净的无机陶瓷基膜超声涂膜30 min,之后置于80 ℃的烘箱烘干,重复超声涂膜3次后将修饰后的无机陶瓷基膜置于马弗炉中,程序升温烧制[11]。
1.3.2 形貌及结构表征
纳米荷电无机膜表面微观形貌及形态结构利用JEOL-5600LV型扫描电子显微镜进行观察分析。nano-MgO的晶体形态采用透射电子显微镜进行测定观察。
1.3.3 OTA脱除实验装置
OTA吸附装置如图1所示,核心组件为nano-MgO荷正电无机陶瓷膜,此外还设置有恒温装置,蠕动进样装置和溶液收集装置,装置接口均保持密封以防止溶液挥发。
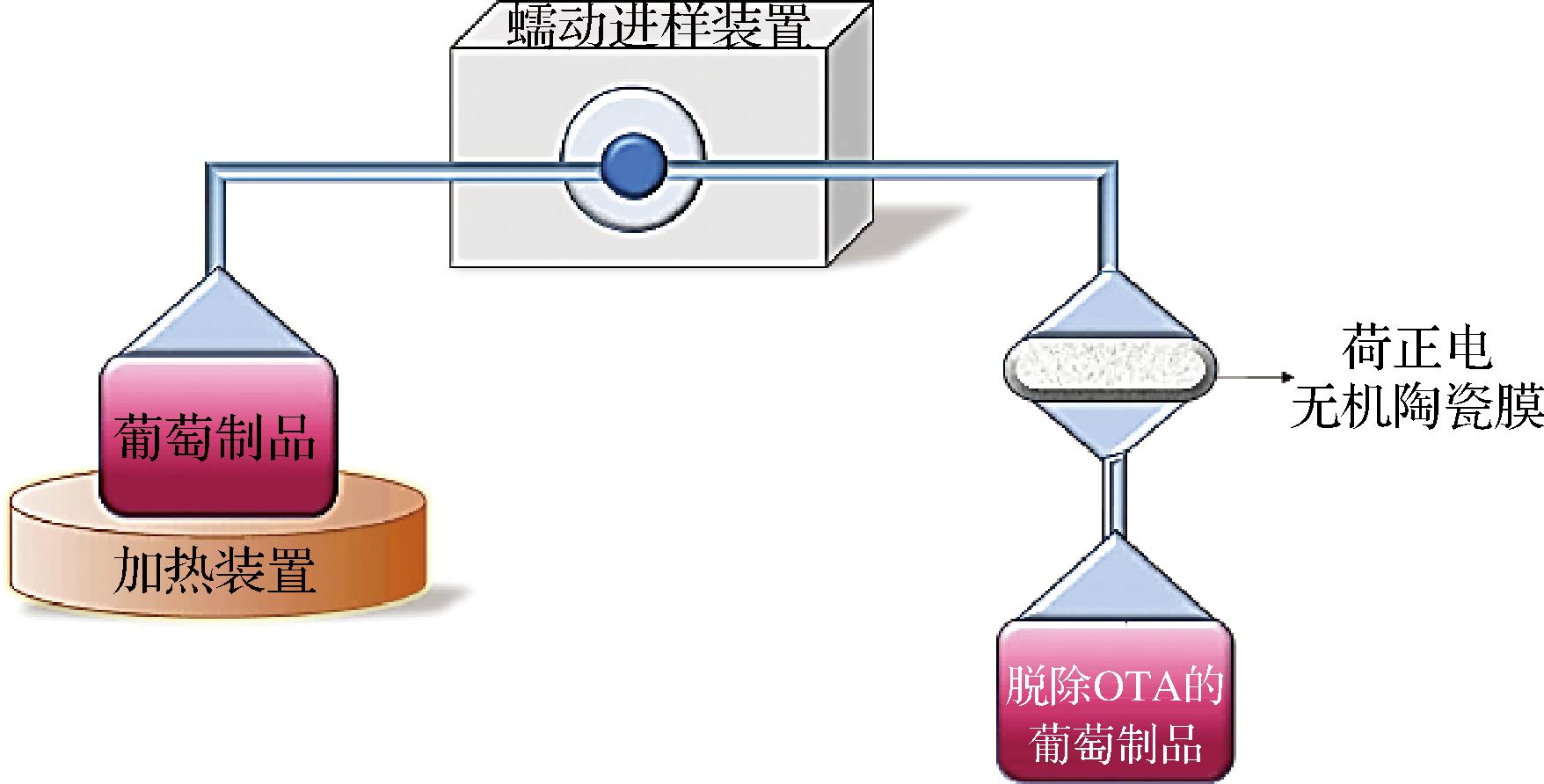
图1 OTA脱除装置示意图
Fig.1 Schematic of OTA removing device
1.3.4 OTA吸附条件筛选
分别改变试验中nano-MgO荷正电无机陶瓷膜质量,溶液pH值,温度,蠕动泵流速中的一个因素,固定其他因素。将25 mL 20 μg/L的OTA溶液通过脱除装置处理,收集滤液并测定其中OTA的含量。
nano-MgO荷正电无机陶瓷膜对OTA吸附率的计算如公式(1)所示[12]:
(1)
式中:R为吸附率;C0为OTA初始质量浓度,ng/mL;Ce为荷电膜处理后OTA溶液的质量浓度,ng/mL。
1.3.5 OTA的分离与测定
处理后的葡萄汁于40 ℃蒸发浓缩至2 mL左右,采用MFC229多功能固相净化柱对其中的OTA进行提取与分离,洗脱液浓缩吹干后用V(乙腈)∶V(水)=51∶49复溶并过滤,采用高效液相色谱-荧光进行分析。流动相同样采用V(乙腈)∶V(水)=51∶49;每次进样50 μL;流速设定为1 mL/min;柱温为35 ℃;荧光检测的激发与发射波长分别设定为333 nm与460 nm。
1.3.6 葡萄酒中OTA的脱除
空白基质(红葡萄汁、紫葡萄汁)中加入OTA标准溶液,配制最终质量浓度分别为10、15、20 μg/L的OTA混合样品,样品于最佳条件通过nano-MgO荷正电无机陶瓷膜,收集OTA吸附处理后的样品并测定OTA含量与品质变化。
1.3.7 葡萄酒的品质测定
还原糖采用3, 5-二硝基水杨酸法以蒸馏水为空白测定520 nm下的吸光度,根据标准曲线计算含量[13]。总酚采用Folin-Ciocalteu比色法测定波长760 nm下的吸光度[14]。采用旋转黏度计测定黏度[15]。采用手持阿贝折光仪法测定可溶性固形物含量。透光率以蒸馏水作为对照,测定波长为625 nm[16]。色值以蒸馏水为对照测定420 nm波长处的吸光度[17]。
品质变化率的计算如公式(2)所示[18]:
(2)
式中:QR为品质变化率;A0为OTA脱除前葡萄汁的品质结果;A1为OTA脱除后葡萄汁的品质结果。
1.3.8 葡萄汁的香气成分测定
移取8.00 mL葡萄汁于20.00 mL的顶空瓶中,加入2.56 g NaCl和内标物(20 μL 40 mg/L的2-辛醇)。葡萄汁在45 ℃下水浴平衡15 min,然后再用固相微萃取(solid-phase micro-extraction,SPME)头萃取40 min,采用气相色谱-质谱仪测定香气成分[19]。采用峰面积归一化法计算葡萄汁中不同种类香气成分的相对百分含量。
2 结果与分析
2.1 分散剂对nano-MgO荷正电无机陶瓷膜制备的影响
纳米材料表面的覆盖度直接受到涂膜液制备的影响,为了增加无机陶瓷膜表面的覆盖度,保证nano-MgO更好的修饰到陶瓷膜内部,可通过加入分散剂来提高涂膜液的稳定悬浮性和分散性[20]。图2对比了加入分散剂PEG前后制备的荷正电无机陶瓷表面nano-MgO的形态。未加入PEG时无机陶瓷膜表面nano-MgO的覆盖度低,无机陶瓷基膜大多裸露在外,易于涂膜液沉积的凹陷部位上纳米材料的修饰密度高,而其他部位修饰度则大大减少。PEG的加入显著提高了陶瓷膜表面纳米材料的覆盖度,可以明显观察到nano-MgO均匀分布在膜的表面与孔径内。由于无机陶瓷膜的荷电性能与nano-MgO的修饰量呈正相关,因此膜表面nano-MgO的修饰度越高,膜的荷电性能越佳;此外,nano-MgO作为OTA的主要结合位点,其固载量越大,吸附OTA的效果越好。由此可见,PEG的使用可有效提高无机陶瓷膜的修饰度,有助于提升荷电膜对OTA的吸附性能。

A-不使用PEG;B-使用PEG
图2 PEG使用前后nano-MgO荷正电无机陶瓷膜的表面形态
Fig.2 Surface morphology of nano-MgO positively charged inorganic ceramic membranes with or without PEG
2.2 nano-MgO荷正电无机陶瓷膜的性能表征
nano-MgO在无机陶瓷膜表面的负载量及分布情况直接影响膜的性能,采用扫描电子显微镜观察无机陶瓷膜修饰纳米材料前后的表面形态(图3),结果发现无机陶瓷膜的表面平滑且具有孔洞结构,表面与孔径内观察不到颗粒状的纳米nano-MgO附着物(图3-A)。而nano-MgO荷电膜可以观察到大量均匀分布的立方体颗粒(图3-B),意味着nano-MgO荷电涂层修饰在了基膜表面和微孔上。由于nano-MgO具有纳米结构使得膜的比表面积显著增加,膜的吸附能力也因此大大提升。采用透射电子显微镜观察表征nano-MgO的晶体形状和大小(图3-C),发现nano-MgO为大小较为均匀的立方体,平均粒径约100 nm。nano-MgO无机陶瓷膜的荷电性能通过Zeta电位进行表征(图4)。结果表明无机陶瓷基膜的Zeta电位值为负值,是电负性无机膜。而涂覆nano-MgO颗粒后,当pH<12.8时,荷电膜的Zeta电位均为正值,说
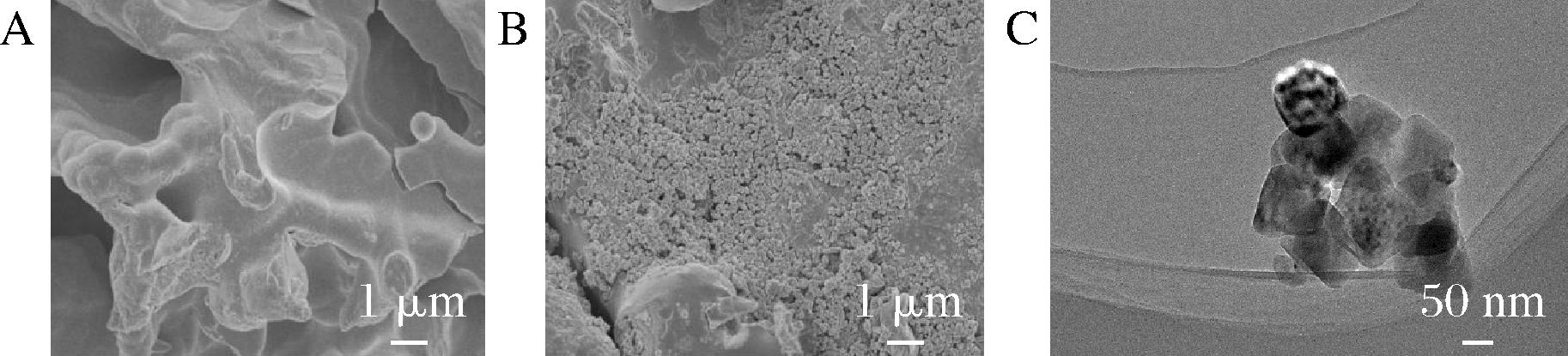
A-nano-MgO修饰前表面形态;B-nano-MgO修饰后表面形态; C-nano-MgO晶体形态
图3 nano-MgO修饰前后无机陶瓷膜的表面及晶体形态
Fig.3 Surface morphology and crystal morphology of inorganic ceramic membranes before and after nano-MgO modification
明pH<12.8的范围内nano-MgO表面具有正电荷结合位点,与溶液中的氢离子结合后带有正电,改变了无机陶瓷基膜的电负性,可通过静电作用吸附带负电的物质。
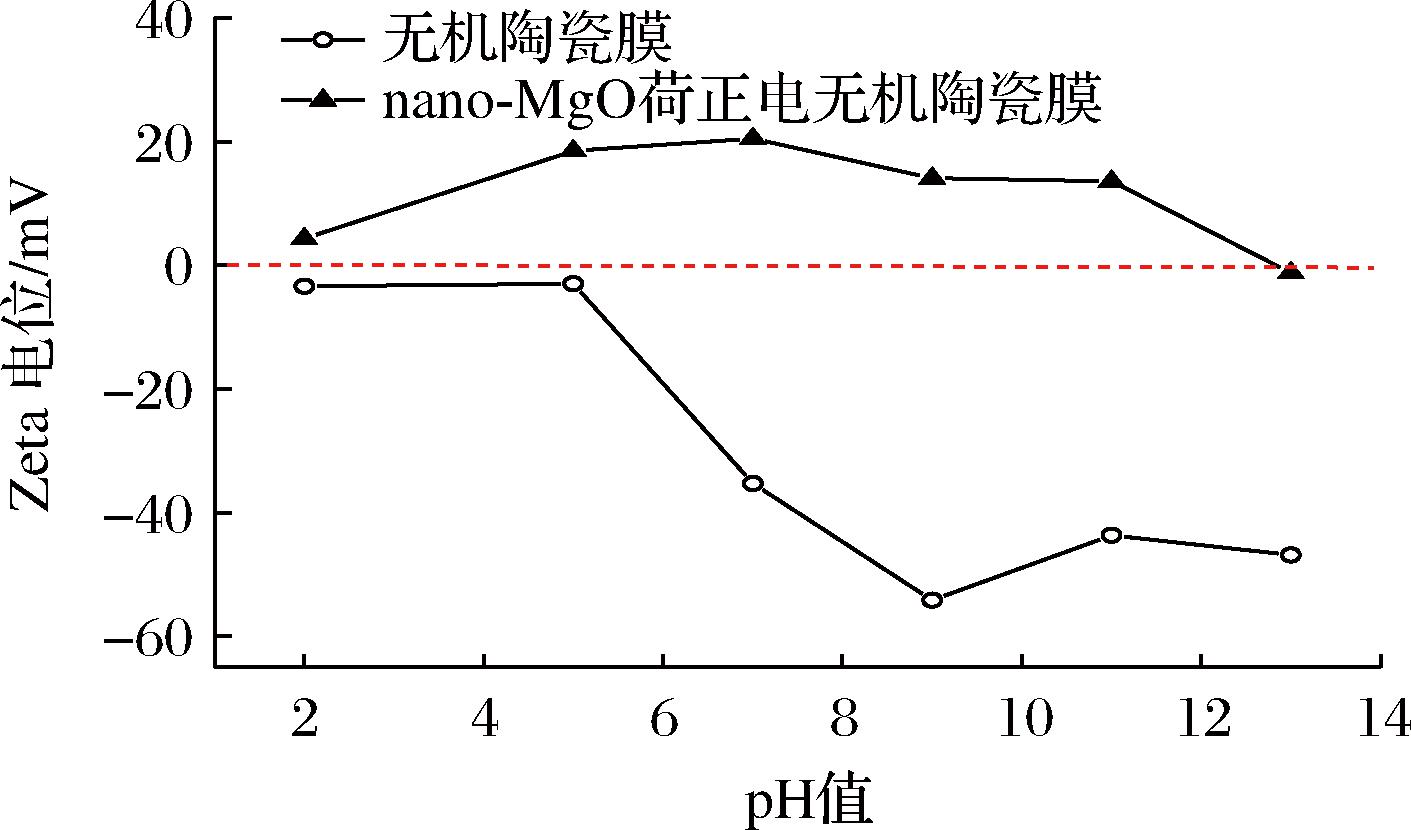
图4 nano-MgO修饰前后无机陶瓷膜的Zeta电位
Fig.4 Zeta potential of inorganic ceramic membranes before and after nano-MgO modification
2.3 OTA脱除条件的筛选
流速会改变OTA分子与荷正电膜的相互作用时间,从而对膜表面的吸附量产生了影响。图5-A为蠕动泵脱除OTA时不同流速对于吸附率影响。当OTA溶液流速为47~470 μL/min时,吸附率随流速的增大而显著降低。流速为47 μL/min和141 μL/min时,OTA吸附率分别达到80%与79%,均能达到良好的脱除效果。但是,流速为47 μL/min时所需的脱除时间(12 h)为141 μL/min(3.5 h)的3.4倍。基于实验结果,选择蠕动泵141 μL/min为最佳流速进行试验。
pH不仅直接决定了OTA在溶液中的存在状态,而且影响了nano-MgO无机陶瓷膜表面的荷正电能力。针对不同pH条件的OTA溶液进行脱除试验,结果如图5-B所示。当溶液pH值由2增加至5时,吸附率随pH的增加而增大;pH值为5和9时,吸附率分别为75.4%和76.5%,没有显著性差异;之后吸附率显著增加至84.3%(pH=11)。虽然当pH=11时脱除效果最佳,但考虑到葡萄汁与葡萄酒多呈弱酸性,因此按照实际样品需求,本实验酸度条件选择为pH=5。
涂膜液对膜内部的涂覆效果与无机陶瓷基膜的质量密切相关,且直接影响膜的荷电性能。采用相同直径、不同质量的基膜制备nano-MgO荷正电无机陶瓷膜,并测试其吸附性能(图5-C)。当基膜质量为0.5~2.0 g时,吸附率随膜质量的增加而显著增大。质量较大的基膜其表面积也较大,可以提供的nano-MgO修饰位点相应也较多,荷正电吸附位点的增加导致OTA的吸附率随之增大。因此,制备荷电膜时确定无机陶瓷基膜的质量为2 g。
无论物理吸附还是化学吸附都会涉及吸热与放热过程,因此温度是研究吸附效果必须考虑的影响因素之一。鉴于此,在25~45 ℃的温度范围内进行OTA的脱除,以此筛选最佳吸附温度。如图5-D所示,OTA的吸附率随温度的升高而降低,且温度从35 ℃升高到45 ℃时,吸附率下降尤其显著。说明nano-MgO

A-溶液流速;B-初始pH值;C-基膜质量;D-吸附温度
图5 溶液流速、初始pH值、基膜质量和吸附温度对OTA吸附率的影响
Fig.5 Effects of flow rates, initial pH, dosage of nano-MgO positively charged inorganic ceramic membranes, and adsorption temperature on the adsorption rate of OTA
注:不同小写字母表示差异显著(P<0.05)(下同)。
无机陶瓷膜对OTA的吸附适宜在低温进行,OTA与荷电膜的相互作用符合放热过程。由于高温不利于OTA吸附,故后续实验选择在25 ℃,即室温条件下进行。
2.4 nano-MgO荷正电无机陶瓷膜对葡萄汁中OTA的脱除
我国及欧盟规定葡萄汁中OTA最大限量标准为2 μg/kg。以此为依据,将试验中OTA在红葡萄汁及紫葡萄中的质量浓度确定为10、15、20 μg/L。将OTA污染的葡萄汁样品通过脱除装置并测定处理后OTA浓度,结果见表1。处理后的葡萄汁中OTA含量明显下降(0.44~1.68 μg/L),均低于2 μg/kg,吸附率达到91.57%~96.67%。由此说明当葡萄汁中OTA质量浓度小于20 μg/L时,以nano-MgO荷正电无机陶瓷膜为主要核心部件的OTA脱除装置可有效对葡萄汁中的OTA进行吸附脱除。有研究采用改性活性炭吸附处理葡萄酒中的OTA,吸附率仅为![]() 等[22]对沸石进行改性后用于OTA的去除,虽然吸附率达到了90%,但是没有评价该吸附剂对样品营养品质的影响。由此说明nano-MgO荷正电无机陶瓷膜对OTA的脱除效果良好,并可用于葡萄汁等实际样品中OTA的脱除。
等[22]对沸石进行改性后用于OTA的去除,虽然吸附率达到了90%,但是没有评价该吸附剂对样品营养品质的影响。由此说明nano-MgO荷正电无机陶瓷膜对OTA的脱除效果良好,并可用于葡萄汁等实际样品中OTA的脱除。
表1 nano-MgO荷正电无机陶瓷膜对葡萄汁中OTA的吸附
Table 1 Adsorption of OTA in grape juice by nano-MgO positively charged inorganic ceramic membranes
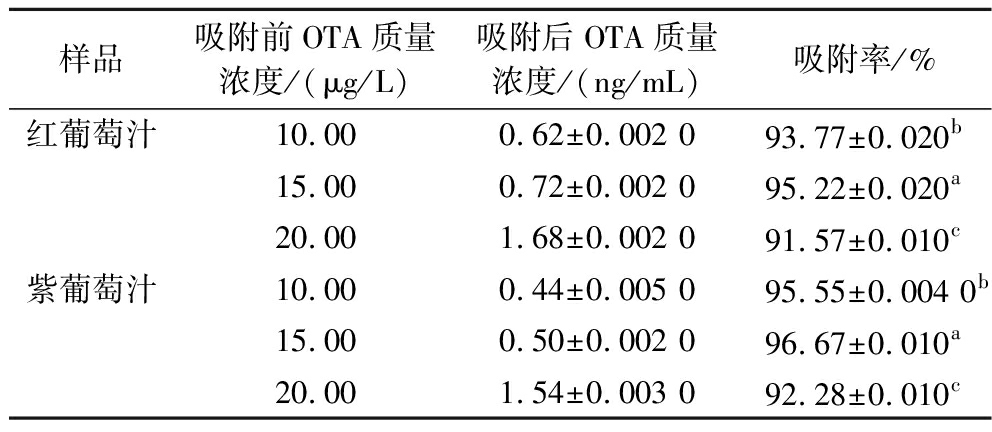
样品吸附前OTA质量浓度/(μg/L)吸附后OTA质量浓度/(ng/mL)吸附率/%红葡萄汁10.000.62±0.002 093.77±0.020b15.000.72±0.002 095.22±0.020a20.001.68±0.002 091.57±0.010c紫葡萄汁10.000.44±0.005 095.55±0.004 0b15.000.50±0.002 096.67±0.010a20.001.54±0.003 092.28±0.010c
注:不同字母表示差异显著(P<0.05)(下同)。
2.5 nano-MgO荷正电无机陶瓷膜对葡萄汁品质的影响
通过物理截留来消除真菌毒素往往伴随着食品的营养品质的损失。为了评价nano-MgO荷正电无机陶瓷吸附OTA前后葡萄汁品质的变化,系统测定了样品中还原糖、总酚、可溶性固形物和色值等品质指标。OTA脱除前后葡萄汁品质见表2。红葡萄汁中的还原糖在荷电膜处理后略有降低,而紫葡萄汁还原糖含量几乎未受影响。2种葡萄汁中总酚含量处理后均有一定程度的增加,这或许与膜处理时水分的损失有关。虽然红葡萄果汁中的可溶性固形物的含量处理前后无显著性变化,但是紫葡萄果汁降低了14.6%。可溶性固形物与黏度的变化趋势一致,如可溶性固形物含量降低,黏度值同样降低。另一方面,黏度多与糖类物质的含量相关,糖的增多不利于保持果胶分子间结构,果汁黏度也会随之增加[23]。因此,随着可溶性固形物与还原糖变化,葡萄汁的黏度也随之改变。处理后紫葡萄汁的透光率增加了35.18%,而红葡萄汁的变化小于紫葡萄汁。紫葡萄汁颜色较深,处理前后色值虽然无显著性差异,但其数值增加了16.24%,变化相对红葡萄汁(4.84%)也较大,变的更加澄清,这可能与膜本身对大分子化合物(如多糖等)的物理截留有关。
2.6 nano-MgO荷正电无机陶瓷膜对葡萄汁香气的影响
葡萄汁具有不同于其他果汁的特殊的香气,对nano-MgO荷正电无机陶瓷膜处理前后葡萄汁的香气变化进行评价,可以进一步评价荷电膜的实用性。如表3所示,nano-MgO荷正电无机陶瓷膜处理对红葡萄汁和紫葡萄汁中香气化合物的种类没有产生影响,香气物质种类分别为36和39种,其中醇类、醛类和酯类化合物所占比例比较高。虽然处理前后香气物质的种类数量没有发生变化,然而香气物质的相对含量发生了变化(图6)。紫葡萄汁中除酸类外其他化合物相对含量均发生了降低,酯类与醇类分别降低了2.2%与1.3%,其他化合物相对含量的变化更小。紫葡萄汁风味化合物的整体水平仅有小幅降低,整体风味得以保持,说明荷电膜对紫葡萄汁香气成分的影响较小。而红葡萄汁中酯类相对含量明显下降(58.6%),醇类则增加了近一倍,其他化合物相对含量的改变相比酯类与醇类较小。葡萄汁的果香味主要来源之一为酯类物质,但是酯类化合物长时间接触氧气会加速其水解,使得酯类物质含量降低[24]。虽然酯类香气成分有一定的损失,但是其他成分相对含量的增加有助于弥补整体风味。
表2 nano-MgO荷正电无机陶瓷膜吸附处理前后葡萄汁的品质变化
Table 2 Nutrient changes of grape juice before and after adsorption treatment with nano-MgO positively charged inorganic ceramic membranes

还原糖/%总酚/(mg/mL)可溶性固形物/%黏度/(mPa·s)透光率/%色值红葡萄汁脱除前3.74±0.002a15.32±0.08b14.47±0.31a1.76±0.02b83.13±0.40a0.62±0.001a红葡萄汁脱除后3.60±0.00b17.11±0.08a14.67±0.31a1.82±0.02a81.00±0.79b0.59±0.001bQR/%3.74-11.68-1.38-3.412.564.84紫葡萄汁脱除前3.77±0.006a47.18±0.04b13.97±0.11a1.75±0.01a5.60±0.20b2.34±0.001a紫葡萄汁脱除后3.72±0.001a59.27±0.02a11.93±0.11b1.50±0.01b7.57±0.51a2.72±0.21aQR/%1.33-25.6414.6014.29-35.18-16.24
表3 nano-MgO荷正电无机陶瓷膜吸附处理前后 葡萄汁的香气物质数量的变化 单位:种
Table 3 Changes of aroma substances before and after adsorption treatment with nano-MgO positively charged inorganic ceramic membranes
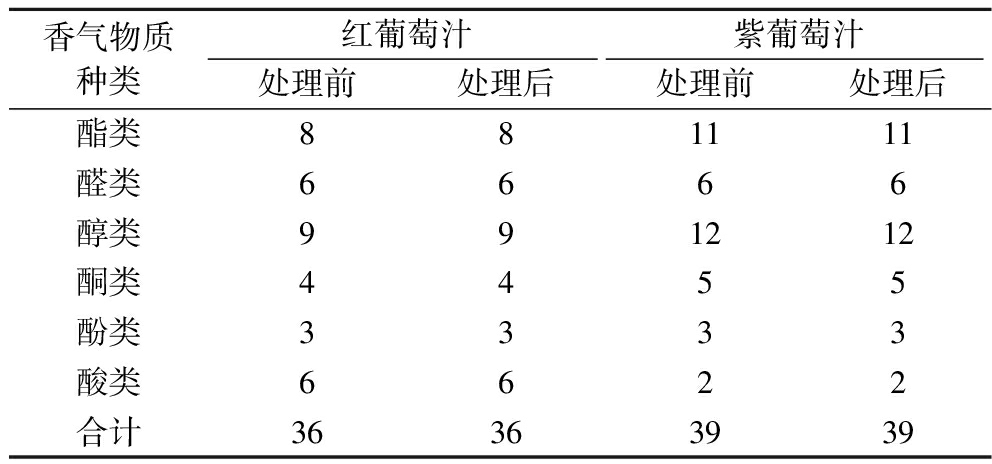
香气物质种类红葡萄汁紫葡萄汁处理前处理后处理前处理后酯类881111醛类6666醇类991212酮类4455酚类3333酸类6622合计36363939
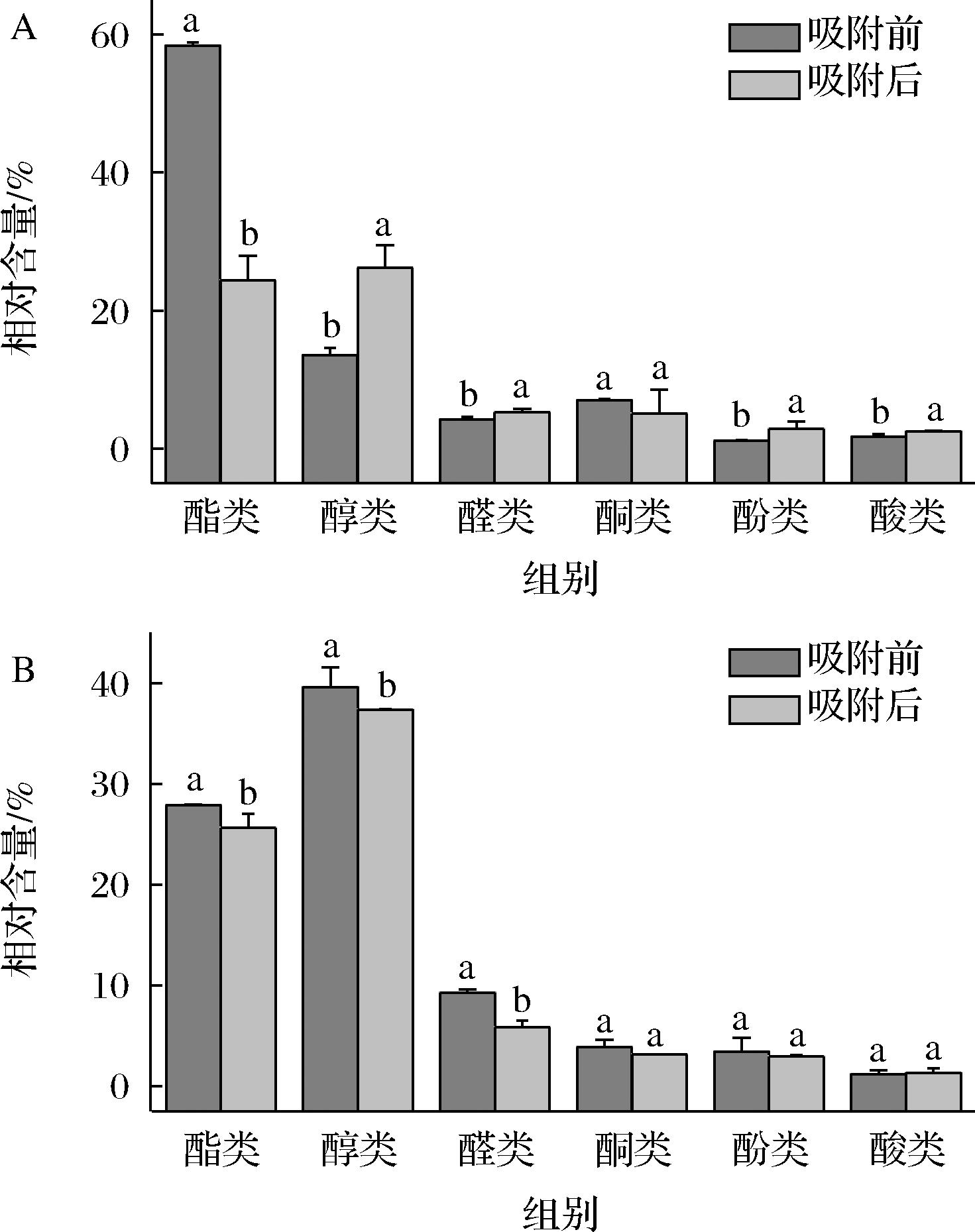
A-红葡萄汁;B-紫葡萄汁
图6 nano-MgO荷正电无机陶瓷膜对红葡萄汁和紫葡萄汁 香气成分相对含量的影响
Fig.6 Effect of nano-MgO positively charged inorganic diatomite ceramic membranes on relative contents of aroma substances of red grape juice and purple grape juice
3 结论
本文采用浸渍-热分解法制备了nano-MgO荷正电无机陶瓷膜,并对材料的表面荷电与晶体形态等进行表征,考察了该材料对葡萄汁中OTA的吸附能力及对其品质的影响。结果表明nano-MgO呈立方体结构并较好的附着在陶瓷膜的表面与孔径内,分散剂的使用可有效提高荷正电膜表面纳米材料的修饰密度与比表面积。当蠕动泵流速为141 μL/min,无机陶瓷基膜质量为2.0 g,溶液温度为25 ℃,溶液pH=5时OTA的脱除效果最佳。该材料对葡萄汁中OTA的脱除率高于91.57%,且葡萄汁中总酚、还原糖、色值和风味物质等整体品质得以保留。nano-MgO荷正电无机陶瓷膜提供了一种可以静电吸附葡萄汁中OTA的新方法,通过改变荷电纳米材料的种类与性质,该材料可推广至其他真菌毒素与农残的去除。
[1] NAN M N, XUE H L, BI Y.Contamination, detection and control of mycotoxins in fruits and vegetables[J].Toxins, 2022, 14(5):309.
[2] ERCEG S, MATEO E, ZIPANCIC I, et al.Assessment of toxic effects of ochratoxin A in human embryonic stem cells[J].Toxins, 2019, 11(4):217.
[3] HASHEMI J, ALIZADEH N.Investigation of solvent effect and cyclodextrins on fluorescence properties of ochratoxin A[J].Spectrochimica Acta Part A:Molecular and Biomolecular Spectroscopy, 2009, 73(1):121-126.
[4] DAHAL S, LEE H J, GU K J, et al.Heat stability of ochratoxin A in an aqueous buffered model system[J].Journal of Food Protection, 2016, 79(10):1748-1752.
[5] SAADULLAH A A M, A BDULLAH S K A.Fungal contamination of dried vine fruits and ochratoxin a detection in grape juice from Duhok, Iraq[J].Revista Innovaciencia, 2018, 6(2):1-8.
[6] WEI D M, WU X H, XU J, et al.Determination of ochratoxin A contamination in grapes, processed grape products and animal-derived products using ultra-performance liquid chromatography-tandem mass spectroscopy system[J].Scientific Reports, 2018, 8(1):2051.
[7] JAMAL Y, MEHRAN V, FIROUZEH N, et al.Occurrence of ochratoxin a in grape juice of Iran[J].Iranian Journal of Pharmaceutical Research, 2018, 17(1):140-146.
[8] CARO J, NOACK M, KÖLSCH P, et al.Zeolite membranes-state of their development and perspective[J].Microporous and Mesoporous Materials, 2000, 38(1):3-24.
[9] CHENG X T, LI N, ZHU M F, et al.Positively charged microporous ceramic membrane for the removal of titan yellow through electrostatic adsorption[J].Journal of Environmental Sciences, 2016, 44(6):204-212. [10] KATTAMURI N, SHIN J H, KANG B, et al.Development and surface characterization of positively charged filters[J].Journal of Materials Science, 2005, 40(17):4531-4539.
[11] ZHANG L L, LI N, ZHU M F, et al.Nano-structured surface modification of micro-porous ceramic membrane with positively charged nano-Y2O3 coating for organic dyes removal[J].RSC Advances, 2015, 5(98):80643-80649.
[12] NAN M N, BI Y, QIANG Y, et al.Electrostatic adsorption and removal mechanism of ochratoxin A in wine via a positively charged nano-MgO microporous ceramic membrane[J].Food Chemistry, 2022, 371:131157.
[13] 王俊丽, 聂国兴, 李素贞, 等.DNS法测定还原糖含量时最适波长的确定[J].河南农业科学, 2010,39(4):115-118. WANG J L, NIE G X, LI S Z, et al.Optimal wavelength for determining the content of reducing sugar by DNS method[J].Journal of Henan Agricultural Sciences, 2010,39(4):115-118.
[14] SHAN T J, SUN W, B WANG X H, et al.Purification of ustiloxins a and B from rice false smut balls by macroporous resins[J].Molecules, 2013, 18(7):8181-8199.
[15] 冯文英, 张继伟, 张博, 等.旋转黏度计法测定4种农药悬浮剂的黏度[J].现代农药, 2015,14(4):16-17;22. FENG W Y, ZHANG J W, ZHANG B, et al.Determination of the viscosity of four pesticides SC by rotational viscometer[J].Modern Agrochemicals, 2015,14(4):16-17;22.
[16] 聂继云, 毋永龙, 李海飞, 等.苹果鲜榨汁品质评价体系构建[J].中国农业科学, 2013, 46(8):1657-1667. NIE J Y, WU Y L, LI H F, et al.Evaluation system established for fresh apple juice quality[J].Scientia Agricultura Sinica, 2013, 46(8):1657-1667.
[17] COSME F, CAP O I, FILIPE-RIBEIRO L, et al.Evaluating potential alternatives to potassium caseinate for white wine fining:Effects on physicochemical and sensory characteristics[J].LWT-Food Science and Technology, 2012, 46(2):382-387.
O I, FILIPE-RIBEIRO L, et al.Evaluating potential alternatives to potassium caseinate for white wine fining:Effects on physicochemical and sensory characteristics[J].LWT-Food Science and Technology, 2012, 46(2):382-387.
[18] 李小红, 曾民鑫, 周良春.单功能化壳聚糖对刺梨果汁单宁及色素吸附的研究[J].食品科技, 2018,43(8):176-183. LI X H, ZENG M X, ZHOU L C.Decolorization and tannin removal efficiency of Rosa roxburghii Tratt juice with monofunctional chitosan[J].Food Science and Technology, 2018,43(8):176-183.
[19] 鲁榕榕, 马腾臻, 张波, 等.不同澄清剂对起泡葡萄酒原酒的澄清作用及对香气品质的影响[J].食品科学, 2018, 39(12):146-153. LU R R, MA T Z, ZHANG B, et al.Effect of different clarifying agents on clarification and aroma quality of sparkling base wine[J].Food Science, 2018, 39(12):146-153.
[20] 张爱娟, 李健生, 孙秀云, 等.陶瓷微滤膜涂膜液的分散性能研究[J].水处理技术, 2003, 29(4):200-202. ZHANG A J,LI J S,SUN X Y, et al.Dispersion behavior of membrane suspensions for ceramic microfiltration membranes[J].Technology of Water Treatment, 2003, 29(4):200-202.
[21] ![]() M, DEL PRETE V, GARCIA-MORUNO E, et al.The development of an activated carbon from cherry stones and its use in the removal of ochratoxin A from red wine[J].Food Control, 2009, 20(3):298-303.
M, DEL PRETE V, GARCIA-MORUNO E, et al.The development of an activated carbon from cherry stones and its use in the removal of ochratoxin A from red wine[J].Food Control, 2009, 20(3):298-303.
[22] ![]() A, ROTTINGHAUS G, et al.Surfactant modified zeolites-new efficient adsorbents for mycotoxins[J].Microporous and Mesoporous Materials, 2003, 61(1-3):173-180.
A, ROTTINGHAUS G, et al.Surfactant modified zeolites-new efficient adsorbents for mycotoxins[J].Microporous and Mesoporous Materials, 2003, 61(1-3):173-180.
[23] 侯燕杰, 郭玉蓉, 牛鹏飞.仙人掌果果汁的流变学特性[J].食品与发酵工业, 2018, 44(12):92-96. HOU Y J,GUO Y R,NIU P F.Rheological properties of cactus fruit juice[J].Food and Fermentation Industries, 2018, 44(12):92-96.
[24] 何义国, 赵兴秀, 邓静, 等.白酒中酯类化合物的稳定性研究[J].酿酒科技, 2012(12):34-36. HE Y G, ZHAO X X, DENG J, et al.Study on the stability of ester compounds in liquor[J].Liquor-Making Science &Technology, 2012(12):34-36.