八月瓜(Akebia trifoliata)是木通科木通属半落叶木质藤本植物三叶木通的果实[1],我国的八月瓜资源丰富,广泛分布在陕西、河北、湖南、四川、云南等省份以及长江流域[2]。八月瓜果实中的维生素C、糖、蛋白质含量均高于大众平时摄取的普通水果,且氨基酸种类较多,富含多种必需氨基酸和为果肉呈现香味的鲜味氨基酸,所占鲜果含量分别为298.4、274.1 mg/100g[3]。八月瓜果皮也具有丰富的营养物质,经检测发现,其矿物质元素含量普遍高于梨、苹果等[4]。研究表明八月瓜籽油中含有30.10%脂肪油,其中多数为不饱和脂肪酸,以单不饱和脂肪酸、油酸和多不饱和脂肪酸亚油酸为主,含量分别占47.63%和27.05%[5],谷氨酸与天冬氨酸含量分别为7.783 4%和4.621 9%[6],并且八月瓜籽油中氨基酸成分含量与联合国粮食及农业组织/联合国世界卫生组织推荐的成人氨基酸模式相似,具有将其作为保健油开发成品的巨大潜力。
纳米乳液是将水、油、表面活性剂与助表面活性剂按一定比例混合,通过一系列手段制成的粒径在50~200 nm的乳液体系,纳米乳液的水相主要由乳化剂和助乳化剂组成[7],油相常采用具有特殊活性的油或是溶解了亲脂性活性物质的油溶液。纳米乳分为3种类型,分别为水包油型 (oil in water,O/W)、油包水型 (water in oil,W/O)以及双连续型。纳米乳液的制备方法一般分为高能乳化法与低能乳化法。常用的高能乳化法有高压均质、超声波乳化、高压微射流化法[8]与膜乳化法[9];低能乳化法与界面动力学联系紧密,在实际中多用来制备O/W型乳液。主要分为自发乳化法、溶剂蒸发法[10]、水凝胶法、反相法[11]等。本研究对八月瓜籽油纳米乳液的制备工艺进行探究,为八月瓜籽油产品开发提供理论参考依据。
1 材料与方法
1.1 材料与试剂
八月瓜籽油,购于湖南省古丈县;吐温-80(食品级),广东润华化工有限公司;丙二醇,天津市科密欧化学试剂有限公司;乙醇,湖南汇虹试剂有限公司;亚甲基蓝,天津市北辰方正试剂厂;苏丹红Ⅲ,上海麦克林生化科技有限公司;ABTS,合肥博美生物有限公司;过硫酸钾,国药集团化学试剂有限公司;试剂均为分析纯。
1.2 仪器与设备
HJS-3A恒温磁力搅拌水浴锅,常州澳华仪器有限公司;722 N紫外可见分光光度计,上海仪电分析仪器有限公司;JE602电子天平,上海浦春计量仪器有限公司;DHG-9140A电热鼓风干燥箱(电热鼓风干燥箱);D-6L高压均质机,美国PhD科技有限公司;Zetasizer Nano ZS纳米粒度与电位分析仪,英国马尔文仪器有限公司;ZOOMAC-L超纯水仪,湖南中沃水务环保科技有限公司;5810R高速离心机,德国艾本德股份公司;FA25D高剪切乳化机,上海弗鲁克公司;SpectraMax iD3多功能酶标仪,美国分子仪器公司。
1.3 实验方法
1.3.1 八月瓜籽油纳米乳液配方和工艺优化
以吐温-80为乳化剂,以溶解度大且无毒的无水乙醇、丙二醇为助乳化剂。分别向2个烧杯中加入4 g八月瓜籽油、0.8 g吐温-80与0.4 g助乳化剂,在37 ℃水浴条件下,以450 r/min的转速下均匀搅拌15 min,加入34.8 g超纯水后继续搅拌30 min形成粗乳液。将得到的粗乳液利用高速剪切机以10 000 r/min的速度剪切2 min,在25 ℃、100 MPa的条件下均质5次,得到粒径较为均一的八月瓜籽油纳米乳液,用超纯水稀释200倍后以纳米粒度和Zeta电位与粒径分布和多分散系数(polydispersity index,PDI)指数为参考指标来确定最佳助乳化剂。
确定最佳助乳化剂后,以纳米粒度和Zeta电位与粒径分布和PDI指数为指标,考察均质压力、均质次数、八月瓜籽油质量分数、乳化剂与助乳化剂比例、复合乳化剂质量分数对八月瓜籽油纳米乳液的影响,方案为:均质压力为70、100、130 MPa,均质次数为1、3、5、7、9,八月瓜籽油质量分数为6%、8%、10%、12%、14%,乳化剂与助乳化剂质量比为3∶1、2∶1、1∶1、1∶2、1∶3,复合乳化剂质量分数为1%、2%、3%、4%、5%,以制备得到的八月瓜籽油纳米乳液用超纯水稀释200倍后的纳米粒度和Zeta电位与PDI指数为指标,确定八月瓜籽油纳米乳液的最佳配方和工艺。
1.3.2 八月瓜籽油纳米乳液质量评价
1.3.2.1 基本评价
将制得的八月瓜籽油纳米乳液稀释200、1 000倍,观察是否有淡蓝色乳光,采用平行光照射后是否产生丁达尔效应,出现一条光亮的通路。将油溶性苏丹红Ⅲ染液与水溶性亚甲基蓝染液分别同时加入制得的八月瓜籽油纳米乳液中,观察2种颜色染料扩散速度的快慢,若亚甲基蓝扩散速度快于苏丹红Ⅲ,则证明乳液为O/W型,若苏丹红Ⅲ扩散速度快于亚甲基蓝,则证明乳液为W/O型,若两者扩散速度一样,则为双连续型[12]。
1.3.2.2 粒径与Zeta电位测定
将八月瓜籽油纳米乳液用超纯水稀释200倍,避免高浓度乳液引起多重散射现象,用Zetasizer Nano-ZS90纳米粒度和Zeta电位分析仪测定乳液微粒粒径、Zeta电位、PDI指数和粒度分布,重复测定3次。
1.3.3 八月瓜籽油纳米乳液稳定性评价
1.3.3.1 贮藏期稳定性
在QIN等[13]方法的基础上稍微修改,将八月瓜籽油纳米乳液分别放置在4、25、60 ℃条件下贮藏,分别于5、10、15、20、25 d测定粒径与PDI,测定方法同1.3.2.2。
1.3.3.2 稀释稳定性
将八月瓜籽油纳米乳液用超纯水稀释到50、200、1 000倍,观察是否分层,若未分层,则证明八月瓜籽油纳米乳液具有良好的稀释稳定性[14]。
1.3.3.3 离心稳定性
在XU等[15]方法的基础上稍微修改,将八月瓜籽油纳米乳液用超纯水稀释200倍,测定其下层液体在500 nm处的吸光度,在2 000×g下离心20 min,吸取离心后下层液体测定其在500 nm处吸光度,重复3次。按照公式(1)计算表征离心稳定性的Ke值。Ke值越小,证明分散的油滴在离心力的作用下上浮或下沉的越少,可判断纳米乳液的物理稳定性。
(1)
1.3.3.4 吸光比测定
在KAUFMAN等[16]方法的基础上稍微修改,室温下将八月瓜籽油纳米乳液用超纯水稀释1 000倍,分别测定其在80、400 nm处的吸光度,用公式(2)计算出的吸光比(specific absorptivity,SRI)判定乳液的稳定性,当吸光比<0.3时纳米乳液较稳定。
(2)
1.3.4 八月瓜籽油纳米乳液对ABTS阳离子自由基的清除能力
参考RE等[17]方法并稍作修改,采用ABTS法对八月瓜籽油、制得的纳米乳液以及不同温度下贮藏25 d的纳米乳液进行测定,准确配制7 mmol/L ABTS水溶液与4.9 mmol/L过硫酸钾水溶液,按体积比为1∶1混合均匀。将混合液置于室温黑暗条件下反应12~16 h,得到ABTS原液。在测定开始前将ABTS原液用无水乙醇稀释至溶液在734 nm处吸光度为0.7。准确称取1 g八月瓜籽油于离心管中,再加入9 g无水乙醇,使用漩涡混合器将其混合均匀,静置30 min后进行测定。将10 μL样品溶液加入96孔板中,再加入190 μL稀释后的ABTS溶液,室温反应30 min后使用酶标仪在734 nm处测定其吸光度,以无水乙醇为空白对照,ABTS阳离子自由基清除能力用每克干样品中Trolox当量表示,单位为μmol Trolox/g。
1.4 数据分析
所有实验重复3次,结果为3次的平均值,采用Origin实验图形的绘制,利用SPSS 20软件进行统计分析。P<0.05则认为有显著性差异。
2 结果与分析
2.1 八月瓜籽油纳米乳液配方和工艺优化
2.1.1 助乳化剂的确定
助乳化剂是一种两亲分子,由于极性头较小,不能稳定乳液本身,但是它可以与乳化剂产生协同作用,有助于纳米乳液的形成,还能够进一步降低界面张力,同时增加了系统的熵。助乳化剂插入乳化剂分子之间,削弱了极性头和非极性尾部的相互作用,生成了一种更灵活的界面膜,能够在液滴周围轻易地变形,醇类在两相之间作用,改善了油相和水相的溶解度[18]。由图1分析发现,当丙二醇作为乳化剂时,乳液微粒粒径与PDI指数更小。丙二醇作为良好的溶剂,可以影响表面活性剂的亲水亲油平衡值,提高纳米乳液体系的稳定性,并且八月瓜籽油在丙二醇中有良好的的溶解性。因此,在后续实验中选择丙二醇作为助乳化剂进行下一步实验。
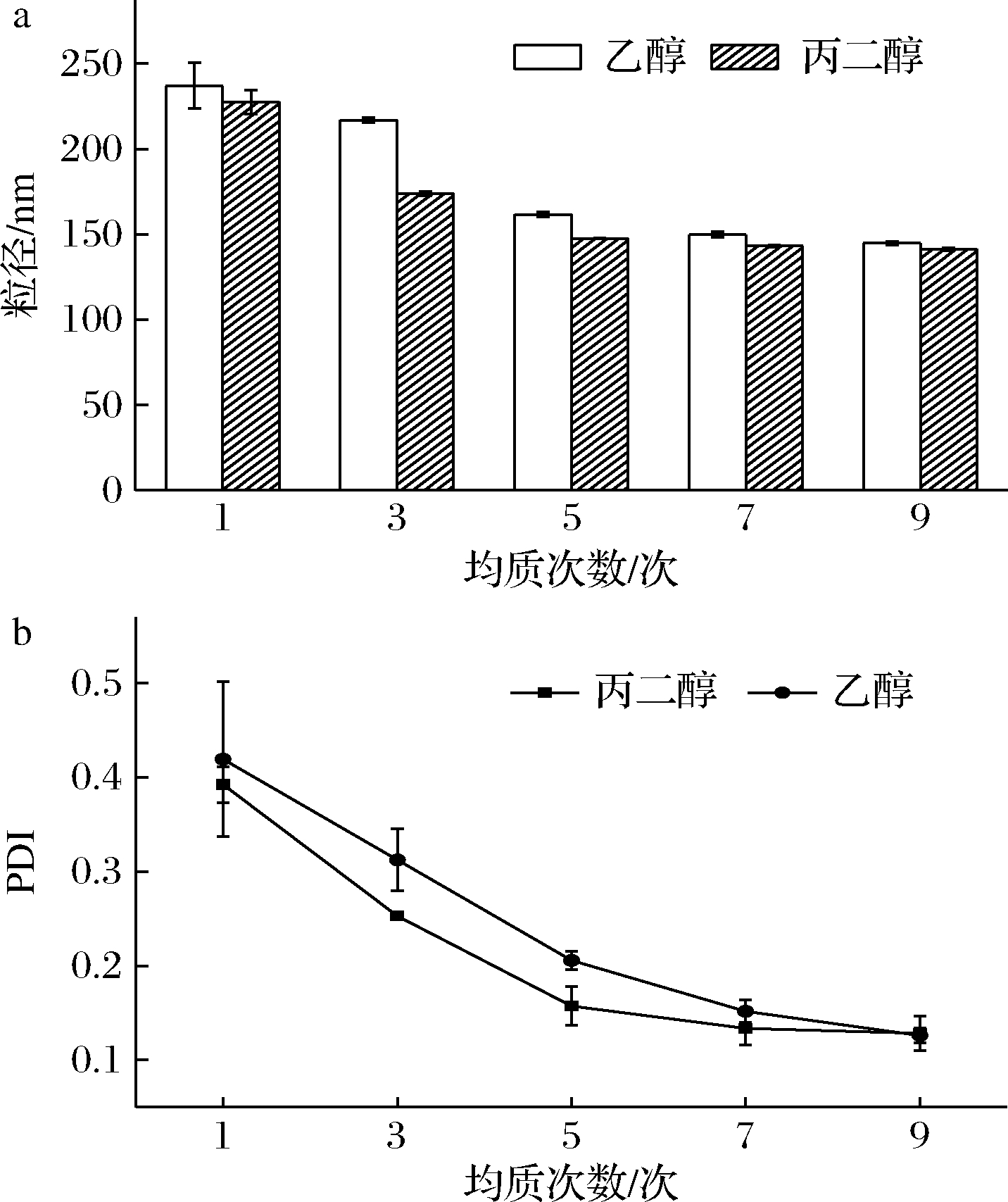
a-粒径;b-PDI
图1 助乳化剂对八月瓜籽油纳米乳液粒径与PDI的影响
Fig.1 Effect of cosurfactant on Akebia trifoliata seed oil nanoemulsion particle size and PDI
2.1.2 均质次数对粒径与PDI的影响
图2为均质次数对八月瓜籽油纳米乳液粒径与PDI的影响,随着均质次数增加到5次后,大部分乳液粒径在140~150 nm,并且PDI也随着均质次数的增加而降低,乳液粒径减小且趋于稳定[19]。均质次数过多会造成工艺繁复,多次均质产生的机械热可能会使乳液温度升高,破坏纳米乳液体系,降低稳定性。综合考虑,均质次数选择5次。
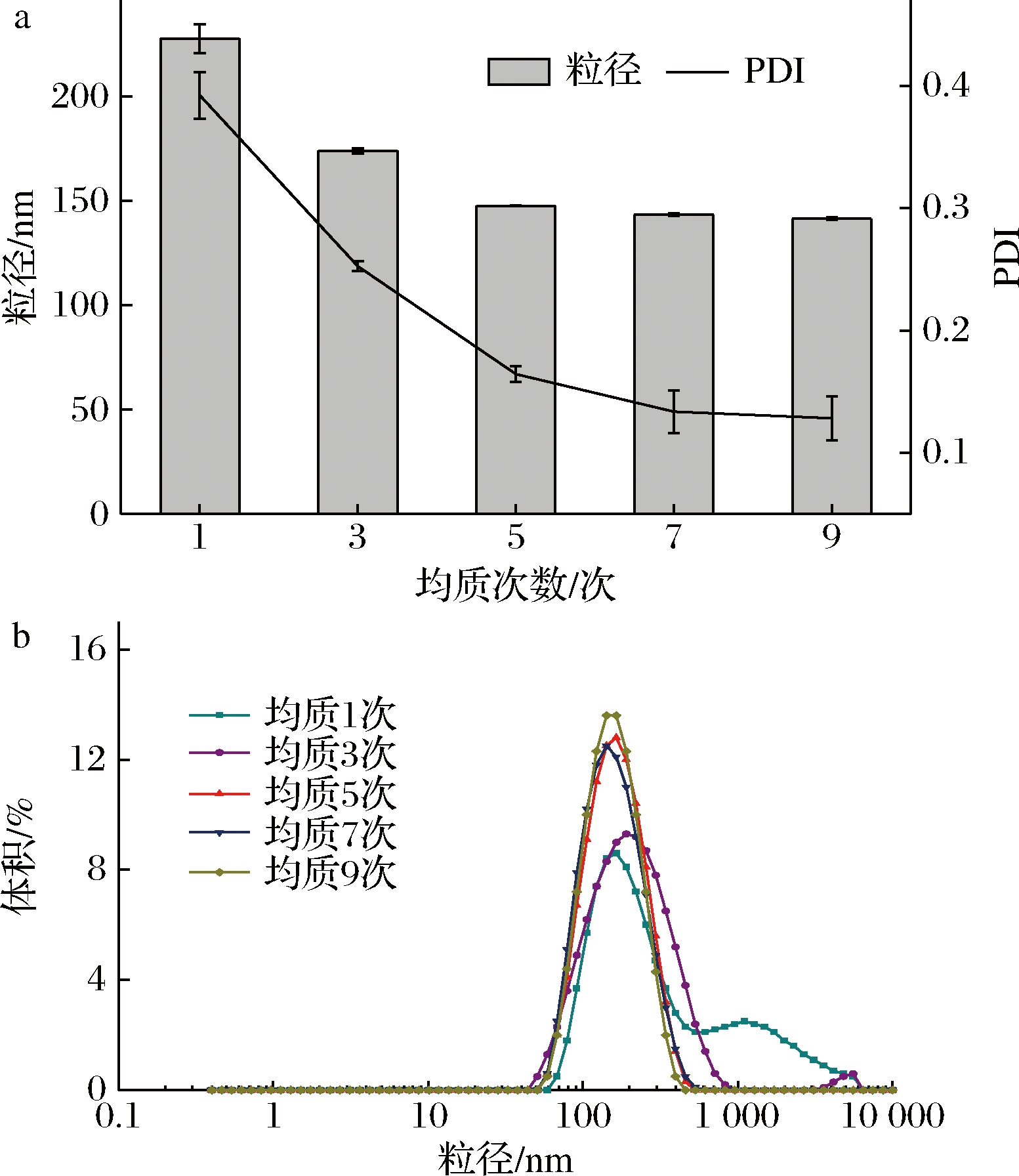
a-粒径、PDI;b-粒径分布
图2 均质次数对八月瓜籽油纳米乳液粒径、PDI及粒径分布的影响
Fig.2 Effect of homogenization number on Akebia trifoliata seed oil nanoemulsion particle size, PDI, and particle size distribution
2.1.3 均质压力对八月瓜籽油纳米乳液粒径、PDI与Zeta电位的影响
由图3可知,在100 MPa下制得的八月瓜籽油纳米乳液粒径与在130 MPa条件下制得的乳液粒径相差不大,PDI指数均在0.2以下,Zeta电位维持在-25 mV左右,具有足够的静电斥力,较为稳定。均质压力过高会导致乳液温度显著升高,加大油脂被氧化的风险[20],为了保证乳液的稳定性以及油脂的活性成分不被破坏,同时降低高压对仪器造成损耗以及保护热敏性活性物质,均质压力不宜过高,均质压力选择为100 MPa。
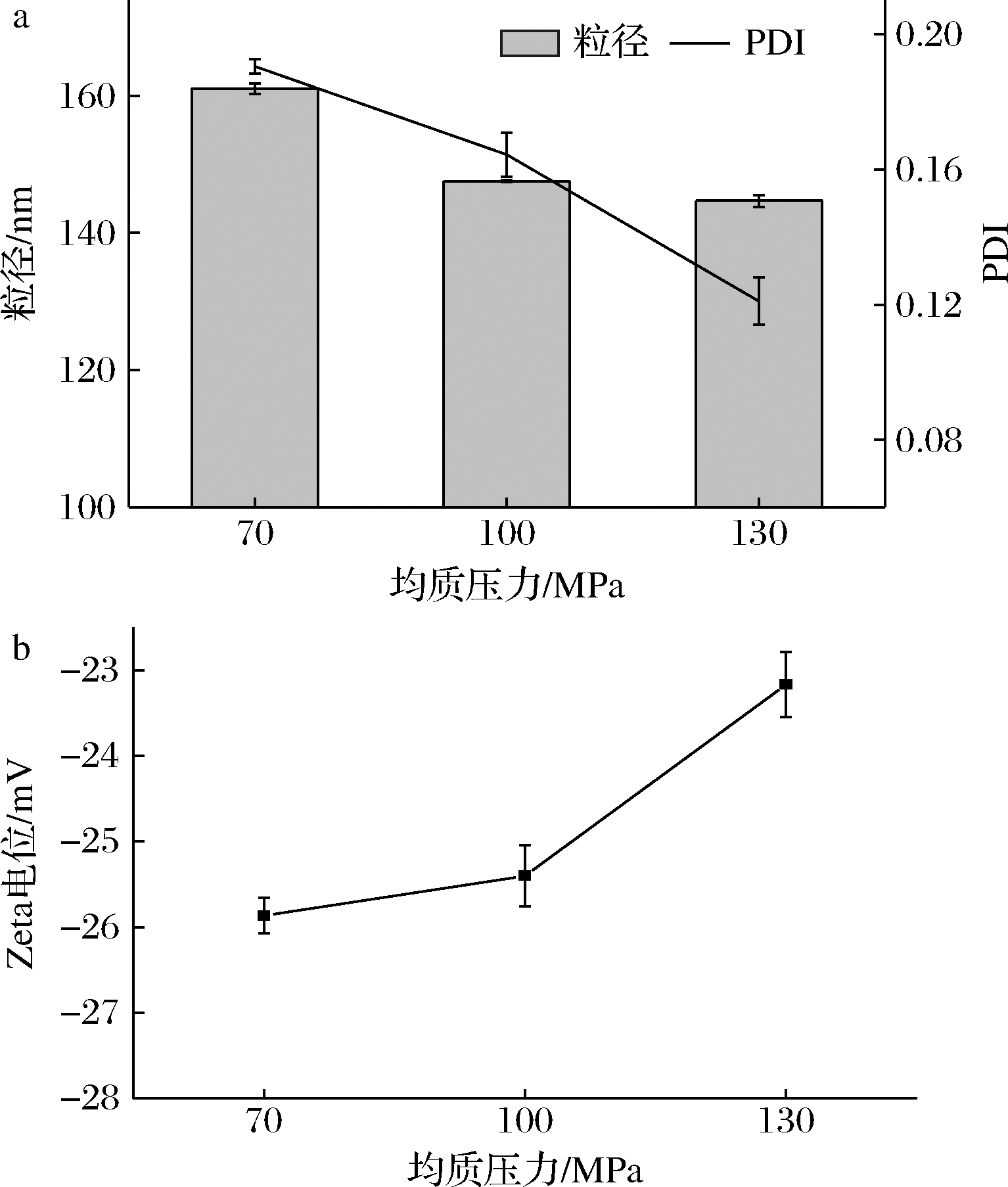
a-粒径、PDI;b-Zeta电位
图3 均质压力对八月瓜籽油纳米乳液粒径、PDI及Zeta电位的影响
Fig.3 Effect of homogenization pressure on Akebia trifoliata seed oil nanoemulsion particle size, PDI, and Zeta potentials
2.1.4 八月瓜籽油质量分数对八月瓜籽油纳米乳液粒径、Zeta电位的影响
由图4可知,随着八月瓜籽油质量分数的增加,乳液粒径也随之增大,Zeta电位绝对值随之减小[21],当八月瓜籽油质量分数为10%时,Zeta电位绝对值最高,证明此时的纳米乳液液滴间存在的静电斥力最大,乳液体系更加稳定。在保证八月瓜籽油纳米乳液稳定性较好的情况下,使载油量保持在较高的水平,以充分利用八月瓜籽油中的各类活性物质,因此确定了八月瓜籽油质量分数为10%。
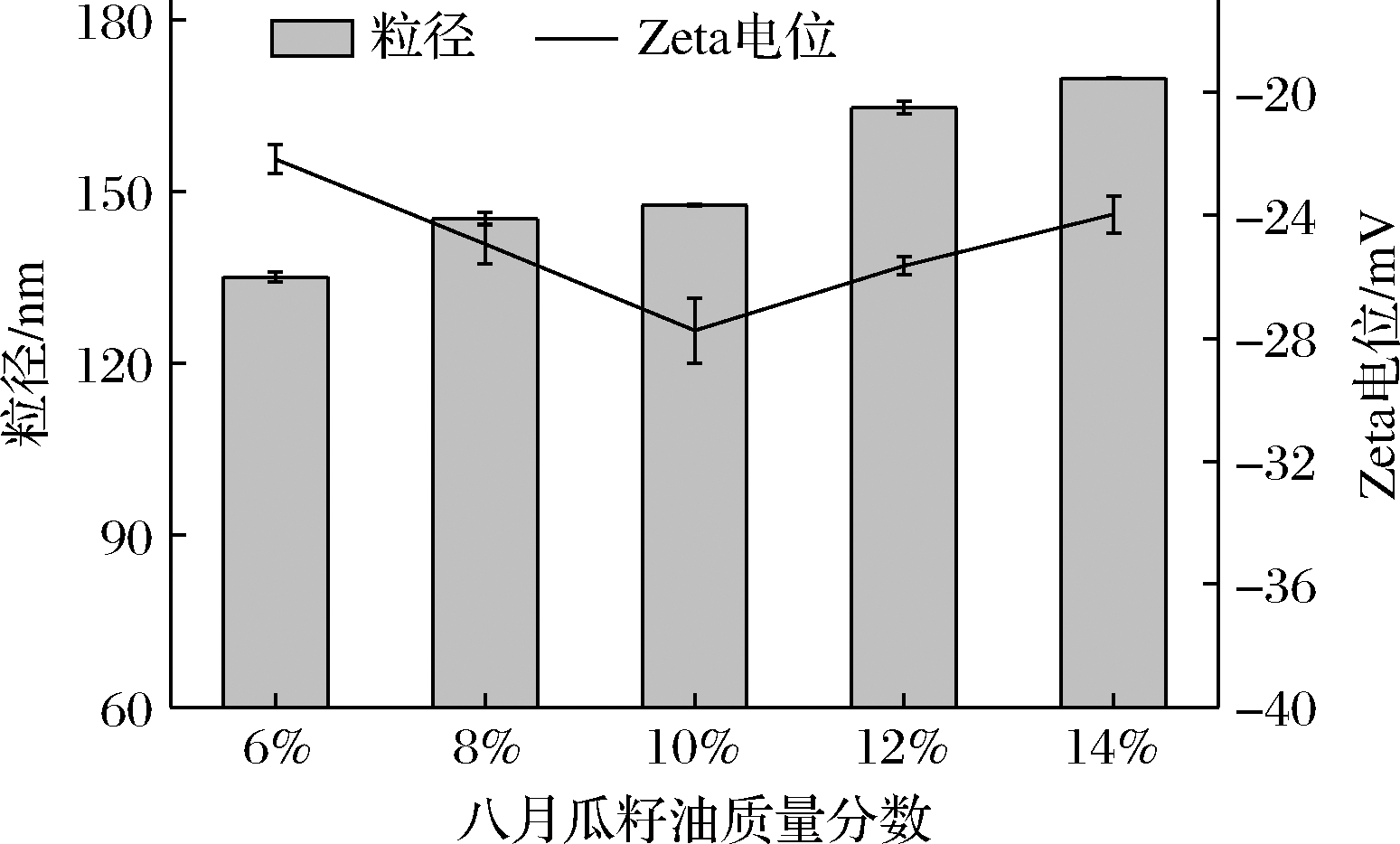
图4 八月瓜籽油质量分数对八月瓜籽油纳米乳液粒径、Zeta电位的影响
Fig.4 Effect of Akebia trifoliata seed oil content on Akebia trifoliata seed oil nanoemulsion particle size, and Zeta potential
2.1.5 乳化剂与助乳化剂的质量比对八月瓜籽油纳米乳液粒径、PDI及粒径分布的影响
由图5可知,随着乳化剂与助乳化剂质量比的降低,乳液粒径与PDI指数增大,在比值为3∶1时,乳液粒径与PDI最小,并且粒径分布最窄,证明此时的粒子大小较为均一,乳液体系最稳定,缺少助乳化剂的助乳化作用,黏度较高,表面张力较大,降低乳化能力,形成微乳粒径也较大[22],因此确定吐温-80与丙二醇的质量分数比为3∶1。
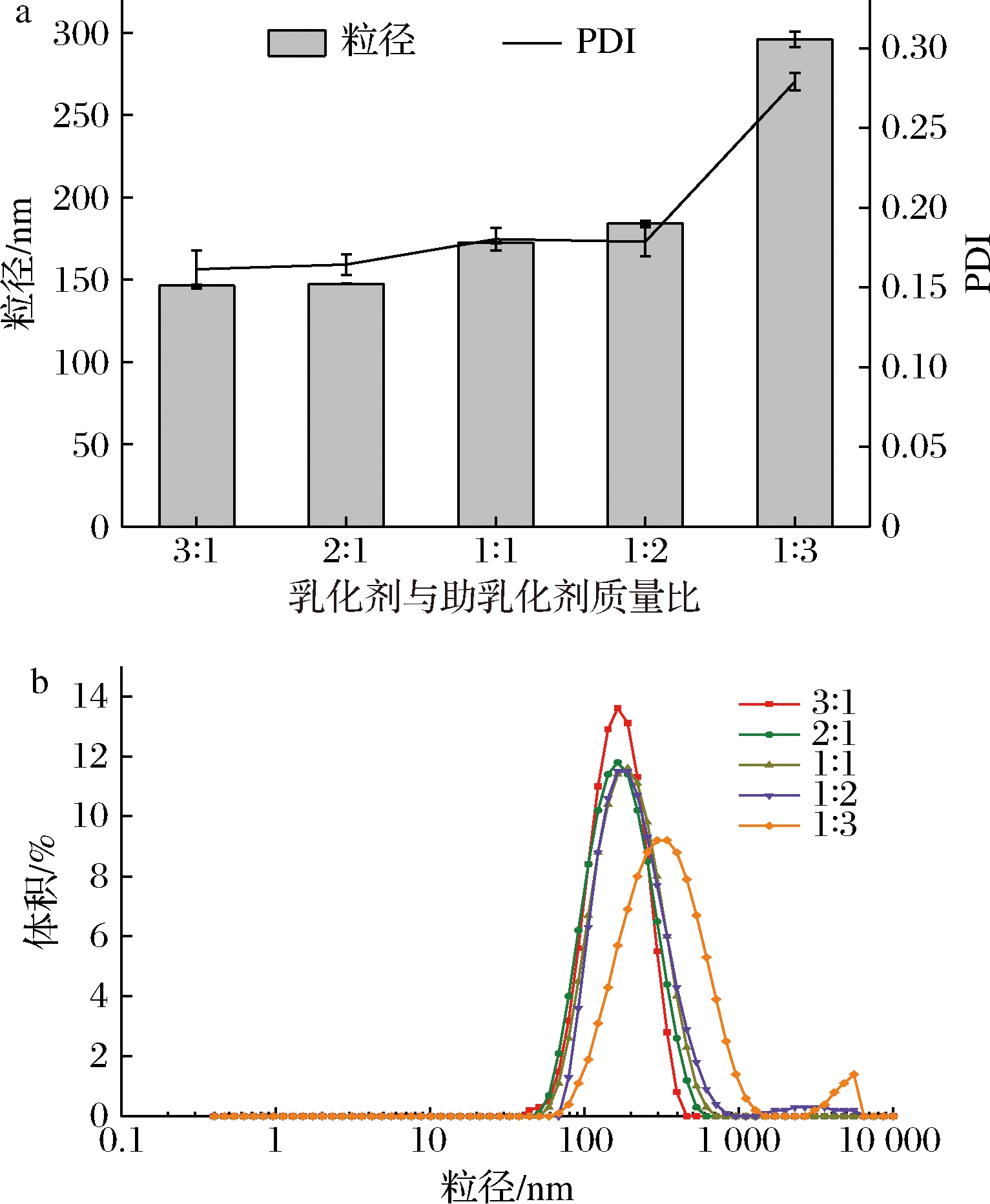
a-粒径、PDI;b-粒径分布
图5 乳化剂与助乳化剂的比例对八月瓜籽油纳米乳液粒径、PDI及粒径分布的影响
Fig.5 Effect of emulsifier-to- cosurfactant ratio on Akebia trifoliata seed oil nanoemulsion particle size, PDI and particle size distribution
2.1.6 复合乳化剂的质量分数对八月瓜籽油纳米乳液粒径、PDI的影响
由图6可知,随着复合乳化剂质量分数的增加,乳液粒径逐渐减小,并且具有显著性差异(P<0.05)。在质量分数为3%时,乳液的PDI最低,此时的乳液体系最稳定。当复合乳化剂质量分数在4%与5%时,粒径虽然在减小,但PDI有增大的趋势,可能是因为随着质量分数的增大,液滴粒径减小,导致布朗运动加快,撞击液滴的分子数量减少,合力不平衡;也可能是吸附在液滴表面的复合乳化剂分子之间产生了聚集,导致乳液液滴之间的平衡状态被破坏,吸附在油滴分子表面的复合乳化剂有互相聚合的趋势,导致PDI产生了细微的增大。欧盟食品科学委员会规定吐温-80的每日最大摄入量为10 mg/kg体重。虽然吐温-80作为非离子表面活性剂广泛应用于食品配方中,通常被认为是无毒、无刺激性的,但为了降低合成添加剂对人体的危害,因此复合乳化剂质量分数选择3%,因2.1.5确定吐温-80与丙二醇的质量比为3∶1,因此吐温-80与丙二醇的质量分数分别为2.25%和0.75%。
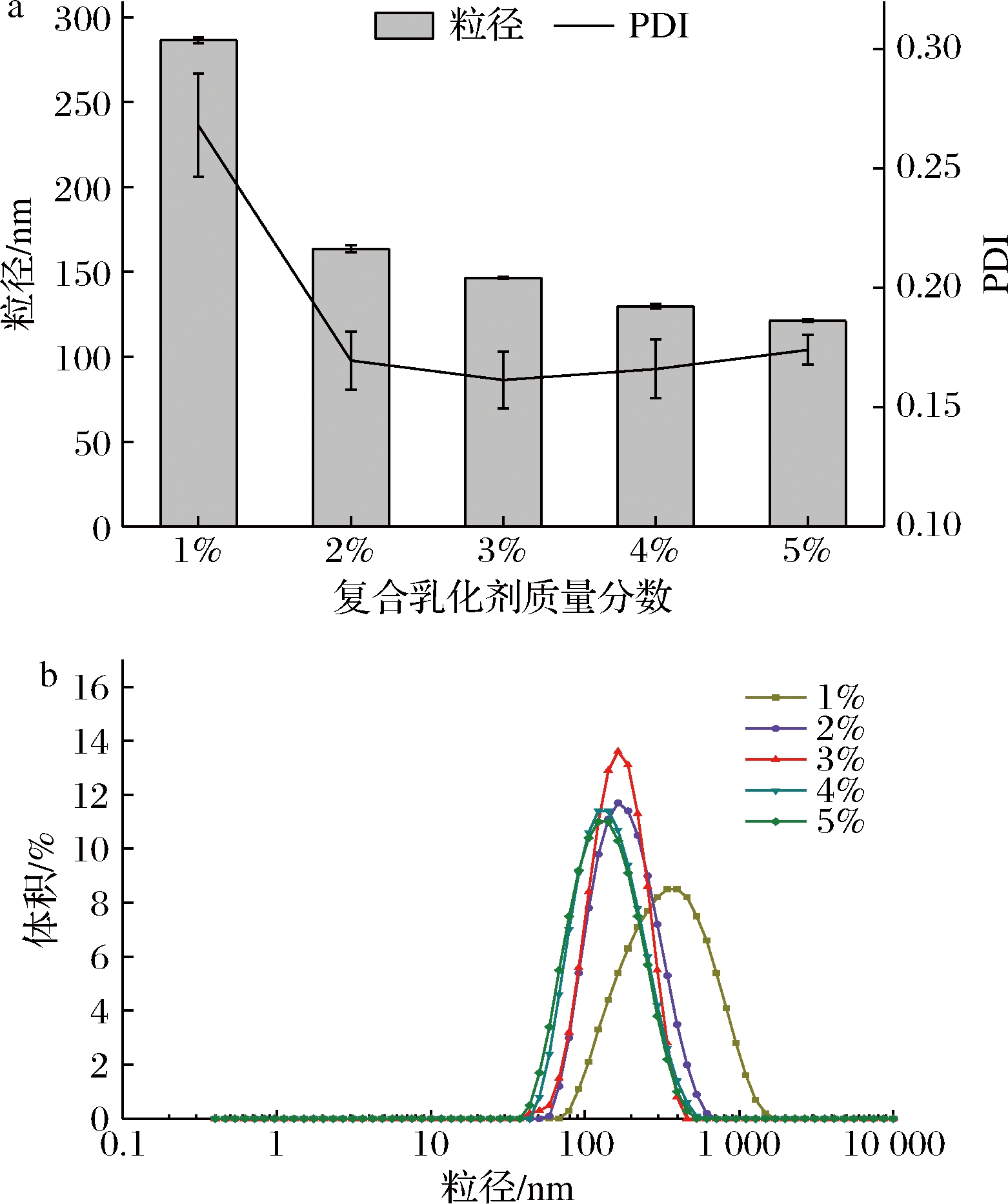
a-粒径、PDI;b-粒径分布
图6 复合乳化剂质量分数对八月瓜籽油纳米乳液粒径、PDI及粒径分布的影响
Fig.6 Effect of composite emulsifier mass fraction on Akebia trifoliata seed oil nanoemulsion particle size, PDI, and particle size distribution
2.2 八月瓜籽油纳米乳液质量评价
由图7-a可知,经过稀释后的乳液澄清透明,具有淡蓝色的乳光。并由图7-b可知,稀释200与1 000倍的乳液经平行光入射后产生了丁达尔效应。分别同时向乳液中滴加亚甲基蓝与苏丹红Ⅲ,观察到图7-c中亚甲基蓝在乳液中先是沉淀在底部,经过轻微的摇晃后均匀分布在乳液中,而苏丹红Ⅲ则是浮在纳米乳液上层,摇晃后也未观察到颜色扩散。因此确定八月瓜籽油纳米乳液为O/W型。经纳米粒度与电位分析仪的测定,确定乳液的平均粒径为(146.43±0.47) nm,Zeta电位为(-25.67±0.21) mV,PDI为0.16±0.01,且由图7-d可知粒径分布峰形细高,证明此时的乳液微粒粒径细小、均一,并且乳液体系较为稳定。
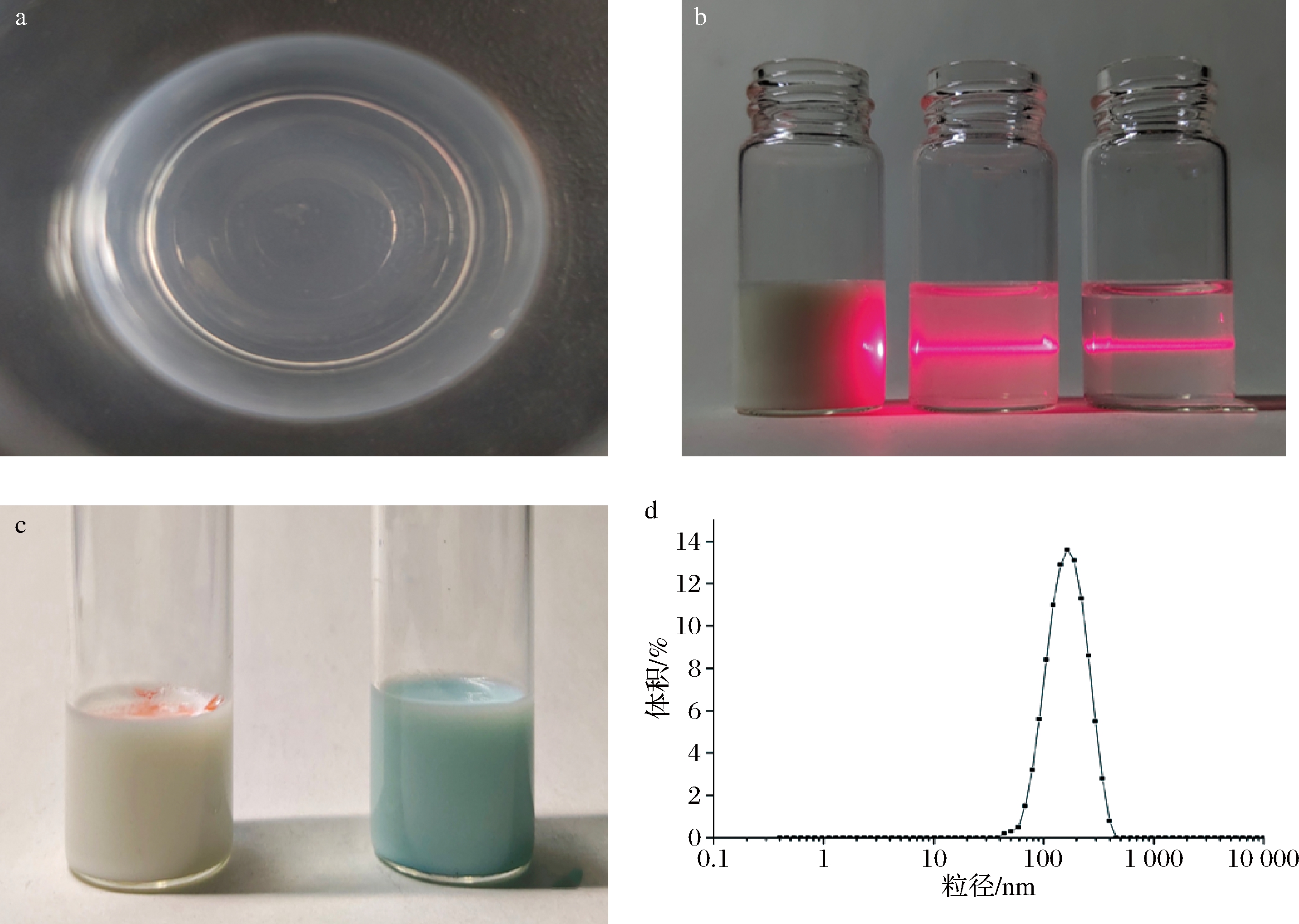
a-稀释液;b-丁达尔效应;c-扩散现象;d-粒径分布
图7 八月瓜籽油纳米乳液稀释液、丁达尔效应、扩散现象和粒径分布
Fig.7 Akebia trifoliata seed oil nanoemulsion Diluent, Tyndall effect, diffusion, and particle size distribution
2.3 八月瓜籽油纳米乳液稳定性评价
2.3.1 贮藏期稳定性
由图8-a可知,在4、25 ℃条件下贮藏25 d的八月瓜籽油纳米乳液粒径基本维持在150 nm,并没有显著变化(P>0.05),而在第25天时,贮藏温度为60 ℃的纳米乳液出现了分层,经测定发现,其平均粒径增大至(197.27±1.85) nm。有研究结果表明,这可能是在高温贮藏条件下乳化剂头基的最佳曲率发生变化或水解导致的结果[23]。由图8-b可知,不同贮藏温度下,PDI指数随着贮藏时间的延长而上升,乳液体系随着时间延长趋于不稳定。在4 ℃下,乳液的PDI指数呈现缓慢上升的趋势。贮藏20 d后,25、60 ℃温度下纳米乳液的PDI值上升趋势明显大于在4 ℃条件下的纳米乳液。结果表明,八月瓜籽油纳米乳液在低温条件下的贮藏稳定性更好。
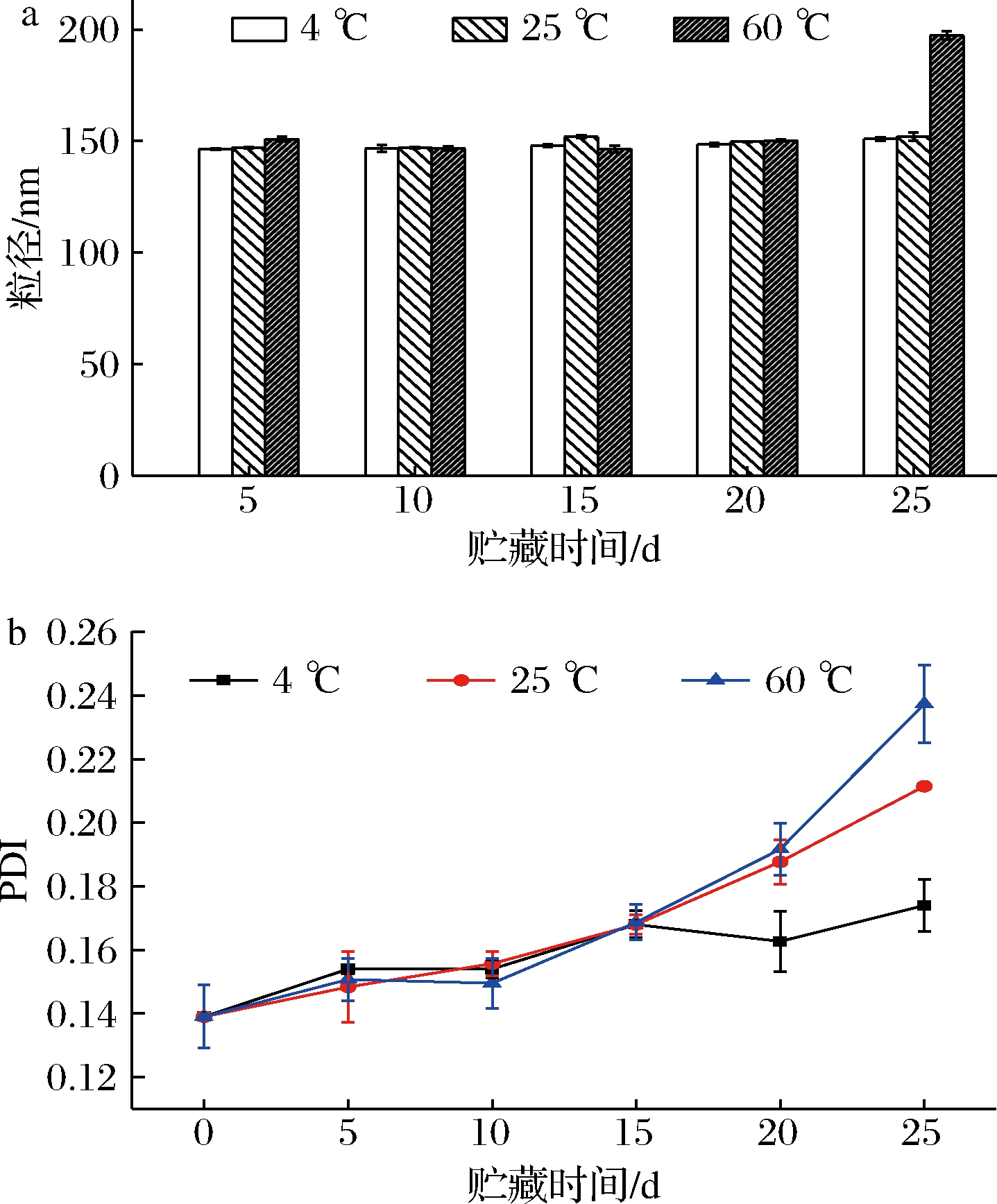
a-粒径;b-PDI
图8 八月瓜籽油纳米乳液在贮藏过程中粒径与PDI的变化
Fig.8 Changes in particle Size and PDI of Akebia trifoliata seed oil nanoemulsion during storage
2.3.2 稀释稳定性
图9为八月瓜籽油纳米乳液分别稀释50、200、1 000倍后,观察到其变为透明,且体系依旧均一,未发生油水分离现象,证明制备的八月瓜籽油纳米乳液具有良好的稀释稳定性。

图9 八月瓜籽油纳米乳液不同稀释倍数效果图
Fig.9 Renderings of different dilution ratios of Akebia trifoliata seed oil nanoemulsion
注:从左至右依次是:稀释1 000倍、200倍、50倍、未稀释
2.3.3 离心稳定性
将乳液稀释200倍后在2 000×g下离心20 min,分别吸取离心前后同样位置的乳液在500 nm处进行测定,并进行计算,得到3组Ke值(表1)。观察到离心后乳液体系均一,且平均Ke值为(2.72±0.001)%,在15%以下,且Ke值越小稳定性越好[24-25]。证明其离心稳定性良好。
表1 八月瓜籽油纳米乳液离心稳定性测定
Table 1 Centrifugal stability determination of Akebia trifoliata seed oil nanoemulsion

试验号离心前离心后Ke值/%10.4290.4182.5620.4320.4202.7830.4270.4152.81
2.3.4 吸光比测定
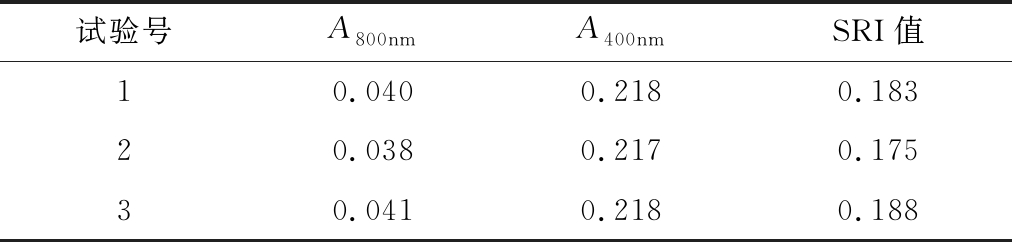
将乳液稀释1 000倍后,分别测定其在800、400 nm处的吸光度,如表2所示,平均SRI值为0.182±0.007,在0.3以下,证明制备的乳液有较好的稳定性。
表2 八月瓜籽油纳米乳液吸光比测定
Table 2 Determination of Specific absorptivity of Akebia trifoliata seed oil nanoemulsion
试验号A800nmA400nmSRI值10.0400.2180.18320.0380.2170.17530.0410.2180.188
2.4 八月瓜籽油纳米乳液对ABTS阳离子自由基的清除能力
通过测定八月瓜籽油、制得的纳米乳液以及不同温度下贮藏25 d纳米乳液对ABTS阳离子自由基清除能力得出,八月瓜籽油纳米乳液的抗氧化活性为(52.29±2.34) μmol Trolox/g,原料油乙醇提取物的抗氧化活性为(45.82±0.20) μmol Trolox/g,提高了14.12%。可以证明八月瓜籽油纳米乳液保留了籽油的抗氧化活性,并且比八月瓜籽油乙醇提取物抗氧化活性更强,这说明该体系能够提高八月瓜籽油对ABTS阳离子自由基的清除能力。由图10可知,贮藏温度的增加导致八月瓜籽油纳米乳液的抗氧化能力有所下降,可能是由于活性物质的热不稳定性,也可能是剧烈的布朗运动造成液滴与氧气接触比较频繁导致活性物质失活。
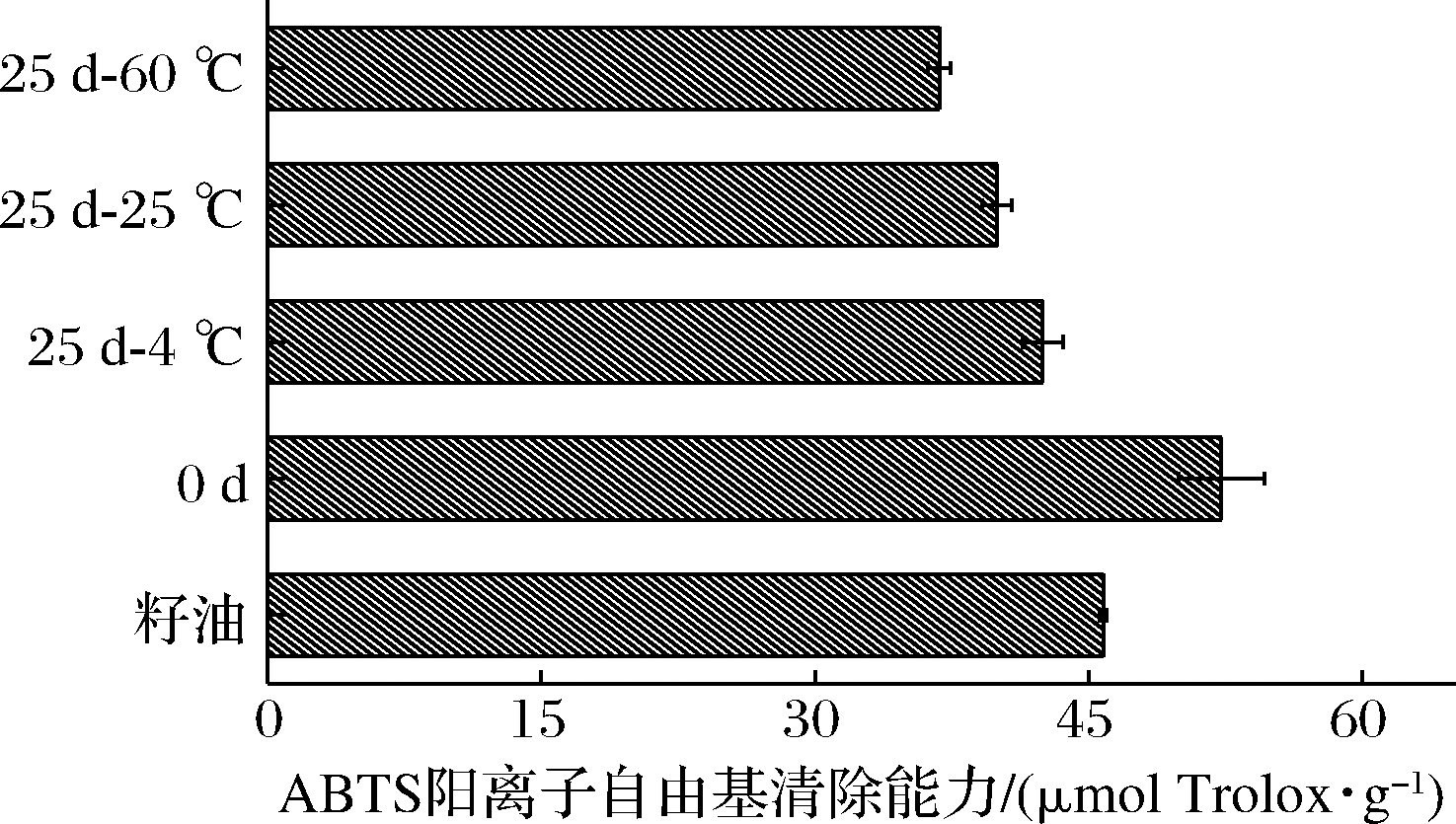
图10 八月瓜籽油纳米乳液在贮藏过程中抗氧化活性的变化
Fig.10 Changes in antioxidant activity of Akebia trifoliata seed oil nanoemulsion during storage
3 结论
本实验对制备八月瓜籽油纳米乳液的配方和工艺进行优化,以食品级的吐温-80作为乳化剂,助乳化剂选择丙二醇,本实验设计单因素试验对制备八月瓜籽油纳米乳液的工艺参数进行优化,以食品级的吐温-80作为乳化剂,最终确定工艺参数为将质量分数为10%的八月瓜籽油,2.25%的吐温-80,0.75%的丙二醇,在100 MPa压力下均质5次,制得八月瓜籽油纳米乳液。制得平均粒径为(146.43±0.47) nm,Zeta电位为(-25.67±0.21) mV,PDI为0.16±0.01的 O/W型纳米乳液。
通过进行稳定性试验,发现离心后的八月瓜籽油纳米乳液并未产生分层、絮凝,且测定的Ke值为(2.72±0.11)%,低于15%,因此乳液具有良好的物理稳定性;分别在800、400 nm测定吸光度,得出SRI为0.182±0.005,<0.3,证明乳液具有较好的稳定性;在低温下贮藏25 d后的结果表明制备的纳米乳液贮藏期稳定性较好;制得的八月瓜籽油纳米乳液对ABTS阳离子自由基清除能力为(52.29±2.341) μmol Trolox/g,比八月瓜籽油乙醇提取物抗氧化活性更强,这说明该体系能够提高八月瓜籽油对ABTS阳离子自由基的清除能力。
本实验对研究八月瓜籽油的运载体系具有一定价值,通过将八月瓜籽油制成纳米乳液,提高了其生物利用度,为利用八月瓜籽油开发新产品提供了新思路。
[1] SURHONE L M, TENNOE M T, HENSSONOW S F, et al.Akebia trifoliata[M].Betascript Publishing, 2010.
[2] 张燕君, 党海山, 杨路路, 等.药用植物三叶木通(Akebia trifoliata subsp.trifoliata)野生资源的地理分布与调查[J].中国野生植物资源, 2013, 32(3):58-62.
ZHANG Y J, DANG H S, YANG L L, et al.Geographical distribution and resource survey of wild medicinal plant Akebia trifoliata subsp.trifoliata[J].Chinese Wild Plant Resources, 2013, 32(3):58-62.
[3] 刘伦沛, 钱增秀.三叶木通果中主要营养成分含量的测定[J].黔东南民族师范高等专科学校学报, 2002, 20(6):39-41.
LIU L P, QIAN Z X.Determination of nutritional components in truit of Akebia trifoliata koidz[J].Journal of Southeast Guizhou National Teacher College, 2002, 20(6):39-41.
[4] 刘红昌, 罗春丽, 李金玲, 等.贵州三叶木通藤茎和果皮中矿质元素及灰分含量[J].贵州农业科学, 2010, 38(11):71-73;77.
LIU H C, LUO C L, LI J L, et al.Determination of mineral elements and ash content in rattan and peel of Akebia trifoliate in Guizhou[J].Guizhou Agricultural Sciences, 2010, 38(11):71-73;77.
[5] 白成科. 猫儿屎和三叶木通种子油中脂肪酸成分的GC-MS分析[J].西北植物学报, 2007, 27(5):1 035-1 038.
BAI C K.Fatty acids analysis in Decaisnea insignis and Akebia trifoliate seed oil by GC-MS[J].Acta Botanica Boreali-Occidentalia Sinica, 2007, 27(5):1 035-1 038.
[6] 孙翔宇, 高贵田, 严勃, 等.三叶木通与猫儿屎种子脂肪酸和氨基酸分析[J].中药材, 2012, 35(9):1 444-1 447.
SUN X Y, GAO G T, YAN B, et al.Analysis of fatty acids and amino acids in the seeds of Agaricum sinensis cat excrement seeds[J].Journal of Chinese Medicinal Materials, 2012, 35(9):1 444-1 447.
[7] 李季楠, 吴艳, 胡浩, 等.食品纳米乳液的研究进展[J].食品与机械, 2019, 35(2):217-225.
LI J N, WU Y, HU H, et al.Research advance on food nano-emulsion delivery system[J].Food and Machinery, 2019, 35(2):217-225.
[8] 靳学远, 刘艳芳.高压微射流制备叶黄素纳米乳液及稳定性研究[J].中国食品添加剂, 2020, 31(10):1-5.
JIN X Y, LIU Y F.Study on preparation of nanoemulsion of lutein by high-pressure microfluidization process and its stability[J].China Food Additives, 2020, 31(10):1-5.
[9] 陈雯烨, 王志高, 鞠兴荣, 等.纳米乳的研究进展与潜在局限性[J].粮食科技与经济, 2020, 45(3):79-83.
CHEN W Y, WANG Z G, JU X R, et al.Research progress and potential limitations of nano-milk[J].Grain Science and Technology and Economy, 2020, 45(3):79-83.
[10] 张建润, 张晶, 宋亮, 等.不同壁材对乳化溶剂蒸发法制备南极磷虾油纳米乳的影响[J].大连工业大学学报, 2018, 37(3):157-162.
ZHANG J R, ZHANG J, SONG L, et al.Effect of different wall materials on the preparation of Antarctic krill oil nanoemulsion by emulsifying solvent evaporation method[J].Journal of Dalian Polytechnic University, 2018, 37(3):157-162.
[11] 邢亚均, 沈勇, 王黎明, 等.O/W型抗紫外纳米乳液的制备及其性能研究[J].应用化工, 2017, 46(3):516-520.
XING Y J, SHEN Y, WANG L M, et al.Preparation and performance of O/W uvioresistant nano-emulsions[J].Applied Chemical Industry, 2017, 46(3):516-520.
[12] 周汉军. 桉叶精油提取、纳米乳化及其抑菌活性研究[D].长沙:中南林业科技大学, 2016.
ZHOU H J.Study on extraction, nanoemulsification and amtimicrobial activity of essential oil from eucalyptus leaves[D].Changsha:Central South University of Forestry and Technology, 2016.
[13] QIN H, ZHOU X T, GU D F, et al.Preparation and characterization of a novel waterborne lambda-cyhalothrin/alkyd nanoemulsion[J].Journal of Agricultural and Food Chemistry, 2019, 67(38):10 587-10 594.
[14] 孙志高, 黄巧娟, 盛冉, 等.β-隐黄素纳米乳的制备及其稳定性研究[J].食品与发酵工业, 2017, 43(3):175-179.
SUN Z G, HUANG Q J, SHENG R, et al.Preparation and stability of β-cryptoxanthin nanoemulsion[J].Food and Fermentation Industries, 2017, 43(3):175-179.
[15] XU J, MUKHERJEE D, CHANG S K C.Physicochemical properties and storage stability of soybean protein nanoemulsions prepared by ultra-high pressure homogenization[J].Food Chemistry, 2018, 240: 1 005-1 013.
[16] KAUFMAN V R, GARTI N.Effect of cloudy agents on the stability and opacity of cloudy emulsions for soft drinks[J].International Journal of Food Science & Technology, 2007, 19(2):255-261.
[17] RE R, PELLEGRINI N, PROTEGGENTE A, et al.Antioxidant activity applying an improved ABTS radical cation decolorization assay[J].Free Radical Biology & Medicine, 1999, 26(9-10):1 231-1 237.
[18] PAVONI L, PERINELLI D R, BONACUCINA G et al.An overview of micro- and nanoemulsions as vehicles for essential oils:Formulation, preparation and stability[J].Nanomaterials(Basel,Switzerland), 2020, 10(1):135.
[19] WANG S S, WANG X Y, LIU M P, et al.Preparation and characterization of Eucommia ulmoides seed oil O/W nanoemulsion by dynamic high-pressure microfluidization[J].LWT, 2020, 121:108960.
[20] 黄剑钊, 黎攀, 许锦伟, 等.美藤果油纳米乳液的制备及稳定性研究[J].食品与发酵工业, 2020, 46(11):216-222.
HUANG J Z, LI P, XU J W, et al.Study on the preparation and stability of sacha inchi oil nanoemulsions[J].Food and Fermentation Industries, 2020, 46(11):216-222.
[21] 綦玉曼, 寻崇荣, 车佳玲, 等.薄荷油纳米乳液的制备及其性质分析[J].食品科学, 2019, 40(10):29-35.
QI Y M, XUN C R, CHE J L, et al.Preparation and properties of peppermint oil nanoemulsions[J].Food Science, 2019, 40(10):29-35.
[22] 刘欣, 周志磊, 毛健.玫瑰精油微乳制备及性质研究[J].食品与生物技术学报, 2019, 38(5):79-85.
LIU X, ZHOU Z L, MAO J.Preparation and characterization of rose essential oil microemulsion and tested its characteristic[J].Journal of Food Science and Biotechnology, 2019, 38(5):79-85.
[23] KATSOULI M, TZIA C.Development and stability assessment of coenzyme Q10-loaded oil-in-water nanoemulsions using as carrier oil:Extra virgin olive and olive-pomace oil[J].Food and Bioprocess Technology, 2019, 12(1):54-76.
[24] XU J, MUKHERJEE D, CHANG S K C.Physicochemical properties and storage stability of soybean protein nanoemulsions prepared by ultra-high pressure homogenization[J].Food Chemistry, 2018, 240:1 005-1 013.
[25] CHANG M, GUO Y W, JIANG Z R, et al.Sea buckthorn pulp oil nanoemulsions fabricated by ultra-high pressure homogenization process:A promising carrier for nutraceutical[J].Journal of Food Engineering, 2020, 287:110129.