我国耕地表层土壤的重金属污染面积占比为15.87%,然而在8种土壤重金属元素中,镉污染概率为25.20%,远超过其他7种土壤重金属元素[1]。但即使在镉污染严重的土壤环境下仍有微生物存活。研究显示大部分的重金属与微生物都能相互作用,重金属环境下的微生物为了永久地调节它们的生命活动,会按照自身所需金属元素浓度进行吸收,以及排除有害金属或消除其他毒害作用[2]。微生物对镉的耐受和吸附的机理非常复杂,其中一种机制是微生物可以通过分泌铁载体来克服镉的毒害影响[3]。
铁载体(siderophore)是微生物主要的铁螯合吸收途径,但在重金属长久胁迫下,微生物能通过该途径螯合重金属来抵抗这种胁迫[4-5]。荧光假单胞菌介导的铁载体已被证明对相关的各种金属离子具有很高的亲和力,如镉、铜、铅、锌和铝等[6]。KURUCZ等[7]发现烟曲霉Af293具有异常高的镉耐受性,镉耐受性还与菌株的铁耐受性和细胞外铁载体产生相关;SINHA等[8]发现镉诱导的高抗镉菌株产生铁载体,通过根系定殖缓解植物镉毒性。基于铁载体对重金属具有一系列相关性,微生物铁载体一直是近年来重金属污染环境修复的一大热点。
目前微生物分泌的铁载体检测主要采用SCHWYN等[9]建立的通用铬天青S(chrome azurol S,CAS)检测方法,其中CAS-铁(Ⅲ)检测液的工作原理是CAS、十六烷基三甲基溴化铵(hexadecyl trimethyl ammonium bromide,HDTMA)和Fe3+能够组成的一种亮蓝色复合物,若复合物的Fe3+被夺去则会产生颜色现象,将检测液与培养基混合可制成CAS-铁(Ⅲ)培养平板。微生物在平板生长分泌铁载体时,菌落周围的Fe3+会被铁载体掠夺形成橘黄色晕圈。但就目前关于CAS与镉的已有的研究,仅能追溯至上世纪90年代慈云祥等[10]和王迪民[11]在化学冶金领域中发表的研究成果,对于研究微生物铁载体与其他重金属离子的螯合关系,则普遍需要借助更为精密的仪器观察,如光谱仪[12]、高效液相色谱-质谱联用仪[13]和正电子发射断层显像仪[14]等。针对部分微生物分泌的铁载体不仅具有能螯合铁而且还能螯合镉的功能,基于CAS-铁(Ⅲ)检测原理改良出一种简便稳定的显示微生物铁载体螯合镉的检测法,更为直观地验明微生物铁载体对镉的相关作用。
伯克霍尔德菌属(Burkholderia)作为重金属污染环境中的镉耐受菌一直被人们所熟知[15],并有相关研究表明该属中的洋葱伯克霍尔德菌对镉不仅具有高度抗性,而且在寡营养条件下具有极强的生物蓄积性[16-17]。由于洋葱伯克霍尔德菌对镉有特异相关性,因此选用洋葱伯克霍尔德菌作为研究对象,拟开展CAS-铁(Ⅲ)平板培养试验和CAS-镉(Ⅱ)的液体、平板试验法检测其铁载体螯合镉的能力,为筛选此类具有螯合镉能力的铁载体微生物奠定了方法基础。
1 材料与方法
1.1 菌株来源
洋葱伯克霍尔德菌(Burkholderia cepacian) ATCC 25416,广东海洋大学保藏并提供。
1.2 仪器与设备
Varioskan Flash全自动酶标仪,美国赛默飞世尔科技公司;SW-CJ-2D型单人双面净化工作台,苏州净化设备有限公司;SPX-250B-Z型生化培养箱、BSD-YX3200型小容量立式摇床,上海博讯实业有限公司医疗设备厂;MDF-U780V型超低温冰箱,冰山松洋生物(大连)有限公司;DL-1型电子万用炉,北京市光明医疗仪器有限公司。
1.3 培养基和试剂配制
酪蛋白氨基酸(KMB)培养基(g/L):酪蛋白氨基酸(去铁)5.00,KH2PO42.50,MgSO4·7H2O 2.50,甘油15.00 mL,pH 6.8。固体培养基则向其中加入20 g/L琼脂。
磷酸缓冲液(g/L):Na2HPO4·2H2O 5.91,Na2HPO4·12H2O 24.27,NH4Cl 2.50,KH2PO40.75,NaCl 1.25,去离子水溶解。高温灭菌备用。
CAS-铁(Ⅲ)检测液:参照文献[18]的方法配制得到1 L蓝色的检测液,高温灭菌备用。
CAS-铁(Ⅲ)培养平板[19]:配制900 mL KMB固体培养基,加热搅拌溶解后于121 ℃高温灭菌20 min;待培养基冷却至60 ℃后,缓慢加入已预热的50 mL磷酸缓冲液和50 mL CAS-铁(Ⅲ)检测液,混合均匀并不产生气泡,倾倒平皿配成CAS-铁(Ⅲ)培养平板。
改良CAS-镉(Ⅱ)检测液[10]:溶液A:称取0.48 g的CAS溶于160 mL的去离子水;溶液B:称取2.50 g的2,2-联吡啶溶于80 mL的无水乙醇;溶液C:称取0.023 g溴化十六烷基吡啶(cetylpyridinium bromide,CPB)溶于60 mL的去离子水;溶液D:称取2.28 g CdCl2·5H2O溶于100 mL的去离子水;溶液E:称取3.81 g的Na2B4O7·10H2O于200 mL去离子水超声溶解,加入适量的NaOH溶液配成pH为11.0~11.5的硼酸钠缓冲溶液。溶液A、B、C混合均匀后,加入20 mL 0.1 moL/L NaOH溶液调至墨绿色,接着加入溶液D进行反应,再加入溶液E混合,最后用适量的去离子水定容至1 L后超声波均匀,即得到深蓝色的CAS-镉(Ⅱ)检测液。制作固体平板则向检测液中加入20 g琼脂。
1.4 实验方法
1.4.1 菌株复苏
将保藏于-80 ℃的洋葱伯克霍尔德菌株接种至5 mL KMB液体培养基中,37 ℃、120 r/min培养18~24 h备用。
1.4.2 铁载体检测
将复苏的洋葱伯克霍尔德菌接种至5 mL KMB液体培养基,37 ℃条件下120 r/min培养18~24 h。将菌液于6 000 r/min离心5 min弃上清液,再用无菌去离子水振荡均匀后6 000 r/min离心5 min弃上清液,重复洗涤2次,最后用无菌去离子水稀释至菌液浓度为OD600=1即制得菌悬液。取3~5 μL菌悬液接种于CAS-铁(Ⅲ)培养平板,置于37 ℃生化培养箱中培养,每天观察和记录实验现象。
1.4.3 菌上清液螯合镉的效果检测
将CAS-镉(Ⅱ)检测液进行全波长扫描,观察检测液的特征吸收峰。若CAS-镉(Ⅱ)检测液络合物中的镉被夺取,则溶液颜色会发生变化。EDTA-2Na作为一种重要金属螯合剂,常在100 mmol/L浓度下用于螯合金属离子和掩蔽金属的化学反应[20],因此选定100 mmol/L浓度开展后续试验。将3 mL的EDTA-2Na、去离子水、KMB液体培养基和细菌培养上清液分别与3 mL CAS-镉(Ⅱ)检测液混合。以EDTA-2Na组作为阳性对照组Ap、去离子水组作为阴性对照组An、KMB液体培养基样品组作为空白对照组和细菌培养上清液样品组作为实验组。测定各组的OD610值,样品As的OD610值应在An~Ap范围内。相对螯合率按公式(1)计算[21]:
相对螯合率![]()
(1)
式中:An,去离子水组测定的OD610值;As,样品组测定的OD610值;Ap,EDTA-2Na组测定的OD610值。其中An≥As≥Ap。
1.5 CAS-镉(Ⅱ)平板法
1.5.1 单层平板法
以EDTA-2Na组作为阳性对照组、去离子水组作为阴性对照组、菌悬液组作为实验组。将EDTA-2Na、去离子水和菌悬液分别滴3~5 μL于CAS-镉(Ⅱ)平板上,置于37 ℃生化培养箱中放置,观察和记录平板上的实验现象。
1.5.2 双层平板法
在制成的CAS-镉(Ⅱ)单层平板上倒入同等体积KMB固体培养基,待其完全冷却即制成双层CAS-镉(Ⅱ)平板。将EDTA-2Na、去离子水和菌悬液分别滴3~5 μL于双层平板上,置于37 ℃生化培养箱中培养和放置,每天观察和记录平板上的实验现象。
1.5.3 三层平板法
在制成的CAS-镉(Ⅱ)单层平板上先后倒入1/2体积的素琼脂和同等体积的KMB固体培养基,待其完全冷却即制成CAS-镉(Ⅱ)三层平板。将EDTA-2Na、去离子水和菌悬液分别滴3~5 μL于三层平板上,置于37 ℃生化培养箱中培养和放置,每天观察和记录平板上的实验现象。
1.6 CAS-镉(Ⅱ)平板覆盖法
EDTA-2Na、去离子水和菌悬液分别滴3~5 μL于KMB固体培养平板,37 ℃培养和放置3~5 d,然后在上方倾倒CAS-镉(Ⅱ)检测液,静置12 h后用去离子水缓慢冲洗平板,观察和记录实验现象。
2 结果与分析
2.1 铁载体检测结果
洋葱伯克霍尔德菌在CAS-铁(Ⅲ)培养平板生长良好,试验菌株菌落周围产生了特征性的铁载体橙色螯合晕圈(图1),表明菌株在培养的过程中分泌了铁载体,铁载体与平板上的Fe3+螯合使平板颜色发生变化,螯合晕圈的大小反映了铁载体产生能力的强弱。随着培养时间延长,螯合晕圈逐渐加大,并于4~5 d后趋于稳定。

图1 洋葱伯克霍尔德菌分泌铁载体情况
Fig.1 Effect of siderophores secreted by B.cepacia
2.2 菌上清液螯合镉结果
深蓝色的CAS-镉(Ⅱ)检测液于610 nm处有特征吸收峰,说明检测液复合物物质单一且稳定(图2-a)。根据EDTA-2Na、去离子水、KMB液体培养基、细菌培养上清液与检测液1∶1混合的结果显示(图2-b),EDTA-2Na螯合检测液中的镉导致颜色由深蓝色变为更加透亮的橙黄色,去离子水组依旧为深蓝色,并无螯合效果。培养基和菌上清液组也存在螯合现象,颜色变为墨绿色,计算相对螯合率分别为28.3%和34.8%,两者并无太大差别(图2-c)。考虑到KMB液体培养基中蛋白等物质具有螯合能力,菌株培养过程中本身消耗部分这类蛋白物质的同时又能分泌铁载体,因此上清液检测法不适用。

a- CAS-镉(Ⅱ)检测液全波长扫描;b-各组与检测液反应的对比图;c-相对螯合率
图2 CAS-镉(Ⅱ)检测液全波长扫描、各组与检测液反应的对比图和各组相对螯合率
Fig.2 Full wavelength scanning results of CAS-Cd (Ⅱ) detection solution, reaction with detection solution, and the relative chelation rate of each group
2.3 CAS-镉(Ⅱ)平板检测结果
2.3.1 单层平板
单层CAS-镉(Ⅱ)平板结果显示(图3),EDTA-2Na液滴处出现橙色螯合晕圈,去离子水滴在平板上无明显现象,说明EDTA-2Na夺取了检测板中复合物的Cd2+形成的褪色橙色圈,表明检测板具有检测能力。菌悬液组平板呈深蓝色,并无明显现象。由此可以判断,菌体本身并不具备螯合镉的能力,考虑检测板中存在高浓度镉和上方缺乏菌株生长的营养物质,继而进行双层平板试验。

图3 CAS-镉(Ⅱ)单层平板实物图(a)和各组平板检测结果(b)
Fig.3 CAS-Cd (Ⅱ) single-layer plate physical diagram (a) and the results of plate detection in each group (b)
2.3.2 双层平板
在双层CAS-镉(Ⅱ)平板试验中,各组平板由深蓝色变为蓝绿色,表明培养基对检测板有轻微的螯合效果。阴阳性对照组平板对比无明显区别,说明EDTA-2Na难以渗透至KMB培养基与检测板反应(图4)。虽然在检测板上层添加了细菌生长所需营养培养基,但由于检测板的毒性过大,依旧能阻碍细菌在培养基上的正常生长。因此双层平板法不适用。

图4 CAS-镉(Ⅱ)双层平板实物图(a)和各组平板检测结果(b)
Fig.4 CAS-Cd (Ⅱ) double-layer plate physical diagram (a) and the results of plate detection in each group (b)
2.3.3 三层平板
虽然在检测板和培养基中间添加了素琼脂,但各组的平板颜色并没有改变,EDTA-2Na滴在上层培养基表面一段时间不能让其渗透至检测板反应,菌株依然难以在培养层上生长,素琼脂并不能将检测板中的有毒物质与培养基有效隔离开(图5)。因此三层CAS-镉(Ⅱ)平板法并不适用。

图5 CAS-镉(Ⅱ)三层平板实物图(a)和各组平板检测结果(b)
Fig.5 CAS-Cd (Ⅱ) three-layer plate physical diagram (a) and the results of plate detection in each group (b)
2.4 CAS-镉(Ⅱ)平板覆盖法结果
CAS-镉(Ⅱ)检测液处理前,菌株在培养基生长良好;CAS-镉(Ⅱ)检测液处理后,除去离子水组外,菌悬液组和EDTA-2Na组平板上产生肉眼可见褪色圈,并且菌落周围的褪色圈比阳性对照更加显著(图6)。由于菌株在培养基上良好生长3~5 d,足以使其菌落在周边分泌多的铁载体与检测液充分反应,因此检测液平板覆盖法适用于产铁载体微生物对镉螯合的观察。

a-处理前;b-处理后
图6 CAS-镉(Ⅱ)平板覆盖法的检测结果
Fig.6 Results of CAS-Cd (Ⅱ) plate detection solution dumping method
3 讨论与结论
CAS-铁(Ⅲ)培养平板验证洋葱伯克霍尔德菌具有产铁载体的能力,在洋葱伯克霍尔德菌K56-2群体感应系统也发现转录调节因子CepR可调控铁载体蛋白[22],但为了进一步证明该菌分泌的铁载体具有螯合镉的特性。首先尝试的CAS-镉(Ⅱ)液体螯合试验,阴阳对照组虽有证明检测液的可用性,但因为培养基中存在蛋白等物质成分,导致培养基组和菌上清液组同时出现螯合现象,所以结果并不能正确反映菌株分泌铁载体具有螯合镉的能力。为了排除培养基中的物质对试验的干扰,让菌株能直接在CAS-镉(Ⅱ)平板上反应或生长,继而设计了3种平板试验法进行尝试。但由于检测板的2,2-联吡啶[23]、CPB[24]和高浓度镉等物质对微生物是剧毒的存在,培养基和素琼脂不能将其有毒物质有效隔离,导致菌株在经典的双层平板[25]和改进的三层平板仍不能生长存活。最终采用的CAS-镉(II)检测液平板覆盖法达到预期的效果。通过该方法,细菌在培养基分泌充足的铁载体能够与CAS-镉(II)检测液充分接触和反应,直接定性细菌铁载体对镉具有螯合作用。王卫星等[26]通过CAS-铁(Ⅲ)覆盖法处理1 h左右能有效地观察到氢氧化细菌分泌的铁载体,但也仅限于观察对铁的作用。相比之下,本研究的平板覆盖法中使用的是去铁培养基,微生物在铁饥饿的培养条件下更容易分泌铁载体[27],另外CAS-镉(Ⅱ)检测液要比CAS-铁(Ⅲ)检测液颜色深,且铁载体天然对铁的亲和力远大于镉[28],因此处理时间延长至12 h使其反应充分后还需要倒掉和冲洗检测液才能观察到现象。不仅如此,CAS-镉(Ⅱ)平板覆盖法结果还能根据褪色圈与菌落的比值大小,比较和定量不同菌株之间分泌铁载体螯合镉能力的强弱[29],并且可以根据菌株生长营养需求更换培养基的同时,也不影响检测液的工作效果,实现该法的通用性和稳定性。然而本研究方法是基于CAS-镉(Ⅱ)检测液开展的一系列试验,仅能鉴别微生物铁载体对镉螯合的能力,在产铁载体微生物对其他的污染重金属元素(如铅、汞、铬和铜等)螯合能力的鉴别还需开发相应的CAS检测液,再通过平板覆盖法实现,以便寻求更多类型的产铁载体微生物,从而解决重金属污染问题。
综上所述,本研究基于CAS-铁(Ⅲ)检测法不仅改良配制出CAS-镉(Ⅱ)检测液,而且对其多种检测方法进行了探究,最终证明CAS-镉(Ⅱ)平板覆盖法的可行性。通过该法能用肉眼直观地鉴别微生物分泌的铁载体是否具备螯合镉的能力,突显其直观、简单、通用和稳定的特点,更加有力地佐证重金属与微生物铁载体的螯合作用,为筛选能螯合镉甚至是其他重金属的产铁载体微生物提供新的方法和思路。
[1] 曾思燕,于昊辰, 马静, 等.中国耕地表层土壤重金属污染状况评判及休耕空间权衡[J].土壤学报, 2022, 59(4):1 036-1 047.
ZENG S Y, YU H C, MA J, et al.Identifying the status of heavy metal pollution of cultivated land for tradeoff spatial fallow in China[J].Acta Pedologica Sinica, 2022, 59(4):1 036-1 047.
[2] KAMALS, PRASAD R, VARMA A.Soil microbial diversity in relation to heavy metals[M]//Soil Biology.Berlin, Heidelberg:Springer Berlin Heidelberg, 2009:31-63.
[3] IZRAEL-ŽIVKOVI L, RIKALOVI
L, RIKALOVI M, GOJGI
M, GOJGI -CVIJOVI
-CVIJOVI G, et al.Cadmium specific proteomic responses of a highly resistant Pseudomonas aeruginosaSan ai[J].RSC Advances, 2018, 8(19):10 549-10 560.
G, et al.Cadmium specific proteomic responses of a highly resistant Pseudomonas aeruginosaSan ai[J].RSC Advances, 2018, 8(19):10 549-10 560.
[4] 张笑雨,朱建明, 蔡中华, 等.海洋微生物铁载体的研究进展[J].生物化学与生物物理进展, 2022, 49(9):1 658-1 671.
ZHANG X Y, ZHU J M, CAI Z H, et al.The research advance of siderophores in marine microbes[J].Progress in Biochemistry and Biophysics,2022, 49(9):1 658-1 671.
[5] HESSEE, O’BRIEN S, TROMAS N, et al.Ecological selection of siderophore-producing microbial taxa in response to heavy metal contamination[J].Ecology Letters, 2018, 21(1):117-127.
[6] BHATTACHARYAA.Siderophore mediated metal uptake by Pseudomonas fluorescensand its comparison to Iron (III) chelation[J].Ceylon Journal of Science (Biological Sciences), 2011, 39(2):147.
[7] KURUCZV, KISS B, SZIGETI Z M, et al.Physiological background of the remarkably high Cd2+tolerance of the Aspergillus fumigatusAf293 strain [J].Journal of Basic Microbiology, 2018, 58(11):957-967.
[8] SINHAS, MUKHERJEE S K.Cadmium-induced siderophore production by a high Cd-resistant bacterial strain relieved Cd toxicity in plants through root colonization [J].Current Microbiology, 2008, 56(1):55-60.
[9] SCHWYNB, NEILANDS J B.Universal chemical assay for the detection and determination of siderophores[J].Analytical Biochemistry, 1987, 160(1):47-56.
[10] 慈云祥,杨明敏.多元络合物显色反应的研究Ⅸ镉(Ⅱ)-铬天青S-2, 2’-联吡啶-溴化十六烷基吡啶体系[J].化学试剂, 1982, 4(4):209-213;257.
CI Y X, YANG M M.Studies on the colour reactions of multicom ponent complexes Ⅸ.Cadmium (Ⅱ)-chromeazurol S-2, 2’-dipyridine-cetylpyridinium bromide system[J].Chemical Reagents, 1982, 4(4):209-213;257.
[11] 王迪民.阴离子交换分离—CAS—Phen—CTMAB分光光度法测定闪锌矿中微量镉[J].冶金分析, 1986, 6(2):26-29.
WANG D M.Spectrophotometric determination of micro amount of cadmium in blende with O-phenanthroline-chromazurol S-cetyltrimethylammonlum bromide by anion exck-ange separation[J].Metallurgical Analysis, 1986, 6(2):26-29.
[12] MEESUNGNOENO, CHANTIRATIKUL P, THUMANU K, et al.Elucidation of crude siderophore extracts from supernatants of Pseudomonas sp.ZnCd2003 cultivated in nutrient broth supplemented with Zn, Cd, and Zn plus Cd [J].Archives of Microbiology, 2021, 203(6):2 863-2 874.
[13] SCHWABER, ANKE M K, SZYMA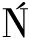 SKA K, et al.Analysis of desferrioxamine-like siderophores and their capability to selectively bind metals and metalloids:Development of a robust analytical RP-HPLC method[J].Research in Microbiology, 2018, 169(10):598-607.
SKA K, et al.Analysis of desferrioxamine-like siderophores and their capability to selectively bind metals and metalloids:Development of a robust analytical RP-HPLC method[J].Research in Microbiology, 2018, 169(10):598-607.
[14] MULARA, SHANZER A, KOZ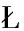 OWSKI H, et al.Cyclic analogs of desferrioxamine E siderophore for68Ga nuclear imaging:coordination chemistry and biological activity in Staphylococcus aureus[J].Inorganic Chemistry, 2021, 60(23):1 7 846-1 7857.
OWSKI H, et al.Cyclic analogs of desferrioxamine E siderophore for68Ga nuclear imaging:coordination chemistry and biological activity in Staphylococcus aureus[J].Inorganic Chemistry, 2021, 60(23):1 7 846-1 7857.
[15] BRAVOD, BRAISSANT O.Cadmium-tolerant bacteria:Current trends and applications in agriculture [J].Letters in Applied Microbiology, 2022, 74(3):311-333.
[16] ZHANGJ H, LI Q, ZENG Y F, et al.Bioaccumulation and distribution of cadmium by Burkholderia cepaciaGYP1 under oligotrophic condition and mechanism analysis at proteome level[J].Ecotoxicology and Environmental Safety, 2019, 176:162-169.
[17] HUANGW, LI Y Q, et al.Isolation, characterization, and evaluation of a high-siderophore-yielding bacterium from heavy metal-contaminated soil[J].Environmental Science and Pollution Research, 2022, 29(3):3 888-3 899.
[18] 许佳露,张平, 李美芳, 等.产铁载体菌株的分离、培养条件优化及初步应用[J].微生物学通报, 2022, 49(3):1 004-1 016.
XU J L, ZHANG P, LI M F, et al.Isolation, culture condition optimization, and preliminary application of siderophore-producing strains[J].Microbiology China, 2022, 49(3):1 004-1 016.
[19] 王东升,王立立, 李取生, 等.产铁载体菌对龙葵修复土壤Cd污染的促进效应[J].环境工程学报, 2018, 12(8):2 311-2 319.
WANG D S, WANG L L, LI Q S, et al.Enhancing effect of siderophore-producting bacteria on remediation of cadmium-contaminated soil by Solanum nigrum L [J].Chinese Journal of Environmental Engineering, 2018, 12(8):2 311-2 319.
[20] CUNNINGHAMT M, KOEHL J L, SUMMERS J S, et al.pH-dependent metal ion toxicity influences the antibacterial activity of two natural mineral mixtures [J].PLoS One, 2010, 5(3):e9456.
[21] PAYNES M.Detection, isolation, and characterization of siderophores [J].Methods in Enzymology, 1994, 235:329-344.
[22] LUTTERE, LEWENZA S, DENNIS J J, et al.Distribution of quorum-sensing genes in the Burkholderia cepaciacomplex[J].Infection and Immunity, 2001, 69(7):4 661-4 666.
[23] PISHCHANYG, HALEY K P, SKAAR E P.Staphylococcus aureusgrowth using human hemoglobin as an iron source[J].Journal of Visualized Experiments:JoVE, 2013(72):50072.
[24] MYERSG E, PYRCH D.Residual bactericidal activity of cetyl pyridinium bromide (Fixanol C) against Staphylococcus aureus[J].The American Journal of the Medical Sciences, 1962, 243:475-479.
[25] MILAGRESA M F, MACHUCA A, NAPOLE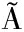 O D.Detection of siderophore production from several fungi and bacteria by a modification of chrome azurol S (CAS) agar plate assay[J].Journal of Microbiological Methods, 1999, 37(1):1-6.
O D.Detection of siderophore production from several fungi and bacteria by a modification of chrome azurol S (CAS) agar plate assay[J].Journal of Microbiological Methods, 1999, 37(1):1-6.
[26] 王卫星,周晓伦, 李忠玲, 等.CAS平板覆盖法检测氢氧化细菌铁载体 [J].微生物学通报, 2014, 41(8):1 692-1 697.
WANG W X, ZHOU X L, LI Z L, et al.Detection of siderophore production from hydrogen-oxidizing bacteria with CAS overlay plate method [J].Microbiology China, 2014, 41(8):1 692-1 697.
[27] ALIS S, VIDHALE N N.Bacterial siderohore and their application:A review [J].International Journal of Current Microbiology and Applied Sciences, 2013, 2(12):303-312.
[28] GHOSHS K, BERA T, CHAKRABARTY A M.Microbial siderophore-A boon to agricultural sciences[J].Biological Control, 2020, 144:104214.
[29] 魏本杰,曾晓希, 刘志成, 等.产铁载体菌的筛选鉴定及活化镉的性能探究[J].环境科学与技术, 2014, 37(11):26-31.
WEI B J, ZENG X X, LIU Z C, et al.Isolation, identification and study on cadmium-mobilization ability of sidorophores-producing bacteria[J].Environmental Science &Technology, 2014, 37(11):26-31.