随着可持续发展和绿色环保理念的推广,各行各业都以此为长期的发展目标。对于食品行业更是如此,可食性墨水在食品的标识、装饰、创新定制等领域的应用,引起了各行各业的关注。因为它可以最大程度保证其成分的可食性、安全性、环保性,并且使食品更具特色和吸引力。可食性墨水的组成成分包括连接料、色料、助剂等。据报道,国内制备可食墨水的连接料常用的物质是多糖类,比如壳寡糖、海藻酸钠、黄原胶,对于蛋白质类连接料的研究相对较少,值得进一步的探究和拓展。
连接料对墨水的分散性非常重要,它不仅能够作为色素的载体,分散色料,并对墨水的黏度、流动性、印刷适性有直接影响。明胶(gelatin,Ge)是由胶原蛋白水解而来的一种大分子水溶性蛋白,具有可食性、分散性、成膜性、生物相容性等优良的理化性质,并且明胶作为生理活性成分载体[1],在食品领域得到了广泛的应用。明胶水溶液可以作为连接料分散色料,其溶液具有一定的黏度,在水中具有三维螺旋结构,明胶链之间相互交叉并与空隙间的水形成三维网络结构,干燥后有利于形成光滑的墨膜[2],因此可潜在制备高性能墨水。
色料可以赋予墨水颜色,使产品更加美观,促进消费。由于传统的合成色素对于人体具有潜在的健康危害,而且消费者对于食品的品质要求有所提升,所以天然色素更受消费者的青睐。胭脂虫红(cochineal carmine,Cc)、栀子蓝(gardenia blue,Gb)、栀子黄(gardenia yellow,Gy),都是水溶性天然色素,也是具有代表性的红、黄、蓝色,是食品应用中较多的3种天然色素。胭脂虫红有一个葡萄糖单元组成,并由一个单元的蒽醌连接的蒽醌类天然色素,色调呈粉红至紫红[3]。胭脂虫红溶于水,具有抗氧化,对光、高温稳定等特性,广泛应用于果酱、冰淇淋、乳制品、肉类食品[4];栀子黄是类胡萝卜素类,分子中存在多个共轭双键,它们是栀子黄的生色基团,同时也是其不稳定的原因,因为共轭双键极易被氧化破坏[5]。栀子黄具有优异的水溶性,耐酸碱和金属离子,可以应用于糕点、饮料、果冻、饼干等食品[6-7];栀子蓝属于环烯醚萜衍生物类,是由甲基环戊烷单元形成的单萜类化合物,通常以游离形式和糖基化形式存在[8],广泛应用于冷冻甜品、烘焙食品、果酱等食品中[9]。本文所选的胭脂虫红、栀子黄、栀子蓝属于颜料三原色(红、黄、蓝),3种颜色复配可以潜在获得多种颜色的可食性墨水,这对其在食品、印刷等行业的应用具有重要的意义。
但仅由连接料和色料组成的可食性墨水的性能不能满足其实际的应用,因此,助剂也是可食性墨水中必不可少的组分。甘油(glycerol,Glc)是一种多元醇(1,2,3-丙三醇),在食品工业中,甘油的应用广泛,比如保湿剂、润滑剂、增稠剂、甜味剂、防冻剂等。甘油具有良好的保湿润滑性能,因甘油中的羟基能与水分子形成氢键[10],所以甘油可以作为可食性墨水的润滑剂,良好的润滑性能可以促进消费者对可食墨水具有较好的书写体验感。
目前,对于明胶基可食性墨水和三色可食墨水的马克笔书写应用研究比较少,有待拓展和深化,相应的机制研究不够成熟,需要进一步研究支撑。因此,研究了明胶基可食性墨水色素、明胶、甘油的最优添加量,采用色差、触变恢复率、冻融稳定性、沉降率、离心稳定性、触变指数等指标逐步优化体系的呈色度、色料分散度、稳定性、润滑性,为可食墨水在食品工业上的应用提供参考。
1 材料与方法
1.1 材料与试剂
明胶(食品级),山东省莱阳市福利明胶厂;栀子蓝、栀子黄、胭脂虫红天然色素,广州市天旭食品添加剂有限公司;甘油(食品级),连云港新爱食品科技有限公司;纯水(分析纯)。
1.2 仪器与设备
JA3003B型电子天平,上海精天电子仪器有限公司;HH-4型数显恒温搅拌器,上海新诺仪器设备有限公司;XQM型立式半圆形行星球磨机,长沙天创粉末科技有限公司;FD-1A-50型真空冷冻干燥仪,北京博伊康实验仪器有限公司;Specturn 100红外光谱仪,美国PerkinElmer公司;XD-52AA型测色仪,深圳市威福光电科技有限公司;SU3500扫描电子显微镜,日本日立公司;MCR302型流变仪,奥地利安东帕公司;DGG-9140A电热恒温鼓风干燥箱,上海齐欣科学仪器有限公司。
1.3 实验方法
1.3.1 样品制备
将纯水加入明胶中,常温静置1 h使其吸水溶胀,随后在50~55 ℃条件下水浴加热并不断搅拌,制备得到1.0 g/L的明胶溶液。冷却至室温后,将栀子蓝色素、栀子黄色素、胭脂虫红天然色素粉末分别加入到明胶溶液中,使明胶天然色素可食性墨水的表观黏度一致后(当剪切速率≥383 s-1),机械搅拌(350 r/min, 15 min)。参考张欢等[11]的方法将可食性墨水高速球磨4 h(每工作30 min间歇30 min,工作总时长4 h),球磨转速410 r/min,使其充分复合分散,制备得到明胶基可食性墨水。经过色素量(0.20、0.40、0.60、0.80、1.00 g/mL色素含量)、明胶量(0.5、1.0、2.0 g/L明胶水溶液)逐步优化并固定最优添加量后,加入不同体积分数的甘油[0.075%(体积分数)、0.1%(体积分数)和0.125%(体积分数)],机械搅拌(350 r/min, 15 min),随后高速球磨(410 r/min,球磨4 h)得到明胶基可食性墨水。
1.3.2 色差测定
以白色标准板为背景校正后,利用测色仪测定可食性墨水样品的L*(亮度值)、a*(红度值)、b*(黄度值)。每个可食性墨水样品平行测定5次取平均值,并计算色差ΔE。色差的计算如公式(1)所示[12-13]:
(1)
式中:ΔE,色差;ΔL*,Δa*,Δb*,被测样品与参考样品(1.0 g/L明胶水溶液L0= 93.52,a0=-0.63,b0=-2.47)之间亮度L*和色度指数a*,b*的差值。其中,ΔE<3,没有明显的差异;3<ΔE<6:非常微小的差异;6<ΔE<9,相当明显的差异;9<ΔE<12,显著的差异;ΔE>12,不同的颜色。
1.3.3 流变特性测定
使用MCR302流变仪探究可食性墨水样品的流变性,采用CP-50锥板(直径50 mm)、BC 12.7探头、间距 0.106 mm,测定可食性墨水的三阶段触变性、触变指数。
三阶段触变性测试(3 interval thixotropy test,3ITT):根据PENG等[13]描述的方法并进行一定的改变。在25 ℃下,样品先在0.01 s-1的恒定剪切速率下预剪切30 s。随后,第一阶段,通过剪切速率0.01 s-1对样品剪切20 s;第二阶段,利用剪切速率50 s-1对样品剪切20 s;第三阶段,采用剪切速率0.01 s-1对样品剪切20 s。触变恢复率的计算如公式(2)所示:
(2)
式中:R,触变恢复率,%;ηa,第三阶段的黏度值,mPa·s;ηb,第一阶段的黏度值,mPa·s。
触变指数:根据轻工QB/T 2625—2011《中性墨水圆珠笔和笔芯》,在25 ℃下,在恒定剪切速率4 s-1和40 s-1下[14]分别测定可食性墨水样品的表观黏度,记为η4和η40,计算如公式(3)所示:
(3)
式中:It,触变指数;η4,剪切速率在4 s-1时的表观黏度,mPa·s;η40,剪切速率在40 s-1时的表观黏度,mPa·s。以触变指数表征可食性墨水的假塑性,触变指数越大,假塑性越强。
1.3.4 傅里叶红外光谱(Fourier transform infrared spectrometer, FTIR)
取1~2 mg经过真空冷冻干燥后的可食性墨水样品,覆盖于红外光谱仪检测孔进行测定。扫描次数:32,分辨率4 cm-1,扫描范围600~4 000 cm-1。
1.3.5 冻融稳定性
不同明胶含量的新鲜可食性墨水样品置于-20 ℃冰箱中冷冻30 min,取出室温放置30 min,以此作为1次冻融循环。每次冻融循环后观察可食性墨水的外观并拍照记录。
1.3.6 沉降率(precipitation ratio,PR)
测量空离心管的质量记为m0,将不同明胶含量的可食性墨水样品置于10 mL离心管中称重,记为m。称重完毕后,离心10 min(4 000 r/min),取出上清液后再次称重,记为m1。PR的计算如公式(4)所示:
(4)
式中:m0,空离心管的质量,g;m,离心前样品与离心管的质量,g;m1,经离心取出上清液后样品与离心管的质量,g。
1.3.7 离心稳定性
将可食性墨水样品稀释1 000倍,使用紫外可见分光光度计测试稀释后样品在440、494、592 nm处吸光度,记为A;使用高速离心机,将上述稀释后样品离心15 min,转速1 000 r/min,随后取上清液分别在440、494、592 nm处测定吸光度,记为B。比吸光度(absorbance ratio,r)计算如公式(5)所示:
(5)
式中:A,离心前样品吸光度;B,离心后上清液吸光度。r越接近于100%,表示离心稳定性越好。
1.3.8 数据分析与处理
每组试验至少重复进行3次测试,获得的实验数据结果采用Microsoft Excel进行数据整理,并使用Origin pro 2022,SPSS进行数据处理、误差分析、图片绘制。
2 结果与分析
2.1 色素量的优化
2.1.1 色差的分析
以1.0 g/L Ge水溶液作为参考样品提供对照颜色参数L0、a0和b0,测定1.0 g/L Ge水溶液中色素不同添加量时的色差。可食墨水的色差分别随着Gb、Cc和Gy添加量的增加而增加,色差值最大时三者添加量均为0.80 g/mL。当添加量过高后,色差值降低,这可能是因为墨水体系中过量的色素发生聚集,从而形成了不稳定的分散体系,易产生大规模沉淀(图1-b)。总体而言,当色素添加量在0.60~0.80 g/mL时,3种可食墨水色差值变化平缓,具有较高的色彩呈现度,表明体系中Gb、Cc和Gy含量可能已经达到了饱和(图1-a),因此随后在色素添加量0.60~0.80 g/mL进一步优化。
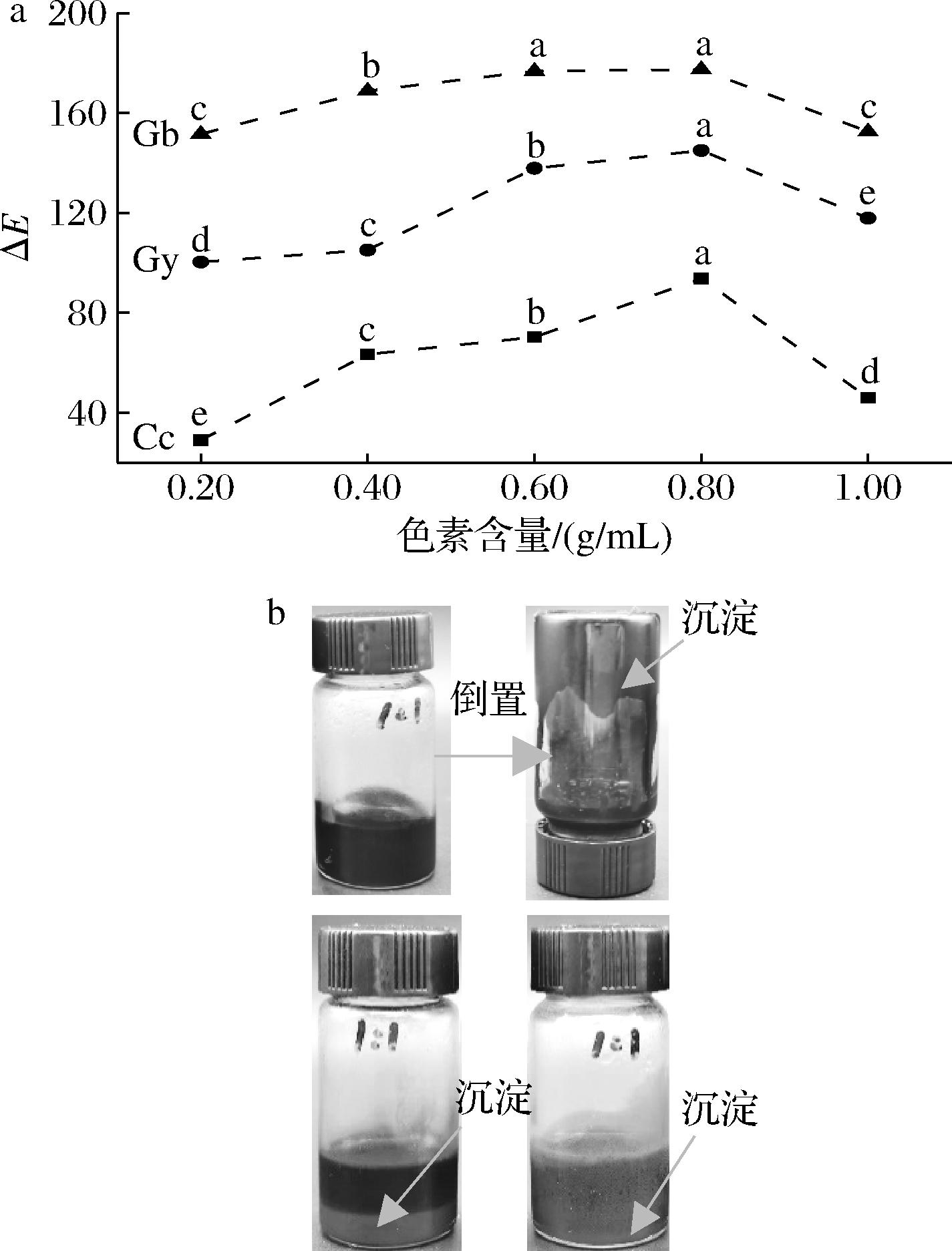
a-明胶基可食性墨水的ΔE;b-明胶基可食性墨水样品图
图1 明胶基可食性墨水ΔE和样品图
Fig.1 ΔE and sample chart of gelatin-based edible ink
2.1.2 3ITT的分析
对色素添加量0.60、0.65、0.70、0.75、0.80 g/mL时的可食墨水进行3ITT测试。在第一阶段(0.01 s-1),墨水黏度较高;第二阶段(50 s-1),高剪切速率减少分子链的缠结,促使样品黏度迅速降低,呈现剪切变稀的特性;第三阶段(0.01 s-1),墨水黏度恢复到一定程度,墨水结构已重新建立[15]。如图2所示,当Gb、Cc和Gy添加量分别为0.75、0.70、0.65 g/mL时,可食墨水的触变恢复率最高、触变性最好;触变恢复率约为75%、91%和66%。
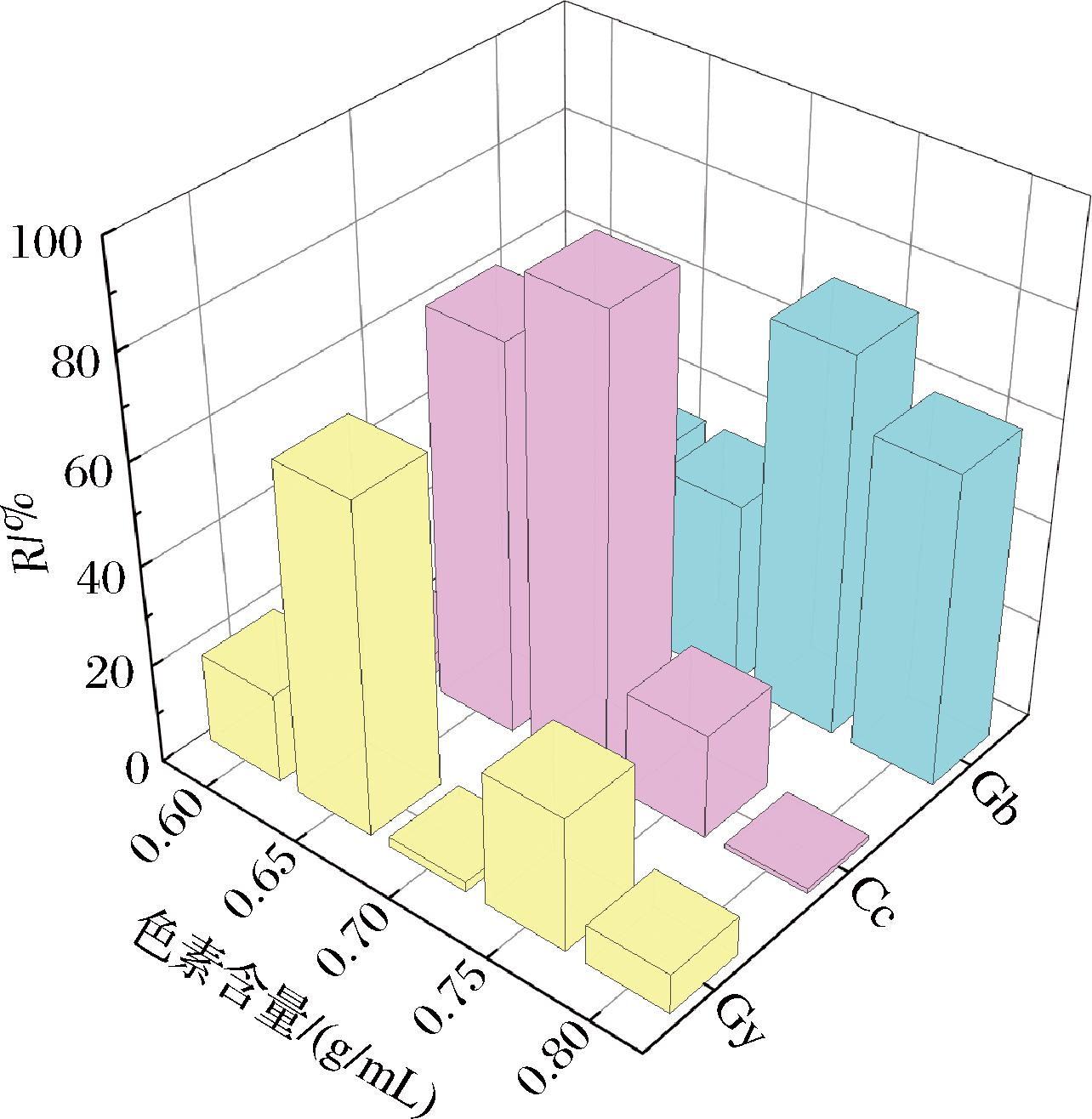
图2 明胶基可食墨水的触变恢复率
Fig.2 Thixotropic recovery rate of gelatin-based edible ink
综上所述,当明胶基墨水中含有0.75 g/mL Gb、0.70 g/mL Cc和0.65 g/mL Gy时,可食墨水体系具有较高的色彩呈现度、触变恢复率和打印适用性[16],固定此添加量作为后续研究的基础。
2.2 明胶量的优化
2.2.1 冻融稳定性
当可食墨水在冷冻或冷藏条件下进行贮存、运输、以及批发和零售过程中,良好的冻融稳定性有利于拓展可食墨水体系的应用场景和范围。由图3可见,0.5 g/L Ge水溶液负载的可食墨水无凝固现象,但部分有沉淀;明胶含量1.0 g/L时几乎无变化;明胶含量2.0 g/L的可食墨水反复冻融后出现凝固。因此,1.0 g/L Ge水溶液负载的可食墨水经过冷链贮运和货架期的温度波动后,可以正常应用,具有较高的冻融稳定性。

a-栀子蓝;b-胭脂虫红;c-栀子黄
图3 明胶基可食墨水栀子蓝、胭脂虫红和栀子黄的冻融稳定性
Fig.3 Freeze-thaw stability of gelatin-based edible Gb, Cc, and Gy ink
2.2.2 沉降率
沉降率在一定程度上可以反映明胶对胭脂虫红、栀子黄和栀子蓝色素的分散负载性。由图4可见,1.0 g/L Ge水溶液配制的可食墨水沉降率低于明胶含量0.5 g/L的可食墨水。是因为低浓度的明胶无法充分分散和负载体系中的色素,从而使未被明胶负载的色素离心后沉降于底部。因此,1.0 g/L Ge水溶液能够充分分散Gb、Cc和Gy,经高速离心仍能负载稳定,得到分散均匀的可食墨水。

图4 明胶基可食墨水的沉降率
Fig.4 Sedimentation rate of gelatin-based edible ink
综上所述,1.0 g/L Ge水溶液制备的可食性墨水体系具有较好的稳定性和分散特性,能克服低温凝固,在低浓度可有效分散和负载Gb、Cc和Gy,可以用于进行后续的实验。
2.3 可食性墨水的润滑性
2.3.1 离心稳定性
离心稳定性可以反映出可食墨水体系的物理稳定性。由图5可见,在一定范围内墨水离心稳定性随着甘油浓度的增加而逐渐增加。这可能是因为甘油中含有较多的羟基,能与水分子形成氢键,从而形成的一定厚度的水化层,增加墨水分散体系中分子运动时的内摩擦力,降低分子碰撞机率和沉降速率,提升体系的离心稳定性[17]。而当甘油体积分数超过0.1%时,离心稳定性有所降低。可能是过量甘油自身发生的聚集影响了墨水分散体系结构,使甘油在明胶和色素表面的吸附性降低,导致体系水化层厚度减少,聚合物的碰撞机率增加,因此更容易沉降,离心稳定性降低[18]。
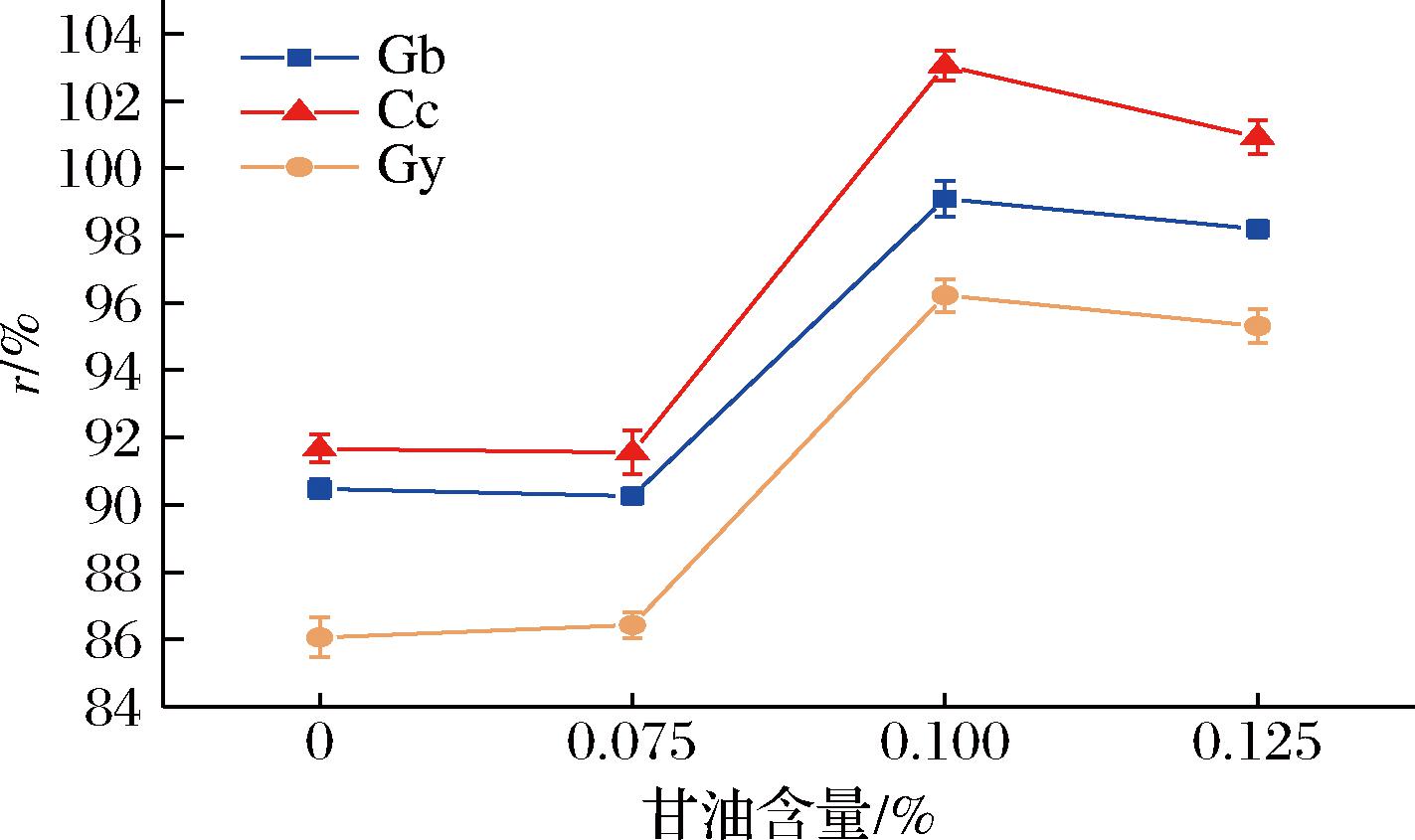
图5 明胶基可食性墨水的离心稳定性
Fig.5 Centrifugal stability of gelatin-based edible ink
2.3.2 触变指数
触变指数可以在一定程度上反映流体在剪切力作用下其结构被破坏后,重新恢复结构的能力[15,19]。通常,触变指数越大,表示触变性越好[14]。由图6可见,随着甘油含量增加可食墨水的触变指数(4 s-1与40 s-1黏度比值)逐渐增加,是由于甘油中含有羟基,甘油分子可以诱导较强的氢键缔合作用,在体系中原有的网络结构上产生附加的架桥作用,增强了体系的触变性[19]。但甘油体积分数超过0.1%时,可食墨水触变指数变小,这是因为用于架桥的甘油过量,多余的—OH使明胶分子支链溶剂化而破坏稳定的网络结构[19],削弱了体系的触变性。
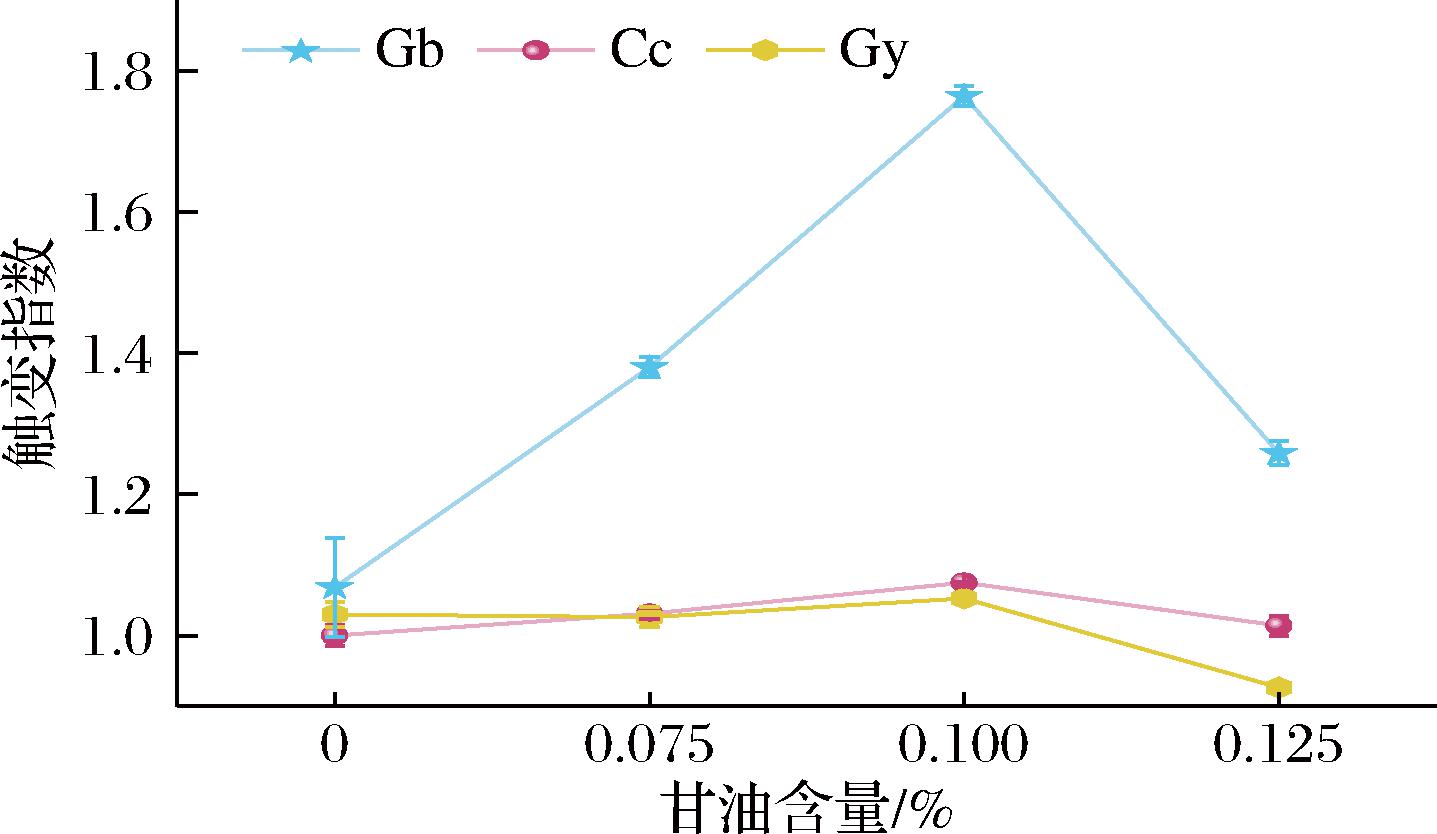
图6 明胶基可食墨水的触变指数
Fig.6 Thixotropic index of gelatin-based edible ink
综上所述,当甘油体积分数为0.1%时,明胶基可食性墨水体系的离心稳定性和触变指数最佳,甘油分子诱导氢键的缔合作用,可以保证可食性墨水体系实际应用时的书写体验。将此条件下的三色明胶基可食墨水分别灌装入空马克笔中进行实际书写,书写基材包括纸张和食品。由图7可知,三色明胶基可食性墨水实际在绘画时清晰明亮、呈色鲜活,书写文字时润滑流畅,具有较高的书写绘画、食品装饰和食品DIY的潜力。

a-明胶基可食性墨水马克笔在纸张和食品表面手绘和书写表现;b-马克笔绘画过程
图7 明胶基可食墨水马克笔在纸张和食品表面手绘和书写表现和绘画过程
Fig.7 Hand-drawn and written expression on paper and foods surfaces and painting process of the marker pen made of gelatin-based edible ink
3 结论
本文利用色差、3ITT测试分析得到三色明胶基可食墨水中Gb、Cc和Gy的最优添加量分别为0.75、0.70、0.65 g/mL;分析冻融稳定性、沉降率,得到明胶基可食墨水的最优明胶添加量为1.0 g/L;最终通过离心稳定性、触变指数确定明胶基可食墨水甘油添加量为0.1%(体积分数)时体系分散性最好,有利于其实际的食品工业应用。因此,以明胶为连接料、水溶性天然色素(Gb、Cc、Gy)为色料、甘油为助剂可制备性质稳定的三色明胶基可食墨水,最优配方的墨水借助马克笔在纸张和食材表面实际绘画时呈色鲜活,书写文字时润滑流畅,具备书写绘画、食品表面装饰和食品创意DIY的潜力,为其应用于食品工业提供了参考。
[1] SHANKAR S, WANG L F, RHIM J W.Effect of melanin nanoparticles on the mechanical, water vapor barrier, and antioxidant properties of gelatin-based films for food packaging application[J].Food Packaging and Shelf Life, 2019, 21:100363.
[2] 刘维维, 马良, 张宇昊, 等.明胶-葡萄皮红色素基可食性油墨的制备及应用[J].食品与发酵工业, 2022, 48(18):121-127.LIU W W, MA L, ZHANG Y H, et al.Preparation and application of gelatin-rape skin red pigment based edible inks[J].Food and Fermentation Industries, 2022, 48(18):121-127.
[3] 刘兰香, 伊冠东, 李凯, 等.Al3+荧光增敏快速检测酸奶和乳酸菌饮料中的胭脂虫红酸[J].食品科学, 2020, 41(2):306-314.LIU L X, YI G D, LI K, et al.Rapid detection of carminic acid in yogurt and Lactobacillus-containing beverage by Al3+-based fluorescence enhancement[J].Food Science, 2020, 41(2):306-314.
[4] GONZ LEZ E A, GARC
LEZ E A, GARC A E M, NAZARENO M A.Free radical scavenging capacity and antioxidant activity of cochineal (Dactylopius coccus C.) extracts[J].Food Chemistry, 2010, 119(1):358-362.
A E M, NAZARENO M A.Free radical scavenging capacity and antioxidant activity of cochineal (Dactylopius coccus C.) extracts[J].Food Chemistry, 2010, 119(1):358-362.
[5] RAHAIEE S, MOINI S, HASHEMI M, et al.Evaluation of antioxidant activities of bioactive compounds and various extracts obtained from saffron (Crocus sativus L.):A review[J].Journal of Food Science and Technology, 2015, 52(4):1881-1888.
[6] LI M X, TIAN X Y, LI X L, et al.Anti-fatigue activity of gardenia yellow pigment and Cistanche phenylethanol glycosides mixture in hypoxia[J].Food Bioscience, 2021, 40:100902.
[7] WANG J S, YE Q, YU N X, et al.Preparation of multiresponsive hydrophilic molecularly imprinted microspheres for rapid separation of gardenia yellow and geniposide from gardenia fruit[J].Food Chemistry, 2022, 374:131610.
[8] ZIELINSKI A A F, DEL PILAR SANCHEZ-CAMARGO A, BENVENUTTI L, et al.High-pressure fluid technologies:Recent approaches to the production of natural pigments for food and pharmaceutical applications[J].Trends in Food Science &Technology, 2021, 118:850-869.
[9] HOBBS C A, KOYANAGI M, SWARTZ C, et al.Genotoxicity evaluation of the naturally-derived food colorant, gardenia blue, and its precursor, genipin[J].Food and Chemical Toxicology, 2018, 118:695-708.[10] SANZ T, FALOMIR M, SALVADOR A.Reversible thermal behaviour of vegetable oil cellulose ether emulsions as fat replacers.Influence of glycerol[J].Food Hydrocolloids, 2015, 46:19-27.
[11] 张欢, 戴宏杰, 陈媛, 等.离子液体-球磨法制备柠檬籽纤维素纳米纤丝及其结构表征[J].食品科学, 2021, 42(7):120-127.ZHANG H, DAI H J, CHEN Y, et al.Preparation and structure characterization of lemon seed cellulose nanofibrils using ionic liquid-assisted ball milling[J].Food Science, 2021, 42(7):120-127.
[12] WANG G N, HUANG S Y, HE H, et al.Fabrication of a “progress bar” colorimetric strip sensor array by dye-mixing method as a potential food freshness indicator[J].Food Chemistry, 2022, 373:131434.
[13] PENG L, WANG H X, DAI H J, et al.Preparation and characterization of gelatin films by transglutaminase cross-linking combined with ethanol precipitation or Hofmeister effect[J].Food Hydrocolloids, 2021, 113:106421.
[14] 张新毅. 中性墨水配方设计及性能评价[D].太原:太原理工大学, 2019.ZHANG X Y.Formulation design and performance evaluation of gel ink[D].Taiyuan:Taiyuan University of Technology, 2019.
[15] CHENG Y, FU Y, MA L, et al.Rheology of edible food inks from 2D/3D/4D printing, and its role in future 5D/6D printing[J].Food Hydrocolloids, 2022, 132:107855.
[16] WANG H X, CHENG Y, ZHU J C, et al.High temperature induced stable gelatin-gardenia blue system with hyperchromic effect and its food application in 2D writing/printing and 3D printing[J].Food Chemistry, 2023, 401:134119.
[17] 宋亚伟, 房宽峻, 蔡玉青, 等.喷墨印花用纳米色素分散液稳定性研究[J].染整技术, 2016, 38(4):20-22.SONG Y W, FANG K J, CAI Y Q, et al.Study on the stability of nano-colorant dispersions for inkjet printing[J].Textile Dyeing and Finishing Journal, 2016, 38(4):20-22.
[18] KHAZAEI N, ESMAIILI M, DJOMEH Z E, et al.Characterization of new biodegradable edible film made from basil seed (Ocimum basilicum L.) gum[J].Carbohydrate Polymers, 2014, 102:199-206.
[19] 张瑞东, 刘守军.水溶性低碳醇对中性墨水触变指数的影响[J].中国制笔, 2008(2):6-8.ZHANG R D, LIU S J.Lower alcohol of water-solubilitty influence to thixotropic index of gel-ink[J].China Writing Instruments, 2008(2):6-8.