黄酒,是以稻米、黍米、小米等淀粉含量高、蛋白质含量较低的谷物为主要原料,经加曲或部分酶制剂、酵母等糖化发酵剂酿造而成的发酵酒(GB/T 13662—2018《黄酒》),其发酵过程中产生的香气主要是由酒曲和酿酒环境中的各种微生物产生的[1]。黄酒发酵过程中会产生不同数量的高级醇、脂肪酸、醛、脂类等[2],并且伴随着水自缔合、与醇缔合及与其他代谢产物的交叉缔合的复杂氢键缔合作用[3]。其中在发酵过程中醇、水氢键缔合的团簇结构变化与酒的刺激和醇厚感紧密相关,对发酵酒的最终风味有重要影响[4]。因此,黄酒酿造中发酵过程的监测显得尤为重要。
在对黄酒发酵过程监测研究方面,PENG等[5]采用GC-MS技术比较了黄酒在后发酵过程中代谢产物的差异,发现不同发酵工艺过程对黄酒风味有重要影响。陈青柳等[6]应用HPLC和GC-MS联用对黄酒中的风味物质进行了动态监测。孙乐平等[7]通过顶空固相微萃取和气相色谱质谱法定量分析了燕麦黄酒发酵过程中高等醇类的变化,并与发酵过程中微生物群落变化进行了关联。这些方法具有高通量、高精度等优势,然而往往需要复杂的分析步骤,抑或是成本较高,在实际生产监测中的应用受到一定的限制。
作为一种快速分析和非破坏性的技术,低场核磁共振(low-field nuclear magnetic resonance,LF-NMR)在研究复杂基质中的水和脂类方面有一定优势,可以根据氢质子在基质中的流动性来区分和描述质子群。目前LF-NMR技术已在部分发酵食品的品质分析中有一定应用[8],如糯米[9]、发酵香肠[10]、纳豆[11]等食品的监测。虽然已有对葡萄酒T2弛豫特性的研究报道[12],但应用低场核磁共振技术对黄酒的研究还相对较少。因此,本文对黄酒酿造过程中5个关键工艺阶段的样品进行了分析,在比较了不同酒精度、陈酿时间和品牌的黄酒的LF-NMR弛豫特性的基础上进行了主成分分析,以探究LF-NMR在监测黄酒发酵过程和辨别不同黄酒类别的可行性。
1 材料与方法
1.1 材料与试剂
不同发酵阶段(浸米、第一次发酵、第二次发酵、煎酒及3年陈酿)的黄酒样品由黄酒生产企业提供;18个市售黄酒样品(A~I)均为经检验后的市场抽样产品,样品真实有效;去离子水由实验室自制。
1.2 仪器与设备
LF-NMR核磁共振分析仪(PQ001,磁场强度(0.5±0.08) T,共振频率21.3 MHz,配套T-Invfit反演拟合软件和Φ15 mm核磁试管),上海纽迈电子科技有限公司;HH·S21恒温水浴锅,上海博讯实业有限公司。
1.3 实验方法
以去离子水为对照,对经过浸米、第一次发酵(发酵1)、第二次发酵(发酵2)、煎酒的样品和3年陈酿的黄酒进行LF-NMR弛豫特性分析;以B品牌酒精度分别12%vol、13%vol和14%vol的8年陈酿黄酒为对象,比较酒精度对LF-NMR弛豫特性的影响;选取品牌B及H(酒精度14%vol,陈酿时间5、8年),品牌F(酒精度15%vol,陈酿时间6、8年)的黄酒,研究陈酿时间对LF-NMR弛豫特性的影响;对品牌C和I(3年陈,13%vol)、品牌B和H(5年陈,14%vol;8年陈,13%vol;8年陈,14%vol)的黄酒LF-NMR弛豫特性进行比较。最后对9个品牌18个黄酒样品进行主成分分析,黄酒样品信息见表1。
表1 黄酒样品信息
Table 1 Information of Huangjiu samples

产地类别样品酒精度/%vol陈酿时间/年绍兴半甜型花雕酒A123123128138绍兴半甜型花雕酒B148148145绍兴半干型加饭酒C133绍兴半甜型花雕酒D125绍兴半甜型花雕酒E1310绍兴半甜型花雕酒F156158嘉善半甜型花雕酒G1210145上海半干型加饭酒H 148138上海半干型加饭酒I1331410
取3 mL样品于核磁管中,32 ℃水浴10 min后置于核磁探头中稳定1 min,选择CPMG序列,检测参数为:采样频率(sampling frequency,SW)为250.0 kHz、重复采样等待时间(time of repetition,TR)为20 000 ms、重复扫描次数(number of repeat scans,NS)为4次、半回波时间(τ)为500 μs、回波个数(echo count,EC)为16 000个、采样点数(sampling number,TD)为4 000 126个(当SW、τ、EC三者确定后,此值可自动确定)。检测时室温:23.7 ℃、湿度:50%。应用T-invfit软件进行单/多组分反演拟合,可得到样品的单组分弛豫时间(T2W),多组分弛豫时间T2i(i=1,2…)、信号幅值及峰面积比例S2i(i=1,2…)等核磁信息。
样品设置3个平行及3次重复,以确保结果的可靠性。
1.4 数据分析处理
应用SPSS 23.0软件对反演拟合获得的5个变量(T2 W、T21、T22、S21、S22)数据进行数据处理和主成分分析(principal component analysis,PCA)。使用ANOVA方差分析和Duncan事后检验,P<0.05时为显著性差异。应用Origin 9.0软件对数据进行绘图分析。
2 结果与分析
2.1 不同酿造阶段样品的LF-NMR弛豫特性
2.1.1 单组分弛豫(T2W)特性
T2W可以反映样品在发酵过程中弛豫特性的整体变化,不同酿造阶段黄酒样品的单组分弛豫时间(T2W)结果如图1所示。
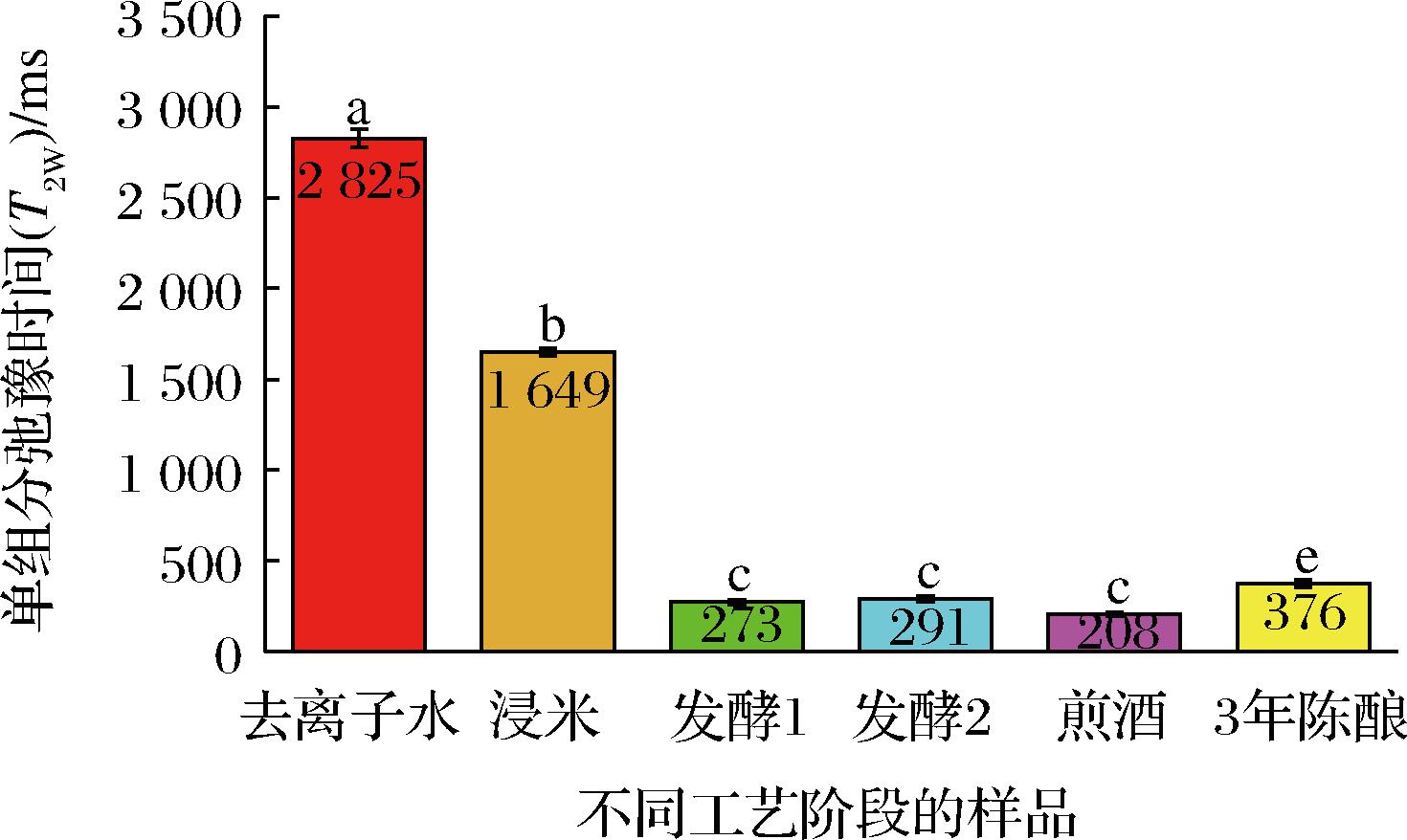
图1 不同酿造阶段样品的单组分弛豫时间(T2W)
Fig.1 The single component relaxation time (T2W) of samples at different brewing stage
注:不同小写字母表示差异显著(P<0.05)(下同)。
图1表明,与去离子水的T2W(2 825 ms)相比,浸米阶段样品的T2W显著降低1 176 ms(P<0.05),这是由于浸入米料后,体系中含有了丰富的氨基酸和其他有机物质,增加了体系中氨基酸态氮、酯类物质与有机酸的含量[13]。第一次发酵后样品的T2W进一步从1 649 ms显著缩短至273 ms,说明发酵过程中产生的醇、氨基酸等物质使样品中氢质子的束缚力相对增强[14]。经过第二次发酵及煎酒后的样品的T2W无显著变化,而经过3年陈酿后样品的T2W又显著长于煎酒后的样品,说明新酿制黄酒体系不够稳定,陈酿过程中随酸与醇酯化反应的进行,黄酒的酒精度降低,而挥发酯含量增加,总体表现为体系中氢质子的束缚力相对减弱。根据LI等[15]对黄酒发酵过程的研究,陈酿可赋予黄酒和谐宜人的香味,在此过程中体系中的氢键缔合作用也发生了改变。
2.1.2 多组分弛豫(T2)特性
不同酿造阶段的黄酒样品的多组分弛豫(T2)图谱如图2所示。将位于100~1 000 ms的弛豫峰命名为T21峰,大于1 000 ms的弛豫峰命名为T22峰,将其多组分弛豫时间(T21, T22)及峰面积比例(S21, S22)的变化情况列于表2。
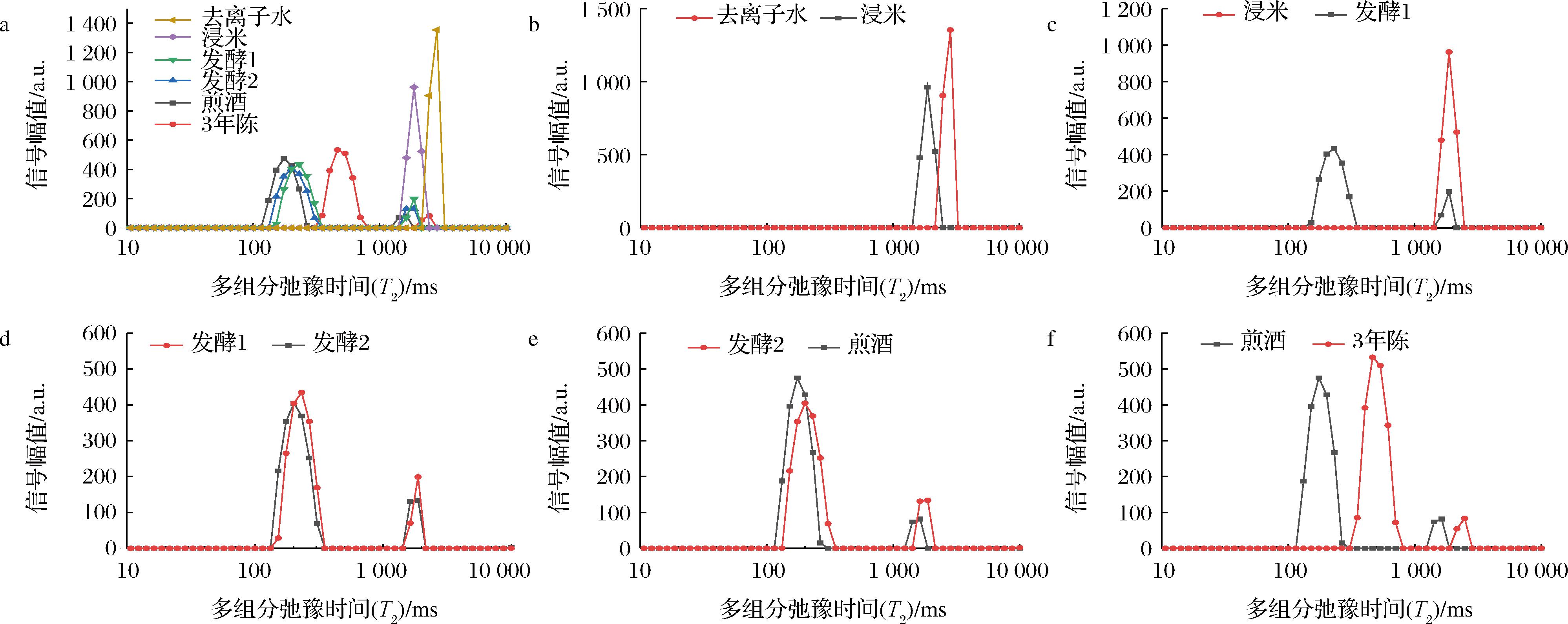
a-各阶段的总体情况;b-去离子水和浸米的样品;c-浸米和发酵1的样品;d-发酵1和发酵2的样品;e-发酵2和煎酒的样品;f-煎酒和3年陈黄酒的样品
图2 不同酿造阶段样品的多组分弛豫图谱(T2)
Fig.2 The multi-component relaxation profiles (T2) of samples at different brewing stage
表2 黄酒发酵过程中的多组分弛豫信息
Table 2 The multi-component relaxation characteristics of Huangjiu

样品酒精度/%volT21/msS21/%T22/msS22/%去离子水/002 009±16100±0浸米/001 221±12100±0发酵115132±386.20±0.741 386±1513.80±0.74发酵218126±086.30±0.031 317±613.70±0.03煎酒18114±085.11±0.081 232±014.8±0.0893年陈17242±592.42±0.101 908±957.58±0.10
由图2-a可知,发酵过程中样品的T2多组分弛豫图谱变化明显。为了更清晰地分析,对相邻2个发酵阶段的T2多组分弛豫图谱进行对比,结果如图2-b~图2-f所示。
图2-b表明,虽然浸米后样品与去离子水的多组分弛豫图谱都表现为一个弛豫峰,且峰形类似,但浸米后样品的弛豫时间更短,由2 009 ms缩短到1 221 ms(表2)。这是由于加米浸泡后体系中含有丰富的营养物质[16],如有机酸、氨基酸、蛋白质、淀粉、糖和维生素等,这些都会增强对样品中水分子的束缚作用,影响到水的氢键缔合[17],体系的布朗运动相对减弱,氢质子的弛豫加快,使其弛豫时间缩短。
由图2-c可知,与浸米阶段的样品相比,经过第一次发酵后的样品的T2多组分弛豫特性发生了显著改变,表现为峰数量的增加和信号幅值的相对降低,该阶段样品呈现2个弛豫峰,其中,新增的弛豫峰位于132 ms处(表2),且所占峰面积比例达到了86.2%,说明该部分氢质子是体系中主要的组成部分,T22峰的弛豫时间也缩短至1 386 ms,S22仅为13.8%。YANG等[18]的研究表明,经过第一次发酵后体系中会形成多种醇类、醛类、酸类、酯类等物质,体系变得更加复杂且会对体系中氢键的缔合产生影响,这与弛豫峰的增加密切相关。
由图2-d可知,与第一次发酵的样品相比,经第二次发酵后的样品也表现为两个弛豫峰,峰形类似,信号幅值略有降低;但弛豫峰相对左移,弛豫时间从132 ms缩短至126 ms(表2),但该峰面积比例几乎无变化(86.3%),T22峰进一步缩短至1 317 ms。经第二次发酵后体系中的醇、酸、酚、酯等物质的种类和含量均相对增加[19],从而使样品中氢质子所受束缚作用增强、弛豫加快。
图2-e中,与第二次发酵相比,煎酒后的样品亦呈现两个弛豫峰,但其分布进一步左移,弛豫时间分别缩短至114 ms和1 232 ms,S21略有减小(85.1%)。这可能是由于煎酒的温度为(90±1) ℃,相对高的温度促进体系中物质的溶解和转变,使物质间的氢键缔合作用进一步增强[16],体系中氢质子所受束缚作用进一步增强,表现为弛豫时间的缩短。
由图2-f可知,与煎酒后的样品相比,经过3年陈酿的黄酒的多组分弛豫仍为2个弛豫峰,但其分布相对右移,弛豫时间相对延长至242 ms和1 908 ms,S21有明显增加(92.4%)。这是由于陈酿贮存期间,微生物作用和化学反应仍在缓慢进行,醇类、酸类、酚类、酯类等物质的含量会发生变化,风味特征得到增强,这也会导致陈酿时的氢键缔合不同于酿造过程中的氢键缔合[20]。随陈酿时间的延长,醇类及易挥发的一些物质的含量相对减少。这使样品中氢质子所受束缚作用相对减弱,弛豫时间延长。
2.2 不同酒精度黄酒的LF-NMR弛豫特性
同一品牌不同酒精度的黄酒样品的LF-NMR弛豫特性如图4所示。
由图3-a可知,随酒精度从12%vol增加至14%vol,黄酒的T2W从376 ms缩短至307 ms(P<0.05)。图3-b中,随酒精度的增加,样品的弛豫分布左移,T21和T22均相对缩短。酒精度的增加意味着体系中乙醇分子的增多,这会使氢质子在溶液中的运动受限[21]。刘敏等[22]的研究亦发现,水-乙醇体系中乙醇浓度的增加会加快氢质子的弛豫。KIRSCHNER等[23]的研究发现,乙醇摩尔分数的增加会使体系中分子的表面密度增加,氢键缔合更加紧密。因此,同一品牌和陈酿时间下,随酒精度的增加,样品的T2 W、T21和T22均相对缩短。
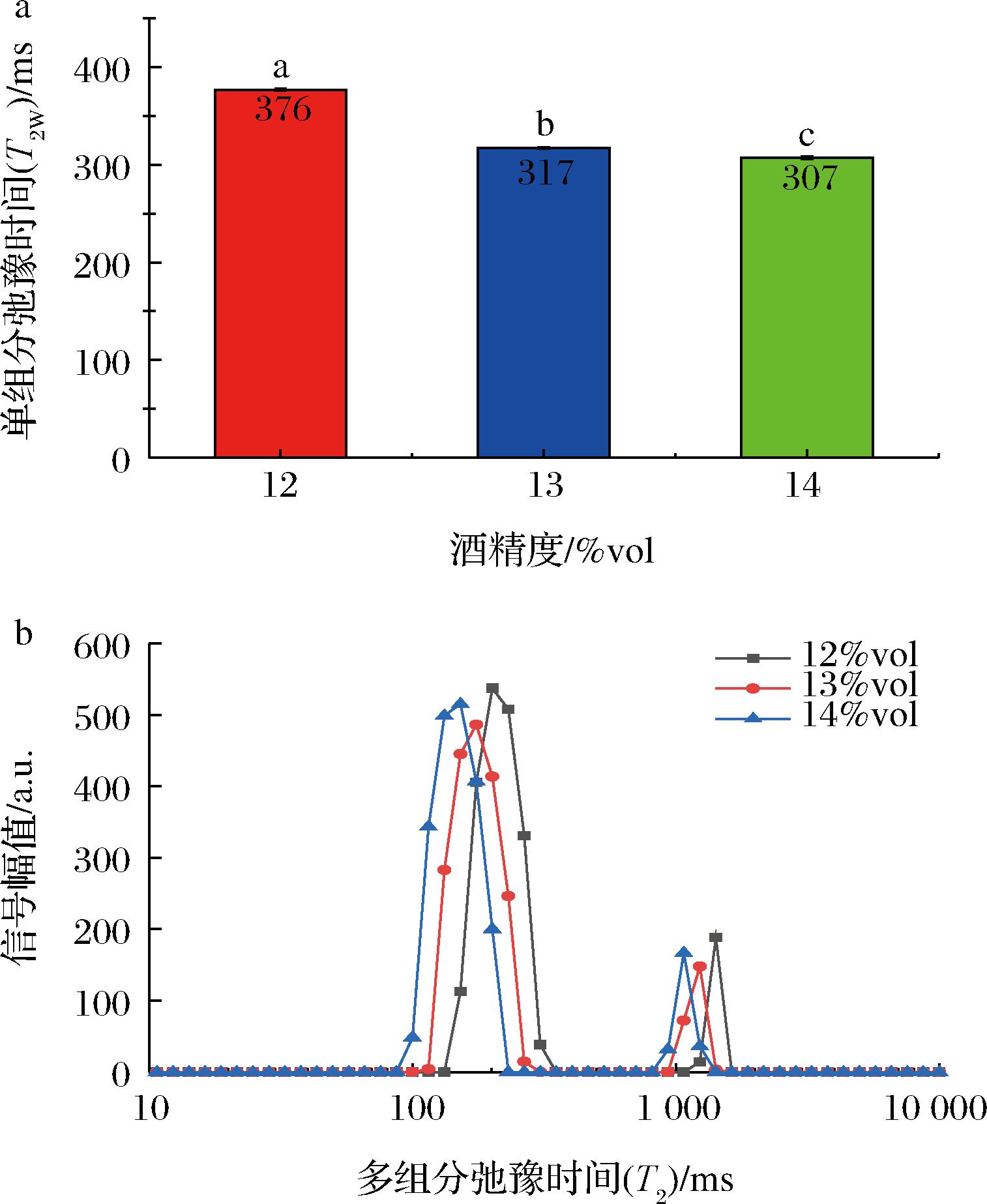
a-单组分弛豫时间;b-多组分弛豫分布
图3 不同酒精度黄酒的单组分弛豫时间和多组分弛豫分布
Fig.3 Single-component relaxation time and multi-component relaxation distribution of Huangjiu with different alcoholicity
2.3 不同陈酿时间黄酒的LF-NMR弛豫特性
同一品牌不同陈酿时间的黄酒样品的LF-NMR弛豫特性比较如表3所示。
表3 不同陈酿时间黄酒的LF-NMR弛豫特性
Table 3 LF-NMR relaxation characteristics of Huangjiu after different aging years
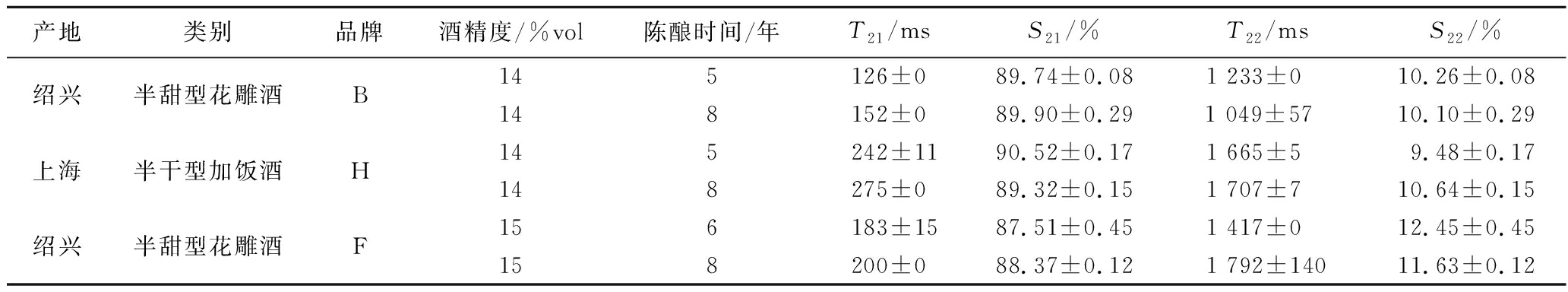
产地类别品牌酒精度/%vol陈酿时间/年T21/msS21/%T22/msS22/%绍兴半甜型花雕酒B145126±089.74±0.081 233±0 10.26±0.08148152±089.90±0.291 049±57 10.10±0.29上海半干型加饭酒H145 242±1190.52±0.171 665±5 9.48±0.17148275±089.32±0.151 707±7 10.64±0.15绍兴半甜型花雕酒F156 183±1587.51±0.451 417±0 12.45±0.45158200±088.37±0.121 792±14011.63±0.12
由表3可知,陈酿时间对黄酒的T2弛豫特性的影响较小。同一品牌的黄酒,当酒精度相同时,陈酿年份较长的黄酒表现出较大的T21,而T22、S21和S22的变化不大。这可能是由于,随着陈酿时间的增加,黄酒中发生了包括氧化、酯化、水解和挥发等物理化学反应,使酒的陈香增加[15],但由于乙醇浓度对体系中醇水缔合作用的影响更为明显,本部分中酒精度相同,故整体上表现为对体系中氢质子的自由度影响较小,仅T21相对延长。
2.4 不同品牌黄酒的LF-NMR弛豫特性
4组不同品牌,同一酒精度、陈酿时间的黄酒样品的LF-NMR弛豫特性比较结果如图4所示。

a-3年陈,13%vol;b-5年陈,14%vol;c-8年陈,13%vol;d-8年陈,14%vol
图4 不同品牌黄酒的多组分弛豫分布(T2)
Fig.4 The multi-component relaxation profiles (T2) of Huangjiu from different brands
由图4-a~图4-d可知,黄酒的多组分弛豫分布峰形相似,但不同品牌间有所区分。在同一酒精度和陈酿时间下,如图4-a,品牌I和C均为加饭酒,但产地不同,品牌I的弛豫分布较品牌C右移。而图4-b~图4-d中,品牌B和H的黄酒类型及产地均不同,即使酒精度和陈酿时间相同,品牌B的弛豫分布均较H左移。这一对比说明,对于同一酒精度和陈酿时间的黄酒,不同品牌黄酒酿造工艺的区别也会使其LF-NMR弛豫特性有所差异。
2.5 不同品牌黄酒的主成分分析
对9个品牌18个黄酒样品共54个样本的LF-NMR弛豫信息进行标准化及主成分分析,提取主成分1(PC1)和主成分2(PC2),主成分表达式分别如下,累计贡献值达到96%,即2个主成分保留了96%的原始数据信息,能很好的反映所有变量的原有信息[24],主成分分析结果如图5所示。
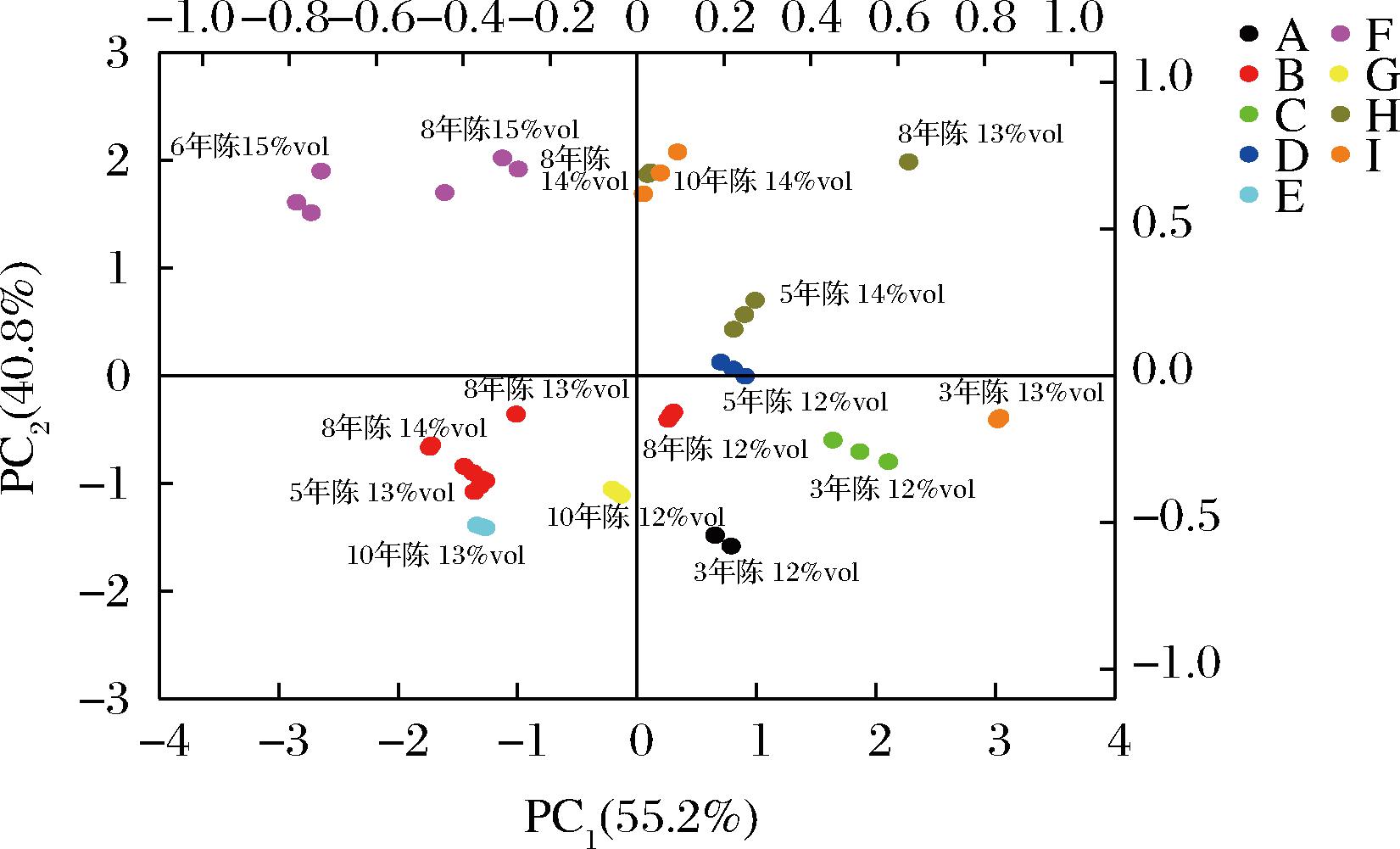
图5 不同品牌黄酒的PC1和PC2得分图
Fig.5 PC1 and PC2 scores of different Huangjiu brands
F1=0.39T21+0.56S21- 0.48T22-0.55S22
F2=0.60T21-0.43S21+0.51T22+0.44S22
由图5可知,不同品牌黄酒的分布有明显区别。这是由于不同品牌黄酒所选用的原料、酿造工艺和黄酒类型有一定的区别[2],这都会对样品的弛豫特性产生影响,从而反映为在主成分分布图的区别。A、C、D、E、G品牌的黄酒样品具有相同的酒精度及陈酿时间,故分布相对集中,而B品牌中,酒精度及陈酿时间都有一定变化,故PCA分布上也有一定区分,8年陈12%vol的黄酒分布于第四象限,其余样品均分布于第三象限,但总体与其他品牌可区分;F品牌的2个陈酿时间的黄酒则位于第二象限,陈酿时间上亦可区分;类似的,H品牌则均分布于图第一象限;I品牌的分布位于图的右上方,其中8年陈14%vol的黄酒由于和H品牌酒精度相同,产地均为上海且两者陈酿时间相近,因此分布较为接近。这说明基于黄酒的LF-NMR弛豫特性和PCA分析可以区分来源于不同生产企业的黄酒产品,且酒精度及陈酿时间也会影响其分布。
3 结论
本文重点探索了基于低场核磁共振技术进行黄酒发酵进程监测及品牌区分的可行性。研究发现,黄酒酿造过程中样品的LF-NMR特性有明显改变。发酵使黄酒的单组分弛豫时间(T2W)显著缩短,而陈酿则会使T2W稍有延长。发酵后样品的T2图谱均呈典型双峰特征,且在发酵过程中弛豫时间相对缩短,陈酿过程会使弛豫时间相对延长。同一品牌及陈酿时间的黄酒,酒精度越高,体系的单组分及多组分时间均越小;陈酿时间对弛豫特性影响较小,同一品牌及酒精度下,陈酿时间仅对T21有一定影响。不同品牌黄酒因酿造工艺的区别而使弛豫分布有一定特点。通过主成分分析可以挖掘黄酒的LF-NMR弛豫信息,实现对不同工艺生产的各品牌黄酒的快速辨别。研究也为后期LF-NMR技术在食品发酵领域的应用提供了一定参考。
[1] 陈麒名, 冯霞, 张蓓蓓, 等.中国黄酒的微生物多样性与风味的研究进展[J].食品与发酵科技, 2021, 57(6):77-82.
CHEN Q M, FENG X, ZHANG B B, et al.Research progress on microbial diversity and flavor of Chinese rice wine[J].Food and Fermentation Sciences &Technology, 2021, 57(6):77-82.
[2] CHEN G M, HUANG Z R, WU L, et al.Microbial diversity and flavor of Chinese rice wine (Huangjiu):An overview of current research and future prospects[J].Current Opinion in Food Science, 2021, 42:37-50.
[3] 刘敏. 低场核磁共振技术(LF-NMR)在酿造酒品质检测中的应用[D].上海:上海理工大学, 2014.
LIU M.Assessment of brewing wine quality by LF-NMR[D].Shanghai:University of Shanghai for Science and Technology, 2014.
[4] NOSE A, MURATA T, HAMAKAWA Y, et al.Effects of solutes on the alcohol-stimulative taste of vodkas[J].Food Chemistry, 2021, 340:128160.
[5] PENG Q, MENG K, ZHENG H J, et al.Metabolites comparison in post-fermentation stage of manual (mechanized) Chinese Huangjiu (yellow rice wine) based on GC-MS metabolomics[J].Food Chemistry:X, 2022, 14:100324.
[6] 陈青柳, 刘双平, 唐雅凤, 等.绍兴机械黄酒发酵过程中风味物质变化[J].食品科学, 2018, 39(14):221-228.
CHEN Q L, LlU S P, TANG Y F, et al.Changes in flavor components during fermentation process of mechanically produced Shaoxing rice wine[J].Food Science, 2018, 39(14):221-228.
[7] 孙乐平, 张伟, 徐嘉良, 等. 燕麦黄酒发酵过程中微生物群落结构变化及对高级醇的影响[J]. 食品科学技术学报, 2020, 38(1):43-52;59.
SUN L P, ZHANG W, XU J L, et al. Changes of microbial community structure and effects on higher alcohols in oat Huangjiu fermentation process[J]. Journal of Food Science and Technology, 2020, 38(1):43-52;59.
[8] 郭启悦, 李烨, 任舒悦, 等.低场核磁共振技术在食品安全快速检测中的应用[J].食品安全质量检测学报, 2019, 10(2):380-384.
GUO Q Y, Ll Y, REN S Y, et al.Application of low field nuclear magnetic resonance technology in food safety rapid detection[J].Journal of Food Safety &Quality, 2019, 10(2):380-384.
[9] LI T, TU C H, RUI X, et al.Study of water dynamics in the soaking, steaming, and solid-state fermentation of glutinous rice by LF-NMR:A novel monitoring approach[J].Journal of Agricultural And Food Chemistry, 2015, 63(12):3261-3270.
[10] ZHANG Q Q, LI W, LI H K, et al.Low-field nuclear magnetic resonance for online determination of water content during sausage fermentation[J].Journal of Food Engineering, 2017, 212:291-297.
[11] WU J, LI Y R, GAO X S.Monitoring a typical fermentation process of natto by low-field nuclear magnetic resonance (LF-NMR) and magnetic resonance imaging (MRI) techniques[J].Analytical Methods, 2016, 8(39):7135-7140.
[12] 李彦, 刘青, 蹇华丽, 等.葡萄酒的低场核磁共振弛豫谱[J].中山大学学报(自然科学版), 2012, 51(5):45-49.
LI Y, LIU Q, JIAN H L, et al.Low-field NMR relaxation spectrum of wine[J].Acta Scientiarum Naturalium Universitatis Sunyatseni, 2012, 51(5):45-49.
[13] 魏桃英, 汪钊.黄酒酿造新工艺研究[J].发酵科技通讯, 2018, 47(3):175-179.
WEl T Y, WANG Z.Study on new technology of yellow wine[J].Bulletin of Fermentation Science and Technology, 2018, 47(3):175-179.
[14] 黄河, 黄婷, 王媚, 等.新型黄酒发酵工艺条件优化[J].中国酿造, 2022, 41(7):179-184.
HUANG H, HUANG T, WANG M, et al.Optimization of the fermentation process conditions of new-type Huangjiu[J].China Brewing, 2022, 41(7):179-184.
[15] LI M, ZHAN P, WANG P, et al.Characterization of aroma-active compounds changes of Xiecun Huangjius with different aging years based on odor activity values and multivariate analysis[J].Food Chemistry, 2023, 405(Part A):134809.
[16] 朱长满. 煎酒对客家黄酒品质及其抗氧化活性的影响[D].广州:仲恺农业工程学院, 2019.
ZHU C M.Effect of decoction process on the quality and antioxidant activity of hakka rice wine[D].Guangzhou:Zhongkai University of Agriculture and Engineering, 2019.
[17] GONG M, ZHOU Z L, JIN J S, et al.Effects of soaking on physicochemical properties of four kinds of rice used in Huangjiu brewing[J].Journal of Cereal Science, 2020, 91:102855.
[18] YANG Y J, HU W Y, XIA Y J, et al.Flavor formation in chinese rice wine (Huangjiu):Impacts of the flavor-active microorganisms, raw materials, and fermentation technology[J].Frontiers in Microbiology, 2020, 11:580247.
[19] LIU H L, SUN B G.Effect of fermentation processing on the flavor of Baijiu[J].Journal of Agricultural and Food Chemistry, 2018, 66(22):5425-5432.
[20] JIA W, MA R T, HU L B, et al.Synergy of physicochemical reactions occurred during aging for harmonizing and improving flavor[J].Food chemistry:X, 2023, 17:100554.
[21] JORA M Z, CARDOSO M V C, SABADINI E.Correlation between viscosity, diffusion coefficient and spin-spin relaxation rate in 1H NMR of water-alcohols solutions[J].Journal of Molecular Liquids, 2017, 238:341-346.
[22] 刘敏, 王欣, 刘宝林.水-乙醇二元体系的低场核磁共振弛豫特性研究[J].现代食品科技, 2015, 31(5):18-24.
LIU M, WANG X, LIU B L.Relaxation characteristics of water-ethanol system by low-field-nuclear magnetic resonance[J].Modern Food Science and Technology, 2015, 31(5):18-24.
[23] KIRSCHNER J, GOMES A H A, MARINHO R R T, et al.The molecular structure of the surface of water-ethanol mixtures[J].Physical Chemistry Chemical Physics, 2022, 24(11):7164.
[24] 秦力悦, 石萍萍, 李荣辉, 等. 基于主成分分析和聚类分析的烘烤类澳洲坚果果仁综合品质评价[J]. 食品工业科技, 2023, 44(18):331-341.
QIN L Y, SHI P P, LI R H, et al. Comprehensive quality evaluation of roasted kernels in Macadamia nuts based on principal component analysis and cluster analysis[J]. Science and Technology of Food Industry, 2023, 44(18):331-341.