中华草龟(Chinemys reevesiis),又名乌龟、草龟、泥龟,生活在淡水水域,分布于全国各地。中华草龟既是一种营养丰富、味道鲜味的水产品,又是一种具有重要医疗价值的药物[1]。中华草龟肉因营养价值丰富,富含多种人体所必需的脂肪酸和氨基酸以及钙、铁、锌、硒等多种矿物质元素,可以加工成泡椒龟肉、香辣龟肉等即食休闲食品[2]。中华草龟的龟肠和龟胃蛋白质、脂肪和灰分含量较高,二者氨基酸种类齐全,组成比例适宜,且鲜味氨基酸含量丰富,可作为良好的氨基酸补充来源;龟肠和龟胃中还含有丰富的钾、磷、铁等多种矿物质元素,不饱和脂肪酸含量均较高,对人体的心脑血管健康十分有益[1]。然而,对草龟资源利用的报道并不多,且多集中于龟肉营养价值、加工特性以及抗肿瘤肽的分离纯化等方面研究[3],关于草龟蛋营养与消化方面的研究甚少。
中华草龟蛋表面粗糙、无光泽、质地较中等、长圆型、个头较鸡蛋小、稍大于鹌鹑蛋。黄喉拟水龟蛋的蛋白质种类丰富,矿物质和不饱和脂肪酸含量高,是一种高价值优质健康食品[4]。红耳龟蛋和中华花龟蛋也是高蛋白低脂肪、富含氨基酸、低胆固醇的营养价值极高的蛋类食品,值得开发利用[5]。此外,甲鱼蛋中水分、粗蛋白质含量高,脂肪含量低,必需氨基酸(essential amino acids, EAA)组成满足理想氨基酸模式,呈味氨基酸含量高,胆固醇含量低,也是一种口感鲜美及营养价值较高的蛋类[6]。而且甲鱼蛋除了营养高、味道鲜,其蛋白还具有一定的生物活性。利用木瓜蛋白酶水解甲鱼蛋蛋白,并通过超滤富集得到的分子质量小于2.5 kDa的降糖组分,在胃消化液中较稳定,在胃肠道中被消化产生了更短的寡肽;并且胃肠道消化后明显提高了该降糖组分的抗氧化活性及α-葡萄糖苷酶的抑制活性,可见经胃肠道消化后的产物有更好的抗氧化性及降糖潜力[7]。
目前中华草龟蛋在市场仅有少量出售,具有极广阔的消费市场;中华草龟蛋的营养物质成分及其体外模拟消化特性和抗氧化活性的影响鲜有研究和报道,基于此,本研究对中华草龟蛋的营养成分及其体外消化特性进行探究,旨在明确中华草龟蛋的营养品质及消化特性,以期为中华草龟蛋的加工利用提供参考,延长中华草龟蛋及其副产物加工产业链。
1 材料与方法
1.1 材料与试剂
中华草龟无精蛋与受精蛋,取自湖南呈宝龟类繁养有限公司。孵育20 d的中华草龟无精蛋、受精蛋各40枚,用清水刷洗干净后,各取20枚进行去壳、冷冻干燥48 h,用于营养成分分析;取剩余20枚,置于95 ℃水浴10 min,去壳后匀浆,用于体外消化特性研究。
盐酸、氢氧化钠、浓硫酸、甲醇、石油醚、苯酚(分析纯),湖南汇虹试剂有限公司;正己烷、乙腈(色谱纯),上海麦克林生化科技有限公司;三羟甲基氨基甘氨酸-十二烷基硫酸钠-聚丙烯酰胺凝胶电泳(tricine-sodium dodecyl sulfate-polyacrylamide gelelectrophoresis, tricine SDS-PAGE)试剂盒,北京酷来搏科技有限公司;AKSU001M葡萄糖含量检测试剂盒、AKPR001M双缩脲法蛋白含量检测试剂盒,北京盒子生工科技有限公司;总抗氧化能力(total antioxidant capacity,T-AOC)测试盒,南京建成生物工程研究所。
1.2 仪器与设备
DSH-50-5水分快速测定仪,上海越平科学仪器有限公司;KT8400自动凯氏定氮仪,福斯分析仪器有限公司;SZF-06A粗脂肪测定仪,上海昕瑞仪器仪表有限公司;Multiskan FC酶标仪,上海旦鼎国际贸易有限公司;AcQuity H class超高效液相色谱仪,美国Waters有限公司;7820A GC-5977E MSD气相色谱-质谱仪,美国安捷伦有限公司;伯乐BIO-RAD Gel Doc XR凝胶成像仪,上海土森视觉科技有限公司。
1.3 实验方法
1.3.1 体外模拟消化实验
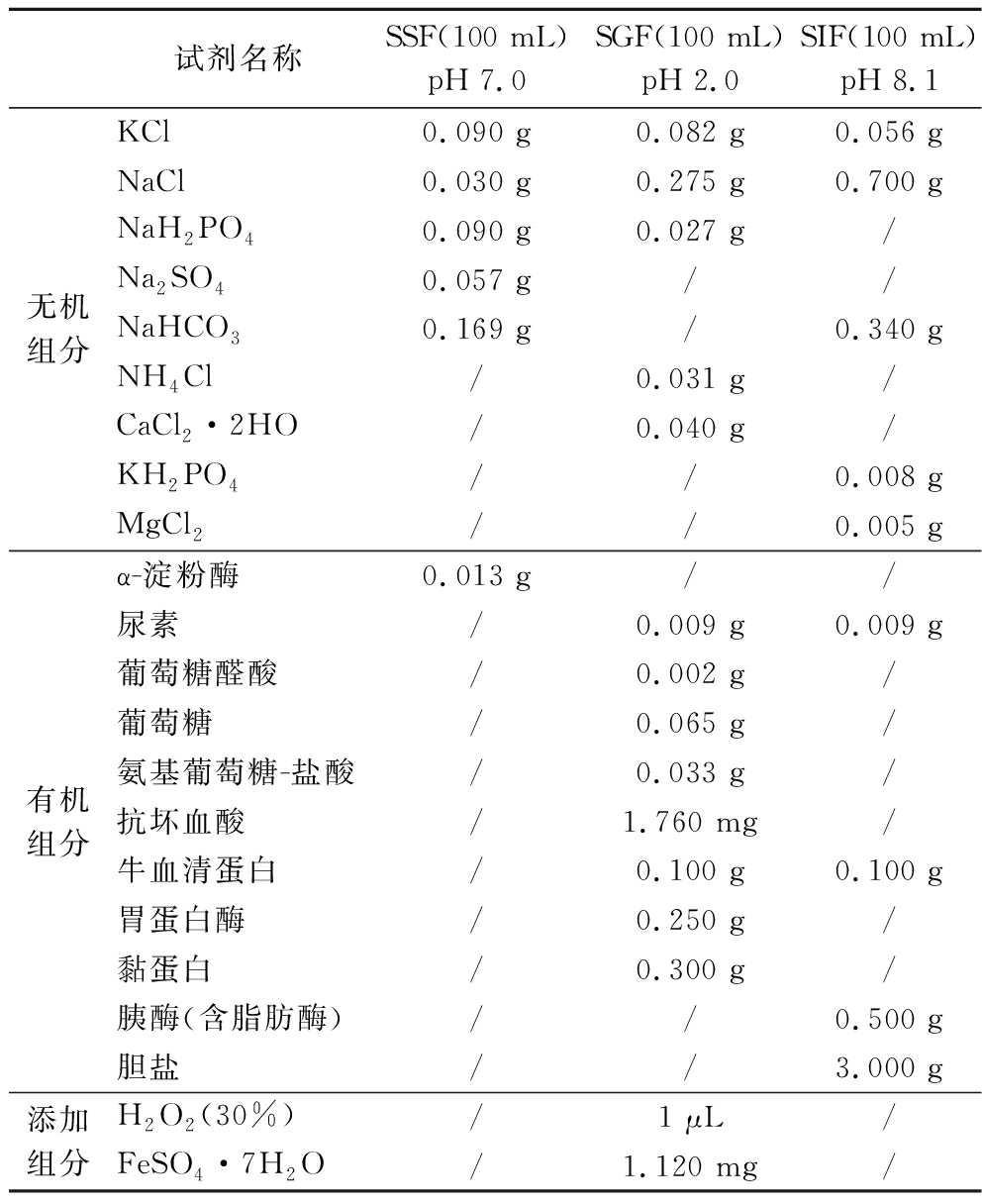
体外模拟消化模型参考文献[8-9]中消化液的配制方法并适当修改,具体如表1所示。称取5 g草龟蛋匀浆液,加入15 mL模拟胃液[pH(2.0±0.2),含胃蛋白酶],37 ℃恒温振荡器消化1 h;再加入15 mL模拟肠液[pH(8.0±0.2),含胰蛋白酶],37 ℃恒温振荡器消化2 h。消化结束后8 000 ×g离心20 min,取上清液置于-80 ℃超低温冰箱待用,每个样品重复3次消化试验。
表1 模拟消化液(唾液、胃液、肠液)成分
Table 1 Compositions of digestive juices used for in vitro digestion
试剂名称SSF(100 mL)pH 7.0SGF(100 mL)pH 2.0SIF(100 mL)pH 8.1无机组分KCl0.090 g0.082 g0.056 gNaCl0.030 g0.275 g0.700 gNaH2PO40.090 g0.027 g/Na2SO40.057 g//NaHCO30.169 g/0.340 gNH4Cl/0.031 g/CaCl2·2HO/0.040 g/KH2PO4//0.008 gMgCl2//0.005 g有机组分α-淀粉酶0.013 g//尿素/0.009 g0.009 g葡萄糖醛酸/0.002 g/葡萄糖/0.065 g/氨基葡萄糖-盐酸/0.033 g/抗坏血酸/1.760 mg/牛血清蛋白/0.100 g0.100 g胃蛋白酶/0.250 g/黏蛋白/0.300 g/胰酶(含脂肪酶)//0.500 g胆盐//3.000 g添加组分H2O2(30%)/1 μL/FeSO4·7H2O/1.120 mg/
注:/表示未添加。
1.3.2 一般营养成分分析
水分:采用DSH水分快速测定仪;灰分:GB 5009.4—2016干法灰化法;脂肪:GB 5009.6—2016索氏提取法;粗蛋白:GB 5009.5—2016凯氏定氮法;总糖:GB/T 9695.31—2008苯酚-硫酸法;葡萄糖:采用葡萄糖含量检测试剂盒(AKSU001M);硫胺素:GB 5009.84—2016食品中维生素B1的测定;核黄素:GB 5009.85—2016食品中维生素B2的测定;胆固醇:GB 5009.128—2016高效液相色谱法;甘油三酯:NY/T 3300—2018植物源性油料油脂中甘油三酯的测定,液相质谱法。
1.3.3 矿物元素分析
参考文献[10]方法,使用电感耦合等离子体原子发射光谱仪(Optima 8300)检测样品中矿物元素含量。
1.3.4 脂肪酸组成分析
参考文献[11]方法,进行脂肪酸甲酯化,在气相色谱质谱仪上测定分析。
1.3.5 总氨基酸组成分析
参考文献[10]方法,使用Elite-AAK氨基酸分析系统的衍生方法进行氨基酸衍生化,高效液相色谱法测定氨基酸含量。
1.3.6 抗氧化能力测定
ABTS阳离子自由基清除能力:使用T-AOC测试盒测定;铁离子还原能力(ferric ion reducing antioxidant power, FRAP):使用T-AOC检测试剂盒进行测定。
1.3.7 可溶性蛋白测定
使用双缩脲法蛋白含量检测试剂盒(AKPR001M)进行测定。
1.3.8 Tricine-SDS-PAGE分析
参考文献[12]方法,使用Tricine-SDS-PAGE电泳试剂盒进行测定分析。
1.4 数据处理
实验结果以平均值±标准差来表示。使用SPSS 16.0软件进行单因素方差分析(One-Way ANOVA),*表示具有显著差异(P<0.05),不同字母表示具有显著性(P<0.05)。使用Excel 2016软件作图。
2 结果与分析
2.1 基本营养成分分析
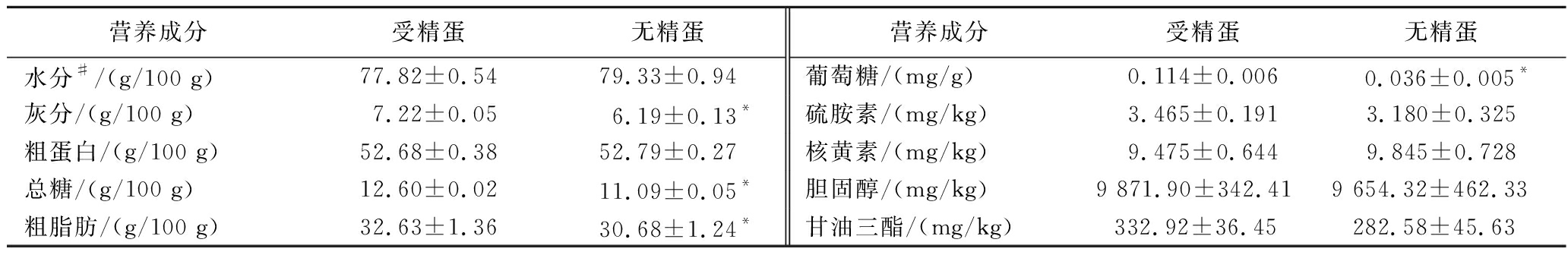
中华草龟的受精蛋与无精蛋的基本营养成分如表2所示,新鲜的无精蛋和受精蛋中分别含有77.82%和79.33%的水分,且两者并无差异。常见的禽蛋如鸡蛋、鸭蛋、鹅蛋、鸽蛋及鹌鹑蛋的全蛋中水分含量均为72.4%~79.6%[13]。黄喉拟水龟蛋的蛋清与蛋黄中水分含量分别为89.43%和64.38%[4],中华草龟全蛋的水分介于两者之间。干基的受精蛋中的灰分、总糖和粗脂肪均明显高于干基的无精蛋中对应的营养成分,而粗蛋白含量两者无明显差异,均约为53%。常见的几种禽蛋中灰分含量为0.88%~1.40%[13],中华草龟蛋鲜蛋中的灰分含量为1.28%~1.60%,略高于禽蛋;而黄喉拟水龟蛋的蛋清和蛋黄中灰分分别为2.77%和0.19%[4],草龟全蛋的灰分含量介于两者之间。灰分中可能含有丰富的钙、镁、钾、钠等矿物质元素。中华草龟蛋鲜蛋的脂肪含量约为6.34%~7.24%,常见禽蛋的全蛋脂肪为4.9%~8.2%,其中鸡蛋的脂肪含量为5.8%,黄喉拟水龟蛋的蛋清无脂肪,蛋黄中脂肪含量为8.94%[4]。草龟鲜蛋的粗蛋白含量约为10.91%~11.68%,禽蛋的全蛋蛋白含量为10.7%~14.7%,黄喉拟水龟蛋的蛋清中蛋白含量为9.78%,蛋黄中蛋白含量为23.42%[4]。草龟鲜蛋中的总糖含量仅为2.29%~2.79%。中华草龟蛋也同样具有高蛋白、低脂肪,低碳水化合物的营养结构特点。
表2 中华草龟全蛋营养成分(干基计)
Table 2 General composition in Mauremys reevesii eggs (in dry weight)
营养成分受精蛋无精蛋营养成分受精蛋无精蛋水分#/(g/100 g)77.82±0.5479.33±0.94葡萄糖/(mg/g)0.114±0.006 0.036±0.005*灰分/(g/100 g)7.22±0.056.19±0.13*硫胺素/(mg/kg)3.465±0.1913.180±0.325粗蛋白/(g/100 g)52.68±0.3852.79±0.27核黄素/(mg/kg)9.475±0.6449.845±0.728总糖/(g/100 g)12.60±0.0211.09±0.05*胆固醇/(mg/kg)9 871.90±342.41 9 654.32±462.33 粗脂肪/(g/100 g)32.63±1.3630.68±1.24*甘油三酯/(mg/kg)332.92±36.45 282.58±45.63
注:#表示鲜基样品营养成分含量,*表示不同样品同一成分具有显著差异(P<0.05)(下同)。
中华草龟蛋的无精蛋中葡萄糖含量显著低于受精蛋,与总糖的结果一致,可能由于受精蛋在孵化前期利用葡萄糖供能[14]。而硫胺素(维生素B1)、核黄素(维生素B2)、甘油三酯及胆固醇含量均无明显差异。硫胺素、核黄素是机体健康和生长所必需的维生素,是多种辅酶的重要组成部分,具有增强机体免疫能力的功能[15]。中华草龟全蛋干基中的硫胺素、核黄素及甘油三酯含量分别约为3.465、9.475、332.92 mg/kg,显著高于鸡蛋黄中硫胺素及核黄素的含量(0.121~1.15、4~5、602.7~675.6 mg/kg)[15]。草龟全蛋的胆固醇含量为9 654~9 872 mg/kg,与中华鳖蛋、红耳龟蛋和中华花龟蛋的蛋黄中胆固醇含量(10 840、9 830、11 140 mg/kg)相近[5-6]。
2.2 矿物元素分析
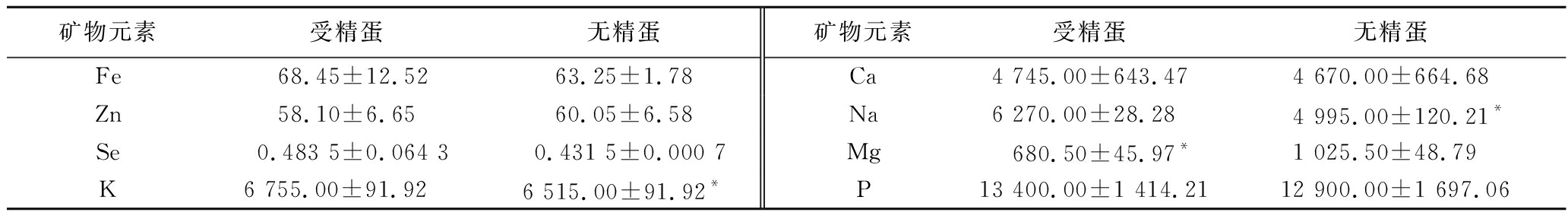
对中华草龟无精蛋与受精蛋的全蛋中的矿物质元素进行测定分析,结果如表3所示。在所测定的8种矿物质元素中,磷含量最高,较高的是钾、钠、钙,其次镁、铁、锌,还含有少量硒元素,约0.43~0.48 mg/kg。除了具有较高含量的钾和钠存在显著性差异外,无精蛋与受精蛋在矿物元素含量中无差异。矿物元素是人体实现正常生命活动所必需的微量元素,磷、钾和钙是构成人体骨骼、牙齿的主要成分,维持机体生长发育;钾、钠调节体液酸碱平衡、维持细胞渗透性;镁具有保护心脏和心血管系统的生理学功效;硒是人和动物的抗氧化酶,有抗氧化、抗衰老、增强免疫力、保护细胞、提高红细胞携氧能力等功效[10-11,16]。草龟全蛋中的灰分含量高,可以间接说明其中含有较高的矿物质元素。禽蛋蛋黄中含有丰富的矿物质,但极易受到饲料种类的影响[13]。中华草龟蛋的磷含量高于黄喉拟水龟全蛋中的磷(9 025.21 mg/kg),而黄喉拟水龟全蛋中的镁(1 301.85 mg/kg)、锌(114.58 mg/kg)和铁(86.33 mg/kg)含量均高于中华草龟;鸡蛋全蛋中的磷(5 573.93 mg/kg)、镁(555.40 mg/kg)均不及龟蛋[4]。
表3 中华草龟全蛋矿物元素含量(干基计) 单位:mg/kg
Table 3 Mineral content in Mauremys reevesii eggs (in dry weight)
矿物元素受精蛋无精蛋矿物元素受精蛋无精蛋Fe 68.45±12.5263.25±1.78Ca4 745.00±643.474 670.00±664.68Zn58.10±6.6560.05±6.58Na6 270.00±28.284 995.00±120.21*Se 0.483 5±0.064 3 0.431 5±0.000 7Mg680.50±45.97*1 025.50±48.79K6 755.00±91.92 6 515.00±91.92*P13 400.00±1 414.2112 900.00±1 697.06
2.3 总氨基酸组成分析
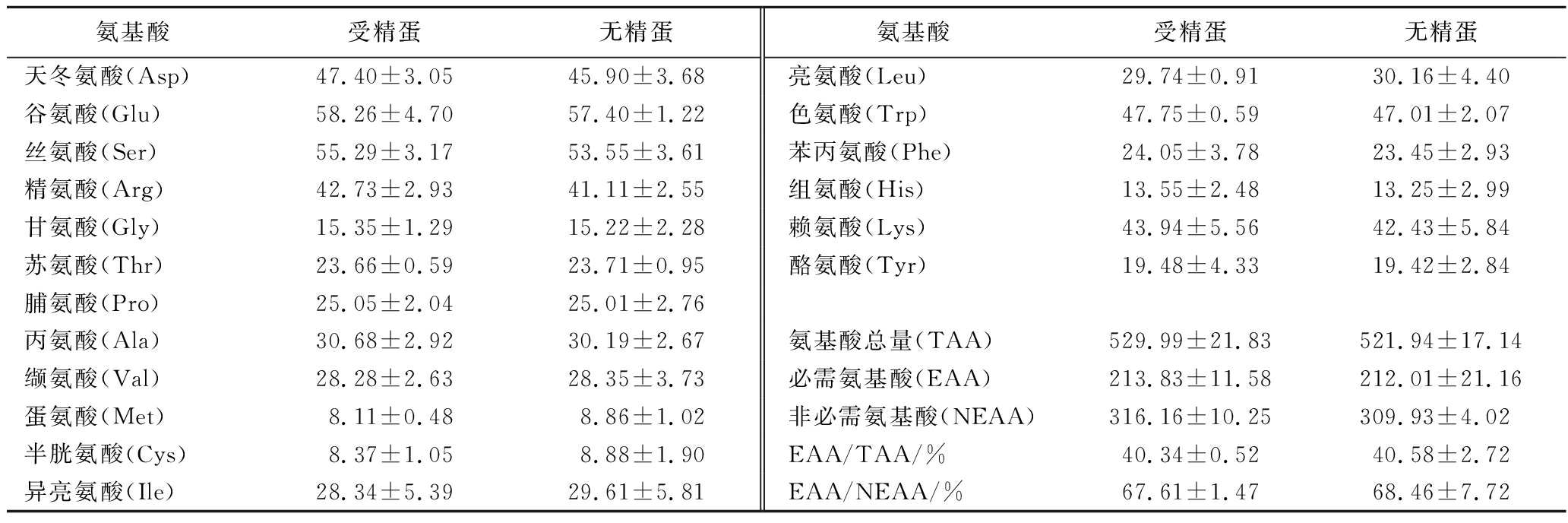
中华草龟全蛋的总氨基酸组成分析如表4所示,共检测出受精蛋和无精蛋均含有18种氨基酸,且总氨基酸(total amino acids, TAA)、EAA、非必需氨基酸(non-essential amino acid, NEAA)及18种氨基酸含量均无差异。EAA对生物体生命活动有重要作用,能提供合成蛋白质的重要原料,同时也为进行正常代谢、维持生命提供了物质基础。中华草龟全蛋里的EAA占氨基酸总量的40%。中华鳖蛋的蛋清和蛋黄(干基)中EAA均占38%,红耳龟蛋和中华花龟蛋的蛋清和蛋黄(干基)中EAA均约占35%,黄喉拟水龟蛋的蛋清和蛋黄中EAA均占37%,中华草龟全蛋的EAA含量高于中华鳖蛋[6]、红耳龟蛋、中华花龟蛋[5]和黄喉拟水龟蛋[4]。据WHO/FAO提出的理想模式标准,质量较好的蛋白质其EAA/TAA的值为40左右,EAA/NEAA的值为60左右[10]。中华草龟蛋的EAA/TAA值和EAA/NEAA值分别约为40和68,说明中华草龟蛋的蛋白质营养价值较高,氨基酸种类齐全。
表4 中华草龟全蛋总氨基酸组成分析(干基计) 单位:mg/g
Table 4 The content of the amino acids in Mauremys reevesii eggs (in dry weight)
氨基酸受精蛋无精蛋氨基酸受精蛋无精蛋天冬氨酸(Asp)47.40±3.0545.90±3.68亮氨酸(Leu)29.74±0.9130.16±4.40谷氨酸(Glu)58.26±4.7057.40±1.22色氨酸(Trp)47.75±0.5947.01±2.07丝氨酸(Ser)55.29±3.1753.55±3.61苯丙氨酸(Phe)24.05±3.7823.45±2.93精氨酸(Arg)42.73±2.9341.11±2.55组氨酸(His)13.55±2.4813.25±2.99甘氨酸(Gly)15.35±1.2915.22±2.28赖氨酸(Lys)43.94±5.5642.43±5.84苏氨酸(Thr)23.66±0.5923.71±0.95酪氨酸(Tyr)19.48±4.3319.42±2.84脯氨酸(Pro)25.05±2.0425.01±2.76丙氨酸(Ala)30.68±2.9230.19±2.67氨基酸总量(TAA)529.99±21.83521.94±17.14缬氨酸(Val)28.28±2.6328.35±3.73必需氨基酸(EAA)213.83±11.58212.01±21.16蛋氨酸(Met)8.11±0.488.86±1.02非必需氨基酸(NEAA)316.16±10.25309.93±4.02半胱氨酸(Cys)8.37±1.058.88±1.90EAA/TAA/%40.34±0.5240.58±2.72异亮氨酸(Ile)28.34±5.3929.61±5.81EAA/NEAA/%67.61±1.4768.46±7.72
注:必需氨基酸为Thr、Val、Met、Ile、Leu、Trp、Phe、Lys的总和,其他氨基酸总和为非必需氨基酸。
由表5可知,中华草龟蛋中必需氨基酸评分(amino acid score,AAS)最高的是异亮氨酸,受精蛋和无精蛋的AAS分别为2.00和2.06,其次是缬氨酸(Val)和赖氨酸(Lys)。EAA的AAS大于1,说明EAA的均衡性相对较好,可以提供较为优质全面的蛋白质。中华草龟蛋中的EAA的AAS均大于1,黄喉拟水龟蛋的蛋清中仅有3种人体EAA的AAS评分值大于1,分别是Leu(1.03)、Lys(1.19)和Phe+Tyr(1.16),而蛋黄氨基酸的AAS均小于1,蛋清蛋白质营养价值高于蛋黄[4]。
表5 中华草龟全蛋必需氨基酸评分
Table 5 Amino acids score of protein in Mauremys reevesii eggs
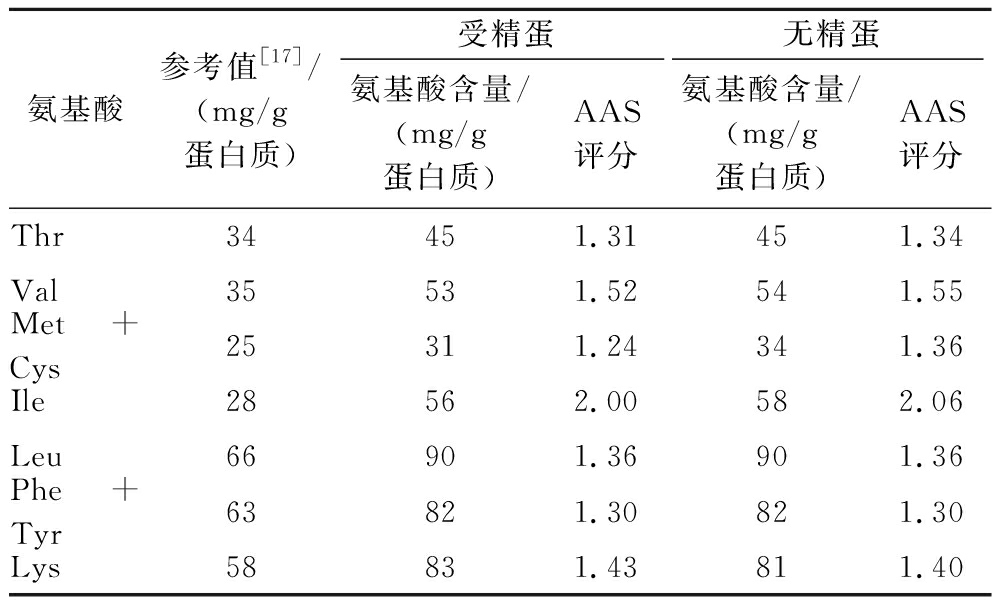
氨基酸参考值[17]/(mg/g蛋白质)受精蛋无精蛋氨基酸含量/(mg/g蛋白质)AAS评分氨基酸含量/(mg/g蛋白质)AAS评分Thr3445 1.31 45 1.34 Val3553 1.52 54 1.55 Met+Cys2531 1.24 34 1.36 Ile2856 2.00 58 2.06 Leu6690 1.36 90 1.36 Phe+Tyr6382 1.30 82 1.30 Lys5883 1.43 81 1.40
2.4 脂肪酸组成分析
中华草龟全蛋的脂肪酸组成(fatty acids, FA)如表6所示,从C10到C22共有28种脂肪酸,其中饱和脂肪酸(saturated fatty acids, SFA)、单不饱和脂肪酸(monounsaturated fatty acid, MUFA)、多不饱和脂肪酸(polyunsaturated fatty acids, PUFA)的含量分别为23.03%~23.71%、47.44%~49.54%、27.23%~28.68%。受精蛋的脂肪酸含量较无精蛋的明显偏低,可能是因为胚胎在孵化期间需要卵黄中的脂类供能而消耗[18],但SFA、MUFA、PUFA占比无显著差异。中华草龟蛋的SFA中棕榈酸(C16∶0)含量最多,棕榈酸是生产蜡烛、肥皂、润滑脂、软化剂和合成洗涤剂的原料[19];MUFA中油酸(C18∶1n9)含量较多,油酸是安全的健康脂肪酸,有抗氧化、调节血脂、降低胆固醇、增强记忆力等功效[20-21];PUFA中,亚油酸(C18∶2n6)、α亚麻酸(C18∶3n3)、γ亚麻酸(C18∶3n6)、花生四烯酸(C20∶4n6)以及二十碳五烯酸(eicosapentaenoic acid, EPA)(C20∶5n3)和二十二碳六烯酸(docosahexaenoic acid,DHA)(C22∶6n3)的含量也都很可观,它们是人体自身不能合成但又不可缺少的必需脂肪酸。亚油酸有软化心脑血管,降低血压血脂,促进新陈代谢的作用,能有效预防动脉硬化发生,提高人体免疫力,促进骨骼发育,提高记忆力[22-25];亚麻酸可以降解血栓、预防心脑血管病、抑制过敏反应、抗炎、抑制衰老、增强智力和保护视力[26-27];花生四烯酸具有胆固醇酯化、降低血中胆固醇和甘油三酯的功效[28];DHA和EPA均产生神经保护代谢物,DHA对大脑发育至关重要,EPA影响行为能力[29]。上述几种脂肪酸在无精蛋中的含量要显著高于受精蛋,可见无精蛋脂肪酸的营养价值要高于受精蛋。黄喉拟水龟蛋黄中不饱和脂肪酸含量(80.72%)显著高于鸡蛋黄(64.32%)[4],而红耳龟蛋黄和中华花龟蛋黄中不饱和脂肪酸总量分别为58.19%和60.63%[5],中华草龟蛋中的MUFA和PUFA约占脂肪酸总量的77%,必需脂肪酸含量丰富,有一定食用价值。
表6 中华草龟全蛋脂肪酸组成(干基计) 单位:mg/g
Table 6 The content of the fatty acid composition in in Mauremys reevesii eggs (in dry weight)
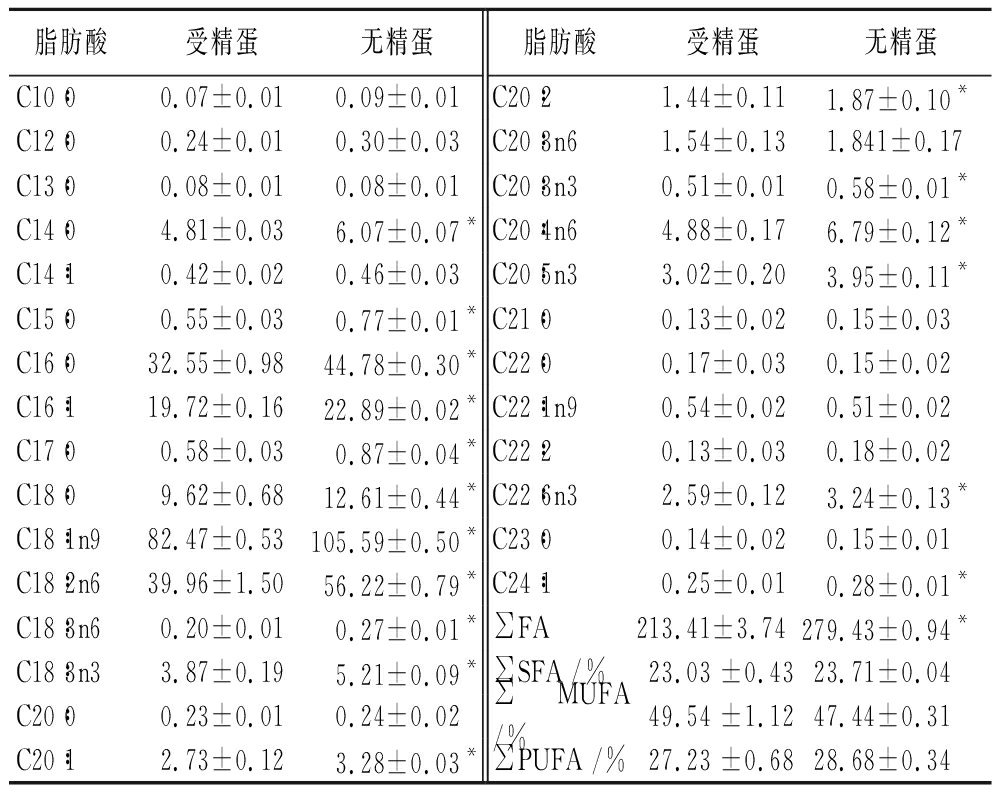
脂肪酸受精蛋无精蛋脂肪酸受精蛋无精蛋C10∶00.07±0.010.09±0.01C20∶21.44±0.111.87±0.10*C12∶00.24±0.010.30±0.03C20∶3n61.54±0.131.841±0.17C13∶00.08±0.010.08±0.01C20∶3n30.51±0.010.58±0.01*C14∶04.81±0.036.07±0.07*C20∶4n64.88±0.176.79±0.12*C14∶10.42±0.020.46±0.03C20∶5n33.02±0.203.95±0.11*C15∶00.55±0.030.77±0.01*C21∶00.13±0.020.15±0.03C16∶032.55±0.9844.78±0.30*C22∶00.17±0.030.15±0.02C16∶119.72±0.1622.89±0.02*C22∶1n90.54±0.020.51±0.02C17∶00.58±0.030.87±0.04*C22∶20.13±0.030.18±0.02C18∶09.62±0.6812.61±0.44*C22∶6n32.59±0.123.24±0.13*C18∶1n982.47±0.53105.59±0.50*C23∶00.14±0.020.15±0.01C18∶2n639.96±1.5056.22±0.79*C24∶10.25±0.010.28±0.01*C18∶3n60.20±0.010.27±0.01*∑FA 213.41±3.74279.43±0.94*C18∶3n33.87±0.195.21±0.09*∑SFA /%23.03 ±0.4323.71±0.04C20∶00.23±0.010.24±0.02∑MUFA /%49.54 ±1.1247.44±0.31C20∶12.73±0.123.28±0.03*∑PUFA /%27.23 ±0.6828.68±0.34
2.5 体外消化过程中ABTS阳离子自由基清除能力
利用总抗氧化试剂盒分析测定中华草龟蛋在模拟口腔(simulated salivary fluid,SSF)、胃(simulated gastric fluid,SGF)和小肠(simulated intestinal fluid,SIF)消化后的消化液的抗氧化能力。消化液的抗氧化能力分别用TEAC(trolox equivalent antioxidant capacity)的物质的量(mmol/L TEAC/g)和(mmol/L FeSO4·7H2O/g)来表示。如图1所示,随着消化过程的进行,中华草龟受精蛋与无精蛋消化液的ABTS阳离子自由基清除能力均有一定程度的增加,且在小肠液中显著增强(P<0.05)。模拟胃肠液消化后,受精蛋与无精蛋的ABTS阳离子自由基清除率显著提高,可能是草龟蛋经模拟胃、肠液消化后,产生了更多亲水性的短肽与氨基酸,使具有抗氧化能力的氨基酸残基得以充分暴露,进而使ABTS阳离子自由基更容易被抑制[30],所以与对照组相比,经蛋白酶消化后的ABTS阳离子自由基清除能力显著提高,且受精蛋与无精蛋之间虽有差异但不显著(P>0.05)。冯晓文等[31]对海洋鱼骨胶原低聚肽的胃肠道消化特性进行了研究,结果与本研究一致,体外胃肠道消化体系均提高了其抗氧化能力。
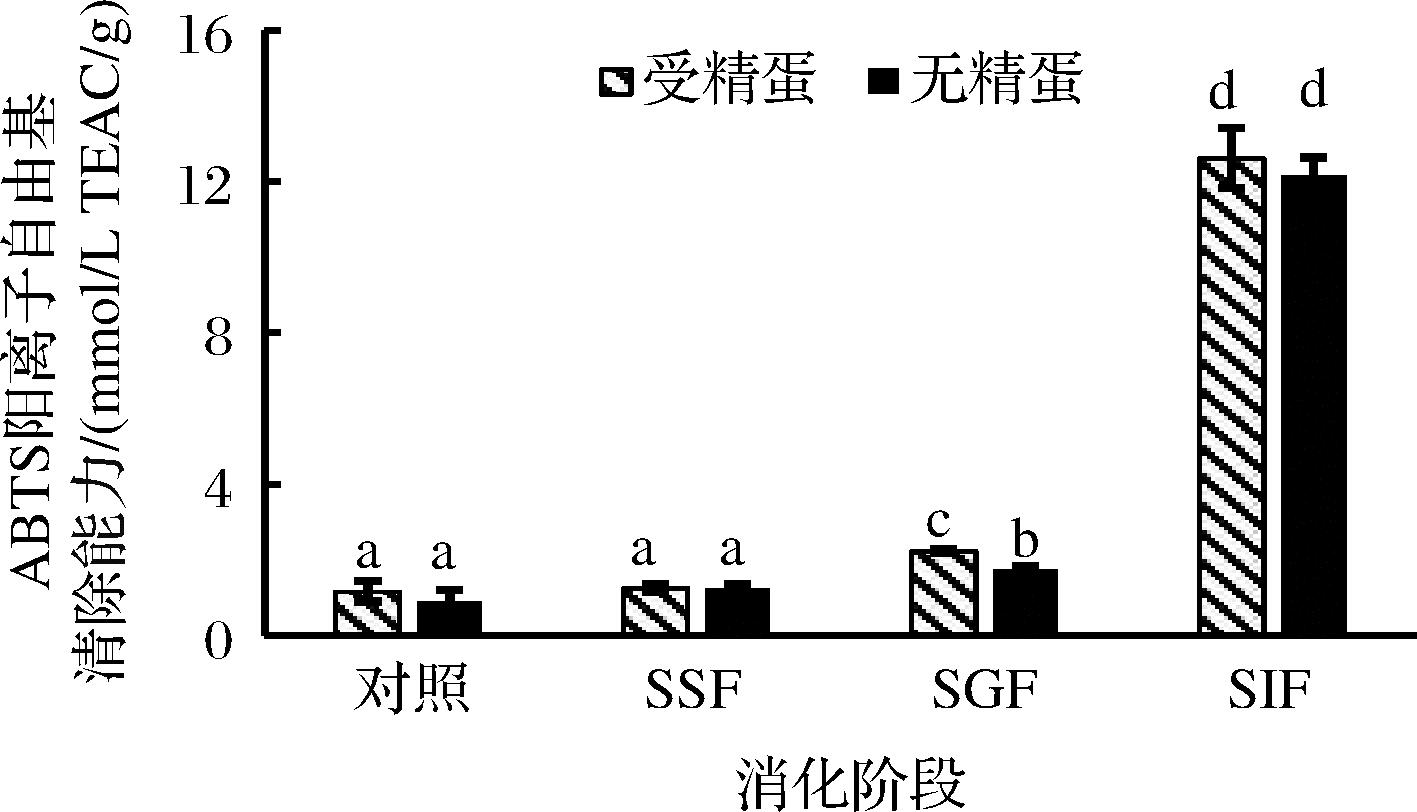
图1 中华草龟蛋消化过程中ABTS阳离子自由基清除能力
Fig.1 Changes of ABTS cationic radical scavenging ability of Mauremys reevesii eggs during digestion in vitro
注:不同字母表示数据有显著性差异(P<0.05)(下同)。
2.6 体外消化过程中FRAP值变化
图2所示,随着消化过程进行,受精蛋与无精蛋的消化液的FRAP也逐渐升高。与对照相比,经胃肠消化后FRAP值显著提升,且受精蛋与无精蛋的小肠消化液的FRAP值显著高于胃消化液(P<0.05)。这表明草龟蛋消化液能够通过氢原子转移阻断自由基链式反应过程实现抗氧化作用[32]。SILVA等[33]发现由于亚麻籽蛋白包含某些活性氨基酸序列,或者具有大量疏水区的肽段特定结构,因而在酶解后抗氧化能力显著提高,且酶解产物肽的分子质量越低,其FRAP值越高。模拟人体胃肠液消化模式下,草龟蛋经酶解后生成更低分子质量的肽,使得一些疏水性基团进一步暴露出来,导致表面疏水性提高,而高含量的疏水性氨基酸或肽通常与较高自由基清除能力有关。可见,草龟蛋在经历口腔、胃与肠道消化后,逐渐被分解为具有抗氧化活性且利于人体吸收的小分子成分。
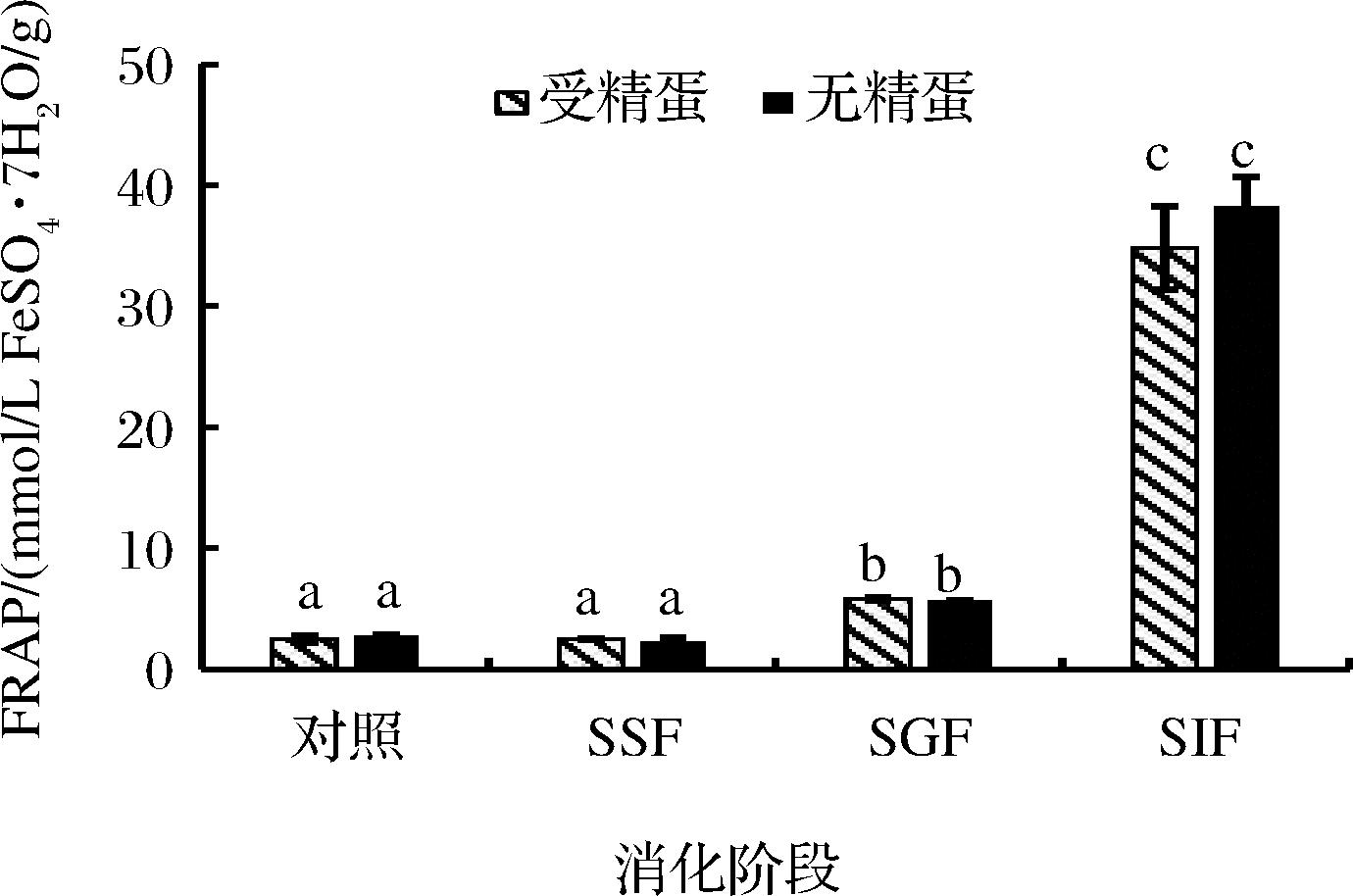
图2 中华草龟蛋消化过程中铁离子还原能力
Fig.2 Changes of ferric ion reducing antioxidant power of Mauremys reevesii eggs during digestion in vitro
2.7 可溶性蛋白含量分析
通过可溶性蛋白含量来评价膳食蛋白质的生物利用率,即衡量草龟蛋被各消化液酶解后释放出多肽的程度。中华草龟蛋消化过程中的可溶性蛋白含量变化如图3所示,中华草龟的无精蛋与受精蛋经消化反应后变化趋势一致,但在每种消化液中可溶性蛋白释放量有显著差别(P<0.05)。草龟蛋经加热处理后,由于样品中蛋白分子间氢键、二硫键的部分断裂,及其空间结构的破坏,导致原本位于内部的蛋白酶作用位点暴露,提高了蛋白与酶的相互作用[31]。草龟蛋经各消化液消化后,可溶性蛋白含量增加,使其膳食蛋白质的生物利用率提高,释放出了更多的肽与氨基酸,这与前文抗氧化活性的研究结果一致。
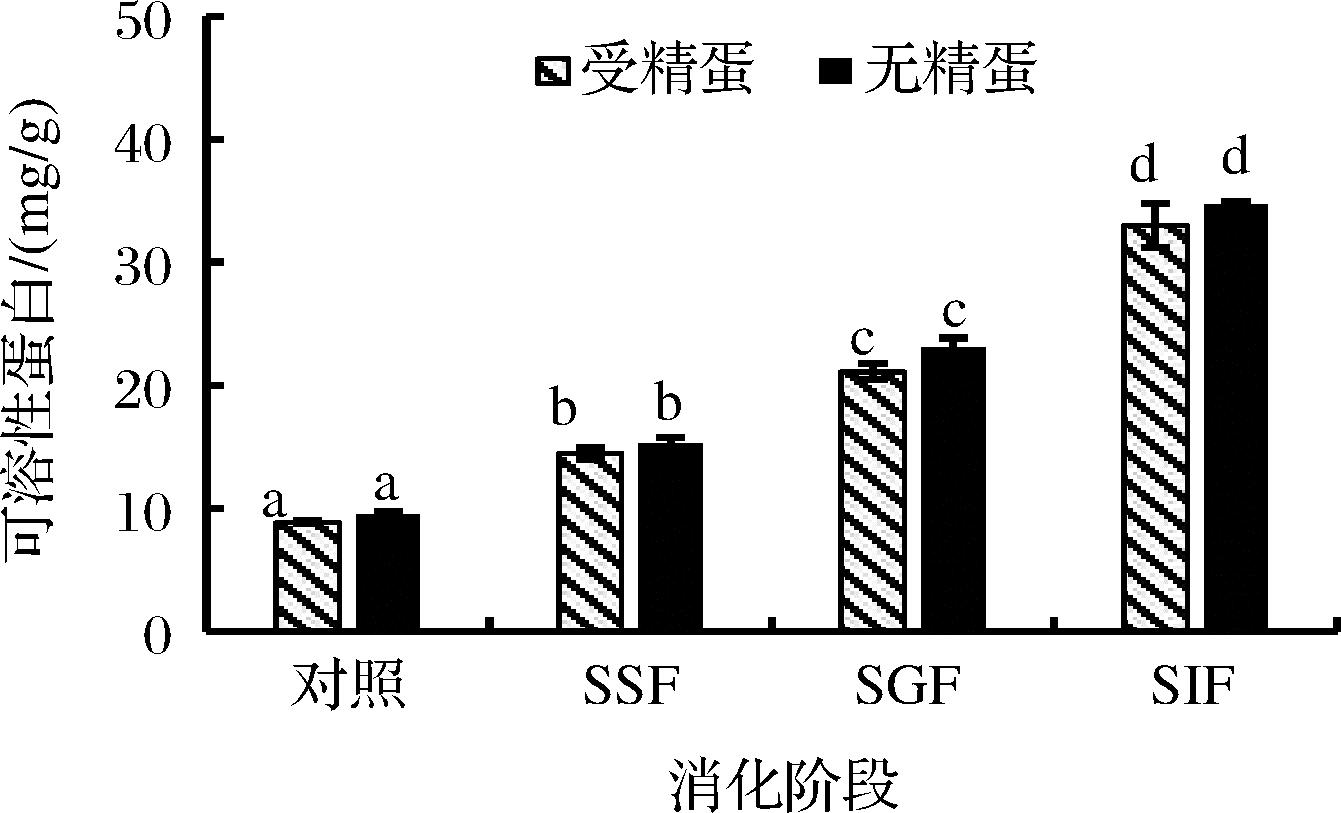
图3 中华草龟蛋消化过程中可溶性蛋白含量变化
Fig.3 Changes of the soluble protein content of Mauremys reevesii eggs during digestion in vitro
2.8 Tricine-SDS-PAGE分析
对中华草龟蛋消化过程中消化液中的蛋白进行Tricine-SDS-PAGE分析,电泳图如图4所示,中华草龟蛋在口腔中的蛋白含量高,且各分子质量大小的蛋白分布均匀;经胃消化液后,部分蛋白条带变得模糊,22 kDa以上的蛋白依然清晰;但经过小肠消化液后,3.3 kDa以上的蛋白条带已不清晰,草龟蛋中被胃蛋白酶部分水解后的蛋白又在小肠中经胰蛋白酶水解成了肽或氨基酸,相对分子质量主要集中于3.3 kDa以下,低分子质量的肽一般具有更好的抗氧化作用[34],与前文实验结果一致。从电泳图分析,受精蛋与无精蛋在模拟肠道消化阶段的水解情况并不明显。在消化液中蛋白质氧化引起了蛋白质展开或聚集,胃消化过程中的氧化主要归因于胃液的低pH值及促氧化剂的存在;肠道消化过程主要是蛋白质和脂质的水解释放大量游离氨基和脂肪酸,部分氧化的蛋白质结构展开,促进了酶解作用[35]。所以草龟蛋的消化产物可能具有潜在的抗氧化性。
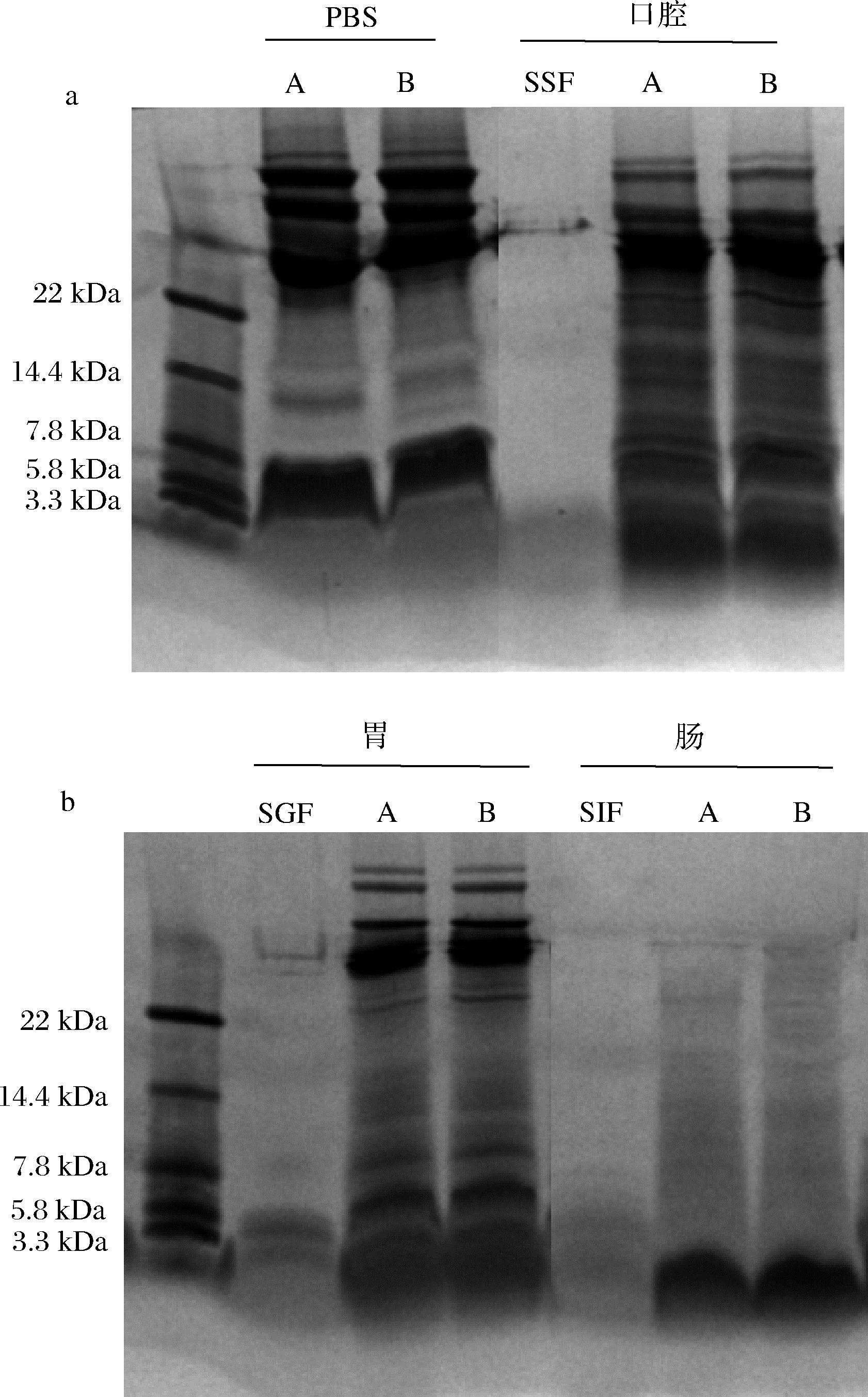
A-受精蛋;B-无精蛋;SSF-模拟口腔消化液空白对照;SGF-模拟胃消化液空白对照;SIF-模拟小肠消化液空白对照
a-PBS、口腔;b-胃、肠
图4 中华草龟蛋消化过程中的蛋白电泳图
Fig.4 Tricine-SDS-PAGE of Mauremys reevesii eggs during digestion in vitro
3 结论
通过对中华草龟蛋营养成分分析后发现,中华草龟蛋同样具有高蛋白、低脂肪、低糖的特点;含有丰富的维生素和矿物质元素,人体必需氨基酸和脂肪酸含量较高,具有较高的营养价值,而且在大部分营养成分中,受精蛋与无精蛋之间并无显著差异。模拟中华草龟蛋在口腔、胃和小肠液中的消化过程发现,草龟蛋随着消化的进行,蛋白的抗氧化性逐渐增强,且在肠消化液中最为显著;经胃肠消化后,草龟蛋的蛋白逐渐降解为小分子的寡肽,有利于人体的吸收,且受精蛋与无精蛋之间无明显差异。中华草龟蛋营养价值可观,在口腔及胃消化液中稳定,能在肠消化液中降解为具有较强抗氧化活性的小分子寡肽,是人类补充蛋白的优质营养源。关于中华草龟蛋在肠消化液中的活性肽类物质的分离纯化、吸收及其功能特性还有待进一步深入探究。中华草龟蛋具有较高的食用价值和开发潜力,本研究可为中华草龟蛋的食用、加工与开发利用提供科学依据。
[1] 王福田, 李正荣, 赖年悦, 等.中华草龟龟肠和龟胃的营养品质分析[J].肉类工业, 2020(4):20-25.
WANG F T, LI Z R, LAI N Y, et al.Analysis of nutritional quality of intestine and stomach of Chinemys reevesii[J].Meat Industry, 2020(4):20-25.
[2] 徐莹莹. 即食龟肉的加工及其风味物质的研究[D].合肥:合肥工业大学, 2017.
XU Y Y.Study on processing of instant turtle meat and its flavor substances[D].Hefei:Hefei University of Technology, 2017.
[3] 张永进, 石扬, 赖年悦, 等.中华草龟抗肿瘤生物活性肽提取工艺的初步研究[J].肉类工业, 2017(7):28-33.
ZHANG Y J, SHI Y, LAI N Y, et al.Preliminary study on extraction technology of antitumor bioactive peptides of Chinemys reevesii[J].Meat Industry, 2017(7):28-33.
[4] 马风娟, 王富云, 江虹锐, 等.黄喉拟水龟蛋营养成分分析及评价[J].食品研究与开发, 2020, 41(2):33-39.
MA F J, WANG F Y, JIANG H R, et al.Nutritional analysis and evaluation of Mauremys mutica egg[J].Food Research and Development, 2020, 41(2):33-39.
[5] 张君, 陆剑锋, 欧阳霞, 等.红耳龟蛋和中华花龟蛋营养成分分析[J].南方农业学报, 2020, 51(4):905-913.
ZHANG J, LU J F, OUYANG X, et al.Nutritional components in eggs of red-eared slider and Chinese flower turtle[J].Journal of Southern Agriculture, 2020, 51(4):905-913.
[6] 张君, 欧阳霞, 陆剑锋, 等.中华鳖蛋营养价值评价[J].动物营养学报, 2019, 31(11):5101-5111.
ZHANG J, OUYANG X, LU J F, et al.Evaluation of nutritional value of eggs of Chinese soft-shell turtle (Pelodiscus sinensis)[J].Chinese Journal of Animal Nutrition, 2019, 31(11):5101-5111.
[7] 赵才冬, 漆姚姚, 雷楚文, 等.甲鱼蛋蛋白水解物的体外消化及对抗氧化和α-葡萄糖苷酶抑制活性的影响[J].中国食品学报, 2022, 22(10):126-133.
ZHAO C D, QI Y Y, LEI C W, et al.The digestion characteristic of protein hydrolysate of soft-shelled turtle egg and its effects on antioxidative and α-glucosidase inhibitory activities[J].Journal of Chinese Institute of Food Science and Technology, 2022, 22(10):126-133.
[8] VAN HECKE T, VANDEN BUSSCHE J, VANHAECKE L, et al.Nitrite curing of chicken, pork and beef inhibits oxidation but does not affect N-nitroso compound (NOC)-specific DNA adduct formation during in vitro digestion[J].Journal of Agricultural and Food Chemistry, 2014, 62(8):1980-1988.
[9] 孟粉, 秦求思, 董烨, 等.蛋白质氧化和酶对草鱼重组鱼肉品质及体外模拟消化的影响[J].中国食品学报, 2021, 21(9):288-295.
MENG F, QIN Q S, DONG Y, et al.Effects of protein oxidation and TGase on the quality of restructured minced grass carp and in vitro simulated digestion[J].Journal of Chinese Institute of Food Science and Technology, 2021, 21(9):288-295.
[10] 徐文思, 胡诗雨, 邓娟丽, 等.小龙虾加工水煮液营养成分与风味物质分析[J].食品与发酵工业, 2021, 47(14):279-286.
XU W S, HU S Y, DENG J L, et al.Analysis of nutrient and flavor compounds in boiled crayfish waste water[J].Food and Fermentation Industries, 2021, 47(14):279-286.
[11] MA R, LIU X H, TIAN H N, et al.Odor-active volatile compounds profile of triploid rainbow trout with different marketable sizes[J].Aquaculture Reports, 2020, 17:100312.
[12] 徐文思, 杨祺福, 张梦媛, 等.两步酶解法制备小龙虾副产物多肽及其抗氧化性研究[J].食品研究与开发, 2021, 42(24):147-154.
XU W S, YANG Q F, ZHANG M Y, et al.Extraction and antioxidant capacity of polypeptides from crayfish by-products by two-step enzymatic hydrolysis[J].Food Research and Development, 2021, 42(24):147-154.
[13] 姚俊峰, 龚绍明, 杨长锁, 等.不同禽蛋营养成分比较研究[J].上海畜牧兽医通讯, 2020(6):22-25.
YAO J F, GONG S M, YANG C S, et al.Comparative study on nutritional components of different poultry eggs[J].Shanghai Journal of Animal Husbandry and Veterinary Medicine, 2020(6):22-25.
[14] 高丹. 鸡胚蛋孵化过程中蛋黄浆质的比较蛋白质组学研究[D].武汉:华中农业大学, 2017.
GAO D.Comparative study on yolk plasma quality during hatching of chicken embryo eggs by protein omics[D].Wuhan:Huazhong Agricultural University, 2017.
[15] 武传香, 薛霞, 卢兰香, 等.鸡蛋中维生素B1的含量检测[J].食品工业, 2022, 43(5):306-311.
WU C X, XUE X, LU L X, et al.Determination of vitamin B1 in eggs[J].The Food Industry, 2022, 43(5):306-311.
[16] 田娟, 许巧情, 田罗, 等.洞庭湖克氏原螯虾肌肉成分分析及品质特性分析[J].水生生物学报, 2017, 41(4):870-877.
TIAN J, XU Q Q, TIAN L, et al.The muscle composition analysis and flesh quality of Procambarus clarkia in the Dongting lake[J].Acta Hydrobiologica Sinica, 2017, 41(4):870-877.
[17] 中国营养学会. 中国居民膳食营养素参考摄入量[M].北京:中国轻工业出版社, 2001.
CHINESE NUTRITION SOCIETY.Chinese Dietary Reference Intakes, DRIs[M].Beijing, 2001.
[18] 彭梦玲. 胚胎期肉鸡脂肪代谢的蛋白质组学和代谢组学分析及(-)-羟基柠檬酸调控机制研究[D].南京:南京农业大学, 2018.
PENG M L.Protein metabonomics and metabonomics analysis of fat metabolism in embryonic broilers and (-)-study on the regulation mechanism of hydroxycitric acid[D].Nanjing:Nanjing Agricultural University, 2018.
[19] 韦露, 司成成, 冯美利, 等.油棕果肉发育过程中的代谢组学和转录组学联合分析[J].分子植物育种, 2023,21(19):6315-6326.
WEI L, SI C C, FENG M L, et al.Analyses of mesocarp development of thin-shelled oil palm (Elaeis guineensis jacq.) by joint metabolomics and transcriptomics approaches[J].Molecular Plant Breeding, 2023,21(19):6315-6326.
[20] 马素换, 郭萍梅, 黄凤洪.魔芋葡甘聚糖及其油酸酯化物的体外抗氧化初步研究[J].中国油脂, 2017, 42(9):55-59.
MA S H, GUO P M, HUANG F H.Preliminary study on antioxidant activity in vitro of konjac glucomannan and its oleic acid esterified product[J].China Oils and Fats, 2017, 42(9):55-59.
[21] BARBOUR J A, HOWE P R C, BUCKLEY J D, et al.Cerebrovascular and cognitive benefits of high-oleic peanut consumption in healthy overweight middle-aged adults[J].Nutritional Neuroscience, 2017, 20(10):555-562.
[22] 李鹏超, 顾学艳.共轭亚油酸对脂质代谢和身体成分组成影响的研究进展[J].食品科学, 2022, 43(7):373-380.
LI P C, GU X Y.A review of the effect of conjugated linoleic acid on lipid metabolism and body composition in humans[J].Food Science, 2022, 43(7):373-380.
[23] MARANGONI F, AGOSTONI C, BORGHI C, et al.Dietary linoleic acid and human health:Focus on cardiovascular and cardiometabolic effects[J].Atherosclerosis, 2020, 292:90-98.
[24] YOON S Y, AHN D, HWANG J Y, et al.Linoleic acid exerts antidiabetic effects by inhibiting protein tyrosine phosphatases associated with insulin resistance[J].Journal of Functional Foods, 2021, 83:104532.
[25] INNES J K, CALDER P C.Omega-6 fatty acids and inflammation[J].Prostaglandins, Leukotrienes and Essential Fatty Acids, 2018, 132:41-48.
[26] 唐佳芮, 魏冰, 石珊珊.α-亚麻酸分离纯化技术研究进展[J].中国油脂, 2020, 45(8):28-31;38.
TANG J R, WEI B, SHI S S.Progress on separation and purification technology of α-linolenic acid[J].China Oils and Fats, 2020, 45(8):28-31;38.
[27] 吴俏槿, 杜冰, 蔡尤林, 等.α-亚麻酸的生理功能及开发研究进展[J].食品工业科技, 2016, 37(10):386-390.
WU Q J, DU B, CAI Y L, et al.Research development of alpha-linolenic acid[J].Science and Technology of Food Industry, 2016, 37(10):386-390.
[28] 李勇, 张健.花生四烯酸及其衍生物在肺动脉高压发生发展中的作用[J].自然杂志, 2022, 44(5):357-368.
LI Y, ZHANG J.The role of arachidonic acid and its derivatives in the development of pulmonary arterial hypertension[J].Chinese Journal of Nature, 2022, 44(5):357-368.
[29] HARAUMA A, HATANAKA E, YASUDA H, et al.Effects of arachidonic acid, eicosapentaenoic acid and docosahexaenoic acid on brain development using artificial rearing of delta-6-desaturase knockout mice[J].Prostaglandins Leukotrienes and Essential Fatty Acids, 2017, 127:32-39.
[30] CHANTAKUN K, BENJAKUL S.Effect of ultrasound-assisted pretreatment in combination with heating on characteristics and antioxidant activities of protein hydrolysate from edible bird’s nest co-product[J].Journal of Food Science and Technology, 2022, 59(10):3908-3917.
[31] 冯晓文, 赵晓涵, 潘骁琦, 等.体外模拟消化对海洋鱼骨胶原低聚肽结构和抗氧化活性的影响[J].食品与发酵工业, 2022, 48(5):173-179.
FENG X W, ZHAO X H, PAN X Q, et al.The effect of simulated digestion in vitro on structure and antioxidant activity of marine fish bone collagen oligopeptides[J].Food and Fermentation Industries, 2022, 48(5):173-179.
[32] PADAYAPPA M, SENTHILKUMAR A, MOORTHI M, et al.Analysis of phytochemical properties, DPPH and frap assay of antioxidant activities of Acalypha indica L.[J].International Journal of Scientific Research, 2021, 9(12):31-34.
[33] SILVA F G D E, HERN NDEZ-LEDESMA L B, AMIGO L, et al.Identification of peptides released from flaxseed (Linum usitatissimum) protein by Alcalase® hydrolysis:Antioxidant activity[J].LWT-Food Science and Technology, 2017, 76:140-146.
NDEZ-LEDESMA L B, AMIGO L, et al.Identification of peptides released from flaxseed (Linum usitatissimum) protein by Alcalase® hydrolysis:Antioxidant activity[J].LWT-Food Science and Technology, 2017, 76:140-146.
[34] 张佩, 陈忠琴, 曹文红, 等.牡蛎抗氧化及降糖肽的结构特征及其体外模拟消化特性[J].食品与发酵工业, 2022, 48(21):196-203.
ZHANG P, CHEN Z Q, CAO W H, et al.Structural characteristics of antioxidant and hypoglycemic peptides from oyster (Crassostrea hongkongensis) and their simulated digestive properties in vitro[J].Food and Fermentation Industries, 2022, 48(21):196-203.
[35] 胡吕霖, 任思婕, 沈清, 等.不同烹饪方式及体外模拟消化环境对鲟鱼蛋白质氧化及消化性的影响[J].食品科学, 2018, 39(20):63-70.
HU L L, REN S J, SHEN Q, et al.Effect of different cooking treatments and in vitro digestion on protein oxidation and digestibility of sturgeon fillets[J].Food Science, 2018, 39(20):63-70.