黄芩苷(C21H18O11,baicalin,BCL)是从双子叶植物黄芩(Scutellaria baicalensis)根部分离得到的一种黄酮类化合物,具有抗炎、抑菌、抗肿瘤等多种药理作用[1]。但由于BCL在水中的溶解度低,极大限制了其在食品及医药行业的应用。为了改善BCL的理化性质,众多研究者将其制备成各种类型的制剂。CHEN等[2]将BCL和大豆磷脂共混后溶解于四氢呋喃中,随后通过恒温水浴回流和真空旋转蒸发制得BCL/大豆磷脂复合物,相较于游离BCL,复合物对1型鸭甲肝病毒表现出更强的抑制作用。LI等[3]将BCL乙醇溶液和β-环糊精水溶液共混60 ℃搅拌24 h后,将得到的悬浮液冷却至室温后过滤,随后将滤液冷冻干燥72 h,制备出BCL/β-环糊精包合物,显著提高了BCL的溶出速率和溶解度,且BCL的相对口服生物利用度提高了2倍。可见,适宜的负载和包封有利于改善BCL的理化性质及生物利用度。然而,上述制剂制备过程多较为复杂。因此,有必要寻求一种简单易行的技术,构建BCL的新制剂,改善其理化性质,扩大其应用范围。
静电纺丝技术是一种制备平均直径在亚微米到纳米范围内超细纤维的新工艺。在此过程中聚合物溶液被置于可控电场中,当施加的电压达到临界值,斥力超过表面张力后,射流就会从溶液的表面喷射出来,当射流向接地的金属收集器移动时,溶剂蒸发,超细干燥纤维沉积[4]。静电纺丝具有简单易行、制备率较高、成本低、纤维性能可控等独特优点;静电纺丝纳米纤维具有纤维直径小、比表面积大、孔隙率高等特点[5];可对功能因子进行负载和可控制释放,提高功能因子的溶出率[6]。YANG等[7]利用静电纺丝技术制备了聚乙烯醇/乙基纤维素/茶多酚复合纳米纤维膜,该纤维膜具有较好耐水性和水蒸气阻隔性能,且表现出良好的抗氧化和抗菌活性,可使猪肉的货架期延长3 d。
虽然目前的静电纺丝基料主要集中在合成聚合物上,但天然生物聚合物具有可再生和可持续的优异特性,使得基于天然聚合物的纤维具有极好的生物相容性和可降解性。因此蛋白质等天然聚合物成为静电纺丝的新型理想基料。
酪蛋白是牛奶中含量最高的蛋白质,由αs1-、αs2-、β-、κ-酪蛋白4部分组成,占牛奶蛋白的80%;其价格低廉,易于获得,可生物降解,并且具有较高的营养价值。天然状态的酪蛋白与钙结合并组装成一种独特的胶束结构,称为酪蛋白胶束(casein micelle,MC),其粒径范围为50~600 nm,平均粒径为150 nm[8]。MC具有内部疏水、表面亲水的特殊结构,是负载活性分子的优良基质。已有研究表明,MC可作为咖啡酸、咖啡酸苯乙酯、原花青素的良好载体,用于改善活性因子的理化性质和抗氧化性[9-10]。然而,目前以MC为基质,通过静电纺丝技术制备纤维膜,以负载活性因子的研究报道较少。
聚乳酸(poly lactic acid,PLA)是一种脂肪族热塑性聚酯,由玉米、土豆等可再生资源生产,具有安全性高、机械性能好、成本低等优点;并且具有良好的生物相容性和生物可降解性,是一种已被美国食品和药物管理局批准的医用辅料[11-12]。近年来,PLA已被广泛用作静电纺丝基料,用于负载活性因子。有报道利用静电纺丝PLA纤维负载香芹酚,实现了香芹酚的控释[13]。另外,采用静电纺丝技术制备的PLA/丝素蛋白纳米纤维用于负载扶他林,可对扶他林进行控释,对大肠杆菌和金黄色葡萄球菌表现出良好的抑制效果[14]。但是,将PLA和MC共混制备静电纺丝纤维并进行生物活性分子的负载研究报道较少。
本文以PLA和MC为基料,采用静电纺丝技术制备出负载BCL的复合纤维膜;采用傅里叶变换红外光谱(Fourier transform infrared,FTIR)、扫描电镜(scanning electron microscope,SEM)等手段表征了复合纤维膜的结构,进而分析了复合纤维膜的理化性质,并评价了复合纤维膜中BCL的释放特性。研究结果不仅可为BCL的负载提供技术依据,而且可为拓宽MC和PLA的应用领域提供参考依据。
1 材料与方法
1.1 材料
黄芩苷、聚乳酸、六氟异丙醇,上海麦克林生化科技有限公司,其他试剂均为分析纯。酪蛋白胶束,实验室自制,总蛋白质含量为(83.26±1.87)%(质量分数)。
1.2 设备
Nicolet iS50型FTIR光谱仪,美国赛默飞世尔科学公司;XD3型X射线多晶衍射仪,北京普析通用仪器有限责任公司;STA 449 F5型TG-DSC热分析仪,德国耐驰仪器制造有限公司;UV-1780双光束紫外可见分光光度计,岛津仪器有限公司;HP-200精密色差仪,河南兄弟仪器设备有限公司;E05静电纺丝机,佛山轻子精密测控技术有限公司;CA200自动型光学接触角测量仪,广东北斗精密仪器有限公司。
1.3 实验方法
1.3.1 纺丝共混溶液的制备
称取适量的MC溶解于六氟异丙醇中,准确称取80 mg的BCL,溶于六氟异丙醇中制成质量浓度为10 mg/mL的溶液。将8 mL的BCL溶液加入8 mL MC溶液中,37 ℃下磁力搅拌1 h。在上述溶液中加入适量的PLA,继续搅拌4 h后得到MC和PLA质量比为1∶3、1∶2、1∶1、2∶1、3∶1的静电纺丝共混溶液(所有比例下MC和PLA总质量为2.56 g)。以不含MC的共混液作为对照。
1.3.2 静电纺丝纤维膜制备
将配制好的MC/PLA/BCL共混溶液吸入10 mL注射器中,配备20 G钢针,安装于注射泵上,采用静电纺丝机进行纤维膜制备。纺丝速度1.0 mL/h,电压19 kV,针尖-滚筒接收间距12.5 cm,滚筒转速120 r/min,纺丝温度25 ℃。将收集的纤维膜置于密封袋中,备用。
1.3.3 SEM表征
将纤维膜置于导电硅胶上,喷金后采用S-3400 N扫描电子显微镜观察表面形貌。
1.3.4 FTIR分析
将纤维膜样品置于衰减全反射元件上,设置光谱分辨率为4 cm-1,扫描32次,记录样品在400~4 000 cm-1的红外光谱。
1.3.5 X射线衍射(x-ray diffraction,XRD)分析
采用X射线单晶衍射仪在Cu Kα辐射下对纤维膜进行XRD扫描。
1.3.6 差示扫描量热-热重(differential scanning calorimetry-thermogravimetry,DSC-TG)分析
用DSC-TG热分析仪测定样品的热分解特性。准确称取6~8 mg样品,置于Al2O3坩锅中,以10 ℃/min的升温速率从30 ℃加热至500 ℃,用空坩埚作空白对照。
1.3.7 色度分析
使用精密色差仪对样品色度进行测量,颜色结果表示为L*(亮度),a*(红度),b*(黄度)。样品色差ΔE的计算如公式(1)所示:
(1)
式中:![]() 的色值;L*、a*、b*,复合纤维膜色值。
的色值;L*、a*、b*,复合纤维膜色值。
1.3.8 接触角测定
将纤维膜裁剪成2 cm×2 cm的矩形,利用接触角仪测量其水接触角,评价复合纤维膜的疏水性。
1.3.9 溶胀性和降解性
参考GHORBANI等[15]的方法对复合纤维膜的溶胀性和降解性进行测定,略有修改。
溶胀性的测定:将纤维膜裁剪成2 cm×2 cm的矩形并称重。随后,将纤维膜浸泡在25 ℃、0.05 mol/L pH 7.4的磷酸盐缓冲液中,分别在0.5、1、1.5、2、2.5、3、4、5、6、8、10、12、24 h时将纤维膜从缓冲液中取出,用吸水纸去除表面水分,称重。溶胀性计算如公式(2)所示:
溶胀率![]()
(2)
式中:m0,纤维膜初始质量,g;mt,纤维膜各时间点溶胀后的质量,g。
降解性的测定:将纤维裁剪成2 cm×2 cm的矩形并称重。随后,将纤维膜在25 ℃、0.05 mol/L pH 7.4的磷酸盐缓冲液中浸泡48 h。然后,将未溶纤维膜小心取出,在60 ℃下干燥48 h,称重。降解性计算如公式(3)所示:
降解率![]()
(3)
式中:m0,纤维膜初始质量,g;m,纤维膜浸泡48 h后剩余质量,g。
1.3.10 黄芩苷的体外释放分析
参考TAN等[16]的方法分析纤维膜中BCL的体外释放特性,略有修改。准确称取100 mg样品,置于具塞锥形瓶中。加入50 mL 0.05 mol/L pH 7.4的磷酸盐缓冲液,于37 ℃、130 r/min下恒温振荡。分别在设定时间点取3 mL溶液,同时补充3 mL缓冲溶液。使用紫外-可见分光光度计在360 nm处测定释放液的吸光度,利用同条件下BCL的标准曲线(y=33.506 74x,R2=0.999 96)计算BCL累积释放率。
释放率![]()
(4)
式中:ρ0,样品中BCL总质量浓度,mg/mL;ρt,t时刻时释放的BCL质量浓度,mg/mL。
1.4 数据统计分析
所有试验重复3次,试验数据采用Excel 2010处理并用平均数±标准偏差表示,用Origin Pro 9.0作图,用SPSS 22进行差异显著性分析,数据间差异显著分析采用Duncan法。
2 结果与分析
2.1 复合纤维膜的微观形貌观察
如图1所示,游离BCL和冻干MC为片层状结构。PLA纤维膜为均匀纤维状结构,直径为1~1.5 μm。添加BCL使PLA纤维出现轻微的卷曲现象,且直径略有增大。这可能是由于BCL与PLA产生相互作用,在PLA分子链间形成了交联作用,进而改变了纺丝溶液的黏度,使纺丝溶液在静电纺丝过程中无法充分拉伸,造成了纤维伸展性降低,与SUN等[17]的研究结果一致。随着MC添加比例在0∶1到1∶1范围内的升高,纤维的整体有序性、均匀性和成纤性逐渐变差,且纤维直径减小,并出现轻微的珠状结构。当MC的添加量进一步增加到与PLA的比例为1∶1时,纤维直径进一步减小,并出现较大的珠状结构。这是因为随着MC添加量的增加,纺丝溶液的黏度降低,共混物中的分子链缠结不足,使其成纤能力下降,纺丝过程中出现静电喷涂现象,产生较大的珠状结构,并使纤维的均匀度下降。BIRANJE等[18]在此前研究中也发现随着酪蛋白添加量的增加,酪蛋白/聚乙烯醇纤维中珠状结构也随之增大。

图1 复合纤维膜SEM图
Fig.1 SEM images of composite fiber membranes
注:0∶1、1∶3、1∶2、1∶1、2∶1和3∶1代表MC和PLA的质量比; 80代表BCL的添加量为80 mg。
研究指出,PLA溶液的流动行为指数小于1,表现为非牛顿剪切稀化行为,这种特性可以增加聚合物链的缠结,进而使静电纺丝纤维直径增大[19-20]。另一方面,MC粒径小于PLA分子链的长度,随着PLA比例的减小,纺丝溶液中的链缠结下降,因此复合纤维直径减小。当MC与PLA质量比进一步增加到2∶1和3∶1时,纤维直径不再减小,约为0.5 μm。这可能是由于MC添加量进一步增大,MC粒子间相互作用增强,通过相互作用形成了稳定的纺丝溶液。可见,MC与PLA质量比为2∶1时具有较好的成纤性能,可通过调节MC和PLA的比例实现对纤维直径的调控。
2.2 复合纤维膜的FTIR分析
如图2所示,MC酰胺I带为1 640 cm-1,酰胺II带为1 516 cm-1。对于单一PLA纤维膜而言,2 990 cm-1处为C—H不对称伸缩振动,1 750 cm-1处为C![]() O伸缩振动,1 454 cm-1和1 382 cm-1处为C—H弯曲振动,1 180 cm-1和1 083 cm-1处为C—O—C伸缩振动,1 043 cm-1处为C—CH3伸缩振动,756 cm-1和869 cm-1处为C—C伸缩振动[13]。BCL在3 481 cm-1处为OH特征峰,在1 606、1 658 cm-1处为C
O伸缩振动,1 454 cm-1和1 382 cm-1处为C—H弯曲振动,1 180 cm-1和1 083 cm-1处为C—O—C伸缩振动,1 043 cm-1处为C—CH3伸缩振动,756 cm-1和869 cm-1处为C—C伸缩振动[13]。BCL在3 481 cm-1处为OH特征峰,在1 606、1 658 cm-1处为C![]() O特征峰,在1 550、1 570 cm-1处为苯环中的C—H特征峰,在1 200~1 300 cm-1处为C—H弯曲振动和C
O特征峰,在1 550、1 570 cm-1处为苯环中的C—H特征峰,在1 200~1 300 cm-1处为C—H弯曲振动和C![]() C伸缩振动[21]。在复合纤维膜中,BCL的特征峰消失,表明BCL被包封在纤维膜内。随着MC比例的增加,复合纤维膜中MC酰胺I带和酰胺II带的特征峰逐渐增强,且MC/PLA的比例大于1∶1后,复合纤维膜在2 826~3 027 cm-1处的特征吸收峰逐渐由PLA特征吸收峰转变为MC特征吸收峰。这一方面可能是因为随着MC比例的增加,纤维直径减小,更有利于纤维内部MC的测定。另一方面,当PLA比例较大时,MC可能位于纤维内部,而当MC/PLA的比例超过1∶1后,由于MC数量较多,而将PLA包封在内部,形成纤维后MC位于表面,因此MC的特征峰强度增大。
C伸缩振动[21]。在复合纤维膜中,BCL的特征峰消失,表明BCL被包封在纤维膜内。随着MC比例的增加,复合纤维膜中MC酰胺I带和酰胺II带的特征峰逐渐增强,且MC/PLA的比例大于1∶1后,复合纤维膜在2 826~3 027 cm-1处的特征吸收峰逐渐由PLA特征吸收峰转变为MC特征吸收峰。这一方面可能是因为随着MC比例的增加,纤维直径减小,更有利于纤维内部MC的测定。另一方面,当PLA比例较大时,MC可能位于纤维内部,而当MC/PLA的比例超过1∶1后,由于MC数量较多,而将PLA包封在内部,形成纤维后MC位于表面,因此MC的特征峰强度增大。
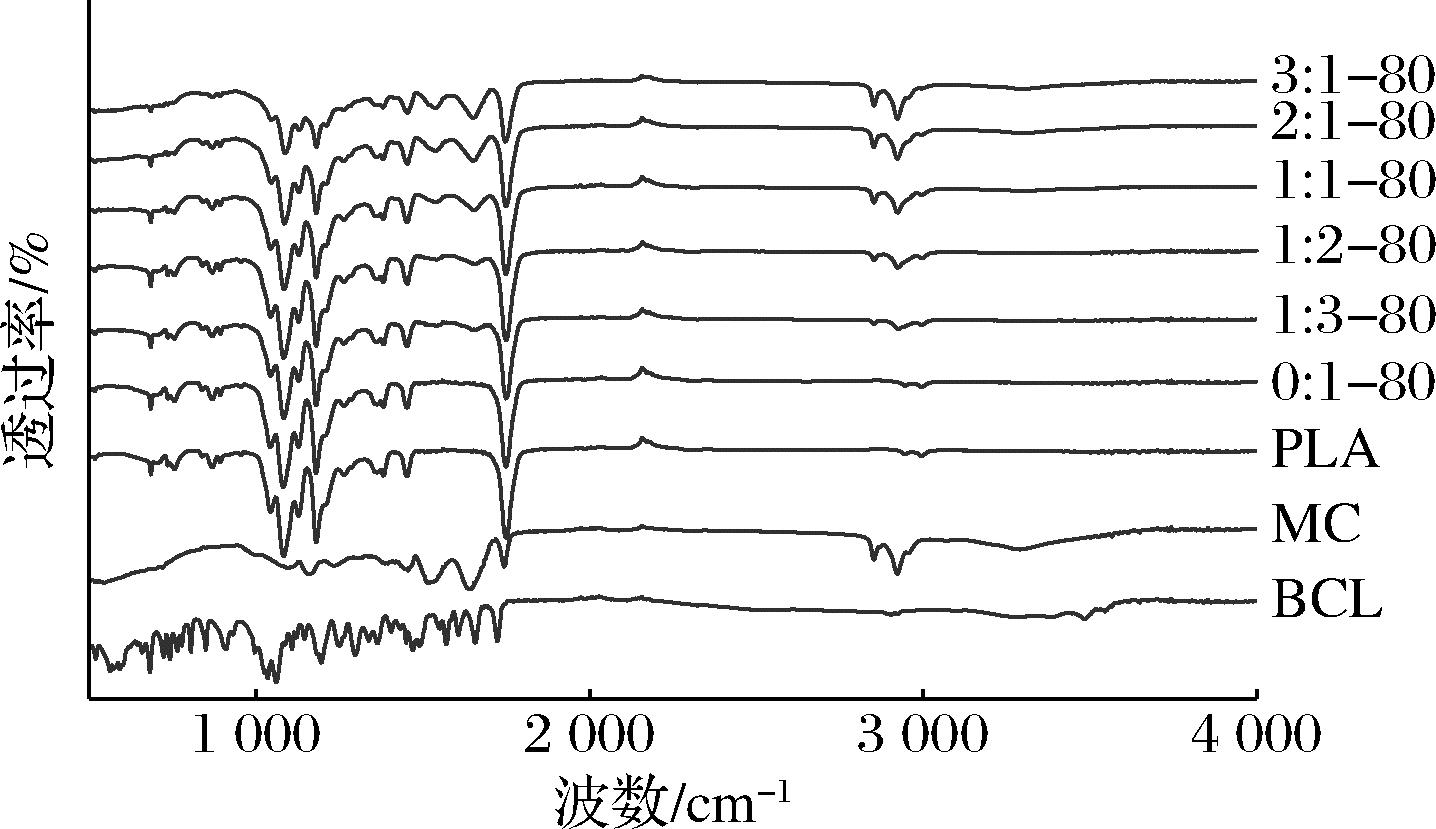
图2 复合纤维膜FTIR图
Fig.2 FTIR images of composite fiber membranes
2.3 复合纤维膜的XRD分析
如图3所示,MC和PLA均出现较宽的峰,说明二者均呈现无定形结构。BCL在12.48°、14.76°、17.08°、21.38°、23.80°、25.52°、28.12°和34.88°处出现特征晶体衍射峰,表明BCL为晶体形态[21]。然而,PLA/BCL和MC/PLA/BCL纤维膜中BCL的特征衍射峰消失,表明BCL被PLA和MC/PLA完全包封,这与FTIR研究结果一致。在MC/PLA/BCL纤维膜中出现MC的衍射峰,但强度小于单一MC的强度,并且轻微左移,这可能是因为PLA的加入改变了原溶液的性质,且产生了非共价相互作用。

图3 复合纤维膜XRD图
Fig.3 XRD images of composite fiber membranes
2.4 复合纤维膜的热分解特性分析
由图4-a可知,BCL在221 ℃附近出现熔融吸收峰;PLA纤维膜在66 ℃附近出现吸收峰,为PLA的玻璃化转变温度[22],且在170 ℃附近出现熔融吸收峰。PLA/BCL和MC/PLA/BCL复合纤维膜表现出与PLA相似的DSC曲线,这是因为复合纤维膜具有相似的结构。但在MC/PLA/BCL复合纤维膜中PLA的玻璃化转变温度略有降低,这可能是因为BCL和MC的加入使PLA在静电纺丝过程中改变了聚合物分子链的排列,打乱了PLA原有分子链的排列规则。HAN等[23]研究发现,茶多酚和肉桂醛的加入使聚乳酸纤维膜的玻璃化转化温度略有降低,与本文研究结果一致。
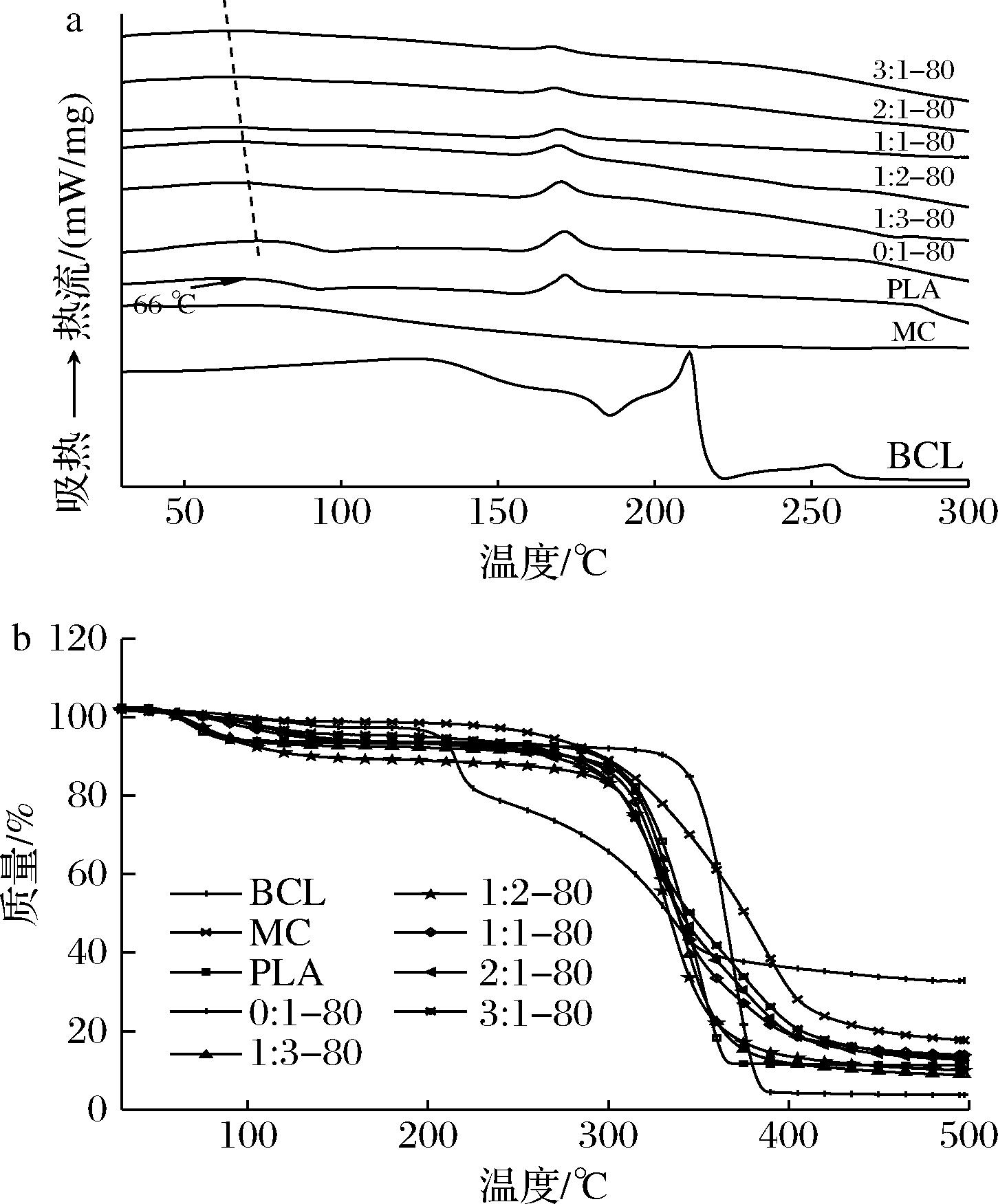
a-DSC曲线;b-TG曲线
图4 复合纤维膜DSC-TG曲线
Fig.4 DSC-TG curves of composite fiber membranes
如图4-b所示,MC和BCL分别在270~410 ℃和200~350 ℃失重,表明分子热分解。PLA纤维膜在260~360 ℃出现较大的质量损失,由PLA链断裂所致[24]。所有纤维膜均在60 ℃开始失重,这是由于溶剂蒸发所致。与PLA纤维膜相比,PLA/BCL纤维膜开始失重的温度升高,表明BCL的添加增强了PLA纤维膜的热稳定性。与PLA/BCL纤维膜相比,MC/PLA/BCL纤维膜表现出更高的质量保留率,表明MC的添加进一步提高了复合纤维膜的热稳定性。这是因为添加MC后,MC与PLA之间可产生非共价相互作用,且MC粒子之间存在相互作用,从而使纤维膜的热稳定性进一步增强。AYDOGDU等[25]研究发现,添加大豆蛋白降低了聚环氧乙烷/羟丙甲纤维素纤维膜的质量损失,增强了复合纤维膜的热稳定性,与本文的研究结果一致。
2.5 复合纤维膜的水接触角和色度分析
由图5和表1可知,PLA膜疏水性较强,是一种典型的疏水材料[26]。所有纤维膜的水接触角均大于90°,表现出明显的疏水特性。BCL对单一PLA纤维膜的水接触角影响不大,这可能是因为BCL添加量较少,且被完全包封在纤维中。随着MC的添加,复合纤维膜的水接触角逐渐减小。这可能是因为随着MC比例的增加,纤维外层的MC增加,使其疏水性下降。另一方面,随着MC添加比例的增大,纤维直径减小,纤维排列成膜时的间隙增加,水接触角减小。有研究表明,纤维直径越小,孔隙率越高,吸水率增大,接触角减小[27]。

图5 复合纤维膜水接触角图
Fig.5 Water contact angle diagram of composite fiber membranes
色度方面,负载BCL的复合膜亮度值L*为93~95,表现出一定的黄色度,这是由于BCL呈现黄色度所致。随着MC添加比例的增大,复合膜的a*值逐渐减小,b*值基本呈现增大的趋势。可见,MC的添加降低了BCL的红色度;且因其呈现乳黄色,因此增加了复合纤维膜的黄色度。
表1 复合纤维膜的接触角及色度
Table 1 Water contact angle and chromaticity of composite fiber membranes

MC∶PLABCL/mg接触角/°色度L∗a∗b∗ΔEBCL80.10±0.342.07±0.0125.64±0.46MC88.92±0.54-0.50±0.056.30±0.15PLA0139.05±1.6994.25±0.160.99±0.15-0.68±0.0429.90±0.460∶180136.27±1.04A93.31±0.26C0.59±0.06B5.95±0.06E23.75±0.48A1∶380134.01±1.18AB93.92±0.12AB0.79±0.02A8.92±0.18CD21.73±0.77B1∶280132.63±0.22B93.26±0.25C0.78±0.06A8.63±0.37D21.55±0.51B1∶180129.06±1.56C93.59±0.22BC0.63±0.06B9.41±0.10BC21.15±0.38B2∶180126.05±2.37D93.21±0.48C0.41±0.03C9.66±0.30AB20.74±0.43B3∶180114.81±1.18E94.23±0.23A0.18±0.02D10.05±0.46A21.13±0.43B
注:不同大写字母表示不同样品同一参数差异显著(P<0.05)(下同)。
2.6 复合纤维膜的降解性分析
如图6所示,PLA纤维膜和PLA/BCL纤维膜在48 h内的降解率均低于8%,负载BCL对PLA纤维膜的降解率影响不大。PLA作为一种典型的疏水材料,其在水中降解性较差。随着MC添加比例在0∶1~1∶1增加,纤维膜的降解率明显增大,这是因为MC增加了纤维膜的溶解性。但当MC比例进一步增加到2∶1和3∶1后,纤维膜的降解率随MC添加量的增加变化不显著(P<0.05),这可能是因为当MC/PLA的比例超过1∶1后,复合纤维膜由PLA包覆MC型转变为MC包覆PLA型,因此MC的添加量增加对复合纤维膜降解率影响不大。另外,在MC与PLA的比例为0∶1~2∶1,复合纤维膜的降解率随MC添加量的增加呈线性增大。可见,可通过添加MC以调节PLA纤维膜的降解率。
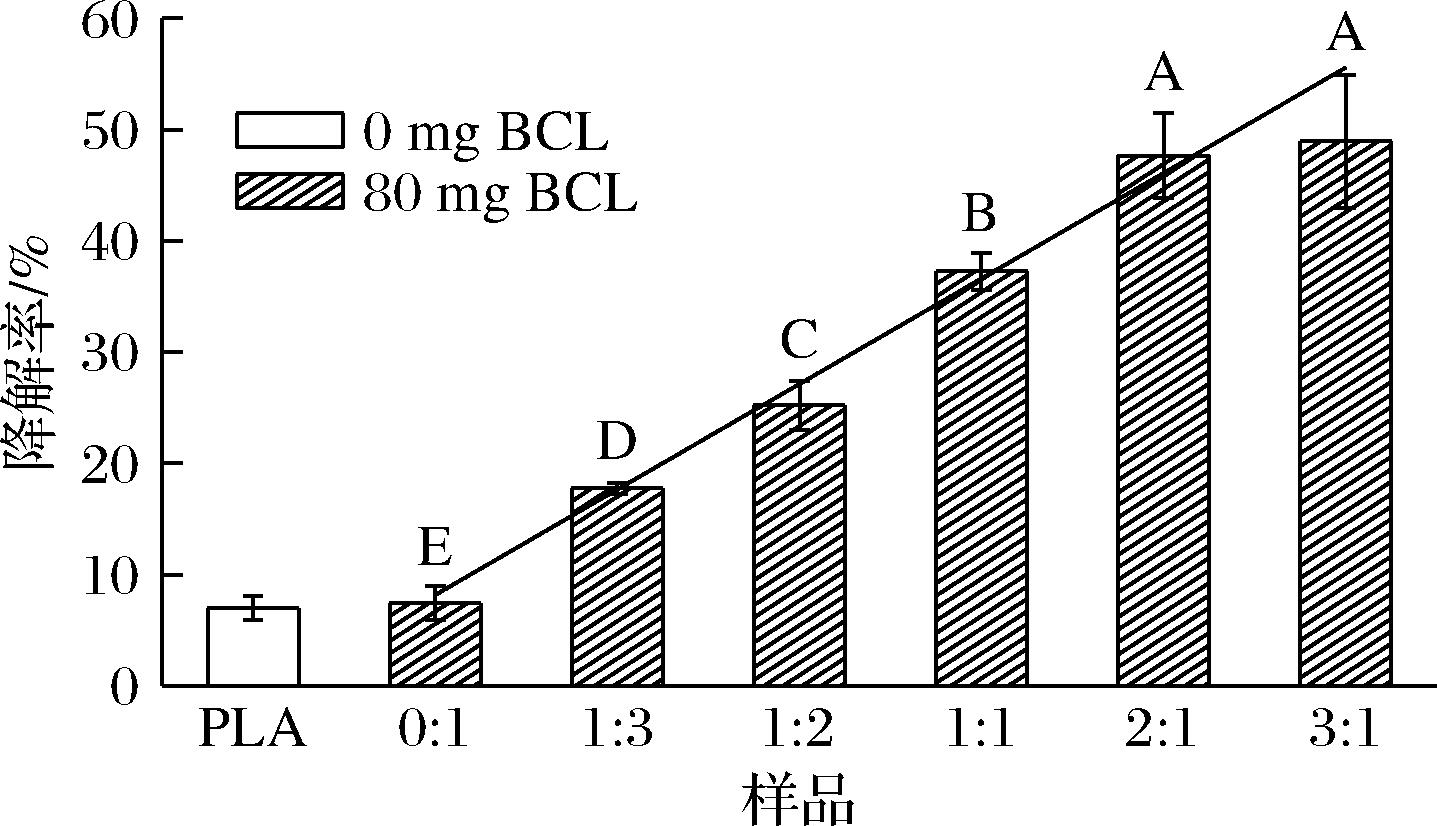
图6 复合纤维膜降解率
Fig.6 Degradation rate of composite fiber membranes
2.7 复合纤维膜的溶胀性分析
由图7和表2可知,PLA纤维膜和PLA/BCL纤维膜在24 h的溶胀率只有(9.25±1.05)%和(8.82±0.62)%。添加一定量MC后,纤维膜的溶胀性迅速增大,这是因为MC为水溶性多孔粒子,具有较高的水合性;且随着MC的添加,纤维直径减小,纤维间孔隙增大,吸水性增强。MC与PLA比例为1∶3的复合纤维膜溶胀性最好,在2 h达到最大溶胀率(228.28±3.95)%。之后,随着MC添加量的进一步增大,复合纤维膜最大溶胀率逐渐降低,达到最大溶胀率的时间也有所减少。这是因为MC是水溶性分子,其在水中溶解,使膜的质量降低所致,与LIU等[28]的研究结果相似。

图7 复合纤维膜溶胀性
Fig.7 Swelling rate of composite fiber membranes
表2 复合纤维膜最大溶胀率及最大溶胀时间
Table 2 Maximum swelling rate and its time of composite fiber membranes

样品名称最大溶胀率/%最大溶胀率时间/hPLA9.25±1.05240∶1-808.82±0.62F241∶3-80228.28±3.95A21∶2-80208.97±6.29B1.51∶1-80151.35±7.44C22∶1-8098.56±2.55D1.53∶1-8088.68±4.63E1
2.8 复合纤维膜中BCL的体外释放性分析
如图8所示,游离BCL在缓冲液中迅速释放,且随着时间的延长释放率降低,说明其发生了轻度降解,与已有报道类似[29]。由于PLA为疏水性分子,经PLA负载后,BCL释放率极低。在MC/PLA/BCL复合纤维膜中,BCL在2 h内迅速释放,之后释放率迅速减缓,并在3 h后维持稳定。由于MC水溶性较好,其添加量越多,BCL释放率越高。包封在玉米醇溶蛋白纤维中的姜黄素也表现出10 min内爆发性释放的特性,与本文研究结果类似[30]。由此可见,添加MC有利于增加BCL从PLA纤维膜中的释放率。

图8 复合纤维膜中BCL释放率曲线
Fig.8 Profiles of BCL release rate from composite fiber membranes
3 结论
以PLA和MC为基质,采用静电纺丝技术制备了复合纤维膜,实现了BCL的负载。当MC与PLA质量比达到2∶1后,复合纤维具有较规则的形貌,且直径较小。添加MC改善了PLA纤维膜的疏水性,提高了其溶胀率,且增加了BCL的释放率。另外,MC的添加降低了纤维膜的红色度,增加了黄色度,改善了颜色。经MC/PLA复合纤维膜负载后,减缓了BCL的释放率。
[1] YANG J Y, LI M, ZHANG C L, et al.Pharmacological properties of baicalin on liver diseases:A narrative review[J].Pharmacological Reports, 2021, 73(5):1230-1239.
[2] CHEN Y, YUAN W J, YANG Y H, et al.Inhibition mechanisms of baicalin and its phospholipid complex against DHAV-1 replication[J].Poultry Science, 2018, 97:3816-3825.
[3] LI J, JIANG Q H, DENG P, et al.The formation of a host-guest inclusion complex system between β-cyclodextrin and baicalin and its dissolution characteristics[J].The Journal of Pharmacy and Pharmacology, 2017, 69(6):663-674.
[4] DOSHI J, RENEKER D H.Electrospinning process and applications of electrospun fibers[J].Journal of Electrostatics, 1995, 35(2-3):151-160.
[5] HUANG H, SONG Y D, ZHANG Y Q, et al.Electrospun nanofibers:Current progress and applications in food systems[J].Journal of Agricultural and Food Chemistry, 2022, 70(5):1391-1409.
[6] CHEN X, LI H H, LU W P, et al.Antibacterial porous coaxial drug-carrying nanofibers for sustained drug-releasing applications[J].Nanomaterials, 2021, 11(5):1316.
[7] YANG Y F, SHI Y Y, CAO X K, et al.Preparation and functional properties of poly(vinyl alcohol)/ethyl cellulose/tea polyphenol electrospun nanofibrous films for active packaging material[J].Food Control, 2021, 130:108331.
[8] FOX P F, BRODKORB A.The casein micelle:Historical aspects, current concepts and significance[J].International Dairy Journal, 2008, 18(7):677-684.
[9] QIN J J, YANG M, WANG Y C, et al.Interaction between caffeic acid/caffeic acid phenethyl ester and micellar casein[J].Food Chemistry, 2021, 349:129154.
[10] 王楠, 杨敏, 郑杰, 等.酪蛋白胶束对原花青素稳定性的影响[J].食品与发酵工业, 2023, 49(3):164-174.
WANG N, YANG M, ZHENG J, et al.Effect of casein micelle on the stability of procyanidins[J].Food and Fermentation Industries, 2023, 49(3):164-174.
[11] DI LORENZO M L.Poly(L-lactic acid)/poly(butylene succinate) biobased biodegradable blends[J].Polymer Reviews, 2021, 61(3):457-492.
[12] ARMENTANO I, BITINIS N, FORTUNATI E, et al.Multifunctional nanostructured PLA materials for packaging and tissue engineering[J].Progress in Polymer Science, 2013, 38(10-11):1720-1747.
[13] ALTAN A, AYTAC Z, UYAR T.Carvacrol loaded electrospun fibrous films from zein and poly(lactic acid) for active food packaging[J].Food Hydrocolloids, 2018, 81:48-59.
[14] MA Y L, LI J.An antibacterial coaxial electrospun polylactic acid/silk fibroin loaded with nano-ZnO and Voltaren[J].Materials Letters, 2022, 325:132804.
[15] GHORBANI M, MAHMOODZADEH F, YAVARI MAROUFI L, et al.Electrospun tetracycline hydrochloride loaded zein/gum tragacanth/poly lactic acid nanofibers for biomedical application[J].International Journal of Biological Macromolecules, 2020, 165:1312-1322.
[16] TAN H Y, ZHANG Y H, SUN L X, et al.Preparation of nano sustained-release fertilizer using natural degradable polymer polylactic acid by coaxial electrospinning[J].International Journal of Biological Macromolecules, 2021, 193:903-914.
[17] SUN C K, ZOU L M, XU Y J, et al.Ibuprofen‐loaded poly (lactic acid) electrospun mats:The morphology, physicochemical performance, and in vitro drug release behavior[J].Macromolecular Materials and Engineering, 2020, 305(12):2000457.
[18] BIRANJE S, MADIWALE P, ADIVAREKAR R V.Porous electrospun Casein/PVA nanofibrous mat for its potential application as wound dressing material[J].Journal of Porous Materials, 2019, 26(1):29-40.
[19] KRIEGEL C, KIT K M, MCCLEMENTS D J, et al.Electrospinning of chitosan-poly(ethylene oxide) blend nanofibers in the presence of micellar surfactant solutions[J].Polymer, 2009, 50(1):189-200.
[20] NEO Y P, SWIFT S, RAY S, et al.Evaluation of Gallic acid loaded zein sub-micron electrospun fibre mats as novel active packaging materials[J].Food Chemistry, 2013, 141(3):3192-3200.
[21] LI Y, HE Z D, ZHENG Q E, et al.Hydroxypropyl-β-cyclodextrin for delivery of baicalin via inclusion complexation by supercritical fluid encapsulation[J].Molecules, 2018, 23(5):1169.
[22] 崔心想, 王艳贺, 韩立彬, 等.聚乳酸/聚酯酰胺复合纳米纤维膜制备及性能[J].工程塑料应用, 2020, 48(3):14-21.
CUI X X, WANG Y H, HAN L B, et al.Preparation and properties of polylactic acid/polyesteramide composite nanofiber film[J].Engineering Plastics Application, 2020, 48(3):14-21.
[23] HAN Y, DING J, ZHANG J T, et al.Fabrication and characterization of polylactic acid coaxial antibacterial nanofibers embedded with cinnamaldehyde/tea polyphenol with food packaging potential[J].International Journal of Biological Macromolecules, 2021, 184:739-749.
[24] GONÇALVES R P, DA SILVA F F F, PICCIANI P H S, et al.Morphology and thermal properties of core-shell PVA/PLA ultrafine fibers produced by coaxial electrospinning[J].Materials Sciences and Applications, 2015, 6(2):189-199.
[25] AYDOGDU A, YILDIZ E, AYHAN Z, et al.Nanostructured poly(lactic acid)/soy protein/HPMC films by electrospinning for potential applications in food industry[J].European Polymer Journal, 2019, 112:477-486.
[26] MIN T T, SUN X L, YUAN Z P, et al.Novel antimicrobial packaging film based on porous poly(lactic acid) nanofiber and polymeric coating for humidity-controlled release of thyme essential oil[J].LWT, 2021, 135:110034.
[27] LIU Y Y, DENG L L, ZHANG C, et al.Tunable physical properties of ethylcellulose/gelatin composite nanofibers by electrospinning[J].Journal of Agricultural and Food Chemistry, 2018, 66(8):1907-1915.
[28] LIU Y W, WANG S Y, LAN W J, et al.Fabrication of polylactic acid/carbon nanotubes/chitosan composite fibers by electrospinning for strawberry preservation[J].International Journal of Biological Macromolecules, 2019, 121:1329-1336.
[29] 王雷, 王学艳, 周雪琴, 等.黄芩苷在不同溶媒中的稳定性研究[J].中国药师, 2006, 9(2):129-131.
WANG L, WANG X Y, ZHOU X Q, et al.Study on the stability of baicalin in different solvents[J].China Pharmacist, 2006, 9(2):129-131.
[30] WANG H L, HAO L L, WANG P, et al.Release kinetics and antibacterial activity of curcumin loaded zein fibers[J].Food Hydrocolloids, 2017, 63:437-446.