海带(Laminaria japonica)属褐藻纲,海带目,常见于东亚国家[1],是我国重要的经济藻类之一;其富含膳食纤维、维生素、矿物质等营养成分[2],且含有海带多糖、活性肽、碘、甘露醇等具有抗炎、抗血栓、降血糖的功能活性物质[3-5]。虽然海带在我国已有很长的食用历史,但目前市面上仍以盐渍、淡干海带、即食海带等初加工产品为主,附加值较低,为促进海带产业进一步发展,我国已逐渐开发出一些附加值较高的精加工产品,如海带面条、海带豆腐等[6-7],但与韩国、日本相比,我国海带精加工产品在产品类型、技术含量等多方面仍需继续创新。
褐藻胶是海带多糖中的一种,由β-D-甘露糖醛酸(β-D-mannuronic acid, M)及其C5差向异构体α-L-古罗糖醛酸(α-L-guluronic acid, G)2种单体随机聚合而成的高分子线性聚合物[8-9]。褐藻胶及其盐类可与Ca2+等二价阳离子交联(主要与G序列结合),形成具有三维网络结构的水凝胶[10]。此凝胶属于热不可逆凝胶,生物相容性高,保水性好,安全无毒,因此常被开发成医用敷料或在食品领域开发成产品、包装材料、食品添加剂等。例如DE等[11]以褐藻酸钙作为包装材料包埋酱油,制成具有良好释放性的酱油胶囊;罗阳等[12]以碳酸钙为钙源,在低脂猪肉中添加适量的褐藻酸钠可有效改善肉糜的质构特性和蒸煮损失率;许加超等[13]研发出具有排铅、补钙、补充膳食纤维功效的褐藻酸缓释钙离子凝胶果冻。
目前以海带为原料开发的褐藻酸钙凝胶食品较少,且有研究表明改变Ca2+浓度可以显著影响褐藻酸钙的凝胶特性[14]。因此在前期研发出海带褐藻胶食用颗粒基础之上[15],进一步探究CaCl2浓度变化对其质构特性、凝胶强度、感官品质、持水率、蒸煮损失率、冻融稳定性和凝胶组织微观结构等指标的影响,并确定制备海带褐藻胶食用颗粒的最适CaCl2浓度,以期为海带褐藻酸钙凝胶类产品提供数据参考,并为海带新产品开发提供理论依据。
1 材料与方法
1.1 材料与试剂
盐渍海带,福建连江;β-环糊精,孟州市华兴生物化工有限责任公司;碳酸氢钠,天津渤化永利化工股份有限公司;氯化钙,江苏科伦多食品配料有限公司;硝酸银,深圳市博林达科技有限公司。
1.2 仪器与设备
TK-12绞肉机,浙江应晓工贸有限公司;HWS-28数显恒温水浴,上海一恒科学仪器有限公司;L18-Y68S静音真空高速破壁机,九阳股份有限公司;TA-XT plus质构仪,英国Stable Micro System公司;Centrifuge 5810R离心机,德国Eppendorf公司;SCIENTZ-30 ND冷冻干燥机,宁波新芝生物科技股份有限公司;SU8100扫描电子显微镜,日本Hitachi公司。
1.3 实验方法
1.3.1 海带褐藻胶食用颗粒的制备[15]
海带褐藻食用颗粒制备工艺:
盐渍海带→清洗→脱盐→脱腥→搅碎→加热转化→磨浆细化→固化成型→漂洗→真空包装
清洗:用海绵刷将盐渍海带在自来水中刷洗干净,再用纯水荡洗干净。
脱盐:盐渍海带采用浸泡脱盐的方法,取150 g盐渍海带,用海绵刷在清水中刷洗干净,随后浸泡在25 ℃、4 L纯水中12 h,每隔3 h换1次纯水(期间每隔1 h搅拌1次),换水时取适量海带浸泡液,往里滴入0.1 mol/L AgNO3溶液观察是否有白色沉淀,并取一小块脱盐海带品尝,当最后1次海带浸泡液加入0.1 mol/L AgNO3溶液后无明显沉淀生成,且脱盐海带入口无明显盐味即为脱盐终点。
脱腥:将脱盐海带切成大小均匀的海带条,25 ℃浸于30 g/L的β-环糊精中脱腥90 min,结束后用纯水漂洗3次洗去多余的脱腥液。
搅碎:用绞肉机将脱腥海带搅碎,制成海带碎。
加热转化:称取100 g海带碎和3 g碳酸氢钠粉末,再加入100 mL纯水将碳酸氢钠与海带碎充分混合,置于100 ℃恒温水浴锅中不断搅拌11 min。
磨浆细化:将加热转化后的海带倒入破壁机中,并加入海带质量与水体积比例为1∶1.1的纯水研磨5 min。
固化成型:用滴管取适量海带浆于圆形模具中,于室温下在不同质量浓度(10、20、30、40、50 g/L)CaCl2溶液中脱模,静置固化4 min。
漂洗:固化时间结束后迅速捞出置于纯水中浸泡,洗去海带褐藻胶食用颗粒表面多余的钙化剂。
真空包装:将漂洗好的海带褐藻胶食用颗粒置于包装袋中真空包装。
1.3.2 感官评价
以定量描述法作为感官评价的方法,组织8位食品专业研究生(4男4女)组成感官评价小组,对海带褐藻胶食用颗粒进行品尝,并从外观、口感、风味这3个维度进行打分,权重分别设置为30%、40%、30%,综合得分去掉最高分及最低分后取平均值。感官综合评分如表1所示。
表1 海带褐藻胶食用颗粒感官综合评分标准
Table 1 Standard of comprehensive sensory evaluation for kelp alginate edible granules

指标评分标准得分/分外观(30%)球形、外表完整光滑、大小、质地均一、嫩绿色、色泽光亮令人愉悦60~100球形、外表较完整光滑、有少量海带碎渣、大小基本一致、深绿色、色泽一般30~59外形不规则、表面粗糙、海带碎渣较多、棕绿色、色泽暗淡令人不悦 0~29口感(40%)硬度适中、富有弹牙感、光滑爽口、无皮肉感60~100较硬或较软、弹牙感一般、有皮肉感30~59很硬或很软、无弹牙感、皮肉感重 0~29风味(30%)有海带香味、无不良味道60~100海带香味较淡、无不良味道30~59无海带香味、不良味道重 0~29
1.3.3 全质构测定
参考CUI等[16]的方法,稍作修改。取一颗样品,用滤纸将表面水分擦干,采用TA-XT质构仪测定其质构特性,测定条件:P/36R探头,全质构(texture profile analysis,TPA)模式,测前速度、测试速度、测后速度都为1.0 mm/s,压缩率30%,自动触发,触发力5 g,重复测定2次,间隔5 s。每次测量6个平行样,结果取平均值。
1.3.4 凝胶强度测定
样品前处理及测定方法同1.3.3节,凝胶强度按公式(1)计算[17]。
凝胶强度![]()
(1)
式中:硬度为第1次压缩的最大峰值。
1.3.5 持水率测定
取2~3 g样品,其质量记作M,将样品置于50 mL离心管中,然后于20 ℃、10 000 r/min离心20 min,结束后取出样品吸干表面多余水分后称重,其质量记作m。持水率按公式(2)计算。
持水率![]()
(2)
1.3.6 蒸煮损失率测定
取约2~3 g海带褐藻胶食用颗粒,精确称重记作m1,随后置于蒸煮袋中密封,并于90 ℃水浴锅中加热20 min,冷却至室温,将样品表面水分擦干立即称重记作m2。样品的蒸煮损失率按公式(3)计算。
蒸煮损失率![]()
(3)
1.3.7 冻融稳定性测定
冻融稳定性是将样品反复解冻冷冻后样品失水程度来表征。参考SHU等[18]的方法稍作修改。取2~3 g样品其质量记作M0于50 mL离心管中,置于-20 ℃下冷冻24 h,之后将样品于25 ℃水浴中解冻1 h,最后在20 ℃、1 000 r/min下离心5 min,离心后将样品表面水分擦干称重,其质量记作m0,以上操作重复5次。析水率按公式(4)计算。
析水率![]()
(4)
1.3.8 扫描电镜分析
将海带褐藻胶食用颗粒对半切后置于冷冻干燥机内真空干燥72 h,将冻干样对半切并紧贴于导电碳膜双面胶上,随后置于离子溅射仪样品台上喷金30 s后用扫描电子显微镜(scanning electron microscope,SEM)观察微观结构。
2 结果与分析
2.1 CaCl2浓度对海带褐藻胶食用颗粒外观影响
由图1可观察到,在其他制备工艺参数一致的情况下,10 g/L CaCl2下制得的产品体积最大,随着CaCl2浓度的增加,产品的体积逐渐变小,当CaCl2浓度为30~50 g/L时,体积变小的幅度趋于稳定。这可能主要是因为随着CaCl2浓度增大,产品接触到高浓度的Ca2+后交联密度提高,褐藻酸盐中带负电的羧基与Ca2+相互作用,在静电吸引下产品球状体收缩[19],使凝胶网络中的水分排出,从而导致产品体积随着Ca2+浓度增加而缩小。

图1 不同CaCl2浓度对海带褐藻胶食用颗粒外观的影响
Fig.1 Effect of CaCl2 concentration on the kelp alginate edible granules appearance
2.2 CaCl2浓度对海带褐藻胶食用颗粒感官评分的影响
感官评价是对产品进行直观评价的重要方法。由图2可知,随着Ca2+浓度的增加,产品的感官评分呈先升高后降低的趋势,当10 g/L CaCl2时,感官评分最低,此时产品外观较好呈现嫩绿色,但海带风味不明显,组织较松散,硬度、咀嚼性低,适口性较差。当2% CaCl2时,感官评分最高,此时产品外观嫩绿晶亮,入口爽滑弹牙,有海带特有风味,适口性好。当Ca2+浓度为30~50 g/L时,产品硬度、咀嚼度降低,导致口感变差,感官评分随之降低。
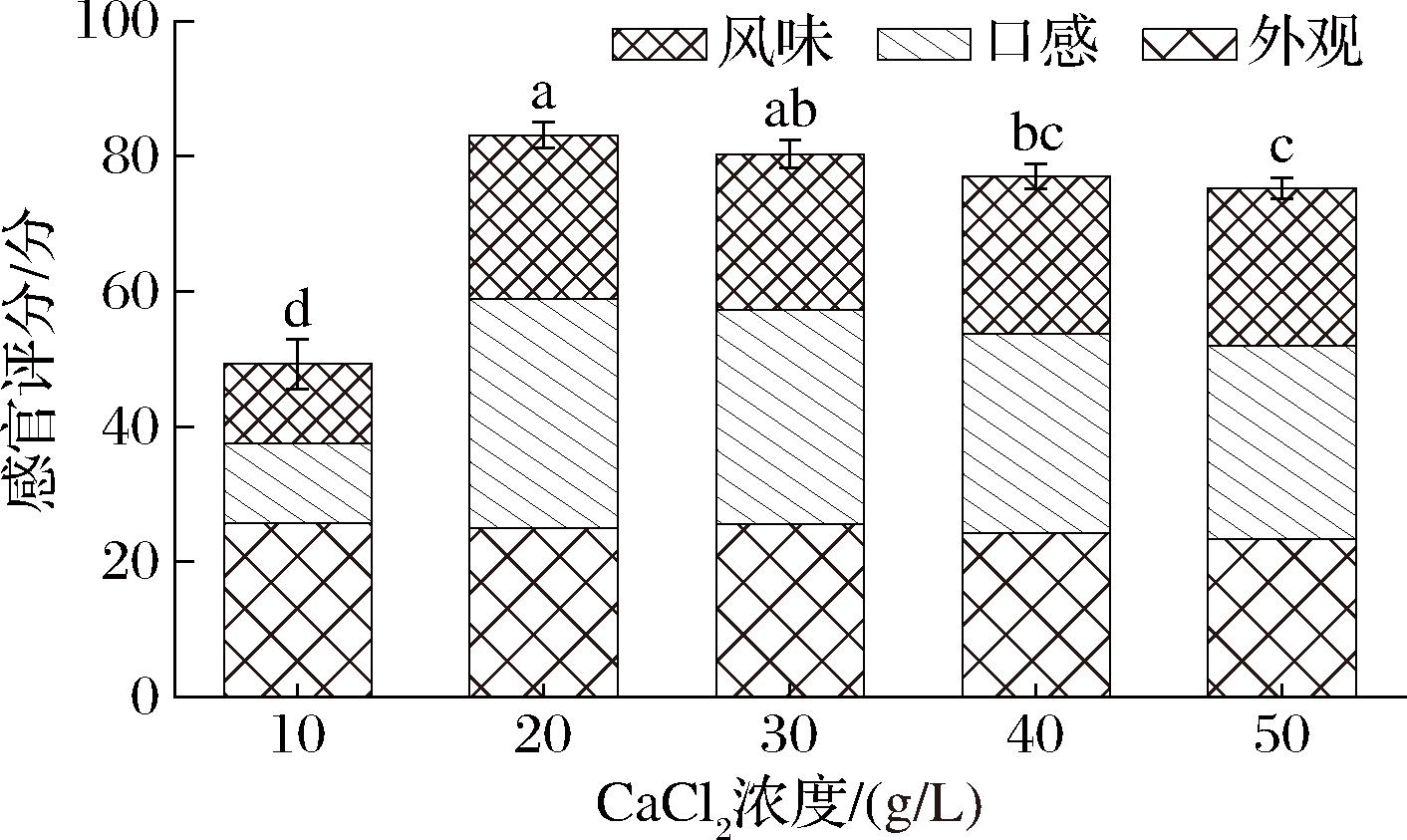
图2 CaCl2浓度对海带褐藻胶食用颗粒感官评分的影响
Fig.2 Effect of CaCl2 concentration on sensory scores of kelp alginate edible granules
注:不同字母代表不同水平之间差异显著(P<0.05)(下同)。
2.3 CaCl2浓度对海带褐藻胶食用颗粒TPA和凝胶强度影响
TPA是模拟人体口腔二次咀嚼试验,是一种重要的综合描述食品物性的质构分析法;凝胶强度是表征凝胶特性的重要指标之一。由表2可知,各组产品之间的硬度、弹性、内聚性、咀嚼性、回复性、凝胶强度均存在差异;随着CaCl2浓度的增加,产品的硬度、咀嚼性、凝胶强度均呈现先增加后降低的趋势,除凝胶强度外其余指标均在20 g/L CaCl2时达到峰值,这与陈梦洁等[20]的研究结果类似;弹性、内聚性则总体呈现逐渐上升的趋势;产品回复性除在50 g/L CaCl2下略有降低外在其余浓度下无显著变化。上述结果说明Ca2+浓度变化可以显著影响产品的质构特性和凝胶强度;Ca2+浓度增加,导致产品硬度、咀嚼性、凝胶强度先上升后下降可能是因为Ca2+浓度较低时,无法与产品中的褐藻酸盐完全交联,导致产品凝胶强度较低,Ca2+浓度继续增加可促进其与褐藻酸盐未结合位点更好的交联,但CaCl2浓度过高可能会促进褐藻酸盐分子之间的交联,抑制构成凝胶网络的均匀蛋盒二聚体的形成[21],从而导致产品凝胶强度和硬度等TPA指标降低。
表2 CaCl2浓度对海带褐藻胶食用颗粒TPA和凝胶强度的影响
Table 2 Effect of CaCl2 concentration on TPA and gel strength of kelp alginate edible granules
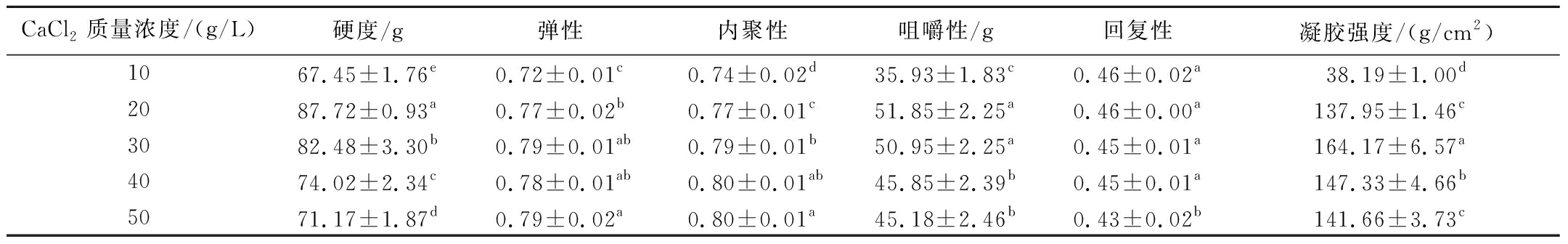
CaCl2质量浓度/(g/L)硬度/g弹性内聚性咀嚼性/g回复性凝胶强度/(g/cm2)1067.45±1.76e0.72±0.01c0.74±0.02d35.93±1.83c0.46±0.02a38.19±1.00d2087.72±0.93a0.77±0.02b0.77±0.01c51.85±2.25a0.46±0.00a137.95±1.46c3082.48±3.30b0.79±0.01ab0.79±0.01b50.95±2.25a0.45±0.01a164.17±6.57a4074.02±2.34c0.78±0.01ab0.80±0.01ab45.85±2.39b0.45±0.01a147.33±4.66b5071.17±1.87d0.79±0.02a0.80±0.01a45.18±2.46b0.43±0.02b141.66±3.73c
注:不同小写字母表示同一列之间的差异显著(P<0.05)。
2.4 CaCl2浓度对海带褐藻胶食用颗粒水分的影响
持水率是水凝胶重要的特性之一,它可以表征凝胶在外界作用力下保留水分的能力;蒸煮损失率可间接表征凝胶稳定性的强弱程度。由图3可知,随着Ca2+浓度增加,产品之间的持水率、蒸煮损失率均存在显著差异。海带褐藻胶食用颗粒的持水率随Ca2+浓度增加而逐渐降低,这与SHU等[18]研究结果一致,10 g/L CaCl2时产品持水率最高为97.02%,50 g/L CaCl2时产品持水率最低为73.24%;产品的蒸煮损失率则随Ca2+浓度增加而逐渐升高,50 g/L CaCl2下制得的产品蒸煮损失率是10 g/L CaCl2下制得的产品蒸煮损失率的4倍,有研究表明持水能力越强,蒸煮损失率则越低[22],这与本实验结果保持一致。
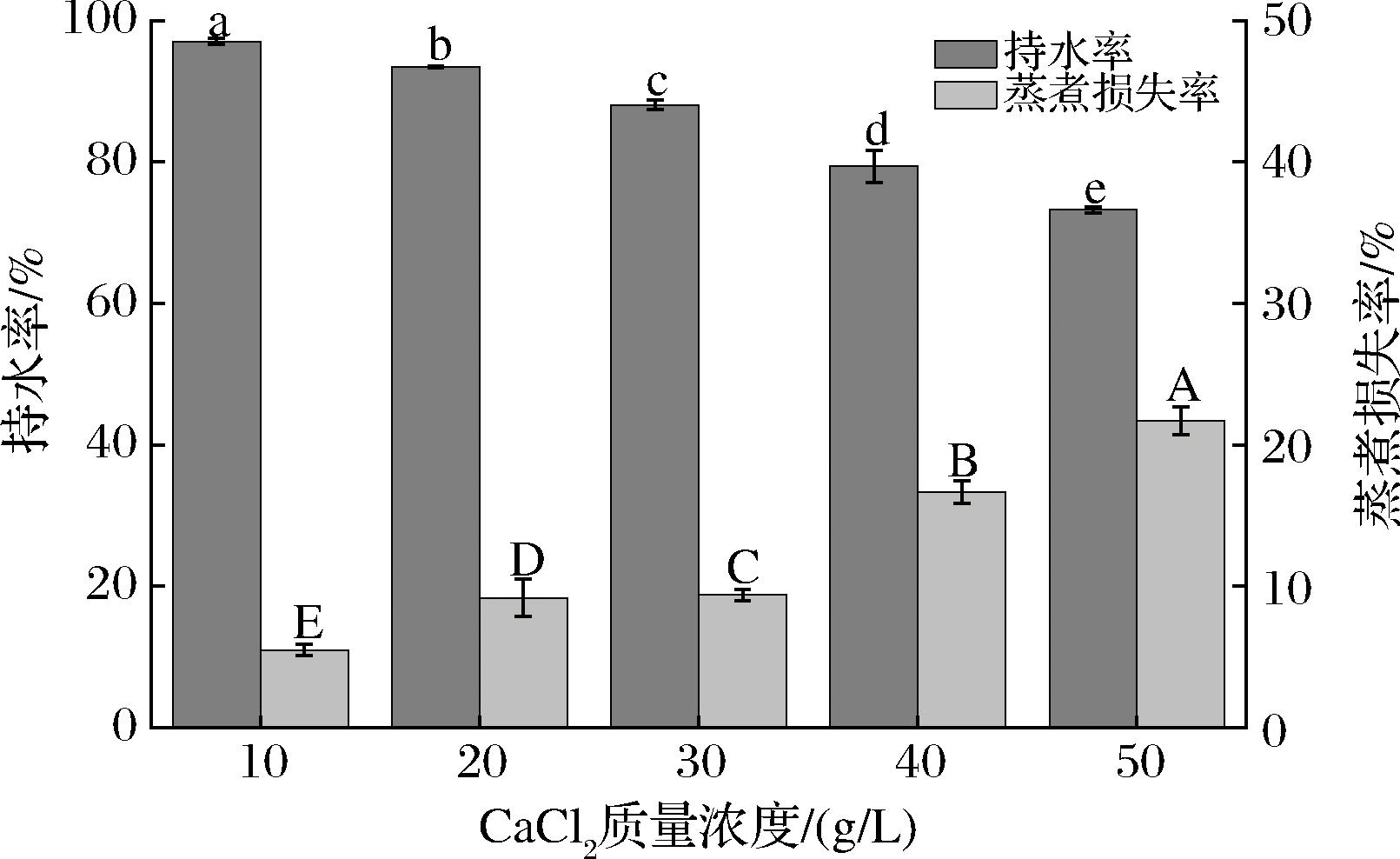
图3 CaCl2浓度对海带褐藻胶食用颗粒持水率和蒸煮损失率的影响
Fig.3 Effect of CaCl2 concentration on water holding capacity and cooking loss of kelp alginate edible granules
冻融稳定性是指将产品反复解冻冷冻后的保水能力。由图4可知,产品的冻融稳定性随着Ca2+浓度的增加而逐渐降低,随着冻融循环次数增加,样品的析水率也逐渐增加。其中10 g/L CaCl2制得的样品冻融稳定性最高,5次冻融循环后析水率达23.87%,50 g/L CaCl2制得的样品冻融稳定性最低,5次冻融循环后析水率达10 g/L CaCl2样品近3倍。综上可知,不管是在离心,高温还是冻融处理下,产品的水分流失都随着Ca2+浓度的增加而显著加剧。
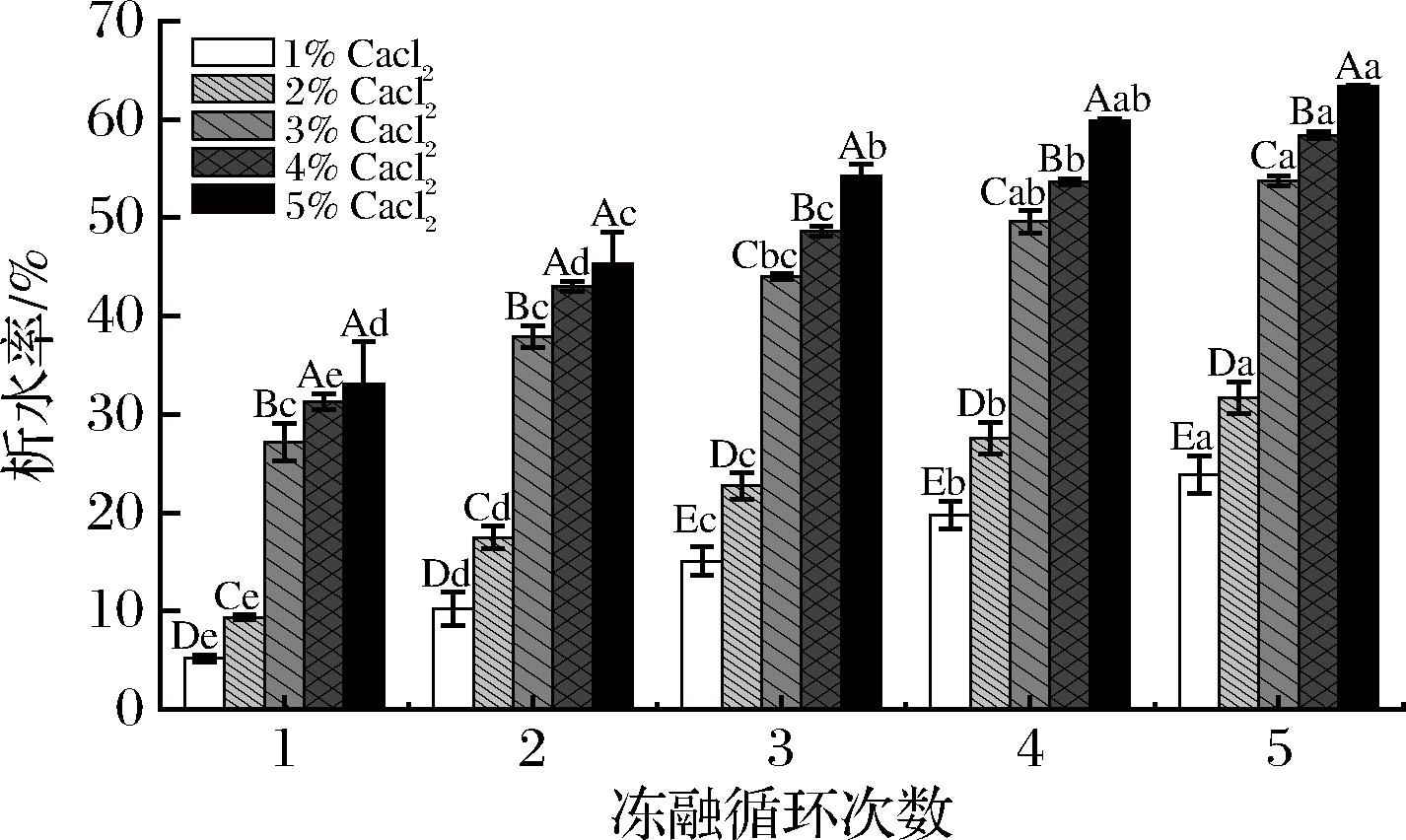
图4 CaCl2浓度对海带褐藻胶食用颗粒冻融稳定性的影响
Fig.4 Effect of CaCl2 concentration on freeze-thaw stability of kelp alginate edible granules
注:不同大写字母表示不同CaCl2浓度样品在相同冻融循环次数下差异显著(P<0.05),不同小写字母表示相同CaCl2浓度样品在不同冻融循环次数下差异显著(P<0.05)。
产生上述现象可能有以下4个原因:a)当Ca2+与褐藻酸盐分子交联时,暴露的亲水基团较少,水分子间可以相互作用,从而增加了凝胶网络中自由水的数量[18];b)Ca2+浓度增加导致产品表面局部接触的Ca2+浓度过高,通过盐桥效应促进产品表面褐藻酸盐快速凝胶化,形成致密外膜,导致Ca2+与产品内部的褐藻酸盐交联不完全,形成的凝胶网络结构不均匀,毛细管束缚水分能力随之下降[23],在离心力作用下自由水易被甩出;c)形成稳定的交联结构至少需要6~8个连续G单体,而过量的Ca2+可通过与MG片段交联导致凝胶网络崩溃,降低凝胶的热力学稳定性,从而导致产品蒸煮损失率增大[24-25];d)冷冻后产品中的水分结冰体积变大,不均匀的网络结构更易被冰晶破坏,导致解冻时水分流失严重,且反复冻融产生的冰晶持续破坏凝胶结构[23],受损的凝胶网络难以保持水分,样品的析水率随之逐渐增加。
2.5 CaCl2浓度对海带褐藻胶食用颗粒SEM的影响
图5是不同Ca2+浓度下制备的海带褐藻胶食用颗粒横截面扫描电镜图。由图5可以看出,Ca2+浓度为10 g/L时产品内部网络结构较疏松,随着Ca2+浓度增加,产品内部的三维网络凝胶结构变的更加丰富、致密。当Ca2+浓度增加到30~50 g/L时,外层和里层开始呈现明显不同的孔径大小,产品表层网络结构与内部相比孔径明显缩小,结构更密实,但产品总体凝胶结构变得更不均匀[26]。海带褐藻胶食用颗粒是用Ca2+扩散法制备而成,其在扩散过程可导致产品内部褐藻酸盐浓度不均匀,在产品与CaCl2溶液接触界面处的褐藻酸盐浓度最高[27],褐藻酸盐接触到高浓度Ca2+后快速交联成外层致密的凝胶膜,阻碍部分Ca2+继续向产品内部扩散与褐藻酸盐结合位点反应,交联速度减缓,交联度降低,且固化时间固定,从而导致产品内部网络结构不均匀。

A-10 g/L;B-20 g/L;C-30 g/L;D-40 g/L;E-50 g/L
图5 CaCl2浓度对海带褐藻胶食用颗粒微观结构的影响
Fig.5 Effect of CaCl2 concentration on microstructure of kelp alginate edible granules
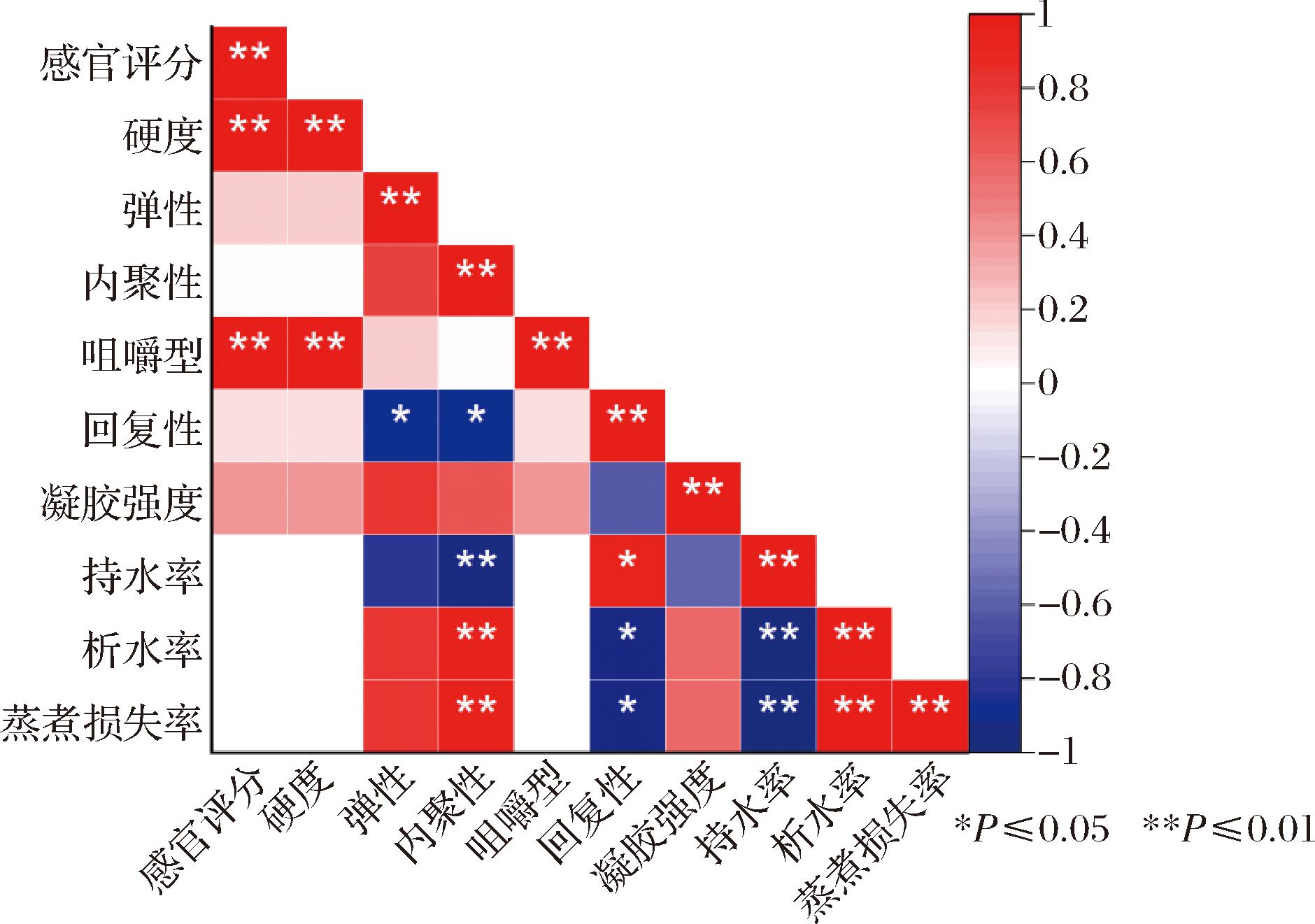
图6 海带褐藻胶食用颗粒各指标相关性分析结果
Fig.6 Spearman correlation analysis of kelp alginate edible granules indicators
2.6 海带褐藻胶食用颗粒品质指标相关性分析
利用Spearman相关性系数对海带褐藻胶食用颗粒各品质指标之间进行相关性分析。分析结果表明,产品感官品质与硬度、咀嚼性密切相关,硬度、咀嚼性越大,感官评分随之越高。内聚性和回复性可以反应产品体系中水分的稳定性,产品内聚性越大,其持水率和冻融稳定性越差,蒸煮损失率越大;回复性越大,产品水分体系越稳定。产品持水率与冻融稳定性呈极显著正相关,与蒸煮损失率呈极显著负相关。
3 结论
本文探讨了不同CaCl2浓度对海带褐藻胶食用颗粒凝胶特性和感官品质的影响。实验结果表明,随着CaCl2浓度的增加,产品的持水率、冻融稳定性逐渐降低,蒸煮损失率逐渐升高,电镜结果显示Ca2+浓度增加会使褐藻酸钙凝胶的网络孔径大小不均匀,毛细管束缚水分能力减弱,从而降低凝胶体系的稳定性;CaCl2质量浓度为20 g/L时产品的感官品质和质构特性均达到最优,产品的水分体系较稳定,此时Ca2+与褐藻酸盐交联较完全,产品凝胶网络结构更致密且均匀,但CaCl2浓度继续升高(30~50 g/L)会导致产品的硬度、咀嚼性等质构特性和感官品质劣化,持水率持续降低,产品水分体系稳定性下降。综上,选择20 g/L CaCl2制备海带褐藻胶食用颗粒既可以达到最优的质构特性和感官品质,还可以最大限度地保持产品的持水率及其凝胶体系的总体稳定性。
[1] AN E K, HWANG J, KIM S J, et al.Comparison of the immune activation capacities of fucoidan and laminarin extracted from Laminaria japonica[J].International Journal of Biological Macromolecules, 2022, 208:230-242.
[2] 李颖, 王茵, 陈婷茹, 等.海带高值化综合利用研究进展[J].渔业研究, 2023, 45(2):192-201.LI Y, WANG Y, CHEN T R, et al.Research progress of high-value comprehensive utilization of Laminaria japonica[J].Journal of Fisheries Research, 2023, 45(2):192-201.
[3] ZHAO X, GUO F J, HU J, et al.Antithrombotic activity of oral administered low molecular weight fucoidan from Laminaria Japonica[J].Thrombosis Research, 2016, 144:46-52.
[4] NI L Y, WANG L, FU X T, et al.In vitro and in vivo anti-inflammatory activities of a fucose-rich fucoidan isolated from Saccharina japonica[J].International Journal of Biological Macromolecules, 2020, 156:717-729.
[5] 李琦. 海带降血糖多肽的分离合成及活性研究[D].大连:大连理工大学, 2021.LI Q.Separation, synthesis and anti-diabetic activity study of peptides from Laminaria japonica[D].Dalian:Dalian University of Technology, 2021.
[6] YE X J, CHEN L, SU Z C, et al.Process optimization, texture and microstructure of novel kelp tofu[J].Food Science and Human Wellness, 2023, 12(1):111-118.
[7] GE H F, ZANG Y Y, CAO Z Y, et al.Rheological properties, textural and compound preservative of kelp recombination noodles[J].LWT, 2020, 118:108729.
[8] 黄友涛, 梁青平, 高筱雅, 等. 不同结构褐藻胶寡糖的制备与功效研究进展[J]. 食品科学, 2024,45 (1):313-325. HUANG Y T, LIANG Q P, GAO X Y, et al. Research progress on preparation and function of alginate oligosaccharides with different structures[J]. Food Science, 2024,45 (1):313-325.
[9] 刘海超, 张健, 王共明, 等.褐藻胶的降解方法及其产物生物活性研究进展[J].食品工业科技, 2020, 41(13):350-357;363.LIU H C, ZHANG J, WANG G M, et al.Advances in degradation methods of alginate and bioactivity of its degradation products[J].Science and Technology of Food Industry, 2020, 41(13):350-357;363.
[10] 孙义凡, 王智慧, 段蕊, 等.褐藻胶的凝胶特性及其在食品中的应用[J].食品研究与开发, 2023, 44(4):209-214.SUN Y F, WANG Z H, DUAN R, et al.Alginate:Gel properties and application in food products[J].Food Research and Development, 2023, 44(4):209-214.
[11] DE FARIAS Y B, P C, ZAPATA NORE A C P.Reverse encapsulation using double controlled gelification for the production of spheres with liquid light soy sauce-core[J].International Journal of Gastronomy and Food Science, 2019, 16:100137.
A C P.Reverse encapsulation using double controlled gelification for the production of spheres with liquid light soy sauce-core[J].International Journal of Gastronomy and Food Science, 2019, 16:100137.
[12] 罗阳, 张连富.海藻酸钠-钙凝胶特性及其在低脂猪肉糜中应用的研究[J].食品工业科技, 2012, 33(6):374-376;385.LUO Y, ZHANG L F.Study on the gelling properties of sodium-calcium alginate and its application in low-fat Pork[J].Science and Technology of Food Industry, 2012, 33(6):374-376;385.
[13] 许加超, 庞作宾, 高昕, 等.褐藻酸缓释钙离子凝胶果冻的研制[R].青岛:中国海洋大学, 2010.XU J C, PANG Z B, GAO X, et al.Preparation of alginate sustained-release calcium gel jelly[R].Qingdao:Ocean University of China, 2010.
[14] 许加超, 卢伟丽, 高昕, 等.氯化钙体系制备的褐藻酸钙凝胶特性的研究[J].渔业科学进展, 2010, 31(1):100-103.XU J C, LU W L, GAO X, et al.Study on the properties of alginate gel made by using of calcium chloride[J].Progress in Fishery Sciences, 2010, 31(1):100-103.
[15] 李颖, 王茵, 陈婷茹, 等.海带褐藻胶食用颗粒制备工艺及其品质特性研究[J].食品与发酵工业, 2024,50(16):177-184.LI Y, WANG Y, CHEN T R, et al.Study on preparation technology and quality characteristics of kelp alginate edible granules[J].Food and Fermentation Industries, 2024,50(16):177-184.
[16] CUI C L, JIANG H, GUAN M H, et al.Characterization and in vitro digestibility of potato starch encapsulated in calcium alginate beads[J].Food Hydrocolloids, 2022, 126:107458.
[17] 刘施琳, 朱丰, 林圣楠, 等.琼脂凝胶强度及弛豫特性的研究[J].食品工业科技, 2017, 38(13):85-89;100.LIU S L, ZHU F, LIN S N, et al.Research of strength and relaxation properties of agar gel[J].Science and Technology of Food Industry, 2017, 38(13):85-89;100.
[18] SHU J X, MCCLEMENTS D J, LUO S J, et al.Effect of internal and external gelation on the physical properties, water distribution, and lycopene encapsulation properties of alginate-based emulsion gels[J].Food Hydrocolloids, 2023, 139:108499.
[19] RAMDHAN T, CHING S H, PRAKASH S, et al.Time dependent gelling properties of cuboid alginate gels made by external gelation method:Effects of alginate-CaCl2solution ratios and pH[J].Food Hydrocolloids, 2019, 90:232-240.
[20] 陈梦洁, 金忠兴, 李志勇, 等.假酸浆子胶与海藻酸钠凝胶球的质构特性[J].食品工业科技, 2017, 38(20):233-239.CHEN M J, JIN Z X, LI Z Y, et al.The texture properties of gel beads from Nicandra physaloides (L.) Gaerthseed gum and sodium alginate[J].Science and Technology of Food Industry, 2017, 38(20):233-239.
[21] FERN NDEZ FARRÉS I, NORTON I T.Formation kinetics and rheology of alginate fluid gels produced by in-situ calcium release[J].Food Hydrocolloids, 2014, 40:76-84.
NDEZ FARRÉS I, NORTON I T.Formation kinetics and rheology of alginate fluid gels produced by in-situ calcium release[J].Food Hydrocolloids, 2014, 40:76-84.
[22] BAREKAT S, SOLTANIZADEH N.Application of high-intensity ultrasonic radiation coupled with papain treatment to modify functional properties of beef Longissimus lumborum[J].Journal of Food Science and Technology, 2019, 56(1):224-232.
[23] LIANG X P, MA C C, YAN X J, et al.Structure, rheology and functionality of whey protein emulsion gels:Effects of double cross-linking with transglutaminase and calcium ions[J].Food Hydrocolloids, 2020, 102:105569.
[24] CAO L Q, LU W, MATA A, et al.Egg-box model-based gelation of alginate and pectin:A review[J].Carbohydrate Polymers, 2020, 242:116389.
[25] BOWMAN K A, AARSTAD O A, NAKAMURA M, et al.Single molecule investigation of the onset and minimum size of the calcium-mediated junction zone in alginate[J].Carbohydrate Polymers, 2016, 148:52-60.
[26] 刘国栋, 徐颖, 李志健, 等.PNIPAM/Fe3+/CNF-c复合水凝胶的制备及其驱动性能研究[J].陕西科技大学学报, 2023, 41(2):1-7.LIU G D, XU Y, LI Z J, et al.Study on preparation and actuating performance of PNIPAM/Fe3+/CNF-c composite hydrogel[J].Journal of Shaanxi University of Science &Technology, 2023, 41(2):1-7.
[27] MARTINSEN A, SKJÅK-BR☞K G, SMIDSRØD O.Alginate as immobilization material:I.Correlation between chemical and physical properties of alginate gel beads[J].Biotechnology and Bioengineering, 1989, 33(1):79-89.