越来越多的研究表明,蔗糖的过量摄取会直接引起血糖升高、肥胖、心血管疾病等健康问题[1],用以代替蔗糖功能的甜味剂逐渐受到业界关注。与蔗糖相比,天然甜味剂则在甜味的品质及稳定性上差异较大[2-3];人工合成甜味剂则具有更多令人不愉悦的副味,如金属味、涩味、苦味等。赤藓糖醇,化学式为C4H10O4,是一种小分子天然糖醇,因其甜味纯正、副味较少的特点而作为常用填充型甜味剂应用在饮料、冰淇淋等食品中。目前,在食品体系的实际应用中发现,不同厂家生产的赤藓糖醇在产品中的感官品质存在较大的差异,由于对赤藓糖醇感官特性及其影响因素的基础研究相对较少,导致这种差异产生的原因尚未可知。
当前对于赤藓糖醇应用方面的研究更多是围绕在不同食品体系下替代蔗糖对体系性质的影响,其中不乏学者从原料角度开展关于赤藓糖醇的感官性质的研究。WEE等[4]测量了16种甜味剂的强度-剂量反应曲线,研究表明赤藓糖醇甜味强度弱于蔗糖,甜味强度随剂量增长的比率与蔗糖近似;TAN等[2]使用TCATA方法对包括赤藓糖醇在内的16种甜味剂的感官性质动态特征进行研究,发现赤藓糖醇起甜快,甜味消失速度快,并伴随着口腔干燥感与金属味等不良风味。以上都是基于赤藓糖醇这一物质的基础感官性质开展的研究。在实际应用中,由于发酵菌种、生产工艺的不同,不同赤藓糖醇商品各项理化指标虽均达到GB 26404—2011《食品安全国家标准 食品添加剂 赤藓糖醇》的质量要求,但其感官品质存在差异。而当前国内外关于赤藓糖醇商品感官品质、理化性质之间的差异以及感官品质影响因素的相关研究鲜见报道。因此对不同赤藓糖醇商品感官性质及影响因素进行研究,有利于赤藓糖醇在食品体系中更广泛的应用。
本研究的目的是对6种赤藓糖醇商品的感官性质进行剖析,通过一系列理化检测分析,探究影响不同赤藓糖醇商品感官性质差异的因素,以期廓清部分理化指标与赤藓糖醇商品感官品质之间的联系,为赤藓糖醇感官品质的稳定化与成品的质量控制提供依据。
1 材料与方法
1.1 试剂和材料
选用市面上6种赤藓糖醇商品,编号为A、B、C、D、E、F,分别来自山东三元生物科技股份有限公司、北京瑞芬生物科技股份有限公司、山东保龄宝生物科技股份有限公司、宁夏伊品生物科技股份有限公司、诸城东晓生物科技有限公司;赤藓糖醇(≥99%)标准品、L-苏糖醇(≥99%)标准品,上海盈芯生物科技有限公司;舒可曼白砂糖,广州福正东海食品有限公司;阿斯巴甜,安徽维多食品配料有限公司;食品级明矾,河南万邦化工科技有限公司;寿全斋红糖,上海寿全斋电子商务有限公司;雀巢醇品咖啡粉,广东东莞雀巢有限公司;德亚脱脂牛奶,品渥食品股份有限公司;食品级无水柠檬酸,河南万邦化工科技有限公司。
1.2 仪器和设备
Waters 2695高效液相色谱,美国Waters公司;ICS-5000 Plus型高效阴离子交换色谱,美国Thermo Scientific科技公司。
1.3 实验方法
1.3.1 感官描述性分析
参考GB/T 16291.1—2012《感官分析 选拔、培训与管理评价员一般导则 第1部分:优选评价员》,在江南大学学生群体中发放问卷筛选出消费添加甜味剂产品频率较高的且无过敏症状的人群,进行感官灵敏度测试及面试,结果筛选出具有较高味觉嗅觉灵敏度,语言表达能力较强的14名评价员(2男12女)。评价小组需先对赤藓糖醇样品进行熟悉了解,根据文献构建甜味剂感官描述词库,通过小组讨论,保留客观的、有代表性的、无歧义的描述性属性[5],进一步对其定义优化,确定参照样。最终确定了12组评价指标。
通过区分能力F值、重复性MSE值以及小组一致性对小组成员的感官评价能力进行检验。经检验筛选12名评价能力良好的评价员(2男10女),进入样品评价阶段。测评阶段,评价员采用15点线性标度,对5%(质量分数,下同)赤藓糖醇溶液进行定量描述性分析。样品盛装在随机三位数编码的无味透明测试杯中。全部样品需完成所有属性的评分[6]。
1.3.2 赤藓糖醇的纯度测定及杂质鉴定
配制5 mg/mL赤藓糖醇样品溶液,2、3、4、5、6、7 mg/mL赤藓糖醇标准溶液,使用Waters XBridge Amide氨基柱,流动相为V(乙腈)∶V(纯水)=80∶20,流速设置为1 mL/min,进样量10 μL,柱温30 ℃。
准确称量6种样品750 g并加入蒸馏水1 000 mL,于70 ℃水浴溶解完全。降温至4 ℃重结晶12 h,过饱和赤藓糖醇结晶析出后,真空抽滤,样品溶液旋蒸(-0.095 MPa,45 ℃)至500 mL。重复降温结晶步骤,直至旋蒸样品溶液至12 mL(固形物含量为25%)。使用蒸馏水稀释至相应浓度,进行离子色谱检测上样。
离子色谱检测浓缩样品:安培检测器(Au工作电极,pH-Ag/AgCl参比电极);CarboPakTM PA200色谱柱(3 mm×250 mm,5.5 μm)。进样方式自动进样;进样量10 μL;柱温30 ℃;流速0.5 mL/min。淋洗条件:0~6.5 min,100 mmol/L NaOH;6.5~18 min,96 mmol/L NaOH,20 mmol/L NaAc;18~22 min,92 mmol/L NaOH,40 mmol/L NaAc。
1.3.3 赤藓糖醇同分异构体的测定
配制1.6 mg/mL赤藓糖醇样品溶液,100、200、400、500、600、700 mg/L的L-苏糖醇标准溶液,使用Sugar PakTMⅠ型糖柱,流动相为纯水(50 mmol/L EDTA-Ca),流速设置为0.4 mL/min,进样量10 μL,柱温85 ℃。
1.3.4 赤藓糖醇金属离子含量的测定
参照刘慧等[7]的方法使用电感耦合等离子体质谱仪(inductively coupled plasma-mass spectrometry,ICP-MS)测定。根据标准溶液中待测元素与内标Ge元素的响应强度制作标准曲线,对样品中的Na、Mg、Al、K、Ca、Mn、Fe、Cu、Zn金属元素含量进行定量分析。
1.3.5 赤藓糖醇阴离子含量的测定
使用高压离子色谱系统对100 mg/mL赤藓糖醇水溶液中的阴离子进行检测,使用Ion Pac AS11-HC分离柱,洗脱液30 mmol/L KOH,流速1 mL/min,温度30 ℃,进样量20 μL。
1.3.6 主要金属阳离子对赤藓糖醇感官品质影响的验证分析
选择具备食品添加许可的金属盐稀释至赤藓糖醇各金属离子含量的对应倍数(1、2、4倍),添加进赤藓糖醇溶液中。以SO42-、Cl-为阴离子,按表1的配比调制不同金属离子浓度的赤藓糖醇溶液。
表1 金属阳离子对5%赤藓糖醇溶液的影响试验设计表 单位:mg/L
Table 1 Experimental design table for the effect of metal cation on 5% erythritol solution

金属盐ⅠⅡⅢFeSO40.1250.250.5ZnSO40.250.51.0MgSO40.250.51.0CaCl22.505.010.0KCl0.250.51.0
1.4 数据分析
使用SPSS 26进行方差分析,使用XLSTAT 2019进行偏最小二乘回归分析(partial least squares regression,PLS)、主成分分析(principal component analysis,PCA),采用Origin进行相关性分析、绘制图表。每次实验重复3次,并计算平均值和标准偏差。
2 结果与分析
2.1 赤藓糖醇的感官分析
2.1.1 赤藓糖醇的感官描述词
为筛选出适合的感官属性来全面分析赤藓糖醇单体样品的感官风味特征,收集前期研究中用以描述天然和人工类甜味剂属性描述词并以此建立24个描述性词汇表。
经讨论后删除样品间差异较小、重复性差或评价员在感知上难以达成一致的词语,最终选择确定出小组引用频率超过80%的12组静态描述性评估属性,其中包括甜味、苦味、酸味、甜后味、涩后味、苦后味、金属味、蜂蜜味、清凉感、人工甜味、红糖味和奶味。在此基础上,评价小组选择对应参照样并建立了对应的参照体系,其中,各指标的定义及参照样分值如表2所示。在测评过程中,依此对6种不同厂家的赤藓糖醇进行静态描述性分析。
表2 5%赤藓糖醇溶液的感官描述词汇定义及参照表
Table 2 Definition and references of 5% erythritol solution sensory descriptive attributes

属性定义参照样的标度甜味入口5 s内口腔感受到的甜味强度值2%(质量分数,下同)蔗糖溶液=3;5%蔗糖溶液=8;8%蔗糖溶液=12甜后味吞咽后感受到的最大甜味强度值2%蔗糖溶液=4;4%蔗糖溶液=8苦味入口感受到的最大苦味强度值0.04%雀巢黑咖啡=2;0.08%雀巢黑咖啡=5;0.15%雀巢黑咖啡=8苦后味吞咽样品后感受到的最大苦味值(包含回味中的苦味)0.04%雀巢黑咖啡=4;0.08%雀巢黑咖啡=8涩后味吞咽样品后感受到的最大涩度值,可为口腔干燥感或是舌的麻痛感,舌表面覆盖一层东西的感觉0.005%食品级明矾=3;0.01%食品级明矾=7酸味入口后舌头两侧感受到的最大酸味强度0.001%柠檬酸溶液=4;0.002%柠檬酸溶液=8清凉感从入口到吞咽,舌头感受到的最强凉度2%蔗糖溶液=2;0.04%薄荷浸泡在水中10 min=6红糖味入口到吞咽感受到的最强红糖的特征风味0.3%红糖溶液=4;0.5%红糖溶液=8人工甜味低热量饮料的风味/人工合成非甘蔗风味的强度4%蔗糖溶液=1;0.08%阿斯巴甜溶液=10蜂蜜味入口到吞咽感受到的最强蜂蜜的特征风味0.30%蜂蜜溶液=3;1.00%蜂蜜溶液=6金属味入口到吞咽感受到的金属气味,类似于血腥味0.000 5%葡萄糖酸亚铁溶液=6;0.001%葡萄糖酸亚铁溶液=13奶味入口到吞咽感受到的最强的牛奶风味0.15%德亚脱脂奶=5;0.30%德亚脱脂奶=9
2.1.2 描述性结果分析
采用Spectrum描述性方法对不同厂家赤藓糖醇配制5%溶液进行静态感官评估,其风味轮廓如图1所示。由图可见,赤藓糖醇的感官属性简单,主要是由基本滋味口感与部分由基本风味与口感相组合成的特殊风味构成[2,8],这是因为赤藓糖醇由微生物发酵生产[9],属于结构简单的小分子化合物,不含引起其他滋味的基团。

图1 5%赤藓糖醇溶液描述性属性蛛网图
Fig.1 Spider plot of descriptive properties of 5% erythritol solution
不同来源商品赤藓糖醇的感官属性特点如表3所示。不同来源赤藓糖醇之间在苦味、苦后味、涩味、蜂蜜味、红糖味、人工甜味、清凉感属性方面没有显著性差异;其中样品C在甜味(2.96)、甜后味(5.50)与样品D均无显著性差异,但显著低于样品A、B、E、F,奶味(4.25)显著高于其他样品;样品A与样品E、样品F均无显著性差异,与样品B(2.79)仅在金属味上有显著性差异;样品D的甜味(3.29)上显著低于样品B(3.86),在甜后味(5.78)上显著低于样品A,在酸味(1.31)、金属味(3.14)上显著高于样品A、F,在奶味(1.76)属性评分上显著低于样品C。
表3 5%赤藓糖醇溶液描述性属性结果
Table 3 Descriptive attribute results of 5% erythritol solution

属性ABCDEF甜味3.54±0.12ab3.86±0.11a2.96±0.02c3.29±0.10bc3.50±0.09ab3.46±0.10ab甜后味6.61±0.48ab6.21±0.80bc5.50±0.48d5.78±0.69cd6.32±0.62abc6.85±0.34a苦味0.93±0.67a1.43±0.61a0.98±0.68a1.50±0.70a1.21±0.74a0.93±0.34a苦后味0.78±0.63a0.71±0.75a0.58±0.34a1.14±1.06a0.85±0.80a0.50±0.40a涩后味1.00±0.26a1.13±0.58a1.36±0.67a1.13±0.35a1.19±0.37a0.75±0.26a酸味0.68±0.45b0.81±0.45ab0.88±0.37ab1.31±0.25a1.00±0.37ab0.62±0.44b金属味0.93±0.73c2.79±0.95ab2.57±1.07ab3.14±0.89a1.54±0.83bc0.93±0.43c奶味1.88±0.62b2.12±0.56b4.25±0.67a1.76±0.58b1.76±0.58b2.48±0.49b蜂蜜味1.50±0.75a1.13±0.34a1.60±0.46a1.25±0.75a1.13±0.64a1.00±0.26a清凉感1.63±0.51a1.75±0.37a2.23±0.87a1.75±0.53a2.25±0.59a1.88±0.69a红糖味0.93±0.62a1.06±0.56a1.47±0.66a1.43±0.49a0.87±0.58a0.87±0.58a人工甜味3.19±0.25a3.06±0.72a2.19±0.67a3.31±0.84a2.44±0.49a2.81±0.59a
注:感官测试结果表示为“平均值±标准差”,同行字母不同样品间存在显著差异(P<0.05)(下同)。
2.2 赤藓糖醇的纯度及同分异构体测定
通过液相色谱法对不同商品赤藓糖醇的纯度进行检测,结果如表4所示。6种商品赤藓糖醇的纯度均>96%;A、B、D、E、F纯度为97.5%~99.0%,均无显著性差异,C的纯度为96.13%,显著低于其他样品。根据TOMASZEWSKA等[10]的研究,发现在以甘油为底物的赤藓糖醇生产中含有副产物甘露糖醇;赵祥颖等[11]在以赤藓糖醇发酵母液为研究对象时,鉴定出含有阿拉伯糖醇、甘露糖醇和少量核糖醇。由此推测商品赤藓糖醇中可能存在其他糖醇类杂质。
表4 不同赤藓糖醇的纯度、苏糖醇含量及其他糖醇检测情况
Table 4 Purity of erythritol, threitol content and detection of other sugar alcohols

品类名称纯度/%苏糖醇含量/%阿拉伯糖醇甘露糖醇核糖醇丙三醇A98.00±0.43a0.20±0.02b未检出未检出未检出未检出B98.30±0.07a0.18±0.03bc未检出未检出未检出未检出C96.13±0.47b0.30±0.02a未检出未检出未检出未检出D98.95±1.79a0.11±0.03d未检出未检出未检出未检出E98.09±0.47a0.19±0.01bc未检出未检出未检出未检出F97.90±0.31a0.14±0.03cd未检出未检出未检出未检出
注:纯度与苏糖醇含量结果表示为“平均值±标准差”,同列字母不同的样品间存在显著差异(P<0.05)。
对样品杂质浓缩不同倍数进行离子色谱检测,结果如表4显示,并未发现其他杂质。可能的原因是,商品赤藓糖醇在粗品精制过程中经过蒸发浓缩得到结晶赤藓糖醇,其他糖醇类杂质在发酵液重结晶提纯过程中并未达到过饱和,从而保留在发酵液废液中,得以在该生产环节被去除。
苏糖醇是赤藓糖醇的非对映同分异构体,在生物发酵过程中可以通过赤藓糖醇分解成赤藓糖、赤藓酮糖经由赤藓糖激酶、赤藓糖醇/苏糖醇脱氢酶催化产生[12]。通过对商品赤藓糖醇浓缩200倍,检测出苏糖醇对应峰并定量,如表4所示。6种样品的苏糖醇含量为0.1%~0.4%;其中样品C的苏糖醇含量(0.30%)显著高于其他样品;样品D与样品F的苏糖醇含量为0.11%~0.14%,无显著性差异,显著低于样品A、B、C、E;样品A、B、E的苏糖醇含量为0.18%~0.2%,无显著性差异。这是因为不同的厂家在进行赤藓糖醇发酵生产中所应用的发酵菌种、发酵工艺等方面的差异造成的。
2.3 赤藓糖醇阳离子和阴离子含量分析
2.3.1 赤藓糖醇阳离子和阴离子含量分析
赤藓糖醇工艺生产中常添加CuSO4、CaCl2、K2HPO4、MgSO4等金属无机盐作为发酵生产助剂,用以维持发酵菌的渗透压稳态,提高发酵过程酶系的活力[13-14]。其在后续工艺提纯过程中,难以通过膜过滤、重结晶等手段完全去除。
因此,测量商品赤藓糖醇中金属离子含量,如表5所示,不同厂家赤藓糖醇的Na+、Mg2+、Al3+、K+、Mn2+、Cu2+、Zn2+离子含量具有显著性差异。
表5 商品赤藓糖醇中各金属离子含量
Table 5 Content of metal ions in erythritol

品类名称Na+/(μg/g)Mg2+/(μg/g)Al3+/(μg/g)K+/(μg/g)Ca2+/(μg/g)Mn2+/(μg/kg)Fe2+/(μg/g)Cu2+/(μg/kg)Zn2+/(μg/g)A28.64±8.52ab15.87±2.86b4.19±0.88c3.81±3.25bc332.46±44.8a539.79±35.33ab1.82±1.03a352.64±74.86c7.39±0.22cB14.83±6.22ab37.73±8.62a5.13±0.22bc1.52±1.09c329.71±71.06a1 183.58±339.46a4.69±3.91a433.79±68.14c8.56±0.40cC34.19±12.37a27.32±14.65ab5.61±1.82bc17.15±5.47a448.77±371.87a947.98±528.63a4.98±4.24a764.19±58.68b9.58±0.86bcD32.63±5.23a27.93±6.46ab7.27±0.53ab9.01±1.12b223.9±162.11a780.70±193.31ab3.07±3.46a991.07±56.08a18.72±2.73aE20.75±3.94ab20.01±1.53ab9.17±0.11a4.11±0.57bc341.46±15.85a495.10±27.09ab1.00±0.29a970.74±25.79a14.22±3.09abF10.40±2.13b10.45±4.04b5.98±0.59bc1.66±0.04c177.59±56.97a159.42±65.62b1.17±0.00a71.64±9.05d1.61±0.20d
注:金属离子含量结果表示为“平均值±标准差”,同列字母不同的样品间存在显著差异(P<0.05)。
样品的Na+含量为10.40~34.19 μg/g,样品C(34.19 μg/g)、D(32.63 μg/g)的Na+含量显著高于样品F(10.40 μg/g);样品的Mg2+含量为10.45~37.73 μg/g,样品B(37.73 μg/g)的Mg2+含量显著高于样品A(15.87 μg/g)、F(10.45 μg/g);样品的Al3+含量为4.19~9.17 μg/g,样品E(9.17 μg/g)的Al3+含量显著高于样品A、B、C、F;样品的K+含量为1.66~17.15 μg/g,样品C(17.15 μg/g)的K+含量显著高于其余样品;样品的Cu2+含量为71.64~991.07 μg/kg,样品D(991.07 μg/kg)、E(970.74 μg/kg)的Cu2+含量显著高于其他样品,样品F(71.64 μg/kg)的Cu2+含量显著低于其他样品;样品的Zn2+含量为1.61~18.72 μg/g,样品D(18.72 μg/g)的Zn2+含量显著高于样品A、B、C、F。
赤藓糖醇中![]() 阴离子含量如图2所示,不同厂家生产的赤藓糖醇之间差异显著。
阴离子含量如图2所示,不同厂家生产的赤藓糖醇之间差异显著。

图2 商品赤藓糖醇的阴离子含量
Fig.2 Anion content of commercial erythritol
其中按F-含量排序,样品C(2.99 μg/g)、D(3.12 μg/g)显著高于其他样品;按Cl-含量排序,样品B(6.05 μg/g)、D(6.12 μg/g)显著高于其他样品;按![]() 含量排序,样品A(6.22 μg/g)、F(5.49 μg/g)显著高于其他样品;按NO3-含量排序,样品A(2.66 μg/g)、B(1.99 μg/g)、D(2.05 μg/g)样品显著高于样品C、E、F;按PO43-含量排序,样品C(1.24 μg/g)、D(1.29 μg/g)、E(1.11 μg/g)显著高于其他样品,其中样品A(0.64 μg/g)显著高于样品B(0.27 μg/g)、F(0.24 μg/g)。关于赤藓糖醇中阴离子的来源,因其数量级与大部分金属离子含量的数量级一致,推测阴离子来源与金属阳离子的来源一致,可能由发酵生产助剂的金属无机盐或生产用水引入。
含量排序,样品A(6.22 μg/g)、F(5.49 μg/g)显著高于其他样品;按NO3-含量排序,样品A(2.66 μg/g)、B(1.99 μg/g)、D(2.05 μg/g)样品显著高于样品C、E、F;按PO43-含量排序,样品C(1.24 μg/g)、D(1.29 μg/g)、E(1.11 μg/g)显著高于其他样品,其中样品A(0.64 μg/g)显著高于样品B(0.27 μg/g)、F(0.24 μg/g)。关于赤藓糖醇中阴离子的来源,因其数量级与大部分金属离子含量的数量级一致,推测阴离子来源与金属阳离子的来源一致,可能由发酵生产助剂的金属无机盐或生产用水引入。
2.3.2 赤藓糖醇的金属离子、阴离子与感官属性的关系分析
分别对赤藓糖醇中检测出的金属离子、阴离子含量与5%赤藓糖醇溶液中感官属性强度做相关性分析。结果如图3-a所示,SO42-、NO3-离子对赤藓糖醇的人工甜味有正相关,相关系数分别为0.87、0.82;F-离子与赤藓糖醇的红糖味,金属味呈正相关,相关系数分别为0.88、0.94。由图3-b可知,Cu2+、Zn2+与酸味呈现正相关,相关系数分别为0.88、0.95,与苦后味呈现正相关,相关系数分别为0.71、0.90,与甜后味呈现负相关,相关系数分别为-0.71、-0.61;K+与红糖味、涩后味属性呈正相关,相关系数分别为0.94、0.92,与甜味、甜后味属性呈现负相关,相关系数分别为-0.98、-0.93。

a-阴离子与感官属性的相关性;b-金属离子与感官属性的相关性
图3 赤藓糖醇的阴离子、金属离子含量与感官属性的相关性热图
Fig.3 Correlation plot of metal ion and anion content of erythritol with sensory properties
如图4所示,金属离子、阴离子对赤藓糖醇溶液的感官属性有一定影响。在PLS图的第二象限,赤藓糖醇溶液的酸味、金属味感官属性与赤藓糖醇样品中的Fe2+、Mg2+、Mn2+、Zn2+含量呈正相关,甜味、甜后味感官属性与之呈现负相关,这与WANG等[15]研究铁对不同水质甜味饮料的味觉感知现象所得出的金属感、甜感受水中矿物质的影响的结论相一致,这可能是因为水中的矿物质可能通过分子间作用力与甜味剂相互作用影响其甜度,从而增加了在金属盐水溶液中甜味的识别阈值;而在第三象限,赤藓糖醇的Ca2+、K+含量与赤藓糖醇溶液的滋味属性涩后味、红糖风味呈现一定的正相关,这与WATANABE等[16]对红糖的研究发现的Ca2+、K+含量对红糖产品的感官属性具有显著相关关系的结论相一致;SO42-、NO3-阴离子集中在t1的正半轴,与甜味、人工甜味属性有一定的正相关性,这与L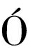 PEZ等[17]对水中的SO42-、NO3-含量对水样的影响进行研究所得到的低浓度的SO42-能够改善水样品质的结论相符合。
PEZ等[17]对水中的SO42-、NO3-含量对水样的影响进行研究所得到的低浓度的SO42-能够改善水样品质的结论相符合。

图4 赤藓糖醇金属离子、阴离子含量与感官属性的PLS图
Fig.4 PLS plot of metal ion and anion content of erythritol with sensory properties
赤藓糖醇的甜味、甜后味呈正相关,与金属味、酸味、苦味等其他属性呈负相关,这是因为赤藓糖醇本身提供甜味,金属离子通过混合物抑制作用或是与甜味剂分子之间的物理化学相互作用,对体系甜味的感知起到影响[15,18];金属味与苦味、酸味也呈一定正相关性,主是因为引起金属感觉的不同的金属盐通过激活口腔中的味觉与三叉神经受体(主要包括TRPV1型化学刺激受体、T1R3型鲜味受体、T2R7型苦味受体等),使得金属感知属于整合了包括味觉、嗅觉和三叉神经通路的多种感觉形式的感觉交互现象,呈现出酸味、苦味等多种感觉复合[19];红糖味与涩后味、酸味等呈一定正相关性,这是因为红糖本身被认为是香气复杂的产物,尤其是红糖在加工生产中不经过离心分蜜过程直接进行浓缩,从而成品中酚酸及非酶促美拉德反应产物等为产品赋予独特的甜味、酸味、涩味、焦香味等复合的风味[20]。
由于不同厂家赤藓糖醇发酵生产工艺的差异,工艺生产中引入金属盐作为生产助剂,以及工艺用水的水质等诸多原因,不同厂家赤藓糖醇产品之间金属离子与阴离子含量存在差异,从而引起产品之间的感官差异。
2.4 主要金属阳离子对赤藓糖醇感官品质影响的验证分析
通过设置金属盐反添加实验,以添加不同金属无机盐的赤藓糖醇样品D作为实验组,以未添加金属无机盐的样品D作为对照组,验证金属离子与感官属性的关系,通过主成分分析实验组与对照组的差异。如图5所示,前两个主成分的方差解释率为76.84%,表明能对样品实现较好地区分,添加实验组与对照组的位置距离随着金属盐添加量的增大而增大,说明金属含量直接影响到赤藓糖醇的感官表现;不同添加实验组在图上的位置不同,说明不同金属离子对赤藓糖醇的感官性质的影响不同。

图5 添加金属盐赤藓糖醇样品PCA载荷图
Fig.5 PCA biplot of metal salt added erythritol sample
其中,Fe2+离子的含量与样品的酸味、金属味具有正相关性,表明Fe2+含量越高,其金属味、酸味属性的评分越高,这与图4中得出的结论相一致,也与VINGERHOEDS等[21]在水样中反矿化实验得出的结论相一致,即Fe2+与感知到的金属味道之间存在正相关关系;Mg2+、K+、Zn2+在低的浓度梯度下,感官属性与对照组相似,均处于第四象限,表明样品中Mg2+、K+、Zn2+含量对赤藓糖醇感官属性的影响比较微弱,推测是这3种金属盐添加量并未达到对应金属盐的感受阈值[22];Mg2+、K+、Ca2+离子含量与样品的涩后味、苦味等具有正相关,表明较高的Mg2+、K+、Ca2+含量,使得赤藓糖醇样品溶液呈现较强的涩后味、苦味,这可能是由于这3种金属盐离子刺激到苦味相关受体,且添加量达到相应的感受阈值,因而形成较强的苦味。
3 结论
本研究对6种商品赤藓糖醇的感官品质进行评估,并对可能影响其感官性质的理化性质的差异进行探讨。感官实验结果显示,不同来源的赤藓糖醇在甜味(2.90~4.00)、甜后味(5.50~6.85)、酸味(0.62~1.31)、金属味(0.93~3.14)、奶味(1.76~4.25)属性方面存在显著性差异。通过对赤藓糖醇的纯度、同分异构体含量、金属离子含量、阴离子含量等进行测定,结果显示,6种赤藓糖醇纯度在96.15%~98.95%,具有显著性差异;6种赤藓糖醇的同分异构体含量在0.11%~0.30%,含量较少,具有显著性差异;样品的金属离子(Na+、Mg2+、Al3+、K+、Mn2+、Cu2+、Zn2+)含量、阴离子(F-、Cl-、SO42-、NO3-、PO43-)含量均具有显著性差异。通过对离子含量与感官性质相关性分析及金属阳离子对感官品质影响的验证分析,结果显示,其中赤藓糖醇的Fe2+离子含量与赤藓糖醇样品的金属味具有正相关性,赤藓糖醇的Mg2+、Ca2+、K+离子含量与涩后味、苦味等不良风味存在正相关性。不同产品由于生产工艺之间的差异导致其金属离子含量之间存在差异,而金属离子通过刺激口腔中不同的感觉受体产生不同味觉的强度,且不同味觉感觉之间产生一系列感觉交互现象,从而导致不同赤藓糖醇的感官品质之间出现差异。本研究通过研究不同商品赤藓糖醇感官品质、理化性质差异,为赤藓糖醇离子含量与产品风味感官性质建立了联系,为商品赤藓糖醇的感官品质分析与成品质量控制提供了依据,但关于不同生产工艺如何造成产品金属离子之间的差异以及金属离子是如何影响赤藓糖醇味觉感知的机理等问题暂未进行探究,因此对于造成这样现象的原因还需统筹赤藓糖醇的生产工艺等系列问题设计相关实验进一步分析。
[1] FITCH C, KEIM K S.Position of the academy of nutrition and dietetics:Use of nutritive and nonnutritive sweeteners[J].Journal of the Academy of Nutrition and Dietetics, 2012, 112(5):739-758.
[2] TAN V W K, WEE M S M, TOMIC O, et al.Temporal sweetness and side tastes profiles of 16 sweeteners using temporal check-all-that-apply (TCATA)[J].Food Research International, 2019, 121:39-47.
[3] PALAZZO A B, BOLINI H M A.Multiple time-intensity analysis:Sweetness, bitterness, chocolate flavor and melting rate of chocolate with sucralose, rebaudioside and neotame[J].Journal of Sensory Studies, 2014, 29(1):21-32.
[4] WEE M, TAN V, FORDE C.A comparison of psychophysical dose-response behaviour across 16 sweeteners[J].Nutrients, 2018, 10(11):1632.
[5] 田欣雨. 甜菊糖苷单体结构与其甜苦味感官表现的相关性研究[D].无锡:江南大学, 2021.
TIAN X Y.Correlation between steviol glycosides structure and their bitterness/sweetness sensory properties[D].Wuxi:Jiangnan University, 2021.
[6] 钱佳仪, 夏熠珣, 侯姣靓, 等.采摘时期对菊花茶汤感官及理化属性的影响[J].食品与生物技术学报, 2023, 42(9):56-65.
QIAN J Y, XIA Y X, HOU J L, et al.Effects of harvesting period on sensory and physicochemical properties of Chrysanthemum infusion[J].Journal of Food Science and Biotechnology, 2023, 42(9):56-65.
[7] 刘慧, 孙秀兰.微波消解-ICP-MS法测定红薯中18种元素[J].粮食与饲料工业, 2021(1):67-71.
LIU H, SUN X L.Determination of 18 elements in sweet potato by microwave digestion-ICP-MS[J].Cereal &Feed Industry, 2021(1):67-71.
[8] GWAK M J, CHUNG S J, KIM Y J, et al.Relative sweetness and sensory characteristics of bulk and intense sweeteners[J].Food Science and Biotechnology, 2012, 21(3):889-894.
[9] 杨利博. Yarrowia lipolytica高渗发酵生产赤藓糖醇及高渗响应机制研究[D].无锡:江南大学, 2015.
YANG L B.Study on the hyperosmotic fermentation of erythritol by Yarrowia lipolytica and mechanisms of high osmotic pressure response [D].Wuxi:Jiangnan University, 2015.
[10] TOMASZEWSKA L, RYWI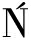 SKA A, G
SKA A, G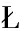 ADKOWSKI W.Production of erythritol and mannitol by Yarrowia lipolytica yeast in media containing glycerol[J].Journal of Industrial Microbiology &Biotechnology, 2012, 39(9):1333-1343.
ADKOWSKI W.Production of erythritol and mannitol by Yarrowia lipolytica yeast in media containing glycerol[J].Journal of Industrial Microbiology &Biotechnology, 2012, 39(9):1333-1343.
[11] 赵祥颖, 张立鹤, 杨丽萍, 等.赤藓糖醇生产母液中糖醇组分的定性鉴定[J].食品与发酵工业, 2014, 40(10):200-204.
ZHAO X Y, ZHANG L H, YANG L P, et al.Identification of the components in the erythritol mother liquor[J].Food and Fermentation Industries, 2014, 40(10):200-204.
[12] HUANG H, CARTER M S, VETTING M W, et al.A general strategy for the discovery of metabolic pathways:D-threitol, L-threitol, and erythritol utilization in Mycobacterium smegmatis[J].Journal of the American Chemical Society, 2015, 137(46):14570-14573.
[13] 王凤伟. 耐高渗赤藓糖醇生产菌的筛选与发酵条件优化[D].无锡:江南大学, 2012.
WANG F W.Screening of osmophilic strain for erythritol production and the optimization of fermentation condition[D].Wuxi:Jiangnan University, 2012.
[14] LI L Z, KANG P, JU X, et al.Enhancement of erythritol production by Trichosporonoides oedocephalis ATCC 16958 through regulating key enzyme activity and the NADPH/NADP ratio with metal ion supplementation[J].Preparative Biochemistry &Biotechnology, 2018, 48(3):257-263.
[15] WANG A L, DUNCAN S E, DIETRICH A M.Effect of iron on taste perception and emotional response of sweetened beverage under different water conditions[J].Food Quality and Preference, 2016, 54:58-66.
[16] WATANABE K, CHAPANYA P, SRIROTH K.Sensory and chemical analyses of non-centrifugal cane sugar for its production in Thailand[J].Sugar Tech, 2019, 21(4):686-690.
[17] L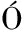 PEZ P, PÉREZ-RODR
PEZ P, PÉREZ-RODR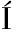 GUEZ I, ESTRANY F, et al.Effects of sulfate and nitrate on the taste of water:A study with a trained panel[J].Journal of Water Supply:Research and Technology-Aqua, 2017, 66(8):598-605.
GUEZ I, ESTRANY F, et al.Effects of sulfate and nitrate on the taste of water:A study with a trained panel[J].Journal of Water Supply:Research and Technology-Aqua, 2017, 66(8):598-605.
[18] HAO J, FISHMAN Z H, MINGYU Y, et al. Top-down control of sweet and bitter taste in the mammalian brain[J]. Cell, 2021, 184(1): 257-271.e216.
[19] ECARMA M J Y, NOLDEN A A.A review of the flavor profile of metal salts:Understanding the complexity of metallic sensation[J].Chemical Senses, 2021, 46:bjab043.
[20] ASIKIN Y, HIROSE N, TAMAKI H, et al.Effects of different drying-solidification processes on physical properties, volatile fraction, and antioxidant activity of non-centrifugal cane brown sugar[J].LWT, 2016, 66:340-347.
[21] VINGERHOEDS M H, NIJENHUIS-DE VRIES M A, RUEPERT N, et al.Sensory quality of drinking water produced by reverse osmosis membrane filtration followed by remineralisation[J].Water Research, 2016, 94:42-51.
[22] MARCUSSEN H, HOLM P E, HANSEN H C B.Composition, flavor, chemical foodsafety, and consumer preferences of bottled water[J].Comprehensive Reviews in Food Science and Food Safety, 2013, 12(4):333-352.