豌豆蛋白(pea protein,PP)是一种优质的植物蛋白,其氨基酸组成较平衡,并且赖氨酸含量丰富[1-2]。作为一种未被充分利用的蛋白,PP不仅具有来源广泛、致敏性低、非转基因的特点,而且具有降低胆固醇、血压等独特的生理活性[3]。由于PP表面疏水性较强且电荷量低,使其溶解性和乳化性较差[4],在以植物蛋白为体系的酸奶和饮料中应用时乳化稳定性不佳,体系通常发生脂肪上浮、油滴絮凝及聚集等失稳现象,严重影响食品品质和货架期[5]。
研究表明多糖可以与蛋白质分子间产生相互作用,从而提高蛋白质乳液的稳定性[6]。果胶是一种应用广泛的天然阴离子多糖,由于其来源丰富、价格低廉成为食品工业中常用的添加剂,根据甲酯化程度(degree of esterification,DE)的不同可分为高脂果胶(high methoxyl pectin,HMP)和低脂果胶(low methoxyl pectin,LMP),与HMP相比,LMP电荷密度较高,与蛋白的结合达到一定量后,游离在水相中的LMP和蛋白之间容易产生静电排斥作用,不利于酸性乳饮料等的稳定[7]。HMP因电荷量较少在蛋白表面吸附较多,可通过疏水以及静电相互作用和蛋白进行复合,提供空间位阻效应维持酸性蛋白体系的稳定性,在食品的结构、理化和功能特性中起到增稠剂、稳定剂、胶凝剂和乳化剂的作用[8]。ALBANO等[9]研究发现大豆蛋白和高甲氧基果胶在pH 3.5时相互作用最强,具有较高的络合性,复合物稳定的乳液具有牛顿力学行为,液滴尺寸较小,可显著提高乳化液的稳定性。GHARSALLAOUI等[10]通过研究高甲氧基果胶对豌豆分离蛋白乳液稳定性的影响,发现在一定条件下添加果胶后,由于果胶吸附产生空间排斥作用以及油水界面膜硬度的提高,可以使乳液更加稳定。
蛋白质和多糖在溶液中受pH、浓度、离子强度等影响,形成共溶体系、离散型相分离体系和静电复合(可溶、不可溶)体系,其中pH是影响蛋白-多糖相互作用的重要因素[11]。薛丽莹等[12]通过研究表没食子儿茶素没食子酸酯[(-)-epigallocatechin-3-gallate,EGCG]与大豆分离蛋白(soy protein isolate,SPI)在pH 3.0、7.0、9.0条件下的相互作用,发现不同pH值下EGCG与SPI的结合力不同,两者之间的相互作用可能会导致氨基酸残基微环境发生改变,使得SPI二级结构发生改变。
综上所述,本研究以PP和HMP为原料,通过分析pH对PP-HMP复合物浊度、粒径、多分散性指数(polydispersity index,PDI)、电位、乳化活性和稳定性以及复合物结构特性的影响规律,阐明不同pH下PP-HMP复合物形成规律,探究PP-HMP复合物乳化特性与其理化和结构特性之间的关系,研究结果为扩大PP-HMP复合物在食品中的应用提供理论基础。
1 材料与方法
1.1 材料与试剂
PP(蛋白含量为81.2%),双塔食品贸易有限公司;HMP[CAS:9000-69-5,来源于苹果,酯化度61%,半乳糖醛酸(干基计)75.1%],上海麦克林生化科技有限公司;大豆油,益海(周口)粮油工业有限公司;KBr(光谱纯)、无水乙醇、NaOH,天津市科密欧化学试剂有限公司;HCl,洛阳昊华化学试剂有限公司;实验所用试剂均为分析纯。
1.2 仪器与设备
SCIENTZ-IID超声波破碎仪、DC-2030低温恒温槽,宁波新芝生物科技股份有限公司;FJS-6恒温数显磁力搅拌水浴锅,常州市顶新实验仪器有限公司;722S可见分光光度计,上海仪电公司;BT-纳米粒度仪(Zeta电位分析仪),丹东百特仪器有限公司;FM200高速剪切分散乳化机,上海弗鲁克科技发展有限公司;Cary Eclipse荧光光谱仪,安捷伦科技(中国)有限公司;IRAffinity-1S傅里叶变换红外光谱仪,日本岛津株式会社;HT-7700透射电子显微镜,日立(中国)有限公司。
1.3 实验方法
1.3.1 PP-HMP复合物的制备
将PP和果胶用蒸馏水溶解,制备质量浓度为8 mg/mL 的PP和HMP溶液,于25 ℃恒温搅拌水合过夜。然后将所制备的PP和HMP溶液以1∶1(质量比)混合,搅拌均匀后用0.1~2 mol/L 的HCl和NaOH溶液将混合溶液的pH值分别调至3.0、4.0、5.0、6.0、7.0、8.0,然后恒温搅拌4 h,超声处理(5.43 W/cm3,15 min,25 ℃)后备用。
1.3.2 PP-HMP复合物理化特性分析
1.3.2.1 浊度的测定
将不同pH值的PP-HMP复合物用分光光度计在600 nm下测定透光率,将待测样品放置于比色皿中,在常温下测定浊度,每组样品重复测定3次[13]。
1.3.2.2 粒径和电位的测定
将颗粒分散液用蒸馏水稀释100倍后,利用纳米粒度仪测定其粒径、PDI和Zeta-电位。平衡时间120 s,测定温度25 ℃,为避免多重光散射,每次循环扫描60次。每个样品重复测定3次[14]。
1.3.2.3 乳化活性和稳定性的测定
取5 mL大豆油加入10 mL PP-HMP混合溶液,在室温下用高速剪切机以13 000 r/min的转速剪切2 min,在第0 min和第40 min于样品底部吸取50 μL乳状液放入装有10 mL 0.1%(质量分数)SDS溶液的离心管中,混匀后立即在500 nm处进行吸光值的测定[15]。乳化活性(emulsifying activty index,EAI)和乳化稳定性(emulsifying stability index,ESI)计算公式如公式(1)、公式(2)所示:
式中:ρ,复合物质量浓度,g/mL,A0,乳状液在第0 min的吸光值,A40,乳状液在放置40 min的吸光值;t,间隔时间,40 min;φ,乳状液中的油相体积分数;T=2.303。
1.3.2.4 稳定性分析
将制备好的PP-HMP复合溶液放置于4 ℃冰箱中,定期观察样品是否出现沉淀,并用纳米粒度仪检测粒径大小和分布。
1.3.3 PP-HMP复合物结构特性分析
1.3.3.1 傅里叶红外光谱
将1.3.1节制备的PP和PP-HMP复合溶液冷冻干燥后取约2 mg与100 mg烘干后的KBr研磨混匀,然后使用压片机压制成薄片后扫描分析,设置波数范围4 000~400 cm-1,扫描次数32次,分辨率4 cm-1,采用Peak t软件分析蛋白的二级结构含量的变化[16]。
t软件分析蛋白的二级结构含量的变化[16]。
1.3.3.2 荧光光谱
将PP和PP-HMP复合溶液稀释10倍后使用荧光分光光度计进行测定,固定激发波长λex为280 nm,激发和发射狭缝宽度分别为2.5 nm和5 nm,扫描范围300~500 nm[17]。
1.3.3.3 透射电镜观察
将PP和PP-HMP溶液进行适当稀释,取约20 μL滴到覆有聚乙烯醇缩甲醛脂膜的铜网上,水平放置2 min使分子聚集体沉积到网面上,用滤纸吸去表面多余溶液,之后滴加2%(质量分数)磷钨酸溶液约20 μL放置2 min使颗粒充分染色,再用滤纸将铜网上多余染液进行吸取,置于红外灯下干燥后用透射电子显微镜观察并拍照[18]。
1.3.4 数据统计分析
每个试验重复3次,试验结果用平均值±标准差表示。采用SPSS 26.0软件Ducan检验法对数值进行差异显著性分析(P<0.05),Origin 8.0软件作图。
2 结果与分析
2.1 pH对PP-HMP复合物理化特性的影响
2.1.1 浊度
浊度是因样品的吸收或颗粒的散射而造成透射光的衰减,可以反映粒子的大小,表征溶液体系中颗粒的聚集程度和稳定性。图1表示PP、HMP和PP-HMP复合物的浊度随pH的变化。单一HMP溶液在不同pH下呈澄清透明状态,浊度值均低于0.1且无显著差异,PP由于在等电点附近会聚集沉淀,因此单一的PP在pH 4.0~6.0的范围内均发生不同程度的沉淀,pH 5时浊度最大,为1.203。而在PP-HMP复合体系中,随着pH的升高,复合物浊度呈现显著降低的趋势,与PP溶液相比,其浊度最大值向酸性pH值偏移。pH 3.0时PP-HMP复合体系出现明显的相分离现象,浊度呈现最大值1.276,此时形成不可溶复合物,颗粒分子相对较大,溶液颗粒聚集并形成沉淀;当pH值升高至6.0的过程中PP-HMP复合体系浊度急剧下降,颗粒分散液的透明度增大,这可能是由于HMP加入后产生的静电排斥和空间位阻效应抑制蛋白的聚集,聚合物开始解离,同时PP与HMP电荷相反部分实现络合,并增强HMP与PP之间的相互作用形成可溶性复合物,均匀分散在溶液中[19];pH值继续增大至8.0时,由于PP和HMP均带负电荷,两者因静电排斥作用而各自以单分子形态共存于溶液中[20]。
2.1.2 粒径和PDI
表1显示了pH对PP-HMP复合物的粒径和PDI的影响。pH对单独HMP的粒径和PDI影响不显著,在不同pH条件下无显著差异,而单独PP和PP-HMP复合物的粒径和PDI在不同pH条件下呈现显著差异。pH值为3.0时,PP溶液粒径和PDI都较小,而PP-HMP复合物的粒径较大为1.8 μm时,此时复合物不稳定容易形成沉淀,意味着不可溶复合物的形成;在pH 4.0~6.0时,单独PP分子间的聚集,粒径和PDI均较大,且粒径分布较为分散,在此条件下加入HMP可抑制蛋白的自聚集,并通过疏水和静电相互作用与蛋白发生络合,形成可溶性复合物,使其获得较小的粒径和更窄的分布[21];当pH值增大至7.0~8.0时得到的复合物粒径较小,这是由于蛋白质分子带净负电荷,与果胶分子之间发生静电排斥,导致果胶分子从颗粒表面解吸而发生共溶现象,得到的粒径也偏小。
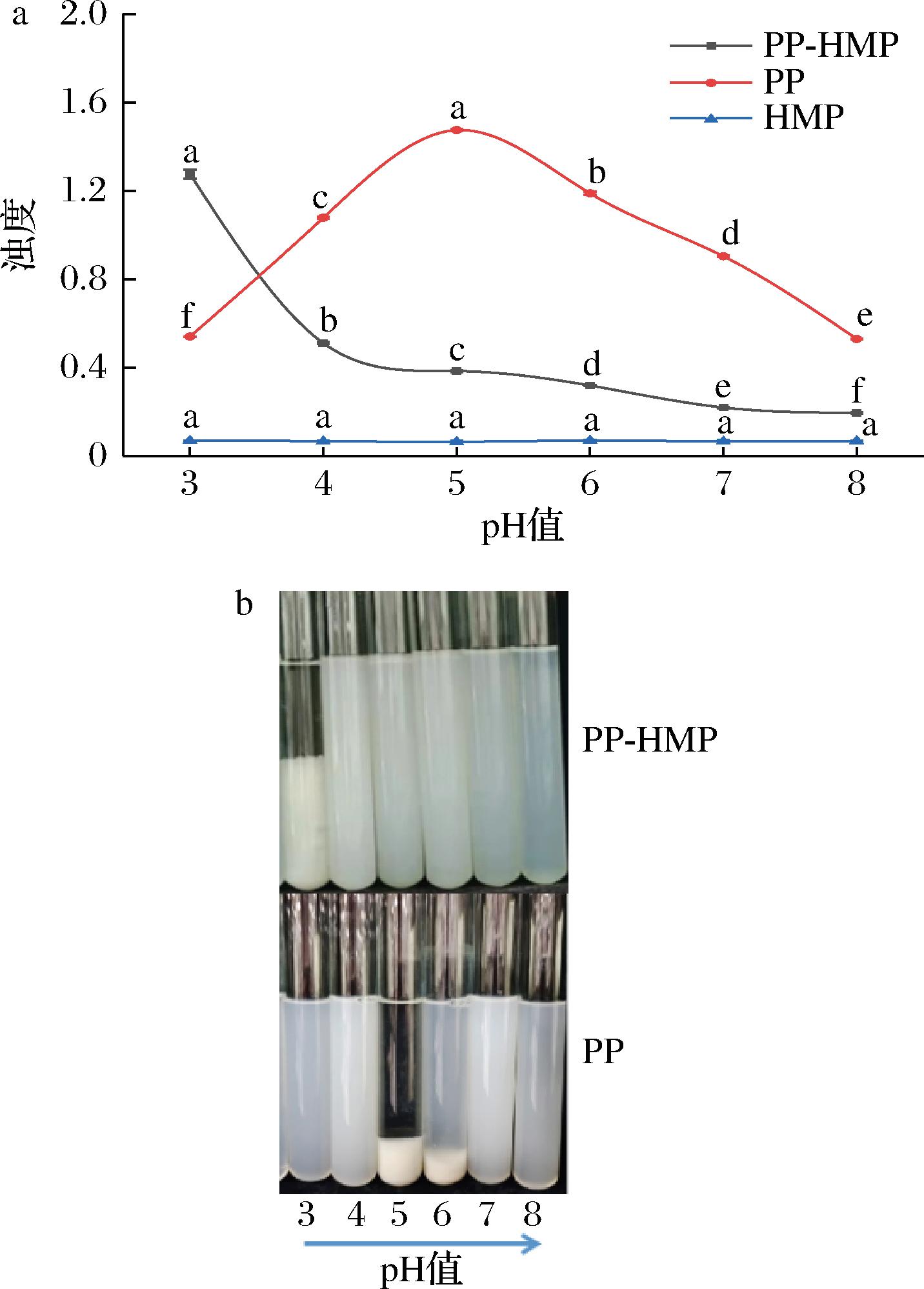
a-PP和PP-HMP复合物的浊度;b-PP和PP-HMP复合物的外观图
图1 pH对PP和PP-HMP复合物浊度的影响
Fig.1 Turbidity of PP and PP-HMP complex by pH 注:不同小写字母表示同一样品不同pH差异显著(P<0.05)(下同)。
表1 pH对PP和PP-HMP复合物粒径和PDI的影响
Table 1 Particle size, PDI of PP and PP-HMP complex by pH
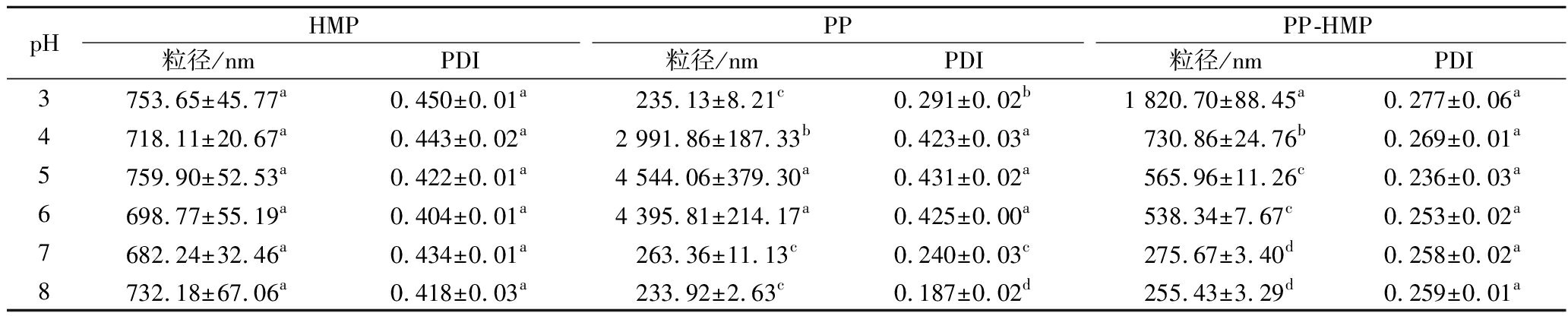
pHHMPPPPP-HMP粒径/nmPDI粒径/nmPDI粒径/nmPDI3753.65±45.77a0.450±0.01a235.13±8.21c0.291±0.02b1 820.70±88.45a0.277±0.06a4718.11±20.67a0.443±0.02a2 991.86±187.33b0.423±0.03a730.86±24.76b0.269±0.01a5759.90±52.53a0.422±0.01a4 544.06±379.30a0.431±0.02a565.96±11.26c0.236±0.03a6698.77±55.19a0.404±0.01a4 395.81±214.17a0.425±0.00a538.34±7.67c0.253±0.02a7682.24±32.46a0.434±0.01a263.36±11.13c0.240±0.03c275.67±3.40d0.258±0.02a8732.18±67.06a0.418±0.03a233.92±2.63c0.187±0.02d255.43±3.29d0.259±0.01a
2.1.3 Zeta-电位
Zeta-电位反映了在水溶性递送系统中分散体的稳定性,一定条件下,体系电位值越高,溶液粒子间的斥力位能越大,体系的稳定性越好[22]。PP-HMP复合物的Zeta-电位随pH的变化如图2所示。PP的Zeta-电位随pH的增加呈现逐渐降低的趋势,pH值接近5.0时约为0 mV,表明此时溶解的蛋白静电荷为0,即为PP的等电点。HMP和PP-HMP复合物的Zeta-电位都呈现出先下降后升高的趋势。pH 3.0时,单独PP带较多正电荷,与阴离子多糖HMP之间存在强烈的静电作用,出现大范围聚集并形成不溶性复合物,此时pH<果胶的pKa(3.5左右),果胶分子的电离过程受到抑制,所携带的电荷量会明显降低,复合物电位绝对值也较低,体系较不稳定;随着pH升高至PP等电点附近时,PP的正静电荷显著减少,可通过静电相互作用有效地与果胶的阴离子基团发生结合形成稳定的可溶性复合物;当pH>PP等电点至6.0时,PP和HMP溶液负电荷都增多,两者之间的静电排斥作用增大,研究表明PP中11S组分的等电点在6.4左右,因此pH 6.0时不仅存在PP局部正电荷区域与HMP之间的静电相互作用,同时存在11S组分与HMP的静电相互作用[20],此时复合物的Zeta-电位绝对值达到最大,形成可溶性复合物,与浊度、外观以及粒径的测定结果一致(图1、表1);pH值继续升高至7.0~8.0时,过量阴离子基团的存在使两者之间存在强烈的静电相斥作用,使蛋白和果胶分子以独立高分子存在,HMP所带负电荷显著减少,溶液水相中的HMP分子减少,导致复合物Zeta电位的绝对值向更小的方向移动。
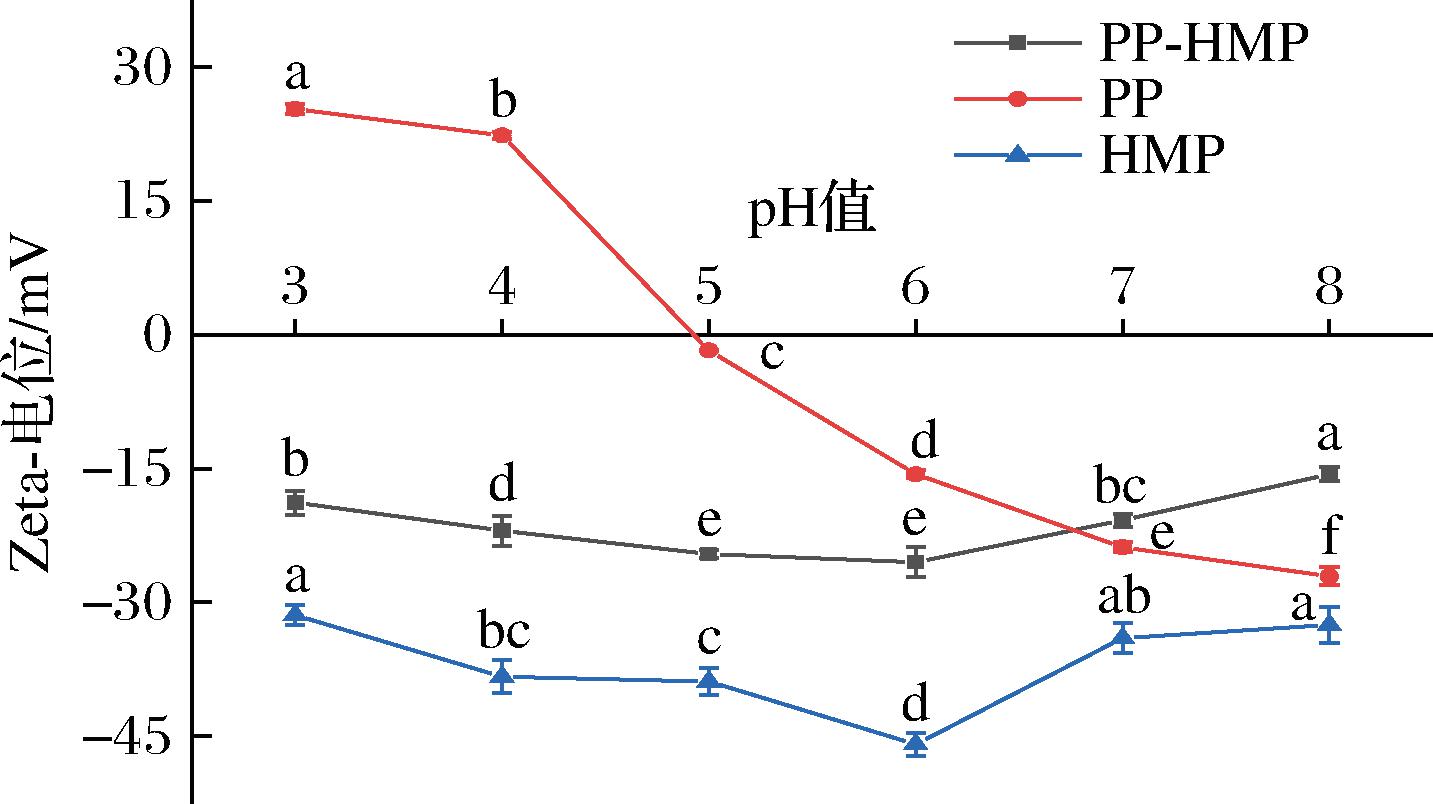
图2 pH对PP和PP-HMP复合物Zeta电位的影响
Fig.2 Zeta-potential of PP and PP-HMP complex by pH
2.1.4 乳化活性和乳化稳定性
图3是pH对PP-HMP复合物乳化活性和稳定性的影响以及乳液放置1 d后的外观图。pH 3.0时PP-HMP复合体系的乳化活性和稳定性均较差,制备的乳液很快出现絮凝并在10 min左右开始分层,此时PP-HMP复合体系形成大颗粒不溶性复合物,乳化后分子之间的桥连作用促进了被包裹的液滴的聚集,而且不溶性聚集体在油水界面上的吸附速度较慢[23],说明pH 3不适合用作乳液制备的条件;随着pH的增大,复合物的乳化活性和稳定性显著增大,放置1 d后分层现象明显改善,当pH值高于6时,带负电的果胶分子从乳液油滴的表面解吸,和液滴表面之间的相互作用也变弱,可能更容易从一个液滴上分离并与另一液滴结合,从而促进桥联絮凝,并且水相中未吸附的果胶也会诱导蛋白包裹的乳液液滴发生絮凝[10]。
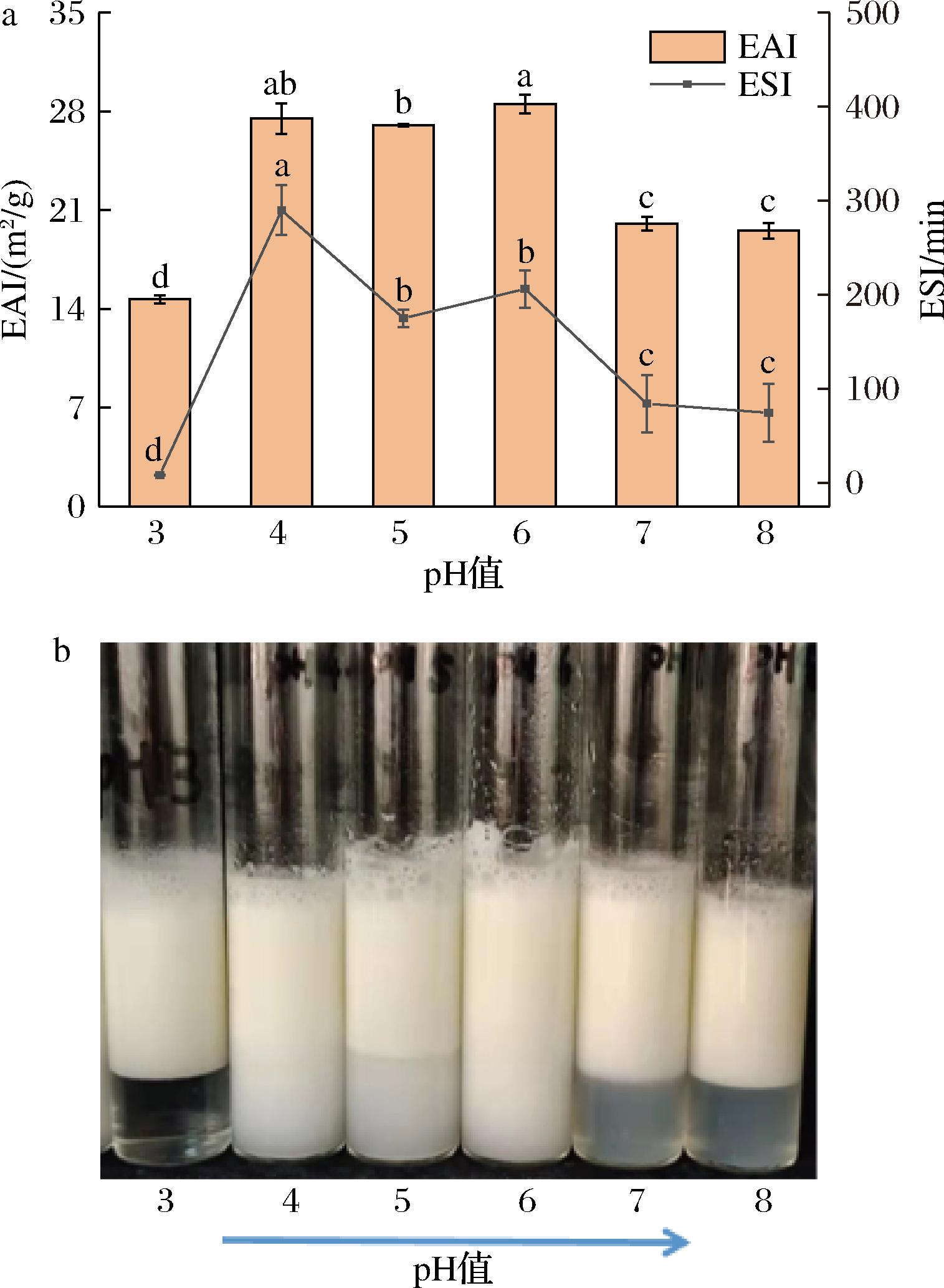
a-PP-HMP复合物的乳化活性和稳定性;b-PP-HMP乳状液的外观图
图3 pH对PP-HMP复合物乳化活性和稳定性的影响
Fig.3 Emulsifying activity and stability of PP-HMP complex by pH
2.1.5 稳定性
图4表示PP-HMP复合物在pH值为3、6、8时的储藏稳定性。PP-HMP复合物在pH 3时放置1 d即出现明显沉淀,随着储藏时间的增加,24 d时复合物粒径显著增大;pH 8下放置6 d时出现轻微沉淀,储藏时间越长粒径越大;而pH 6下放置24 d粒径显著增大但未出现明显沉淀,表明PP-HMP复合物在pH 6时具有相对良好的储存稳定性,显示了此时复合物较高的实际应用价值。
2.2 pH对PP-HMP复合物结构特性的影响
2.2.1 内源荧光光谱
蛋白质的内源荧光主要来源于色氨酸(Trp)残基,可以反映蛋白质的三级结构和极性变化。图5为PP-HMP复合物的荧光光谱图。与单独的PP溶液相比,PP-HMP复合物在pH 6的最大发射波长发生明显红移,说明复合物的形成改变了Trp残基的微环境,表明疏水相互作用参与了复合物的形成,降低了蛋白分子中氨基酸残基的暴露程度,使其形成了更紧密的三级构象[24];相对于pH 6,PP-HMP复合物在pH 3和pH 8的最大吸收波长发生明显蓝移,且随着pH的减小,最大荧光强度明显降低,可能是由于蛋白质结构的重排和解折叠使得Trp等氨基酸残基由于分子内相互作用力处于更为疏水的环境,从而减弱了复合物的猝灭效率[25]。
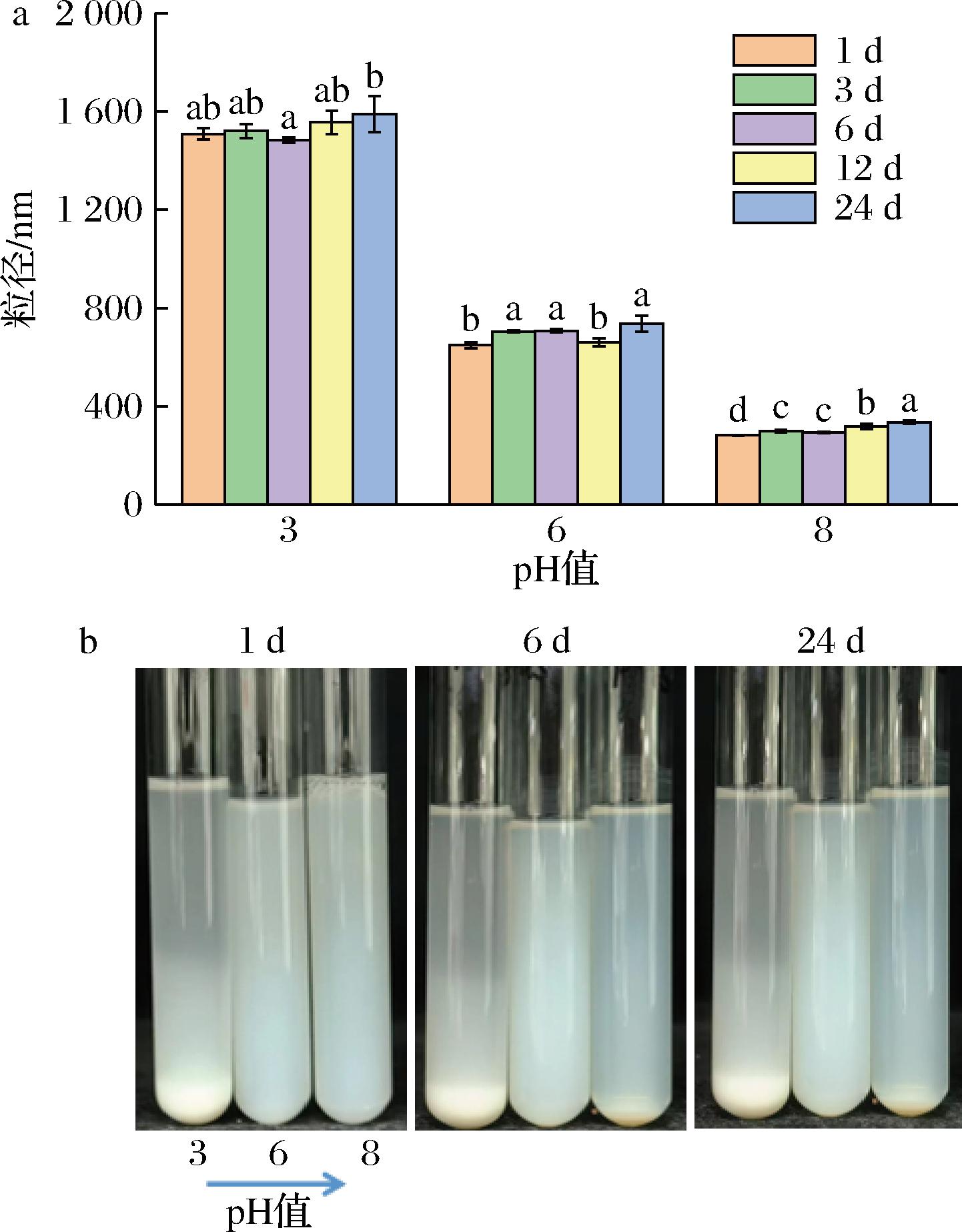
a-PP-HMP复合物的粒径;b-PP-HMP复合物储藏不同时间的外观图
图4 不同pH下PP-HMP复合物的粒径随储藏时间的变化
Fig.4 Change of particle size of PP-HMP complexes with storage time at different pH 注:不同字母表示同一pH样品在不同储存条件差异显著(P<0.05)。
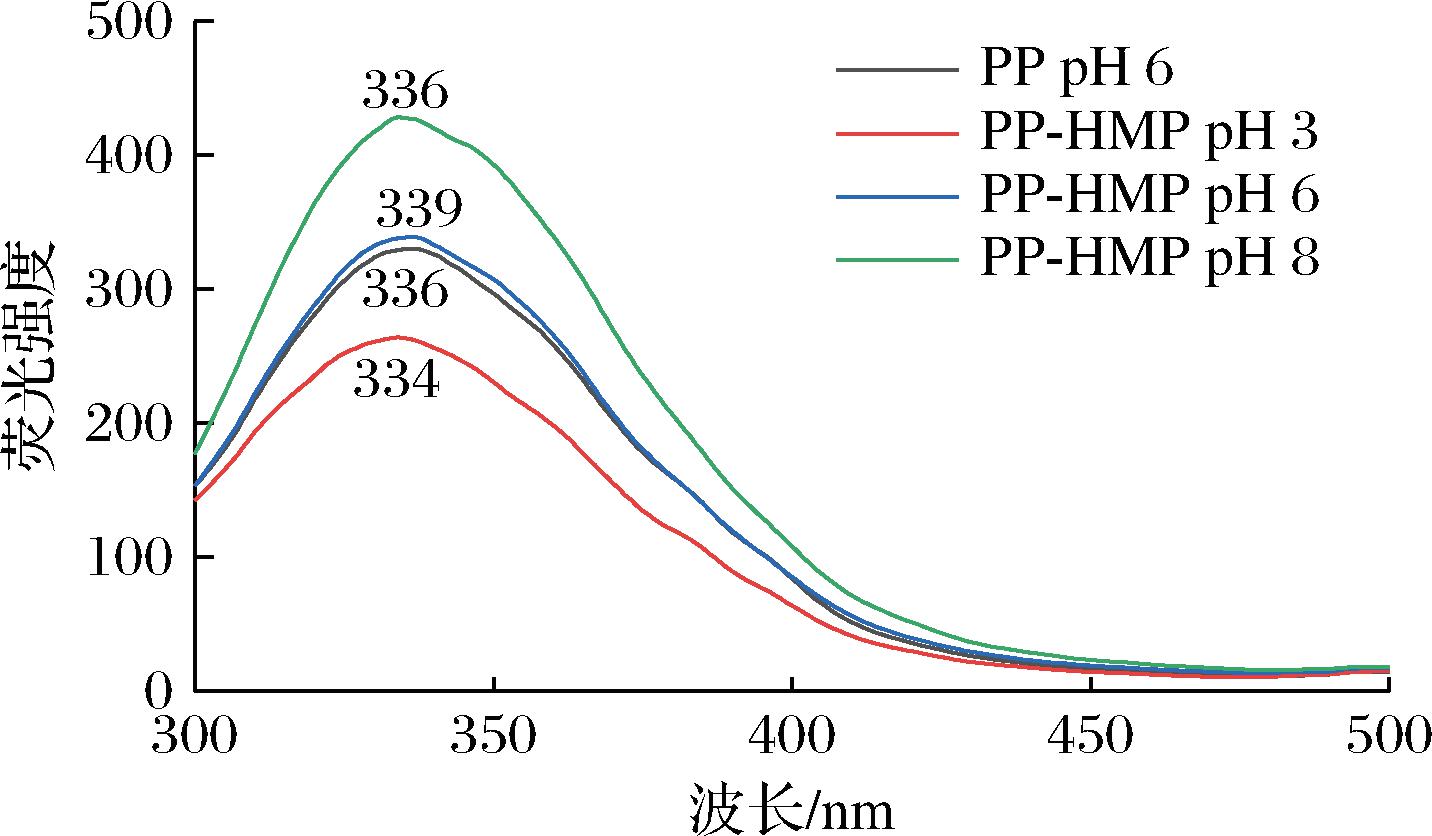
图5 PP-HMP复合物的荧光光谱图
Fig.5 Fluorescence spectra of PP-HMP complex
2.2.2 红外光谱特性
图6-a为PP-HMP的FTIR图谱,加入HMP之后,PP-HMP复合物与单独PP相比在1 103~1 020 cm-1 和1 747 cm-1处出现新的吸收峰,其中1 103~1 020 cm-1处吸收峰是由羧基形成的—COOR(C—O)和—COO—伸缩振动引起,是HMP中的半乳糖醛酸在指纹区(1 473~1 000 cm-1)的特征吸收峰[26],表明PP和HMP之间存在相互作用,而不同pH的PP-HMP复合物在不同波段的吸收峰出现不同程度的蓝移或者红移。PP-HMP复合物在pH 3.0条件下酰胺A带和B带红移,说明N—H、O—H、C—H发生伸缩振动,两者之间存在氢键相互作用,酰胺Ⅱ带出现红移,酰胺Ⅲ带出现大幅蓝移说明PP和HMP之间的相互作用可能涉及C—N共价键的相互作用;复合物在pH 6.0时的光谱图酰胺Ⅱ带和酰胺A带发生红移,代表N—H发生弯曲振动、C—N、N—H及C—C键发生伸缩振动,而且O—H伸缩振动带发生明显红移,这说明HMP通过氢键和疏水相互作用与PP发生结合[12];此外,pH 8.0时—OH发生伸缩振动,这可能是由于HMP上的羟基在碱性条件下被氧化,C—N共价键的伸缩引起振动酰胺Ⅲ带出现轻微蓝移[27]。傅里叶红外光谱图表明pH值会影响PP和HMP之间的相互作用。
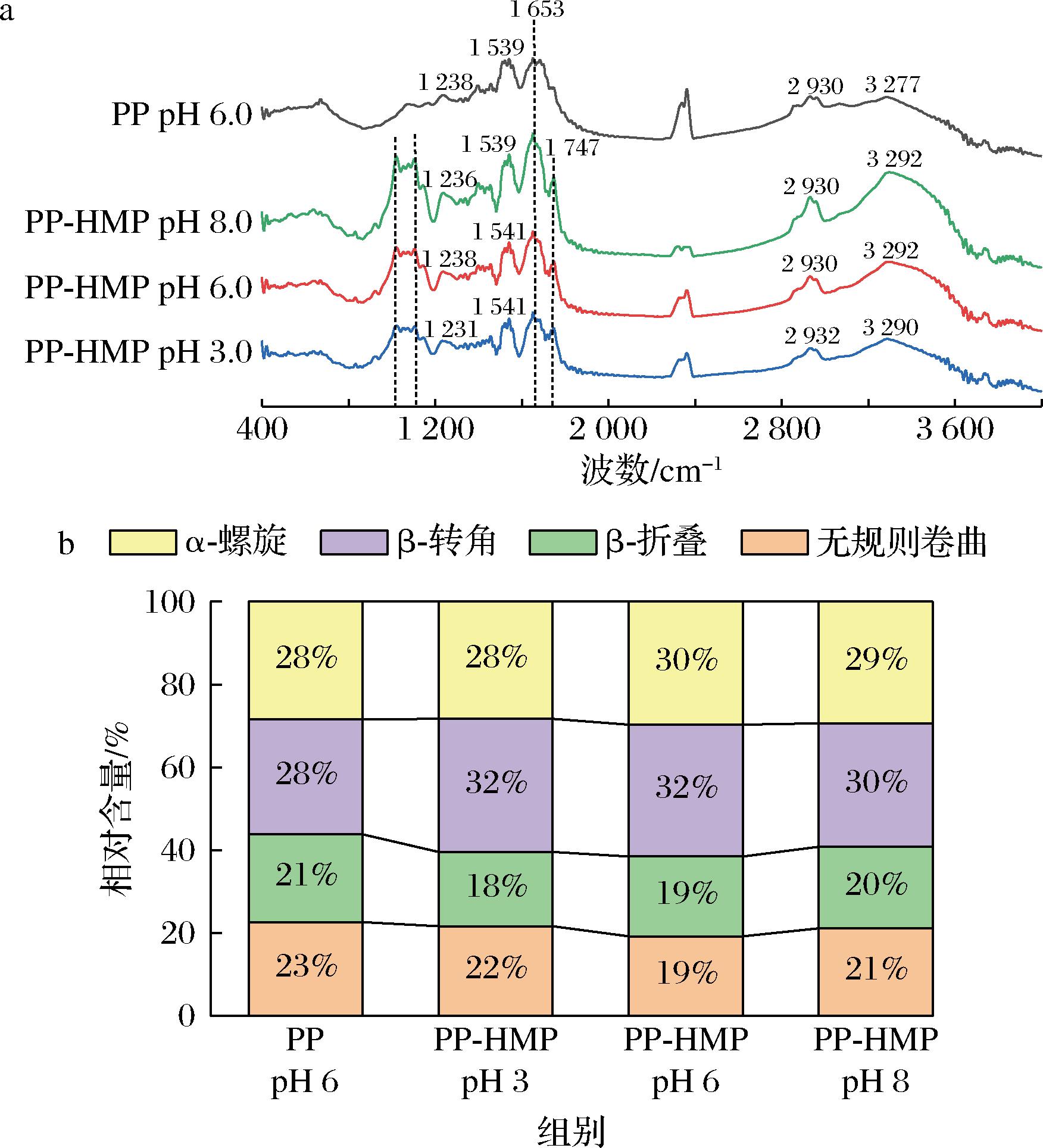
a-红外光谱图;b-二级结构相对含量
图6 PP-HMP复合物的红外光谱图和二级结构相对含量
Fig.6 FTIR and secondary structure fractions of PP-HMP complex
蛋白质二级结构的定量信息如图6-b所示。与PP相比,PP-HMP可溶复合物的β-折叠和无规卷曲相对含量减少,β-转角和α-螺旋相对含量增大,表明在pH 6条件下HMP能够抑制PP的聚集,可以使PP的结构更加有序,刚性结构增强,同时更易于形成界面吸附,提高PP-HMP复合物的乳化活性和乳化稳定性[28]。不同pH会影响PP-HMP复合物二级结构的相对含量,与pH 6相比,pH 3和pH 8时复合物的无规卷曲结相对含量增加,而α-螺旋相对含量减少,复合物在这2种pH条件下形成较多无序的分子结构导致乳化活性和稳定性较低,不利于乳液的制备。
2.2.3 透射电镜观察
图7为PP-HMP复合物的透射电镜图,浅灰色为HMP的网络结构,黑色部分为PP的显色,单独PP在pH 6.0时呈现出形态规则的球状结构(图7-a),加入果胶后,从图7-c中可以看出果胶的网络结构嵌入蛋白的球状结构中,复合颗粒形成形态统一并且规则有序的花蕾状结构,且粒径较小并分散均匀,说明pH 6时的PP和HMP通过复合形成了具有核-壳结构的纳米颗粒,有利于乳液的稳定。而pH 3状态下PP结构展开和果胶相互作用被果胶大量覆盖,导致聚合物桥联絮凝,乳液不稳定而快速分层,跟上述乳化活性和稳定性的结果一致。在pH 8条件下蛋白和果胶分别以各自独立的形态存在,呈现出形态大小均不太规则的类似球形结构。
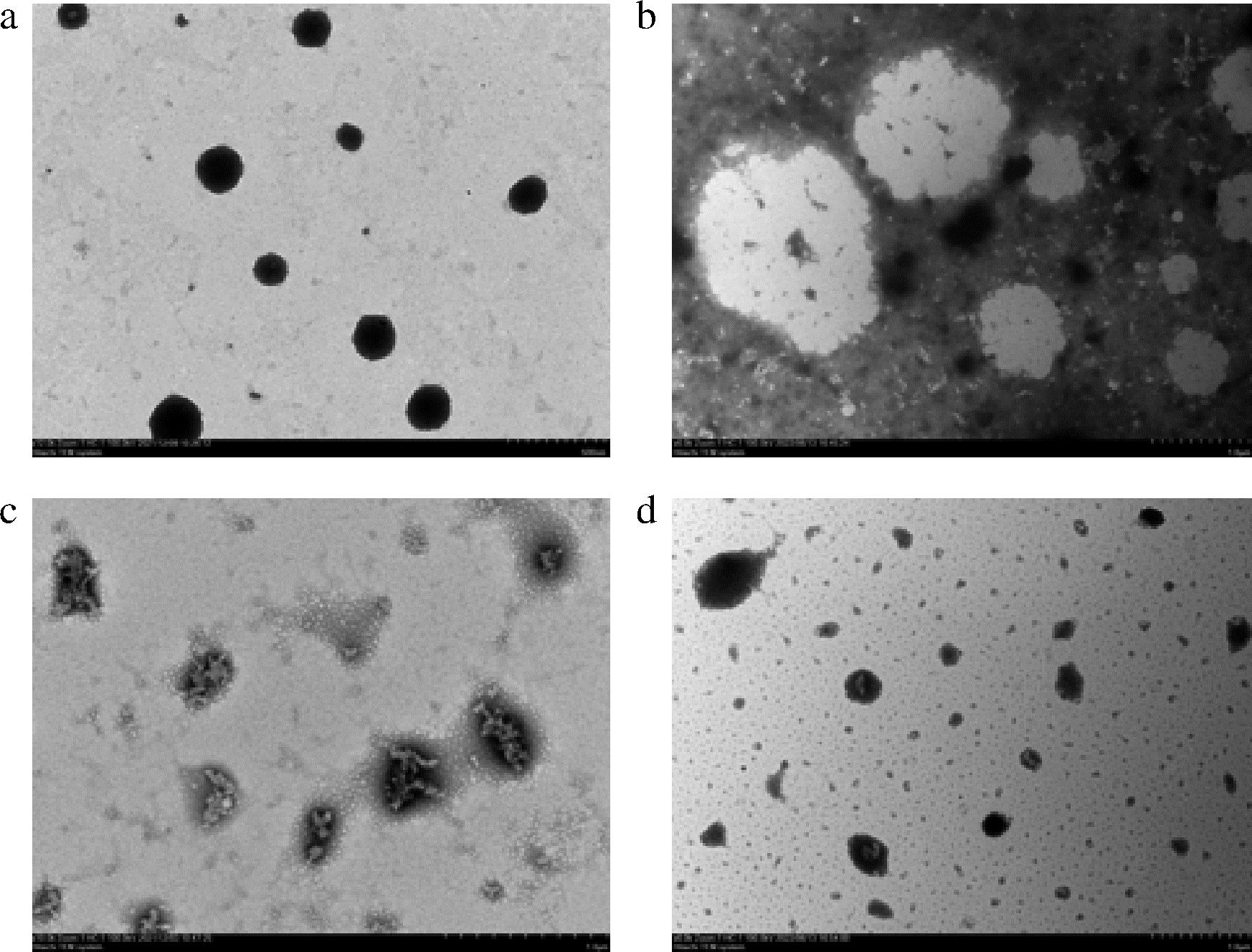
a-PP-pH 6;b-PP-HMP pH 3;c-PP-HMP pH 6; d-PP-HMP pH 8
图7 PP-HMP复合物的透射电镜图
Fig.7 Transmission electron micrographs of PP and PP-HMP complex
3 结论
本文研究了不同pH对PP-HMP复合物理化和结构特性的影响,得出以下结论:PP和HMP在pH 3.0、6.0和8.0时分别以不可溶复合物、可溶性复合物和共溶状态存在;与pH 3.0和8.0相比,PP-HMP复合物在pH 6.0时Zeta-电位绝对值、乳化活性和稳定性较高,放置24 d未发生分层现象,并且与单独PP相比,PP-HMP复合物的β-转角和α-螺旋相对含量增大,色氨酸残基的暴露程度降低,结构更加有序紧密。透射电镜结果显示,pH 3.0、8.0时,PP-HMP复合物呈现出形态大小不规则的结构;pH 6.0时PP-HMP复合物呈现分散均匀且形态规则有序的结构,适合乳液的制备。研究结果表明,pH可以改善PP-HMP复合物的理化和功能特性,为蛋白-多糖复合物在食品中的应用提供理论基础。
[1] BOYE J, ZARE F, PLETCH A.Pulse proteins:Processing, characterization, functional properties and applications in food and feed[J].Food Research International, 2010, 43(2):414-431.
[2] 张争全, 田少君, 王艳红, 等.豌豆蛋白-阿拉伯胶相互作用及其复合物乳化特性研究[J].食品科技, 2021, 46(2):232-237. ZHANG Z Q, TIAN S J, WANG Y H, et al.Study on the interaction between pea protein and gum Arabic and the emulsifying properties of the complex[J].Food Science and Technology, 2021, 46(2):232-237.
[3] LI X L, XIE Q T, LIU W J, et al.Self-assembled pea protein isolate nanoparticles with various sizes:Explore the formation mechanism[J].Journal of Agricultural and Food Chemistry, 2021, 69(34):9905-9914.
[4] KARACA A C, LOW N, NICKERSON M.Emulsifying properties of chickpea, faba bean, lentil and pea proteins produced by isoelectric precipitation and salt extraction[J].Food Research International, 2011, 44(9):2742-2750.
[5] AROGUNDADE L A, TSHAY M, SHUMEY D, et al.Effect of ionic strength and/or pH on Extractability and physico-functional characterization of broad bean (Vicia faba L.) Protein concentrate[J].Food Hydrocolloids, 2006, 20(8):1124-1134.
[6] KLEMMER K J, WALDNER L, STONE A, et al.Complex coacervation of pea protein isolate and alginate polysaccharides[J].Food Chemistry, 2012, 130(3):710-715.
[7] LIU J R, NAKAMURA A, CORREDIG M.Addition of pectin and soy soluble polysaccharide affects the particle size distribution of casein suspensions prepared from acidified skim milk[J].Journal of Agricultural and Food Chemistry, 2006, 54(17):6241-6246.
[8] DICKINSON E.Interfacial structure and stability of food emulsions as affected by protein-polysaccharide interactions[J].Soft Matter, 2008, 4(5):932-942.
[9] ALBANO K M, CAVALLIERI  L F, NICOLETTI V R.Electrostatic interaction between soy proteins and pectin in O/W emulsions stabilization by ultrasound application[J].Food Biophysics, 2020, 15(3):297-312. [10] GHARSALLAOUI A, YAMAUCHI K, CHAMBIN O, et al.Effect of high methoxyl pectin on pea protein in aqueous solution and at oil/water interface[J].Carbohydrate Polymers, 2010, 80(3):817-827.
L F, NICOLETTI V R.Electrostatic interaction between soy proteins and pectin in O/W emulsions stabilization by ultrasound application[J].Food Biophysics, 2020, 15(3):297-312. [10] GHARSALLAOUI A, YAMAUCHI K, CHAMBIN O, et al.Effect of high methoxyl pectin on pea protein in aqueous solution and at oil/water interface[J].Carbohydrate Polymers, 2010, 80(3):817-827.
[11] LIANG L, LUO Y C.Casein and pectin:Structures, interactions, and applications[J].Trends in Food Science &Technology, 2020, 97:391-403.
[12] 薛丽莹, 田泽鹏, 陈若桐, 等.pH处理对EGCG与大豆蛋白相互作用的影响[J].食品科技, 2022, 47(7):121-128. XUE L Y, TIAN Z P, CHEN R T, et al.Effect of pH treatment on the interaction between EGCG and soy protein[J].Food Science and Technology, 2022, 47(7):121-128.
[13] LEE H, YILDIZ G, DOS SANTOS L C, et al.Soy protein nano-aggregates with improved functional properties prepared by sequential pH treatment and ultrasonication[J].Food Hydrocolloids, 2016, 55:200-209.
[14] SOUZA C J F, GARCIA-ROJAS E E.Effects of salt and protein concentrations on the association and dissociation of ovalbumin-pectin complexes[J].Food Hydrocolloids, 2015, 47:124-129.
[15] PEARCE K N, KINSELLA J E.Emulsifying properties of proteins:Evaluation of a turbidimetric technique[J].Journal of Agricultural and Food Chemistry, 1978, 26(3):716-723.
[16] TATULIAN S A.FTIR analysis of proteins and protein-membrane interactions[J].Methods in Molecular Biology, 2003:281-325.DOI:10.1007/978-1-4939-9512-7_13.
[17] BASAK S, CHATTOPADHYAY K.Studies of protein folding and dynamics using single molecule fluorescence spectroscopy[J].Physical Chemistry Chemical Physics, 2014, 16(23):11139-11149.
[18] 冷小京, 柴智, 任发政, 等.应用动态光散射和透射电镜研究热力学不相容条件下果胶与乳清蛋白混合体系的微观结构[J].光谱学与光谱分析, 2010, 30(8):2196-2200. LENG X J, CHAI Z, REN F Z, et al.Study of microstructure of pectin and whey protein isolate mixtures under incompatible conditions using dynamic light scattering and transmission electron microscopy[J].Spectroscopy and Spectral Analysis, 2010, 30(8):2196-2200.
[19] WEINBRECK F, DE VRIES R, SCHROOYEN P, et al.Complex coacervation of whey proteins and gum Arabic[J].Biomacromolecules, 2003, 4(2):293-303.
[20] 喻靖. 柑橘果胶-大豆分离蛋白静电相互作用、界面吸附特性及其乳化稳定性研究[D].武汉:华中农业大学, 2016. YU J.Research on citrus pectin-soy protein isolate electrostatic interaction, characteristic of interafacial adsorption and emulsifying stability[D].Wuhan:Huazhong Agricultural University, 2016.
[21] 石佳卉, 张安琪, 陈爽, 等.大豆分离蛋白-维生素D3复合物的结构及性质[J].中国食品学报, 2022, 22(7):49-55. SHI J H, ZHANG A Q, CHEN S, et al.Structure and properties of soy protein isolate-vitamin D3 complex[J].Journal of Chinese Institute of Food Science and Technology, 2022, 22(7):49-55.
[22] TIAN Y, ZHANG Z, TAHA A, et al.Interfacial and emulsifying properties of β-conglycinin/pectin mixtures at the oil/water interface:Effect of pH[J].Food Hydrocolloids, 2020, 109:106145.
[23] BUSU N M, AMONSOU E O.Fractionation pH of Bambara groundnut (Vigna subterranea) protein impacts the degree of complexation with gum Arabic[J].Food Hydrocolloids, 2019, 87:653-660.
[24] XUE F, LI C, ZHU X W, et al.Comparative studies on the physicochemical properties of soy protein isolate-maltodextrin and soy protein isolate-gum acacia conjugate prepared through Maillard reaction[J].Food Research International, 2013, 51(2):490-495.
[25] 曾琪, 胡淼, 王欢, 等.pH值处理对黑豆分离蛋白结构、流变特性及乳化性能的影响[J].食品科学, 2020, 41(22):15-21. ZENG Q, HU M, WANG H, et al.Effect of pH treatment on structure, rheological properties and emulsifying properties of black bean protein isolate[J].Food Science, 2020, 41(22):15-21.
[26] 梁婉玲. 高酯果胶的结构及功能特性研究[D].广州:华南理工大学, 2021. LIANG W L.Study on structure and functional properties of high methoxyl pectin[D].Guangzhou:South China University of Technology, 2021.
[27] WANG Q M, TANG Y W, YANG Y X, et al.Interaction between wheat gliadin and quercetin under different pH conditions analyzed by multi-spectroscopy methods[J].Spectrochimica Acta Part A:Molecular and Biomolecular Spectroscopy, 2020, 229:117937.
[28] 龙慧, 李祎, 朱叶力, 等.银耳多糖与大豆分离蛋白的相互作用及流变性能[J].食品科学, 2022, 43(16):160-168. LONG H, LI Y, ZHU Y L, et al.Interaction between Tremella fuciformis polysaccharide and soybean protein isolate:Rheological properties of their mixtures[J].Food Science, 2022, 43(16):160-168.