
a-AFM图像;b-直径;c-长度
图1 不同质量分数硫酸水解制备的CNCs的AFM图像、直径和长度分布频率
Fig.1 AFM images, and length distribution frequency of CNCs prepared at different concentrations of sulfuric acid solution
纤维素是地球上最丰富的天然聚合物之一,纳米纤维素是具有纳米尺寸的纤维素衍生物,广泛来源于农业废弃物(如茶渣、甘蔗渣、玉米壳、菠萝皮渣等[1-2])。纤维素纳米晶(cellulose nanocrystals,CNCs)是纤维素精细化处理后获得的一类棒状、高结晶度的纳米级纤维素材料,因其强机械性能而备受关注,同时兼具较好的可持续性、生物相容性、生物降解性、亲水性和高比表面积等优良特性[3-5]。近年来,由于CNCs独特的纳米结构、天然两亲性和环境稳定性,其作为食品级乳化剂应用于Pickering乳液领域受到广泛关注[2,6-9]。CNCs的天然两亲性依赖于(200)β/(220)α的疏水边缘平面,同时CNCs还可以沿着油/水界面弯曲(适应油滴的曲率),这种在界面上的小变形促进了CNCs在油水界面的润湿和吸附,而CNCs的粒径形貌和电荷会影响其在界面上的吸附,进而影响乳液稳定性[9-10]。目前研究纳米纤维素形貌对Pickering乳液的影响主要集中在不同类型的纳米纤维素(如CNCs和纤维素纳米纤丝),关于不同粒径CNCs稳定的Pickering乳液研究鲜有报道。此外,对CNCs的粒径适当调控,可能对Pickering乳液界面和连续相形成双向调控,具有重要的研究价值。
CNCs的表面特性主要与其制备方法有关[11]。酶解法时间长并且成本高,氧化降解法无法回收化学试剂,有机酸法反应效率低,而无机酸法高效且产品均一性、稳定性相对较好[12]。目前酸水解制备CNCs中最常用的是质量分数为64%的硫酸溶液,硫酸水解导致纤维素结构中的无定形区域和亚结晶区域优先被破坏和去除,而结晶区域由于结构紧密,对酸具有较强抵御力而不易水解[13]。此外,硫酸通过酯化过程与纤维素的表面羟基进行反应,允许阴离子硫酸酯基团的接枝,进而产生强静电排斥促进CNCs在水中的分散[14]。需要注意的是,酸水解制备CNCs的形貌和理化特性因纤维素来源和酸水解参数的差异而影响较大。考虑到生产成本、经济和环境效益,适量降低硫酸水解时的酸浓度对生产CNCs具有重要意义,同时可能会实现对CNCs表面特性(如粒径、电位)的有效调控。
因此,本研究以典型果蔬加工副产物菠萝皮渣为原料提取纤维素,以前期预试验验证的可水解生成CNCs的有效硫酸浓度范围为基础,进一步研究不同质量分数硫酸(58%~64%)水解菠萝皮渣纤维素制备CNCs,从官能团、粒径、电位、热稳定性等方面对CNCs的结构和理化性质分析;进一步以CNCs作为稳定剂制备Pickering乳液,考察CNCs浓度和形态对Pickering乳液粒径、微观结构和储藏稳定性的影响。研究结果将为硫酸水解制备果蔬皮渣来源的CNCs提供基础数据,并为不同形貌和粒径的CNCs稳定Pickering乳液应用提供参考。
菠萝皮渣,重庆市北碚区永辉超市提供;菠萝皮渣纤维素,自制;葵花籽油,上海佳格食品有限公司;硫酸、NaOH、NaClO2,重庆川东化工(集团)有限公司;NaCl,成都金山化学试剂有限公司。所有试剂均为分析纯。
Heraeus Multifuge X3R型台式高速冷冻离心机,美国赛默飞世尔科技公司;BX 53型荧光正置显微镜,日本OLYMPUS公司;Spectrun 100型红外光谱仪,美国PerkinElmer公司;DTG-60A/60AH型热重仪,日本岛津公司;FD-1-50型真空冷冻干燥机,中国北京博益康实验仪器有限公司;XHF-DY型高速分散器,宁波新芝有限公司;KQ3200DV型超声波清洗仪,昆山超声仪器有限公司;Mastersizer 3000型激光粒度仪、ZEN 3690型马尔文纳米粒度电位仪,英国Malvern公司。
1.3.1 菠萝皮渣CNCs的制备
以课题组前期制备的菠萝皮渣纤维素为原料[15-16],采用传统硫酸水解法进一步制备CNCs。配制质量分数为58%、61%和64%的硫酸溶液,将菠萝皮渣纤维素与硫酸溶液按料液比1∶20(g∶mL)混合,45 ℃水浴搅拌加热1.5 h,然后加入10倍体积预冷蒸馏水(4 ℃)以终止反应,多次离心(4 000 r/min,15 min)和蒸馏水洗涤以洗去酸液,直至出现浑浊CNCs悬浮液,收集悬浮液后透析,4 ℃保存备用,部分冷冻干燥用于结构表征。根据水解时使用硫酸溶液质量分数,制备的CNCs分别命名为CNCs-58%、CNCs-61%和CNCs-64%。
1.3.2 原子力显微镜(atomic force microscope,AFM)分析
将CNCs悬浮液稀释至质量分数为0.01%,经超声波处理后,吸取一滴悬浮液滴于新鲜剥离的云母片上,室温干燥5 h,采用带有硅悬臂探头(5 N/m)的AFM仪器测试样品粒径和形貌,最后使用Nano Measurer 1.2软件对图片进行处理。
1.3.3 红外光谱(Fourier transform infrared spectroscopy,FTIR)测定
采用KBr压片法制样,使用FTIR光谱仪在4 000~600 cm-1的波数范围内进行扫描,扫描频率为4 cm-1,扫描次数为 32次。
1.3.4 粒径和电位测定
采用马尔文纳米粒度电位仪测定CNCs的粒径和Zeta电位。将CNCs悬浮液稀释至质量分数为0.1%后进行测试,测试温度为25 ℃,平衡时间为120 s。
1.3.5 热重分析(thermogravimetric analysis,TGA)
分别准确称取10 mg干燥CNCs样品,使用热重分析仪在N2氛围下以10 ℃/min的加热速率对样品进行热性能测试,测试温度范围为30~550 ℃。
1.3.6 CNCs稳定的Pickering乳液制备
以CNCs悬浮液为水相,葵花籽油为油相制备乳液,油相体积分数为50%。制备乳液之前先在CNCs悬浮液中加入50 mmol/L NaCl以屏蔽部分电荷,油水相混合后在15 000 r/min下高速剪切均质1 min形成Pickering乳液,储存在4 ℃冰箱中备用。在固定油相比例的条件下,制备不同CNCs和颗粒浓度(质量分数0.2%、0.5%和1.0%)下稳定的Pickering乳液。
1.3.7 乳液外观与光学显微镜观测
使用相机拍摄乳液外观照片以直观观察乳液的分层现象。使用光学显微镜观察乳液,获得乳液的显微镜图像。
1.3.8 乳液粒径和电位测定
采用激光粒度分析仪测定液滴粒径和尺寸分布,乳液粒径测量报告为体积平均直径(d4,3)所有样品测量3次,取平均值。采用纳米粒度电位仪测定Zeta电位,每个样品至少测量3次,取平均值。
所有样品至少重复测量3次,获得的部分数据表示为平均值±标准偏差,使用SPSS Statistics 23、Origin 2018和Nano Measurer 1.2等软件进行数据分析。
不同浓度硫酸水解制备的CNCs的AFM图像如图1-a所示。CNCs-58%呈现相对较长的细丝状形貌,分散不均匀,存在一定聚集缠绕形貌;CNCs-61%呈较短的细棒状,粒径有所减小,同时其良好的分散性能使其呈现相互缠结的纤维网络结构;CNCs-64%表现出传统CNCs的典型短棒状形貌结构,粒径明显较小,CNCs颗粒分散较好且粒径尺寸相对均匀,不具有相互缠绕的网络结构。

a-AFM图像;b-直径;c-长度
图1 不同质量分数硫酸水解制备的CNCs的AFM图像、直径和长度分布频率
Fig.1 AFM images, and length distribution frequency of CNCs prepared at different concentrations of sulfuric acid solution
CNCs的直径和长度分布分别如图1-b和1-c所示。CNCs-58%的长度和直径分别主要分布在350~500 nm和9~21 nm,且各范围分布占比相对平均,表明整体尺寸均一性相对较差;CNCs-61%长度主要分布在250~300 nm,直径主要分布在7~13 nm,尺寸均一性较好;CNCs-64%长度主要分布在150~200 nm,直径主要分布在9~15 nm,粒径最短且整体尺寸均一性较好。整体上,随着硫酸溶液浓度的增加,纤维素非晶区域水解程度增强,获得的CNCs直径和长度均明显降低,产品均一性增加。
不同质量分数硫酸水解制备的CNCs的FTIR图谱如图2所示。所有样品均表现出相似的纤维素特征吸收峰,包括3 350~3 450 cm-1(—OH拉伸振动),2 899 cm-1(C—H拉伸振动),1 050 cm-1(C—O—C拉伸振动),1 430 cm-1(—CH2弯曲振动)和896 cm-1(β-糖苷键)[17],表明所制备的CNCs在基团结构上不存在明显差异[15]。此外,CNCs在1 645 cm-1处的吸收峰为纤维素吸附水的特征峰,更高质量分数硫酸制备的CNCs在此处吸收峰降低,表明亲水性降低,这与在3 400 cm-1处吸收峰强度的变化趋势一致[13]。此外,随着硫酸质量分数的增加,硫酸与结晶区表面的纤维素分子发生酯化反应的程度增强,在C6位引入磺酸基,制备的CNCs表现出在1 204 cm-1处的吸收峰增强,这是磺酸基的伸缩振动造成的[18]。
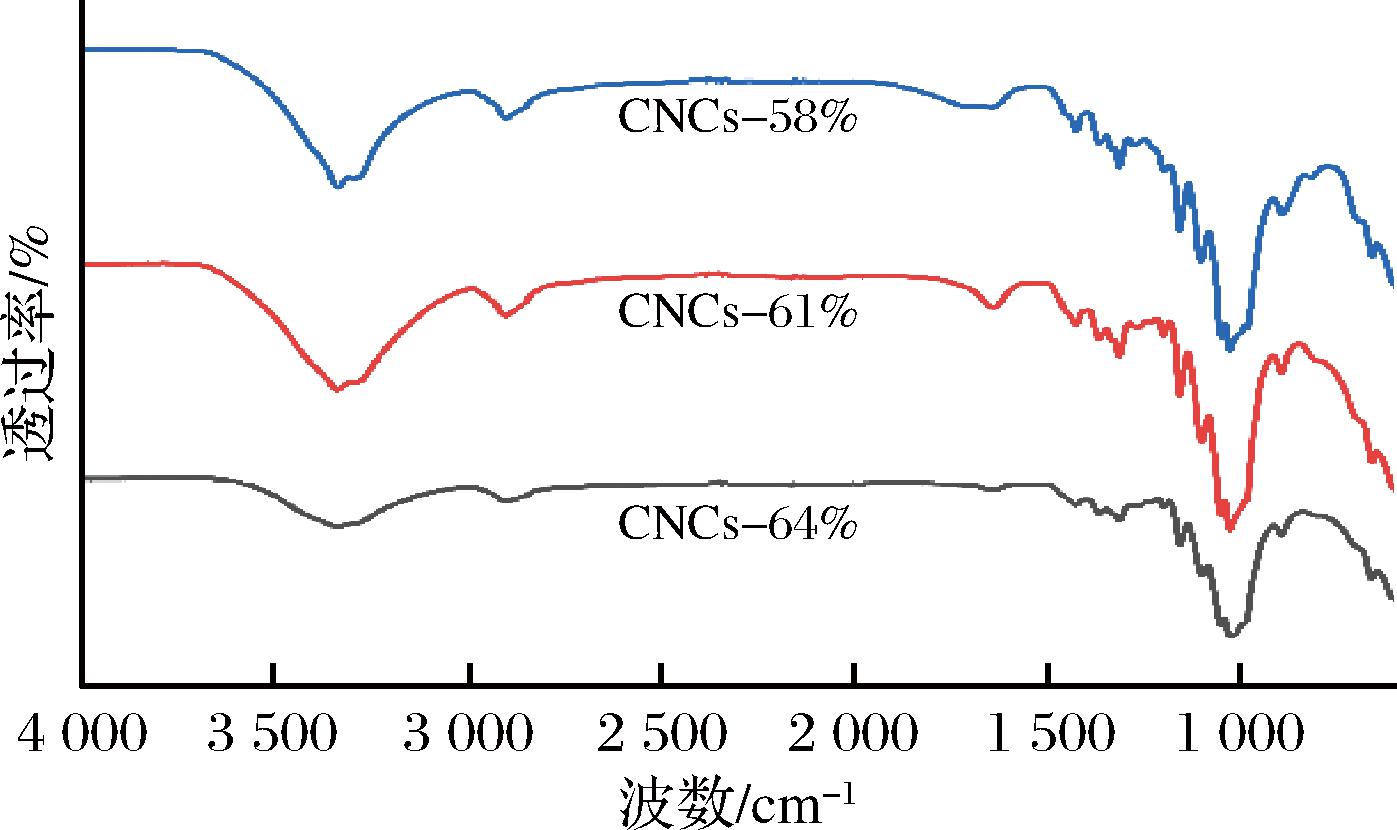
图2 不同质量分数硫酸制备的CNCs的FTIR图谱
Fig.2 FTIR spectra of CNCs prepared at different concentrations of sulfuric acid solution
不同质量分数硫酸水解制备的CNCs的粒径和Zeta电位如图3所示。如图3-a所示,CNCs主要呈现较强的单一主峰分布且粒径存在明显差异,通过激光粒度仪粗略得到的CNCs-58%、CNCs-61%和CNCs-64%的平均粒径分别为479、299和273 nm,这与AFM的粒径变化趋势大致相符。CNCs-64%的平均粒径和AFM分析结果存在一定差异,这可能是其在超过1 μm处的小峰造成的,这与制样过程中的CNCs发生轻微团聚有关。由图3-b所示,CNCs-58%、CNCs-61%和CNCs-64%的Zeta电位值分别为-33.5、-43.6和-45.7 mV。纤维素表面羟基与硫酸反应脱氢生成磺酸根离子,使生成的CNCs带负电荷。通常,CNCs的稳定悬浮液显示出低于-25 mV的Zeta电位值[15]。在当前测试的硫酸质量分数范围内,所有CNCs悬浮液的Zeta电位绝对值均大于25 mV,表明稳定性较好。Zeta电位值随着酸质量分数的增加逐渐增加,CNCs稳定性提升。
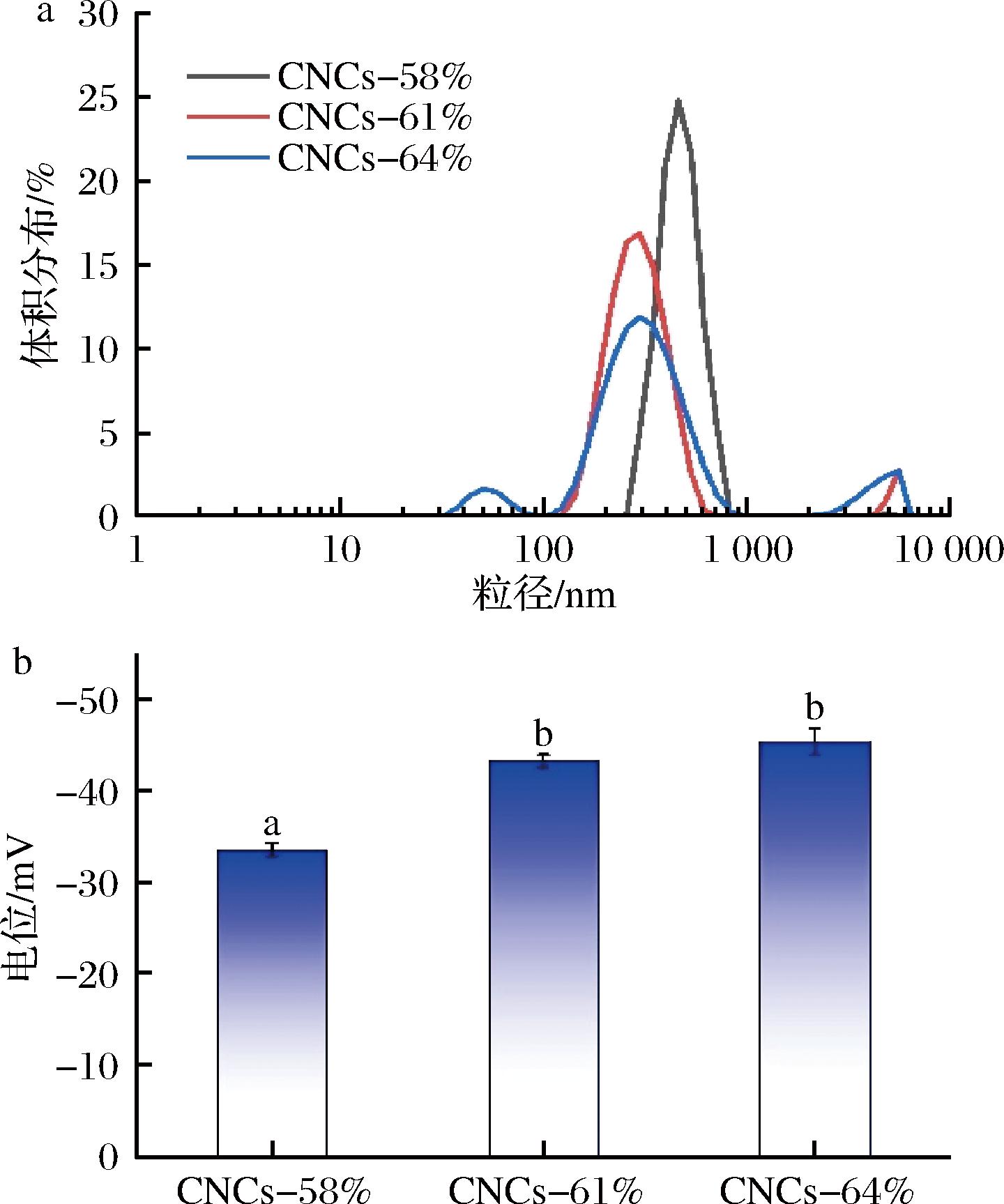
a-粒径分布;b-Zeta电位值
图3 不同质量分数硫酸制备的CNCs的粒径分布和Zeta电位值
Fig.3 Particle size distribution and Zeta potential value of CNCs prepared at different concentrations of sulfuric acid solution
CNCs的TG曲线如图4-a所示。从图中可以发现,CNCs的失重可分为三个阶段:第一阶段发生在35~100 ℃范围内,主要是由CNCs物理吸附的水分蒸发引起的;第二阶段发生在120~220 ℃范围内,主要涉及CNCs自身的热分解;第三阶段是氧化和分解碳残渣形成更小分子质量气态产物而损失的质量[4,15]。所有样品的最终残余质量差距较小(26.62%、24.67%和25.52%),这与其组分一致有关。CNCs的DTG曲线如图4-b所示。低于100 ℃的DTG峰对应CNCs吸附自由水的蒸发损失质量;CNC-58%、CNC-61%和CNC-64%的最大降解峰分别出现在218、200和151 ℃,进一步升温形成的较高温度的降解峰分别出现在352、363和387 ℃,对应于纤维素糖苷键的断裂、脱水和解聚等热解反应。整体上,提高酸浓度降低了CNCs的热稳定性,这主要是部分—OH被—OSO32-—取代,—OSO32-在高温下会催化糖苷键的分解,导致热稳定性降低[19]。此外,CNC-64%的尺寸相对更小,在热解聚过程中会暴露出更大的受热面积,CNCs表面末端和外露反应活性基团也增加,最终加速热量分布而降低热稳定性[20]。
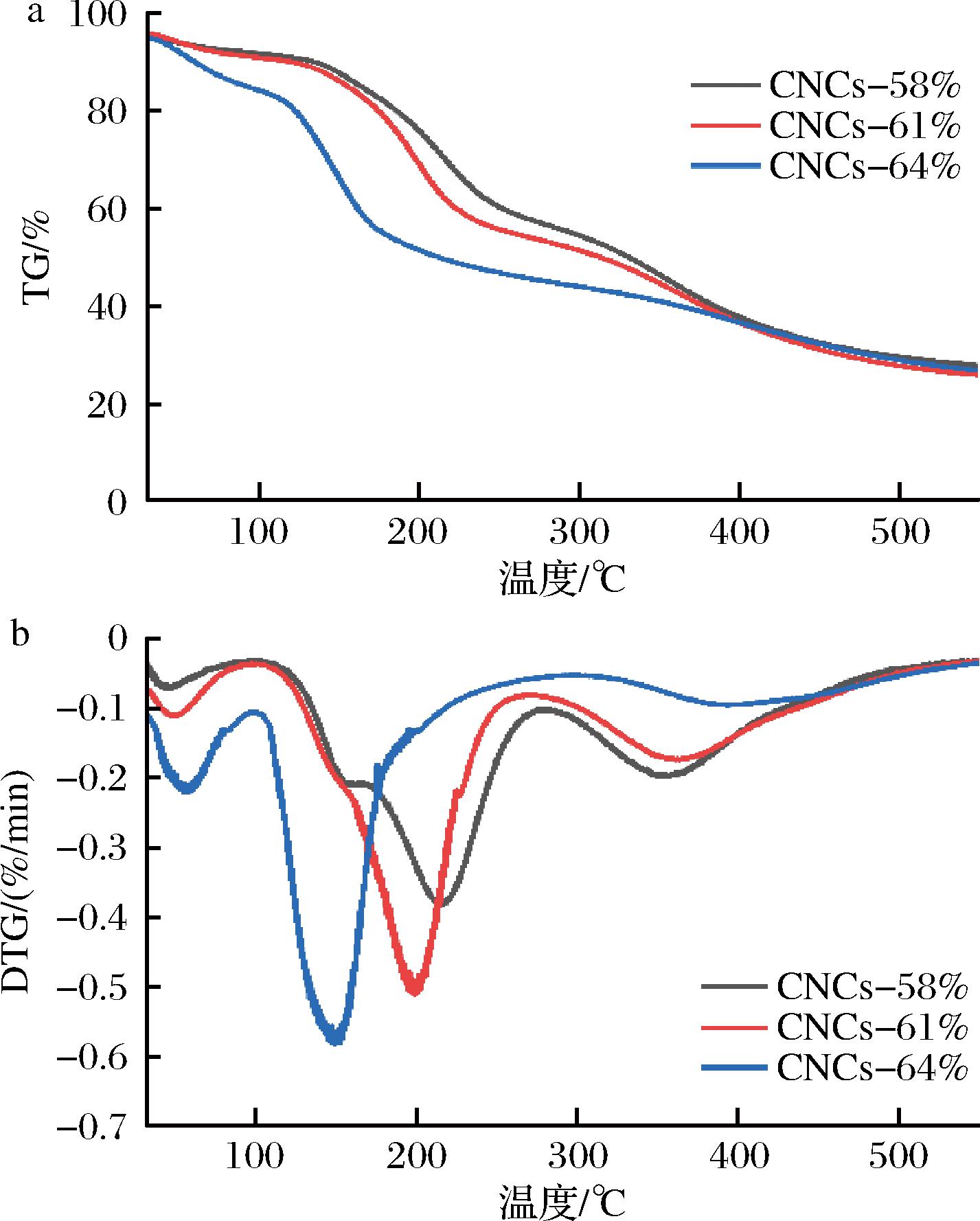
a-TG曲线;b-DTG曲线
图4 不同质量分数硫酸制备的CNCs的TG曲线与DTG曲线
Fig.4 TG and DTG curves of CNCs prepared at different concentrations of sulfuric acid solution
一般颗粒尺寸越小,越容易吸附在油滴界面上形成乳液层,形成的乳液越稳定[21]。如图5所示,与CNCs-58%相比,CNCs-61%和CNCs-64%稳定的Pickering乳液的液滴粒径明显更小。但在相对较低的CNCs质量分数(0.2%)下,与CNCs-58%、CNCs-61%稳定的乳液相比,CNC-64%稳定乳液的析水程度更高,且下层水相相对浑浊,这与CNCs的形貌结构和表面电荷有关[22]。CNCs-58%和CNCs-61%的尺寸相对较长且电荷较少,能够相互缠结形成网络结构而稳定乳液,增大空间位阻从而增强液滴对聚结的抵抗力[23]。而CNCs-64%粒径相对较小且携带电荷较多,乳液网络形成能力相对较弱且未吸附颗粒相对较多。随着CNCs颗粒浓度的增加,析水现象消失,液滴尺寸减小且分布更加均匀,表明在较高的CNCs浓度下乳液稳定性更好,这可能是因为足够颗粒的存在促进了网络结构的形成且提供了更多的空间位阻来抑制絮凝,使得液滴更加稳定[24]。总体上,当前条件下制备的CNCs稳定Pickering在4 ℃下储存15 d后,所有乳液的外观和光学显微镜基本保持稳定,表现出较好的储藏稳定性。
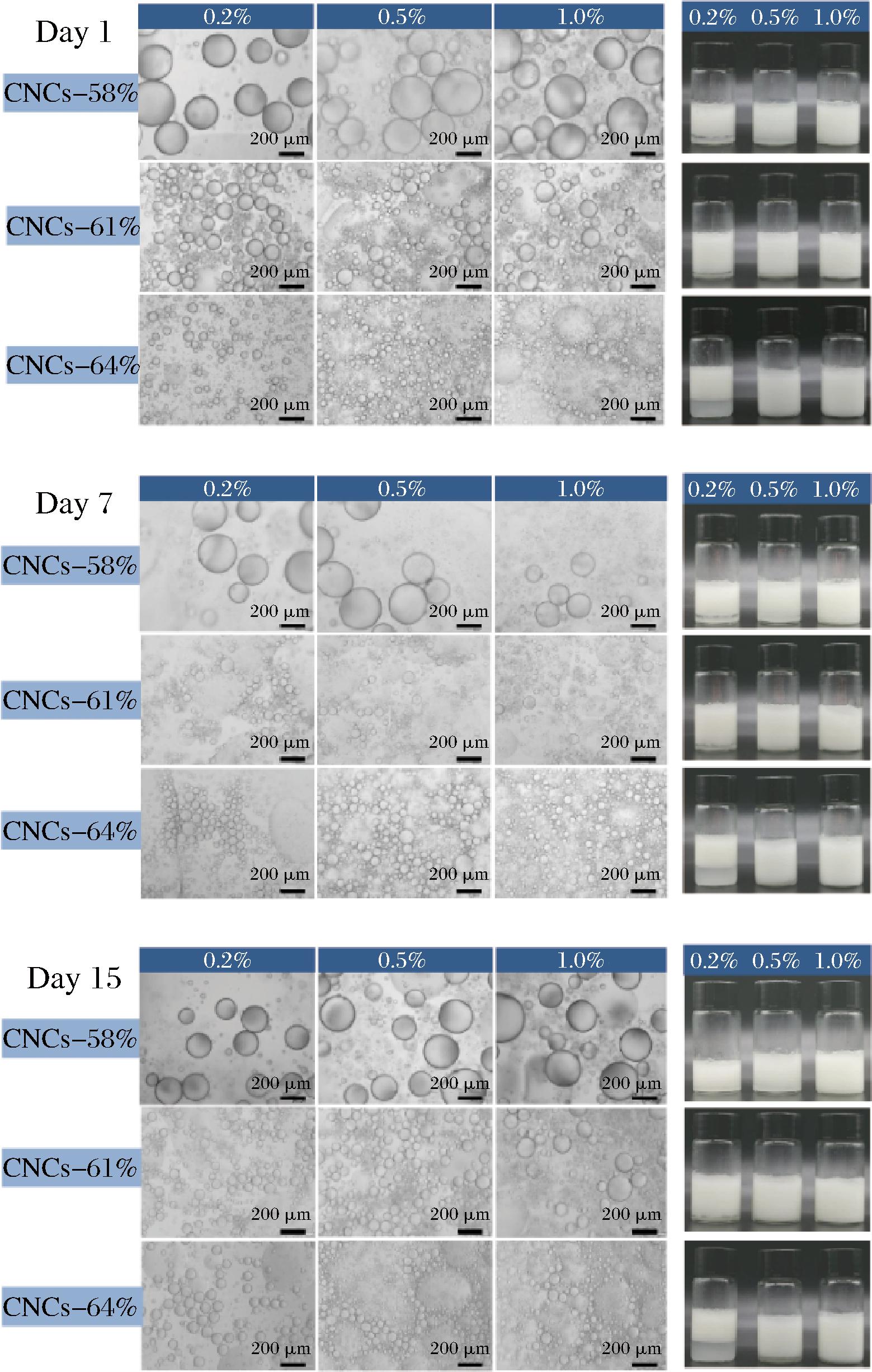
图5 CNCs稳定Pickering乳液的外观与微观形貌
Fig.5 Appearance and micromorphology of CNCs stabilized Pickering emulsions
颗粒浓度和储藏时间对CNCs稳定Pickering乳液的粒径分布影响如图6所示。
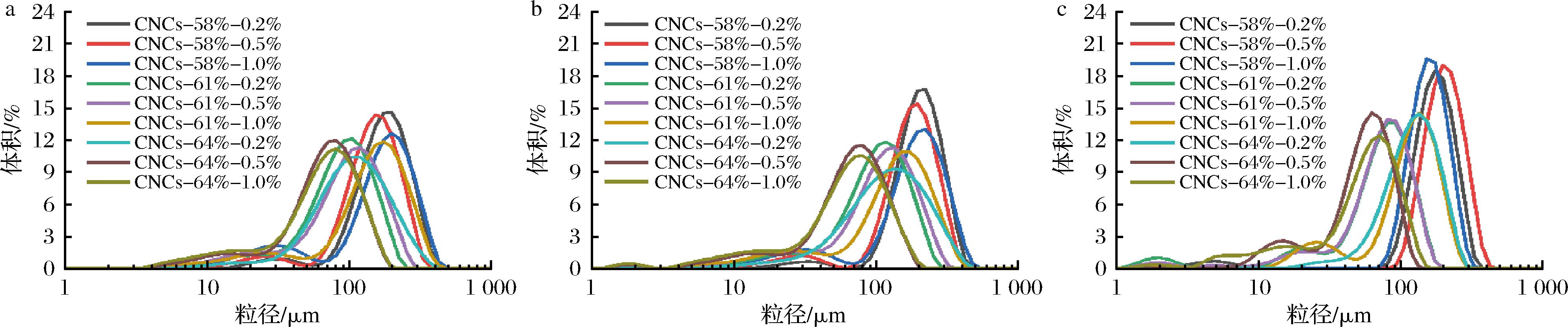
a-Day1;b-Day7;c-Day15
图6 CNCs稳定Pickering乳液的粒径分布
Fig.6 Particle size distribution of CNCs stabilized Pickering emulsions
储藏1 d后,CNCs-58%在0.2%、0.5%和1.0%质量分数下稳定的乳液液滴平均粒径(d4,3)分别为181、172、151 μm,CNCs-61%分别为154、104、94 μm,CNCs-64%分别为120、72、70 μm;进一步储藏7 d后,CNCs-58%稳定的乳液粒径分别为211、192和183 μm,CNCs-61%分别为168、116和106 μm,CNCs-64%分别为139、72、70 μm。CNCs稳定乳液的粒径稳定性、较长的纵横比与连续相网络结构形成有关[23, 25];从粒径变化数值来看,CNCs-61%和CNCs-64%稳定乳液的储藏稳定性相对较好。随着CNCs颗粒浓度的增加,乳液液滴逐渐变小且稳定性增加,这是由更多的CNCs颗粒可用于稳定更高的整体界面面积和增加的乳液连续相浓度造成的[23,25]。
如图7所示,所有乳液的电位值均为负值,这是由于液滴界面吸附的带负电荷的CNCs颗粒形成的界面膜造成的。相对较高的乳液电位绝对值会增强液滴之间的静电斥力,以防止液滴聚集并保持乳液稳定性[26]。随着储藏时间增加,乳液电位绝对值有所减小,尤其是CNCs-58%稳定的乳液,这与其储藏稳定性结果一致。随着CNCs质量分数的增大,乳液液滴表面吸附颗粒增加,乳液电位绝对值相应增大,稳定性增强。整体上,CNCs-61%和CNC-64%在较高质量分数(0.5%~1.0%)下均可以形成稳定性较好的Pickering乳液。
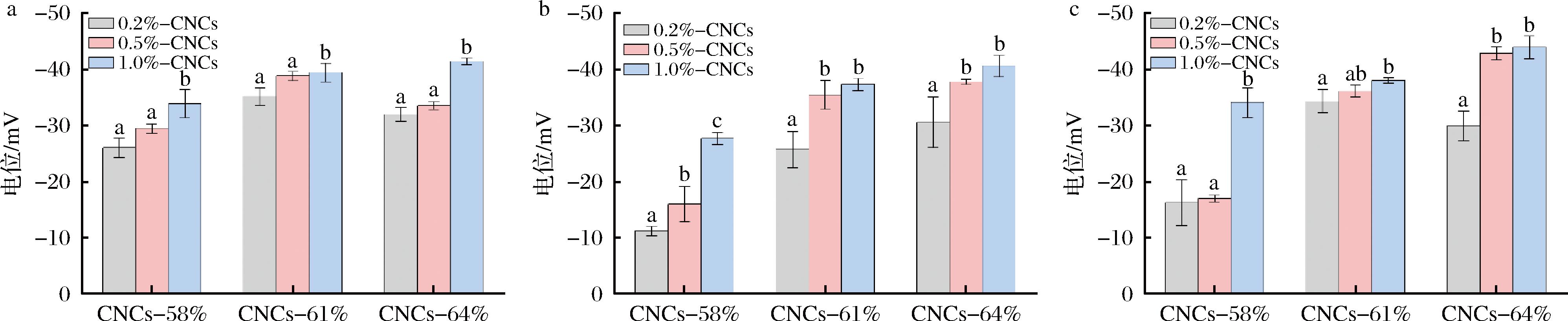
a-Day1;b-Day7;c-Day15
图7 CNCs稳定Pickering乳液的Zeta电位值
Fig.7 Zeta potential values of CNCs stabilized Pickering emulsions
通过不同质量分数硫酸溶液水解菠萝皮渣纤维素制备CNCs并对其性质进行调控。随着硫酸溶液质量分数增加,CNCs的尺寸逐渐减小且均一性增加,悬浮液稳定性提高,但热稳定性降低。由于粒径尺寸和表面电荷的差异性,不同硫酸质量分数水解的CNCs具有不同的稳定Pickering乳液性能。与CNCs-58%相比,CNCs-61%和CNCs-64%稳定的Pickering乳液具有更小、更均一的液滴粒径,且乳液储藏稳定性相对较好。在较低CNCs颗粒浓度下,CNCs-58%稳定乳液的析水程度相对较低;随着CNCs质量分数增加,更多的CNCs颗粒参与界面吸附,乳液粒径逐渐减小,乳液稳定性、持水性增加。本研究通过控制硫酸质量分数来调控CNCs形貌尺寸和稳定乳液性能,为CNCs稳定Pickering乳液的应用提供基础数据,后续可进一步研究不同粒径尺寸CNCs的界面性能和对乳液流变性质的影响。
[1] SUN Y, CHU Y L, WU W B, et al.Nanocellulose-based lightweight porous materials:A review[J].Carbohydrate Polymers, 2021, 255:117489.
[2] DAI H J, WU J H, ZHANG H, et al.Recent advances on cellulose nanocrystals for Pickering emulsions:Development and challenge[J].Trends in Food Science &Technology, 2020, 102:16-29.
[3] LONG W, OUYANG H, HU X, et al.State-of-art review on preparation, surface functionalization and biomedical applications of cellulose nanocrystals-based materials[J].International Journal of Biological Macromolecules, 2021, 186:591-615.
[4] ZHANG H, CHEN Y, WANG S S, et al.Extraction and comparison of cellulose nanocrystals from lemon (Citrus limon) seeds using sulfuric acid hydrolysis and oxidation methods[J].Carbohydrate Polymers, 2020, 238:116180.
[5] HUANG S T, LIU X H, CHANG C Y, et al.Recent developments and prospective food-related applications of cellulose nanocrystals:A review[J].Cellulose, 2020, 27(6):2991-3011.
[6] SO B R, YEO H J, LEE J J, et al.Cellulose nanocrystal preparation from Gelidium amansii and analysis of its anti-inflammatory effect on the skin in vitro and in vivo[J].Carbohydrate Polymers, 2021, 254:117315.
[7] 张欢, 戴宏杰, 陈媛, 等.纳米纤维素的制备及其在Pickering乳液中的应用研究进展[J].食品研究与开发, 2020, 41(15):173-181.
ZHANG H, DAI H J, CHEN Y, et al.Research progress in nanocellulose preparation and its application in Pickering emulsions[J].Food Research and Development, 2020, 41(15):173-181.
[8] 陈媛, 张欢, 余永, 等.纤维素纳米晶稳定Pickering乳液及其环境响应性研究进展[J].食品与发酵工业, 2020, 46(24):234-241.
CHEN Y, ZHANG H, YU Y, et al.Research progress of cellulose nanocrystals stabilized Pickering emulsion and its environmental responsiveness[J].Food and Fermentation Industries, 2020, 46(24):234-241.
[9] LI Q, WU Y L, FANG R X, et al.Application of Nanocellulose as particle stabilizer in food Pickering emulsion:Scope, Merits and challenges[J].Trends in Food Science &Technology, 2021, 110:573-583.
[10] KALASHNIKOVA I, BIZOT H, CATHALA B, et al.Modulation of cellulose nanocrystals amphiphilic properties to stabilize oil/water interface[J].Biomacromolecules, 2012, 13(1):267-275.
[11] 吕天艺, 张书敏, 陈媛, 等.不同形态纳米纤维素的制备方法研究进展[J].食品与发酵工业, 2022, 48(8):281-288.
LYU T Y, ZHANG S M, CHEN Y, et al.Research progress on preparation methods of different morphologies of nanocellulose[J].Food and Fermentation Industries, 2022, 48(8):281-288.
[12] 张艳玲, 段超, 董凤霞, 等.纳米纤维素制备及产业化研究进展[J].中国造纸, 2021, 40(11):79-89.
ZHANG Y L, DUAN C, DONG F X, et al.Research advances in nanocellulose preparation and industrialization[J].China Pulp &Paper, 2021, 40(11):79-89.
[13] FENG X, MENG X H, ZHAO J P, et al.Extraction and preparation of cellulose nanocrystals from dealginate kelp residue:Structures and morphological characterization[J].Cellulose, 2015, 22(3):1763-1772.
[14] 朱顺顺, 木泰华, 孙红男.纤维素纳米晶制备方法及应用研究进展[J].核农学报, 2022, 36(1):174-182.
ZHU S S, MU T H, SUN H N.Research progress in preparation and application of cellulose nanocrystals[J].Journal of Nuclear Agricultural Sciences, 2022, 36(1):174-182.
[15] DAI H J, OU S Y, HUANG Y, et al.Utilization of pineapple peel for production of nanocellulose and film application[J].Cellulose, 2018, 25(3):1743-1756.
[16] DAI H J, HUANG Y, ZHANG Y H, et al.Green and facile fabrication of pineapple peel cellulose/magnetic diatomite hydrogels in ionic liquid for methylene blue adsorption[J].Cellulose, 2019, 26(6):3825-3844.
[17] OH S Y, YOO D I, SHIN Y, et al.FTIR analysis of cellulose treated with sodium hydroxide and carbon dioxide[J].Carbohydrate Research, 2005, 340(3):417-428.
[18] 邢新月, 蒋绮雯, 李奇明, 等.废纸基纤维素纳米晶的制备与表征[J].中国造纸学报, 2020, 35(2):1-8.
XING X Y, JIANG Q W, LI Q M, et al.Preparation and characterization of cellulose nanocrystals from waste paper[J].Transactions of China Pulp and Paper, 2020, 35(2):1-8.
[19] 杨成秀, 梁美蓉, 林远雄, 等.龙须草纳米微晶的制备与表征[J].纸和造纸, 2018, 37(5):23-28.
YANG C X, LIANG M R, LIN Y X, et al.Preparation and characterization of cellulose nanocrystals from Eulaliopsis binata[J].Paper and Paper Making, 2018, 37(5):23-28.
[20] 岑钰, 汪力生, 项舟洋, 等.催化和机械辅助柠檬酸水解法高得率制备纤维素纳米晶体[J].中国造纸, 2023, 42(2):1-10.
CEN Y, WANG L S, XIANG Z Y, et al.High-yield preparation of cellulose nanocrystals by citric acid hydrolysis combined with catalyst and mechanical assistance[J].China Pulp &Paper, 2023, 42(2):1-10.
[21] WANG W Y, ZHU G H, LI L, et al.Facile hydrothermal synthesis of flower-like Co-Mo-S catalysts and their high activities in the hydrodeoxygenation of p-cresol and hydrodesulfurization of benzothiophene[J].Fuel, 2016, 174:1-8.
[22] CAPRON I, CATHALA B.Surfactant-free high internal phase emulsions stabilized by cellulose nanocrystals[J].Biomacromolecules, 2013, 14(2):291-296.
[23] DAI H J, ZHANG H, CHEN Y, et al.Co-stabilization and properties regulation of Pickering emulsions by cellulose nanocrystals and nanofibrils from lemon seeds[J].Food Hydrocolloids, 2021, 120:106884.
[24] JIA Y Y, ZHENG M M, XU Q Q, et al.Rheological behaviors of Pickering emulsions stabilized by TEMPO-oxidized bacterial cellulose[J].Carbohydrate Polymers, 2019, 215:263-271.
[25] N.A.Michael Eskin, 倪洋, 段慧, 等.纤维素纳米晶体颗粒稳定剂在食品Pickering乳液中的应用[J].粮油食品科技, 2021, 29(3):39-46.
MICHAEL E, NI Y, DUAN H, et al.The application of cellulose nanocrystals in Pickering emulsion as the particle stabilizer[J].Science and Technology of Cereals, Oils and Foods, 2021, 29(3):39-46.
[26] NI Y, LI J W, FAN L P.Production of nanocellulose with different length from ginkgo seed shells and applications for oil in water Pickering emulsions[J].International Journal of Biological Macromolecules, 2020, 149:617-626.